-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Prevalence protilátek proti viru hepatitidy E v České republice – sérologický přehled
The prevalence of antibodies against Hepatitis E Virus in the Czech Republic: serological survey
Aim:
To determine the prevalence of antibodies against hepatitis E virus in the general population of the Czech Republic of age 15 to 64, to analyse the age and sex distribution of these antibodies, and to evaluate the benefit of the immunoblot test for the confirmation of the specificity of the enzyme immunoassay (EIA) screening test.Material and methods:
Sera from the last available multipurpose serological survey conducted in 2001 were tested. Anti-HEV IgG was detected by the RecomWell HEV IgG EIA test (Mikrogen Diagnostik, Germany). The immunoblot assay RecomLine HEV IgG/IgM (Mikrogen Diagnostik, Germany) was used for confirmation.Results:
Using the RecomWell IgG EIA test, anti-HEV IgG reactivity was found in 115 (6.7%) of 1715 sera. No significant difference in the anti-HEV IgG reactivity was found between men 58 (6.9%) and women 57 (6.6%). The prevalence of anti-HEV IgG increased with age from 3.5% in the age group 15–24 years to 16.8% in 55-64-year-olds.Conclusions:
The prevalence of hepatitis E IgG antibodies determined in the serological survey in the age group 15–64 years was 6.7%. Recalculated for the general population of the Czech Republic, the prevalence was 8.6%. The prevalence of anti-HEV antibodies increased with age, reaching a peak of 16.8% in the age group 55–64 years. The prevalence was not significantly different between men and women.
Using the immunoblot RecomLine IgG test for the confirmation of the specificity of the screening test in the seroprevalence study was not of clear benefit.KEYWORDS:
hepatitis E virus – anti-HEV – prevalence – EIA – immunoblot
Autori: V. Němeček 1
; P. Butovičová 1; M. Malý 1
; Petr Dítě 2
; M. Veřtátová 1; I. Vodičková 1; B. Kříž 1,3
Pôsobisko autorov: Státní zdravotní ústav, Praha 1; Univerzita obrany, Brno 2; Univerzita Karlova, 3. lékařská fakulta, Praha 3
Vyšlo v časopise: Epidemiol. Mikrobiol. Imunol. 66, 2017, č. 1, s. 3-7
Kategória: Původní práce
Súhrn
Cíl práce:
Zjistit prevalenci protilátek proti viru hepatitidy E (HEV) v populaci České republiky ve věku od 15 do 64 let a provést analýzu podle věku a pohlaví a zhodnotit přínos imunoblotového testu pro ověření specificity základního screeningového EIA testu.Materiál a metody:
Pro studii byla využita séra z mnohoúčelového sérologického přehledu z roku 2001. K vyšetření anti-HEV IgG byl použit test enzymové imunoanalýzy (EIA) RecomWell HEV IgG (Mikrogen Diagnostik, SRN). Následné konfirmační vyšetření bylo provedeno imunoblotovým testem RecomLine HEV IgG/IgM (Mikrogen Diagnostik, SRN).Výsledky:
EIA testem RecomWell IgG bylo vyšetřeno celkem 1715 sér a reaktivita anti-HEV IgG byla zjištěna u celkem 115 vzorků (6,7 %). U mužů bylo zjištěno 58 reaktivních sér (6,7 %) a u žen 57 (6,6 %). Prevalence anti-HEV IgG s věkem stoupá z hodnoty 3,5 % ve věkové skupině 15–24letých na 16,8 % ve skupině 55–64letých.Závěry:
Na základě sérologického přehledu byla zjištěna séroprevalence protilátek proti viru hepatitidy E v České republice ve věkové skupině 15–64 let. Celková séroprevalence v přehledu činila 6,7 %, přepočtená na počet osob v ČR pak 8,6 %. Prevalence anti-HEV stoupá s věkem s maximem 16,8 % ve věkové skupině 55–64 let. Nebyl zjištěn rozdíl v prevalenci podle pohlaví. Použití imunoblotového testu RecomLine IgG pro ověření výsledků vyšetření protilátek anti-HEV třídy IgG v séroprevalenční studii nelze jednoznačně hodnotit jako přínosné.KLÍČOVÁ SLOVA:
virus hepatitidy E – anti-HEV – prevalence – EIA – imunoblotÚVOD
Virus hepatitidy E (HEV) je řazen do rodu Hepevirus z čeledi Hepeviridae. Jeho genom tvoří jednořetězcová (+) RNA délky 7,2 kb, která obsahuje tři kódující oblasti ORF1, ORF2 a ORF3. Jsou známy čtyři genotypy (gt) infikující člověka HEV 1 až 4 [1], které mají rozdílnou geografickou distribuci [2]. Genotyp 1 se vyskytuje převážně v Asii a severní Africe, genotyp 2 v Mexiku a Jižní Americe, genotyp 3 v Evropě a Severní Americe a genotyp 4 v jihovýchodní Asii. HEV gt1 a gt2 se vyskytují zejména v oblastech s nízkou úrovní hygieny a šíří se fekálně orální cestou, převážně kontaminovanou vodou. Genotyp 3 a 4 se šíří hlavně zoonoticky [3]. Rezervoárem jsou domácí i divoká zvířata, nejčastěji prase domácí i divoké a spárkatá zvěř. K přenosu většinou dochází požitím nedostatečně tepelně zpracovaného masa, ale uplatňuje se i fekálně orální přenos. Možný je i přenos krví např. transfuzí nebo injekční aplikací drog [4].
HEV vyvolává u člověka asymptomatickou infekci nebo manifestní onemocnění, které zpravidla probíhá jako akutní hepatitida, končící úzdravou. U imunokompromitovaných osob může dojít k perzistenci viru a chronickému onemocnění [5].
Laboratorní diagnostika virové hepatitidy E (VHE) je založena na stanovení protilátek IgM a IgG proti HEV, případně stanovení HEV RNA [6]. Sérologické diagnostické testy využívají syntetické peptidy nebo rekombinantní proteiny odvozené z kódujících oblastí ORF2/ORF3. HEV má jeden sérotyp, a proto se v diagnostických testech vyskytují antigeny odvozené od různých genotypů.
Protilátky anti-HEV IgM dosahují zpravidla vysokých hladin již v době objevení klinických příznaků a vymizí ve většině případů po 32 týdnech [6]. Protilátky anti-HEV IgG dosahují nejvyšších hodnot většinou čtyři týdny po objevení symptomů. Pro prevalenční studie je důležitá informace o dlouhodobém přetrvávání protilátek IgG. Literárních údajů však není mnoho a doba přetrvávání protilátkové odpovědi není přesně známa. Chadha M. S. et al. potvrdili přetrvávání anti-HEV IgG pět let po infekci u všech vyšetřovaných osob [7], zatímco Rapicetta M. et al. za stejnou dobu jen u 37 % [8]. Khuroo et al. zjistili, že 47 % osob má prokazatelné anti-HEV IgG protilátky ještě 14 let po prožité VHE [9].
K výrazným epidemiologickým charakteristikám virové hepatitidy E, které by se měly odrazit i v datech o séroprevalenci anti-HEV protilátek, je nemocnost podle věku a pohlaví. Nemocnost VHE v ČR s věkem výrazně narůstá a maxima dosahuje ve věkových skupinách 50–69 let – graf 1(EPIDAT). Dlouhodobě je pozorován vyšší výskyt VHE u mužů než u žen – graf 2 (EPIDAT). Cílem naší studie bylo zjistit prevalenci protilátek proti HEV v populaci České republiky ve věkových skupinách od 15 do 64 let, provést analýzu podle věku a pohlaví a zhodnotit přínos imunoblotového testu pro ověření specificity základního screeningového EIA testu.
Graf 1. Průměrná nemocnost VHE v ČR v závislosti na věku Figure 1. Mean viral hepatitis E morbidity in the Czech Republic by age 
Graf 2. Nemocnost VHE v ČR podle pohlaví Figure 2. Viral hepatitis E morbidity in the Czech Republic by gender 
MATERIÁL A METODY
Pro určení prevalence protilátek proti viru hepatitidy E třídy IgG (anti-HEV IgG) v České republice byla využita séra z mnohoúčelového sérologického přehledu z roku 2001. Séra byla získána náhodným výběrem od osob z běžné populace bez známek horečnatého onemocnění a byla uchovávána v alikvotech v sérové bance Centra epidemiologie a mikrobiologie SZÚ při teplotě -20 °C. Pro prevalenční studii bylo použito 1 715 vzorků sér osob ve věku 15–64 let, z nichž 48,2 % bylo mužů a 51,8 % žen.
K vyšetření anti-HEV IgG byl použit test enzymové imunoanalýzy (EIA) RecomWell HEV IgG (Mikrogen Diagnostik, SRN). Doplňkové následné konfirmační vyšetření bylo provedeno imunoblotovým testem RecomLine HEV IgG/IgM (Mikrogen Diagnostik, SRN). Oba testy byly provedeny a výsledky vyhodnocovány podle postupu uvedenému v návodu výrobce.
Statistické hodnocení bylo provedeno programem STATA v. 9.2, Stata Corp. LP, College Station, TX, USA, χ 2 testem nebo Armitageovým testem. Hodnoty p < 0,05 byly považovány za statisticky významné. Údaje o nemocnosti VHE podle věku a pohlaví byly získány ze systému hlášení vybraných infekčních onemocnění EPIDAT.
VÝSLEDKY
EIA testem RecomWell IgG bylo vyšetřeno celkem 1 715 sér prevalenční studie a reaktivita anti-HEV IgG byla zjištěna u celkem 115 vzorků (6,7 %), z nich podle kritérií výrobce bylo 13 hraničně reaktivních v tzv. šedé zóně. U mužů bylo zjištěno 58 reaktivních vzorků (6,9 %) a u žen 57 (6,6 %). Výsledky výskytu v jednotlivých věkových skupinách jsou uvedeny celkem a zvlášť pro muže a ženy, v absolutních počtech i relativně v tabulce 1.
Tab. 1. Prevalence protilátek anti-HEV IgG v sérech ze sérologického přehledu 2001 Table 1. The prevalence of anti-HEV IgG antibodies in sera from the 2001 serological survey 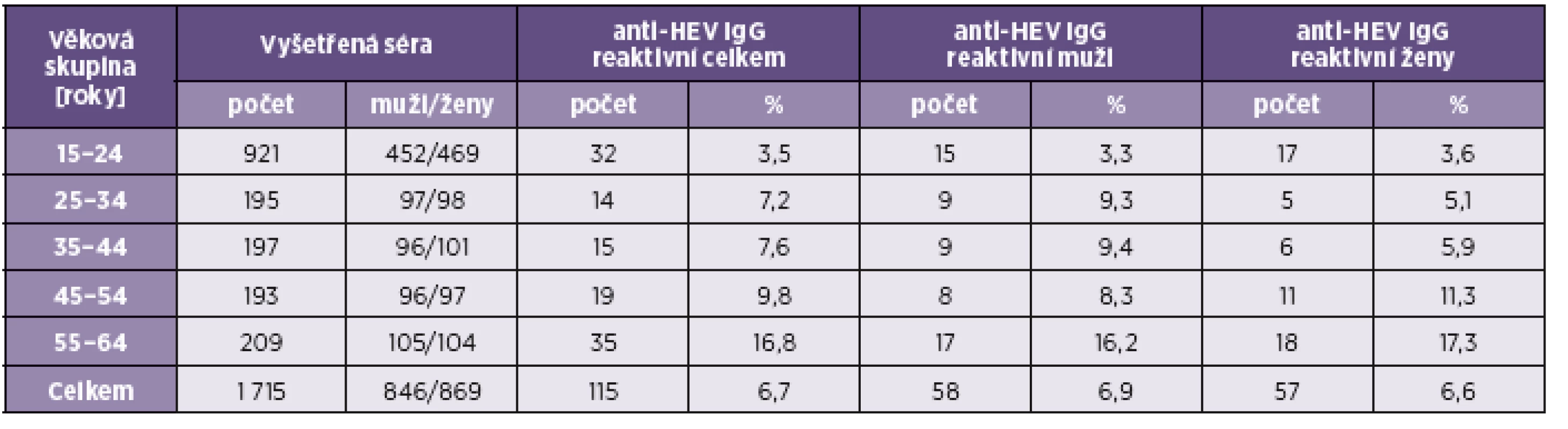
Prevalence anti-HEV IgG s věkem stoupá z hodnoty 3,5 % ve věkové skupině 15–24letých na 16,8 % ve skupině 55–64letých. Statistické hodnocení lineárního trendu vzestupu přes jednotlivé věkové skupiny provedené Armitageovým testem vykazuje výsledek vysoce statisticky významný (p < 0,001), tzn. že trend je prokazatelný. Nárůst prevalence anti-HEV IgG s věkem je v souladu s údaji o nárůstu nemocnosti v závislosti na věku, který ukazuje graf 1. Rozdíl v celkové prevalenci anti-HEV IgG u mužů (6,9 %) a žen (6,9 %) není statisticky významný (p = 0,8188). Ani ve věkové skupině 25–34letých, kde byla zjištěna největší odlišnost hodnot prevalence mezi muži (9,3 %) a ženami (5,1 %), není tento rozdíl statisticky významný (p = 0,2931). Graf 2 ukazuje, že od roku 2001 je setrvale zaznamenávána vyšší nemocnost virovou hepatitidou E u mužů než u žen a tento rozdíl je v jednotlivých letech vždy statisticky významný.
Graf 3 ukazuje podíl (%) anti-HEV IgG reaktivních nálezů z počtu vyšetřených testem EIA podle okresů v ČR.
Graf 3. Podíl anti-HEV IgG pozitivních vzorků z počtu vyšetřovaných (%) geograficky podle okresů Figure 3. The percentage of anti-HEV IgG positive samples of the total tested by district 
K ověření specifity výsledků anti-HEV IgG byl použit imunoblotový test RecomLine IgG. Ze 1 715 vzorků souboru bylo testem RecomLine IgG vyšetřeno 115 vzorků reaktivních a též 68 vzorků negativních v EIA testu RecomWell IgG. Ze 115 reaktivních vzorků byl výsledek konfirmačního testu pozitivní u 75 vzorků (65,2 %), u 40 vzorků tj. 34,8 %,se reaktivita výsledku EIA testu konfirmačním testem nepotvrdila. RecomWell IgG je test kvalitativní, u něhož je reaktivní výsledek vymezen hodnotou S/CO, tj. poměrem extinkce vzorku a hladiny pozitivity větším než 1. Hodnota S/CO však vyjadřuje míru reaktivity vzorku. V souboru anti-HEV IgG reaktivních sér byly zaznamenány hodnoty S/CO v intervalu 1–11. Nejčetnější byly S/CO hodnoty v rozmezí 1–1,99 tj. hraniční pozitivity (49/115) a hodnoty 2–2,99, tj. slabé pozitivity (25/115) dohromady 74/115 (64,3 %). Podíl výsledků potvrzených testem RecomLine v závislosti na hodnotě S/CO u vzorků pozitivních v testu RecomWell je uveden v tabulce 2. Z tabulky vyplývá, že v kategorii hraničních EIA výsledků S/CO 1–1,99 imunoblotový test potvrdil jen 18, tj. 36,7 % EIA pozitivních výsledků. Pro hodnoty S/CO 2–3,99 shoda výsledků vzrostla na 76,0 %, pro S/CO ≥ 4 je shoda s jednou výjimkou 100%.
Tab. 2. Podíl výsledků potvrzených testem RecomLine podle S/CO hodnoty v testu RecomWell Table 2. Comparison of the distribution of the RecomWell S/CO values in the RecomLine positive or negative samples 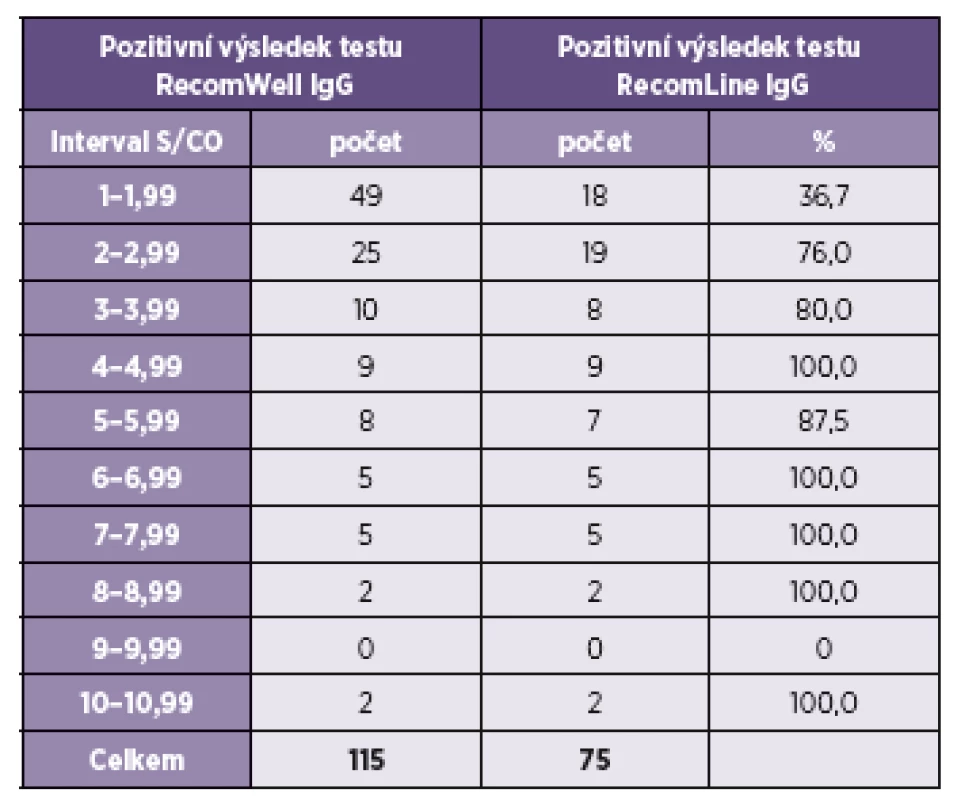
Imunoblotovým testem RecomLine bylo vyšetřeno i 68 vzorků negativních v EIA testu RecomWell IgG. U 59 sér byl výsledek imunoblotového testu rovněž negativní, ale u 9 vzorků (13,2 %) byl výsledek pozitivní. Výsledek dovyšetření těchto 9 vzorků dvěma dalšími EIA testy DiaPro IgG (Diagnostic BioProbes s.r.l., Italy) a MP HEV ELISA IgG (MP Diagnostics, Singapore) byl rovněž negativní. Specificitu výsledků imunoblotového testu nebylo u těchto 9 vzorků možné dále ověřit. Z uvedených výsledků je zřejmé, že byly zjištěny výrazné rozdíly mezi EIA testem RecomWell IgG a imunoblotovým testem RecomLine IgG, které nelze hodnotit jen jako rozdíly v citlivosti testů. Použití imunoblotového testu RecomLine IgG pro ověření výsledků vyšetření protilátek anti-HEV třídy IgG v séroprevalenční studii nelze jednoznačně hodnotit jako přínosné.
Celkový výskyt protilátek anti-HEV IgG v celém souboru 1715 sér osob ve věku 15–64 let na podkladě vyšetření EIA testem RecomWell IgG je 6,7 %. Počet vzorků v sérologickém přehledu v jednotlivých věkových skupinách a v podílu mužů a žen neodpovídá zcela zastoupení ve skutečné populaci ČR, proto byly výsledky z jednotlivých věkových skupin na skutečné počty podle údajů Ústavu zdravotnických informací a statistiky (ÚZIS) přepočítány. Celková prevalence anti-HEV IgG protilátek po přepočtení ve věkové skupině 15–64 let je 8,6 % (95% interval spolehlivosti je 4,4–15,0 %). Pokud se zohlední i výsledky konfirmačního vyšetření imunoblotovým testem RecomLine IgG, pak celková přepočtená prevalence ve věkové skupině 15 až 64 let je 5,4 % (95% interval spolehlivosti je 2,2–11,0 %).
DISKUSE
Přítomnost samotných protilátek anti HEV IgG je znakem prožité infekce. Vzhledem k tomu, že v ČR není k dispozici očkování, nemohou být protilátky důsledkem vakcinace.
Bylo zjištěno, že mezi výsledky získanými dostupnými diagnostickými testy na protilátky anti-HEV IgG jsou značné rozdíly [10, 11]. S touto variabilitou testů, která může velmi výrazně ovlivnit hodnoty prevalence, je potřeba počítat při porovnávání dat s údaji zjištěnými v různých studiích. Výsledky studií prováděné novějšími testy mohou být 3–5násobně vyšší ve srovnání s hodnotami prevalence získanými staršími testy. Například prevalence anti-HEV v jihozápadní Anglii zjištěná testem „první generace“ byla 3,6 %, avšak při použití novějšího citlivějšího testu činila 16 % [12]. Sérologické diagnostické testy využívají proteiny odvozené z kódujících oblastí ORF2/ORF3. I při genotypové rozdílnosti má HEV jeden sérotyp [13]. V diagnostických testech se využívají antigeny odvozené od HEV různých genotypů, ale není prokázáno, že by tato skutečnost měla podstatný vliv na citlivost a specifitu testů. Ukazuje se, že lepší vlastnosti mají testy využívající rekombinantní proteiny než syntetické peptidy [14]. V současnosti nejcitlivější test Wantai HEV využívá rekombinantní protein (PE2) spontánně tvořící homodimery nebo polymery, což výrazně podporuje jeho antigenicitu oproti monomerním formám [12]. Analytickou citlivost testů na stanovení anti-HEV IgG lze stanovovat a porovnávat na podkladě referenčního preparátu WHO [15] vytvořeném Národním institutem pro biologické standardy a kontrolu (NIBSC).
V Evropě se prevalence protilátek proti HEV může výrazně lišit jak mezi státy, tak v rámci jednotlivých zemí i při použití shodných nebo porovnatelných testů. Často citovaný je rozdíl v prevalenci v jižní a severní Francii, či v jižní Anglii a Skotsku. Při mezinárodním srovnávání úrovně prevalence jsou častější údaje týkající se dárců krve. Séroprevalenční studie odpovídající sérologickým přehledům v ČR jsou ojedinělé. Dárce krve je možné považovat za skupinu relativně blízkou obecné populaci. Publikovaná data u dárců krve, získaná vysoce citlivým Wantai, jsou k dispozici např. z Německa, kde prevalence činí 29 %, Nizozemska 27 %, jihozápadní Anglie 16 %, jihozápadní Francie 52 % [16].
Hodnota prevalence zjištěná z námi provedeného sérologického přehledu pro populaci ve věku 15–64 let testem RecomWell je 6,7 %. Podle Strakové et al., která publikovala výsledky na základě téhož sérologického přehledu pouze ze dvou okresů ČR, avšak testem DiaPro, byla prevalence 5,7 % [17]. Prevalence anti-HEV protilátek s věkem narůstá, což je ve shodě s věkovou distribucí nemocnosti v ČR a odpovídá i zahraničním publikovaným údajům [18]. Prevalence protilátek u mužů a žen nebyla statisticky významně rozdílná ani celkově, ani v jednotlivých věkových skupinách, což je ve shodě s údaji některých Evropských zemí, např. Německa [19]. Tento nález však není v souladu s údaji o nemocnosti v ČR, která je od roku 2000 setrvale statisticky významně vyšší u mužů (viz graf 2). Graf 3 ukazující geografickou distribuci podílu pozitivních výsledků anti-HEV IgG podle okresů nelze porovnávat s údaji o nemocnosti v důsledku velmi nízkého počtu hlášených případů VHE (13 případů) v roce 2001. Značná část reaktivních výsledků testem RecomWell IgG (34,8 %) se imunoblotovým testem RecomLine IgG nezkonfirmovala. To je překvapivé zjištění v případě, že oba testy jsou od shodného výrobce. Výsledky uvedené v tabulce 2 ukazují, že naprostá většina výsledků nepotvrzených imunoblotovým testem patří do skupiny hraničních či slabých v EIA testu (interval S/CO 1–2,99). Uvedené výsledky je nesnadné vysvětlit jen vyšší specificitou imunoblotového testu, s ohledem na skutečnost, že vyšetření 68 vzorků negativních v RecomWell IgG testu vedlo ke zjištění pozitivity imunoblotovým testem u 9 vzorků (13,2 %), přičemž hodnoty S/CO u uvedených vzorků nebyly blízké hladině pozitivity (CO). Těchto 9 vzorků bylo negativních i při vyšetření dvěma dalšími EIA testy DiaPro a MP. RecomLine je jediným komerčním imunoblotovým testem, proto je obtížné specifitu těchto nálezů déle ověřit.
Při vyhodnocování séroprevalenčních dat získaných na podkladě výsledků EIA testů doplněných o konfirmační vyšetření je proto namístě opatrnost. To potvrzuje např. studie testující soubor dárců krve paralelně třemi EIA testy a imunoblotovým testem, kdy byla prevalence zjištěná testem MP Diagnostics 4,9 %, testem Dia.Pro 4,2 % a testem Fortress 21,8 % a imunoblotovým testem RecomLine byly výsledky testů MP Diagnostics a Dia.Pro potvrzeny v 80 %, ale výsledky testu Fortress v 42,3 % [20].
ZÁVĚR
Na základě sérologického přehledu byla zjištěna séroprevalence protilátek proti viru hepatitidy E v České republice ve věkové skupině 15–64 let. Celková séroprevalence v přehledu činila 6,7 %, přepočtená na počet osob v ČR pak 8,6 %. Prevalence anti-HEV stoupá s věkem s maximem 16,8 % ve věkové skupině 55–64 let. Nebyl zjištěn rozdíl v prevalenci podle pohlaví. Použití imunoblotového testu RecomLine IgG pro ověření výsledků vyšetření protilátek anti-HEV třídy IgG v séroprevalenční studii nelze jednoznačně hodnotit jako přínosné.
Poděkování
Studie byla podporována Interní grantovou agenturou Ministerstva zdravotnictví, projekt č. NT/13884/2012.
Do redakce došlo dne 8. 3. 2016.
Adresa pro korespondenci:
RNDr. Vratislav Němeček, CSc.
Státní zdravotní ústav
Šrobárova 48
100 42 Praha 10
e-mail: vratislav.nemecek@szu.cz
Zdroje
1. Lu L, Li C, Hagedorn CH. Phylogenetic analysis of global hepatitis E virus sequences: genetic diversity, subtypes and zoonosis. Rev Med Virol, 2006;16 : 5–36.
2. Hoofnagle JH, Nelson KE, Purcell RH. Hepatitis E. N Engl J Med, 2012;367 : 1237–1244.
3. Pavio N, Meng XJ, Renou C. Zoonotic hepatitis E: animal reservoirs and emerging risks. Vet Res, 2010;41 : 46.
4. Boxall E, Herborn A, Kochethu G, Pratt G, Adams D, Ijaz S, Teo CG. Transfusion – transmitted hepatitis E in a 'nonhyperendemic' country. Transfus Med, 2006;16 : 79–83.
5. Bihl F, Negro F. Chronic hepatitis E in the immunosuppressed: a new source of trouble? J Hepatol, 2009;50 : 435–437.
6. Huang S, Zhang X, Jiang H, Yan Q, Ai X, Wang Y, Cai J, Jiang L, Wu T, Wang Z, Guan L, Shih JW, Ng MH, Zhu F, Zhang J, Xia N. Profile of acute infectious markers in sporadic hepatitis E. PLoS One, 2010;5:e13560.
7. Chadha MS, Walimbe AM, Arankalle VA. Retrospective serological analysis of hepatitis E patients: a long-term follow-up study. J Viral Hepat, 1999;6 : 457–461.
8. Rapicetta M, Kondili LA, Pretolani S, Stroffolini T, Chionne P, Villano U, Madonna E, Casali F, Gasbarrini G. Seroprevalence and anti-HEV persistence in the general population of the Republic of San Marino. J Med Virol, 1999;58 : 49–53.
9. Khuroo MS, Kamili S, Dar MY, Moecklii R, Jameel S. Hepatitis E and long-term antibody status. Lancet, 1993;341 : 1355.
10. Wenzel JJ, Preiss J, Schemmerer M, Huber B, Jilg W. Test performance characteristics of Anti-HEV IgG assays strongly influence hepatitis E seroprevalence estimates. J Infect Dis, 2013;207 : 497–500.
11. Echevarria JM. Light and Darkness: Prevalence of Hepatitis E Virus Infection among the General Population. Scientifica (Cairo), 2014 : 481016.
12. Bendall R, Ellis V, Ijaz S, Ali R, Dalton H. A comparison of two com-mercially available anti-HEV IgG kits and a re-evaluation of anti-HEV IgG seroprevalence data in developed countries. J Med Virol, 2010;82 : 799–805.
13. Emerson SU, Clemente-Casares P, Moiduddin N, Arankalle VA, Torian U, Purcell RH. Putative neutralization epitopes and broad cross-genotype neutralization of Hepatitis E virus confirmed by a quantitative cell-culture assay. J Gen Virol, 2006;87 : 697–704.
14. Mast EE, Alter MJ, Holland PV, Purcell RH. Evaluation of assays for antibody to hepatitis E virus by a serum panel. Hepatitis E Virus Antibody Serum Panel Evaluation Group. Hepatology, 1998;27 : 857–861.
15. Ferguson M, Walker D, Mast E, Fields H. Report of a collaborative study to assess the suitability of a reference reagent for antibodies to hepatitis E virus. Biologicals, 2002;30 : 43–48.
16. Kamar N, Dalton HR, Abravanel F, Izopet J. Hepatitis E virus infec-tion. Clin Microbiol Rev, 2014;27 : 116–138.
17. Strakova P, Kriz B, Rudolf I, Hubalek Z. Seroprevalence study of hepatitis E virus infection in two districts of the Czech Republic. Epidemiol Mikrobiol Imunol, 2014;63 : 92–94.
18. Legrand-Abravanel F, Kamar N, Sandres-Saune K, Lhomme S, Mansuy JM, Muscari F, Sallusto F, Rostaing L, Izopet J. Hepatitis E virus infection without reactivation in solid-organ transplant recipients, France. Emerg Infect Dis, 2011;17 : 30–37.
19. Faber MS, Wenzel JJ, Jilg W, Thamm M, Hohle M, Stark K. Hepatitis E virus seroprevalence among adults, Germany. Emerg Infect Dis, 2012;18 : 1654–1657.
20. Schnegg A, Burgisser P, Andre C, Kenfak-Foguena A, Canellini G, Moradpour D, Abravanel F, Izopet J, Cavassini M, Darling KE. An analysis of the benefit of using HEV genotype 3 antigens in detecting anti-HEV IgG in a European population. PLoS One, 2013;8:e62980.
Štítky
Hygiena a epidemiológia Infekčné lekárstvo Mikrobiológia
Článok vyšiel v časopiseEpidemiologie, mikrobiologie, imunologie
Najčítanejšie tento týždeň
2017 Číslo 1- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Očkování proti virové hemoragické horečce Ebola experimentální vakcínou rVSVDG-ZEBOV-GP
- Koronavirus hýbe světem: Víte jak se chránit a jak postupovat v případě podezření?
-
Všetky články tohto čísla
- Nespecifická imunoterapie inhibuje angiogenezi – výsledky monitorování sérových hladin vaskulárního endotelového růstového faktoru a matrixmetaloproteinázy 8 v průběhu adjuvantní léčby vysokodávkovaným interferonem u pacientů s maligním melanomem
- Trend a výzva v prenose syfilisu z matky na dieťa
- Prevalence protilátek proti viru hepatitidy E v České republice – sérologický přehled
- Management akutní anafylaxe v klinické praxi v kontextu doporučených postupů
- Alimentárny botulizmus – staronová výzva pre verejné zdravotníctvo
- Možnosti implementace sekvenace celého genomu (WGS) Neisseria meningitidis do molekulární surveillance invazivního meningokokového onemocnění v České republice
- Doc. MUDr. Juraj Strauss, CSc. – 100 let
- Zemřel významný český virolog doc. MUDr. Dimitrij Slonim, CSc.
- Infekční choroby a laboratorní diagnostika v podmínkách Židovského ghetta Terezín
- Epidemiologie, mikrobiologie, imunologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Management akutní anafylaxe v klinické praxi v kontextu doporučených postupů
- Prevalence protilátek proti viru hepatitidy E v České republice – sérologický přehled
- Alimentárny botulizmus – staronová výzva pre verejné zdravotníctvo
- Infekční choroby a laboratorní diagnostika v podmínkách Židovského ghetta Terezín
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



