-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Zkušenosti s léčbou virové hepatitidy C u injekčních uživatelů návykových látek v programu substituční léčby metadonem
Experience with viral hepatitis C treatment among people who inject drugs and participate in a methadone substitution treatment program
Objectives: Long-term monitoring of the mutual effects of chronic viral hepatitis C (VHC) treatment and tailored addiction treatment. In 2016, the World Health Organization (WHO) published an action plan to eliminate viral hepatitis C globally by 2030. People who inject drugs (PWID) are a key population that needs increased attention and care. Two decades before the announcement of the WHO plan for the global elimination of HCV (hepatitis C virus), the Remedis Medical Facility, where the study was conducted, established a “Comprehensive Care Program for patients with substance use disorders and addictive behaviour”.
Methods: We evaluated all patients who were in the methadone program as of 1 March 2020, regardless of OST duration, OST dosage, age or gender. Their epidemiological and demographic data obtained during a structured clinical interview and laboratory test results were analysed.
Results: Of 24 patients on methadone substitution therapy, 12 (50%) were anti-HCV negative before starting OST. None of them became newly infected with hepatitis C virus (HCV) during OST. The remaining 12 of the study patients were anti-HCV positive. Ten of them have already undergone successful treatment for viral hepatitis. Two patients were re-infected with HCV.
Conclusion: The presented work confirms the high efficacy of chronic VHC treatment among PWID in inducing suitable conditions. We consider combination of HCV infection treatment and targeted tailored addiction treatment as a starting point for achieving control over the HCV epidemic in the Czech Republic, with a possible positive impact on other blood-borne infections related to risky behaviour.
Keywords:
HCV (hepatitis C virus) – VHC (viral hepatitis C) – PWID (People Who Injected Drugs) – OST (opioid substitution treatment) – MTD (methadone) – Remedis, Prague
Autori: L. Krekulová 1,2; L. Vavrinčíková 1
Pôsobisko autorov: Remedis, s. r. o. Praha 1; IV. Interní klinika, 1. lékařská fakulta, Univerzita Karlova a Všeobecná fakultní nemocnice v Praze 2
Vyšlo v časopise: Epidemiol. Mikrobiol. Imunol. 70, 2021, č. 1, s. 18-25
Kategória: Původní práce
Súhrn
Cíl práce: Dlouhodobé sledování vzájemného efektu léčby chronické virové hepatitidy C (VHC) a individualizované adiktologické péče. Světová zdravotnická organizace (WHO) v roce 2016 zveřejnila akční plán s cílem globální eliminace VHC do roku 2030. Injekční uživatelé návykových látek (PWID) jsou skupina, které je potřeba věnovat zvýšenou pozornost a péči. Dvě dekády před vyhlášením plánu globální eliminace VHC infekce vznikl ve zdravotnickém zařízení Remedis, kde byla práce realizována, „Program komplexní péče pro pacienty s komorbiditou závislosti“.
Metody: Hodnotili jsme všechny pacienty, kteří byli v metadonovém programu k 1. 3. 2020, bez ohledu na individuální délku trvání substituce, dávku substituční medikace, věk nebo pohlaví. Byla zpracována jejich epidemiologická a demografická data získaná při strukturovaném interview a laboratorní nálezy.
Výsledky: Ve skupině 24 pacientů na substituční léčbě metadonem bylo před zahájením péče anti-HCV negativních celkem 12 (50 %) pacientů. U žádného z těchto 12 subjektů nedošlo během substituční léčby k nové infekci HCV (virus hepatitidy C). Dalších 12 pacientů ze sledované skupiny bylo anti-HCV pozitivních. Deset pacientů již úspěšně absolvovalo léčbu VHC, u dvou došlo k reinfekci po léčbě.
Závěr: Předložená práce potvrzuje vysokou účinnost léčby VHC mezi PWID při navození vhodných podmínek. Spojení léčby HCV infekce a cílené individualizované adiktologické péče považujeme za předpoklad k dosažení kontroly nad epidemií VHC v ČR, s možným pozitivním dopadem také na další krví přenosné infekce související s rizikovým chováním.
Klíčová slova:
virus hepatitidy C (HCV) – virová hepatitida typu C (VHC) – osoby injekčně užívající návykové látky (PWID – People Who Injected Drugs) – opiátová substituční léčba (OST) – metadon (MTD) – Remedis, Praha
ÚVOD
Pandemie chronické virové hepatitidy C (VHC) je intenzivně sledována řadu let. Postupně se mění spektrum pacientů, kteří jsou HCV infikováni. Z původně iatrogenního onemocnění se ve vyspělých evropských zemích a v Spojených státech amerických (USA) stalo onemocnění asociované převážně s injekční aplikací návykových látek (NL). Zavedením nových účinných virostatik je VHC vyléčitelné onemocnění. Tím se podstatně změnil přístup k diagnostice a léčbě této závažné chronické nemoci. V roce 2016 byl zveřejněn akční plán WHO s cílem globálně eliminovat HCV infekci do roku 2030.
Výskyt HCV infekce mezi PWID
Podle posledních odhadů je celosvětově infikováno přibližně 1 % populace. Asi 71 milionů osob žije s HCV infekcí [1, 2]. Globální incidence HCV, odhadovaná matematickým modelováním, byla 23,7 : 100 000, tedy 1,75 milionů nově infikovaných osob v roce 2015 [1].
Zpráva WHO z roku 2017 odhaduje 1,34 milionů úmrtí asociovaných s chronickými virovými hepatitidami, a to 720 000 v souvislosti s fatálními komplikacemi jaterní cirhózy a 470 000 úmrtí na hepatocelulární karcinom [3, 4]. Od roku 2000 se počty těchto úmrtí zvýšily o 22 %. Na rozdíl od mortality asociované s HIV/AIDS či tuberkulózou, mortalita spojená s virovými hepatitidami dosud nekulminovala.
Pandemie VHC postihuje s různou prevalencí všechny regiony. Podle WHO je nejvíce zasažen Blízký východ s incidencí 62,5/100 000 obyvatel a na druhém místě figuruje Evropa s incidencí 61,8/100 000 obyvatel. Za většinou nových HCV infekcí ve vyspělých zemích stojí injekční aplikace návykových látek mezi PWID [5, 6, 7, 8]. Podle aktuálního odhadu z roku 2019 je nakaženo až 6,1 miliónů PWID [9, 10]. V roce 2015 bylo z celkového počtu 1,7 milionu nových infekcí 23 % mezi PWID [11, 12, 13]. V Evropě jsou 2/3 nových HCV infekcí v přímé souvislosti s injekční aplikací NL [14]. Globální prevalence VHC mezi PWID je odhadována kolem 40 % [15, 16]. V Evropské unii (EU) je diagnostikováno pouze 36 %, zatímco v USA až 50 % nemocných [16, 17].
Česká republika (ČR) patří mezi země s nízkou séroprevalencí HCV, zejména díky velmi dobré úrovni zdravotnictví, používání jednorázových pomůcek a rychlému zavedení testování dárců krve na přítomnost anti-HCV protilátek. Podstatnou roli mají též efektivní preventivní a léčebné tzv. „harm reduction“ programy v rámci adiktologické péče o rizikově se chovající uživatele NL. Tyto programy byly v ČR zaváděny již začátkem 90. let minulého století, čímž zabránily a dosud účinně brání rozšíření HIV/AIDS mezi PWID a udržují relativně stabilní situaci s ohledem na šíření HCV infekce v této rizikové skupině. Podle séroprevalenčního přehledu z roku 2001 byla anti-HCV séroprevalence v obecné populaci v ČR 0,2 % [18].
Před objevem viru HCV a před zavedením screeningového vyšetřování dárců krve v roce 1992 se nákaza HCV v ČR šířila převážně iatrogenně [19, 20]. Po zavedení testování dárců krve a jednorázového injekčního materiálu ve zdravotnictví se hlavní cestou šíření HCV stala injekční aplikace NL [21]. U nás je situace specifická i tím, že k masovému užívání NL došlo ve srovnání s ostatními vyspělými státy relativně pozdě, až v 90. letech minulého století, v souvislosti s politickými změnami.
Reprezentativní multicentrická séroprevalenční studie mezi klienty nízkoprahových center z roku 2006 udává průměrnou séropozitivitu u PWID 34,97 % s významnou variabilitou v jednotlivých regionech [22]. V roce 2018 realizovalo Národní monitorovací středisko pro drogy a závislosti (NMS) celorepublikovou studii Séroprevalence VHC u injekčních uživatelů drog 2018. Jednalo se o multicentrickou průřezovou dotazníkovou studii s testováním anti-HCV protilátek. Testování proběhlo pomocí rychlých imunochemických testů z kapilární krve nebo ze slin. Studijní populaci tvořili aktivní PWID kontaktovaní v nízkoprahových centrech po celé ČR. Výsledná séroprevalence v popsané studii je 37,1 %, opět s významnými rozdíly v jednotlivých krajích ČR [23]. Míra incidence HCV infekcí mezi PWID byla v ČR v minulé dekádě hlášena mezi 11–15 případy na 100 sledovaných osob a rok [24, 25].
Pro posouzení rozsahu výskytu HCV v ČR musíme vycházet z odhadů velikosti rizikové populace uživatelů NL a kvalifikovaných odhadů rizikovosti jejího chování. Můžeme se opřít o výroční zprávy NMS, jehož poslední vydaná zpráva zahrnuje zpracovaná data z roku 2018 [23]. Při odhadovaném počtu 43 700 PWID v ČR [26], séroprevalenci 34,97 % [22] a předpokládaném 70% přechodu VHC infekce do chronicity lze odhadnout 9 500–12 000 aktivních PWID s chronickou HCV infekcí[26].
WHO PLÁN GLOBÁLNÍ ELIMINACE VHC
V roce 2016 prezentovala WHO akční plán, jehož cílem je získat kontrolu nad šířící se HCV infekcí a následně toto onemocnění eliminovat. Plán globální eliminace HCV infekce předpokládá do roku 2030 naplnění tří klíčových cílů: 1. dosáhnout 65% poklesu mortality v souvislosti s jaterními onemocněními, 2. snížit počty nových HCV infekcí o 90 % a 3. zvýšit podíl diagnostikovaných infekčních pacientů na 90 % [27].
Se zavedením přímo působících virostatik (DAA, Direct-Acting Antiviral) do léčby VHC v EU od roku 2014 se první cíl, snížení počtu úmrtí v souvislosti s pokročilou HCV infekcí, jeví jako dosažitelný. DAA režimy na rozdíl od předchozích terapeutických možností mají významně vyšší účinnost, hodnoceno proporcí setrvalých virologických odpovědí (SVR, sustained virological response). Navíc jsou indikované a dobře tolerované i u pacientů s komorbiditami nebo pokročilým jaterním onemocněním, což bylo při léčbě režimy s interferonem zásadním limitem [28, 29]. Zavedením DAA do léčby HCV infekce je v EU od roku 2014 jasně patrný nárůst léčených pacientů.
Největší výzvou je požadavek na snížení počtu nových HCV infekcí. PWID představují v EU nejrizikovější skupinu pro přenos HCV. Pouze širší nabídka harm reduction programů a nelimitovaná léčba DAA režimy v rizikově se chovající populaci povede reálně ke snížení rizika nových infekcí v této skupině. Nová strategie „léčba jako prevence VHC“ mezi PWID je efektivní [30].
Již uvedená skutečnost, že skoro 2/3 infikovaných osob o své chorobě vůbec neví, akcentuje nutnost zlepšit a rozšířit dostupnost testování anti-HCV protilátek v EU i celosvětově. V tak vyspělé oblasti, jako je EU, stále více než polovina infikovaných osob s HCV infekcí o svém onemocnění neví [17].
WHO explicitně označila problematické subpopulace (PWID, lidé bez domova, vězni, migranti z rozvojových zemí a endemických oblastí pro HCV, muži, mající sex s muži, osoby s koinfekcí HIV/HCV) [13], kterým je potřeba věnovat zvýšenou pozornost a péči. V těchto skupinách k šíření HCV aktivně dochází a jsou novými ohnisky infekce. Jedinci z uvedených podskupin, které se často překrývají, mají významně omezený přístup k jakékoli zdravotní péči, včetně testování na krví přenosné infekce a tím i k případné léčbě HCV infekce. Je popsána řada překážek, ať již ze strany potenciálních pacientů, poskytovatelů péče nebo zdravotnického systému, které brání PWID v zahájení léčby, v udržení se v léčebném programu a v úspěšném dokončení léčby HCV infekce. Velmi časté jsou stigmatizace PWID, nedostatek informací, špatná sociální situace, obavy z léčby a vedlejších účinků, nedůvěra, neempatický přístup zdravotníků a nedostatek zkušeností při práci s PWID [31, 32].
Program komplexní péče pro pacienty s komorbiditou závislosti v Remedis
Program poskytuje široké spektrum odborné péče v rámci jednoho zdravotnického zařízení. S cílem dlouhodobé stabilizace je pacientům nabízena léčebně preventivní péče internistou a gastroenterologem, poskytována intenzivní péče adiktologů a sociálních pracovníků, spolu s podporou psychiatra a klinického psychologa. Infekčním PWID je nabízena specifická protivirová terapie, v minulosti se jednalo o dlouhodobou léčbu interferonem a ribavirinem, v současné době jsou pacienti léčeni DAA režimy. Smyslem našeho přístupu není pouze léčba infekčního onemocnění. Dlouhodobá spolupráce s pacientem pomáhá udržovat změny životního stylu a je prevencí relapsu závislosti nebo reinfekce HCV.
Substituční léčba metadonem
Metadonová substituční terapie se obecně zaměřuje na zlepšení zdravotního, psychického a sociálního stavu osob s diagnostikovanou závislostí s preferencí opioidů. Léčba je určena pacientům, kteří nejsou schopni stabilizace bez použití agonistů opiátových receptorů. Nástrojem OST je poskytování substituční látky (metadonu, MTD), a to v množstvích, která funkčně potlačují odvykací příznaky a umožňují všestranně zlepšit kvalitu života pacienta. Program má striktně stanovená pravidla, jejich dodržování je průběžně kontrolováno a vyžadováno. MTD program v Remedisu je schopen poskytovat komplexní péči ambulantní formou maximálně 30 pacientům v daném čase.
METODY
Soubor pacientů
Hodnotili jsme všechny pacienty, kteří byli k 1. 3. 2020 substituováni metadonem, bez ohledu na individuální délku trvání OST, dávku substituční medikace, věk nebo pohlaví. Práce probíhala monocentricky. Standardně byl každý pacient před zahájením MTD programu vyšetřován internistou a gastroenterologem, testován na virové hepatitidy A, B a C, dále na infekci virem HIV 1, 2 a na syfilis. Všem bylo také provedeno elektrokardiografické vyšetření (EKG), ultrasonografické vyšetření břicha a od roku 2015 fibroscan. Rentgenové vyšetření srdce a plic bylo provedeno u pacientů starších 40 let nebo u pacientů s anamnézou bezdomovectví, pobytu ve výkonu trestu odnětí svobody (VTOS) nebo kontaktu s tuberkulózou. Testování na krví přenosné infekce se v našem OST programu standardně opakuje v 6–12měsíčním intervalu a vždy po rizikovém chování. U pacientů na OST metadonem je navíc každé 3 měsíce kontrolováno EKG. Součástí ambulantní adiktologické péče je také předtestové poradenství a edukace o možnostech léčby krví přenosných infekcí.
Všichni pacienti podepsali informovaný souhlas se zpracováním poskytnutých údajů v této studii. U všech subjektů byla získávána anamnestická a epidemiologická data formou strukturovaného interview a pomocí anamnestického dotazníku, který je v Remedisu využíván již několik let. Během opakovaných kontaktů byly anamnestické a epidemiologické údaje průběžně aktualizovány.
Laboratorní vyšetření
U všech subjektů byly z krevního séra testovány základní biochemické parametry (AST, ALT, ALP, GGT a bilirubin) a markery přenosných chorob: virové hepatitidy typu A, B, C, infekce HIV/AIDS a lues. Testování krevních vzorků probíhalo v certifikované laboratoři, standardizovanými sérologickými testy protilátek Abbott na analyzátorech ARCHITECT. V případě pozitivity anti-HCV protilátek byla diagnóza virové hepatitidy typu C dále konfirmována pomocí virologických testů založených na přímém průkazu virové RNA pomocí polymerázové řetězové reakce (PCR). K virologické diagnostice byly opět využity standardní diagnostické sety. Kit pro Real-time PCR: ARTUS HCV RG RT-PCR Kit (Qiagen), přístroj pro Real-time PCR: RorGene Q (Qiagen). Genotypizace byla prováděna pomocí Kitu HCV genotypizace (Kitgen).
Zpracování dat
Osobní, demografická a epidemiologická data získaná při odběru anamnézy a strukturovaném interview byla dále analyzována s využitím statistických programů Microsoft Excel a IBM SPSS software. Studie byla schválena etickou komisí organizace.
VÝSLEDKY
Ve sledovaném intervalu bylo v OST metadonem léčeno celkem 24 osob, tedy přibližně 10 % všech substituovaných pacientů v Remedisu. Modality substituční léčby dokumentuje graf na obrázku 1.
Obr. 1a, 1b. Modality substituční léčby – porovnání OST Remedis a OST v ČR podle posledních údajů NMS
a) poskytovaná substituční látka v OST, Remedis v roce 2019
b) poskytovaná substituční látka v ČR podle posledních údajů Národního monitorovacího střediska pro drogy a závislosti
Figure 1a, 1b. OST modalities – comparison of OST at Remedis and OST in the Czech Republic based on the most recent of data of National Monitoring Center for Drugs and Addictions
(a) provided substitution substance in OST, Remedis in 2019
(b) provided substitution substance in the Czech Republic according to the latest data of the National Monitoring Center for Drugs and Addictions
Sledovaný soubor pacientů představuje relativně stabilní skupinu, průměrná doba léčby OST MTD v této skupině je 26,55 měsíců, v rozmezí 7–85 měsíců. Muži jsou v substituci MTD průměrně 19,5 měsíců (7–40), ženy 45 měsíců (14–85). Každý pacient dochází pravidelně pro denní dávku MTD, průměrná dávka 101 mg MTD na den (min. 9 mg – max. 140 mg, medián 110). Subjektům bylo v průměru 44,87 roku (32–65 let). Celkem bylo v MTD programu 20 mužů (83 %) s průměrným věkem 44,45 roků (medián 42,5) a 4 ženy (17 %) s průměrným věkem 47,75 roků (medián 49,5).
Ve skupině 24 pacientů na OST metadonem byla před zahájením substituční léčby, zjištěna protilátka proti viru hepatitidy A – anti-HAV total (IgG) u 8 mužů a 3 žen (u 46 % osob). V průběhu sledování a léčby v OST programu došlo u jednoho pacienta, který byl vstupně negativní k vytvoření protilátky anti-HAV total. Nebyl si vědom, že by někde podstoupil očkování proti HAV (virus hepatitidy A) nebo prodělal v mezičase novou infekci. Příznaky akutní virové hepatitidy typu A ve sledovaném období neměl, což ale nevylučuje asymptomatický průběh.
Žádný ze sledovaných pacientů na metadonové substituci nebyl vstupně HBsAg pozitivní a neměl známky akutní či chronické virové hepatitidy B (VHB), u nikoho také nedošlo během sledovaného období do 3/2020 k nové infekci HBV (virus hepatitidy B). Deset pacientů (42 %) mělo detekovatelné protilátky svědčící o prodělané VHB před zahájením OST v Remedisu, další 3 pacienti (13 %) – 2 muži a 1 žena – byli očkováni.
V době vstupních odběrů před zahájením OST bylo anti-HCV negativních celkem 50 % pacientů (11 mužů a 1 žena). U žádného z těchto 12 subjektů nedošlo během sledování po zahájení substituční léčby k nové HCV infekci. Průměrná doba sledování těchto anti-HCV negativních subjektů v OST v Remedisu byla 28 měsíců.
Výsledky sérologických vyšetření shrnuje tabulka 1.
Tab. 1. Výsledky sérologie pacientů před zahájením OST MTD
Table 1. Serology results of patients before initiation of OST with MTD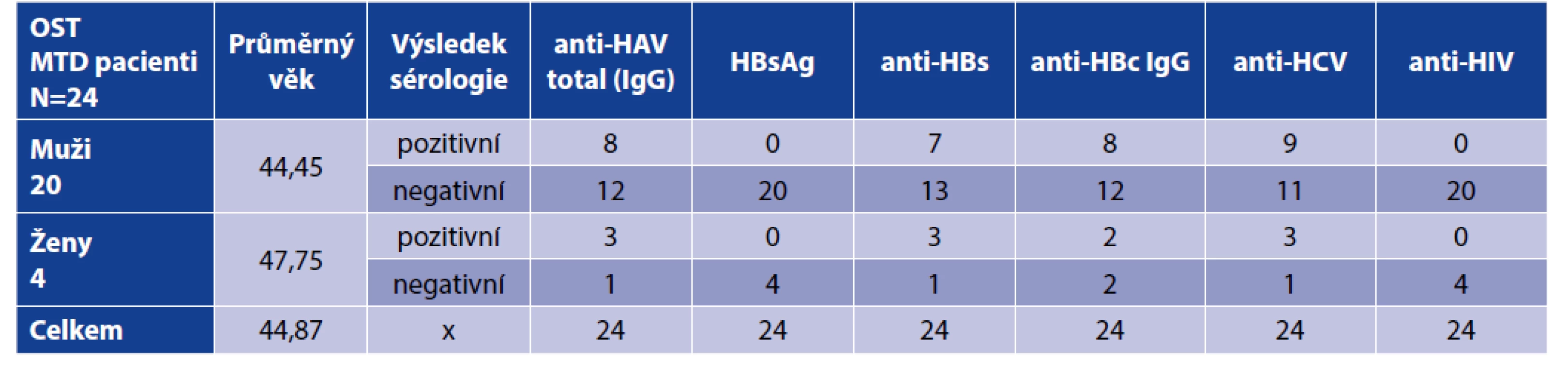
Ze sledované skupiny bylo 50 % pacientů (9 mužů a 3 ženy) anti-HCV pozitivních. Průměrný věk anti-HCV pozitivních pacientů byl 50 let (49,82 let). U 75 % anti-HCV pozitivních osob (6 mužů a 3 ženy) byla potvrzena i HCV RNA v krevním séru. Jednalo se o subjekty s chronickou HCV infekcí. Podle anamnestických údajů byla průměrná doba trvání HCV infekce 82 měsíců v době potvrzení diagnózy v Remedisu.
Tři pacienti byli anti-HCV pozitivní a bez průkazu virémie (PCR HCV RNA negativní) v době zahájení OST. Jeden z nich nebyl nikdy specificky léčen, je to pacient po spontánní clearance HCV infekce. Ve dvou případech se jednalo o muže, kteří byli v naší péči ještě před nástupem do OST. Oba léčbu HCV podstoupili ve výkonu trestu odnětí svobody (VTOS), v roce 2012, respektive 2014. Byli léčeni v té době standardní 2k léčbou (dvojkombinací pegylovaného interferonu alfa a ribavirinu), vyléčili se a dosáhli setrvalé virologické odpovědi (SVR). Po propuštění z VTOS navázali na spolupráci a nastoupili substituční léčbu. Oba dobře spolupracují v rámci OST programu a jsou bez detekovatelné HCV virémie celkem 13, respektive 84 měsíců od zdokumentované SVR.
Pacienti, kteří měli vstupně diagnostikovanou replikující HCV infekci, podstoupili specifickou léčbu HCV infekce v průběhu OST metadonem. U všech pacientů byly v souladu s předchozím pozorováním genotypového zastoupení u PWID v ČR detekovány pouze HCV genotypy 1 (subtyp 1a a 1b) a 3 (3a) [33, 34].
První žena, 55letá, absolvovala léčbu VHC krátce po zahájení OST v Remedisu již v roce 2013. Léčila se ještě 2k (tedy kombinací pegylovaného interferonu alfa a ribavirinu), dosáhla SVR a je dlouhodobě zdravotně i sociálně stabilní bez detekovatelné HCV virémie.
Čtyři muži a jedna žena absolvovali léčbu DAA režimy a dosáhli SVR, která je po léčbě DAA dokumentovaná 12. týden po dokončení farmakoterapie a jsou dlouhodobě bez detekovatelné virémie (tabulka 2).
Tab. 2. Charakteristika viremických pacientů – vztah OST a specifické virostatické léčby HCV infekce
Table 2. Characteristics of viremic patients – relationship between OST and specific virostatic treatment of HCV infection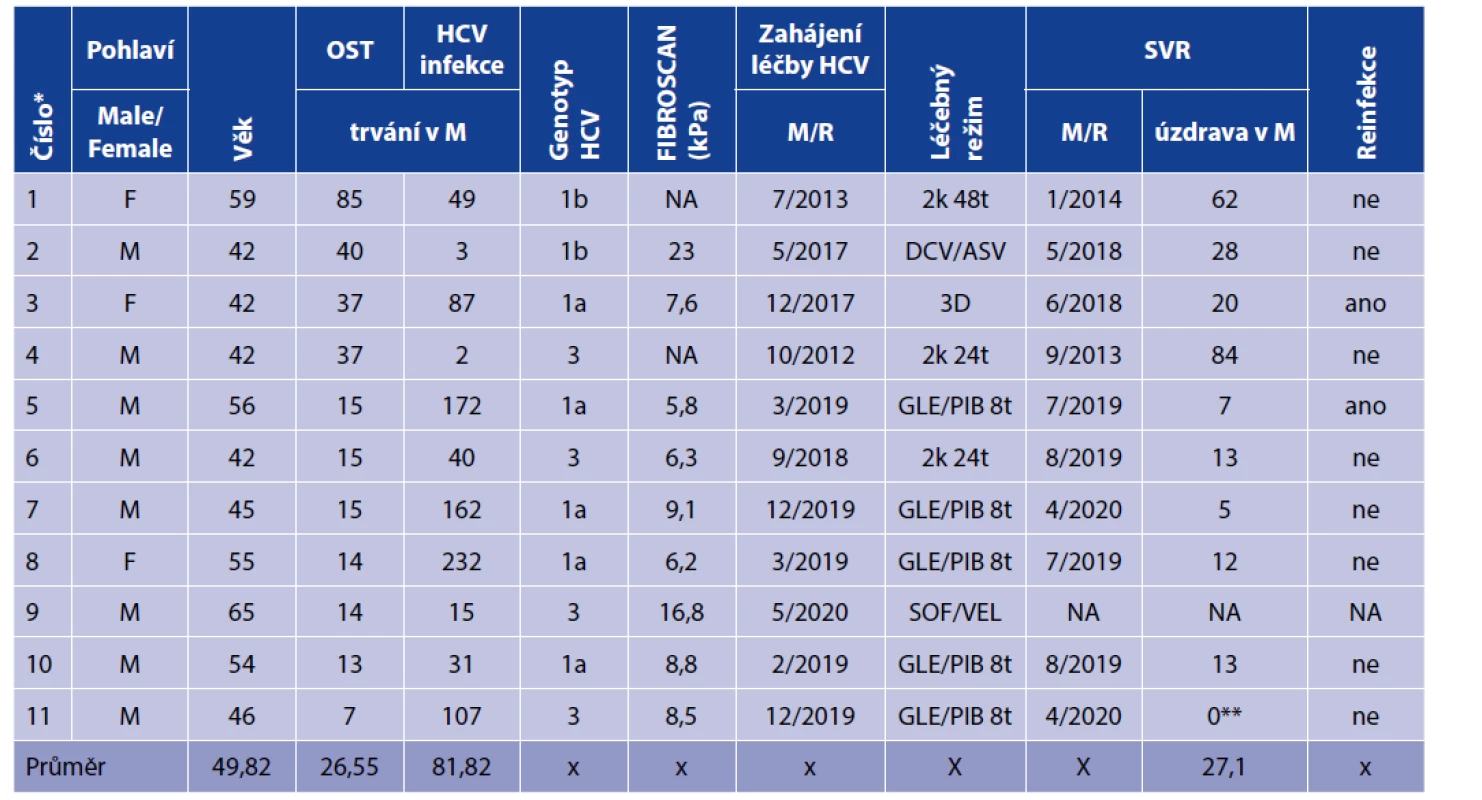
Legenda:
M = měsíc, M/R = měsíc/rok
*pacienti řazeni podle délky OST
**dosud nerealizovaný odběr 6 měsíců po SVR
NA = není k dispozici/neaplikovatelné
Léčebné režimy: 2k – pegylovaný interferon alfa + ribavirin; SOF/VEL – Sofosbuvir + velpatasvir; DCV/ASV – daclatasvir + asunaprevir; 3D – ombitasvir + paritaprevir + ritonavir + dasabuvir (+ ribavirin); GLE/PIB – glecaprevir +pibrentasvir
Legend:
M=month, M/R = month/year
*patients in order by OST duration
**sample still waiting to be collected six months after sustained virologic response (SVR)
NA = not available/not applicable
Therapeutic regimens: 2k – pegylated interferon alpha + ribavirin; SOF/VEL – sofosbuvir + velpatasvir; DCV/ASV – daclatasvir + asunaprevir; 3D – ombitasvir + paritaprevir + ritonavir + dasabuvir (+ ribavirin); GLE/PIB – glecaprevir +pibrentasvirSVR byla po terapii DDA režimem dokumentovaná také u dalšího muže (56 let). Při posledním odběru 9 měsíců po potvrzení SVR však měl opět zjištěnou HCV RNA v séru. Vzhledem k předchozím výsledkům a skutečnosti, že se jednalo o záchyt jiného subtypu, než pro který byl pacient léčen (původně 1b, následně 1a), se jedná o reinfekci HCV. Tento pacient zvládá metadonový program v bazálním režimu, jako harm reduction podporu. K reinfekci došlo při metamfetaminovém relapsu.
Třetí žena se rovněž léčila v průběhu OST DAA režimem a dosáhla SVR. Při kontrolních odběrech 21 měsíců od dokumentované SVR jsme u ní zaznamenali reinfekci. Nejednalo se o porušení pravidel OST (relaps), pacientka uvedla jako zdroj infekce nechráněný pohlavní styk s rizikovým partnerem (PWID), který se prezentoval jako zdravý, z HCV infekce vyléčený.
Nejstarší pacient, 65letý muž s genotypem 3, byl k léčbě více než rok připravován. Jde o dlouholetého PWID, který má četné zdravotní (akutní a chronické) komplikace a je značně sociálně nestabilní (casus socialis). Specifickou léčbu již zahájil, ale její výsledek zatím nelze hodnotit.
Sumárně bylo v metadonovém programu 11 pacientů (46 % souboru) indikovaných k léčbě chronické HCV infekce. U všech pacientů došlo při léčbě k dosažení virologické odpovědi. Po terapii je 8 pacientů, kteří dosáhli SVR a dál zůstávají v kontaktu. Průměrná délka sledování je 27 měsíců od zdokumentované SVR po terapii bez reinfekce. Další pacient specifickou léčbu zahájil až v současné době, jeho výsledky zatím nemůžeme vyhodnotit. U dvou pacientů, 56letý muž, krátkodobý pacient (10 měsíců v OST) a 42letá žena, která patří, co se týče délky OST v našem programu mezi střednědobé pacienty s 33 měsíci na OST, došlo k reinfekci HCV po úspěšné léčbě. Charakteristiky viremických pacientů v OST v Remedis shrnuje tabulka 2.
DISKUSE A ZÁVĚR
Prezentované výsledky s minimem nových infekcí a reinfekcí HCV dokumentují účinek realizovaných preventivních a léčebných intervencí. Nabízené služby umožňují pacientům postupně měnit návyky a zvyšovat bezpečnost jejich chování. Cílená adiktologická péče, konzultační a poradenský servis a pravidelný kontakt PWID se specialisty zvyšuje účinnost léčby. Multidisciplinární péče v Remedisu je zaměřena na omezení zdravotních, psychických a sociálních rizik spojených s užíváním NL, cílem je stabilizace pacienta a/nebo dosažení abstinence. Respektujeme momentální stav pacienta a jeho možnosti, každému je nabízeno takové spektrum péče, kterou je schopen zvládnout a aktivně se na ní spolupodílet. Kontakt majoritní populace s PWID v zdravotnickém zařízení má potenciál snižovat marginalizaci uživatelů NL a jasný destigmatizační efekt. V důsledku stárnutí populace PWID [35] se ukazuje potřeba OST ve smyslu paliativní péče (reinfekce 56letého pacienta), posílení edukace stran bezpečnějšího sexuálního chování a podpoření harm reduction intervencí, jako například distribuce kondomů (reinfekce 42leté pacientky).
Zavedení DAA režimů až s 95% účinností do léčby VHC dává reálnou šanci eliminovat HCV infekci [36]. Pro snížení incidence podle stávajícího plánu WHO do roku 2030, je třeba dostat pod kontrolu šíření HCV mezi PWID [37]. Práce dokumentuje, že při vhodných podmínkách lze navázat kontakt i s jinak obtížně dostupnou rizikovou populací PWID. Ukazuje také, jak strukturovaná může být péče o PWID pacienty s komorbiditou krví přenosných infekcí. Zahraniční studie jednoznačně prokázaly, že OST snižuje riziko nové HCV infekce o 50 % mezi participanty harm reduction programů a efekt substituční léčby se zvýší až na 74 % při současném používání výhradně nových parafernálií k injekční aplikaci [38, 39, 40].
Studie s aktivními PWID potvrdily, že současné užívání NL a/nebo OST účinnost DAA režimů nesnižuje a není racionální důvod neléčit tuto subpopulaci [39]. Také ve zde prezentované skupině léčených pacientů dosáhli všichni SVR.
Mezi PWID jsou další překážkou plánované eliminace reinfekce. V literatuře jsou zatím dostupné převážně práce sledující reinfekce po předchozí terapii HCV interferonem. Riziko reinfekce bylo 6 % za rok u pacientů, kteří pokračovali v injekční aplikaci NL po skončení léčby [41, 42, 44]. Po léčbě DAA byl počet reinfekcí 4,2 na 100 osob za rok – podle pozorování mezi 74 účastníky studie C-EDGE CO-STAR, kteří dosáhli SVR a následně opět injekčně aplikovali NL [43]. Reinfekce se budou mezi PWID objevovat. Je to důsledek jejich základního onemocnění – závislosti. Důležité je s PWID pacienty zůstat v kontaktu i po proběhlé léčbě, dále pokračovat a podporovat jejich participaci v programech OST a současně nabízet opakované testování – ideálně 2krát do roka a vždy po epizodách rizikového chování [11, 44].
Většina našich dlouhodobých pacientů je po úspěšné léčbě sledována více než 2 roky. Při kontaktu s pacientem po léčbě a jeho pravidelném testování (dispenzární péče) jsme schopni reinfekce časně diagnostikovat a pacienty o změně zdravotního stavu informovat. Tím přispíváme ke snížení rizika dalšího šíření v pacientově nejbližším sociálním okolí, zejména mezi jeho PWID kontakty. WHO doporučuje nelimitovaný přístup PWID pacientů k testování a léčbě infekcí (treatment-as-prevention) a reinfekcí [45, 46]. Pravidelné testování na přítomnost infekčních krví či sexuálně přenosných onemocnění, by mělo být standardní součástí péče o všechny adiktologické pacienty. Edukaci o harm reduction tématech a motivaci k léčbě krví a pohlavně přenosných onemocnění doporučujeme jako nedílnou součást individuální adiktologické péče o pacienty.
Do redakce došlo dne 18. 5. 2020.
Adresa pro korespondenci:
PhDr. Lenka Vavrinčíková, PhD.
Remedis s. r. o.
Táborská 325/57
140 00 Praha 4
e-mail: vavrincikova@remedis.cz
Zdroje
1. Global Hepatitis Report 2017 [online]. Geneva: World Health Organization [cit. 2020-02-28]. Dostupný na www: https://apps.who.int/iris/bitstream/handle/10665/255016/9789241565455-eng.pdf?sequence=1.
2. Blach S, Zeuzeum S, Manns M, et al. Global prevalence and genotype distribution of hepatitis C virus infection in 2015: a modelling study. The Lancet [online], 2017;2(3):161–176. [cit. 2020-05-01]. Dostupný na www: https://linkinghub.elsevier.com/retrieve/pii/S2468125316301819.
3. Stanaway D, Flaxman AD, Naghavi M, et al. The global burden of viral hepatitis from 1990 to 2013: findings from the Global Burden of Disease Study 2013. The Lancet [online], 2016; 388(10049):1081–1088 Dostupný z www: https://linkinghub.elsevier.com/retrieve/pii/S0140673616305797.
4. Razavi H, Elkhoury C, Elbasha E, et al. Chronic hepatitis C virus (HCV) disease burden and cost in the United States. Hepatology, 2013;57(6):2164–2170. Dostupný z www: http://doi.wiley.com/10.1002/hep.26218.
5. Buckley GJ, Strom BL. Eliminating the public health problem of hepatitis B and C in the United States: phase one report. Washington, DC: the National Academies Press, 2016.
6. Zibbel JE, Iqbal KC, Patel RC, et al. Increases in hepatitis C virus infection related to injection drug use among persons aged ≤30 years – Kentucky, Tennessee, Virginia, and West Virginia, 2006-2012. MMWR. Morbidity and mortality weekly report, 2015; 64(17): 453–458.
7. Suryaprasad AG, White JZ, Xu F, et al. Emerging Epidemic of Hepatitis C Virus Infections Among Young Nonurban Persons Who Inject Drugs in the United States, 2006–2012. Clinical Infectious Diseases [online], 2014; 59(10): 1411-1419. [cit. 2020-04-16]. Dostupný na www: https://academic.oup.com/cid/article-lookup/doi/10.1093/cid/ciu643.
8. Guidelines for the screening care and treatment of persons with chronic hepatitis C infection, 2016. Updated version April 2016. Geneva: World Health Organization. ISBN 978-92-4-154961-5. [cit. 2020-04-16]. Dostupný na www: https://apps.who.int/iris/bitstream/handle/10665/205035/9789241549615_eng.pdf?sequence=1.
9. Hajarizadeh B, Cunningham EB, Reid H, et al. Direct-acting antiviral treatment for hepatitis C among people who use or inject drugs: a systematic review and meta-analysis [online], 2018;3(11). [cit. 2020-03-31]. Dostupný z www: https://linkinghub.elsevier.com/retrieve/pii/S2468125318303042.
10. Grebbely J, Larney S, Peacock A, et al. Global, regional, and country-level estimates of hepatitis C infection among people who have recently injected drugs. Addiction [online], 2019;114(1):150–166. [cit. 2020-03-31]. Dostupný z www: http://doi.wiley.com/10.1111/add.14393.
11. Hagan H, Pouget ER, Des Jarlais DC, et al. Meta-Regression of Hepatitis C Virus Infection in Relation to Time Since Onset of Illicit Drug Injection: The Influence of Time and Place. American Journal of Epidemiology [online], 2008;168(10):1099–1109. [cit. 2020-03-31]. Dostupný na www: https://academic.oup.com/aje/article-lookup/doi/10.1093/aje/kwn237.
12. Wiessing L, Ferri M, Grady B, et al. Hepatitis C Virus Infection Epidemiology among People Who Inject Drugs in Europe: A Systematic Review of Data for Scaling Up Treatment and Prevention. PLoS ONE [online], 2014; 9(7): Dostupný na www: https://dx.plos.org/10.1371/journal.pone.0103345.
13. Global Health Sector Strategy on Viral Hepatitis 2016 - 2021: Towards ending viral hepatitis [online], 2016. In: Geneva: World Health Organization, s. 1–56 [cit. 2020-07-31]. Dostupný na www: https://apps.who.int/iris/bitstream/handle/10665/246177/WHO-HIV-2016.06-eng.pdf?sequence=1.
14. Degenhardt L, Charlson F, Stanaway J, et al. Estimating the burden of disease attributable to injecting drug use as a risk factor for HIV, hepatitis C, and hepatitis B: findings from the Global Burden of Disease Study 2013. The Lancet Infectious Diseases [online], 2016;16(12): 1385–1398. [cit. 2020-03-31]. Dostupný na www: https://linkinghub.elsevier.com/retrieve/pii/S1473309916303255.
15. Degenhardt L, Peacock A, Colledge S, et al. Global prevalence of injecting drug use and sociodemographic characteristics and prevalence of HIV, HBV, and HCV in people who inject drugs: a multistage systematic review. The Lancet Global Health [online], 2017;5(12):1192–1207. [cit. 2020-03-31]. Dostupný na www: https://linkinghub.elsevier.com/retrieve/pii/S2214109X17303753.
16. Edlin BR, Eckhardt BJ, Shu MA, et al. Toward a more accurate estimate of the prevalence of hepatitis C in the United States: a multistage systematic review. Hepatology [online], 2015;62(5):1353–1363. [cit. 2020-07-31]. Dostupný na www: http://doi.wiley.com/10.1002/hep.27978.
17. Denniston M, Klevens R, Mcquillan G, et al. Awareness of infection, knowledge of hepatitis C, and medical follow-up among individuals testing positive for hepatitis C: National Health and Nutrition Examination Survey 2001–2008. Hepatology [online], 2012;55(6): 1652–1661. [cit. 2020-07-31]. Dostupný na www: http://doi.wiley.com/10.1002/hep.25556.
18. Němeček, VJ, Částková P, Fritz A, et al. The 2001 serological survey in the Czech Republic-viral hepatitis. Central European Journal of Public Health, 2003;11(Supplement): S54–61.
19. Horák J, Střítezký J. Chronické hepatitidy. Praha: Grada, 1999.
20. Husa P, Střítezký J. Léčba virových hepatitid. Praha: Triton. Levou zadní, 2000.
21. Mravčík V, Chomynová P, Grohmannová K, et al. Výroční zpráva o stavu ve věcech drog pro Evropské monitorovací středisko pro drogy a drogové závislosti: Česká republika, 2017. Praha: Úřad vlády ČR, 2018. ISBN 978-80-7440-219-7.
22. Zabransky T, Mravcik V, Korcisova B, et al. Hepatitis C Virus Infection among Injecting Drug Users in the Czech Republic – Prevalence and Associated Factors. European Addiction Research [online], 2006;12(3):151–160. [cit. 2020-03-31]. Dostupný na www: https://www.karger.com/Article/FullText/92117.
23. Mravčík, V, Chomynová P, Grohmannová K, et al. Výroční zpráva o stavu ve věcech drog v České republice v roce 2018. Praha: Úřad vlády ČR, 2019. ISBN 978-80-7440-237-1.
24. Mravčík V, Šebáková H. Výskyt virových hepatitid typu B a C u injekčních uživatelů drog v okrese Karviná. Adiktologie, 2002;2(2):19–27.
25. Mravčík V. Výskyt VHC u injekčních uživatelů drog: Výsledky studie prováděné mezi klienty nízkoprahových zařízení v letech 2002–2005 [online], 2009. Praha: Úřad vlády České republiky. [cit. 2020-01-27]. Dostupný na www: https://www.drogy-info.cz/data/download/91330/393423/file/5_Vyskyt_VHC_u_injekcnich_uzivatelu_drog_ePubl.pdf.
26. Mravčík V., Janíková B., Dlouhý P. (ed.) Eliminace virové hepatitidy typu C mezi uživateli drog v České republice: východiska a akční plán na období 2019–2021. Praha: Úřad vlády České republiky, 2019.
27. Global Health Sector Strategy on Viral Hepatitis 2016 - 2021: Towards ending viral hepatitis [online], 2016. In: Geneva: World Health Organization, p. 1–56 [cit. 2020-07-31]. Dostupný na www: https://apps.who.int/iris/bitstream/handle/10665/246177/WHO-HIV-2016.06-eng.pdf?sequence=1.
28. Mitchell O, Gurakar A. Management of Hepatitis C Post-liver Transplantation: a Comprehensive Review. Journal of Clinical and Translational Hepatology [online], 2015;3(2). [cit. 2020-07-31]. Dostupný na www: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4548349/pdf/JCTH-3-140.pdf.
29. Limketkai, BN, Mehta S, Sutcliffe CG, et al. Relationship of Liver Disease Stage and Antiviral Therapy With Liver-Related Events and Death in Adults Coinfected With HIV/HCV. JAMA [online], 2012 : 308(4). [cit. 2020-03-31]. Dostupný na www: http://jama.jamanetwork.com/article.aspx?doi=10.1001/jama.2012.7844.
30. Hickman M, De Angelis D, Vickerman P, et al. Hepatitis C virus treatment as prevention in people who inject drugs. Current Opinion in Infectious Diseases [online], 2015;28(6):576–582. Dostupný na www: http://journals.lww.com/00001432-201512000-00012.
31. Tucker JD, Meyers K, Best J, et al. The HepTestContest: a global innovation contest to identify approaches to hepatitis B and C testing. BMC Infectious Diseases [online], 2017;17(S1). [cit. 2020-07-31]. Dostupný na www: http://bmcinfectdis.biomedcentral.com/articles/10.1186/s12879-017-2771-4.
32. Edland-Gryt M, Skatvedt AH. Thresholds in a low-threshold setting: An empirical study of barriers in a centre for people with drug problems and mental health disorders. International Journal of Drug Policy [online], 2013;24(3):257–264. [cit. 2020-07-31]. Dostupný na www: https://linkinghub.elsevier.com/retrieve/pii/S0955395912001193.
33. Krekulova L, Rehak V, Madrigal N, et al. Genotypic and Epidemiologic Characteristics of Hepatitis C Virus Infections among Recent Injection Drug User and Nonuser Populations. Clinical Infectious Diseases [online], 2001;33(8):1435–1438. [cit. 2020-03-31]. Dostupný na www: https://academic.oup.com/cid/article-lookup/doi/10.1086/323199.
34. Krekulová L, Řehák V, Oktábec Z, et al. HCV genotype shift occurred over the 15 years in PWIDs in the Czech Republic. Epidemiology, Microbiology, Immunology [online], 2019;68(1): 3–8. [cit. 2020-03-31]. Dostupný na www: https://www.prolekare.cz/casopisy/epidemiologie/2019-1-20/vyvoj-v-zastoupeni-genotypu-hcv-u-injekcnich-uzivatelu-drog-v-ceske-republice-behem-15-let-112615/download?hl=cs.
35. European Drug Report: Trends and Developments [online]. In: Luxembourg: Publications Office of the European Union. Lisbon: The European Monitoring Centre for Drugs and Drug Addiction, 2016 : 1–84. [cit. 2020-07-31]. Dostupný na www: https://www.emcdda.europa.eu/system/files/publications/2637/TDAT16001ENN.pdf .
36. Asselah T, Marcellin P, Schinazi RF. Treatment of hepatitis C virus infection with direct-acting antiviral agents: 100% cure?. Liver International, 2018;38(2):7–13. DOI: 10.1111/liv.13673. ISSN 14783223. [cit. 2020-03-31]. Dostupný na www: http://doi.wiley.com/10.1111/liv.13673.
37. Dillon JF, Lazarus JV, Razavi HA. Urgent action to fight hepatitis C in people who inject drugs in Europe. Hepatology, Medicine and Policy [online], 2016;1(1). Dostupný na www: http://hmap.biomedcentral.com/articles/10.1186/s41124-016-0011-y.
38. Platt L, Minozzi S, Reed J, et al. Needle and syringe programmes and opioid substitution therapy for preventing HCV transmission among people who inject drugs: findings from a Cochrane Review and meta-analysis. Addiction, 2018;113(3):545–563. DOI: 10.1111/add.14012. ISSN 09652140. Dostupný na www: http://doi.wiley.com/10.1111/add.14012.
39. Grebely J, Dalgard O, Conway B, et al. Sofosbuvir and velpatasvir for hepatitis C virus infection in people with recent injection drug use (SIMPLIFY): an open-label, single-arm, phase 4, multicentre trial. The Lancet Gastroenterology & Hepatology [online], 2018;3(3):153–161 [cit. 2020-08-20]. DOI: 10.1016/S2468-1253(17)30404-1. ISSN 24681253. [cit. 2020-07-31]. Dostupný na www: https://linkinghub.elsevier.com/retrieve/pii/S468125317304041.
40. Midgard H, Bjǿro B, MÆland, A, et al. Hepatitis C reinfection after sustained virological response. Journal of Hepatology, 2016;64(5):1020–1026. DOI: 10.1016/j.jhep.2016.01.001. ISSN 01688278. Dostupný na www: https://linkinghub.elsevier.com/retrieve/pii/S0168827816000039.
41. Midgard H, Weir A, Palmateer A, et al. HCV epidemiology in high-risk groups and the risk of reinfection. Journal of Hepatology, 2016;65(1):S33–S45. DOI: 10.1016/j.jhep.2016.07.012. ISSN 01688278. Dostupný na www: https://linkinghub.elsevier.com/retrieve/pii/S0168827816303361.
42. Simmons B. Saleem J, Hill A, et al. Risk of Late Relapse or Reinfection With Hepatitis C Virus After Achieving a Sustained Virological Response: A Systematic Review and Meta-analysis. Clinical Infectious Diseases, 2016;62(6):683–694. DOI: 10.1093/cid/civ948. ISSN 1058-4838. Dostupný na www: https://academic.oup.com/cid/article-lookup/doi/10.1093/cid/civ948.
43. Dore GJ, Greberly J, Altice F, et al. Hepatitis C Virus (HCV) Reinfection and Injecting Risk Behavior Following Elbasvir (EBR)/Grazoprevir (GZR) Treatment in Participants on Opiate Agonist Therapy (OAT): Co-STAR Part B [ABSTRACT 195]. Hepatology, 2017;66(S1):112A. DOI: 10.1002/hep.29500. ISSN 02709139. Dostupný na www: https://aasldpubs.onlinelibrary.wiley.com/doi/epdf/10.1002/hep.29500.
44. Page KM, Morris D, Hahn JA, et al. Injection Drug Use and Hepatitis C Virus Infection in Young Adult Injectors: Using Evidence to Inform Comprehensive Prevention. Clinical Infectious Diseases, 2013;57(suppl_2):S32–S38. DOI: 10.1093/cid/cit300. ISSN 1537-6591. Dostupný na www: http://academic.oup.com/cid/article/57/suppl_2/S32/397297/Injection-Drug-Use-and-Hepatitis-C-Virus-Infection.
45. Heffernan A, Cooke GS, Nayagam S, et al. Scaling up prevention and treatment towards the elimination of hepatitis C: a global mathematical model. The Lancet [online], 2019;393(10178): 1319–1329. [cit. 2020-07-31]. Dostupný na www: https://linkinghub.elsevier.com/retrieve/pii/S0140673618322773.
46. Martin NK, Vickerman P, Hickman M. Mathematical modelling of hepatitis C treatment for injecting drug users. Journal of Theoretical Biology [online], 2011;274(1):58–66. [cit. 2020-07-31]. Dostupný na www: https://linkinghub.elsevier.com/retrieve/pii/S0022519311000038..
Štítky
Hygiena a epidemiológia Infekčné lekárstvo Mikrobiológia
Článek Reinfekce covidem-19Článek Za MUDr. Vladimírem Verhunem
Článok vyšiel v časopiseEpidemiologie, mikrobiologie, imunologie
Najčítanejšie tento týždeň
2021 Číslo 1- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Očkování proti virové hemoragické horečce Ebola experimentální vakcínou rVSVDG-ZEBOV-GP
- Koronavirus hýbe světem: Víte jak se chránit a jak postupovat v případě podezření?
-
Všetky články tohto čísla
- Opakovaně negativní PCR u pacientů s projevy covid-19: Mají či nemají infekci SARS-CoV-2?
-
Invazivní pneumokoková onemocnění u dospělých pacientů hospitalizovaných v Nemocnici Na Bulovce:
sérotypový replacement po zavedení plošné vakcinace dětí - Zkušenosti s léčbou virové hepatitidy C u injekčních uživatelů návykových látek v programu substituční léčby metadonem
- Analýza invalidity pro onemocnění HIV za roky 2010–2018
- Preventivní opatření, rizikové chování a nejčastější zdravotní obtíže u českých cestovatelů: prospektivní dotazníková studie u pacientů ošetřených na ambulanci cestovní medicíny
- Listerióza – analýza výskytu humánních případů v České republice v letech 2008–2018
- Enzymová léčba infekcí kůže a měkkých tkání
- Reinfekce covidem-19
- Potenciálny problém spoločného výskytu pandemického covidu-19 a sezónnej chrípky
- Prvé laboratórne potvrdené invazívne meningokokové ochorenie séroskupiny C s abdominálnou klinickou prezentáciou na Slovensku, 2019
-
Zemřel MUDr. Vladimír Zikmund, CSc.
(27. 5. 1925–18. 10. 2020) - Za MUDr. Vladimírem Verhunem
- Epidemiologie, mikrobiologie, imunologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Opakovaně negativní PCR u pacientů s projevy covid-19: Mají či nemají infekci SARS-CoV-2?
- Listerióza – analýza výskytu humánních případů v České republice v letech 2008–2018
- Reinfekce covidem-19
- Enzymová léčba infekcí kůže a měkkých tkání
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



