-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Časné chirurgické a cévní komplikace po resekcích aneuryzmat aortoilické oblasti
Early surgical and vascular complications after open repairs of aortoiliac aneurysms
Introduction:
The surgical procedures due to aortoiliac aneurysm (AAA) represent the most demanding procedures in conventional vascular surgery. This is due, among other things, to the relatively frequent systemic and surgical complications in polymorbid and often urgently operated patients. Surgical and vascular complications after resections of aortoiliac aneurysms are relatively common, and reintervention due to these complications is reported to range around 14%.
Method:
Retrospective clinical study of a group of patients undergoing surgical management for aortoiliac aneurysms in the period from 1 January 2010 to 31 December 2017 at the Department of Vascular and Plastic Surgery of Pardubice Hospital NPK.
Results:
In a group of 240 patients (205 males, 35 females), mortality reached a total of 10.4%, with mortality in elective cases 3.4% and 31.1% in urgent procedures (37.5% in AAA rupture). Overall, in the elective group, we recorded a total of 29 (16.2%) surgical and/or vascular complications with the necessity of 16 (8.9%) surgical, endovascular or combined interventions. In the emergency group, these complications were recorded 30 times (49%) with the need for intervention in 19 cases (31.1% of emergency procedures).
Conclusion:
Open surgical procedures on AAA are accompanied by a high incidence of systemic and surgical and/or vascular complications. These patients therefore require high attention and quality of intensive care in the postoperative period, focusing on early diagnosis and subsequent treatment of these complications.
Key words:
aortoiliac aneurysm − surgical complications – bleeding − limb ischemia − abdominal compartment syndrome
Autori: M. Pirkl 1,2; F. Krampota 1; T. Daněk 1; Michal Černý 1
Pôsobisko autorov: Oddělení cévní a plastické chirurgie, Chirurgická klinika, Pardubická nemocnice, NPK, a. s. 1; Fakulta zdravotnických studií, Univerzita Pardubice 2
Vyšlo v časopise: Rozhl. Chir., 2018, roč. 97, č. 11, s. 499-503.
Kategória: Původní práce
Súhrn
Úvod:
Operační zákroky pro aneuryzma aortoilického povodí (dále AAA) se řadí mezi velké výkony běžné cévní chirurgie. A to mimo jiné i z důvodu relativně častých systémových a chirurgických komplikací u mnohdy polymorbidních pacientů. Tyto komplikace po resekcích aortoilických výdutí jsou poměrně časté a vynucené reintervence se literárně pohybují kolem 14 %.
Metoda:
Ve své práci jsme retrospektivně hodnotili soubor pacientů operačně řešených pro aneuryzma aortoilické oblasti v období 1. 1. 2010 až 31. 12. 2017 na Oddělení cévní a plastické chirurgie Pardubické nemocnice NPK, a. s.
Výsledky:
V souboru 240 operovaných pacientů (205 mužů, 35 žen) jsme sledovali letalitu, která dosáhla celkově 10,4 %, přičemž u elektivních výkonů činila 3,4 % a u urgentních výkonů pak 31,1 % (u ruptur aneuryzmatu 37,5 %). V elektivní skupině jsme zaznamenali celkem 29 (16,2 %) chirurgických a/nebo cévně-chirurgických komplikací s nutností 16 (8,9 %) chirurgických, endovazálních nebo kombinovaných intervencí. Ve skupině urgencí pak tyto komplikace byly zaznamenány 30x (49 %) s nutností intervence v 19 případech (31,1 % urgentních výkonů).
Závěr:
Chirurgické resekční výkony na aortoilických aneuryzmatech jsou zatíženy vysokou četností výskytu systémových, chirurgických nebo cévně-chirurgických komplikací. Tito pacienti proto vyžadují vysokou pozornost a kvalitu perioperační péče se zaměřením na včasnou diagnostiku a následnou terapii těchto komplikací.
Klíčová slova:
aneuryzma aorty − chirurgické komplikace – krvácení − končetinová ischemie − břišní compartment syndrom
Úvod
Prevalence aortoilického aneuryzmatu v populaci je 5 % u mužů starších 60 let s rostoucí četností s přibývajícím věkem, u žen je výskyt 5x nižší. Základním parametrem hodnocení je rozměr a lokalizace postižení aorty a pánevních tepen. K chirurgické či endovaskulární léčbě jsou indikovány výdutě dosahující šíře nad 5,5 cm u mužů a 5,0 cm u žen vzhledem k vzrůstajícímu riziku ruptury. Taktéž jsou k léčbě indikována aneuryzmata s rychlým růstem (více než 5 mm za půl roku). Dalším indikačním kritériem je symptomatologie výdutě [1].
Operační výkony pro AAA se řadí mezi velké cévní operace. A to mimo jiné i z důvodu relativně častých komplikací systémových a chirurgických u polymorbidních a často urgentně operovaných pacientů. Četnost vynucených reintervencí z důvodu chirurgických a cévních komplikací se literárně pohybuje kolem 14 % [2]. V souboru pro potřeby našeho sdělení jsme sledovali časné komplikace (ve 30denním pooperačním období), i když z chirurgického hlediska jsou zajímavé a důležité i pozdní komplikace, jako jsou především incizionální hernie a případné infekty protetických náhrad.
Cílem práce není porovnávat výsledky a četnosti komplikací mezi endovaskulárními intervencemi pro aneuryzmata aortoilické oblasti (EVAR) a otevřeným chirurgickým přístupem (OR), poněvadž počty prováděných endovaskulárních intervencí pro AAA jsou na našem pracovišti nízké.
V diskuzi uvádíme pouze pro ucelení informací a pro srovnání některá data známá z problematiky EVAR.
Metoda
Retrospektivně jsme analyzovali pacienty operované na Oddělení cévní a plastické chirurgie Pardubické nemocnice, NPK, a. s., v období od 1. 1. 2010 do 31. 12. 2017 pro diagnózu aneuryzmatu abdominální aorty (AAA) nebo pánevních tepen (AAI). Zaměřili jsme se především na výskyt časných (tedy v 30denním intervalu od operace) cévních a chirurgických komplikací a letalitu po elektivních i urgentních otevřených operačních výkonech (OR) pro AAA nebo AAI. Z hodnocení našeho souboru byli vyloučeni nemocní, kteří při urgentním stavu (ruptura výdutě) a celkově infaustní prognóze nebyli operováni (celkem za sledované období 3 nemocní) a nemocní, kteří byli indikováni primárně ke stentgraftu (EVAR) – celkem se jednalo o 7 pacientů. Všichni pacienti s AAA nebo AAI, kteří byli operováni, byli retrospektivně dosledováni pomocí dat v NIS (nemocniční informační systém) v horizontu sledovaného období 30 dnů po operaci.
Soubor
Ve sledovaném období jsme na Oddělení cévní a plastické chirurgie Pardubické nemocnice, NPK, a. s, provedli celkem 240 operací (OR) pro AAA a/nebo AAI. V souboru dominovali muži – 205, proti 35 ženám.
Průměrný věk v našem souboru činil 72,9 roku (muži 72,3, ženy 75,9), medián 67,4 roku (20–91 let). Elektivně jsme realizovali 179 operací a urgentně 61 (z toho 48x pro rupturu) výkonů. Jako přidružený primární vaskulární výkon jsme třikrát přistoupili k replantaci dolní mezenterické tepny (AMI) a jedenkrát jsme replantovali levostrannou renální tepnu.
Výsledky
Smrtnost v našem souboru činila 10,4 % celkově (25 případů). U elektivních výkonů činila letalita 3,4 % (6 případů). U urgentních výkonů to přitom bylo 31,1 % (19 pacientů), přičemž u ruptur AAA nebo AAI jsme časné úmrtí zaznamenali celkem v 18 případech (smrtnost 37,5 % u rAAA, rAAI) a z toho pětkrát mors in tabula (10,4 % rAAA, rAAI).
Chirurgické, cévní a cévně-chirurgické komplikace (dále již jen komplikace) jsme zaznamenali celkem 59x, přičemž u elektivních zákroků pak 29x (16,2 % elektivních OR) a u urgencí jsme tyto komplikace zaznamenali 30x (49 % všech urgentních výkonů). Tyto komplikace vedly k pooperační intervenci (chirurgické, endovazální, kombinované…) celkem 35x (14,6 %) – po elektivních výkonech jsme reintervenovali 16x (8,9 % z elektivních OR) a po urgentních výkonech 19x (31,1 % všech urgentních výkonů).
Výskyt výše uvedených komplikací v našem souboru výrazně zhoršoval životní prognózu operovaných nemocných, a to především ve skupině elektivních výkonů. Úmrtí jsme ve skupině elektivních OR s komplikací zaznamenali 5x (z celkových šesti pacientů s komplikacemi) a ve skupině urgencí s komplikací jsme úmrtí zaznamenali celkem 8x.
Doba hospitalizace byla průměrně 11,9 dne (u urgencí 14,9 dne). U elektivních OR bez komplikací byla průměrná doba hospitalizace 10,6 dne, u urgentních OR bez komplikací pak 9,7 dne. Komplikace výrazně prodloužily dobu hospitalizace na 18,3 dne u elektivních OR a na 20,5 dne u urgentních OR. Četnost komplikací u urgentních a elektivních výkonů a jejich vztah k letalitě a délce hospitalizace shrnujeme v Tab. 1.
Tab. 1. Četnost komplikací a vztah k letalitě a délce hospitalizace u urgentních a elektivních resekcí aortoilických aneuryzmat
Tab. 1: Frequency of complications and their relation to mortality and length of hospitalization for urgent and elective open repairs of aortoiliac aneurysms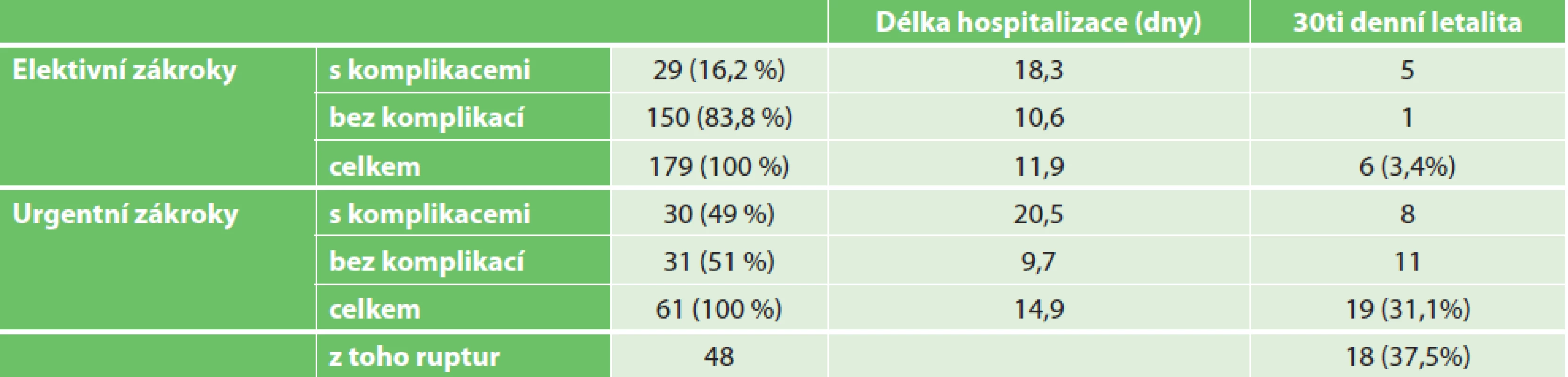
V našem souboru jsme celkem 10x sekundárně řešili krvácivé komplikace (léze horní mezenterické žíly, krvácení z omenta či sleziny, anastomotický leak, retroperitoneální krvácení bez zjevného chirurgického zdroje). Pro tyto komplikace jsme po elektivních OR revidovali 6x (3,4 %) a po urgentních OR 4x (6,6 %).
Akutní ischemii dolních končetin jsme zaznamenali celkem 21x – u elektivních výkonů 10x (5,6 %), u urgentních pak 11x (18 %). Celkem 13x jsme tuto komplikaci diagnostikovali a řešili perioperačně chirurgicky (konverze na bifurkační náhradu, extenze distální anastomózy z pánevních tepen na femorální tepny, embolektomie). Pooperačně jsme akutní končetinovou ischemii intervenovali 4x a celkem 8x jsme pro tuto komplikaci volili endovazální intervenci. Ve čtyřech z výše zmíněných případů jsme postupovali kombinovaně chirurgicky a endovazálně. Důsledkem akutní končetinové ischemie byla 2x vysoká amputace (9,5 % všech těchto příhod, 0,8 % všech operantů), 2x nízká amputace pro blue toe syndrom (mikroembolizace do pedálních a digitálních tepen) a 1x peroneální paréza. Třikrát jsme provedli fasciotomii bércových compartmentů.
Abdominální compartment syndrom nebo ischemii colon jsme zaznamenali celkem 8x (3,3 %), z toho u elektivních OR 3x (1,7 %), u urgencí pak 5x (8,2 %). Řešení této komplikace shrnujeme v Tab. 2.
Tab. 2. Typy chirurgických zákroků při revizi pro břišní compartment syndrom
Tab. 2: The types of surgical procedures due to abdominal compartment syndrome
Z dalších komplikací chirurgického typu je pak nutno uvést 1x akutní cholecystitidu, 1x disekci hrudní aorty typu B, 3x eventraci a 2x ileus z adhezí. Jako ne zcela chirurgickou, ale obecně aktuálně diskutovanou komplikaci je nutno zmínit i 8x zachycenou clostridiovou kolitidu – řešenou vždy konzervativně.
Diskuze
Evropské registry uvádějí ve výsledcích EVAR a OR veliké rozdíly v letalitě a morbiditě mezi jednotlivými zeměmi Evropské unie – v dánských registrech je souhrnná letalita OR 3,3 % a v britských 4,8 % u elektivních výkonů [3]. Ale i v rámci jednotlivých zemí jsou významné rozdíly mezi zdravotnickými zařízeními (high a low volume centra). Například kolektiv autorů (Trenner et al.) v Německu prezentuje rozdíly mezi low volume a high volume pracovišti v letalitě elektivních i urgentních výkonů pro aneuryzma aortoilického úseku (7,6 % vs. 4,5 % u OR, resp. 52 % vs. 39 % u OR) [4].
Krvácivé komplikace se po OR pohybují kolem 1,2 % procenta u elektivních výkonů, u ruptur pak mezi 12 % a 14 % (ve srovnání se 7–10 % po EVAR) [5,6]. Příčina krvácivých komplikací může být na straně operatéra. Jsou nicméně akcentovány u urgentních výkonů u pacientů mnohdy v kritickém stavu. Při hemorrhagickém šoku a centralizovaném oběhu nemusí být zdroj krvácení na konci operačního zákroku patrný. Teprve po stabilizaci nemocného v pooperačním období může pak dojít k rozkrvácení v operačním poli. Stejně tak šokový stav narušuje schopnost hemostázy organismu, která se považuje za první cílový „orgán“ šoku. Tyto komplikace zpravidla vedou k operační revizi s vyhledáním a ošetřením zdroje krvácení.
Ischemie dolních končetin je u výkonů na aneuryzmatech častěji vyjádřená než u ostatních cévních výkonů v této oblasti z důvodu typické přítomnosti detritu a trombu ve vaku výdutí. Manipulace s AAA včetně naložení a uvolnění aortální svorky mohou vést k embolizaci těchto hmot do periferní cirkulace. Incidence této komplikace po OR se pohybuje mezi 0,6–5 % [7]. V počátcích EVAR ischemie dolních končetin byly popisovány u 4–17 % případů [8]. Ale s dalším vývojem technik a instrumentária pro EVAR se v některých novějších pracích udává incidence pouze kolem 0,9 % [9]. Mikroembolizace jsou mnohem častější než masivní tromboembolie [7]. U ruptur AAA nebo AAI je po OR incidence ischemie dolních končetin kolem 5 %. Vyšší četnost této ischemické komplikace u ruptur výdutí nejspíše souvisí s nutností naložení aortální svorky bez systémové heparinizace. Pokud je vyjádřena významná ischemie dolní končetiny po výkonu na aneuryzmatu aortoilické oblasti, je riziko amputace 13−20 % [6].
Střevní ischemie a neokluzivní střevní ischemie (NOIC) představují potenciálně fatální komplikaci výkonů na AAA. Mezi rizikové faktory NOIC patří ruptura AAA, koagulopatie a peroperační arteriální hypotenze, přičemž v případě přítomnosti jednoho z těchto faktorů je pravděpodobnost vzniku NOIC 10 % a za přítomnosti dvou, resp. tří stoupá predikce na 50 %, resp. 90 % [10]. Nepochybně existují i další stavy a klinické situace, kdy lze rozvoj NOIC předpokládat s vyšší pravděpodobností. Stále se hojně diskutuje otázka replantace dolní mezenterické tepny (AMI) do cévní protézy. Dnes se většina odborné veřejnosti shoduje, že vzhledem k bohatému kolaterálnímu tepennému zásobení levé poloviny tlustého střeva (Drummondova a Riolanova anastomóza) je pro cévní zásobení dostačující průchodné povodí horní mezenterické tepny (AMS) a vnitřních ilických tepen (AII) – především levé. AMI se proto doporučuje reimplantovat do cévní protézy v případě exkluze vnitřních ilických tepen, jako je tomu především u aortálních aneuryzmat typu Eurostar D. Nutnost suprarenálního naložení aortální svorky (iuxta-, resp. suprarenální aneuryzmata) rovněž zvyšuje pravděpodobnost rozvoje ischemie splanchniku. Hypoperfuze colon postihuje v první řadě mukózu, která je koncovým kapilárním povodím tepenného zásobení. Při další progresi nebo při razantnějším hypoperfuzním inzultu se ischemické změny posouvají směrem k větším cévám – tedy do submukózy a serózy střeva. Incidence této komplikace je také závislá na typu operace – po aortobifemorálních náhradách dosahuje až 22 %, po aortoaortálních 4 % a po aortobilických 2,7 % [6].
Neokluzivní ischemii colon (NOIC) dělíme na tři stupně. První stupeň je definován jako mukózní ischemie, která má transientní charakter a zpravidla mírný průběh. Stupeň druhý je definován jako ischemie mukózní a muskulární a podle klinického průběhu se dělí na další dva podstupně – s, nebo bez multiorgánového selhávání (MODS). Stupeň třetí je charakterizován jako transmurální ischemie s gangrénou, až perforací trávicí trubice a je vždy doprovázen rozvojem MODS [11]. První a druhý stupeň bez MODS se doporučuje léčit konzervativně za dodržení obecně platných postupů léčby šoku a ochrany colon včetně plné parenterální výživy. Vyšší dva stupně s MODS je nutno bezprostředně po stanovení diagnózy NOIC řešit operačně – tedy resekcí ischemického úseku colon (většinou levostrannou hemikolektomií s terminální transverzostomií nebo subtotální kolektomií s terminální ileostomií) podle rozsahu gangrenózních změn. U chirurgické léčby je jednou ze zásad ponechání co nejkratšího distálního pahýlu rekta k prevenci jeho ischemické dehiscence. Primární střevní anastomóza se z této indikace po resekčních výkonech zásadně nedoporučuje. Progrese ischemie ponechaného střeva však není nikdy zcela vyloučena [11]. Menegaux et al. v prospektivní studii zachytili NOIC po 1786 resekcích AAA ve 49 případech (2,7 %), z nichž 24 bylo zprvu diagnostikováno jako první nebo druhý stupeň bez MODS, a tedy léčeno podle výše uvedených doporučení konzervativně. U tří čtvrtin nemocných z této skupiny (18 pacientů) ischemie colon progredovala a vyžádala si dodatečnou resekci trávicí trubice. V konzervativně léčené skupině s nulovou letalitou zůstalo nakonec pouhých 6 pacientů (12,2 %), kdežto 43 nemocných (87,8 %) bylo nutno operovat (ať už primárně, nebo v dalším průběhu). Letalita nemocných s druhým stupněm s MODS byla 37,5 % a u nemocných s třetím stupněm NOIC pak 57,1 % [12].
Incidence břišního compartment syndromu (ACS) po OR pro rAAA se pohybuje kolem 20 %. Letalita u nemocných po rAAA s rozvojem ACS je 5x vyšší než ve skupině bez ACS [13].
ACS je definován vzestupem nitrobřišního tlaku (IAP) nad 20 mmHg se současně vyjádřenou orgánovou dysfunkcí nebo IAP větší než 25 mmHg bez orgánové dysfunkce [14]. Rizikové faktory pro vznik ACS jsou: hemoperitoneum a retroperitoneální hematom, masivní tekutinová resuscitace (nad 5 l/24 hod.), velký počet transfuzí (víc než 10 jednotek/24 hod.), koagulopatie (trombocyty pod 55x109/l, dvojnásobná délka aPTT, INR více než 1,5), hypotermie (pod 33 °C), acidóza (pH méně než 7,2), dlouhý čas svorky, délka operačního výkonu [15].
Pokud je indikována dekompresní laparostomie pro ACS, pak letalita dosahuje až 56 % ve srovnání s 9 % u primárních uzávěrů břišní stěny. Primární indikací k open-abdomen postupu jsou: hladina hemoglobinu nižší než 100 g/l, předoperační kardiální zástava, systolický krevní tlak pod 90 torr po dobu delší než 18 minut, potřeba parenterálního přísunu tekutin nad 3,5 l/hod. operace, tělesná teplota pod 33 °C, base-deficit pod 13 mmol/l [15]. Pokud je výkon na rAAA v indikovaných případech ukončen primárně formou open-abdomen, pak tito nemocní oproti dekompresním laparostomiím při ACS mají nižší mortalitu (51 % vs. 70 %) a nižší incidenci multiorgánového selhání (MOF) (11 % vs. 70 %) [16]. Obavy z pozdního infektu protetického materiálu nejsou u open-abdomen nejspíše opodstatněné [17].
Závěr
Kromě obecně známé vysoké kardiovaskulární komorbidity cévně-chirurgických pacientů, která je právě akcentována mnohdy u pacientů s aneuryzmatem aortoilického povodí, předkládáme širší chirurgické veřejnosti i problematiku specifických chirurgických, resp. cévně-chirurgických komplikací. Tak jako ve viscerální nebo úrazové chirurgii péče o pacienta nekončí úspěšně provedenou operací, stejně tak (a možná ve větší míře) operací nekončí péče o pacienta s AAA nebo AAI. Bez větší nadsázky lze tvrdit, že operací teprve vše začíná.
Naše sdělení si nekladlo za cíl pojednávat o neméně významné problematice systémových komplikací u nemocných po operacích aortoilického aneuryzmatu. Taktéž jsme si nekladli za cíl diskutovat nebo obšírněji rozebírat problematiku EVAR, která má v dnešní době své nezastupitelné místo. Nízké počty těchto výkonů v českých podmínkách souvisejí s finančními limity i s dosud omezeným přístupem cévních chirurgů k této metodice.
Seznam zkratek
AAA – aneuryzma břišní aorty
AAI – aneuryzma pánevních tepen
ABI – index poměrů tlaků ankle/brachial
ACS – břišní compartment syndrom
AII – vnitřní pánevní tepna
AMI – dolní mezenterická tepna
AMS – horní mezenterická tepna
aPTT – aktivovaný parciální tromboplastinový čas
EVAR – endovaskulární řešení aneuryzmatu
IAH – nitrobřišní hypertenze
IAP – nitrobřišní tlak
INR – protrombinový čas
MODS – multiorgan dysfunction syndrom
MOF – multiorgan failure
NOIC – neokluzivní ischemická kolitida
OR – otevřené chirurgické řešení aneuryzmatu
pH – vodíkový exponent, kyselost
rAAA – rupturované aneuryzma břišní aorty
rAAI – rupturované aneuryzma pánevních tepen
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
MUDr. Miloslav Pirkl
Šafaříkova 682
534 01 Holice
e-mail: miloslav.pirkl@nempk.cz
Zdroje
- Opatrný V, Třeška V, Moláček J, et al. Gigantické aneuryzma abdominální aorty a pánevních tepen. Rozhl Chir 2016;95 : 123−5.
- Kieffer WKM, Sonnenberg S, Windhaber RA, et al. Complications and reintervention following elective open abdominal aortic aneurysm repair: a 10-year retrospective analysis. Ann R Coll Surg Engl 2012; 94 : 177–80.
- Motte L, Jensen LP, Vogt K, et al. Outcomes after elective aortic aneurysm repair: A nationwide Danish cohort study 2007−2010. Eur J Vasc Endovasc Surg 2013;46 : 57−64.
- Trenner M, Kuehnl A, Salvermoser M, et al. Editor´s choice – High annual hospital volume is associated with decreased in hospital mortality and complication rates following treatment of abdominal aortic aneurysm: Secondary data analysis of the nationwide German DRG statistics from 2005–2013. Eur J Vasc Endovasc Surg 2018;55 : 185−94.
- Woo YE, Damrauer SM. Abdominal aortic aneurysms: Open surgical treatment. In: Cronenwett JL, Johnston KW, et al. Rutherford´s vascular surgery. 8th edition. Elsevier Saunders 2014 : 2025−45.
- Mehta M, Byrne J. Abdominal aortic aneurysms: ruptured. In: Cronenwett JL, Johnston KW, et al. Rutherford´s vascular surgery. 8th edition. Elsevier Saunders 2014 : 2063−82.
- Toursavadkohi S, Stavros Kakkos SK, Rubinfeld I,et al. Lower extremity microembolism in open vs. endovascular abdominal aortic aneurysm repair. Front Surg 2016;3 : 1−5.
- Marin ML, Veith FJ, Cynamon J, et al. Initial experience with transluminally placed endovascular grafts for the treatment of complex vascular lesions. Ann Surg 1995,222 : 449–69.
- Maldonado TS, Rockman C, Riles TS. Ischemic complications after endo-vascular abdominal aortic aneurysm repair. J Vasc Surg 2004;40 : 703–9.
- Gerhart CD, Nicholas GG, Reed JF. Predictive model for colonic ischemia following abdominal aortic aneurysm repair. Vasc Endovas Surg 1994;28 : 161–6.
- Pirkl M, Daněk T, Šebesta P, et al. Neokluzivní ischemická kolitida po resekci aneuryzmatu abdominální aorty: zkušenosti z našeho pracoviště a shrnutí problematiky. Slov chir 2012;9 : 102–10.
- Menegaux F, Trésallet Ch, Kieffer E, et al. Aggressive management of nonocclusive ischemic colitis following aortic aeconstruction. Arch Surg 2006;141 : 678–82.
- Bozeman MC, B. Ross CB. Intra-abdominal hypertension and abdominal compartment syndrome in association with ruptured abdominal aortic aneurysm in the endovascular era: Vigilance remains critical. Crit Care Res Pract 2012. Available from: doi:10.1155/2012/151650
- WSACS Consensus Guidelines Summary. Available from: http:/www.wsacs.org.
- Moll FL, Powell JT, Fraedrich G, et al. Management of abdominal aortic aneurysms clinical practice guidelines of the European society for vascular surgery. Eur J Vasc Endovasc Surg 2011;41:S1−S58.
- Rasmussen TE, Hallett JW, Noel AA, et al. Early abdominal closure with mesh reduces multiple organ failure after ruptured abdominal aortic aneurysm repair: guidelines from a 10-year case-control study. J Vasc Surg 2002;35 : 246–52.
- Ross CB, Irwin CL, Mukherjee K, et al. Vacuum-pack temporary abdominal wound management with delayed-closure for the management of ruptured abdominal aortic aneurysm and other abdominal vascular catastrophes: absence of graft infection in long-term survivors. Am Surg 2009;75 : 565–70.
Štítky
Chirurgia všeobecná Ortopédia Urgentná medicína
Článek Chirurgie, s. r. o.?Článek ESCP 2018, Nice, Francie
Článok vyšiel v časopiseRozhledy v chirurgii
Najčítanejšie tento týždeň
2018 Číslo 11- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
-
Všetky články tohto čísla
- Chirurgie, s. r. o.?
- Indikace k otevřené chirurgické revaskularizaci viscerálního řečiště v endovaskulární éře
- Aorto-ilická endarterektomie: staro-nová metoda?
- Časné chirurgické a cévní komplikace po resekcích aneuryzmat aortoilické oblasti
- Poranenia extrakraniálnych ciev mozgu pri traume krčnej chrbtice
- Větvený pedální bypass v léčbě kritické končetinové ischemie – zkušenosti našeho centra
- Zkušenosti našeho centra v chirurgické léčbě Dunbarova syndromu
- Aneuryzma vnitřní pánevní tepny − kazuistika
- Postavte si simulátor laparoskopických dovedností
- ESCP 2018, Nice, Francie
- Rozhledy v chirurgii
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Zkušenosti našeho centra v chirurgické léčbě Dunbarova syndromu
- Aneuryzma vnitřní pánevní tepny − kazuistika
- Poranenia extrakraniálnych ciev mozgu pri traume krčnej chrbtice
- Indikace k otevřené chirurgické revaskularizaci viscerálního řečiště v endovaskulární éře
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



