Vliv stáří transfuzních jednotek erytrocytů na koncentrace vybraných biochemických veličin
Age of packed red blood cells and its influence on concentration of selected biochemical values
Objective:
Administration of blood transfusion is associated with risk and adverse effects. Large-volume transfusion can cause electrolyte and acid-base balance disturbances. The influence of metabolism and decomposition of erythrocytes in the transfusion unit can change the initial values of some biochemical parameters; the age of the transfusion unit may play the major role. The aim of this study was to describe the influence of the age of the transfusion unit of packed red blood cell (PRBC) on biochemical values in vitro.
Design:
Prospective observational study.
Setting:
Multidisciplinary intensive care unit (ICU) in a tertiary care centre.
Materials and methods:
We examined samples from 80 PRBC units of different age (the expiration process is defined by national and local hospital standards). The samples originated from the transfusion department where PRBCs were stored in standard conditions. The samples were analysed by a standard-controlled analyser (Critical Care Xpress®, Nova Biomedical) and we recorded the data about the biochemical values in dependence on the PRBC age.
Results:
We found that PRBC age determines a rise of K+ and lactate values and a decrease in pH, Na+ and glycaemia. The measured values were in the range of: potassium 4.0–40.5 mmol/l; lactate 4.1–28.0 mmol/l; pH 7.0–6.65; glycaemia 29.0–14.0 mmol/l; sodium 137–116 mmol/l. Calcium concentration remained stable.
Conclusion:
The administration of large-volume blood transfusion, particularly close to the expiry date of the PRBC unit, can pose a significant risk of possible disturbances in the electrolyte and acid-base balance of the patient.
Keywords:
erythrocyte – PRBC – hyperkalaemia – lactate – metabolic acidosis
:
Uvízl Radovan; Fritscherová Šárka; Neiser Jan; Šafránek Petr; Adamus Milan
:
Klinika anesteziologie a resuscitace, Fakultní nemocnice Olomouc
:
Anest. intenziv. Med., 20, 2009, č. 5, s. 257-261
:
Intensive Care Medicine - Original Paper
Cíl studie:
Podávání krevních náhrad je spojeno s řadou rizik a nežádoucích účinků. Vlivem metabolismu erytrocytů a jejich rozpadem dochází v konzervě erytrocytů ke změnám výchozí koncentrace některých biochemických veličin. Transfuze většího množství erytrocytů se může následně podílet na změnách vnitřního prostředí. Předmětem práce bylo sledování vlivu stáří koncentrátu erytrocytů na hladiny biochemických veličin v těchto konzervách in vitro.
Typ studie:
Prospektivní observační studie.
Typ pracoviště:
Resuscitační oddělení fakultní nemocnice.
Materiál a metoda:
Vyšetřili jsme prospektivně sestavený soubor vzorků 80 erytrocytárních koncentrátů různého stáří v průběhu celého cyklu exspirace, získaných z krevní banky, skladovaných za standardních podmínek. Vyšetřením na kombinovaném acidobazickém analyzátoru jsme stanovili průběh změn koncentrací sledovaných veličin v závislosti na stáří konzervy.
Výsledky:
Bylo zjištěno, že stáří erytrocytárního koncentrátu má vliv na vzestup hladiny K+ a laktátu, pokles pH, Na+ a glykémie. Naměřené hodnoty se pohybovaly v rozmezí: kalium 4,0–40,5 mmol/l; laktát 4,1 až 28,0 mmol/l; pH 7,0–6,65; natrium 137–116 mmol/l; glykémie 29,0–14,0 mmol/l. Hodnoty koncentrace ionizovaného kalcia se měnily minimálně a setrvávaly na hodnotě blízké 0,17 mmol/l.
Závěr:
Podání většího množství konzerv erytrocytárních koncentrátů především na konci doby exspirace může být vzhledem ke zjištěným hodnotám rizikem pro možné změny vnitřního prostředí.
Klíčová slova:
erytrocyty – hyperkalemie – laktát – metabolická acidóza
Úvod
Podávání transfuzních přípravků, obsahujících buněčné elementy, je spojeno s řadou rizik a možných nežádoucích účinků. Vlivem metabolismu erytrocytů, jímž je anaerobní glykolýza, dochází v konzervě erytrocytárního koncentrátu ke změnám výchozích koncentrací některých biochemických veličin. Transfuze většího množství transfuzních jednotek erytrocytárních koncentrátů (erytrocyty bez buffy coatu resuspendované) se může následně podílet na změnách vnitřního prostředí pacienta [1].
Cíl studie
Účelem práce bylo zhodnocení vlivu stáří erytrocytů na koncentrace sledovaných biochemických veličin ve vzorcích erytrocytárních koncentrátů.
Metody
Vyšetřili jsme prospektivně sestavený soubor náhodně vybraných vzorků 80 transfuzních jednotek erytrocytárních koncentrátů různého stáří v průběhu celého cyklu exspirace, určených k bezprostřednímu podání pacientům, u nichž byla transfuze indikována. Zhodnocením dat získaných z vyšetřených vzorků jsme sestavili grafy průběhu jednotlivých sledovaných biochemických veličin v konzervách erytrocytárních koncentrátů v závislosti na stáří těchto konzerv.
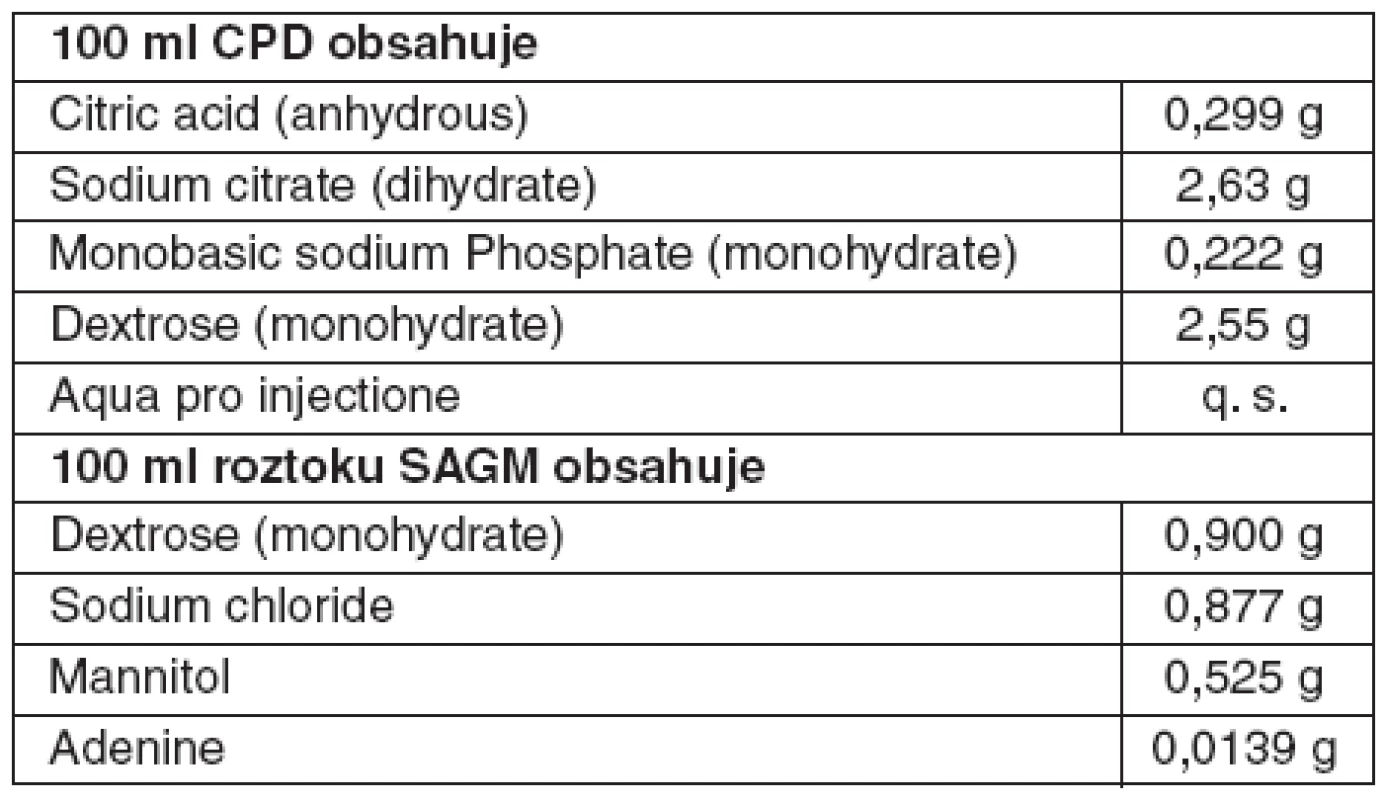
Vyšetřovány byly vzorky transfuzních jednotek erytrocytárních koncentrátů, které splňovaly tato kritéria: objem 280 ± 50 ml, Hb nad 43 g/TU, HCT 50–70 %, leukocyty pod 1,2 . 109 . l-1, trombocyty pod hodnotou 20 . 109 . l-1, plazmatické bílkoviny pod 2 g . l-1. Exspirace byla až 42 dní, doporučené použití do 35 dnů po odběru [2]. Práce byla provedena na lůžkové části KAR FN Olomouc. Erytrocytární koncentráty jsme získali z krevní banky, kde byly skladovány za standardních podmínek při teplotě 2–6 °C, a k lůžku pacienta byly doručeny v termoboxu. Do 2 minut po vyjmutí a opatrném promíchání obsahu transfuzní jednotky jsme odebrali vzorek 0,5 ml erytrocytárního koncentrátu odběrovou stříkačkou Marquest Quik A.B.G. a analyzovali jej v Kombinovaném acidobazickém analyzátoru Stat Profile CCX, Nova Biomedical. Vyšetřením takto získaných vzorků jsme stanovili průběh změn koncentrací sledovaných veličin v závislosti na stáří konzervy. Ke konzervaci 1 transfuzní jednotky erytrocytárního koncentrátu bylo u vyšetřovaných vzorků použito 20 ml roztoku SAGM a 100 ml roztoku CPD (složení obou v tabulce 1).
Statistické zpracování
Závislost sledovaných parametrů (Na+, K+, Ca++, Na+, glykémie, pH) na stáří konzerv erytrocytárních koncentrátů jsme vyjádřili graficky. Závislost hladiny K+ na pH jsme znázornili pomocí regresní přímky.
Výsledky
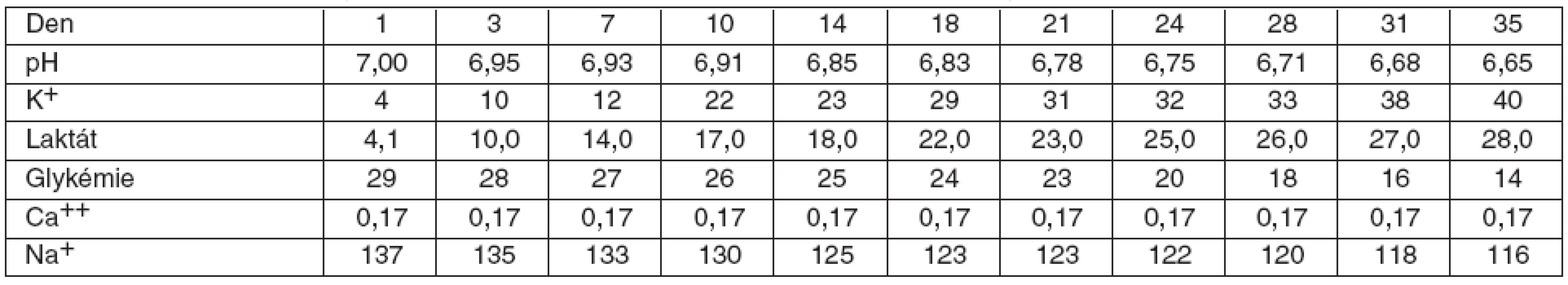
- V koncentrátu erytrocytů dochází k nárůstu hladiny K+ v čase (tab. 2 a graf 1).
- V koncentrátu erytrocytů dochází k poklesu pH v čase (viz tab. 2 a graf 2), zároveň se vzestupem K+ (graf 3).
- V koncentrátu erytrocytů dochází k nárůstu hladiny laktátu (viz tab. 2, graf 4).
- V koncentrátu erytrocytů nedochází k výraznější změně hladiny Ca++ (viz tab. 2).
- V koncentrátu erytrocytů dochází k poklesu hladiny Na+ (viz tab. 2, graf 5).





Diskuse
Zvýšení koncentrace kalia u starších jednotek erytrocytárních koncentrátů je podmíněno kromě rozpadu erytrocytárních buněk také blokádou enzymu adenozintrifosfatázy chladem. Dochází k uvolňování K+ extracelulárně a vstupu iontů Na+ do erytrocytů. Nitrobuněčná koncentrace iontů kalia se pohybuje v rozmezí 100–140 mmol . l-1 [3]. Na transcelulárním gradientu K+ mezi extracelulárním a intracelulárním prostorem se v největší míře podílí enzym Na+- K+-adenozintrifosfatáza (sodíková pumpa). Zajišťuje transport 2 iontů K+ do buňky výměnou za 3 ionty Na+. Ke zvýšení hladiny K+ v čerstvé konzervě erytrocytárního koncentrátumůže přispět i svalová aktivita – opakované svírání pěsti dárce v průběhu odběru krve. Může tak dojít ke zvýšení sérové koncentrace K+ v krvi v místě odběru na předloktí dárce o více než 1 mmol . l-1 [4]. Naměřené koncentrace jsme porovnali se staršími publikovanými daty (tab. 3), avšak k důvodu rozdílnosti některých dosažených hodnot (především laktátu a glykémie) se nelze jednoznačně vyjádřit, neboť neznáme složení použitého fixačního roztoku.
![Hodnoty biochemických veličin v krevní konzervě volně podle Millera [5]](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/e7835bd55e1eec06508d0410e21e72e0.png)
Důvodem poklesu pH ve vyšetřovaných vzorcích erytrocytárních koncentrátů jsou jednak metabolity erytrocytů – laktát a pyruvát, ale také pH konzervačního roztoku. Na poklesu pH konzervy se podílí i vzestup pCO2 jejího obsahu. Při acidóze dochází k pufrování nadbytku H+ iontů v buňkách a k přestupu K+ extracelulárně. Tento přesun je způsoben snahou o zachování elektroneutrality. In vitro se uplatňuje méně než při orgánové acidóze, ketoacidóze nebo laktátové acidóze [6]. V konzervě erytrocytárního koncentrátu dochází k nárůstu hladiny laktátu jako důsledku anaerobního metabolismu krevních buněk. Samotný zdroj energie – glukóza – je při glykolýze metabolizován na laktát za spotřeby 2 molekul adenozintrifosfátu. V konzervě erytrocytárního koncentrátu dochází k poklesu hladiny Na+ (viz tab. 2 a graf 5). Důvodem je zmíněný proces výměny K+- Na+ mezi intracelulárním a extracelulárním prostorem erytrocytů.
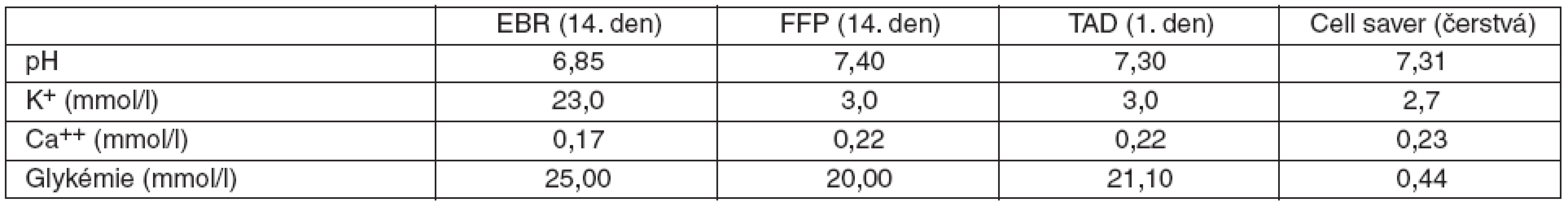
V průběhu skladování dochází také k poklesu 2,3-difosfoglycerátu v erytrocytech. Míra tohoto poklesu je úměrná stáří konzervy, vede k posunu disociační křivky Hb doleva, a tedy ke zvýšení afinity Hb ke kyslíku. Důsledkem je snížené uvolňování kyslíku ve tkáních a hrozba tkáňové hypoxie. Tzv. „storage laesions“ se netýkají pouze biochemických změn, ale v průběhu skladování dochází i ke změnám metabolickým (elevace prozánětlivých cytokinů) a molekulárním (deformace tvaru a elasticity erytrocytů s následnými poruchami mikrocirkulace). Případná rekuperace skladované erytrocytární náhrady odstraní velké mikroagregáty, větší než 17 μm, neodstraní však mikroagregáty menší než 7 μm. V současné době je zaměřen zájem rovněž na imunomodulační účinek transfundovaných erytrocytů jako možného mechanismu zvýšení morbidity a mortality hospitalizovaných pacientů po podání erytrocytů. Důsledkem je vznik nozokomiálních infekcí, ALI (acute lung injury) nebo možný rozvoj autoimunitních onemocnění v pozdější době [7, 8]. Výsledky naznačují, že deleukotizovaná krev může působit méně imunomodulačně než krev nedeleukotizovaná [7, 9, 10]. „The American Association of Blood Banking“ proto doporučuje zhodnotit potřebu podání krevní náhrady raději s ohledem na parametry závažnosti onemocnění a klinického stavu než na arbitrárně stanovené hodnoty hladin hemoglobinu [11]. Neexistuje žádná izolovaná hodnota hemoglobinu, která ospravedlňuje nebo vyžaduje podání transfuze. Konečným faktorem pro rozhodnutí o podání krevní náhrady by mělo být zhodnocení pacientova klinického stavu [12], neboť organismus má schopnost adaptace na anémii prostřednictvím nárůstu srdečního výdeje (při absenci objemové deplece), změnami mikrocirkulace a nárůstem koncentrace 2,3-difosfoglycerátu v erytrocytech (tedy posunem disociační křivky hemoglobinu doprava) [13]. Téměř neexistují důkazy o tom, že rutinní podávání transfuzí erytrocytů u nekrvácejících pacientů s hodnotou hemoglobinu nad 70 mg . l-1 vede ke zlepšení jejich outcome [13]. Naše práce byla zaměřena na hodnocení změny biochemických veličin, ke kterým dochází pouze v koncentrátech erytrocytů bez buffy coatu resuspendovaných (EBR), a proto je nelze beze zbytku přenášet na hodnoty získané z jiných transfuzních přípravků, kterými jsou: erytrocyty resuspendované (ER), erytrocyty deleukotizované (ERD) a erytrocyty z aferézy resuspendované (EAR). Ostatní typy krevních derivátů, jako jsou čerstvě zmražená plazma (FP), trombocyty z aferézy (TA) nebo trombocyty z aferézy, deleukotizované (TAD) buněčné elementy neobsahují [2]. Výrazně se v nich liší koncentrace sledovaných biochemických veličin (tab. 4). Z tabulky průměrných koncentrací K+, pH, laktátu, Ca++, Na+ a glykémie v konzervách 1.–35. den (viz tab. 2) vyplývá možnost dosažení, eventuálně překročení maximální dodávky kalia, která je podle doporučení stanovena na 20 mmol . h-1 [14]. Tato dodávka kalia může být teoreticky dosažena, popř. i překročena, již při podání 1000 ml koncentrátu erytrocytů/hod, staršího cca 14 dní. Aboudra et al. ve výsledcích klinické studie u traumatologických pacientů uvádějí, že podání více než 7 transfuzních jednotek erytrocytárních koncentrátů vedlo k rozvoji hyperkalémie [15]. Zároveň se změnami pH tak může v průběhu podávání masivní krevní náhrady dojít k výraznému nárůstu kalémie [16]. Takto získaná hyperkalémie může vést až k srdeční zástavě [17]. V retrospektivní studii (z let 1998–2006) Smith et al. identifikovali 16 pacientů, u nichž došlo k srdeční zástavě v souvislosti s hyperkalémií při podání masivní krevní náhrady přetlakem, přičemž hodnota kalémie u těchto pacientů dosahovala střední hodnoty 7,2 mmol . l-1. Téměř u všech pacientů byla v různé míře spolu s hypotermií rozvinutá metabolická acidóza, hyperglykémie a hypokalcémie [17]. V dalším sledování a výzkumu se zaměříme na posouzení intenzity vlivu masivní krevní náhrady na možné změny vnitřního prostředí pacienta a na klinickou odezvu.
Závěr
Ze zjištěných biochemických hodnot erytrocytárních koncentrátů vyplývá nejen možnost rozvoje hyperkalémie, ale i komplexní poruchy vnitřního prostředí. Toto riziko je tím větší, čím je náhrada erytrocytů masivnější, rychlejší, a čím jsou podávané erytrocyty blíže konci své exspirace. Vhodné je proto v průběhu masivní krevní náhrady intermitentní sledování biochemických parametrů k včasnému zachycení změn ABR a hladiny iontů, a tedy možnost nasazení odpovídající terapie.
Došlo 23. 4. 2009.
Přijato 30. 7. 2009.
Adresa pro korespondenci:
MUDr. Radovan Uvízl
KAR FN Olomouc
I. P. Pavlova 6
775 20 Olomouc
e-mail: radovan.uvizl@seznam.cz
Sources
1. Brecher, M. E. Noninfectious complications of blood transfusion. AABB technical manual, 2005, p. 577–600.
2. Cetkovský, P. et al. Intenzivní péče v hematologii. 1. vydání, Praha: Galén, 2004, p. 169–179. ISBN 80-7262-255-2.
3. Hillyer, C. D., Hillyer, K. L., Strobl, F. J., Jefferies, L. C., Silberstein, L. E. Handbook of transfusion medicine. Academic Press, 2001, p. 275–282.
4. Sever, M. S., Erek, E., Vanholder, R., Kantarci, G. Serum potassium in the crush syndrome victims of the Marmara disaster. Clin. Nephrol., 2003, p. 59.
5. Larsen, R. Anestezie. 7. vydání, Praha: Grada, 2004, p. 718–753. ISBN 80-247-0476-5.
6. Rose, B. D., Post, T. W. Clinical Physiology of Acid – Base and Electrolyte Disorders. 5th ed. New York: McGraw-Hill, 2001, p. 383–396, 898–910.
7. Raghavan, M., Marik, P.E. Anemia, allogenic blood transfusion, and immunomodulation in the critically ill. Chest, 2005, 127, p. 295–307.
8. Toy, P., Popovsky, M. A., Abraham, E., et al. Transfusion-related acute lung injury: Definition and review. Crit. Care Med., 2005, 33, p. 721–726.
9. Fergusson, D., Khanna, M. P., Tinmouth, A., et al Transfusion of leukoreduced red blood cells may decrease postoperative infections: Two meta-analyses of randomized controlled trials. Can. J. Anaesth., 2004, 51, p. 417–424.
10. Hebert, P. C., Tinmouth, A., Corwin, H. L. Controversies in RBC transfusion in the critically ill. Chest, 2007, 131, p. 1583–1590.
11. Consensus conference: Perioperative red blood cel transfusion. JAMA, 1988, 260, p. 2700–2703.
12. Guidelines for red blood cell and plasma transfusion for adults and children. Expert Working Group. Can. Med. Assoc. J., 2008, 156, 11 suppl., p. S1–S24.
13. Marik, P. E., Corwin, H. L. Efficacy of red blood cell transfusion in the critically ill. A systematic review of the literature. Crit. Care Med., 2008, 36, 9, p. 2667–2674.
14. Vítovec, J., Špinar, J. Intenzivní péče v kardiologii. IPVZ : Brno, 1994, p. 150. ISBN 80-7013-170-5.
15. Aboudara, M. C., Hurst, F. P., Abbott, K. C., Perkins, R. M. Hyperkalemia after packed red blood cell transfusion in trauma patients. J. Trauma, 2008, 64, 2 Suppl., p. S86–91.
16. Hillyer, C. D., Hyllier, K. L., Strobl, F. J., Jefferies, L. C., Silberstein, L. E. Handbook of transfusion medicine. Academic press, 2001, p. 263–271.
17. Smith, H. M., Farrow, S. J., Ackerman, J. D., Stubbs, J. R., Sprung, J. Cardiac arrest associated with hyperkalemia during red blood cell transfusion: a case series. Anesth. Analg., 2008, 106, 4, p. 1062–1069.
Labels
Anaesthesiology, Resuscitation and Inten Intensive Care MedicineArticle was published in
Anaesthesiology and Intensive Care Medicine

2009 Issue 5
Most read in this issue
- Induction and recovery times for general anaesthesia – a prospective study
- Cancellations of scheduled surgical procedures in three Czech university hospitals – a prospective study
- Regional citrate anticoagulation during continuous renal replacement therapy (CRRT) in a cardiac surgery patient with a high risk of bleeding – case report
- Age of packed red blood cells and its influence on concentration of selected biochemical values
