Kvalita, kontrola a validace glukometrů a CGM systémů. Přehled stavu.
Quality, control and validation of glucometers and CGM systems. Status overview
The communication deals with current state of analytical quality for measuring the glucose in blood by glucometers and continuous glucose monitoring (CGM).Quality requirements for blood glucose measurement of ISO 15197 and FDA 2014 standards are described and results of recent studies of their evaluations in used glucometers are introduced. These results show very different level of quality in glucometers and high degree of lot-to-lot variation. Also, programs of external quality assessment provide similar picture on measurement quality. We describe current limited possibilities of control materials in quality assessment, namely in case of bias determination. Quality requirements based on recommendations of US FDA guidance is also part of this publication. We summarize the recent state of quality measurement of continuous glucose monitoring.
Keywords:
Glucometers, continuous monitoring of glucose, quality requirements, quality assessment.
:
B. Friedecký 1,2; J. Kratochvíla 2; D. Springer 3
:
Ústav klinické biochemie a diagnostiky Fakultní nemocnice Hradec Králové
1; SEKK s. r. o. Pardubice
2; Ústav lékařské biochemie a laboratorní diagnostiky 1. LF UK a VFN Praha
3
:
Klin. Biochem. Metab., 24, 2016, No. 2, p. 75-81
Cílem sdělení jsou informace o požadavcích na analytickou kvalitu měření glukózy v krvi POCT glukometry, při kontinuálním sledování její koncentrace a informace o jejím současném stavu. Jsou uvedeny hodnoty požadovaných indikátorů kvality v normách ISO 15197 a FDA 2014. Uvádíme souhrnně i výsledky recentních studií kvality běžně používaných glukometrů. Výsledky ukazují velké rozdíly v kvalitě různých typů glukometrů, pocházejících od různých výrobců. Je pojednáno o důležitém faktoru bezpečného používání glukometrů-o variabilitě mezi šaržemi testovacích proužků, která může dosahovat hodnot až nad 10 %. Pojednáváme stručně o programech externího hodnocení kvality a jejich významu a omezeních daných současným stavem a možnostmi kontrolních materiálů a o možnostech zlepšení situace. Požadavky na zajištění kvality glukometrů, doporučované úřadem US FDA, kvalita a kalibrace systémů kontinuálního monitorování glukózy (CGM), jsou další součástí sdělení.
Klíčová slova:
glukometry, kontinuální sledování glukózy, požadavky na kvalitu, hodnocení kvality.
Úvod
Podle dat Mezinárodní federace pro diabetes (IDF) bylo na světě v roce 2013 již 386 miliónů diabetiků a jejich počet prudce narůstá. V České republice bylo podle údajů, převzatých od Diabetické asociace ČR v roce 2012 více než 841 000 diabetiků. Se zahrnutím doposud nediagnostikovaných jedinců je velmi pravděpodobné, že počet diabetiků překračuje v ČR 1 milion osob [31]. Uvedené počty diabetiků znamenají výrobu a používání obrovských počtů glukometrů patrně v řádu desítek milionů. Jaké jsou současné poznatky o stavu kvality měření glukózy glukometry? Pokoušíme se v tomto článku o aspoň částečnou odpověď. Bereme v úvahu fakt, že v řadě zdravotních zařízení existují sítě glukometrů, supervizované klinickými laboratořemi, které mají potenciální schopnost podílet se na řízení kvality glukometrů i mimo tuto síť.
Požadavky na kvalitu
Současné požadavky na kvalitu měření glukometrů jsou shrnuty v Tabulce 1. Data vycházejí z příslušných norem a Směrnic [1, 2]. Indikátorem analytické kvality glukometrů jsou hodnoty rozdílů mezi výsledky, získanými glukometry a laboratorními metodami. Dobře kontrolované laboratorní metody jsou metrologicky návazné na referenční metody a certifikované referenční materiály a samy slouží jako sekundární reference pro posouzení kvality glukometrů. Bez spolupráce pacientů, diabetologů a klinických laboratoří je dosažení kvality měření glukózy v selfmonitoringu, v ambulancích a na nemocničních odděleních iluzorní.
Kvalita systémů a variabilita šarží
Při posuzování kvality glukometrů se obvykle současně hodnotí celková chyba měření ve srovnání s výše uvedenými normativními požadavky (viz Tabulka 1) a často současně i variabilita mezi šaržemi testovacích proužků. Výsledky jsou publikovány v řadě prací [3 – 9].
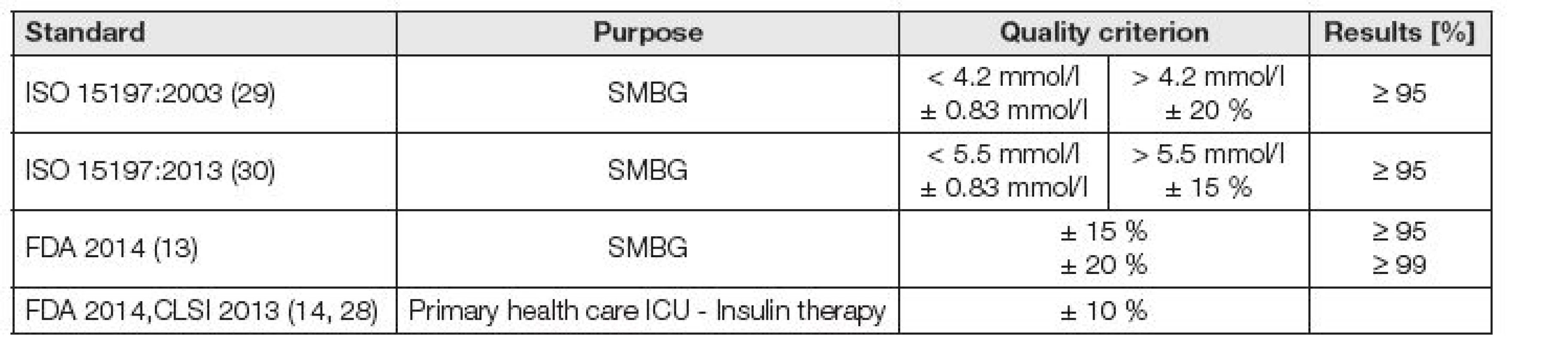
Data, charakterizující současný stav kvality a variability mezi šaržemi uvádíme v Tabulkách 2 a 3.
Z Tabulky 2 je zřejmá významně rozdílná úroveň kvality různých systémů a testovacích proužků. Některé systémy jsou schopné vyhovět i přísnému požadavku použití v primární zdravotní péči (celková chyba TE ≤ 10 %), jiné nevyhovují ani požadavkům starší a překonané normy kvality ISO 15189 : 2003 (≤ 20 %). Kvalita měření glukózy tedy začíná již výběrem vhodného systému. To může představovat zásadní problém zejména při selfmomitoringu pacientů.
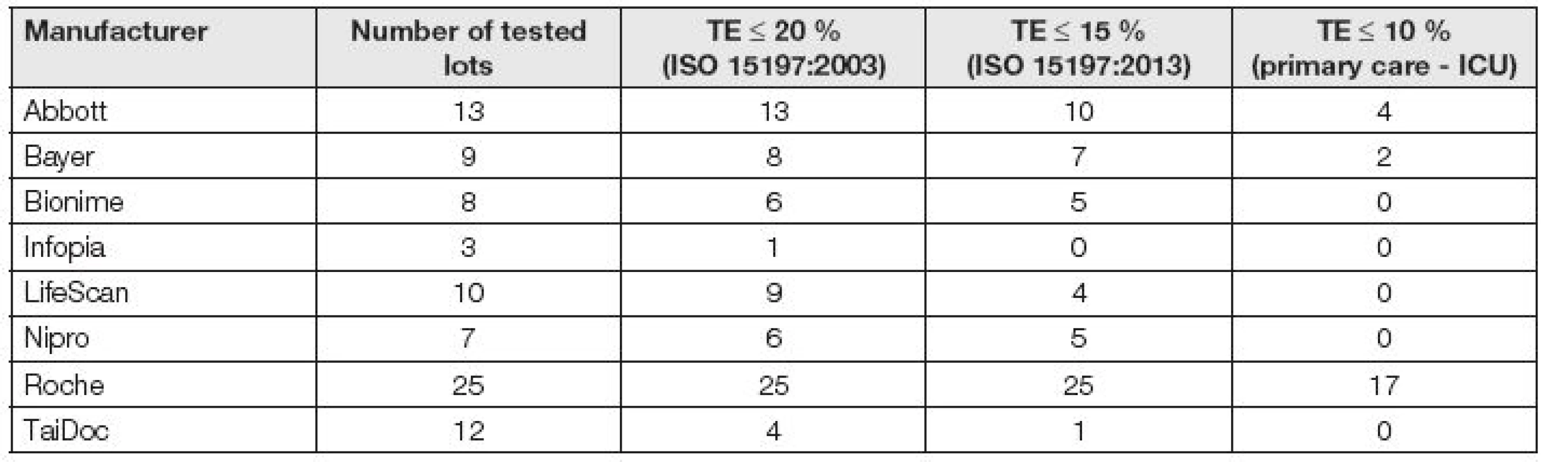
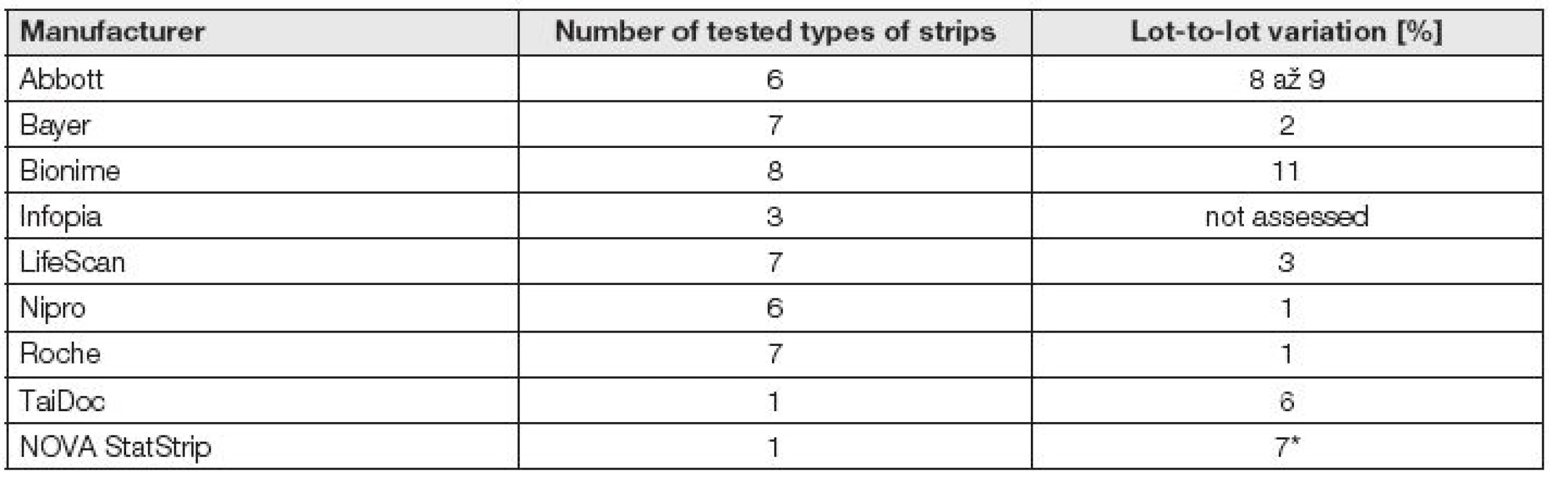
V práci Müllera a spol. [3] jsou shrnuty velmi přehledně v grafické podobě parametry kvality glukometrů včetně variabilit mezi šaržemi proužků, získané zpracováním dat 8 výrobců, 87 různých šarží vždy 50 proužků, sledovaných v letech 2008 až 2014 ve firmě Roche a v Institut für Diabetes Technologie na univerzitě v německém Ulmu. Testovány byly různé typy glukometrů Contour (Bayer), OneTouch (LifeScan), Accu-Chek (Roche), FreeStyle (Abbott) a firem Bionime, Nipro, TaiDoc a Infopia. Počty různých druhů testovaných proužků, vyráběných a distribuovaných osmi výrobci a také variability mezi šaržemi jsou uvedeny v tabulce 3. Lot-to-lot variabilita (vyjádřená jako maximální pozorovaná diference mezi minimy a maximy hodnot jednotlivých šarží) se pohybovala v intervalu 1 % až 11 % [8].
Texty norem kvality ISO 15197 : 2003 a ISO 15197 : 2013 respektují významnou roli variability šarží proužků a vyžadují při testování a verifikaci glukometrů použití tří různých šarží proužků testovaného systému.
Data systémů Roche prozrazují, že ani velký počet různých podskupin (podle názvů) glukometrů není na překážku kvalitě a srovnatelnosti, pokud tato reálně existuje. V protikladu k tomu je z Tabulky 2 zřejmé, že často různé typy proužků stejných výrobců porovnatelnou kvalitu nemají (LifeScan, Infopia, TaiDoc) a někdy nemají ani kvalitu, požadovanou již překonanou normou kvality ISO 15197 : 2003 (celková chyba TE = ± 20 %).
Velký počet různých druhů a šarží proužků na trhu, zřejmý z Tabulky 3 může významně ztížit objektivitu hodnocení kvality glukometrů v programech EHK i při nutných hodnoceních ve skupinách (peer groups). Za stávajících podmínek (stejné glukometry stejných výrobců se v různých zemích prodávají často pod různými názvy) nelze zaručit spolehlivost údajů o zařazení do stejnorodých skupin ani ze strany laboratoří, ani ze strany distributorů proužků a glukometrů a ani poskytovatele EHK. Často proto není vyjasněna situace ani v názvech, ani u distributorů a výrobců glukometrů a testovacích proužků a následně pak logicky ani v laboratořích a ambulancích. Často je hlavním důvodem změn názvů prakticky totožných glukometrů v různých zemích cenová politika firmy.
Jde možná o situaci, obdobnou v potravinářství, kdy stejné obaly (teoreticky stejných výrobků) použité v různých zemích mohou obsahovat různící se složení [10]. Jako příklad lze uvést problém se skupinou glukometrů Bayer Contour. Ta je alternativně prodávaná také jako Bayer Contour NEXT (hlavně v USA). V ČR je dostupný systém pod názvem Bayer Contour PLUS (podle informace zastoupení se jedná o samostatný typ); a v Německu je zase převážným typ Contour XT (podle informace ovšem plně odpovídá systému „NEXT“), který se ale u nás neobjevuje, je hojně uváděn ve Skandinávii a testován tam organizací SKUP (Scandinavian evaluation of laboratory equipment for primary health care) jako Contour NEXT/TX již v roce 2012.
Skupina, označená v SEKK jako Arkray je uváděna v seznamu SKUP pod (patrně správným) názvem GlucoCard a obdobně. Je na místě poznamenat, že není snadné získat od řady distributorů systémů měření glukózy v krvi informace v potřebné šíři.
Velikost chyb je významně ovlivněna i kvalitou obsluhy. U čtyř glukometrů, úspěšných i v programu SEKK (Accu-Chek, Contour XT, FreeStyle Lite a OneTouch Verio) byly požadavky ISO 15197 splněny jen ve dvou případech jak v rukou laboratorních profesionálů, tak i pacientů. V rukou profesionálů pak u všech čtyř [9].
Testování glukometrů před uvedením na trh
Při nákupu glukometrů od výrobců a jejich distributorů by měly být požadavky na jejich kvalitu důsledně zohledňovány. Jako příklad systematického testování kvality přístrojů POCT včetně glukometrů před uvedením na trh lze uvést právě skandinávskou organizaci SKUP – zmiňovanou již výše - http://www.skup.nu. Požadavek na chybu měření koncentrace glukózy je při testování ve SKUP převzat z norem ISO 15189 : 2003 (20 %) a ISO 15197 : 2013 (15 %). Od roku 2014 se hodnotí glukometry paralelně podle obou norem. Ke stanovení celkové chyby měření se používá standardní postup vyhodnocení diference mezi výsledky vzorků pacientů a referenční metodou. Jako referenční metoda slouží hexokinázová metoda, verifikovaná analýzou certifikovaných referenčních materiálů SRM NIST 965 s certifikovanými hodnotami, získanými metodou ID-GC(LC)/MS. Používá se 90 až 100 vzorků plné krve pacientů. Dalším indikátorem kvality SKUP je preciznost měření testovaného glukometru s požadovanou hodnotou CV ≤ 5 %. Je velmi důležité, že výsledky testování jsou volně přístupné a archivované na výše uvedené webové adrese [11]. Testování SKUP, zahrnuje obvykle výsledky, dosažené laboratorními profesionály i pacienty a jeho součástí je rovněž důležitý faktor komfortu a snadnosti úrovně obsluhy. Evaluační výsledky SKUP, jsou dlouhodobým zdrojem cenných informací o kvalitě POCT systémů pro měření glukózy.
Externí hodnocení kvality, matrice, metrologická návaznost kalibrace
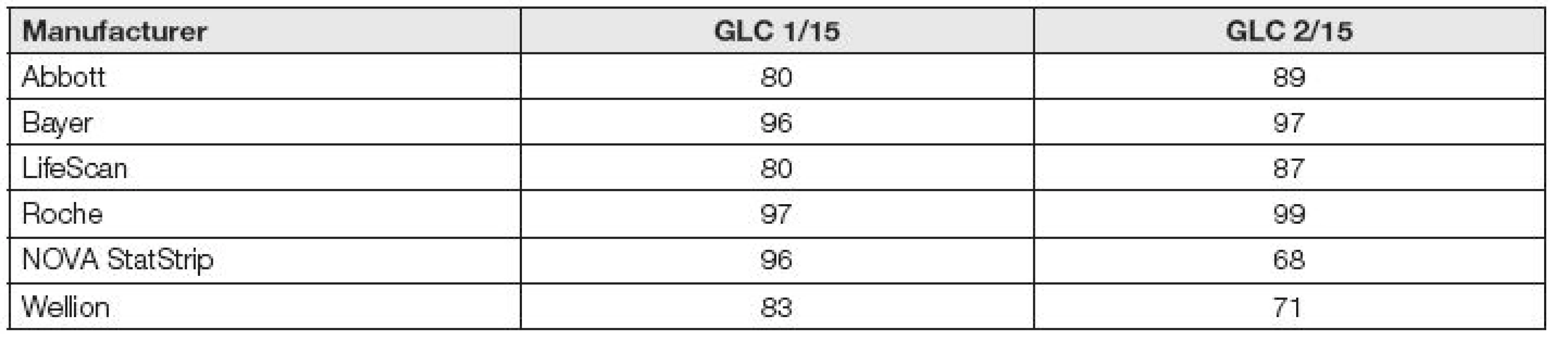
Rozdíly v úspěšnosti různých glukometrů při aplikaci kontrolního limitu Dmax = 10 % a průměru stejnorodé skupiny jako referenční hodnoty v programu EHK-SEKK jsou velmi významné, a ukazují podobně jako data testování glukometrů v Tabulkách 2 a 3, významné rozdíly v jejich kvalitě (Tabulka 4). U kontrolních cyklů GL 2013 až 2015 programu Referenzinstitut für Bioanalytik (RfB Bonn Německo) byla zjištěna průměrná hodnota reprodukovatelnosti CV =18,2 % a úspěšnosti účastníků 90 až 93 % při povolené odchylce Dmax = 15 %. I zde je jako referenční metoda při hodnocení kvality použito hodnot průměrů stejnorodých skupin. U obou programů EHK (SEKK, RfB) je zřejmé, že stále 10 až 30 % výsledků měření vykazuje kontroverzní klinickou kvalitu, že jsou významné rozdíly v kvalitě různých systémů často i téhož výrobce a že občas patrně sehraje roli i nestabilita kvality testovacích proužků (viz Tabulka 4, výrobce Nova). Naopak existují systémy, jejichž úspěšnost se blíží 100 %.
Metrologická návaznost kalibrace glukometrů k měření glukózy v krvi je realizována měřením ve vzorcích plasmatické glukózy, získaných z těchto vzorků a analyzovaných referenční metodou. Obvykle se používá hexokinázové metody, kontrolované certifikovanými referenčními materiály s hodnotami, získanými referenční metodou ID-LC/MS. Přímá návaznost plné krve na referenční metodu není možná kvůli nestabilitě vzorků a kvůli negativnímu efektu velmi nízkých používaných objemů vzorku u glukometrů. Proto případným použitím vzorků plné krve v EHK sice dosáhneme shody matrice kontrolních materiálů s reálnými vzorky pacientů, avšak bez návaznosti na referenci, tedy bez stanovení hodnoty bias. V programech EHK (například v SEKK a RfB Bonn) bývají sice hodnoty referenčních metod k dispozici, ale zatím jich nelze k hodnocení výsledků použít, protože rozdíly průměrů skupin glukometrů od referenční hodnoty jsou u různých glukometrů různé, a to dokonce u různých typů glukometrů stejných výrobců. Typicky lze tyto rozdíly pozorovat mezi skupinou Bayer Contour TS a Bayer Contour Plus, nebo mezi skupinami Abbott Free Lite a Abbott Xceed, kde lze pozorovat interval diferencí (d) od referenční metody až d ± 20 %. To také vysvětluje nutnost používat při hodnocení kvality glukometrů v programech EHK průměrů hodnot, dosažených měřením stejnými glukometry.
Plasma je stabilní a k zajištění metrologické návaznosti na referenční metodu vhodná, ale její získanou certifikovanou hodnotu by bylo nutné korigovat na základě znalosti vztahu mezi koncentrací glukózy v plné krvi a plasmě (průměr hodnoty tohoto faktoru je f = 1,11, nicméně měla by být stanovena specifická hodnota faktoru pro každý systém/glukometr). Tento postup je plánován pro získání ideálního kontrolního materiálu pro programy EHK a má být otestován ještě v roce 2016 [12].
Schéma navrženého postupu, který by umožnil návaznost a hodnocení bias u glukometrů za současné eliminace matricových vlivů je uveden na obr. 1.

Validace šarží proužků a optimalizace dat v dokumentaci výrobců
Navržená podoba dat o analytické kvalitě glukometrů v dokumentaci výrobců a postupy při změně šarže reagenčních proužků jsou uvedeny ve Směrnici FDA (Food and Drug Administration) USA [13] a ve Směrnici amerických endokrinologů k monitorování koncentrace glukózy u ambulantních pacientů [14]. Ve správně vypracované dokumentaci glukometru by měla být podle doporučení FDA data, charakterizující analytickou kvalitu vycházet z údajů 350 uživatelů a měla by být uvedena četnost výsledků s chybami o velikostech do 5 %, 10 % a 15 % tedy rozdělených do tří tříd kvality od nejvyšší s chybou do 5 % po ještě akceptovatelnou s chybou do 15 %. V Tabulce 5 je uveden příklad testování glukometru Bayer Contour Plus s výsledky, provedenými podle tohoto schématu [15].
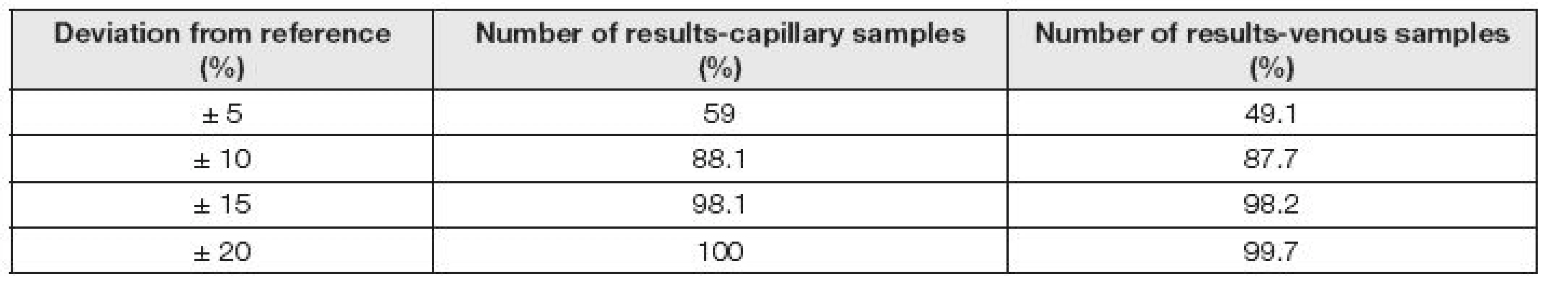
Postup při výměně šarží je navržen ve Směrnici FDA [13]. Směrnice doporučuje trvání verifikace 5 dní, za získání 10 výsledků od každé koncentrace, dosažených na dvou glukometrech. Hodnotí se rozdíl mezi starou a novou šarží. Jako materiál mohou být použity kontrolní vzorky výrobce nebo krve pacientů. Kritéria preciznosti a systematické diference směrnice přesně nespecifikuje, ale doporučuje, aby jejich hodnoty nepřekročily 5 %. Bias se hodnotí zvlášť srovnáním výsledků měření, získaných glukometry s laboratorní metodou pomocí rozdělených vzorků krve pacientů. Tento postup by měl zajistit po nasazení nové šarže testovacích proužků zachování konzistence výsledků a přispět významným způsobem k bezpečnosti pacientů.
Doporučení FDA poskytuje cenné informace uživatelům, případně supervizorům nemocničních sítí glukometrů o systémech měření nad rámec standardní firemní dokumentace a je obrazem toho, jaký důraz je již v současnosti kladený na problémy kvality v této oblasti. Srovnání dvou následných šarží proužků v základní podobě formou paralelních analýz firemních kontrolních materiálů by mělo být nástrojem verifikace šarží i při jejich výměně v supervizovaných sítích glukometrů.
Kontinuální monitorování glukózy (CGM) a jeho analytická kvalita
Koncentrace glukózy se zde většinou průběžně v čase měří v intersticiální tekutině a naměřené hodnoty jsou převáděny na hodnoty koncentrace v krvi v procesu kalibrace. Klíčovými indikátory analytické kvality jsou veličiny ARD (absolute relatived deviation) a MARD (mean of absolute relative deviation).
ARD = 100 x [ I XCGM - YRBG I / YRBG ]
ARD je procentuální rozdíl mezi výsledkem měření glukózy CGM (XCGM) a výsledkem referenčního měření glukózy (YRBG) v krvi u vzorku, změřeného CGM a odebraného pro měření RBG v přibližně stejném čase.
Hlavním ukazatelem analytické kvality je pak hodnota MARD (Mean Absolute Relative Deviation), průměrná hodnota všech hodnot ARD. Systémy CGM jsou kalibrovány v naprosté většině pomocí glukometrů, takže kvalita jejich výsledků měření je přísně závislá na kvalitě použitých glukometrů. Ta je, jak víme, zase závislá na výrobci a typu glukometru a není vždy v souladu s požadavky na ní kladenými příslušnými institucemi (ISO, FDA). Hodnoty MARD < 15 % jsou považovány za akceptovatelné pro CGM systémy, používané na jednotkách intenzivní péče [15]. Spolehlivost uváděných hodnot MARD však může být problematická. Jsou závislé na úrovni referenčních měření, na statistickém zpracování dat (lognormální rozdělení by mělo být preferováno), na počtu hodnocených párů výsledků CGM a referenčních měření a na způsobu kalibrace [16].
Recentní sdělení uvádí, že kalibrace na kapilární a žilní vzorky poskytují diference MARD až o 2 % a v případě hypoglykemických stavů až o 15 % vyšší [17]. Při srovnávání systémů více výrobců se hodnoty MARD pohybuji obvykle v intervalu 10 až 20 % [18 – 20].
Nečastěji jsou testované systémy Medtronic, Guardian, Navigator, FreeStyle, Seven Plus, Enlite, Dexcon G4-G5 (Platinum).
Hodnoty MARD se silně zhoršují s poklesem koncentrace glukózy [21, 22]. Při hypoglykémiích (cgluk < 4 mmol/l) bývají běžně vyšší než 25 % [23]. Kalibrace systému CGM je obvykle prováděna pomocí vzorků kapilární krve, měřených glukometry v četnosti několikrát denně. Ve vývoji jsou i způsoby on line kalibrace [24]. Systémy Free Style používají kalibrace s použitím pevného firemního kalibračního faktoru s hodnotou MARD = 11,4 %, tedy srovnatelnou s ostatními, na glukometry kalibrovanými systémy [25].
Stručný přehled charakteristik aktuálních systémů CGM používaných v USA uvádí Tabulka 6. [26].
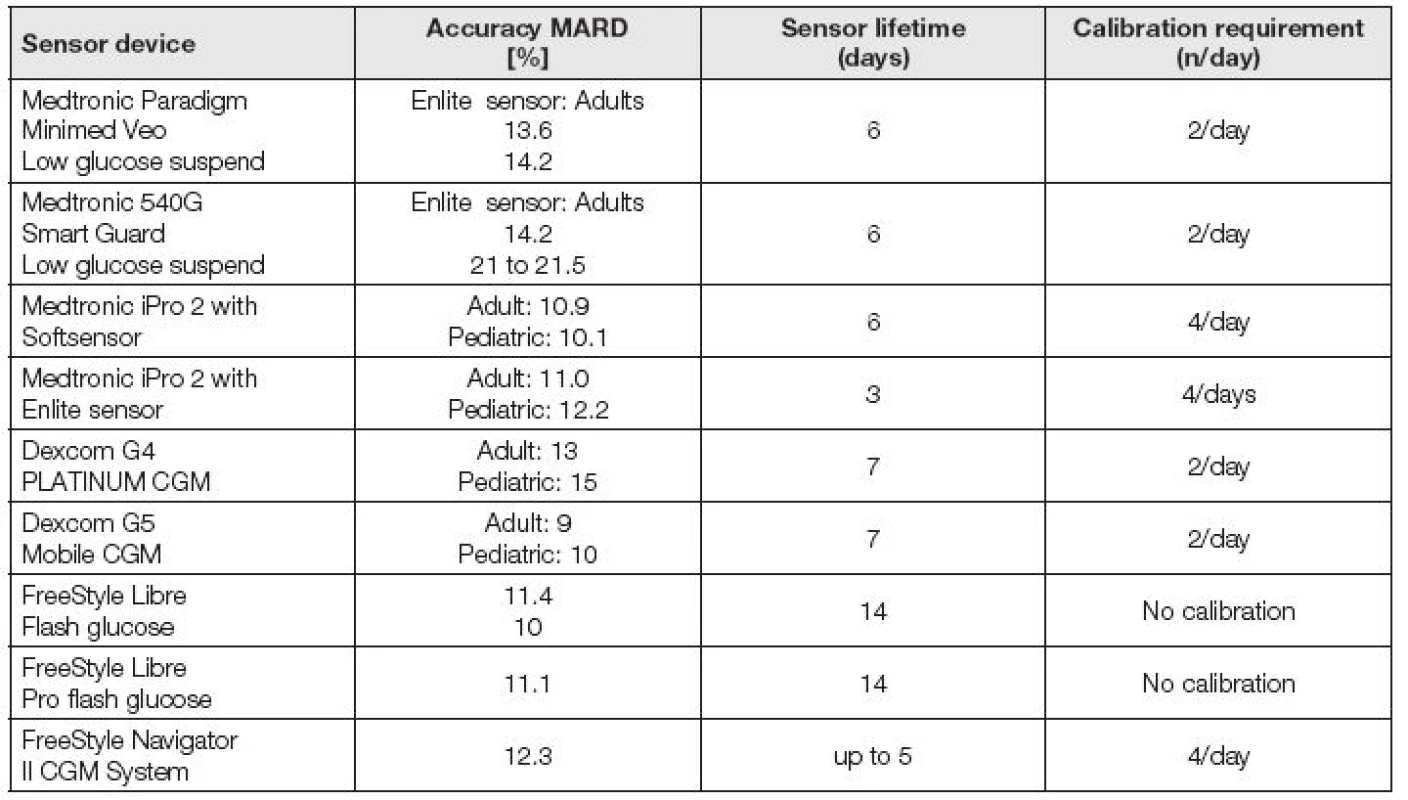
Výhody i nedostatky CGM jsou podrobně popsány v souborné práci Rodbarda [26]. Demonstrací současného možného trendu monitorování glukózy je testování glukometru, použitého v bezdrátovém propojení s inzulinovou pumpou Medtronic [27].
Závěr
Základním indikátorem analytické kvality měření glukózy glukometry a systémů CGM je celková chyba měření, kalkulovaná jako odchylka od referenční hodnoty. U glukometrů se hodnotí počtem výsledků (%), vyhovujících kritériu, u kontinuálního monitorování glukózy CGM pak průměrem diferencí párů vzorků, odebraných/změřených ve stejném čase (MARD). Kritéria pro určení kvality měření glukometry jsou standardizovaná a uvedena v příslušných normách.
Kvalita glukometrů je u jednotlivých typů a výrobců významně rozdílná. S vývojem kontinuálního sledování glukózy lze očekávat výrazný nárůst požadavků na kvalitu a vývoj k harmonizaci výsledků měření CGM s referenčními postupy měření glukózy v plasmě.
Výsledky premarketingových testování, důkladná kvalitní dokumentace výrobců v souladu se Směrnicemi FDA a ISO normami (obsahující i základní metrologická data), omezení variability mezi šaržemi, náhrada méně precizních typů systémů za moderní a externí hodnocení kvality, úplné informace o jednotlivých systémech měření jsou cesty ke zvýšení jeho kvality.
Klíčovými problémy kvality měření glukózy glukometry stále zůstávají:
- kvalita měření glukózy pomocí selfmonitoringu
- kvalita měření v sítích glukometrů ve zdravotnických zařízeních
- úroveň dokumentace systémů předávané výrobci uživatelům
- závislost úrovně kalibrace CGM systémů na kvalitě použitých glukometrů.
Do redakce došlo 16. 3. 2016
Adresa pro korespondenci
RNDr. Bedřich Friedecký, Ph.D.
ÚKBD FN Hradec Králové
Sokolská 581
500 05 Hradec Králové
e-mail: friedecky@sekk.cz
Sources
1. Freckmann, G., Schmid, C., Baumstark, A., Rutschmann, M., Haug, C., Heinemann, L. Analytical performance requirements for self-monitoring of blood glucose with focus on system accuracy:relevant differences among ISO 15197 : 2003, ISO 15197 : 2013 and FDA recommendations. J. Diabet. Sci. Technol., 2015. DOI: 10.1177/1932296815580160.
2. Sacks, D. B., Bruns, D. E., Horton, J., Lindberg, S., Mahoney, J. J., Manzella, S. et al. Point-of - Care Glucose Testing in Acute and Chronic Care Facilities. Approved Guideline –Third Edition. CLSI 2013: POCT 12-A3. Dostupné na: http://shop.clsi.org/point-of-care-documents/POCT12.html.
3. Müller, P., Hattener, A., Stephen, P. Assessing system accuracy of blood glucose monitoring systems using rectangle target plots. J. Diabetes Sci. Technol., 2015, 1932296815612496, first published on October 9, 2015 as doi:10.1177/1932296815612496.
4. Freckmann, G., Link, M., Baumstark, A., Schmid, C., Pleus, S. et al. System accuracy evaluation of 10 SMBG systems with 3 lots each following ISO 15197 : 2013 against 2 different comparison methods. 50th EASD annual meeting Vienna 2014. Poster Nr.1017.
5. Freckmann, G., Schmid, C., Baumstark, A., Pleus, S., Link, M., Haug, C. System accuracy evaluation of 43 blood glucose according to DIN EN ISO 15197. J. Diabetes Sci. Technol., 2012, 6: p. 1060-1075.
6. Freckmann, G., Schmid, C., Pleus, S., Baumstark, A., Link, M. et al. System accuracy evaluation of systems for point-of-care testing of blood glucose: a comparison of a patient-use system with six professional-use systems. Clin. Chem. Lab. Med., 2014, 52/7: p. 1079-1086.
7. Brazg, R., Klaff, L. J., Parkin, C. G. Performance variability of seven commonly used self-monitoring of blood glucose systems: clinical considerations for patients and provider. J. Diabetes Sci. Technol., 2013, 7/1: p. 144-152.
8. Hofmans, M., Oyaert, M., De Schriver, P., Nobels, F., Van Hoovels, L. Clinical laboratories have a critical role in test strips lot management in glucose point-of-care testing. Clin. Chem. Lab. Med. DOI 10.1515/cclm-2015-0820.
9. Selvik, U. O., Risa, M., Jacobsen, C. E., Monsen, G., Sandberg, S. Performance of 10 systems for self-monitoring of blood glucose by trained healthcare professionals and in the hands of the users. Clin. Chem., 2015, 61/5: p. 772-774.
10. Springer, D., Omastová, K., Zima, T. Nástrahy testování POCT systémů pro stanovení glukózy. Klin. Biochem. Metab., 2015, 3: p. 145. Celostátní sjezd klinické biochemie Brno 2015. Poster P-9.
11. Friedecký, B., Kratochvíla, J. SKUP – cesta ke zvýšení kvality péče o pacienty. Prakt. Lék., 2012, 10: p. 492-494.
12. Schumann, G. POCT for glucose measurements in different matrix-reference systems can provide solutions for improved analytical quality. Labquality Days 2016 Helsinki. Dostupné na: http://www.labquality.fi/labquality-paivat/in-english/labquality-days-2016/program/.
13. US Food and Drug Administration: Self-momitoring Blood Glucose Test Systems for Over-the-Counter Use. Draft Guidance for Industry and Food and Drug Administration Staff. 2014. UCM 380327.pdf. Dostupné na: http://www.fda.gov.
14. Bailey, T. S., Grunberger, G., Bode, B. W., Handelmann, Y., Hirsch, I. B., Jovanovič, L. et al. American Association of Clinical Endocrinologists and American College of Endocrinology 2016. Outpatient glucose monitoring consensus statement. Endocrinology Practice, 2016, 22/2: p. 231-261.
15. Ji, L. N., Guo, L. X., Liu, L. B. Accuracy and Presision Assessment of a New Blood Glucose Monitoring System. Clin. Chem. Lab. Med., 2016, 54: p. 181-188.
16. Wilinska, M. E., Hovorka, R. Glucose control in the intensive care unit by use of continuous glucose monitoring: what level of measurement error is acceptable? Clin. Chem., 2014, 60: p. 1500-1509.
17. Kirchsteiger, H., Heinemann, L., Freckmann, G., Lodwig, V., Schmelzeisen-Redeker, G. et al. Performance comparison of CGM systems: MARD values are not always a reliable indicator of CGM system accuracy. J. Diabetes Sci. Technol., 2015, 9: p. 1030-1040.
18. Andelin, M., Kropff, J., Matuleviciene, V., Joseph, J. I., Attwall, S., Theodorsson, E. et al. Assessing the accuracy of continuous glucose monitoring (CGM) calibrated with capillary values using capillary or venous glucose levels as a reference. J. Diabetes Sci. Technol., 2016 pii:1932296815626724.
19. Matuleviciene, V., Joseph, J. I., Andelin, M., Kirsch, I. B., Attwall, S., Pivodic, A. et al. A clinical trial of the accuracy and treatment experience of the Dexcon G4 sensor and Enlite Sensor (guardian real time system) tested simultaneously in ambulantory patients with type I diabetes. Diabetes Technol. Ther., 2014, 16: p. 759-767.
20. Damiano, E. R., McKeon, K., El-Khabib, F. H., Zheng, H., Nathan, D. M., Russel, S. J. et al. A comparative effectiveness analysis of three continuous glucose monitors:The Navigator,G4 Platinum and Enlite. J. Diabetes Sci. Technol., 2014, 8: p. 699-708.
21. Garcia, A., Rack-Gomer, A. L., Bhavaraju, N. C., Haripriyan, H., Kanath, A., Peyser, T. et al. Dexcon G4AP an advanced continuous glucose monitor for the artificial pancreas. J. Diabetes Sci. Technol., 2013, 7: p. 1436-1445.
22. Laffel, L. Improved accuracy of continuous glucose monitoring systems in pediatric patients with diabetes mellitus:results from two studies. Diabetes Technol. Ther., 2016 Suppl.2 S223-S233 DOI:10.1089/dia.2015.0380.
23. Peyser, T., Nakamura, K., Price, D., Bonnett, L. C., Hirsch, I. B., Bato, A. et al. Hypoglycemic accuracy and improved low glucose alerts of the latest Dexcom G4 Platinum continuous monitoring systém. Diabetes Technol. Ther., 2015, 17: p. 548-554.
24. Vetoretti, M., Facchinetti, A., Del Favero, S., Sparacino, G., Cotelli, C. On-line calibration of glucose sensors from the measured current by a time-varying calibration function and Bayesian priors. IEEE Trans. Biomed. Eng., 2015 E pub
25. Bailey, T., Bode, B. W., Christiansen, H. P., Klaff, L. J., Alva, S. The Performance and Usability of a Factory-Calibrated Flash Glucose Monitoring System. Diabetes Technol. Ther., 2015, 17: p. 787-794.
26. Rodbard, D. Continuos glucose monitoring: A review of successes, challenges and opportunities. Diabetes Technol. Ther., 2016, 18, Suppl.2: S2 3-13.
27. Bailey, T., Wallace, J. F., Greene, C., Pardo, S., Brown, D., Pflug, D. I., Klaff, L. J. Accuracy and user performance evaluation of the Contour Next Link 2.4.blood glucose monitoring system. Clin. Chim. Acta, 2015, 448, 25: p. 135-146.
28. POCT 12 A3. Point-Of-Care Blood Glucose Testing in Acute and Chronic Care Facilities. Approved Guideline-Third Edition. Clinical Laboratory Standard Institute 2013.
29. ČSN EN ISO 15197 : 2004. Systémy diagnostických zkoušek in vitro - Požadavky na systémy monitorování glykémie pro sebekontrolu pacientů s diabetes mellitus. UNMZ 2004.
30. ČSN EN ISO 15197 : 2013. Systémy diagnostických zkoušek in vitro - Požadavky na systémy monitorování glykémie pro sebetestování pacientů s diabetes mellitus. UNMZ 2016.
31. Materiál UZIS 2013, dostupné na webové adrese: http://www.uzis.cz
Labels
Clinical biochemistry Nuclear medicine Nutritive therapistArticle was published in
Clinical Biochemistry and Metabolism

2016 Issue 2
-
All articles in this issue
- Chips and Capillary Electrophoresis Based Immunoassays
- The verification of the applicability of NPHS2/SYNPO ratio for diagnosis of FSGS and MCD
- Activity of phosphomannomutase 2 in patients with suspected congenital disorder of glycosylation
- Quality, control and validation of glucometers and CGM systems. Status overview
- Postanalytical phase and interpretation of laboratory tests
- Changes in Paraoxonase 1 activity and concentration of conjugated dienes in connection with number of metabolic syndrome components
- Clinical Biochemistry and Metabolism
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Quality, control and validation of glucometers and CGM systems. Status overview
- Postanalytical phase and interpretation of laboratory tests
- Activity of phosphomannomutase 2 in patients with suspected congenital disorder of glycosylation
- The verification of the applicability of NPHS2/SYNPO ratio for diagnosis of FSGS and MCD
