Vrozená centrální choriorentinitida toxoplasmové etiologie - kazuistika
:
K. Maršolková 1; J. Timkovič 1,2; V. Lesková 3; J. Němčanský 1,2; H. Wiedermannová 3,4
:
Oční klinika, Fakultní nemocnice Ostrava
1; Katedra kraniofaciálních oborů, Lékařská fakulta, Ostravská univerzita
2; Oddělení neonatologie, Fakultní nemocnice Ostrava
3; Katedra dětského lékařství a neonatologie, Lékařská fakulta, Ostravská univerzita Oční klinika, Fakultní nemocnice Ostrava, 17. listopadu 1790/5, 708 00, Ostrava, přednosta: MUDr. Jan Němčanský, PhD.
4
:
Čes. a slov. Oftal., 74, 2018, No. 3, p. 114-118
:
Case Report
prolekare.web.journal.doi_sk:
https://doi.org/10.31348/2018/1/6-3-2018
Kongenitální toxoplasmosa je celosvětově rozšířené onemocnění způsobené transplacentárním přenosem intracelulárního parazita Toxoplasma gondii. V případě vertikálního přenosu může infekce způsobit závažné multiorgánové komplikace až úmrtí plodu v závislosti na fázi těhotenství v okamžiku nákazy a na celkovém stavu imunitního systému matky. Z příznaků je známá častá triáda chorioretinitida, hydrocefalus a intrakraniální kalcifikace. Právě toxoplasmová chorioretinitida je jejím nejčastějším očním projevem a v případě zasažení centrální oblasti sítnice může vést k závažnému postižení centrální zrakové ostrosti nebo až ke slepotě dítěte. V současné době je v České republice prenatální screening tohoto onemocnění dobrovolný.
Práce dokumentuje případ chorioretinitidy toxoplasmové etiologie u novorozeného chlapce zachycené v aktivním stádiu a vývoj sítnicového nálezu v čase. Dále se věnuje celkovým multiorgánovým komplikacím popsaným u tohoto pacienta, kdy na základě diagnostikovaného hydrocefalu bylo indikováno oční vyšetření, které stanovilo závažné změny na očním pozadí. Hydrocefalus u chlapce byl následně řešen.
V textu práce je popsán stručný souhrn dostupných diagnostických a terapeutických metod a možnosti screeningu onemocnění v porovnání s jinými zeměmi.
Klíčová slova:
kongenitální toxoplasmosa, chorioretinitis, multiorgánové komplikace, screening, hydrocefalus
Úvod
Kongenitální toxoplasmosa vzniká po primární infekci matky během gravidity intracelulárním parazitem Toxoplasma gondii a následným transplacentárním přenosem parazita na plod. Incidence se pohybuje mezi 1 až 10 na 10 000 živě narozených dětí v zemích Evropy a USA [1,12,13,15], v České republice je to okolo 0,2/10 000 [23].
Výskyt závažných příznaků je nepřímo úměrný pravděpodobnosti infikování matky během celého těhotenství [1,13]. To znamená, že pravděpodobnost infekce Toxoplasmou vzrůstá s gestačním věkem, avšak je také závislá na celkovém stavu imunitního systému matky. Nejzávažnějšími komplikacemi onemocnění jsou potrat, úmrtí plodu nebo neurosenzorické poruchy novorozence, ale jejich výskyt je nejčastější v prvním trimestru, kdy je riziko nákazy mezi 10 až 25 % [1,12]. Ve druhém trimestru stoupá riziko nákazy na 30 – 45 %, ale závažnost příznaků klesá [1,12]. Nejčastěji jsou popisovány projevy akutní infekce jako encefalitida, pneumonie, hepatosplenomegalie či lymfadenopatie. Přestože pravděpodobnost infekce novorozence během třetího trimestru je až 60–80 %, nemusí být patrná téměř žádná klinická manifestace onemocnění nebo jen nespecifické příznaky. Onemocnění se však může manifestovat až v pozdějším životě dítěte [1,6,12,13].
Toxoplasmová chorioretinitida je nejčastější oční komplikací celkového onemocnění. Objevuje se u 70–90 % pacientů s vrozenou formou onemocnění, méně často pak jako komplikace získané primární nákazy [13]. Z dalších očních příznaků kongenitální toxoplasmosy jsou popisovány mikroftalmie, kongenitální katarakta, glaukom anebo strabismus [5,10,12,13,14,19].
Prvním lékařem, který u nás pozoroval a v literatuře popsal nález toxoplasmové uveitidy a chorioretinitidy, byl profesor Josef Janků, jehož publikace byly později citovány také v zahraniční literatuře [7,8,9].
Cílem předložené práce je popsat klinický průběh onemocnění u novorozence s kongenitální formou toxoplasmosy manifestující se postižením obou očí a centrálního nervového systému (CNS).
Kazuistika
Chlapec se narodil z druhé gravidity ve 38. gestačním týdnu, screening matky na Streptococcus agalactiae byl negativní. Fyziologický prenatální průběh byl zdokumentovaný až do 26. gestačního týdne, kdy proběhlo poslední ultrazvukové vyšetření plodu, další doporučená vyšetření již matka odmítla. Porod proběhl spontánně, mimo zdravotnické zařízení za přítomnosti porodní asistence. Chlapec se rodil záhlavím, porod provázel odtok mírně zkalené plodové vody. Anamnesticky bezprostředně po porodu přítomné dechové potíže novorozence po prodýchnutí ustoupily a následně dítě ventilovalo pravidelně. Byla zjištěna porodní hmotnost 3245 g a délka 50 cm. Ihned po porodu byla patrná nápadně velká hlavička, jinak bylo dítě bez výraznějších pozoruhodností. (Obr. 1) Následující den matka navštívila ambulanci pro rizikové novorozence, kde byl zjištěn obvod hlavy chlapce 38,5 cm (fyziologická norma dle růstové křivky pro daný věk je 32,5 až 37,5 cm) [14]. Po ultrasonografickém vyšetření hlavy (USG), které prokázalo známky hydrocefalu (Obr. 2), byl chlapec bezprostředně odeslán a následně přijat na jednotku intenzivní péče Oddělení neonatologie Fakultní nemocnice v Ostravě. Obr. 1
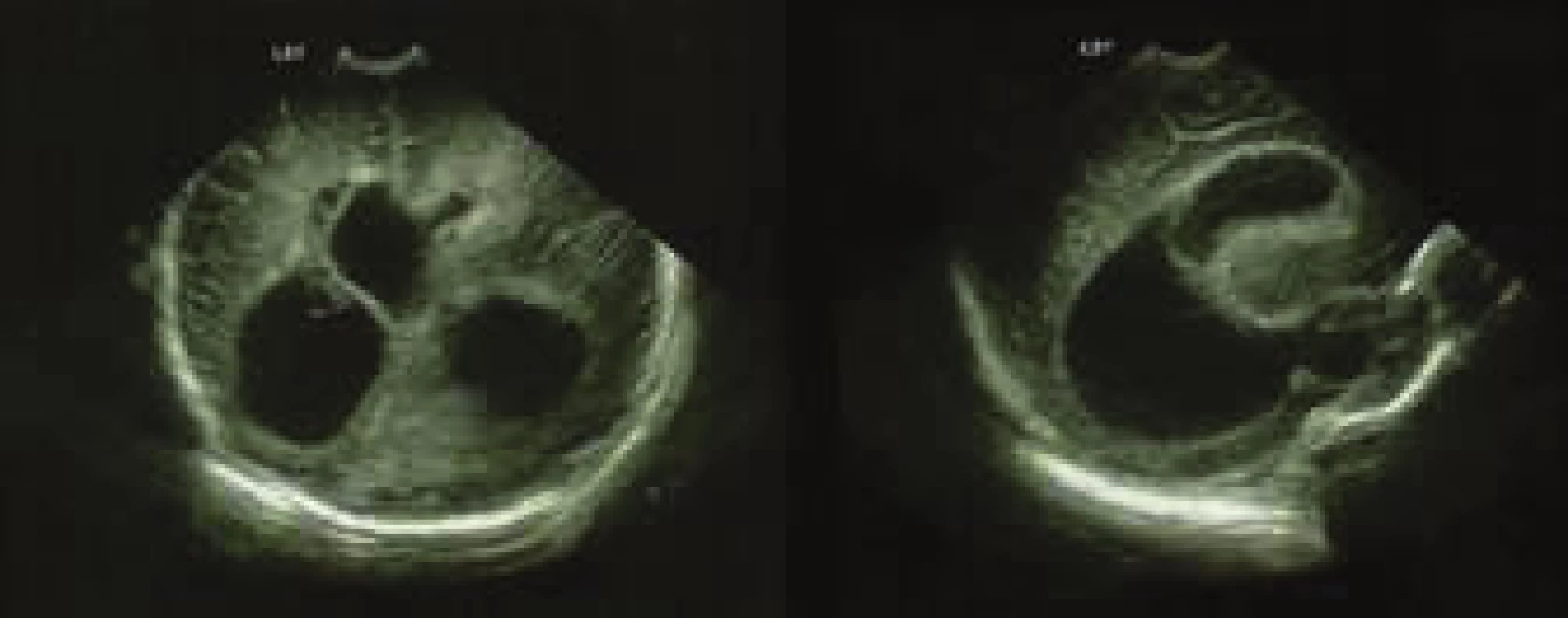
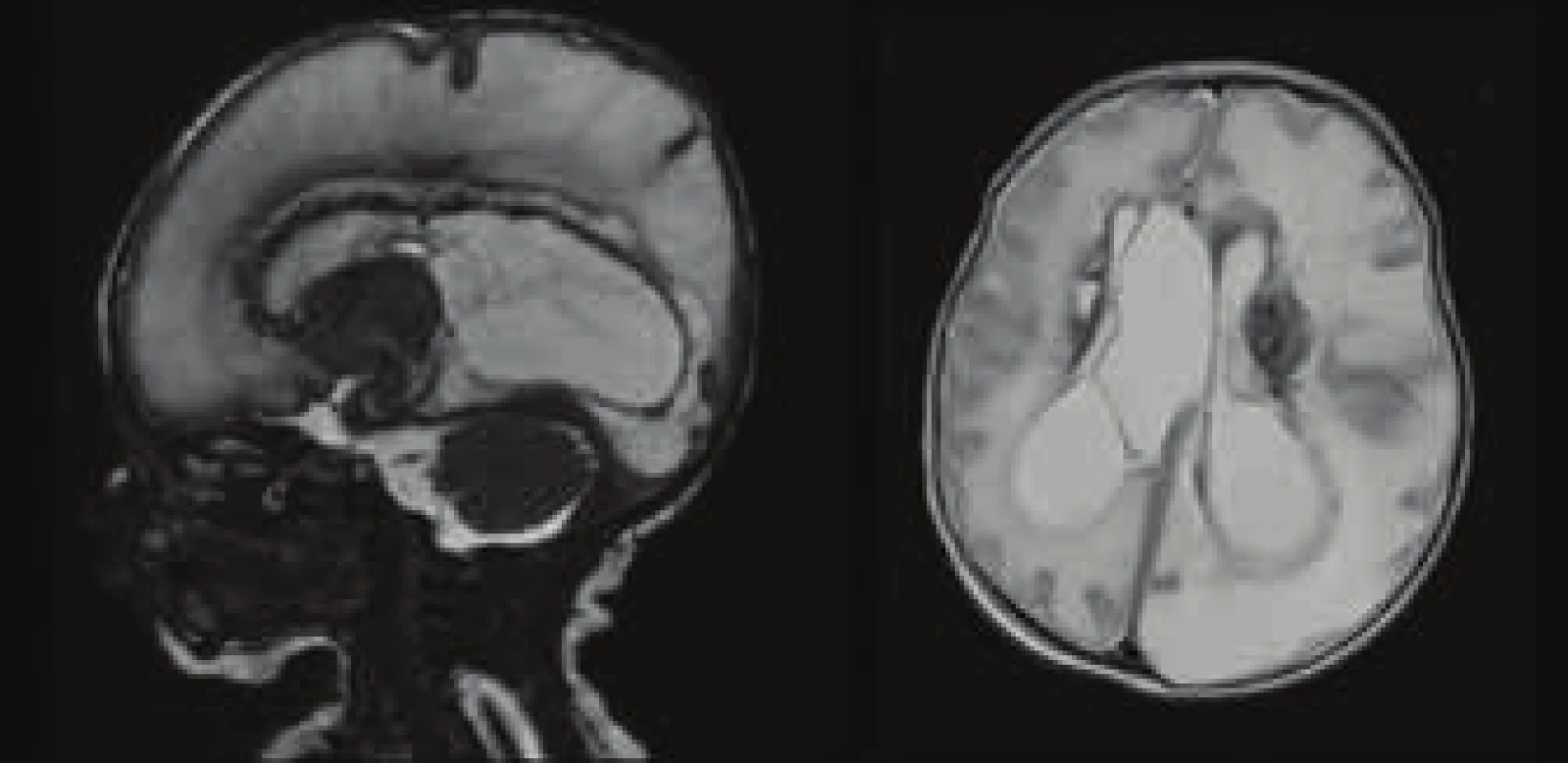
Při vstupním vyšetření byl chlapec kardiopulmonálně stabilní, spontánně ventilující a kromě většího obvodu hlavičky byl celkový fyzikální nález bez pozoruhodností. Nález dilatace mozkových komor při vyšetření magnetickou rezonancí (MRI) potvrdil podezření na hydrocefalus. Na snímcích z magnetické rezonance byla kromě obstrukčního hydrocefalu přítomna rovněž rozsáhlá postischemická a prokrvácená ložiska v obou mozkových hemisférách, jako následek hypoxického stavu. (Obr. 3) Z indikace neurochirurga byla u chlapce provedena zevní komorová drenáž, ta byla následně vzhledem k malfunkci nahrazena Ommaya rezervoáry zavedenými parietookcipitálně. Byly odebrány krevní vzorky na sérologické vyšetření panelu TORCH (Toxoplasma gondii, rubeola, cytomegalovirus, Herpes simplex). Obrázek č. 2 a 3
V rámci konziliárního vyšetření bylo ve 40. postkoncepčním týdnu věku chlapce provedeno první oftalmologické vyšetření. Nález na předním segmentu byl fyziologický. Vyšetření očního pozadí v arteficiální mydriáze odhalilo v centrální krajině sítnice na obou očích přítomnost aktivního chorioretinálního zánětlivého ložiska bělavé barvy, velikosti trojnásobku průměru optického disku (PD), zasahující foveu. Při okraji zánětlivého ložiska byl cirkulárně patrný edém, vlevo byl nasální a horní okraj ložiska již jemně pigmentovaný. Ostatní sítnice byla bez hrubých ložiskových změn (Obr. 4a). Bylo vysloveno podezření na chorioretinitidu toxoplasmové etiologie.
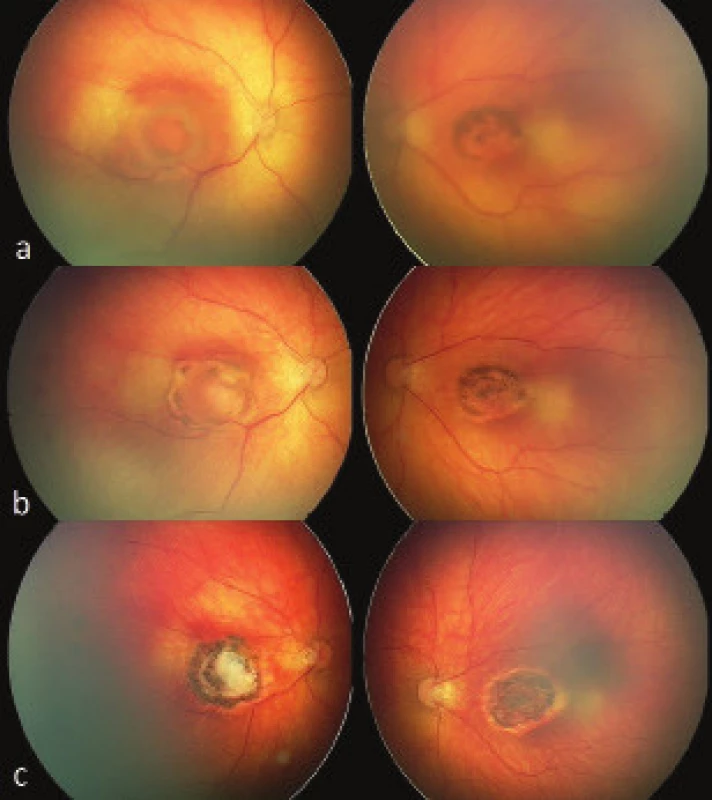
Byla provedena lumbální punkce s negativním nálezem kultivačního průkazu patogena. V krevních odběrech chlapce byla patrná elevace zánětlivých markerů (C reaktivní protein). V sérologickém vyšetření byl pak popsán nález pozitivity protilátek IgG proti Toxoplasma gondii s nízkou aviditou (179,63 IU/ml), přičemž hodnota protilátek IgA a IgM v séru byla hraniční. Kongenitální infekce se potvrdila také pomocí techniky PCR (polymerázové řetězové reakce). Dítěti byla nasazena celková terapie pyrimethaminem v dávce 1 mg/kg/den a sulfadiazinem 100 mg/kg/den. Celková terapie byla doplněna o kalciumfolinat v dávce 10 mg denně s cílem omezit negativní toxický účinek antitoxoplasmové medikace. Obrázek č. 4
Oční vyšetření v odstupu čtyř týdnů po zahájení celkové léčby prokázalo oboustranně ustupující zánětlivou aktivitu i edém a při okraji ložisek pokračující pigmentaci. (Obr. 4b) Celkovou léčbu nastavili a vedli infekcionisté, z očního hlediska byl zvolen konzervativní postup a byl nastaven pravidelný režim očních kontrol s fotodokumentací. Během dalších několika týdnů se chorioretinální atrofická ložiska zajizvila centrálně a okraje lézí byly oboustranně cirkulárně pigmentované již bez přítomnosti edému či jiných známek aktivity zánětu. Periferní sítnice byla bez nových ložiskových změn. (Obr. 4c) Při všech oftalmologických kontrolách byl přední segment oka bez zjevné patologie.
Z neurologického hlediska byl u chlapce diagnostikován centrální hypertonický syndrom. Pro riziko rozvoje spasticity byla zahájena intenzivní rehabilitace. Nález se postupně na USG stabilizoval a dítě bylo po téměř dvou měsících hospitalizace propuštěno ve stabilizovaném stavu do ambulantní péče, již bez známek nitrolební hypertenze. Byla nastavena celková medikace podle protokolu [4], kdy po 3 měsících je vždy pyrimethamin a sulfadiazin na měsíc nahrazen spiramycinem v dávce 100 mg/kg/den střídavě až do jednoho roku dítěte. Při dimisi byl nastaven pravidelný režim pediatrických, neurologických, neurochirurgických a očních kontrol.
Při dalších oftalmologických kontrolách nebyly zjištěny změny sítnicového nálezu ani reaktivace při okrajích ložiska, avšak při kontrole v devátém měsíci věku chlapce upoutaly již při aspekci zřetelné bloudivé až nystagmoidní pohyby očních bulbů. Chlapec fixoval na světlo pouze krátkodobě a při vyšetření předního segmentu byl červený reflex rušen patrným bělavým odleskem centrálního atrofického ložiska sítnice. Velikost ložisek je i nadále bez vývoje v čase, jejich okraje zůstávají výrazně hyperpigmentované s atrofickým centrem (Obr. 4c). Vzhledem k oboustrannému těžkému zrakovému postižení a vývoji okulogenního nystagmu byla rodičům doporučena zraková stimulace. Při posledních neurologických kontrolách byl chlapec celkově zaléčen pro zaznamenané opakované záchvaty epilepsie charakteru myoklonií. Chlapec je i nadále v multioborové péči a vývoj jeho celkového i lokálního očního nálezu je důkladně sledován a dokumentován.
Diskuse
Infekce parazitem Toxoplasma gondii je v dnešní době v populaci velmi rozšířená. Její výskyt se odhaduje okolo 25–30 % celosvětově, ale může se výrazně lišit mezi jednotlivými kontinenty či státy [15,17]. Popsány jsou rovněž rozdíly mezi různými komunitami v rámci jednoho regionu [1,15,19]. K rozdílům v incidenci přispívá kromě sociálních podmínek obyvatel dané oblasti také různá virulence jednotlivých sérotypů. Sérologický typ II je rozšířen hlavně v Evropě a Severní Americe a je méně virulentní. Oproti tomu více virulentní atypické sérotypy I a III vyskytující se hlavně ve Střední a Jižní Americe jsou asociovány s vyšším výskytem intraokulárních komplikací, a to i při nákaze imunokompetentního pacienta postnatálně [1,10,15,24].
K nákaze plodu dochází vertikálním přenosem parazita při primární infekci matky (nejčastěji alimentárně) během nebo až do šesti měsíců před počátkem těhotenství. Sekundární infekce s následným fetálním přenosem byla popsaná, v našich podmínkách je ale extrémně vzácná. [6]. O průniku tachyzoitů parazita do amniové tekutiny a poté do fetálního prostoru rozhoduje imunitní kontrola placentárního přenosu, avšak celý mechanismus ani faktory jej ovlivňující nebyly zcela objasněny [17].
Toxoplasmová chorioretinitida je nejčastější oční komplikací způsobující zhoršení centrální zrakové ostrosti až kompletní ztrátu visu. Parazit invaduje buňky sítnice, ve kterých může v cystickém stádiu setrvat různě dlouhou dobu. V okamžiku, kdy se mikroorganismy aktivují a začnou se intracelulárně množit, může dojít k projevům chorioretinitidy, a to i několik desítek let po kongenitální nákaze [3,18,24].
K potvrzení diagnózy je nutné sérologické vyšetření krevního vzorku postiženého, které prokáže pozitivitu IgG a IgM protilátek proti Toxoplasmě. V případě potřeby lze k definitivnímu rozhodnutí provést molekulární vyšetření amniové tekutiny pomocí techniky PCR [2,3,6,13,17,25]. Poté je nutno ihned zahájit celkovou léčbu matky (již během těhotenství) a následně i novorozence. Včasné určení diagnózy a zahájení léčby ovlivňuje závažnost průběhu infekce i vývoj pozdních komplikací. Standardně se nasazuje celková léčba v trojkombinaci pyrimethamin, sulfadiazin a kyselina listová. Ta se podává k omezení vedlejších toxických účinků antitoxoplasmové terapie, jelikož pyrimethamin způsobuje útlum krvetvorby v kostní dřeni. Léčbu eventuálně doplňujeme o kortikosteroidy. Tato trojkombinace se vždy po 3 měsících nahrazuje spiramycinem a léčba pokračuje až jeden rok [4,13,11,25]. Další popisovanou možností celkové terapie je čtyřkombinace s kotrimoxazolem a klindamycinem, která má méně nežádoucích účinků a byla popsána i rychlejší regrese ložisek onemocnění na sítnici v porovnání s klasickou trojkombinací [10,18].
V poslední době je často diskutována možnost podání léčby intravitreálně. Byly popsány případy regrese aktivního ložiska toxoplasmové chorioretinitidy a zlepšení centrální zrakové ostrosti u dospělých pacientů po intravitreálním podání klindamycinu v kombinaci s dexamethasonem [26]. Autoři studie zabývající se možnostmi intravitreální terapie toxoplasmové chorioretinitidy jako alternativy ke klasické kombinaci léčiv popsali dobrý efekt a zlepšení centrální zrakové ostrosti minimálně o dva řádky ETDRS optotypu (early treatment diabetic retinopathy study). Po podání kombinace léčiv trimetoprim/sulfametoxazol/dexamethasone intravitreálně došlo k rychlé regresi sítnicových ložisek [22]. Všechny tyto možnosti by byly dobrou alternativou u pacientů s nežádoucími účinky či alergií na celkovou léčbu, což by mohlo výrazně zkrátit dobu podání celkové terapie a tím zlepšit compliance pacientů.
V případě rozvoje pozdní komplikace v podobě choroidální neovaskulární membrány jsou k dispozici další terapeutické postupy, jako laserová fotokoagulace sítnice nebo fotodynamická terapie [11,16]. Dobrý efekt byl rovněž popsán po intravitreální aplikaci anti-VEGF preparátů pravděpodobně proto, že VEGF (vaskulární endotelový růstový faktor), zde hraje roli nejenom v procesu neoangiogeneze a tedy tvorbě neovaskulární membrány, ale také jako prozánětlivý mediátor [11]. Ke zlepšení sítnicového nálezu došlo po aplikaci bevacizumabu (Avastin – u nás se jedná o off-label terapii) [16], ranibizumabu [20] či afliberceptu (jedná se o pilotní studii) [11].
K dalším očním komplikacím, které byly v literatuře popsány, patří vitritida, epiretinální membrána, subretinální kolekce tekutiny až vývoj serózního odchlípení sítnice [19,26].
Vzhledem k tomu, že celková i lokální léčba je organizačně velmi náročná a finančně nákladná, byl již v některých státech Evropy zaveden povinný pravidelný prenatální screening tohoto onemocnění (Belgie, Francie, Rakousko, Slovensko, Slovinsko) [23]. Mnohé studie z těchto zemí dokazují, že z dlouhodobého hlediska může plošné vyšetřování těhotných zavčas odhalit infekci a lze tak ihned zahájit léčbu matky. Výsledkem je zmírnění následků infekce postiženého novorozence a v neposlední řadě také pozitivní ovlivnění vývoje pozdních komplikací infekce Toxoplasmou [15,21,24,25]. Všechny děti s diagnostikovanou kongenitální toxoplasmosou by měly být pravidelně dispenzarizovány oftalmologem až do dospělosti, jelikož i při včasném zahájení léčby nelze vyloučit pozdní manifestaci či reaktivaci onemocnění [3,24]. Zároveň se ukazuje, že zavedení povinného screeningu infekce Toxoplasma gondii by bylo výhodné i z finančních důvodů [15].
Závěr
Novorozené dítě s podezřením na vrozenou toxoplasmovou infekci by mělo být komplexně vyšetřeno od krevních odběrů až po zobrazovací metody jako je ultrasonografie, počítačová tomografie či magnetická rezonance. Dále by mělo být vyšetřeno specialistou v oboru neurologie, infekčního lékařství a oftalmologie a v případě potvrzení vrozené toxoplasmosy či její oční formy by měla být bezprostředně zahájena celková léčba.
Diagnostika i terapie tohoto onemocnění je velmi náročná, a proto by se měla pozornost věnovat také způsobům omezení šíření infekce. Účinným prostředkem by bylo zavedení povinného screeningu infekce v graviditě. Je však také úkolem zdravotnického personálu informovat gravidní ženy, aby se vyvarovaly rizikového chování a pokud možno dodržovaly během těhotenství zdravý životní styl.
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmů a není podpořeno žádnou farmaceutickou firmou.
Do redakce doručeno dne: 17.5.2018
Do tisku přijato dne: 19.7.2018
MUDr. Kristýna Maršolková
Oční klinika, Fakultní nemocnice Ostrava, 17. listopadu 1790/5, 708 52, Ostrava
Sources
1. Bischoff, A.R., Friedrich, L., Cattan, J.M. et al.: Incidence of Symptomatic Congenital Toxoplasmosis During Ten Years in a Brazillian Hospital. Pediatr Infect Dis J, 35; 2016 : 1313-1316.
2. Boyer, K., Hill, D., Mui, E. et al.: Unrecognized Ingestion of Toxoplasma gondii Oocysts Leads to Congenital Toxoplasmosis and Causes Epidemics in North America. CID, 53; 2011 : 1081-1089.
3. Faucher, B., Garcia-Meric, P., Franck, J., et al.: Long-term ocular outcome in congenital toxoplasmosis: A prospective kohort of treated children. J Infect, 64; 2012 : 104-109.
4. Geleneky, M., Prášil, P., Kodym, P.: Doporučený postup pro diagnostiku a léčbu toxoplasmózy [online]. Schváleno výborem Společnosti infekčního lékařství ČLS JEP v červnu 2017, datum vydání 7. listopadu 2017. Dostupné na WWW: < https://www.infekce.cz/DoporToxo17.htm >.
5. Guha, R., Miley, L., Aspiri M. et al.: Congenital Toxoplasmosis. Pediatr Neurol, 70; 2017 : 81-82.
6. Handl, V.K., Klingelhöfer, D., Schlöffel, N. et al.: Kongenitale Toxoplasmose und Toxoplasma gondii. Zbl Arbeitsmed, 66; 2016 : 239-248.
7. In Pepose J.S., Holland, G.H., Wilhalmus, K.R.: Ocular Infection Immunity. Mosby, St.Lois, 1996, p. 1183-1224.8.
8. Janků, J.: Pathogenesa a patologická anatomie tak nazvaného vrozeného kolobomu žluté skvrny v oku normálně velikém a mikrophtalmickém s nálezem parasitů v sítnici.Cas Lek Ces, 62; 1923 : 1021-1027.
9. Janku J.: Die patogenese ung pathologishe Anatomie des sogenannten angeborenen Koloboms des gelben Fleckes im normal grossen sowie im mikrophthalmishen Auge mit Parasitenbefund in der Netzhaut. Cls Parasit, 6; 1959 : 9-16.
10. Kartasasmita, A., Muntur, W.P., Enus, S. et al.: Rapid resolution of toxoplasma chorioretinitis treatment using quadruple therapy. Clin Ophthalmol, 11; 2017 : 2133-2137.
11. Korol, A.R., Zborovska, O., Kustryn, T. et al.: Intravitreal aflibercept for choroidal neovascularization associated with chorioretinitis: a pilot study. Clin Ophthalmol, 11; 2017 : 1315-1320.
12. Melamed, J., Eckert, G.U., Spadoni, V.S. et al.: Ocular manifestations of congenital toxoplasmosis. Eye, 24; 2010 : 528-534.
13. Modrzejewska, M., Patalan, J., Kulik, U. et al.: Ocular manifestation of congenital toxoplasmosis, clinical implication – case report. Ginekol Pol, 87; 2016 : 226-230.
14. Paulová M., Vignerová J., Riedlová J.: Individuální hodnocení růstu pomocí růstových grafů se zaměřením na děti do 2 let. Neonatologické listy 15; 2009 : 3-9.
15. Prusa, A-R., Kasper, D.C., Sawers, L. et al.: Congenital toxoplasmosis in Austria: Prenatal screening for prevention is cost-saving. PloS Negl Trop Dis. 2017, č. 11 [cit. 2017-04-21]. Dostupný na WWW: < http://doi.org/10.1371/journal.pntd.0005648 >.
16. Rishi P.,Venkataraman A., Rishi E.: Combination photodynamic therapy and bevacizumab for choroidal neovascularization associated with toxoplasmosis. Indian J Ophthalmol. 2011;59(1):62-64.
17. Robert-Gangneux, F., Dard M.-L.: Epidemiology of and Diagnostic Strategies for Toxoplasmosis. Clin Microbiol Rev. 2012 Apr; 25(2): 264–296.
18. Rothova, A., Meenken, C., Buitenhuis, H.J. et al.: Therapy for Ocular Toxoplasmosis. Am J Ophthalmol, 115; 1993 : 517-523.
19. Sahinoglu-Keskek, N., Unal F., Cevher, S. et al.: Cause of visual impairment in patiens with ocular toxoplasmosis. J Infect dev Ctries, 11; 2017 : 192-195.
20. Shah NJ, Shah UN.: Intravitreal ranibizumab for the treatment of choroidal neovascularization secondary to ocular toxoplasmosis. Indian J Ophthalmol. 2011;59(4):318-319.
21. Smit, S.A., Padalko, E., Acker, J.V. et al.: Public Health Impact of Congenital Toxoplasmosis and Cytomegalovirus Infection in Belgium, 2013: A Systematic Review and Data Synthesis. CID, 20; 2017 : 1-8.
22. Souza, C.E., Nascimento, H., Lima, A. et al.: Intravitreal Injection of Sulfametoxazole and Trimethoprim Associated with Dexamethasone as an Alternative Therapy for Ocular Toxoplasmosis. Ocul Immunol Inflamm, 00; 2017 : 1-4.
23. Surveillance Atlas of Infectious Diseases. Dataset provided by ECDC based on data - provided by WHO and Ministries of Health from the affected countries. Dostupné na WWW: < http://atlas.ecdc.europa.eu/public/index.aspx >.
24. Wallon, M., Garweg, J.G., Abrahamowicz, M. et al.: Ophthalmic Outcomes of Congenital Toxoplasmosis Followed Until Adolescence. Pediatrics, 133; 2014: e601-e608.
25.. Wallon, M., Peyron, F.: Congenital Toxoplasmosis: A Plea for a Neglected Disease. Pathogens, 7; 2018 : 25.
26. Zamora, Y.F., Arantes, T., Reis, F.A. et al.: Local treatment of toxoplasmic retinochoroiditis with intravitreal clindamycin and dexamethasone. Arq Bras Oftalmol, 78; 2015 : 216-219.
Labels
OphthalmologyArticle was published in
Czech and Slovak Ophthalmology
2018 Issue 3
-
All articles in this issue
- Ophthalmological finding in a patient with lowe syndrome
- Marshall and stickler syndrome in one family
- Congenital central toxoplasmic chorioretinitis - case study
- Asphercial iols and their effect on visual, depth of field, spherical aberration and contrast sensitivity
- Conjuctival lesions - the relationship of papillomas and squamous cell carcinoma to HPV infection
- Ophthalmic manifestations of acute leukaemias
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Ophthalmic manifestations of acute leukaemias
- Asphercial iols and their effect on visual, depth of field, spherical aberration and contrast sensitivity
- Congenital central toxoplasmic chorioretinitis - case study
- Marshall and stickler syndrome in one family

