Vplyv aplikácie botulotoxínu A v neurooftalmologických indikáciách na výsledky Schirmerovho testu a osmolarity sĺz
Authors:
P. Žiak 1; J. Halička 1; K. Kapitánová 1; P. Mojžiš 2
Authors‘ workplace:
Očná klinika, Jesseniova Lekárska fakulta v Martine, Univerzita Komenského v Bratislave, Slovenská Republika. Prednosta: MUDr. Peter Žiak, Ph. D.
1; Premium Clinic, Teplice, Česká republika Vedúci: MUDr. Peter Mojžiš, Ph. D., FEBO
2
Published in:
Čes. a slov. Oftal., 75, 2019, No. 2, p. 74-77
Category:
Original Article
doi:
https://doi.org/10.31348/2019/2/3
Overview
Botulotoxín A (BT-A) sa používa v neurooftalmologických indikáciách ako terapia esenciálneho blefarospazmu a faciálneho hemispazmu, už viac ako 20 rokov. Napriek tomu, že dlhodobý efekt opakovaných aplikácií BT-A bol opakovane potvrdený, názory na vplyv BT-A na produkciu a retenciu sĺz nie sú jednoznačné. V našej práci sme sledovali vplyv lokálne aplikovaného BT-A u pacientov s esenciálnym blefarospazmom a hemifaciálnym spazmom na výsledky Schirmerovho testu a osmolaritu sĺz. Hodnotili sme zmeny vo výsledkoch Schirmerovho testu a osmolarity sĺz pred a 14 dní po lokálnej aplikácií BT-A (Botox inj, Allergan, Irvine, USA) do musculus orbicularis oculi v rámci terapie neurooftalmologických ochorení. Použili sme dávky 16-18 U u unilaterálnej a 32-36 U u bilaterálnej aplikácie.
Priemerná hodnota Schirmerovho testu bola pred aplikáciou BT-A 8,38 ± 0,63 mm (n = 50), 2 týždne po aplikácií BT-A bola 7,12 ± 0,6 mm (n = 50). Pred podaním BT-A bola osmolarita sĺz 305,4 ± 9,2 mOsm (n = 13), 14 dní po podaní BT-A ostala osmolarita sĺz na úrovni 305,2 ± 8,6 mOsm (n = 13).
Zistili sme signifikantný rozdiel medzi oboma skupinami v kvantite (p < 0,012), ale nie v kvalite sĺz (p > 0,05). Vplyv aplikácie BT-A na výsledky Schirmerovho testu sa prejavil v zmysle zníženia množstva sĺz. Uvedené výsledky potvrdzujú, že empirické klinické skúsenosti vedúce k doporučeniu aplikácie umelých sĺz u pacientov po aplikácii BT-A v neurooftalmologických indikáciách majú racionálny základ.
Klíčová slova:
botulotoxín – Schirmerov test – osmolarita sĺz – suché oko – blefarospazmus – hemispazmus
Úvod
Niekoľko štúdií potvrdzuje, že pacienti s tvárovými dystóniami trpia na suché oko [1-3]. Botulotoxín A (BT-A) sa používa na liečbu esenciálneho blefarospazmu a hemifaciálneho spazmu, už viac ako 20 rokov. Dlhodobý terapeutický efekt opakovaných aplikácií BT-A bol opakovane potvrdený a aplikácia BT-A je považovaná za metódu voľby [4]. Naopak, názory na vplyv BT-A na produkciu a tiež retenciu sĺz v spojovkovom vaku nie sú celkom jednotné. Vplyv BT-A môže byť vyvolaný jednak blokádou parasympatickej inervácie slznej žľazy (v zmysle zníženia sekrécie), ale aj inhibičným vplyvom na svalovú pumpu a tým odtok sĺz blokádou kontrakcie m.orbicularis oculi v oblasti mihalníc a dysfunkciu meibomských žliaz [5] (v zmysle zvýšenej retencie sĺz). Niektorí autori udávajú zlepšené parametre slzného filmu po aplikácii BT-A [13]. Objektívnou a najdostupnejšou technikou na meranie produkcie a súčasne retencie sĺz je Schirmerov test. Meranie osmolarity sĺz sa postupne dostáva do klinickej medicíny, jeho hlavnou výhodou je najmä jednoduchosť vyšetrenia.
Materiál a metodika
Súbor tvorilo 27 pacientov (17 žien, 10 mužov, priemerný vek 63,4 roka) s esenciálnym blefarospazmom (46 očí 23 pacientov) a hemifaciálnym spazmom (4 oči 4 pacientov). Všetci pacienti podstúpili opakované podanie BT-A pre blefarospazmus v minulosti, nešlo o BT-A naivných pacientov. Pred aplikáciou BT-A bol u 62 % pacientov (n = 31) Schirmerov test pozitívny (< 10 mm za 5 minút).
U všetkých pacientov sme použili preparát BOTOX (Botox inj, Allergan, Irvine, USA) aplikovaný do 6 bodov do m. orbicularis oculi v dávke 16 až 18 U/oko, v riedení 20U/ml fyziologického roztoku. Použili sme doporučenú schému aplikačných bodov (obrázok 1).
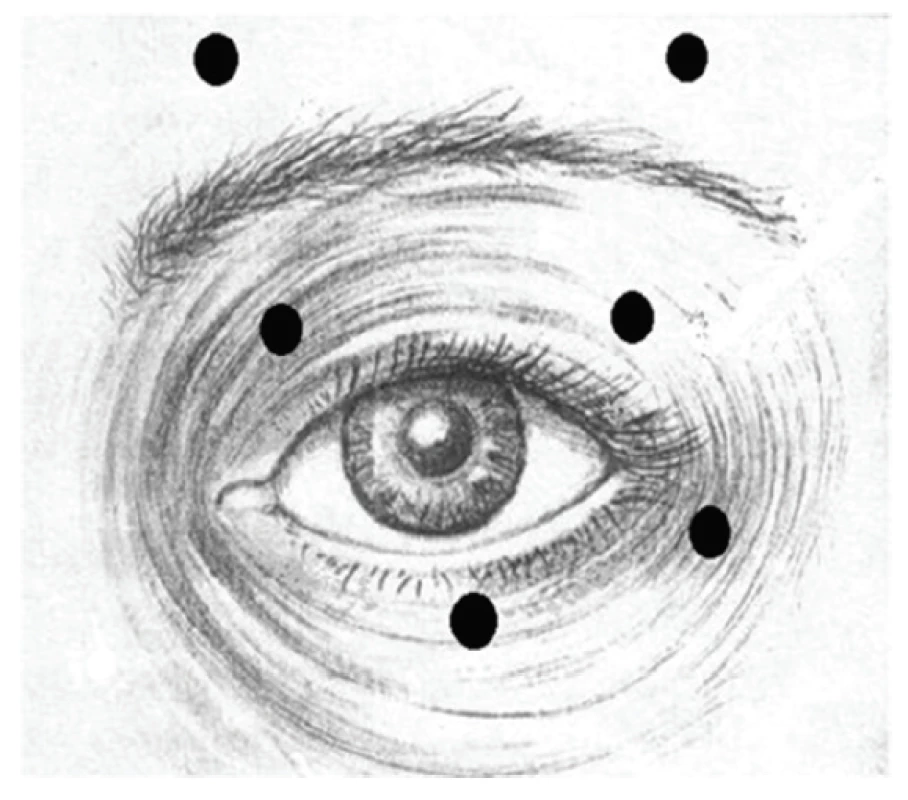
Schirmerovým testom (Schirmer I, trvanie 5 minút, bez použitia anestetických kvapiek) sme vyšetrili pacientov liečených BT-A v neurooftalmologických indikáciách. Schirmer I vyšetruje bazálnu i reflexnú produkciu sĺz. U časti pacientov (n=13) sme vyšetrili zmenu osmolarity (TearLab, USA) a ako doplňujúcu informáciu sme zmerali Schirmer II (n = 10).
Schirmerov test a vyšetrenie osmolarity sĺz sme vykonali bezprostredne pred aplikáciou BT-A (za neprítomnosti terapeutického efektu predchádzajúcej dávky) a 14 dní po aplikácií BT-A (kedy možno predpokladať maximálny terapeutický efekt) bez použitia anestetických kvapiek.
Na štatistickú analýzu, vzhľadom k negaussovej distribúcii hodnôt Schirmerovho testu, zistenej pomocou Shapiro-Wilkovho testu, sme rozdiel v tomto parametri pred a po aplikácii BT-A zisťovali pomocou neparametrického Wilcoxonovho testu. Na štatistickú analýzu osmolarity sĺz pred a po aplikácii BT-A sme použili Studentov T-test.
Výsledky
Celkové ani lokálne komplikácie po aplikácii BT-A sme nezaznamenali.
Priemerná hodnota Schirmerovho testu I pred aplikáciou BT-A bola 8,38 ± 0,63 mm (n = 50), z toho 31 očí (62 %) dosiahlo hodnotu menej ako 10 mm za 5 minút. Priemerná hodnota Schirmerovho testu po aplikácií BT-A bola 7,12 ± 0,6 mm (n = 50), z toho 39 očí (78 %) dosiahlo hodnotu menej ako 10 mm za 5 minút. Výsledky uvádzame v v tabuľke 1 a 2. Schirmer test II bol pred aplikácou 5,58 ± 0,98 mm (n = 10).
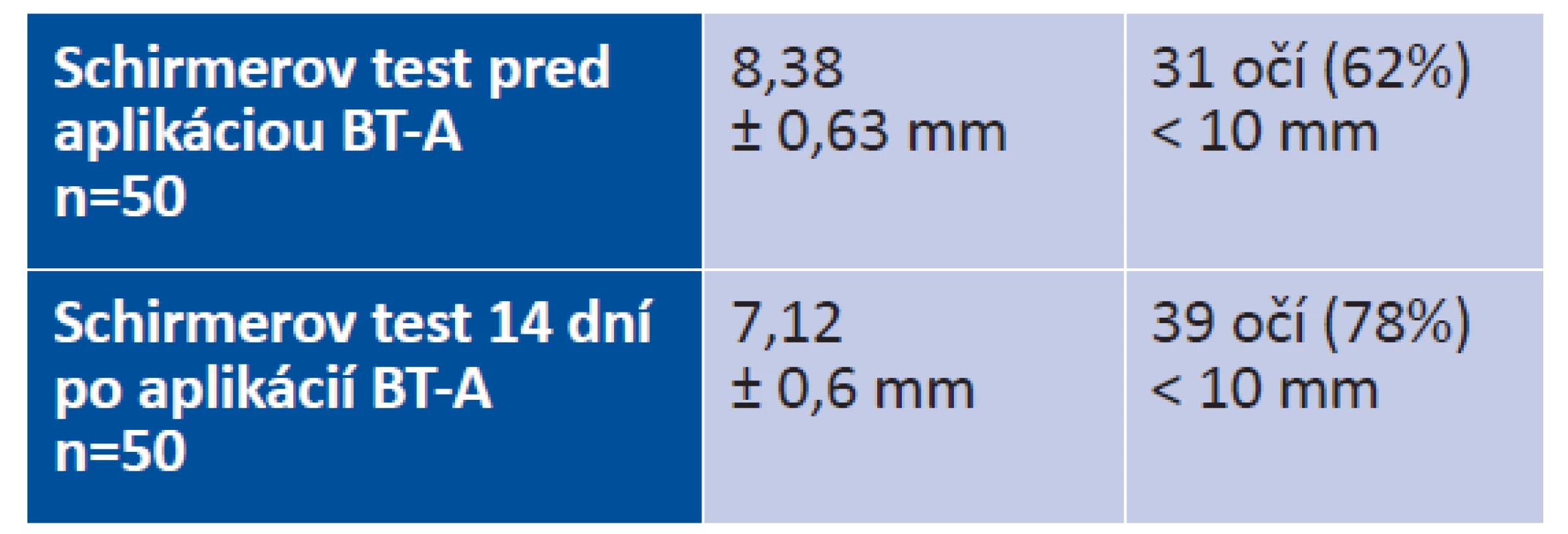
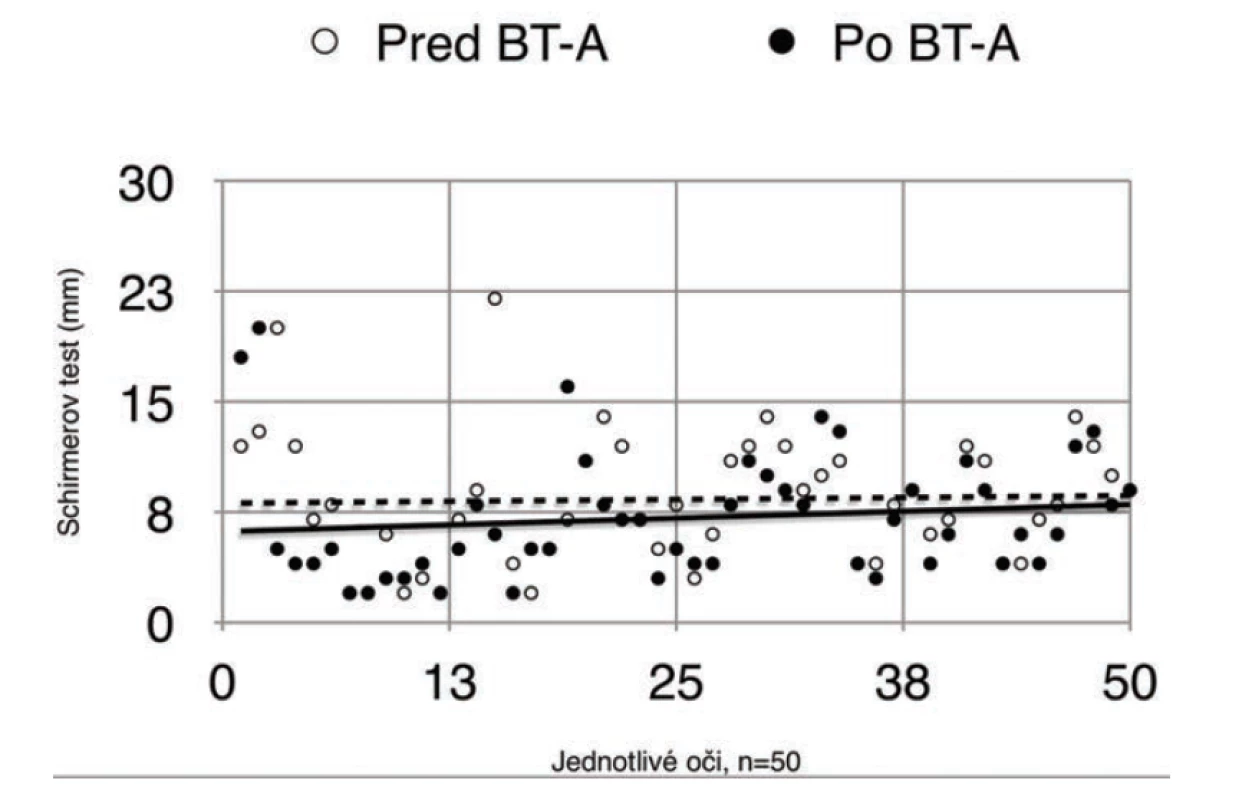
V priebehu liečby došlo k signifikantnému poklesu hodnoty Schirmerovho testu (p < 0,012, n = 50). U 29 pacientov (58 %) došlo k signifikantnému poklesu hodnoty sekrécie sĺz po podaní BT-A (p < 0,012). Zvýšenie retencie nastalo u 11 pacientov (22 %) a u 10 (20 %) pacientov nedošlo k zmene.
Pred podaním BT-A bola osmolarita sĺz 305,4 ± 9,2 mOsm (n = 13), 14 dní po podaní BT-A ostala osmolarita sĺz na úrovni 305,2 ± 8,6 mOsm (n = 13), p > 0,05.
Diskusia
Podstatou terapeutického účinku BT-A je blokáda nervovosvalových spojení presynaptickou blokádou uvoľňovania vezikúl obsahujúcich neurotransmiter acetylcholín. Účinkuje na SNA (synaptosomal-associated protein) a bolo zistené že štiepi proteíny potrebné pre vstup sekretorických vezikúl cez bunkovú membránu aj do acínov slznej žľazy [6,7]. Rovnaký mechanizmus je zodpovedný aj za reguláciu sekrécie potných žliaz, čo sa využíva aj v praxi [8,9]. Botulotoxín znižuje sekréciu sĺz pri priamej aplikácii do slznej žľazy [10,11]. Nie sú celkom jednoznačné názory na vplyv BT-A na retenciu sĺz v spojovkovom vaku, ale samotná aplikácia BT-A blízko horného a dolného slzného bodu môže zlepšiť prejavy suchého oka [17]. Dôvodom je možný vplyv BT-A na svalovú pumpu facilitujúcu odtok sĺz zo spojovkového vaku, čo bolo dokázané aj dacryoscintigrafiou [12]. Táto pumpa je tvorená anatomickým usporiadaním vlákien m.orbicularis oculi vo vzťahu k horizontálnym úsekom canaliculus lacrimalis a laterálnej stene slzného vaku. V obvykle používaných schémach aplikácie BT-A do oblasti m. orbicularis oculi sa do oblasti predpokladanej svalovej pumpy (vnútorná tretina dolnej mihalnice) BT-A neaplikuje, vplyv aplikovaného BT-A by mal byť preto minimálny. Napriek tomu nemožno vylúčiť difúziu BT-A z okolia. V našej práci sme pozorovali vplyv BT-A na výsledky Schirmerovho testu v zmysle jeho poklesu, čo je v súlade s literatúrou [13]. Schirmer I vyšetruje bazálnu i reflexnú produkciu sĺz, limitáciou našej práce je nerozlíšenie zmeny bazálnej a reflexnej slzivosti osobitne. Podľa výsledkov Schirmer II testu boli naši pacienti primárne zaťažení suchým okom.
Nezaznamenali sme rozdiel v osmolarite slzného filmu podobne ako iní autori [16], vyvetlením zrejme bude komplexnosť stavu a chronicky zmenená regulácia u suchého oka u pacientov s hemi - alebo blefarospazmom. Samotná denervácia slznej žľazy BT-A zrejme nestačí na zmenu osmolarity.
Rovnaký pokles bol pozorovaný po aplikácií BT-A pre korekciu vrások [14]. Možno preto predpokladať že prevláda inhibícia sekrécie slznej žľazy nad prípadnou zvýšenou retenciou spôsobenou difúziou BT-A do oblasti svalovej slznej pumpy, to platí pre klasický spôsob aplikácie BT-A s vynechaním nazálneho bodu aplikácie na dolnej mihalnici. Podobne ako v iných prácach [15] sme zistili u viac ako 60 % pacientov pred aplikáciou BT-A znížené hodnoty Schirmerovho testu pod 10 mm. Prevalencia suchého oka je v populácii 7,4 - 33,7 % [19], častejšie sa vyskytuje u žien a s vekom incidencia stúpa, presné údaje pre náš región nie sú dostupné. Funkciu slzného filmu zhoršujú opakované aplikácie BT-A [18] s rozvojom postupnej atrofizácie okolitého tkaniva [20].
Blefarospazmus a suché oko sú dve na sebe nezávislé choroby, ale môžu sa vyskytnúť súčasne. Hoci aplikácia BT-A zlepšuje prejavy blefarospazmu, neobnovuje normálne slzenie. Naopak môžeme po aplikácii pozorovať zhoršenie symptómov suchého oka. Pri liečbe pacientov, ktorí trpia blefarospazmom v kombinácii so suchým okom, by mala byť liečba suchého oka dlhodobá, najmä u pacientov po opakovaných aplikáciách.
Záver
Aplikácia BT-A v dávke 16-18 U/ 1 oko signifikantne znižuje sekréciu sĺz a tým aj výsledky Schirmerovho testu. U takmer 60 % pacientov s diagnózou esenciálny blefarospazmus a hemifaciálny spazmus je prítomné detekovateľné zníženie sekrécie sĺz aj pred aplikáciou BT-A. Používanie substitúcie sĺz u pacientov s EB a HS pred a najmä po aplikácii BT-A je vhodné pre odstránenie symptómov suchého oka a jej dlhodobá aplikácia má racionálny základ.
Autori práce prehlasujú, že vznik aj téma odborného článku a jeho zverejnenie nie sú v konflikte záujmov a nie sú podporené žiadnou farmaceutickou firmou.
Do redakce doručeno dne: 14. 6. 2018
Do tisku přijato dne: 10. 3. 2019
MUDr. Peter Žiak, Ph.D.
Očná klinika JLF UK a UNM
Kollárova ul.č. 2
036 59 Martin
Slovenská republika
E-mail: ocnesekr@unm.sk
Sources
1. Lu, R., Huang, R., Li, K., et al.: The influence of benign essential blepharospasm on dry eye disease and ocular inflammation. Amer J Ophthalmol, 157; 2014 : 591 – 597
2. Defazio, G., Abbruzzese, G., Aniella, MS., et al.: Eye symp - toms in relatives of patients with primary adult-onset dystonia. Movement Disord, 27; 2012 : 305–307.
3. Huang, XF., Wang, KY., Liang, ZH., et al.: Clinical analysis of patients with primary blepharospasm: A report of 100 cases in China. Euro Neurol, 73; 2015 : 337–341.
4. Ziak P.: [Results of long term treatment of essential blepharospasm and facial hemispasm with botulinum toxin A]. Cesk Slov Oftalmol, 60; 2004 : 37-44.
5. Call, CB., Wise, RJ., Hansen, MR., et al.: In vivo examination of meibomian gland morphology in patients with facial nerve palsy using infrared meibography. Ophthalm Plast Reconstruct Surg, 28(6); 2012 : 396–400.
6. Mense, S.: Neurobiological basis for the use of botulinum toxin in pain therapy. J Neuro, 251; 2004 : 11–17.
7. Wang, Y., Jerdeva, G., Yarber, FA., et al.: Cytoplasmic dynein participates in apically targeted stimulated secretory traffic in primary rabbit lacrimal acinar epithelial cells. J Cell Sci, 116; 2003 : 2051–2065.
8. Bushara, K., Park, D., Jones, J., et al.: Botulinum toxin-a possible new treatment for axillary hyperhidrosis. Clin Exp Dermatol, 21; 1996 : 276-278.
9. Naumann, M., Flachenecker, P., Bröcker, E., et al.: Botulinum toxin for palmar hyperhidrosis. The Lancet, 349; 1997 : 252.
10. Riemann, R., Pfennigsdorf, S., Riemann, E., et al.: Successful treatment of crocodile tears by injection of botulinum toxin into the lacrimal gland. Ophthalmology, 106; 999 : 2322-2324.
11. Suwan-Apichon, O., Rizen, M., Rangsing, R., et al.: Botulinum toxin B induced mouse model of keratokonjunctivitis sicca. Invest Ophthalmol Vis Sci, 47; 2006 : 133-139.
12. Park, D., Shin, H., Lee, S., et al.: Tear production and drainage after botulinum toxin A injection in patients with essential blepharospasm. Acta Ophthalmologica, 91; 2013: 108-112.
13. Gunes, A., Demirci, S., Koyuncuoglu, HR., et al.: Corneal and Tear Film Changes After Botulinum Toxin-A in Blepharospasm or Hemifacial Spasm. Cornea, 34; 2015 : 906 - 910.
14. Matarasso, S.: Decreased Tear Expression with an Abnormal Schirmerʼs Test Following Botulinum Toxin Type A for the Treatment of Lateral Canthal Rhytides. Dermatol Surg, 28; 2002: 149-152.
15. Price, J., O Day, J.: A Comparative Study of Tear Secretion in Blepharospasm and Hemifacial spasm Patients Treated with Botulinum Toxin. J Clin Neuro Opth, 13; 1993; 67-71.
16. Mali, YP., Schultze, RL., Wladis, EJ.: Evaluating the effects of Botulinum Toxin A on tear metrics in patients with hemifacial spasm. Orbit, 36; 2017 : 307-310.
17. Bukhari, AA.: Botulinum neurotoxin type A versus punctal plug insertion in the management of dry eye disease. Oman J Ophthalmol, 7; 2014 : 61-65.
18. Ainsworth, JR., Kraft, SP.: Long-term Changes in Duration of Relief with Botulinum Toxin Treatment of Essential Blepharospasm and Hemifacial Spasm. Ophthalmology, 102; 1995, 2036-2040.
19. Gayton, JL.: Etiology, prevalence, and treatment of dry eye disease. Clin Ophthalmol, 2009; 405-12.
20. Krasný, J., Šach, J.: Aplikace Dysportu – možnost doprovodného vedlejšího efektu na postavení víček (klinicko-histologická studie). Cesk Slov Oftalmol, 68; 2012 : 216-220.
Labels
OphthalmologyArticle was published in
Czech and Slovak Ophthalmology
2019 Issue 2
-
All articles in this issue
- Očná klinika Lekárskej fakulty Univerzity Komenského v Bratislave oslavuje 100-TÉ VÝROČIE činnosti – 1. časť
- Normotenzní versus hypertenzní glaukom – přehled
- Korekce myopie a myopického astigmatismu laserovou metodou laser in situ keratomileusis za asistence femtosekundového laseru – naše zkušenosti
- Vplyv aplikácie botulotoxínu A v neurooftalmologických indikáciách na výsledky Schirmerovho testu a osmolarity sĺz
- Periferní exsudatívní hemoragická chorioretinopatie
- Oboustranná jamka terče zrakového nervu s makulopatií – kazuistika
- Suprachoroideální hemoragie v pooperačním období antiglaukomového zákroku, kazuistika
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Normotenzní versus hypertenzní glaukom – přehled
- Oboustranná jamka terče zrakového nervu s makulopatií – kazuistika
- Suprachoroideální hemoragie v pooperačním období antiglaukomového zákroku, kazuistika
- Periferní exsudatívní hemoragická chorioretinopatie
