Risperdal Consta – dlouhodobě působící injekce v léčbě schizofrenie a schizoafektivní poruchy: předběžné 12měsíční výsledky projektu e-STAR v České a Slovenské republice
Risperdal Consta – Long-term Acting Injections in the Treatment of Schizophrenia and Schizoaffective Disorders: Preliminary 12-Month Results of the Project e-STAR in the Czech and Slovak Republics
E-STAR is an international, long-term, prospective, observational study of patients with schizophrenia and schizoaffective disorder switched to treatment with Risperidone Consta long acting injection (Consta). Data are collected both retrospectively for a period of 1 year and prospectively every 3 months up to 2 years. This interim analysis presents results of a group of 280 patients who have completed one-year prospective treatment with Risperdal Consta in the Czech and Slovak Republics. Long-acting risperidone reduced relapse rates and need for hospital services and increased the rate of symptomatic remission during the first year. Treatment with Consta injection was associated with improvement of activities of daily living and overall clinical global improvement. Moreover, Consta significantly reduced suicidal tendencies and violent behavior. The proportion of patients treated with combination of antipsychotics has decreased, compared with the retrospective one-year period. Long-acting risperidone has the potential to improve adherence to the antipsychotic treatment in patients suffering from schizophrenia and schizoaffective disorder. E-STAR project provides important information about the pharmacological treatment of schizophrenia and schizoaffective disorder in a usual clinical practice setting.
Key words:
schizophrenia, schizoaffective disorder, risperidone long acting injection, maintenance treatment, adherence.
Authors:
I. Tůma 1; J. Pečeňák 2; P. Mohr 3; E. Češková 4; M. Anders 5
Authors‘ workplace:
Psychiatrická klinika LF UK a FN, Hradec Králové
1; Psychiatrická klinika LF UK a FN, Bratislava
2; Psychiatrické centrum Praha a Psychiatrická klinika 3. LF UK, Praha
3; Psychiatrická klinika LF MU a FN, Brno
4; Psychiatrická klinika 1. LF UK a VFN, Praha
5
Published in:
Čes. a slov. Psychiat., 104, 2008, No. 2, pp. 59-67.
Category:
Original Article
Overview
E-STAR je mezinárodní dlouhodobá, observační studie zaměřená na pacienty, kteří jsou pro schizofrenii nebo schizoafektivní poruchu převedeni na léčbu Risperidonem Consta dlouhodobě působícími injekcemi (Consta). Data jsou získávána retrospektivně za období jednoho roku a prospektivně v tříměsíčních intervalech po dobu dvou let. Tato předběžná analýza reprezentuje výsledky skupiny 280 nemocných, kteří dokončili jednoroční prospektivní sledování léčby Constou v České a Slovenské republice. Jednoroční výsledky ukazují, že Consta redukovala počet relapsů a potřebu hospitalizace a zvýšila podíl nemocných v remisi. Léčba Constou byla spojena se zlepšením denních životních aktivit a zlepšeno bylo celkové klinické hodnocení nemocných, navíc vedla k významné redukci suicidálních tendencí a násilného jednání. Podíl nemocných léčených kombinacemi antipsychotik byl při léčbě Constou menší než v retrospektivním jednoročním období. Risperidon ve formě dlouhodobě působících injekcí zlepšuje adherenci nemocných schizofrenií a schizoafektivní poruchou k antipsychotické léčbě. Projekt e-STAR umožňuje hodnotit farmakologickou léčbu schizofrenie a schizoafektivní poruchy v prostředí běžné klinické praxe.
Klíčová slova:
schizofrenie, schizoafektivní porucha, risperidon dlouhodobě působící injekce, udržovací terapie, adherence.
ÚVOD
Antipsychotická terapievýznamně redukuje riziko relapsu schizofrenie [15]. Přesto nemocní relabují mnohem častěji než by odpovídalo efektivitě antipsychotické léčby. Jednou z příčin tohoto neuspokojivého výsledku dlouhodobé udržovací léčby schizofrenie a schizoafektivní poruchy je nedostatečná spolupráce nemocných při léčbě. Ta se projevuje nepravidelným užíváním ordinovaných léků nebo ukončením léčby proti radě lékaře. Nepravidelné užívání antipsychotik nebo jejich vysazení bývá častou příčinou relapsu onemocnění [28]. Psychotický relaps vede k narušení života nemocného a jeho rodiny, zhoršuje prognózu nemoci a může vést k rezistenci na další antipsychotickou léčbu [5, 14]. Problém s adherencí je pozorován u více než 35 % pacientů v prvních 6 týdnech léčby a po dvou letech jsou problémy s adherencí nalézány až u 74 % nemocných [9, 16].
Adherence k antipsychotické léčbě je z velké části negativně ovlivňována nedostatkem náhledu a kognitivním deficitem [6]. Adherenci také významně ovlivňuje snášenlivost antipsychotika. Zavedení antipsychotik druhé generace do klinické praxe vedlo k očekávání lepší adherence vzhledem k jejich příznivějšímu profilu nežádoucích účinků v porovnání s antipsychotiky první generace. Klinická praxe a cílená sledování adherence však přinesly zklamání. Ukázalo se, že orálně podávaná antipsychotika druhé generace nezaručují významně lepší adherenci než orální formy klasických antipsychotik první generace [14, 16]. Vysoká míra non-adherence je pozorována již v časných stadiích onemocnění schizofrenií, nezávisle na typu podávaného antipsychotika druhé generace [17].
S cílem zlepšit adherenci k léčbě byly v 60. letech dvacátého století vyvinuty depotní injekční formy antipsychotik. Jejich zavedení do praxe v léčbě schizofrenie vedlo ke snížení morbidity i mortality [13]. Parenterální podávání umožnilo používat menší dávky antipsychotik a snížilo jejich hepatotoxicitu. Výhodnou farmakologickou charakteristikou depotních forem antipsychotik je zabezpečení dostatečné biologické dostupnosti účinné látky při nepřítomnosti vlivu absorpčních výkyvů u prvního průchodu játry a menší interindividuální rozdíly plazmatických hladin při stejném dávkování [8].
Depotní injekční formy antipsychotik první generace byly omezeny jen na molekuly, které bylo možno esterifikovat a umožnit tak jejich vazbu na olejovou bázi. Významnou výhodou depotních injekčních forem antipsychotik je snadná kontrola adherence, použití depotních antipsychotik první generace zvyšuje adherenci o 10 %-40 % [21]. Nina Schooler [22] srovnávala výsledky šesti randomizovaných klinických studií s orálními a depotními antipsychotiky. Zjistila, že ve skupině nemocných léčených orálními antipsychotiky došlo v průběhu prvního roku k relapsům ve 42 %. Ve skupině s depotní injekční léčbou relabovalo jen 27 % pacientů. Systematickou meta-analýzu s použitím dat z Cochrane databáze publikovali Adams a spol. [2]. Meta-analýza prokazovala, že depotní antipsychotika zlepšují sociální schopnosti nemocných významně více než orální antipsychotika. V nedávno publikované observační studii pacientů s první epizodou schizofrenie byl v prevenci dalšího relapsu ze všech antipsychotik, klasických i atypických, nejúčinnější jediný zástupce depotních antipsychotik, depotní perfenazin [26].
Přes prokázaný potenciál k redukci relapsů nebyly a nejsou depotní injekční formy antipsychotik první generace užívány tak často, jak by se dalo očekávat. Důvodů je několik. Mezi nejčastější patří nadhodnocení adherence orální léčby ze strany lékaře, dále obava lékaře, že v případě nesnášenlivosti není možno s podanou dávkou dlouhodobě působícího léku manipulovat a také stereotyp podávání depotních antipsychotik u refrakterních, obtížně léčitelných nemocných. Obávané riziko vzniku nežádoucích účinků, zvláště motorických, je podobné jako při orálním podávání stejného farmaka [2]. Někdy se lékaři i pacienti obávají, že přechod mezi orálním podáním antipsychotika a depotní formou může být obtížný. Rozhodování lékařů ovlivňuje obava, jak bude pacientem depotní forma přijímána. Výzkumy však ukázaly, že mnozí nemocní preferují depotní parenterální formu před denním orálním užíváním antipsychotika [12, 27].
Risperidon je prvním antipsychotikem druhé generace, které je možno podávat ve formě mikrosfér jako dlouhodobě působící injekce. Inovativní farmaceutická forma umožňuje pomalé uvolňování aktivní látky ze svalového depozita, zajišťuje terapeutickou plazmatickou hladinu po dobu dvou týdnů (po ustálení hladiny farmaka v plazmě) a výrazně snižuje bolestivost při podání injekce. Podrobnou farmakologickou charakteristiku dlouhodobě působících injekcí risperidonu podává ve svém článku Švestka [25].
METODIKA
Projekt e-STAR (electronic – Schizophrenia Treatment Adherence Registry) je mezinárodní postmarketingovou studií adherence k léčbě Risperdalem Consta - injekčním risperidonem s dlouhodobým účinkem (dále jen Consta). Studie e-STAR probíhá jako sledování v běžných klinických podmínkách. Do sledování jsou zařazováni nemocní trpící schizofrenií nebo schizoafektivní poruchou, muži a ženy starší 18 let. Vstup nemocných do sledování nebyl určován žádnými vstupními kritérii, pouze nebyly zařazovány těhotné a kojící ženy nebo ženy plánující těhotenství. O převedení nemocného na Constu rozhoduje výhradně ošetřující lékař. Současné podávání jiných farmak není omezováno. Data nemocných jsou v anonymní formě ukládána ošetřujícím lékařem do elektronické databáze. Anonymita je zajištěna procesem dvojího kódování.
Cílem studie je prospektivně zhodnotit postupy při léčbě schizofrenie se zaměřením na klinický účinek a výsledky dlouhodobé léčby Constou v naturalistickém uspořádání. Získaná retrospektivní data umožní porovnat výsledky léčby Risperdalem Consta s předchozí antipsychotickou léčbou.
Ve studii e-STAR je hodnocena adherence k léčbě Constou (setrvání v léčbě). Získávány jsou informace o důvodech převedení nemocných na Constu, o použitém dávkování Consty v běžné klinické praxi, o kombinacích Consty s jinými antipsychotiky a dalšími psychofarmaky. Zrcadlovým srovnáním retrospektivních a prospektivních údajů je hodnocena potřeba hospitalizace za stejná časová období. Účinnost je prospektivně hodnocena v tříměsíčních intervalech na škále CGI-S (Clinical Global Impression) [10], škálou Global Assessment of Functioning (GAF scale) [1] a dosažením remise, definované podle Andreasena a spol. [3]. Při podávání Consty je dále sledován výskyt autoagresivního jednání (suicidální tendence, sebepoškozování) a heteroagresivního jednání. Snášenlivost je hodnocena nestrukturovaným záznamem nežádoucích účinků.
Pro statistické srovnání kategorických proměnných byl použit McNemarův test a pro hodnocení kontinuálních proměnných byl použit T-test.
VÝSLEDKY
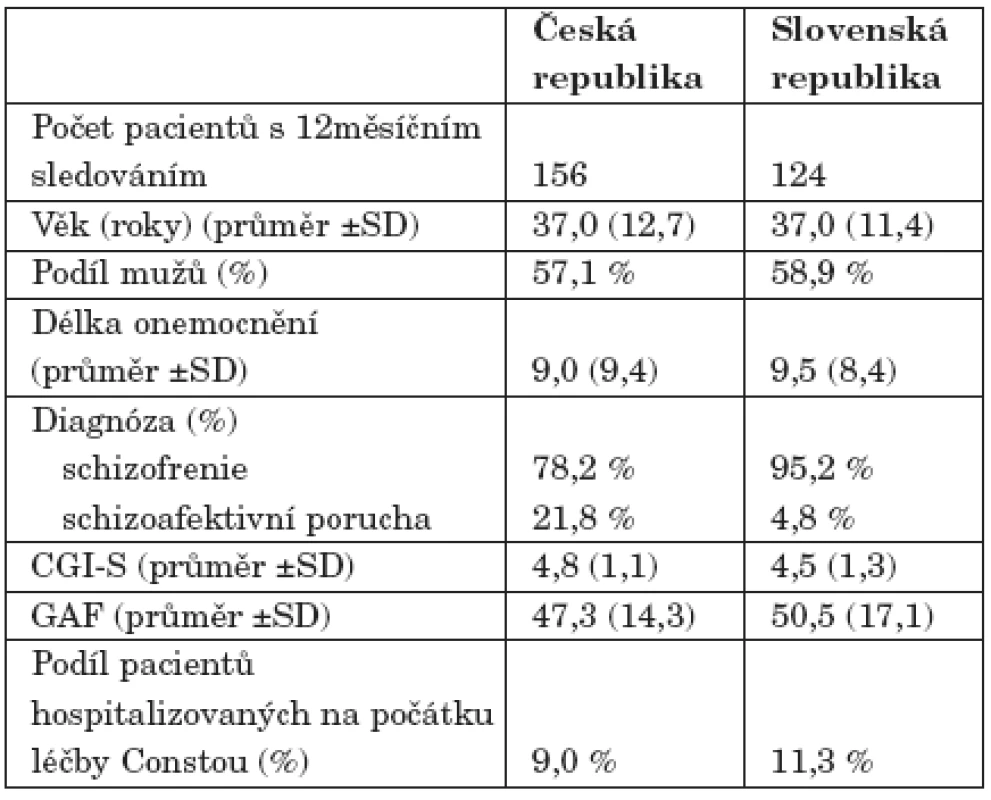
Celkem bylo do studie e-STAR v České republice (ČR) a ve Slovenské republice (SR) zařazeno 1262 nemocných s diagnózou schizofrenie nebo schizoafektivní poruchy. Průběžné výsledky, které jsou obsahem tohoto článku, jsou zpracovány pro skupinu 280 nemocných, kteří k datu 30. 5. 2007 byli ve studii nejméně 12 měsíců (tab. 1). Ve vstupních kritériích byly oba národní soubory srovnatelné až na relativně vyšší podíl nemocných léčených pro schizoafektivní poruchu v českém souboru. Všechna prozatímní hodnocení jsou vztažena k 12 měsícům léčby Constou.
Nejčastějším důvodem převedení na Constu byla nedostatečná adherence nemocných k předchozí antipsychotické léčbě (40,4 % v ČR; 46,8 % v SR). Druhým nejčastějším důvodem byl nedostatečný klinický účinek předchozí léčby (35,3 % v ČR; 26,6 % v SR) (graf 1).

Adherence byla ve sledovaném souboru vysoká a umožnila vysokou míru udržení nemocných na léčbě Constou po dobu 12 měsíců (retence 95% v ČR a 98% v SR) (graf 2). Pouze u 10 nemocných byla v průběhu 12 měsíců léčba Constou ukončena. Průměrná doba do přerušení léčby byla 221,9 dní (+/ - 58,6 dní). Nejčastějším důvodem ukončení podávání Consty byl nedostatečný efekt (N=5). Nespolupráce (rozhodnutí pacienta přerušit léčbu) byla příčinou přerušení léčby u čtyř nemocných. Nežádoucí účinky byly důvodem vysazení Risperdalu Consta pouze u jednoho nemocného.

Dávkování Consty použité ve sledované skupině bylo u většiny nemocných 25 mg na počátku sledování i ve 12. měsíci v obou národních souborech. Vývoj dávkování v průběhu 12měsíčního sledování byl poněkud odlišný v obou zemích. Ve slovenském souboru bylo více nemocných postupně převáděno na vyšší dávkování (graf 3, graf 4).


Podíl nemocných hospitalizovaných při jednoroční léčbě Constou statisticky významně poklesl v porovnání se stejným obdobím před nasazením Consty (graf 5). V období 12 měsíců před nasazením Consty bylo hospitalizování celkem 73 nemocných (46,8 %) sledovaného souboru. Po nasazení Consty bylo po dobu 12 měsíců hospitalizováno 27 nemocných (17,3 %) (p<0,001, McNemarův test).

V zrcadlovém 12měsíčním srovnání došlo při léčbě Constou ke statisticky významné (p<0,001) redukci počtu hospitalizací na jednoho pacienta (z 0,6 na 0,23 v ČR; z 0,71 na 0,22 v SR) a rovněž ke statisticky významné (p<0,001) redukci počtu dní hospitalizace na jednoho pacienta (z 32,1 na 8,4 v ČR; z 26,5 na 6,9 v SR). V průběhu jednoročního sledování bylo rehospitalizováno 11 nemocných. Průměrná doba do nové hospitalizace byla v této podskupině nemocných 144,2 dní (+/ - 98,5 dní).
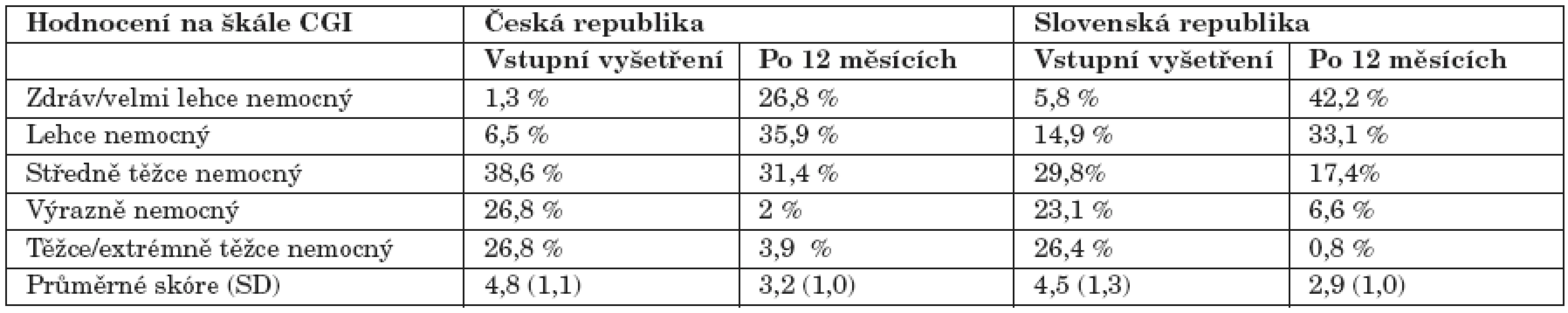
Sledování klinického stavu škálou CGI ukázalo ve dvanáctém měsíci léčby Constou statisticky významné zlepšení (p<0,001, párový T-test) v porovnání se stavem před zahájením podávání Consty. Na počátku sledování před zahájením léčby Constou byla většina nemocných v obou národních souborech klasifikována v rozmezí „středně těžce – těžce nemocný“. Po 12 měsících léčby se klasifikace posunula do rozmezí „velmi lehce – středně těžce nemocný“ (tab. 2).
V průběhu dvanáctiměsíční léčby Constou byl snižován počet nemocných, kterým byla Consta podávána v kombinaci s jinými antipsychotiky. Při nasazení Consty bylo v obou národních souborech celkem 173 nemocným (61,8 %) podáváno další antipsychotikum druhé generace. Na konci ročního sledování dostávalo takovou kombinaci pouze 49 pacientů (17,5 %). Orální antipsychotika první generace byla na počátku sledování kombinována s Constou u 15,4 %, po roce pouze ve 2,9 %. Depotní antipsychotika první generace byla zpočátku podávána v kombinaci s Constou u 24 nemocných (8,6 %), na konci prvního roku byl touto kombinací léčen jen jeden nemocný (0,4 %).
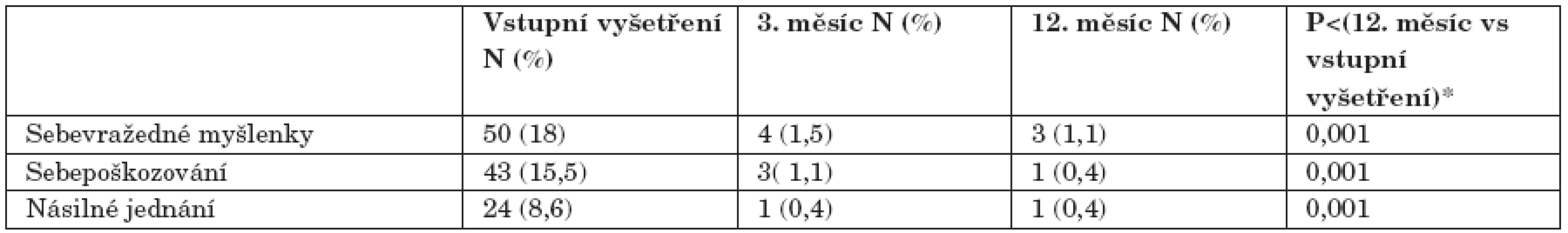
V celém hodnoceném souboru (ČR+SR; N=278, u dvou nemocných schází data) byl zaznamenán statisticky významný pokles frekvence výskytu sebevražedných myšlenek, sebepoškozování a násilného jednání již ve třetím měsíci léčby Constou a při všech dalších kontrolních vyšetřeních v porovnání se vstupním vyšetřením (tab. 3).
V průběhu 12měsíční léčby Constou se statisticky významně zlepšily sociální schopnosti v obou národních souborech. Průměrné skóre na škále GAF se zvýšilo o 22 bodů (směrodatná odchylka 18,8). Nemocní v obou souborech byli na počátku sledování hodnoceni jako „závažně postižení“ s průměrnou hodnotou 48,7 (SD=15,6). Po jednom roce léčby bylo průměrné skóre na škále GAF na úrovni „mírného postižení“ při průměrné hodnotě 69,7 (SD=14,7). Vzestup průměrného skóre byl statisticky významný na hladině významnosti p<0,001 (párový T-test).
Podíl nemocných, kteří splňovali kritéria pro remisi [3], se od 6. do 12. měsíce sledování zvýšil o 19,4 % (1,2 % v šestém měsíci; 20,6 % ve dvanáctém měsíci).
DISKUSE
Observační postmarketingová sledování vyplňují mezeru v klinickém poznání mezi kontrolovanými dvojitě slepými studiemi a individuální klinickou zkušeností. Kontrolované studie jsou nenahraditelným nástrojem k ověřování klinické účinnosti v porovnání s placebem nebo léky stejné lékové skupiny. Svým uspořádáním omezují vliv subjektivní předpojatosti jak ze strany nemocných, kteří se klinické studie účastní, tak ze strany hodnotícího výzkumníka. Nevýhodou kontrolovaných studií je často velmi úzce definovaný zkoumaný soubor. Výběr testovaných subjektů je zúžen již na samém počátku vstupními a vyřazovacími kritérii, do studie zpravidla nemohou vstoupit pacienti příliš mladí nebo naopak staří, nemocní s dalšími komorbidními somatickými chorobami, kteří současně užívají návykové látky, kteří jsou hodně a nebo naopak málo nemocní, kteří jsou potenciálně agresivní, suicidální, ženy, které mohou otěhotnět. Přitom všichni tito pacienti, které jsme a priori vyloučili z testování, tvoří naši klinickou populaci. Naše znalosti o efektivitě a bezpečnosti léčby v populaci a podmínkách, které se nejvíce blíží skutečným klinickým podmínkám, mohou rozšířit naturalistické observační studie, někdy nazývané také pragmatické. Observační studie se zpravidla týkají širšího spektra pacientů, vstupní kritéria jsou mnohem volnější, sledovaný soubor má větší velikost, nejsou tolik limitovány délkou trvání, používají přirozená kritéria hodnocení účinnosti. V konečném výsledku je jejich externí validita, přenosnost výsledků do jiných podmínek mnohem větší a stávají se tak komplementárním doplňkem kontrolovaných randomizovaných studií.
Příkladem takovéto pragmatické studie je studie e-STAR, prospektivní observační sledování účinnosti Risperdalu Consta inj. v České a Slovenské republice. Předběžné výsledky po prvním roce léčby ukazují, že tato forma léčby nemocných trpících schizofrenií nebo schizoafektivní poruchou přináší klinické i sociální zlepšení s vysokou mírou retence (pouze 10 z 280 nemocných nedokončilo roční léčbu). Zrcadlové srovnání prokázalo, že léčba Constou významně snižuje potřebu hospitalizace. Klinické zlepšení bylo v obou národních skupinách doprovázeno výraznou redukcí autoagresivního a heteroagresivního jednání. Dobrého klinického výsledku léčby bylo dosaženo u více než poloviny nemocných při použití nejnižšího dávkování Consty. Na konci jednoročního sledování bylo v českém souboru léčeno Constou v dávce 25 mg 62 % nemocných, ve slovenském souboru 50 % nemocných. Přestože byl počet pacientů léčených kombinací antipsychotik v prospektivním období menší než v jednoročním období před převedením na Constu, byla část nemocných kombinacemi antipsychotik léčena (v 18 % na konci jednoročního sledování).
Retence je v obou národních souborech velmi vysoká. V českém souboru zůstává v léčbě 95 % nemocných, ve slovenském souboru dokonce 98 %. Vysoká míra retence v našich národních souborech je srovnatelná s předběžnými mezinárodními analýzami projektu e-STAR. Olivares a spolupracovníci publikovali na 10. evropském kongresu ISPRO (International Society for Pharmacoeconomics and Outcomes Research) v Dublinu předběžné výsledky, hodnotící skupinu 1874 pacientů zařazených do registru e-STAR v několika evropských zemích (Španělsko, Belgie, Česká republika, Slovenská republika, Holandsko a Švédsko). Jednoroční retence v tomto souboru byla 89,6% [18]. Ve španělském souboru e-STAR (N=1345) byla popsána retence po dvou letech léčby Constou ve výši 81,8 % [19].
Retence v otevřených studiích je také vyšší než ve dvojitě slepých kontrolovaných studiích, kde podmínky studie zpravidla nedovolují podávat nemocným jiné antipsychotikum než risperidon v monoterapii při fixním dávkování a nemocní byli při relapsu ze studie vyřazováni. Simpson a spolupracovníci pozorovali retenci v jednoroční dvojitě slepé studii (N=324) porovnávající dvě dávky Consty (25 mg a 50 mg) v rozmezí 50 % - 52 % [24].
Ve dvanáctitýdenní dvojitě slepé paralelní, placebem kontrolované studii [13], do které bylo zařazeno 400 nemocných se schizofrenií, byl podíl nemocných, kteří předčasně ukončili léčbu Constou, vysoký (68% v placebové skupině a 51 % až 52 % ve skupinách s různým dávkováním Consty). Nonadherence jako příčina předčasného ukončení léčby byla pozorována v10 %-20 %. Nejčastější další příčinou přerušení léčby byl nedostatečný efekt (12%-22%) a nežádoucí účinky (11%-14%). Ve dvacetitýdenní studii [11] byly srovnávány obě formy risperidonu, orální forma a dlouhodobě působící injekční forma. Po prvních 8 týdnech orální léčby bylo 640 nemocných randomizováno k jedné ze sledovaných forem a za dvojitě slepých podmínek léčeno 12 týdnů. Pro nežádoucí účinky léčbu nedokončilo 5 %-6 % nemocných. Podobný podíl nemocných nedokončil léčbu z důvodu nedostatečné účinnosti (4 %-5 %). Zajímavým výsledkem bylo pozorování poklesu hladiny prolaktinu v rozmezí od 10 % do 19 % ve skupině nemocných léčených injekční formou. V projektu e-STAR nejsou hladiny prolaktinu sledovány.
Lepší adherence a účinnost v našich souborech v projektu e-STAR byla pravděpodobně spojena s relativně mírnějším klinickým stavem při převedení na Constu. Téměř 50 % nemocných ve studii Kanea a spolupracovníků [13] vstupovalo do studie v době, kdy byli hospitalizováni. V našich souborech bylo na počátku sledování hospitalizováno pouze 10 % nemocných. Navíc účinnost a adherence je v našem souboru posilována kombinovanou antipsychotickou terapií, která není v projektu e-STAR nijak omezována, rovněž při relapsu nebyla obvykle léčba Constou ukončována.
S projektem e-STAR je nejlépe srovnatelná třetí velká klinická studie, která probíhala v otevřeném uspořádání a sledovala jednoroční účinnost léčby Constou při flexibilním dávkování [7]. Alespoň jedna injekce Consty byla podána 615 symptomaticky stabilním pacientům se schizofrenií nebo schizoafektivní poruchou. Jednoroční léčbu dokončilo 65 % pacientů. Více než 20% zlepšení celkového skóre škály PANSS bylo pozorováno u 49 % nemocných, kteří byli převedeni na Constu z předchozí antipsychotické léčby (z toho 233 pacientů bylo v předchozím období léčeno depotními antipsychotiky první generace). Účinnost nižších dávek Consty (25 mg nebo 50 mg) byla větší než dávky 75 mg. Obdobně v české části studie e-STAR zůstává na konci jednoročního sledování nadpoloviční většina nemocných léčena nejnižší dávkou Consty (25 mg).
Naše studie má metodologická omezení. Protože část dat byla sbírána retrospektivně, validita těchto dat byla závislá na kvalitě záznamů ve zdravotní dokumentaci. Druhým problémem zrcadlového uspořádání je srovnávání hospitalizací u těch nemocných, u kterých byla léčba Constou zahájena během hospitalizace (9 % v českém souboru a 11 % ve slovenském). Důvodem těchto hospitalizací byla selhání předchozí antipsychotické léčby, přesto byly dny hospitalizace po nasazení Consty započítávány do prospektivního období, což mírně znevýhodňuje léčbu Constou. I přes toto znevýhodnění se délka hospitalizace v prospektivním období statisticky významně, oproti retrospektivnímu období, zkrátila.
Přestože je v současné době k dispozici široká škála antipsychotik s různými farmakodynamickými vlastnostmi, zůstává nevyřešen problém non-adherence. Při prokazatelně dobré účinnosti antipsychotik první i druhé generace je non-adherence největší překážkou využití terapeutického potenciálu antipsychotických léků. Zatím nejúspěšnější cestou překonávání této bariéry je používání parenterálních depotních, dlouhodobě působících forem antipsychotik. Vedle dalších očekávaných depotních forem antipsychotik druhé generace (olanzapin, paliperidon) jsou ve fázi preklinického testování depotní antipsychotické implantáty (haloperidol, risperidon), u nichž se předpokládá udržení plazmatické hladiny a klinické účinnosti po dobu několika měsíců [20, 23].
ZÁVĚR
Předběžné jednoroční hodnocení výsledků projektu e-STAR prokázalo v obou národních skupinách, že převedení nemocných se schizofrenií nebo schizoafektivní poruchou na Risperidon Consta, dlouhodobě působící injekce, významně zvýšilo adherenci k léčbě. V porovnání se stavem na počátku léčby Constou vedla léčba v průběhu dvanácti měsíců ke zvýšení podílu pacientů v remisi o 19 %. S klinickým zlepšením korespondovalo zlepšení sociálních schopností nemocných a také redukce suicidálních tendencí, sebepoškozování a násilného jednání. Léčba Constou umožnila redukovat antipsychotickou polyfarmakoterapii. V zrcadlovém srovnání s jednoročním retrospektivním obdobím byla při léčbě Constou výrazně redukována potřeba hospitalizace. Protože nejčastější příčinou hospitalizace je relaps onemocnění, je možno označit výsledek jednoroční léčby jako velmi příznivý ve smyslu ochrany pacientů před dalšími relapsy choroby.
Prohlášení o smluvních vztazích
Autoři článku jsou konzultanty firmy Janssen-Cilag pro projekt e-STAR
Projekt e-STAR je organizačně i finančně zajišťován firmou Janssen-Cilag.
Poděkování
Autoři děkují za spolupráci všem lékařům v České a Slovenské republice, kteří se projektu e-STAR zúčastnili.
Prim. MUDr. Ivan Tůma, CSc.
Psychiatrická klinika LF UK a FN
Sokolská 581
500 05 Hradec Králové
Sources
1. American Psychiatric Association: Diagnostic and Statistical Manual. Fourth Edition. Washington DC, American Psychiatric Assoc., 1994, p. 32.
2. Adams, C. E., Fenton, M. K. P., Auraishi, S., David, A. S.: Systematic meta-review of depot antipsychotic drugs for people with schizophrenia. Br. J. Psychiatry, 179, 2001, pp. 290-299.
3. Andreasen, N. C., Carpenter, W. T. Jr., Kane, J. M., Lasser, R. A., Marder, S. R., Weinberger, D. R.: Remission in schizophrenia: proposed criteria and rationale for consensus. Am. J. Psychiatry, 162, 2005, pp. 441-449.
4. Adams, C E, Fenton, M. K., Quraishi, S., David, A. S.: Systematic meta-review of depot antipsychotic drugs for people with schizophrenia. Br. J. Psychiatry, 179, 2001, pp. 290-299.
5. Češková, E.: Nové trendy v léčbě schizofrenie. Psychiat. pro praxi, 9, 2008, s. 40-43.
6. Češková, E., Přikryl, R., Kašpárek, T., Kučerová, H.: Nedostatek náhledu a nonkompliance a jejich vzájemný vztah u schizofrenie. Čes. a slov. Psychiat., 103, 2007, s. 336-340.
7. Fleischhacker, W. W., Eerdekens, M., Karcher, K., Remington, G., Llorca, P. M., Chrzanowski, W., Martin, S., Gefvert, O.: Treatment of schizophrenia with long-acting injectable risperidone: a 12-month open-label trial of the first long-acting second-generation antipsychotic. J. Clin. Psychiatry, 64, 2003, pp. 1250-1257.
8. Gerlach, J.: Depot neuroleptik in relace preventiv: advantages and disadvantages. Int.Clin. Psychopharmacol., 9, 1995 (Suppl. 5), pp. 17-20.
9. Gilmer, T. P., Dolder, C. R., Lacro, J. P., Folsom, D. P., Lindamer, L., Garcia, P., Jeste, D. V.: Adherence to treatment with antipsychotic medication and health care costs among Medicaid beneficiaries with schizophrenia. Am. J. Psychiatry, 161, 2004, pp. 692-699.
10. Guy, W.: Clinical global Impression. ECDEU assessment manual for psychopharmacology. Rockville (MD): U.S. Department of Health and Human Services, 1976.
11. Chue, P., Eerdekens, M., Augustyns, I., Lachaux, B., Molcan, P., Eriksson, L., Pretorius, H., David, A. S.: Comparative efficacy and safety of long-acting risperidone and risperidone oral tablets. Eur. Neuropsychopharmacol., 15, 2005, pp. 111-117.
12. Kane, J. M.: Strategies for improving compliance in treatment of schizophrenia by using a long-acting formulation of an antipsychotik: clinical studies. J. Clin. Psychiatry, 64, 2003 (Suppl. 16), pp. 34-40.
13. Kane, J. M., Eerdekens, M., Lindenmayer, J. P., Keith, S. J., Lesem, M., Karcher, K.: Long-acting injectable risperidone: efficacy and safety of the first long-acting atypical antipsychotic. Am. J., Psychiatry, 160, 2003, pp. 1125-1132.
14. Kane, J. M.: Review of treatments that can ameliorate nonadherence in patients with schizophrenia. J. Clin. Psychiatry, 67, 2006 (Suppl. 5), pp. 9-14.
15. Kissling, W.: Compliance, quality assurance and standards for relapse prevention in schizophrenia. Acta Psychiat. Scand., 89, 1994( Suppl.), pp. 16-24.
16. Lieberman, J. A., Stroup, T. S., McEvoy, J. P., Swartz, M. S., Rosenheck, R. A., Perkins, D. O., Keefe, R. S., Davis, S. M., Davis, C. E., Lebowitz, B. D., Severe, J., Hsiao, J. K.: Effectiveness of antipsychotic drugs in patients with chronic schizophrenia. N. Engl. J. Med., 353, 2005, pp. 1209-1223.
17. McEvoy, J. P., Lieberman, J. A., Perkins, D. O., Hamer, R. M., Gu, H., Lazarus, A., Sweitzer, D., Olexy, C., Weiden, P., Strakowski, S. D.: Efficacy and tolerability of olanzapine, quetiapine, and risperidone in the treatment of early psychosis: a randomized, double-blind 52-week comparison. Am. J. Psychiatry, 164, 2007, pp. 1050-1060.
18. Olivares, J. M., Peuskens, J., Pecenak, J., Tuma, I., van Koten, M., Eriksson, L., Povey, M., Lam, A., Zhao, Z. on behalf of the e-STAR study group: Treatment retention with Risperidone Long Acting Injection (RLAI) in European patients with schizophrenia: 12-month interim results from the electronic schizophrenia treatment adherence registry (e-STAR). 10th European Congress, Dublin, Ireland, 20-23 October 2007.
19. Olivares, J. M., Rodriguez-Morales, A., Diels, J., Lam, A., Zhao, Z. on behalf of the e-STAR study group: 24 months treatment discontinuation rates in patients with schizophrenia treated with Risperidone Long Acting Injection (RLAI) versus oral antipsychotics: results from the electronic schizophrenia treatment adherence registry (e-STAR) in Spain. 10th European Congress, Dublin, Ireland, 20-23 October 2007.
20. Rabin, C., Liang, Y., Ehrlichman, R. S., Budhian, A., Metzger, K. L., Majewski-Tiedeken, C., Winey, K. I., Siegel, S. J.: In vitro and in vivo demonstration of risperidone implants in mice. Schizophrenia Res., 98, 2008, pp. 66-78.
21. Remington, G. J., Adams, M. E.: Depot neuroleptic therapy: clinical considerations. Can. J. Psychiatry, 40, 1995, pp. S5-S11.
22. Schooler, N. R.: Relapse and rehospitalization: comparing oral and depot antipsychotics. J. Clin. Psychiatry, 64 (Suppl. 16), 2003, pp. 14-17.
23. Siegel, S. J., Winey, K. I., Gur, R. E., Lenox, R. H., Bilker, W. B., Ikeda, D., Gandhi, N., Zhang, W. X.: Surgical implantable long-term antipsychotic delivery system for the treatment of schizophrenia. Neuropsychopharmacology, 26, 2002, pp. 817-823.
24. Simpson, G. M., Mahmoud, R. A., Lasser, R. A., Kujawa, M., Bossie, C. A., Turkoz, I., Rodriguez, S., Gharabawi, M.: A 1-year double-blind study of 2 doses of long-acting risperidone in stable patients with schizophrenia or schizoaffective disorder. J. Clin. Psychiatry, 67, 2006, pp. 1194-1203.
25. Švestka, J.: Prvé antipsychotikum 2. generace v depotní formě: risperidon mikrosféry v intramuskulárních injekcích. Psychiatrie, 6, 2002, s. 261-267.
26. Tiihonen, J., Walhbeck, K., Lönnqvist, J., Klaukka, T., Ioannidis, J. P., Volavka, J., Haukka, J.: Effectiveness of antipsychotic treatments in a nationwide cohort of patients in community care after first hospitalization due to schizophrenia and schizoaffective disorder: observational follow-up study. BMJ, 333, 2006, pp. 224-229.
27. Walburn, J., Gray, R., Gournay, K., Quraishi, S., David, A. S.: Systematic review of patient and nurse attitudes to depot antipsychotic medication. Br. J. Psychiatry, 179, 2001, pp. 300-307.
28. Weiden, P. J., Kozma, C., Grogg, A., Locklear, J.: Partial compliance and risk of rehospitalization among California Medicaid patients with schizophrenia. Psychiatr. Serv., 55, 2004, pp. 886-891.
Labels
Addictology Paediatric psychiatry PsychiatryArticle was published in
Czech and Slovak Psychiatry

2008 Issue 2
- Memantine Eases Daily Life for Patients and Caregivers
- Memantine in Dementia Therapy – Current Findings and Possible Future Applications
- Hope Awakens with Early Diagnosis of Parkinson's Disease Based on Skin Odor
- Deep stimulation of the globus pallidus improved clinical symptoms in a patient with refractory parkinsonism and genetic mutation
Most read in this issue
- Risperdal Consta – dlouhodobě působící injekce v léčbě schizofrenie a schizoafektivní poruchy: předběžné 12měsíční výsledky projektu e-STAR v České a Slovenské republice
- Výsledky podrobného sledování použití omezovacích prostředků během hospitalizace – projekt EUNOMIA, výsledky v ČR
