Současný stav problematiky sexuálně přenosných onemocnění
State of the Art in Sexually Transmitted Diseases
Coordinated intervention against spread of STD is getting more important considering a marked increase of HIV infection incidence in the Czech Republic in the year 2007 and epidemiologic synergy of HIV and STD. Intervention against STD also prevents HIV transmission. Article summarizes epidemiology, classification, transmission risk and prevention of STD with special interest in chlamydial infections.
Key words:
STD-risk groups – transmission risk – Chlamydia trachomatis
:
I. Kuklová; M. Kojanová; P. Velčevský
:
Dermatovenerologická klinika 1. LF UK a VFN, Praha
přednosta prof. MUDr. Jiří Štork, CSc.
:
Čes-slov Derm, 83, 2008, No. 3, p. 115-121
:
Reviews (Continuing Medical Education)
V souvislosti s výraznějším nárůstem počtu nově zjištěných HIV infekcí v České republice v průběhu roku 2007 a vzhledem k epidemiologické synergii HIV a STD nabývá na významu koordinovaný postup proti šíření sexuálně přenosných onemocnění. Intervence proti STD je zároveň preventivním opatřením proti šíření HIV. Článek poskytuje přehled o epidemiologii, klasifikaci, riziku přenosu a prevenci sexuálně přenosných onemocnění se zaměřením na chlamydiové infekce.
Klíčová slova:
STD – ohrožené skupiny – riziko přenosu – Chlamydia trachomatis
Úvod
Problematika sexuálně přenosných onemocnění (STD – sexually transmitted diseases, STI – sexually transmitted infections) je velmi dynamická a nelze ji zdaleka omezovat jen na klasické pohlavní nemoci, ke kterým patří syfilis, gonorea, lymphogranuloma venereum, ulcus molle a granuloma inguinale. S rozvojem diagnostických metod nabývají na významu další bakteriální, virové, mykotické, protozoální a parazitární infekce. Identifikace mnohých patogenních agens, celosvětově významných, se odehrála až v posledních třech dekádách, např. lidský papilomavirus (HPV) byl identifikován v roce 1976, HTLV I a II v letech 1980–1982, HIV 1 a 2 v letech 1983–1986, lidský herpes virus (HSV) typ 8, podílející se na vzniku Kaposiho sarkomu, až v roce 1995. Zpřesnění diagnostiky, genomové studie a širší použití molekulárně-genetických testů do rutinní praxe přineslo nový pohled na etiologii a epidemiologii některých STD. Tak např. čeleď Chlamydiaceae je nyní dělena na dva rody: rod Chlamydia s druhem Chlamydia trachomatis a rod Chlamydophila. Díky novým diagnostickým metodám byla upřesněna identifikace vyvolavatele endemického ulcerativního STD – granuloma inguinale, je jím Klebsiella granulomatis (dříve Calymmatobacterium granulomatis). Převrat v prevenci sexuálně přenosného nádorového onemocnění žen – karcinomu děložního hrdla vyvolaného onkogenními typy papilomavirů představují nově zavedené kvadrivalentní (HPV typ 6, 11, 16 a 18) a bivalentní (HPV typ 16 a 18) vakcíny.
Distribuce případů STD v populaci je velmi nehomogenní, existují vysoce rizikové „core groups“, populační segmenty s vysokým výskytem STD, ve kterých nákaza cirkuluje (10, 17). V západoevropských velkoměstech se vyskytly případy až doposud endemického onemocnění tropů a subtropů – lymphogranuloma venereum – vyvolaného C. trachomatis sérotypu L1-L3. Infekce probíhaly u homosexuálních mužů pod obrazem proktokolitidy (20). Pro STD je typické, že se sdružují, vytvářejí smíšené infekce s odlišnou inkubační dobou a různým klinickým obrazem, často probíhají asymptomaticky a vyžadují odlišné terapeutické postupy. Zdravotním rizikům sexuálně přenosných onemocnění zvláště u mladých žen je potřeba věnovat zvýšenou pozornost, protože jsou vůči STD zranitelnější než muži, a navíc u nich nákaza probíhá často nepozorovaně. Mohou být zdrojem infekce, aniž by si to uvědomovaly. Nelze opomíjet ani psychosociální aspekty STD. Řada pacientů trpí obavou z přenosu onemocnění, strachem z rekurencí, mají pocit viny,obávají se reakcí sexuálního partnera, často dochází k rozpadům partnerských vztahů. Zvláště rekurentní infekce mohou být příčinou sexuálních dysfunkcí. Dalším negativním důsledkem STD je stigmatizace nebo sociální vyloučení (17, 29).
Interakce STD a HIV
Mnoho studií potvrzuje hypotézu o vzájemné interakci STD a HIV infekce. STD mohou zvyšovat infekčnost osoby, která je zdrojem nákazy, a zvyšují vnímavost u osoby, která je exponována. Jedná se především o ulcerativní a zánětlivá STD (uretritidy, cervicitidy a vulvovaginitidy). Tak např. paralelní infekce chlamydiemi zrychluje dynamiku replikace HIV, asociace mezi HIV a bakteriální vaginózou byla prokázána na rozsáhlých souborech žen. Herpes simplex zvyšuje pětinásobně riziko přenosu HIV vzhledem k infiltraci puchýřů CD4+ lymfocyty, které jsou cílovými buňkami HIV infekce. U pacientů se syfilidou byla ve vředech prokázána vyšší koncentrace makrofágů a T-lymfocytů s receptory pro HIV. Lipoproteiny Treponema pallium navíc stimulují makrofágy ke zvyšování produkce cytokinů. Riziko přenosu HIV je u zánětlivých STD nejméně pětinásobné, u ulcerativních minimálně dvacetinásobné. Pro tento vztah se někdy užívá termín „epidemiologická synergie“. Intervence proti STD je zároveň preventivním opatřením proti šíření HIV (13, 15, 17, 19, 26).
Klasifikace STD
Sexuálně přenosné choroby lze dělit podle různých aspektů (13, 15, 17, 19). Podle způsobu přenosu etiologického agens je možno rozlišit:
1. Infekce šířené téměř výhradně pohlavním stykem patřící ke „klasickým“ pohlavním nemocem (PN), které podléhají podle současných zákonů České republiky povinnému hlášení:
- příjice (syphilis), původce Treponema pallidum;
- kapavka (gonorea), původce Neisseria gonorrhoeae;
- měkký vřed (ulcus molle), původce Haemophilus ducreyi;
- lymphogranuloma venereum (čtvrtá pohlavní nemoc), původce Chlamydia trachomatis sérotypu L1-L3;
- granuloma inguinale (pátá pohlavní nemoc), původce Klebsiella granulomatis.
2. Infekce šířené převážně pohlavním stykem:
- urogenitální chlamydiové infekce (Chlamydia trachomatis sérotypů D-K), další urogenitální bakteriální nekapavčité infekce (streptokoky, stafylokoky, enterokoky, gramnegativní aerobní a anaerobní bakterie např. Gardnerella vaginalis);
- infekce vyvolané prvoky (např. Trichomonas vaginalis, Entamoeba histolytica, Giardia lamblia, Cryptosporidium);
- infekce mykotické – urogenitální kandidózy (Candida albicans, C. tropicalis, C. glabrata);
- infekce virové (virus lidského imunodeficitu HIV 1,2, herpes simplex virus HSV 1 a 2, human papilloma virus – HPV, virus infekční hepatitidy typu B, poxviry);
- infekce ektoparazitární (Sarcoptes scabiei, Pediculus capitis, Phtirius pubis aj.);
- infekce vyvolané L-organismy (Mycoplasma hominis, Ureaplasma urealyticum).
Podle klasifikace CDC (Centers for Disease Control) se sídlem v Atlantě, která vychází převážně z klinické symptomatologie, jsou sexuálně přenosná onemocnění klasifikována následovně (4):
- ulcerativní (syfilis, herpes simplex, ulcus molle, lymphogranuloma venereum, granuloma inguinale);
- cervicitidy a uretritidy (gonorea, chlamydiální infekce, trichomoniáza, genitální herpetické infekce aj.);
- vulvovaginitidy (trichomoniáza, kvasinkové infekce, bakteriální vaginóza, infekce vyvolané mykoplazmaty);
- ostatní, s převážně kožními projevy (papilomavirové infekce, parazitární infekce – scabies, pedikulóza).
Charakteristiky ohrožených osob
Mladiství
Výskyt některých STD je nejvyšší ve skupině mladistvých osob, jedná se např. o chlamydiové a gonoroické infekce, jejichž prevalence je u žen nejvyšší ve věkové skupině 15–19 let, rovněž HPV infekce bývá častá v období dospívání (3, 4, 10). Mezi dospívajícími s akutní hepatitidou B (HBV) jsou nejčastěji uváděnými rizikovými faktory sexuální kontakt s chronicky infikovanými osobami, vyšší počet sexuálních partnerů a případná homosexuální orientace (1, 7). Mladiství jsou biologicky náchylnější k infekci, praktikují častěji nechráněné pohlavní styky, mají krátkodobé vztahy a často odmítají návštěvu zdravotnických zařízení. Zvýšené riziko STD u sexuálně aktivních osob do 15 let věku hrozí především mladistvým v nápravných zařízeních, mužům s homosexuální orientací a uživatelům intravenózně podávaných drog (4).
Děti
Diagnostika a léčba dětí s podezřením na STD vyžaduje citlivý přístup, spolupráci mezi odborníky různých lékařských oborů, sociálními pracovníky a příslušnými laboratořemi. Některá onemocnění, jako gonorea, syfilis nebo chlamydiové infekce, pokud jsou získána postnatálně (ne transplacentárně nebo perinatálně), jsou téměř 100% indikátorem sexuálního kontaktu. U jiných onemocnění, jako jsou HPV infekce nebo vaginitida, není asociace se sexuálním kontaktem tak jednoznačná (4).
Homosexuální muži
Frekvence nechráněného sexu, bakteriálních infekcí a incidence HIV u homosexuálních mužů od 80. let do poloviny 90. let minulého století v USA a dalších průmyslově vyspělých zemích klesala. K nárůstu počtu STD (hlavně syfilidy, kapavky, chlamydiální infekce) došlo během poslední dekády v důsledku rizikového sexuálního chování v souvislosti s dostupností efektivnější léčby HIV (5, 8, 9).
Lékaři by se měli u sexuálně aktivních homosexuálních mužů soustředit na klinické příznaky spojené s STD, k nimž patří uretrální výtok, dysurie, genitální a perianální vředy, regionální lymfadenopatie, exantém nebo anorektální symptomy spojené s proktitidou.
Rutinní laboratorní screening na běžné STD je podle doporučení CDC indikován u všech sexuálně žijících homosexuálních mužů, a to nejméně jedenkrát ročně (4). Ke screeningu patří:
- sérologie HIV (u HIV negativních mužů nebo pokud nebyli testováni v průběhu předchozího roku);
- sérologie syfilidy;
- test na uretrální infekci N. gonorrhoeae a Chlamydia trachomatis u mužů, kteří měli během předchozího roku insertivní pohlavní styk;
- test na rektální infekci N. gonorrhoeae a C. trachomatis u mužů, kteří měli během předchozího roku receptivní anální styk;
- test na faryngeální infekci N. gonorrhoeae u mužů, kteří během předchozího roku uvedli receptivní orální styk (testování na faryngeální infekci C. trachomatis není doporučováno);
Častější STD screening (každých 3–6 měsíců) je doporučován u homosexuálních mužů, kteří:
- mají více partnerů;
- mají sexuální styky s náhodnými neznámými partnery;
- jsou uživateli, nebo jejichž partner je uživatelem ilegálních drog.
Vakcinace proti hepatitidě A i B je doporučována všem homosexuálním mužům, u kterých není možno prokázat předchozí infekci nebo imunizaci (1, 7).
Epidemiologie STD a HIV
I když Česká republika patří k zemím s nízkým výskytem HIV/AIDS, byl v průběhu posledních let zaznamenán strmější nárůst počtu infikovaných pacientů. Během prvního pololetí roku 2007 bylo zachyceno 64 nových případů HIV/AIDS, což představuje 10% nárůst oproti stejnému období loňského roku. Celkem je k 30. 6. 2007 registrováno 1248 HIV pozitivních osob (984 u českých občanů a rezidentů a 264 u cizinců převážně z východní Evropy), z toho u 225 infikovaných bylo diagnostikováno plně rozvinuté onemocnění AIDS. K témuž datu bylo zaznamenáno 127 úmrtí na AIDS. Nejčastějším způsobem přenosu je přenos sexuální (přes 85 %), nejvíce exponovanou populační skupinou zůstávají v ČR homosexuální muži (55,6 % nově diagnostikovaných případů infekce HIV), četnost infikovaných žen je kolem 21 % (2).
K největšímu nárůstu počtu případů syfilidy v České republice došlo mezi rokem 1990, kdy bylo hlášeno 164 nových případů, a rokem 2001, kdy bylo hlášeno 1376 případů. V posledních třech letech se počet případů syfilidy pomalu snižuje na 502 onemocnění hlášených v roce 2006 (tab. 1). Podíl časných forem syfilidy v relaci s pozdními a jinými formami dosáhl svého vrcholu v roce 1996 (71,0 %), v roce 2006 klesá na 35 %. Nejrizikovější věkovou skupinou jsou u příjice 20–24letí a 25–29letí. Je pozorován import infekce především z bývalého SSSR (11, 13, 22).
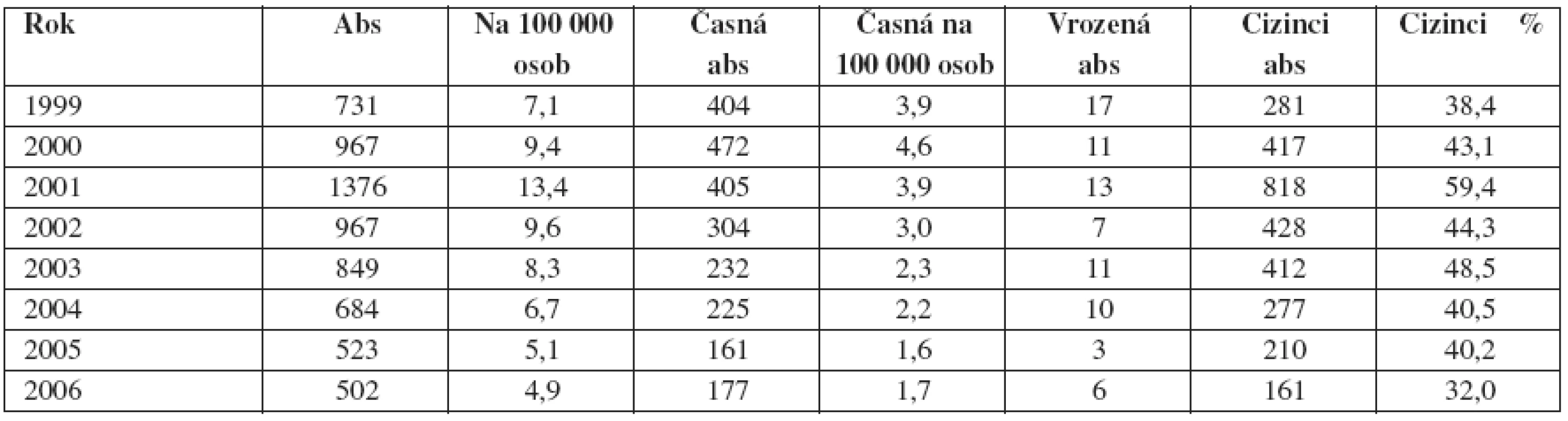
V zemích západní Evropy dosáhla syfilis nejnižších hladin v časných 90. letech, což bylo v rozporu s výrazným vzestupem infekce ve státech bývalého Sovětského svazu. Od roku 1996 je syfilis na vzestupu v mnoha státech severní a západní Evropy. K nárůstu infekce došlo v letech 1999 a 2001 v Holandsku, Norsku, Irsku a Francii především u homosexuálních mužů včetně těch, kteří byli infikováni HIV (4, 8, 9).
U gonorey dochází v ČR po přechodném nárůstu v letech 1990–1992 k trvalému poklesu hlášených případů (11, 13, 22). V roce 1992 byl absolutní počet hlášených gonokokových infekcí celkem 7455, v roce 2005 poklesl na 859 případů (8,4 na 100 000 obyvatel) (tab. 2). Tento trend neodpovídá skutečnosti a může být způsoben nedůsledností při vyplňování povinných hlášení, léčbou bez cíleného venerologického vyšetření a bez dispenzarizace nebo samoléčbou. Důkazem nedůslednosti při vyplňování a odesílání povinných hlášení jsou epidemiologická data z pražské populace. V Praze je v posledních letech (r. 2002 – 2006) hlášeno ročně průměrně 320 případů gonorey, z toho 284 (88,5 %) případů připadá na STD centrum Dermatovenerologické kliniky 1. LF UK a VFN. Znamená to, že všechna ostatní pražská zdravotnická zařízení se na hlášení podílejí pouhými 11,5 %.
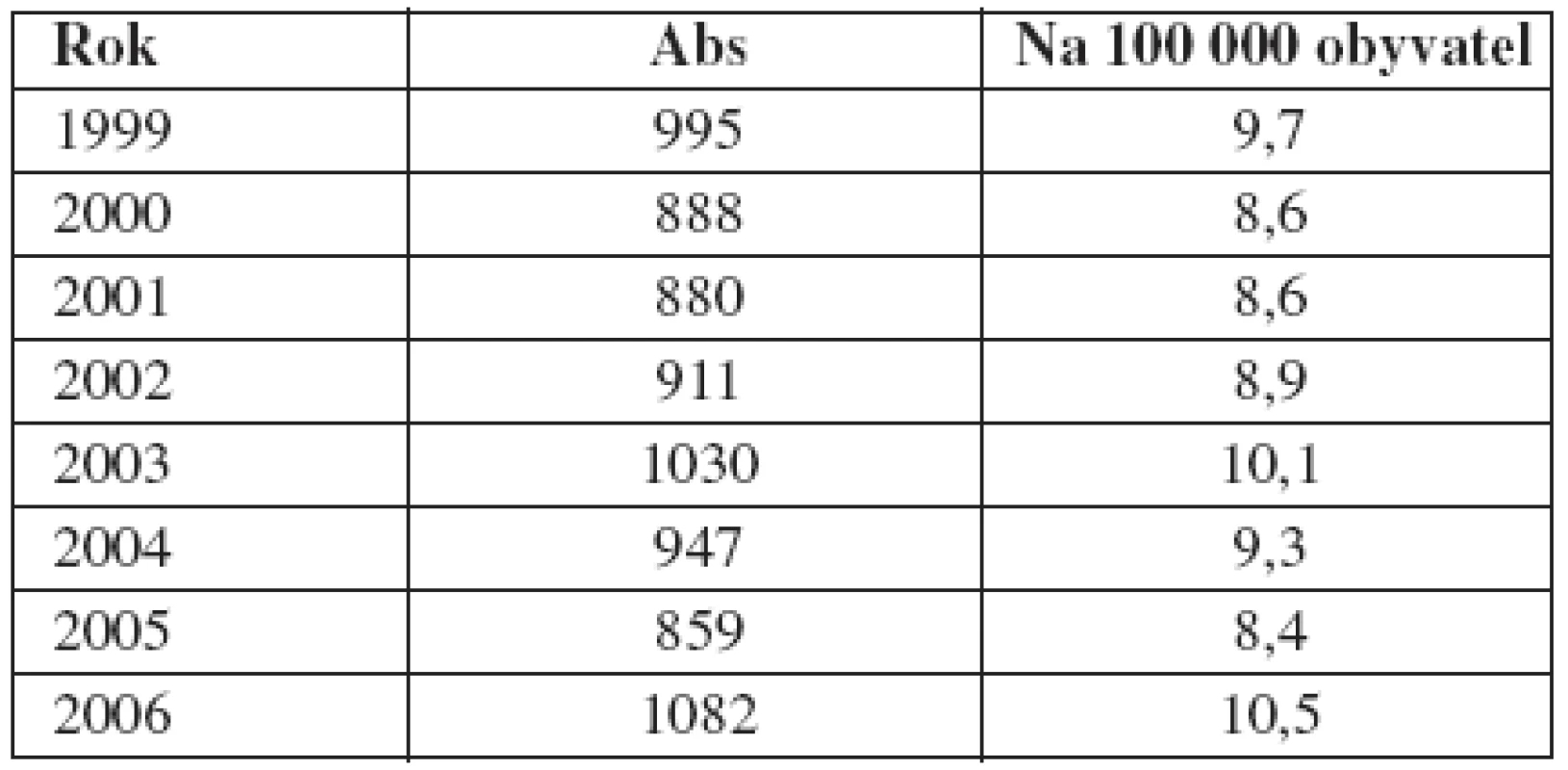
V zemích západní Evropy došlo po roce 1995 k nárůstu počtu případů, např. v Anglii byl zaznamenán nejvyšší nárůst mezi rokem 1999 a 2000 (29 %). Podobný trend byl pozorován v Rakousku, Francii, Irsku, naopak v Norsku došlo k poklesu počtu případů. Nejvyšší incidence je pozorována u mladých sexuálně vysoce aktivních osob ze slabších socioekonomických vrstev (5).
Riziko přenosu STD a HIV
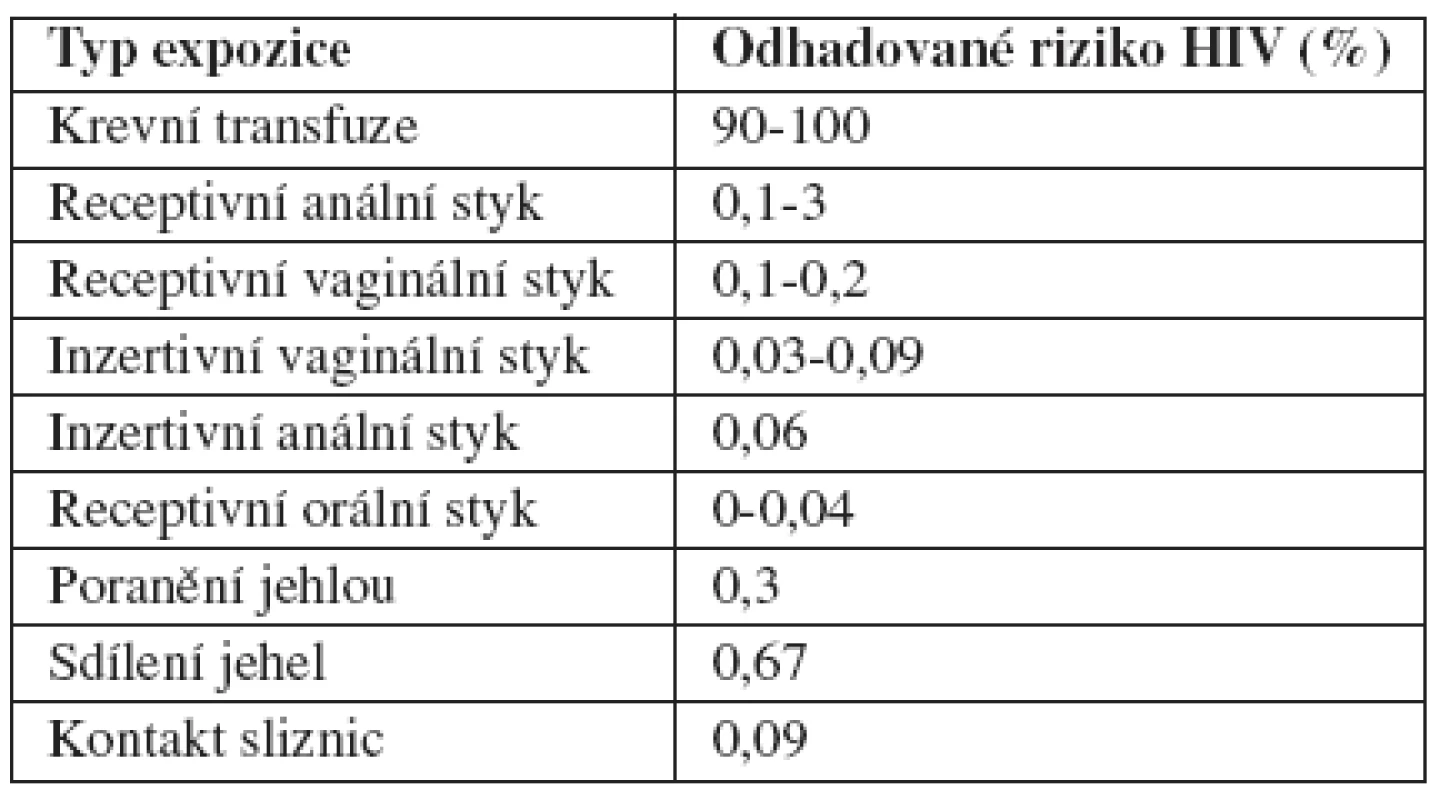
Riziko přenosu HIV v závislosti na typu expozice je uvedeno v tab. 3, nejrizikovější je receptivní anální styk. Vaginální styk znamená vyšší riziko pro ženu, doba expozice HIV je po receptivním vaginálním styku u ženy výrazně delší, a kromě toho je množství virů ve spermatu vyšší než ve vaginálním sekretu. Riziko přenosu gonorey při jednom sexuálním styku (transmission efficiency) z infikovaného muže na neinfikovanou ženu je 50–60 % a z infikované ženy na neinfikovaného muže 20 % (17). Významným zdrojem infekce jsou ženy a muži s asymptomatickou uretritidou, přičemž u žen jsou asymptomatické infekce mnohem častější než u mužů. Četnost přenosu chlamydiální infekce je u obou pohlaví stejná a pohybuje se kolem 68 %. Trichomoniáza se může přenášet tělesnými sekrety (moč, vaginální sekret, sperma). Přenos je častější z muže na ženu. Za 48 hodin po expozici onemocní přibližně 85 % žen a 70 % mužů (17). U asymptomatických mužů je rezervoárem infekce prostata. U mužů může infekce spontánně vymizet. Trichomonády mohou přežívat krátkou dobu i ve vlhkém prostředí (bazén). Bakteriální vaginóza (BV) vzniká v důsledku nerovnováhy vaginálního ekosystému. Prostředí, v němž převažují kyseliny produkující laktobacily, se mění v prostředí, v němž převažuje Gardnerella vaginalis a anaerobní bakterie. BV není striktně považována za STD, i když ke spouštěcím faktorům patří vyšší počet sexuálních partnerů a četné pohlavní styky (16). U syfilidy se infekčnost v časném období (do dvou let po infekci) pohybuje od 10 do 60 % (uplatňuje se vliv prostředí, velikost infekční dávky, vlastnosti mikro - i makroorganismu). Je vázána na kontakt s materiálem obsahujícím živá virulentní treponemata. S trváním infekce a přechodem do pozdního latentního období nemoci riziko infekce postupně klesá (17, 19, 28). Condylomata accuminata vyvolaná lidským papilomavirem (HPV) jsou vysoce kontagiózní, přibližně u dvou třetin jedinců, kteří mají kontakt s partnerem s manifestní formou akuminátních kondylomat, dochází k rozvoji klinicky manifestní infekce. Významnou roli hraje věk (nejčastěji postihuje osoby mladšího věku) a různé parametry sexuální aktivity. Patří k nim časný nástup sexarché, celoživotní počet sexuálních partnerů a počet sexuálních kontaktů partnera, nechráněné pohlavní styky, nulliparita a současná infekce jinou STD. Dalším rizikovým faktorem je imunosuprese. K přenosu dochází i při asymptomatickém nosičství nebo subklinických projevech (4, 14, 23). Virus hepatitidy B (HBV) se přenáší krví a tělesnými tekutinami obsahujícími krev, např. spermatem, vaginálním sekretem, event. exsudátem z infikovaných ran. Hlavní způsob šíření infekce je sexuální kontakt. To vysvětluje velmi vysoký výskyt hepatitidy B mezi homosexuály a u promiskuitních heterosexuálů. HBV se daleko snadněji šíří sexuálním kontaktem než HCV (virus hepatitidy C) nebo HIV.
Chlamydiové infekce
V souvislosti s problematikou STD je v dermatovenerologické literatuře nejčastěji zmiňována syfilis a gonorea, objevují se i publikace věnované herpetickým infekcím a papilomavirům (11, 12, 13, 14, 21, 26, 28). Ačkoliv chlamydiální infekce patří k nejčastějším bakteriálním STD, existuje jen omezený počet publikací, které by se věnovaly jejich problematice a interpretaci sérologických nálezů s korelací s klinickým obrazem. Pro dermatovenerology jsou důležité z hlediska diferenciální diagnostiky STD charakterizovaných výtokem. Dříve byl v rámci čeledi Chlamydiaceae rozeznáván jediný rod Chlamydia se čtyřmi druhy: Chlamydia trachomatis, Chlamydia pneumoniae, Chlamydia psittaci a Chlamydia pecorum. Nyní je podle fylogenetických a genomových studií čeleď Chlamydiaceae dělena na dva rody:
- Chlamydia s druhem Chlamydia trachomatis ;
- Chlamydophila s druhy Chlamydophila pneumoniae, Chlamydophila psittaci a Chlamydophila pecorum.
V humánní medicíně mají hlavní význam Chlamydia trachomatis a Chlamydophila pneumoniae, zatímco Chlamydophila psittaci je primárně zvířecí patogen s možností přenosu na člověka. Výraz chlamydie se obvykle vztahuje k celé čeledi (27).
Chlamydie jsou intracelulární energetičtí paraziti, kteří nejsou vybaveni vlastním systémem pro tvorbu ATP a ke svým metabolickým procesům využívají ATP hostitelské buňky. Jsou vnímavé k účinku antibiotik a množí se ve zvláštním růstovém cyklu. Extracelulárně mají podobu drobných infekčních elementárních tělísek (250–400 nm). Až v napadených buňkách, tedy intracelulárně, se elementární tělísko transformuje v neinfekční, ale metabolicky aktivní retikulární tělísko (800–1200 nm). Již po 8–9 h probíhá první binární dělení, jehož výsledkem jsou po kondenzaci dvě nová elementární tělíska. To vše za spotřeby „hostitelské“ ATP (energetický parazitismus). Podle typově specifických proteinových antigenů na povrchu elementárních tělísek se rod Chlamydia dělí na 18 sérotypů (sérovary) a na tři biotypy (biovary): trachom, LGV (lymphogranuloma venereum), třetí biovar zahrnuje původce pneumonitidy u myší. Biovar trachoma má afinitu k cylindrickému epitelu sliznic, biovar LGV k lymfatické tkáni (16, 17, 27).
Trachom je chronická konjunktivitida vyvolaná Chlamydia trachomatis, biovar trachoma, sérotypu A, B, Ba a C, je nejčastější příčinou endemické slepoty v rozvojových zemích, nepřenáší se sexuálně, ale kontaktem z očí do očí. Celosvětově postihuje 500 miliónů osob.
Oční infekce vyvolanáChlamydia trachomatis, biovar trachoma, sérotypu D-K postihuje převážně dospělé, sexuálně aktivní osoby, děti bývají infikovány od matky. Projevuje se formou inkluzní konjunktivitidy (paratrachom) a u dospělých bývá spojena s genitální infekcí. U dospělých má většinou jen mírný průběh a spontánně vymizí.
Existují dva odlišné typy sexuálně přenosných infekcí vyvolaných C. trachomatis:
- urogenitální chlamydiová infekce (C. trachomatis, biovar trachoma, sérotyp D-K);
- lymphogranuloma venereum (C. trachomatis, biovar LGV, sérotyp L1-L3).
Urogenitální chlamydiová infekce vyvolaná Chlamydia trachomatis sérotypu D-K je v Evropě i USA nejčastější bakteriální STD, odhaduje se, že v průmyslových zemích představuje kolem 50 % všech urogenitálních nákaz. Chlamydiové infekce jsou dnes častější než infekce gonokokové a často se s nimi kombinují. U žen je průběh až v 80 % asymptomatický a může vést k závažným pozdním komplikacím, k nimž se řadí pánevní zánětlivá nemoc (PID), infertilita, tubární sterilita a mimoděložní těhotenství. U mužů probíhá infekce v 75 % případů symptomaticky a je charakterizována uretrálním výtokem, dysurií, event. příznaky epididymitidy a prostatitidy. Mladí muži mohou být postiženi Reitrovým syndromem charakterizovaným artritidou, uretritidou a konjunktivitidou. Někdy je doprovázen plantární hyperkeratózou (keratodermia blenorrhagica).
Často se sdružuje s gonoreou nebo se projeví až jako přetrvávání obtíží po její léčbě (postgonokoková uretritida). Vždy je nutno vyšetřit a léčit sexuální partnery. Novorozenci, kteří se narodí matkám s cervikální chlamydiovou infekcí, mají 60–70% pravděpodobnost, že budou nakaženi konjunktivitidou nebo pneumonií.
Chlamydiální infekce podobně jako jiné cervicitidy a uretritidy zvyšuje riziko přenosu HIV.
Diagnostika
K vyšetření se zasílá uretrální nebo endocervikální výtěr, výtěr z rekta, event. vzorek prvního proudu ranní moči, u konjunktivitid výtěr ze spojivky. Výsledek vyšetření je závislý na správně provedeném odběru, skladování a transportu vzorku. Doporučuje se používat komerčně dostupné speciální odběrové sety nebo cytokartáčky. Odběr musí být dostatečně razantní vzhledem k nutnosti získání potřebného množství epitelií. Při odběru z endocervixu je nutno nejprve odstranit hlen, zavést tampon 2 cm do cervikálního kanálu a rotací odebrat uvolněné epiteliální buňky. Při odběru z uretry se tampon zavádí 3 cm hluboko. Kontaminace krví může mít negativní vliv na výsledek některých testů. Při odběru ze spojivek se provádí stěr ze spojivky dolního i horního víčka. Materiál je nutno transportovat do 24 hodin při teplotě 2–8 °C. Průkaz zahrnuje detekci antigenu metodou přímé imunofluorescence nebo metodou ELISA. Specifické úseky bakteriální DNA lze detekovat molekulárně-genetickými metodami – amplifikační metodou (PCR, LCR) nebo hybridizací. Při amplifikační metodě PCR (polymerázová řetězová reakce) dochází k amplifikaci jedinečného úseku bakteriálního genomu pomocí synteticky připravených sond (primerů) a termostabilní DNA polymerázy. Produkty reakce jsou detekovány po obarvení ethidium bromidem pomocí elektroforézy v agarovém gelu, nebo pomocí hybridizace se značenými sondami, a to buď v průběhu reakce (real-time PCR) nebo na jejím konci (imunohistochemická detekce hybridů). Citlivost amplifikačních metod je odhadována na 90–98 %. Při hybridizační reakci se z klinického materiálu extrahuje bakteriální RNA, která hybridizuje s DNA sondou. Vzniklé RNA-DNA hybridy jsou vychytávány na mikročástice s magnetickým povrchem a detekovány pomocí chemiluminiscence. Citlivost je v porovnání s kultivací vyšší, ale v porovnání s amplifikací nižší. Chlamydie lze kultivovat na tkáňových kulturách, citlivost této metody je obvykle nižší než 50 %.
Nepřímý průkaz detekce protilátek sérologickými metodami je méně informativní, význam má průkaz signifikantního vzestupu jejich titru. Při průkazu akutní infekce většinou nelze činit závěr z jednoho vyšetření, ale je nutné testování párových vzorků séra s minimálním odstupem tří týdnů.
Pro průkaz chronické infekce (PID, Reiterův syndrom) je využití sérologických testů ještě problematičtější: protilátky mohou dlouhodobě přetrvávat, takže je obtížné odlišit současnou a minulou infekci. Lze použít metody detekce typově specifických nebo rodově specifických protilátek. Při detekci typově specifických protilátek se prokazují IgG, IgA a IgM protilátky proti typově specifickým antigenům, hlavně proti MOMP (main outer membrane protein) metodou mikroimunofluerescenčního testu (MIF). Tento test má v porovnání s ostatními sérologickými metodami vysokou citlivost a specificitu. Druhou variantou je průkazu typově specifických IgG, a IgA pomocí ELISA testů, které využívají rekombinantní typově specifické antigeny. Pro stanovení rodově specifických protilátek (antigeny jsou společné pro všechny druhy chlamydií) se používá test ELISA, imunodominantním antigenem je rekombinantní lipopolysacharidový komplex. Nevýhodou je, že rodově specifické IgA i IgM mohou po prodělané infekci dlouhodobě přetrvávat (několik měsíců) a jsou méně specifické (je zde možnost křížové reaktivity s jinými gram-negativnimi bakteriemi). Naopak výhodou je, že se při primoinfekci vytvářejí dříve než typově specifické protilátky. Samotný nález rodově specifických protilátek nelze považovat za průkaz infekce. Jako suspektní probíhající nebo prodělanou infekci hodnotíme:
- současný průkaz typově specifických IgG a IgM protilátek;
- nález vysokého titru typově specifických IgG protilátek (1 : 512 a výše) a současně zvýšeného titru typově specifických IgA protilátek (1 : 16 a výše);
- signifikantní vzestup typově specifických protilátek v párových vzorcích séra.
Sérologie má význam hlavně při detekci chlamydiové pneumonie při primoinfekci u novorozenců, kde detekujeme IgM (16, 17).
Přehled laboratorních metod v diagnostice chlamydií:
Přímý průkaz:
- přímý průkaz DNA C. trachomatis pomocí amplifikace (PCR, LCR) nebo hybridizace;
- detekce antigenů imunofluorescenčním testem (IF test);
- tkáňové kultury.
Detekce rodově a druhově specifických protilátek (pomocné vyšetření s nižší informativní hodnotou):
- MIF (mikroimunofluorescenční test, druhově specifický test) ,
- ELISA test (druhově nebo rodově specifický test ).
Lymphogranuloma venereum
Invazivnější biovar C. trachomatis – biovar lymphogranuloma venereum, sérotyp L1–L3 vyvolává onemocnění endemických oblastí lymphogranuloma venereum. Holandští autoři analyzovali 62 případů LGV diagnostikovaných u homosexuálních mužů v roce 2003 a 2004 v západoevropských velkoměstech. Pouze u jednoho pacienta mělo onemocnění typický průběh s tvorbou vředů a inguinální lymfadenopatií, ostatní měli klinické známky proktokolitidy. C. trachomatis byla detekována z rektálních vzorků, výtěry z uretry byly negativní (20). V současné době se v našich laboratořích neprovádí sérotypizace, je možno provést vyšetření metodou PCR.
Závěr
Rozdílnost systémů státní kontroly, diagnostiky a léčby STD v jednotlivých zemích ukazuje, že je nutné vyvinout lépe koordinovanou celoevropskou strategii pro ochranu sexuálního zdraví. Je nutno zdůraznit potřebu systematického vyhledávání kontaktů a zdrojů (contact tracing, partner notification) u osob s prokázanou STD. Každá potencionálně ohrožená osoba by měla být pozvána na vyšetření a léčbu. V Evropě je tento systém zaveden od roku 1900, ve švédské legislativě se objevuje v roce 1918, v USA v roce 1930. Cílem vyhledávání kontaktů a zdrojů je přerušení epidemiologických sítí, které má v prevenci STD i HIV klíčovou roli. Důležitý je systematický a přesný sběr statistických dat a vyhledávání nejvíce ohrožených skupin (5, 15, 24).
Lepší kontrolu STD může přinést rozsáhlejší spolupráce na úrovni EU, zejména pak sdílení poznatků o nových přístupech v oblasti prevence STD. Je nutné:
- vytvořit jednotnou koncepci prevence rizikového sexuálního chování, která by měla oporu v kvalitním výzkumu, vzdělávání a metodické podpoře;
- vytvořit vzorové preventivní programy s ohledem na věk a vzdělání cílové skupiny;
- zabezpečit lepší spolupráci rodiny a školy;
- propojit zdravotní, sociální a výchovné intervence, např. propojit intervence proti STD s intervencemi proti užívání návykových látek;
- zlepšit komunikaci mezi státními a nestátními neziskovými subjekty;
- zefektivnit financování celého systému.
Práce podpořena grantem České akademie dermatovenerologie.
Došlo do redakce: 7. 5. 2008
MUDr. Ivana Kuklová, CSc.
Dermatovenerologická klinika 1. LF UK a VFN
U Nemocnice 2
128 00 Praha 2
E-mail: ikuklova@post.cz
Sources
1. Alter, M J. Epidemiology of hepatitis B in Europe and worldwide. J Hepatol, 2003, 39 (Suppl), p. 64-69.
2. Brůčková, M., Malý, M., Vandasová, J.: Výskyt a šíření HIV/AIDS v ČR v roceprvním pololetí 2007. Zprávy CEM (SZÚ Praha), 2007, 16 (8), p. 368-371.
3. Burchell, AN., Richardson, H., Mahmud, SM. et al. Modeling the sexual transmissibility of human papillomavirus infection using stochastic computer simulation and empirical data from a cohort study of young women in Montreal, Canada. Am J Epidemiol, 2006, 163(6), p. 534-543.
4. CENTERS FOR DISEASE CONTROL. Sexually transmitted diseases treatment guidelines, 2006. MMWR Recomm Rep, 2006, 55, p. 1-94.
5. Fenton, KA., Lowndes, CM. The European Surveillance of Sexually Transmitted Infections. Recent trends in the epidemiology of sexually transmitted infections in the European Union (ESSTI) Network. Sex Transm Infect, 2004, 80, p.255-263
6. Fisher, M., Benn, P., Evans, B. et al. UK guideline for the use of post-exposure prophylaxis for HIV following sexual exposure. Int J STD AIDS, 2006, 17, p. 81-92.
7. Gilbert, LK., Bulger, J., Scanlon, K. et al. Integrating hepatitis B prevention into sexually transmitted disease services: U.S. Sexually Transmitted Disease Program and Clinic Trends – 1997 and 2001. Sex Transm Dis, 2005, 32(6), p.346-350.
8. Goh, BT. Syphilis in adults. Sex Transm Inf, 2005, 81(6), p. 448 - 452.
9. Hopkins, S., Lyons, F., Coleman, C. et al. Resurgence in infectious syphilis in Ireland. Sex Transm Dis, 2004, 31(5), p. 317-321.
10. Kahn, RH., Mosure, DJ., Blank, S. et al. Chlamydia trachomatis and Neisseria gonorrhoeae prevalence and coinfection in adolescents entering selected US juvenile detencion centers, 1997-2002. Sex Transm Dis, 2005, 32(4), p. 255-259.
11. Kaštánková, V.: Epidemiologická situace pohlavních chorob v České republice. Státní zdravotní dozor ve venerologii. Prakt Lék, 2000, 80, p. 336-339.
12. Kaštánková, V. Venerologická příčina akutní břišní příhody u mladé ženy s rizikovým sexuálním chováním. Prakt Lék, 2006, 86 (4), p.206-208.
13. Křemenová, S. Sexuálně přenosné choroby – historie a současné problémy. In: Benáková, N. (ed). Dermatovenerologie, dětská dermatologie a korektivní dermatologie 2006/2007. Praha: Triton, 2006, p. 149-165.
14. Litvík, R. Anogenitální akuminátní kondylomata – možnosti terapie pohledem venerologa. Farmakoterapie, 2007, 4, p. 271-278.
15. MADKAN, VK., GIANCOLA, AA., Sra, KK., Tyring, SK. Sex differences in the transmission, prevention, and disease manifestations of sexually transmitted diseases. Arch. Dematol, 2008, 142, p. 365-370.
16. Mašata, J., Jedličková, A. a kol.: Infekce v gynekologii a porodnictví. Praha: Maxdorf, 2004, 371 p.
17. McMillan, A., Young, H., Ogilvie, MM., Scott, GR. Clinical practice in sexually transmissible infections. Saunders, 2002, 591 p.
18. MEYER, T. Moderne Diagnostik der Chlamydia-trachomatis-infektion. Hautarzt, 2007, 58, p. 24-30.
19. Morse SA, Ballard RC, Holmes KK (ed). Atlas of Sexually transmitted diseases and AIDS, 3rd edition. Edinburgh, London, New York: Mosby, 2003, 408 p.
20. Nieuwenhuis, RF., Ossewaarde, JM., Götz, HM. et al. Resurgence of lymphogranuloma venereum in western Europe: an outbreak of Chlamydia trachomatis serovar L2 proctitis in the Netherlands among men who have sex with men. Clin Infect Dis, 2004, 39, p. 996-1003.
21. Pánková, R., Kaštánková, V., Kuklová, I., Vosmík, F. Risky sexual behavior – reason for an increased coincidence of sexually transmitted diseases, a case report. Bulletin CEEDVA, 2000, 2, p. 47-48.
22. Pohlavní nemoci 2005, Praha: ÚZIS, 2006.
23. Radcliffe, K. European STD guidelines. Int J STD AIDS, 2001, 12 (S3), p. 1-101.
24. Resl, V. Státní dozor ve venerologické práci. Čes-slov Derm, 2005, 80 (2), p. 102-103.
25. Roubalová, K., Janečková, L. Doporučené metody pro diagnostiku Chlamydia trachomatis. Zprávy CEM (SZÚ, Praha), 2005, 14(12), p. 510 – 514.
26. SALAVEC, M. Virová onemocnění kůže a sliznic působená herpes simplex viry a lidskými papilomaviry. Čes-slov Derm, 2006, 81 (5), p. 249-269.
27. Votava, M a kol. Lékařská mikrobiologie speciální. Brno, Neptun, 2003, 495 p.
28. Zákoucká, H., Kuklová, I. Diagnostika klasických pohlavních chorob. Čes-slov Derm, 2007, 82 (2), p. 65-74.
29. ZIKMUNDOVÁ, M., WEISS, P. Komerční sex a riziko HIV. Čes a slov Psychiatr, 2004, 100 (2), p. 78-83.
Labels
Dermatology & STDs Paediatric dermatology & STDsArticle was published in
Czech-Slovak Dermatology

2008 Issue 3
Most read in this issue
- Treatment of Sexually Transmitted Diseases
- Benign Symmetric Lipomatosis Launois-Bensaude
- State of the Art in Sexually Transmitted Diseases
- The Beginning of Czech Dermatology and Syphilidology
