Dispenzarizace pacientů s maligním melanomem
Follow-up of Patients with Melanoma
The analysis included patients with melanoma from the group followed at the melanoma clinic of The Department of Dermatology School 2nd Faculty of Medicine and Faculty Hospital Bulovka in the years 1989–2009. Those examined in the year 2009 were included in the study. We evaluated risk factors and photo-type of patients with diagnosed metastasis. Also the appearance of the second primary cancer was assessed.
The whole-life follow-up in melanoma patients is recommended, the frequency of controls depends on the stage of the disease. The aim of the follow-up is an early detection of progression and recurrence of melanoma as well as appearance of other malignancies
Key words:
metastatic melanoma – follow-up – risk factors
Authors:
N. Vojáčková; Z. Kružicová; L. Vrbová; J. Hercogová
Authors‘ workplace:
Dermatovenerologická klinika UK 2. LF a FN Na Bulovce, přednosta prof. MUDr. Jana Hercogová, CSc.
Published in:
Čes-slov Derm, 86, 2011, No. 3, p. 144-147
Category:
Clinical and laboratory Research
Overview
Soubor zahrnuje pacienty s diagnózou melanomu, kteří byli zařazeni do dispenzarizace melanomové poradny Dermatovenerologické kliniky 2. LF UK a FN Na Bulovce v období 1989–2009. Analyzovali jsme pacienty souboru, kteří docházeli aktivně na kontroly v roce 2009. Při hodnocení jsme se zaměřili na identifikaci rizikový faktorů a fototyp pacientů, u kterých byla diagnostikována metastáza. Dále jsme sledovali vznik druhých primárních malignit. Dispenzarizace pacientů s melanomem se doporučuje celoživotní, rozsah a frekvence kontrol se odvíjí především od stadia onemocnění. Cílem dispenzarizace je včasná detekce progrese a recidivy onemocnění a ostatních malignit.
Klíčová slova:
metastazující melanom – dispenzarizace – rizikové faktory
ÚVOD
Systematické sledování pacientů s diagnózou kožního melanomu se na Dermatovenerologické klinice UK 2. lékařské fakulty a FN Na Bulovce provádí od roku 1989. Frekvence a rozsah kontrol se řídí podle stadia onemocnění a upravuje se podle délky sledování s přihlédnutím k dalším faktorům: věku pacienta, přidruženým chorobám, dalším kožním změnám. Při každé kontrole se provádí klinické vyšetření (jizva a okolí, spádové lymfatické uzliny, celý kožní povrch), u indikovaných pacientů laboratorní testy a přístrojová vyšetření (krevní obraz, jaterní enzymy, urea, kreatinin a laktátdehydrogenáza, RTG plic, ultrasonografie břicha a spádových lymfatických uzlin, při patologii CT, NMR scintigrafie, PET).
Sledování pacientů s melanomem se doporučuje celoživotní. K vyřazení z dispenzarizace vedou různé důvody, kromě exitu je to vznik komplikací a předání do péče jiné příslušné odbornosti, změna bydliště a předání do péče jiné melanomové poradny, odmítnutí další péče ze strany pacienta.
Cílem dispenzarizace je včasná detekce recidivy a metastáz a jejich následná včasná léčba, kontrola pigmentových névů, identifikace podezřelých lézí a jejich preventivní odstranění, detekce prekanceróz a jiných kožních nádorů a jejich léčba [3]. Melanom metastazuje lymfatickou nebo hematogenní cestou, metastázy se dělí na časné (do pěti let) a pozdní, asi 3 % metastáz se objeví po deseti i více letech [8, 11, 14].
MATERIÁL A METODIKA
Soubor zahrnuje pacienty s diagnózou melanomu, kteří byli zařazeni do dispenzarizace melanomové poradny Dermatovenerologické kliniky 2. LF UK a FN Na Bulovce v období 1989–2009. Analyzovali jsme pacienty souboru, kteří docházeli aktivně na kontroly v roce 2009. Sledovali jsme pohlaví, věk v době diagnózy, lokalizaci melanomu, tloušťku nádoru v milimetrech podle Breslowa, výskyt druhého primárního nádoru a vznik metastáz. U pacientů s metastázou jsme dále hodnotili rozdělení podle pohlaví, klasifikaci podle Breslowa primárního melanomu a jeho lokalizaci, dobu od excize melanomu k detekci metastázy a její lokalizaci.
VÝSLEDKY
V letech 1989–2009 bylo do dispenzarizace melanomové poradny zařazeno celkem 1122 pacientů. Z toho 454 pacientů nadále aktivně na kontroly dochází, 101 pacientů bylo předáno do péče jiné melanomové poradny, 285 pacientů přestalo na pravidelné kontroly docházet bez udání důvodu a 282 pacientů zemřelo.
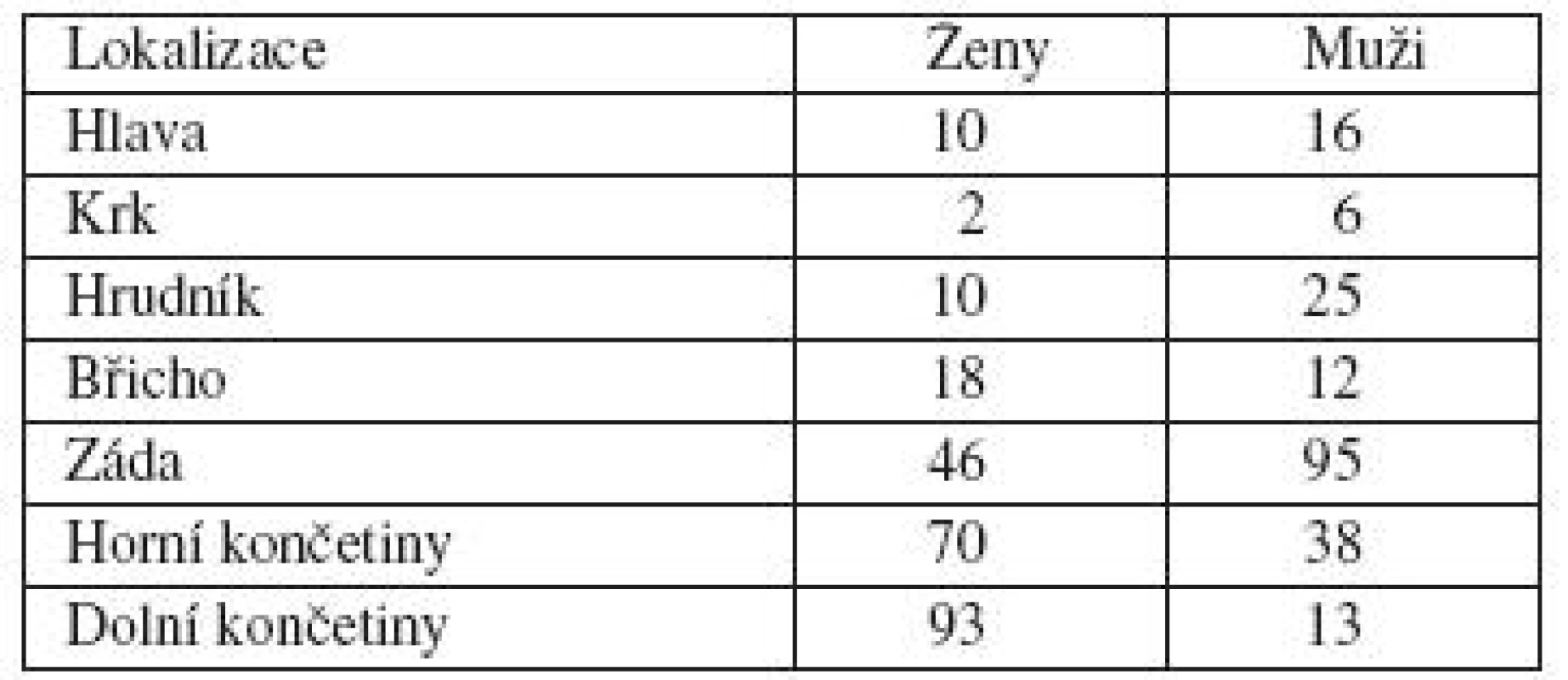
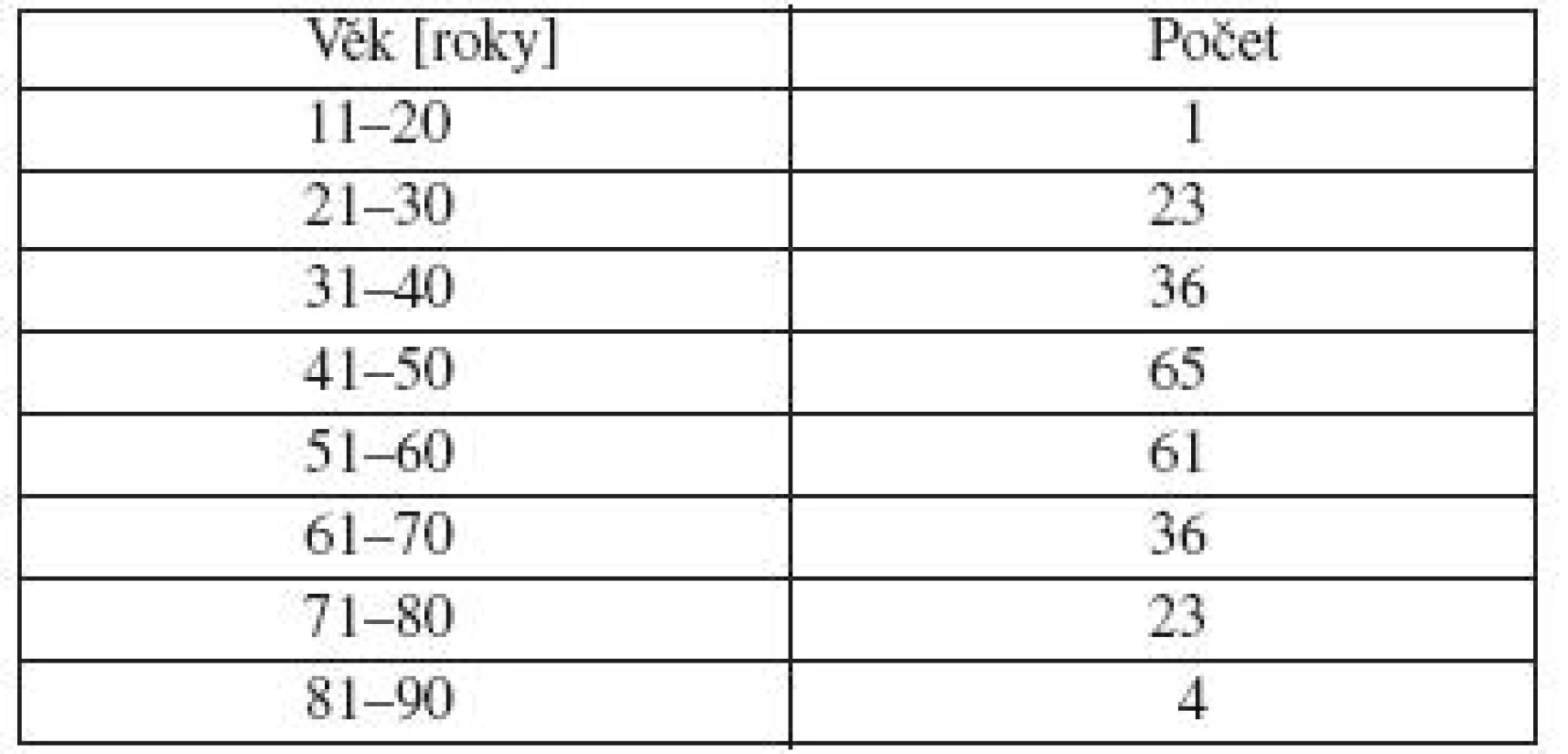
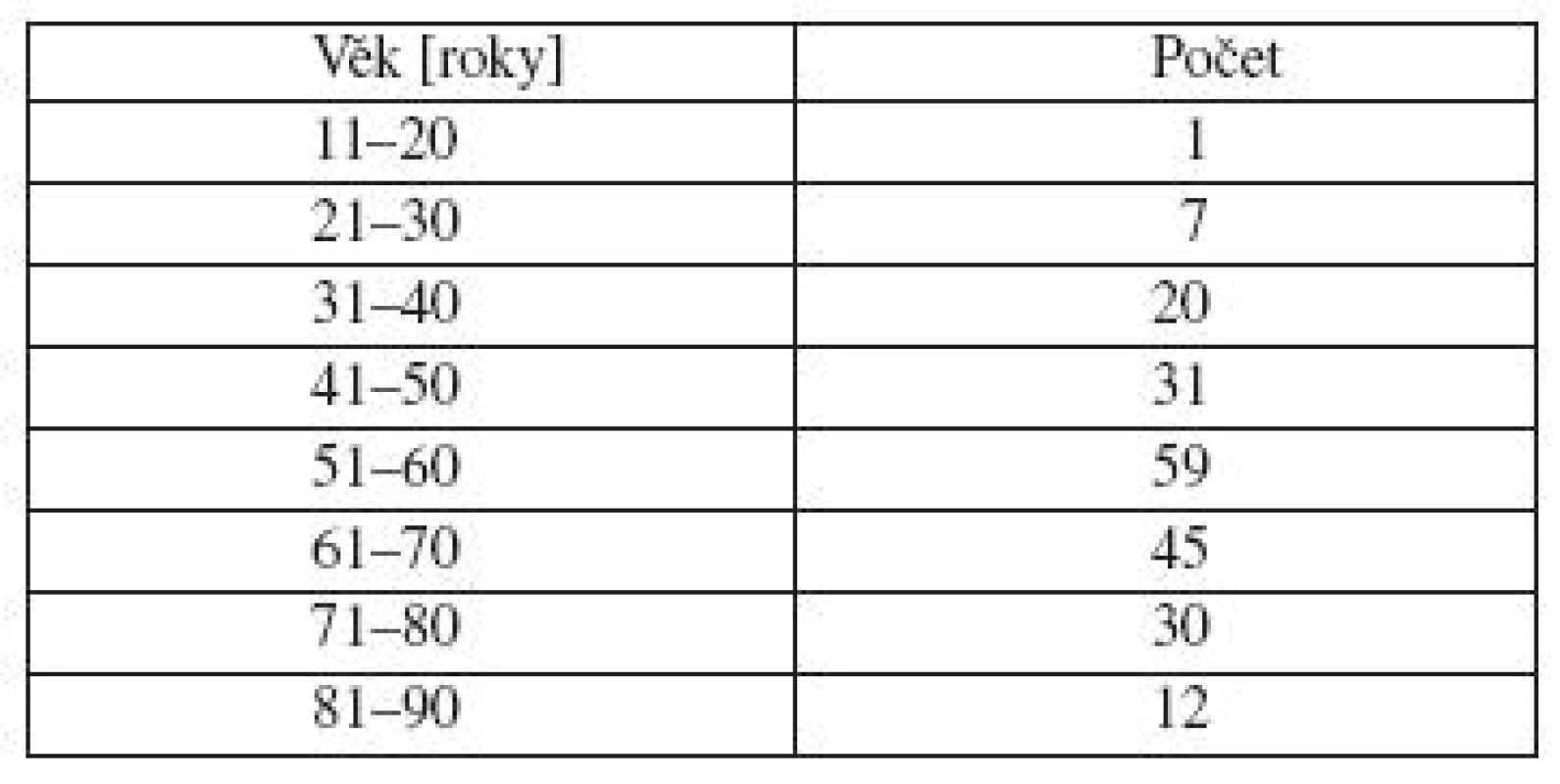
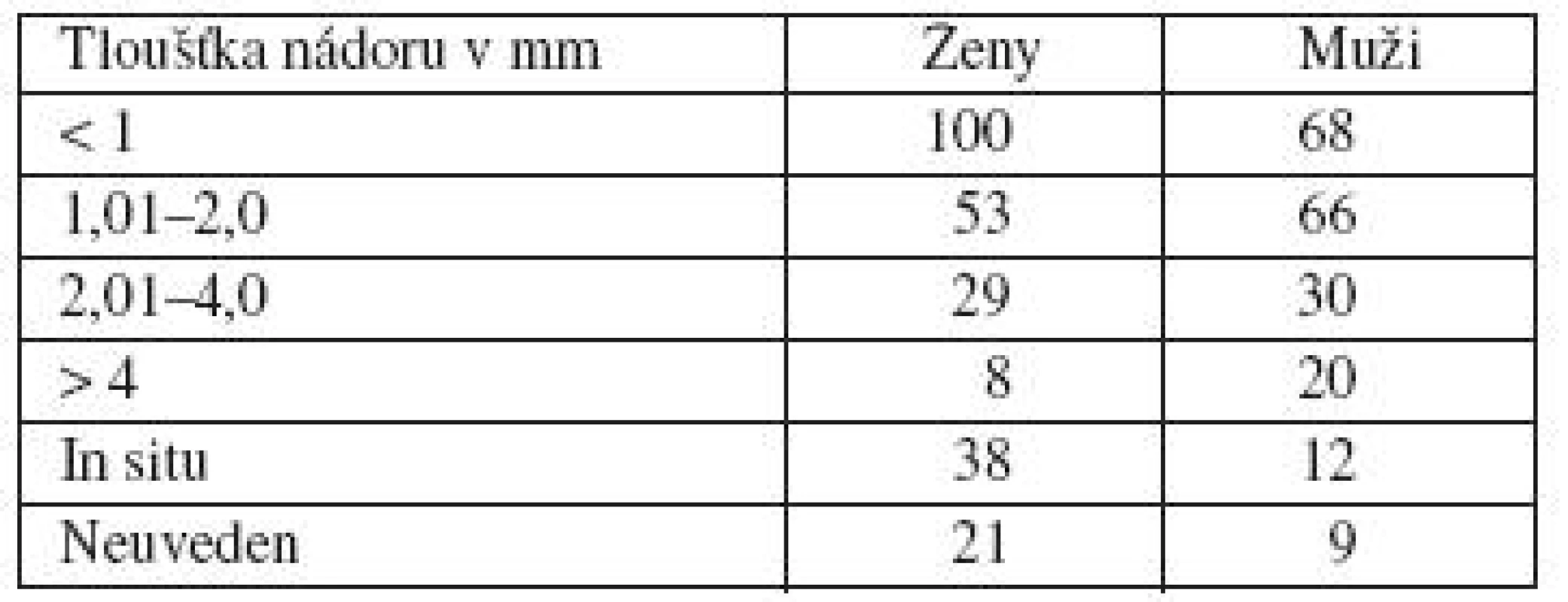
Analyzovali jsme skupinu 454 pacientů, kteří docházeli na kontroly v roce 2009. Jednalo se o 249 žen a 205 mužů. Lokalizace melanomu byla u žen nejčastěji na končetinách, více na dolních. U mužů byla nejčastějším místem výskytu záda (tab. 1). Nejvíce žen bylo ve věku 41–60 let, nejvíce mužů ve věku 51–60 let, směrem do mladších a starších věkových skupin se počty snižují (tab. 2 a 3). Dalším sledovaným parametrem byla tloušťka nádoru v milimetrech podle Breslowa. U žen jsme zaznamenali největší počet melanomů s tloušťkou do 1 mm. U mužů byly melanomy zastoupeny přibližně stejným počtem v kategorii tloušťky do 1 mm a v kategorii tloušťky 1–2 mm (tab. 4).
V našem souboru jsme sledovali výskyt kožních i mimokožních druhých primárních nádorů. Druhý melanom se vyskytl u 24 pacientů, z toho u 11 žen a 13 mužů. Nižší hodnota podle Breslowa druhého melanomu byla zjištěna v 8 případech u žen a 12krát u mužů. Bazocelulární karcinom byl diagnostikován u 50 pacientů, z toho u 17 žen a 33 mužů. Z mimokožních nádorů jsme u našich pacientů odhalili karcinom mamy [7], karcinom ledviny [6], karcinom střev [3], karcinom prostaty [2], chronickou lymfatickou leukémii [1], karcinom močového měchýře [1], karcinom dělohy [1], karcinom žaludku [1] a seminom [1].
Metastázy melanomu jsme odhalili u 16 žen a 19 mužů. V souboru žen klasifikaci podle Breslowa primárního melanomu ukazuje tabulka 5. Lokalizace byla častější na končetinách (horní končetiny 4krát, dolní končetiny 5krát) než na trupu (hlava 3krát, záda 3krát, břicho 1krát). Doba od excize melanomu do vzniku metastázy byla do 1 roku v 5 případech, od 2 do 5 let ve 3, od 5 do 10 let v 5 a nad 10 let ve 2 případech. U 8 pacientů se jednalo o metastázy kožní, v 7 případech metastázy do regionálních lymfatických uzlin a u 1 pacientky byly detekovány metastázy do pankreatu.

V souboru mužů klasifikaci podle Breslowa primárního melanomu ukazuje tabulka 6. Lokalizace byla nejčastější na trupu v 10 případech, dále na končetinách (horní končetiny 4krát, dolní končetiny 2krát), na hlavě v 1 a na krku ve 2 případech. Doba od excize do vzniku metastázy byla nejčastěji do 1 roku (9krát), do 2–5 let a 5–10 shodně u 4 pacientů, nad 10 let u 2 pacientů. U 9 nemocných se jednalo o metastázy kožní, v 6 případech o metastázy do regionálních lymfatických uzlin, 2krát byly diagnostikovány metastázy do plic a po jednom případě do sleziny a mozku.

Nejdelším intervalem od excize melanomu k detekci metastázy bylo 17 let. Žena (ročník 1955) podstoupila excizi melanomu na hrudníku v roce 1991. Histopalogická klasifikace byla SSM, Clark IV, Breslow 0,74 mm. V roce 2008, tedy po 17 letech, vznikla rezistence v blízkosti jizvy na hrudníku. Byla provedena její exstirpace s histopatologickým závěrem: intradermální metastáza melanomu. V roce 2000 a 2003 byly u této pacientky provedeny excize nehojících se ložisek charakteru bazocelulárního karcinomu na trupu. Obdobným případem byl muž (ročník 1935), který podstoupil excizi melanomu v roce 1992. Lokalizován byl na hrudníku, jednalo se o SSM, Clark IV, Breslow 1,8 mm. Po 17 letech, v roce 2009, se objevila rezistence na hrudníku, šlo o kožní metastázu.
Ne vždy se podezření na metastázu u našich pacientů prokázalo. Pacient (muž, ročník 1956) měl melanom na zádech (SSM, Clark IV, Breslow 1 mm), který byl chirurgicky odstraněn v roce 2008. Na RTG plic a následně i na CT plic byla popsána vícečetná ložiska. S podezřením na metastatický rozsev byl pacient odeslán na plicní vyšetření. Byla provedena doplňující vyšetření, včetně biopsie z ložiska se závěrem: sarkoidóza plic.
Pacient (muž, ročník 1944) s nehojícím se ložiskem na temeni hlavy podstoupil v roce 1999 chirurgickou excizi, jednalo se o lentigo maligna. Za 9 měsíců byla v rámci kontroly zjištěna recidiva v jizvě: SSM, Clark III, Breslow 1 mm. V roce 2006 byl pro nejasný nález na RTG plic odeslán na CT vyšetření, kde byla popsána ložiska suspektní z metastatického rozsevu. Na podkladě dalších vyšetření a biopsie ložiska byl diagnostikován kacinoid bronchu a pacient podstoupil plicní operaci.
DISKUSE
Frekvence výskytu druhého melanomu se udává v literatuře 0,5–5,5 % [1, 2] z celkového počtu pacientů s melanomem, respektive 1,3–8 % [4, 13] v jiných studiích. Mezi rizikové faktory vzniku vícečetných melanomů patří: pozitivní rodinná anamnéza, přítomnost mnohočetných atypických névů, vyšší hodnota hloubky invaze podle Breslowa u prvního melanomu, mužské pohlaví, jiný nádor v osobní anamnéze. V našem souboru jsme zaznamenali druhý primární melanom u 4,4 % žen a u 6,3 % mužů. Nižší hodnota Breslowa u druhého melanomu byla stanovena u 8 žen z 11 a 12 mužů ze 13. Bazocelulární karcinom, který je nejčastějším kožním nádorem a nejčastějším nádorem v populaci, jsme identifikovali u 50 pacientů (11%). Nejčastějším mimokožním nádorem byl karcinom prsu – 7 případů a karcinom ledviny – 6 případů.
Rozlišujeme metastázy regionální a vzdálené, regionální rozdělujeme dále na mikrometastázy (v bezprostředním okolí nádoru), satelitní (do 2 cm od nádoru) a intranzitní (> 2 cm) metastázy a metastázy do regionálních lymfatických uzlin. Vzdáleně může metastazovat do kteréhokoli orgánu, častěji to bývají plíce, játra, kosti, mozek [8]. V našem souboru výrazně převažovaly metastázy kožní a do regionálních lymfatických uzlin.
Rizikové faktory pro metastazující melanom jsou mužské pohlaví, starší věk, lokalizace melanomu na hlavě, krku a trupu, z histopatologických znaků primárního melanomu: vyšší tloušťka nádoru, přítomnost ulcerace, venolymfatické invaze, vyšší počet mitóz a infiltrace lymfocyty. Význačným faktorem je pozitivní sentinelová uzlina [6]. Metastázy vznikají častěji v prvních letech po odstranění melanomu, ale nejsou výjimkou metastázy po mnoha i více než 10 letech [10, 12]. U našich dvou pacientů jsme zaznamenali metastázy po 17 letech. Rozlišujeme metastázy časné (do 3 let, podle některých autorů do 5 let) a pozdní (více než 5 či 8 let). Byla vyslovena otázka, zda jsou stejné rizikové faktory pro časné a pozdní metastázy melanomu. U některých nádorů byly identifikovány signifikantní rozdíly v těchto rizikových faktorech (karcinom žaludku a jater). Počet žen s časnými a pozdními metastázami byl přibližně stejný, u mužů převažovaly metastázy časné.
U metastazujícího melanomu se 5leté přežití udává méně než 10% [8, 16]. Péči o naše pacienty s melanomem by usnadnila možnost odhadnout míru rizika vzniku metastáz, možnost odhadnout, zda bude melanom metastazovat a kam, zda se bude jednat o metastázy lokoregionální či vzdálené již v době diagnózy primárního melanomu [12]. Jako nejvýznamnější faktor pro tyto účely se zdá být tloušťka nádoru v milimetrech. Na druhou stranu je známo, že 5–25 % tenkých melanomů (< 1mm) metastazuje a naopak 25–50 % pacientů s tlustým melanomem (> 4mm) přežívá bez progrese [16].
Všichni pacienti s diagnostikovaným melanomem by měli být dispenzarizováni. Rozsah a frekvence kontrol se řídí stadiem onemocnění, délkou sledování a podléhá zvyklostem země [7, 11, 14]. Jednotné „guidelines“ v České republice pro schéma dispenzarizace neexistují, máme k dispozici evropská a americká doporučení [11, 14]. Dispenzarizace by měla být celoživotní. Cílem je včasná diagnostika recidivy a progrese onemocnění, včasná detekce prekanceróz, druhých melanomů a jiných kožních nádorů, sledování atypických névů [15]. Další součástí sledování je poskytnout psychosociální podporu pacientům, zvláště v prvním období po sdělení diagnózy, edukace pacientů o povaze onemocnění, možnostech prevence a nutnosti samovyšetřování. Nedílnou součástí dispenzarizace je vedení dokumentace o průběhu choroby a monitorování adjuvantní terapie, pokud je tato indikována [3, 5, 9]. Součástí každé dispenzární kontroly je klinické vyšetření. Pohled na indikaci laboratorních testů a přístrojových vyšetření se různí, jsou data pro provádění RTG plic a ultrasonografie břicha a spádových lymfatických uzlin a jsou data proti pravidelnému vyšetřování, zvláště s ohledem na fakt, že nemáme k dispozici účinné léčebné metody metastazujícho melanomu. Tato vyšetření se potom doporučuje provádět při symptomech.
V naší melanomové poradně sledujeme pacienty s melanomem in situ 1krát ročně klinicky. Pacienti s prognosticky příznivou hodnotou Breslowa do 1 mm jsou zváni na kontroly 1krát za 6 měsíců 10 let, provádíme laboratorní testy, RTG plic a ultrasonografii břicha 1krát za 6–12 měsíců, po deseti letech docházejí pacienti na klinické kontroly 1krát ročně. Pacienti s hodnotou Breslowa 1–4 mm jsou kontrolováni první rok po 3 měsících, po 6 měsících do 10 let, zároveň s klinickou kontrolou provádíme laboratorní testy, RTG plic, ultrasonografii břicha a spádových lymfatických uzlin. Po deseti letech je interval klinické kontroly 1krát za rok. Pacienti s vysokým rizikem (hodnota Breslowa nad 4 mm, pozitivní sentinelová uzlina) dochází na kontroly 1krát za 3 měsíce 2–3 roky, dále v 6měsíčních intervalech. Spolu s klinickou kontrolou indikujeme laboratorní a přístrojová vyšetření.
Pokud u pacienta s melanomem zjistíme orgánový ložiskový proces, vždy jako první pomýšlíme na metastázu. Ne vždy se o metastatický proces jedná, může to být nádorová duplicita či jiné onemocnění, příkladem je plicní sarkoidóza.
ZÁVĚR
Melanom je dobře detekovatelný už v časné fázi, přesto incidence melanomu v populaci stále vzrůstá a mortalita neklesá. Dopad primární prevence, zahrnující především ochranu před slunečním a arteficiálním UV zářením, se dá předpokládat až s odstupem desítek let. Úsilí je nutno napnout na včasnou detekci. Cílem je vypracovat screeningové programy, vytipovat rizikové jedince, zaměřit se na edukaci v samovyšetřování.
Do redakce došlo dne 13. 1. 2011.
Kontaktní adresa:
MUDr. Naděžda Vojáčková
Dermatovenerologická klinika
UK 2. LF a FN
Na Bulovce
Budínova 2
180 00 Praha 8
e-mail: nadavojackova@seznam.cz
Sources
1. DIFRONZO, L. A., WANEK, L. A., MORTON, D. L. Earlier diagnosis of second primary melanoma confirms the benefits of patient education and routine postoperative follow-up. Cancer, 2001, 15, p. 1520–1524.
2. DIFRONZO, L. A., WANEK, L. A., ELASHOFF, R., MORTON, D. L. Increased incidence of second primary melanoma in patients with a previous cutaneous melanoma. Ann. Surg. Oncol., 1999, 6, 7, p. 705–711.
3. DUMMER, R., HAUSCHILD, A., PENTHEROUDAKIS, G. Cutaneous malignant melanoma: ESMO Clinical, Recomendations for diagnosis, treatment and follow-up. Ann. Oncol., 2009, 20, p. 129–131.
4. FERRONE, C. L., BEN, P. L., PANAGEAS, K. S. et al. Clinicopathological features of and risk factors for multiple primary melanomas. JAMA, 2005, 294, 13, p. 1647–1654.
5. GELLER, A. C., SWETTER, S. M., BROOKS, K. et al. Screening, early detection, and trends for melanoma: Current status (2000-2006) and future directions. J. Am. Acad. Dermatol., 2007, 57, 4, p. 555–572.
6. GOLDBERG, M. S., DOUCETTE, J. T., LIM, H. W. et al. Risk factors for presumptive melanoma skin cancer screening: American Academy of Dermatology National Melanoma/Skin Cancer screening Program experience 2001–2005. J. Am. Acad. Dermatol., 57, 2007, 1, p. 60–66.
7. HENGGE, U. R., WALERAND, A., STUTZKI, A. et al. Cost-effectiveness of reduced follow-up in malignant melanoma. JDDG, 2007, 5, p. 898–907.
8. KRAJSOVÁ, I. Melanom. Maxdorf: Praha 2006, s. 336.
9. LEITER, U., GARBE, C. Epidemiology of melanoma and nonmelanoma skin cancer-the role of sunlight. Exp. Med. Biol., 2008, 624, p. 89–103.
10. LIVESTRO, D. P., KAINE, E. M., MICHAELSON, J. S. et al. Melanoma in the Young: Differences and Similarities With Adult Melanoma. Cancer, 2007, 110, 3, p. 614–624.
11. NCCN, Practise Guidelines in Oncology-v. 2. 2010, Melanoma.
12. PSATY, E. L., SCOPE, A., HALPERN, A. C. et al. Defining the patient at high risk for melanoma. Int. J. Dermat., 2010, 49, p. 362–376.
13. SAVOIA, P., QUAGLINO, P., VERRONE, A. et al. Multiple primary melanomas: analysis of 49 cases. Mel. Res., 1998, 8, 4, p. 361–366.
14. STERRY, W., GRIFFITHS, C., KORTING, H. C. et al. Guidelines for Dermatology in Europe. 2009, Berlin, ABW Wissenschaftsverlag GmbH, p. 35–52.
15. ULIASZ, A., LEBWOHL, M. Patient education and regular surveillance results in earlier diagnosis of second primary melanoma. Int. J. Dermatol., 2007, 46, p. 575–577.
16. WEINLICH, G. Metallothionein-overexpression as a prognostic marker in melanoma. G. Ital. Dermatol. Venerol., 2009, 144, p. 27–38.
Labels
Dermatology & STDs Paediatric dermatology & STDsArticle was published in
Czech-Slovak Dermatology

2011 Issue 3
Most read in this issue
- Pityriasis rubra pilaris
- Miliaria pustulosa
- Význam diagnostické hypoalergenní diety u pacientů s atopickým ekzémem
- Dispenzarizace pacientů s maligním melanomem