ICON – souhrn nejnovějších doporučení v managementu průduškového astmatu u dětí
ICON – a summary of the latest recommendations for management of bronchial asthma in children
Bronchial asthma is the leading chronic lower respiratory tract disease in children. Major advances were made in understanding its pathophysiology and pathogenesis as well as in asthma therapy. Nevertheless, the disease remains poorly controlled in significant proportion of patients. In the past years several national and international documents focused on childhood asthma were published. The focus is on implementing the latest advances into clinical practice.
The ICON (International Consensus ON pediatric asthma) document, published in 2012, is a collaborative work of leading pediatric allergists and pulmonologists. Its aim is to compare existing recommendations and unify their conclusions. Main topics of the ICON document are reviewed in this article.
Key words:
bronchial asthma, asthma phenotypes, children, diagnosis, therapy
Authors:
L. Hoňková; K. Beránková; P. Pohunek
Authors‘ workplace:
Pediatrická klinika UK 2. LF a FN Motol, Praha
přednosta prof. MUDr. J. Lebl, CSc.
Published in:
Čes-slov Pediat 2014; 69 (1): 21-28.
Category:
Reviews
Overview
Průduškové astma je chronické onemocnění dýchacích cest s vysokou prevalencí v dětské populaci. I přes výrazný posun v pochopení patofyziologie a patogeneze astmatu a přes rozvoj nových možností léčby přetrvává celosvětově významný podíl pacientů, u kterých není astma dlouhodobě pod kontrolou. V posledních letech bylo publikováno několik národních a mezinárodních dokumentů, které se zaměřují výhradně na problematiku astmatu v dětském věku s cílem implementovat současné poznatky do každodenní praxe. Závěry jednotlivých dokumentů však nejsou zcela jednotné.
Na základě spolupráce předních světových odborníků v oboru dětské alergologie a pneumologie vznikl v roce 2012 dokument ICON (International Consensus ON pediatric asthma) s cílem porovnat dostupná doporučení a sjednotit jejich závěry. Nejdůležitější body dokumentu ICON představujeme v tomto přehledovém článku.
Klíčová slova:
průduškové astma, fenotypy astmatu, děti, diagnostika, terapie
Úvod
Průduškové astma je nejčastějším chronickým onemocněním dolních cest dýchacích u dětí v industrializovaných zemích včetně České republiky. Vzhledem k postupnému vyzrávání dýchacích cest a imunitního systému v dětském věku je astma v tomto období specifické svou etiopatogenezí a klinickým průběhem. Pro dětskou populaci proto nelze pouze převzít a aplikovat doporučení určená dospělým pacientům. Naopak je zde naléhavá potřeba diagnostických a terapeutických postupů zaměřených výhradně na problematiku této nemoci v dětské populaci. ICON (International Consensus ON pediatric asthma) [1] je souhrnný dokument publikovaný v roce 2012 v časopisu Allergy. Jeho cílem je sjednotit doposud publikovaná národní a mezinárodní doporučení zabývající se problematikou astmatu v dětství, zdůraznit klíčové informace a usnadnit tak implementaci doporučených postupů do klinické praxe.
Definice
Navzdory vysoké incidenci a prevalenci průduškového astmatu v dětském věku zůstává přesná definice onemocnění stále diskutovaným tématem. Za základní charakteristiky jsou pokládány chronický zánětlivý proces, bronchiální hyperreaktivita a typická klinická symptomatologie. Vzájemný vztah mezi jednotlivými složkami a příčinná souslednost jevů nejsou v současné době jednoznačně ustanoveny.
|
Astma je chronické zánětlivé onemocnění spojené s variabilní obstrukcí a bronchiální hyperreaktivitou. Projevuje se rekurentními epizodami pískotů, kašle, dušnosti a tlaku na hrudi. |
Klasifikace
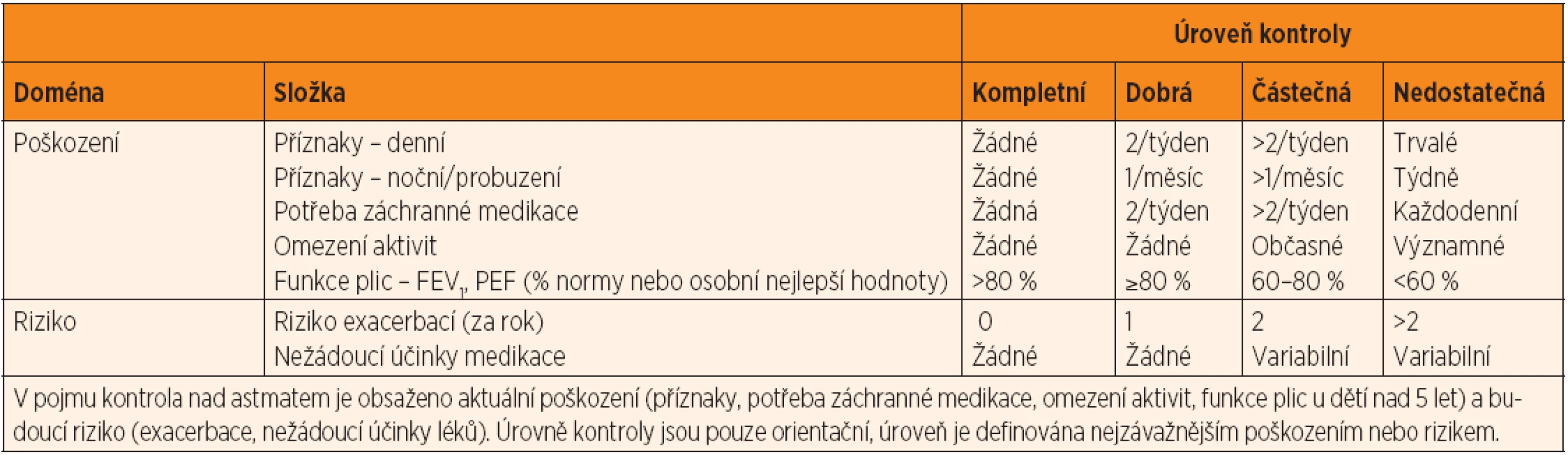
Otázka klasifikace astmatu v dětství není v současné době jednotná. Jednotlivá doporučení upřednostňují různé klasifikační faktory. Společným prvkem, zdůrazňovaným ve všech porovnávaných dokumentech, je věk pacienta. Vzhledem k charakteristikám dětského věku jsou jako hlavní milníky vnímány věk 5 a 12 let. Některé dokumenty navíc zdůrazňují potřebu rozlišovat tzv. infantilní astma u dětí do 2, resp. 3 let věku, pro které je typický tzv. recurrent wheezing. Mezi méně konzistentní faktory, které hrály významnou úlohu v klasifikaci astmatu zejména v minulosti, patří termíny tíže a perzistence onemocnění. Tyto faktory v poslední době ustupují ve prospěch dynamičtějšího a klinicky lépe využitelného konceptu kontroly nad astmatem. Předpokládá se, že do budoucna bude kladen stále větší důraz na hodnocení tzv. současného poškození a individuálního budoucího rizika [2, 3].
Stále častěji se také diskutuje o tzv. fenotypizaci onemocnění zejména na podkladě různých spouštěčů klinických symptomů (virové, ponámahové, alergické a neobjasněné astma) [4]. Úskalím tohoto přístupu je, že v některých případech se vyskytuje více spouštěčů u jednoho pacienta a že zatím neexistují specifické biomarkery, které by umožnily jednotlivé fenotypy jednoznačně rozlišit.
Patogeneze a patofyziologie
Obecně je průduškové astma chápáno jako chronické zánětlivé onemocnění, které se projevuje histologickými a funkčními změnami bronchiální stěny, jež se souhrnně nazývají remodelace [5]. V důsledku opakovaných akutních epizod tyto změny postupně progredují a v případě, že astma není adekvátně léčeno, se mohou stát ireverzibilními. Otázka specificity těchto remodelačních změn pro průduškové astma je v současné době stále více diskutována. Předpokládá se, že obdobné změny lze sledovat i u jiných chronických respiračních zánětlivých onemocnění doprovázených bronchiální obstrukcí (např. cystická fibróza) [6]. Klinickým korelátem chronického zánětu je zužování průsvitu dýchacích cest a zvýšená reaktivita hladké svaloviny jako odpověď na různé exogenní stimuly (inhalační alergeny, virové infekce, znečištěné ovzduší, změny počasí aj.).
První příznaky onemocnění se mohou projevit v kterémkoliv věku, nejčastěji však v časném dětství [7, 8]. Etiopatogeneze onemocnění je multifaktoriální, v různé míře se uplatňují zejména genetická dispozice a exogenní vlivy prostředí. Většina současných doporučení klade důraz na primární prevenci, tedy omezení expozice možným spouštěčům a potenciátorům onemocnění. Avšak doposud jediné jednoznačně podložené doporučení se týká eliminace expozice tabákovému kouři [9]. Současně je intenzivně studována role výživy matky během gravidity, úloha vitaminu D [10], nebo možnost využití modulátorů imunitní odpovědi (např. bakteriálních produktů), s cílem nasměrovat imunitní odpověď z proalergenní s převahou Th2 lymfocytů ve prospěch imunitní reakce zprostředkované cestou Th1 buněk.
Diagnostika
V rámci diagnostického přístupu k dítěti s podezřením na průduškové astma (tab. 1) je velmi důležitým hlediskem jeho věk. Cílem vyšetřovacích postupů je stanovit správnou diagnózu co nejdříve. Je potvrzeno, že první remodelační změny vznikají u malých astmatiků již velmi brzy. Možnost včasného terapeutického zásahu a prevence rozvoje remodelačních změn je v současnosti velmi diskutována. Hlavním diagnostickým vodítkem u malých dětí [11] zůstávají typické klinické projevy – epizody opakovaných pískotů, suchý kašel a dušnost. Arbitrárně je pro rozlišení „obstrukční bronchitidy“ od potenciálního průduškového astmatu stanoven počet 3 a více uvedených epizod. Současně se významně uplatňuje i hodnocení osobní a rodinné anamnézy, jejichž aspekty spolu s dalšími faktory hodnotí tzv. asthma predictive index (API) [12]. V případě pozitivity API při počtu tří a více epizod pískotů je diagnóza průduškového astmatu velmi pravděpodobná a doporučuje se s přihlédnutím ke klinickému kontextu zahájení preventivních léčebných opatření. Vždy je však nutné pamatovat, že astmatické symptomy nejsou patognomické a je tedy nutné vyloučit i jiná onemocnění, zejména není-li efekt preventivních a terapeutických opatření dostatečný (tab. 2).
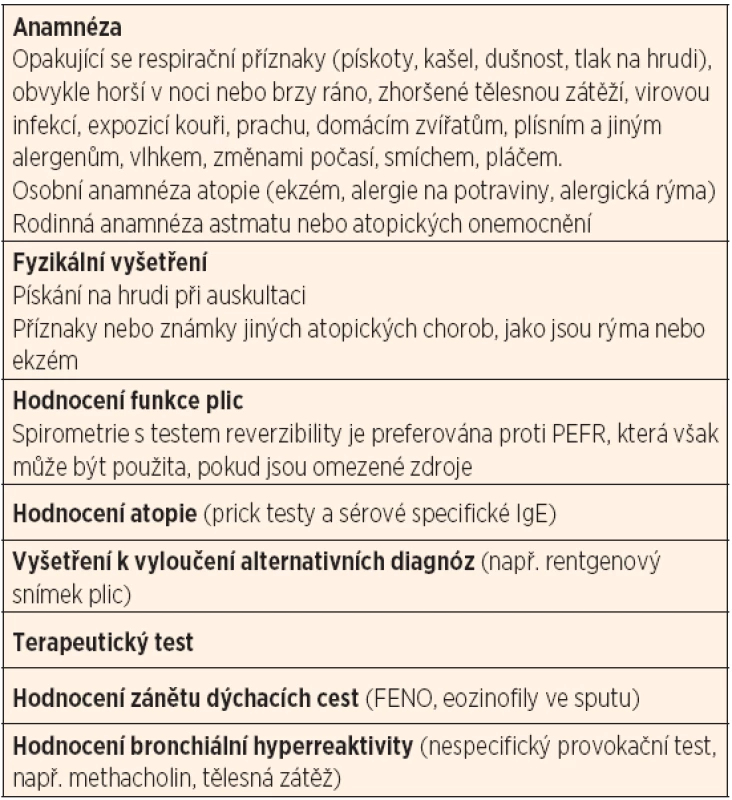
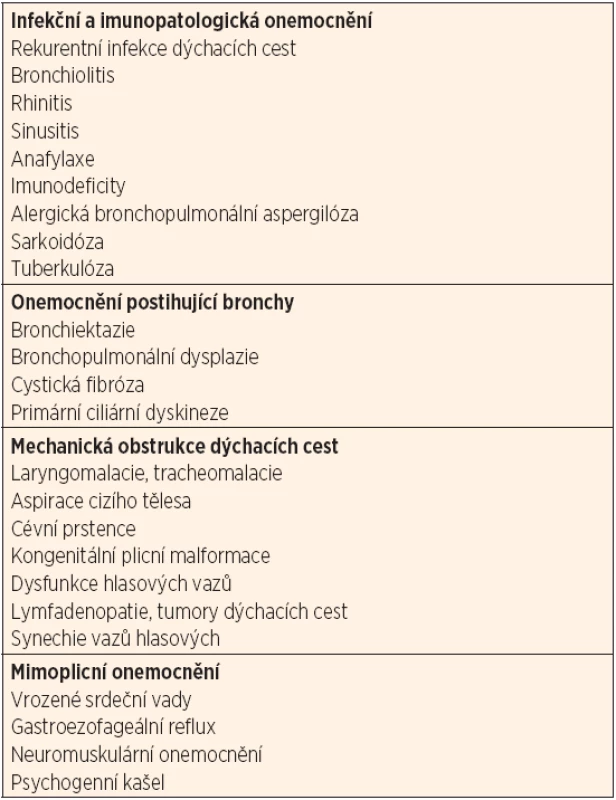
U dětí ve věku od 5 let (v praxi 3–7 let) je v rámci diagnostiky a dalšího monitorování onemocnění velmi důležité vyšetření funkce plic. Vždy je nutné pamatovat, že normální funkce plic nevylučuje diagnózu astmatu. U mladších dětí je možné využít metod, které nevyžadují spolupráci dítěte – impulzní oscilometrie, pletyzmografické vyšetření specifické rezistence dýchacích cest či vyšetření usilovného výdechu rychlou thorakoabdominální kompresí. Mimo specializovaná centra nejsou tato vyšetření v České republice dostupná. Vyšetření bronchiální reaktivity je v dětském věku přijímáno s daleko větší opatrností než u dospělých pacientů. V současné době nejsou ustanoveny přesné standardy pro různé věkové skupiny. Přesnost měření je rovněž ovlivněna podanou inhalační dávkou, která je u všech pacientů stejná a není tak přizpůsobena velikosti pacienta. Provedení i interpretace takového testu patří vždy do rukou zkušeného odborníka. Ačkoliv většina současných doporučení neklade důraz na vyšetření oxidu dusnatého ve vydechovaném vzduchu (FENO), mohlo by se v budoucnu stát důležitou metodou i v časném dětském věku [13]. Výsledek umožňuje předpovídat efekt preventivní terapie inhalačními kortikosteroidy a monitorovat spolupráci pacienta. Hodnocení atopie patří k základním vyšetřením u dětí s podezřením na průduškové astma. Lze využívat obě metody testování – in vivo (skin prick test) a in vitro (specifické IgE protilátky v krvi). Tato vyšetření napomáhají identifikovat rizikové alergeny i možné specifické spouštěče akutní dušnosti, jejichž expozici lze v některých případech účinně eliminovat.
Léčba
Primárním předpokladem úspěšné léčby astmatu v dětském věku je, stejně jako u mnoha dalších chronických onemocnění, důkladné poučení pacienta a jeho rodiny. Edukace není chápána pouze jako jednorázová intervence, ale jako pravidelná součást každé kontroly. Opakovaně by mělo být zdůrazňováno, že se jedná o chronické onemocnění, které vyžaduje kontinuální terapii i v době, kdy pacient nemá žádné klinické obtíže.
Základem přístupu by měl být konzistentní terapeutický plán, v ideálním případě sepsaný a individuálně vedený ve spolupráci s pacientem a/nebo jeho rodiči. Uvedena by měla být nejen pravidelná medikace, ale také přesná doporučení, která umožní včasnou identifikaci klinických příznaků akutní exacerbace a doporučí postup při jejím rozvoji. S přihlédnutím k věku a vyspělosti dítěte je pak velmi důležité postupné převádění kompetencí z pečujících osob na samotného pacienta.
Nezbytnou součástí základního managementu onemocnění je identifikace specifických i nespecifických spouštěčů onemocnění. Všeobecně je kladen největší důraz na eliminaci aktivního a pasivního kouření. Rozsah a benefit dalších specifických opatření, především eliminace alergenů, je stále předmětem diskusí.
Významným a často opomíjeným rizikovým faktorem je i obezita. Pacient by měl být poučen o správné životosprávě s důrazem na pravidelnou fyzickou aktivitu.
Farmakoterapie zůstává nejdůležitější součástí léčby astmatu. Jejím cílem je redukce klinických projevů onemocnění a minimalizace rizika dlouhodobého poškození (tab. 3). Tradičně se dělí na dlouhodobou preventivní léčbu a léčbu akutních exacerbací.
Dlouhodobá preventivní léčba
Inhalační kortikosteroidy (IKS) zůstávají lékem volby v rámci dlouhodobé prevence průduškového astmatu (tab. 4). Cílem léčebné strategie je minimalizace udržovací dávky IKS a redukce možných nežádoucích účinků léčby. Nedaří-li se udržet onemocnění pod kontrolou v průběhu 1–3 měsíců od zahájení terapie, je nutné zhodnotit faktory, které mohou vést k selhání léčby (např. nespolupráce pacienta, nesprávný způsob aplikace, nedodržení režimových opatření) a zvážit správnost diagnózy. Teprve pak lze navýšit dávkování. Naopak je-li pacient na zavedené léčbě bez obtíží déle než 3 měsíce, lze zahájit postupné snižování terapie až na nejmenší účinnou dávku. Při snižování terapie se v žádném případě nemají přijímat kompromisy (např. omezení tělesné aktivity) – uplatňuje se koncept kontroly s plnou kvalitou života. U většiny pacientů se daří udržet onemocnění pod kontrolou pomocí nízkých nebo nejvýše středních dávek IKS. Účinnost nízkých dávek IKS u malých dětí jako prevence intermitentních a viry indukovaných pískotů je limitovaná [14] a smysl takového postupu zůstává nadále kontroverzní.
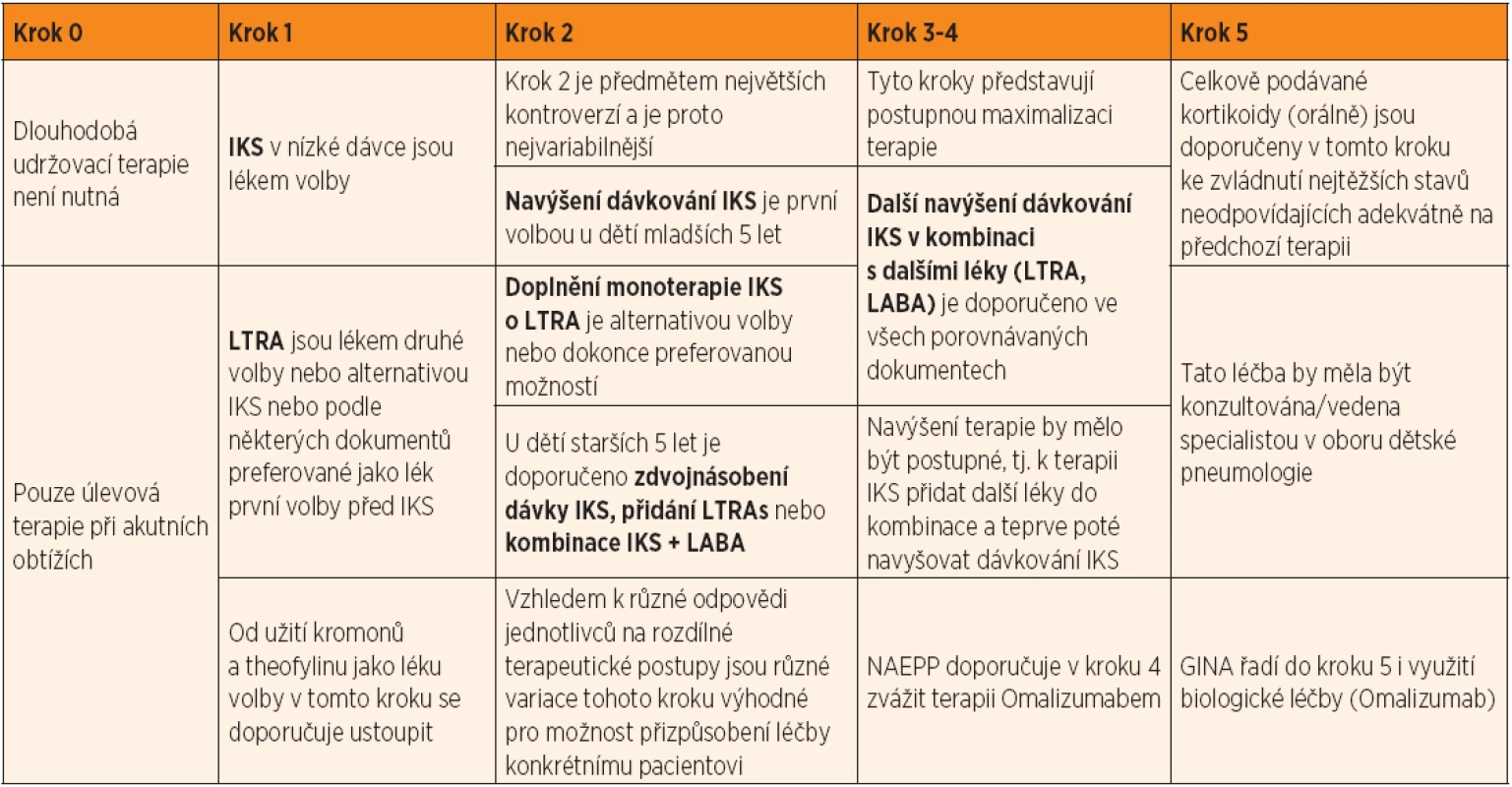
Antagonisté leukotrienových receptorů (LTRA) jsou podle většiny porovnávaných dokumentů doporučovány jako lék druhé volby, vhodný pro všechny věkové skupiny [15]. Jsou všeobecně vnímány jako méně účinné než IKS, ačkoliv některé studie ukazují srovnatelný efekt. To může být dáno i jednodušší formou jejich aplikace [16]. Existují studie vypovídající o lepší účinnosti LTRA u ponámahového astmatu [17].
Dlouhodobě působící beta-2 adrenergní agonisté (LABA) by měly být předepisovány pouze v kombinaci s IKS, jako samostatná léčebná modalita nejsou v dětském věku doporučovány [18, 19]. Většina dokumentů řadí kombinovanou léčbu IKS-LABA do svých doporučení až od věku 5 let.
Kromony zůstávají uvedeny jako druhý krok v léčbě mírného a ponámahového astmatu. Užívání tohoto léku je však v poslední době na ústupu vzhledem k prokázané omezené účinnosti.
Podobně se v posledních letech ustupuje od užívání theofylinů s přihlédnutím k velmi úzkému terapeutickému oknu a potenciálně závažným nežádoucím účinkům.
Omalizumab, monoklonální protilátka proti IgE, je indikován u dětí s těžkým, obtížně léčitelným alergickým astmatem, u nichž se i přes výbornou spolupráci a po maximalizaci terapie nedaří udržet onemocnění pod kontrolou. V současné době je k dispozici pro děti ve věku od šesti let. Léčba probíhá pouze ve specializovaných centrech.
Léčba akutní exacerbace
V současné době nejsou stanovena přesná kritéria akutní exacerbace, která by jasně odlišila akutní zhoršení od dlouhodobě nedostatečné kontroly nad onemocněním. V popisné definici je zdůrazněno zhoršení klinických symptomů spojené s objektivním nálezem poklesu funkce plic.
|
Akutní exacerbace astmatu je akutní či subakutní epizoda progresivního nárůstu astmatických obtíží, které jsou doprovázeny nálezem obstrukce při vyšetření funkce plic. |
Exacerbace je klasifikována podle závažnosti do 3 až 4 stupňů (mírná – středně těžká – těžká – život ohrožující) (tab. 5).
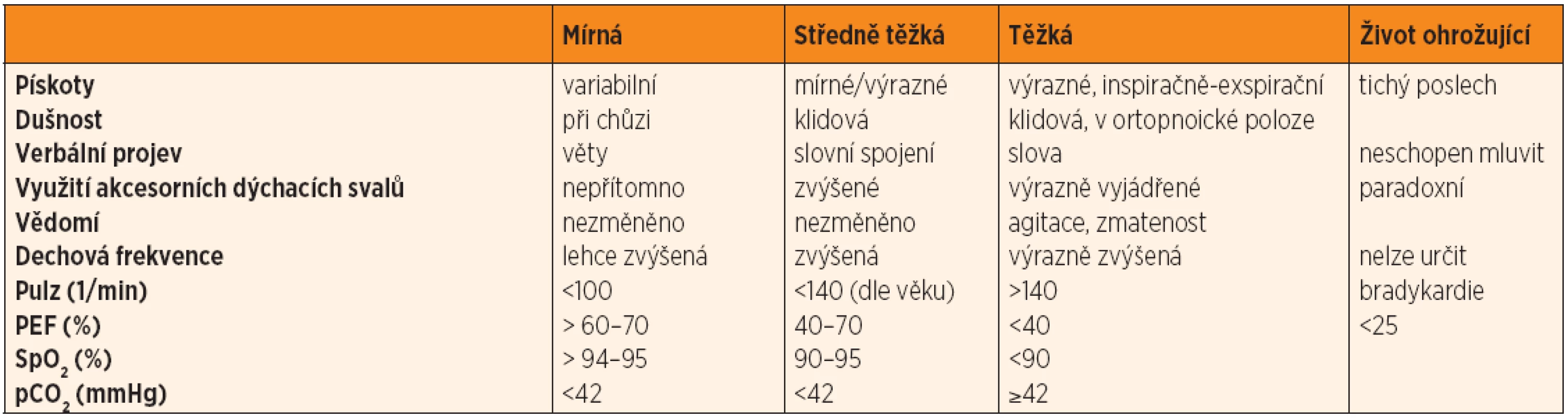
Základním lékem v managementu akutní exacerbace jsou inhalačně podávané krátkodobě působící beta-2 agonisté (SABA) (tab. 6). Léčba se zahajuje již v domácím prostředí podáváním salbutamolu v dávce 2–10 aplikací každých 20 minut během první hodiny. Následně je zhodnocen efekt a v případě nedostatečné úpravy klinických symptomů je nutné vyhledat lékařskou pomoc a případně indikovat další terapii za hospitalizace. Perorální podávání SABA se všeobecně nedoporučuje. Lékem druhé volby, který může vést k dalšímu zlepšení klinických symptomů, jsou inhalační anticholinergika (ipratropium bromid).

Systémové kortikosteroidy, přednostně v perorální formě, mají nejvyšší účinnost, pokud se jejich podávání zahájí časně po rozvoji obtíží. Doporučená dávka je 1–2 mg/kg/den prednisonu po dobu 3–5 dnů. Inhalační kortikoidy mohou být preventivně navýšeny po dobu probíhajícího akutního infektu, klinický efekt tohoto postupu nicméně nebyl dostatečně podložen [20].
Závěr
Vzhledem k vysoké prevalenci astmatu se s tímto onemocněním setkává většina lékařů během své každodenní praxe. I přes četná souhrnná doporučení zůstává významná část pacientů, u nichž nejsou klinické symptomy pod optimální kontrolou. Příčiny mohou vyplývat z nejednotnosti publikovaných postupů a nedostatečné informovanosti o možných praktických aspektech selhání léčby, které vyplývají zejména z předpokladu dokonalé spolupráce mnoha odborníků a ideální compliance ze strany pacienta a rodiny.
ICON je prvním mezinárodním dokumentem, který se zaměřil na porovnání dostupných dokumentů s cílem vytvořit přehledný článek zdůrazňující specifické aspekty průduškového astmatu v dětském věku, vyzdvihující možné příčiny selhání diagnostických a léčebných postupů s přihlédnutím k věku pacienta. Zvláštní důraz klade na důsledné a opakované informování rodiny a pacienta o charakteru onemocnění. ICON se snaží o individualizaci přístupu nejen s ohledem na vyzrálost pacienta, ale i charakter a zázemí rodiny, což jsou nezbytné předpoklady ke správnému vedení léčby. ICON zcela nově zavedl pojem kontroly s plnou kvalitou života, ta by měla být hlavním cílem péče o pacienta s diagnózou průduškového astmatu.
Grantové podpory: GAUK 360213, IGA MZ NT/ 11444.
Došlo: 16. 5. 2013
Přijato: 30. 8. 2013
MUDr. Lenka Hoňková
Pediatrická klinika UK 2. LF
FN Motol
V Úvalu 84
150 06 Praha 5
e-mail: lenka.honek@gmail.com
Sources
1. Papadopoulos NG, Arakawa H, Carlsen KH, et al. International Consensus ON (ICON) Pediatric Asthma. Allergy 2012; 67 : 976–997.
2. Global Strategy for Asthma Management and Prevention. The Global Initiative for Asthma, 2011; http://www.ginasthma.org/ uploads/users/fi les/GINA_Report2011_May4.pdf.
3. Expert Panel Report 3: Guidelines for the Diagnosis and Management Asthma. National Hearth, Lung, and Blood Institute (US), Bethesda, 2007. http://www.nhlbi.nih.gov/guidelines/ asthma/asthgdln.pdf.
4. Bacharier LB, Boner A, Carlsen KH, et al. Diagnosis and treatment of asthma in childhood: a PRACTALL Consensus Report. Allergy 2008; 63 : 5–34.
5. Bossé Y, Paré PD, Seow CY. Airway wall remodeling in asthma: from the epithelial layer to the adventitia. Current Allergy and Asthma Reports 2008; 8 : 357–366.
6. Regamey N, Jeffery PK, Alton EWFW, et al. Airway remodelling and its relationship to inflammation in cystic fibrosis. Thorax 2010; 66 : 624–629.
7. Pohunek P, Warner JO, Turzíková J, et al. Markers of eosinophilic inflammation and tissue remodelling in children before clinically diagnosed bronchial asthma. Pediatr Allergy Immunol 2005; 16 : 43–51.
8. Saglani S, Payne DN, Zhu J, et al. Early detection of airway wall remodeling and eosinophilic inflammation in preschool wheezers. Am J Respir Crit Care Med 2007; 176 : 858–864.
9. Gilliland DF, Yu-Fen L, Peters MJ. Effects of maternal smoking during pregnancy and environmental tobacco smoke on asthma and wheezing in children. Am J Respir Crit Care Med 2001; 163 : 429–436.
10. Bozzetto S, Carraro S, Giordano G, et al. Asthma, allergy and respiratory infections: the vitamin D hypothesis. Allergy 2012; 67 : 10–17.
11. Global Strategy for the Diagnosis and Management of Asthma in Children 5 Years and Younger. The Global Initiative for Asthma, 2009; http://www.ginasthma.org/uploads/users/fi les/ GINA Under5 2009 CorxAug11.pdf.
12. Castro-Rodríguez JA, Holberg CJ, Wright AL, et al. A clinical index to define risk of asthma in young children with recurrent wheezing. Am J Respir Crit Care Med 2000; 162 : 1403–1406.
13. Dweik RA, Boggs PB, Erzurum SC, et al. An official ATS clinical practice guideline: Interpretation of Exhaled Nitric Oxide Levels (FENO) for Clinical Applications. Am J Respir Crit Care Med 2011; 184 : 602–615.
14. McKean M, Ducharme F. Inhaled steroids for epizodic viral wheeze of childhood. Cochrane Database Syst Rev 2000;(2):CD001107.
15. Lipworth BJ. Leukotriene – receptor antagonists. Lancet 1999; 353 : 57–62.
16. Scaparrotta A, Di Pillo S, Attanasi M, et al. Montelukast versus inhaled corticosteroids in the management of pediatric mild persistent asthma. Multidiscip Respir Med 2012; 7 : 13.
17. Stelmach I, Grzelewski T, Majak P, et al. Effect of different antiasthmatic treatments on exercise-induced bronchoconstriction in children with asthma. J Allergy Clin Immunol 2008; 121 : 383–389.
18. Nelson HS, Weiss ST, Bleecker ER, et al. The Salmeterol Multicenter Asthma Research Trial: a comparison of usual pharmacotherapy for asthma or usual pharmacotherapy plus salmeterol. Chest 2006; 129 : 15–26.
19. Salpeter SR, Buckley NS, Ormiston TM, et al. Meta-analysis: Effect of Long-Acting Beta-Agonists on Severe Asthma Exacerbations and Asthma-Related Deaths. Ann Intern Med 2006; 144 : 904–912.
20. Ducharme FM, Lemire C, Noya FJ, et al. Preemptive use of high-dose fluticasone for virus-induced wheezing in young children. N Engl J Med 2009; 360 : 339–353.
Labels
Neonatology Paediatrics General practitioner for children and adolescentsArticle was published in
Czech-Slovak Pediatrics

2014 Issue 1
- What Effect Can Be Expected from Limosilactobacillus reuteri in Mucositis and Peri-Implantitis?
- The Importance of Limosilactobacillus reuteri in Administration to Diabetics with Gingivitis
-
All articles in this issue
- Tranzitorní pseudohypoaldosteronismus – nefro-urologické „puzzle“
- Adipsický diabetes insipidus u pacienta s dysgenézou corpus callosum
- Péče o předčasně narozené dítě: Kdy začíná a kdy končí?
- ICON – souhrn nejnovějších doporučení v managementu průduškového astmatu u dětí
- Kryptorchizmus – potreba včasnej diagnostiky a liečby
- Vědecké důkazy o prospěšnosti výživy mateřským mlékem
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Kryptorchizmus – potreba včasnej diagnostiky a liečby
- Tranzitorní pseudohypoaldosteronismus – nefro-urologické „puzzle“
- Péče o předčasně narozené dítě: Kdy začíná a kdy končí?
- Adipsický diabetes insipidus u pacienta s dysgenézou corpus callosum
