Efficacy and safety of extracorporeal shock wave lithotripsy in the 21th century – controversy and clinical practice.
Efficacy and safety of extracorporeal shock wave lithotripsy in the 21th century – controversy and clinical practice.
Objective:
Evaluation of extracorporeal shock wave lithotripsy efficacy and safety in a prospectively followed group of patients treated by this procedure. Determination of the factors that may affect efficacy of the procedure and analysis of the possible risk factors for the development of renal parenchymal damage due to the use of shock wave.
Methods:
We assessed 301 extracorporeal shock wave lithotripsy procedures performed in 250 patients from December 2012 to October 2015. All procedures were performed under analgosedation with the use of the electromagnetic source EMSE 140f machine Dornier Compact Sigma on the basis of the standardized protocol which was determined before the study. This protocol took into account the size and the localization of the stones. Efficacy quotient (EQ) and stone free rate (SFR) were used in order to evaluate the procedure effectiveness. The relationship between the procedure efficacy and body mass index (BMI), the lithiasis size and the location and the overall energy dose applied (Edose) was analysed. For the purpose of the procedure safety evaluation ultrasound examination aiming at the presence of subcapsular or perirenal haematoma were performed after each procedure. Positive findings were subsequently verified by spiral CT examination. We tried to analyse the possible risk factors for the development of renal parenchymal injury after the use of shock waves.
Results:
Ultrasound, native nephrogram or CT was performed three months after the procedure to assess the treatment results. SFR and EQ were achieved in 78.6 % and 56.6 % of our patients respectively. Development of the renal hematoma was detected in 11 patients (4.5 %), from this group three patients had symptomatic hematoma (1.23 %). The patients with ureterolithiasis were excluded from the procedure safety evaluation as the shock wave trajectory in these patients makes the risk of renal injury quite improbable. BMI and Edose proved to have influence on the efficacy and safety of the procedure in our study. The same applies for previous renal infection and urinary tract stenting.
Conclusion:
We demonstrated good efficacy of ESWL (extracorporeal shock wave lithotripsy) and at the same time we confirmed the assumption that the incidence of kidney damage is higher than it was supposed in the past. The overall energy dose applied is essential for the efficacy and safety of the procedure. Due to the absence of any general guidelines we consider important that every department monitors their own results and to optimize the energy dose for every particular lithotriptor. We further recommend introduction of an efficacy safety quotient (ESQ) and close monitoring of the factors influencing the efficacy and safety of the procedure. Therapeutic approach towards the peripheral lithiasis and lower pole calyx peripheral lithiasis in particular remains challenging and problematic.
KEY WORDS:
Extracorporeal shock wave lithotripsy, stone free rate, efficacy quotient, energy dose, efficacy safety quotient.
Authors:
Vít Paldus 1; Vladimír Šámal 1,2; Jan Mečl 1; Jan Fogl 1; Gabriela Čečerle 1; Jiří Pírek 1
Authors‘ workplace:
Urologické oddělení Krajské nemocnice Liberec, a. s.
1; Urologická klinika Fakultní nemocnice a Lékařské fakulty UK, Hradec Králové
2
Published in:
Ces Urol 2017; 21(2): 161-171
Category:
Original Articles
Overview
Cíl:
Zhodnocení účinnosti a bezpečnosti extrakorporální litotrypse v prospektivně sledovaném souboru pacientů léčených tímto přístupem. Stanovení faktorů, které můžou ovlivnit účinnost postupu a analýza možných rizikových faktorů pro rozvoj poškození renálního parenchymu v důsledku užití rázové vlny.
Metodika:
V období od prosince 2012 do října 2015 jsme zhodnotili 301 výkonů extrakorporální litotrypse u celkem 250 pacientů. Výkony jsme provedli v analgosedaci pomocí elektromagnetického zdroje EMSE 140f přístroje Dornier Compact Sigma na základě předem určených aplikačních schémat, ve kterých jsme zohlednili velikost a lokalizaci litiázy. K hodnocení efektivity jsme použili koeficient účinnosti (EQ) a stone free rate (SFR). Efektivitu jsme následně posoudili ve vztahu k BMI, velikosti, lokalizaci litiázy a celkově užité energetické dávce (Edose). Po každém výkonu jsme za účelem hodnocení bezpečnosti provedli ultrazvukové vyšetření zaměřené na přítomnost subkapsulárního nebo perirenálního hematomu. Pozitivní nálezy byly následně ověřeny pomocí spirálního CT vyšetření. Pokusili jsme se analyzovat možné rizikové faktory vzniku poranění renálního parenchymu po užití rázových vln.
Výsledky:
Definitivní hodnocení výsledků jsme provedli za tři měsíce od zákroku sonograficky, pomocí nativního nefrogramu či spirálního CT. V souboru jsme zaznamenali SFR u 78,6 % pacientů, EQ dosáhl 56,6 %. Rozvoj hematomu ledviny jsme zaznamenali celkem u 11 pacientů (4,5 %), z toho u tří pacientů byl hematom symptomatický (1,23 %), z hodnocení posuzující poranění ledvin jsme vyloučili pacienty s ureterolitiázou, kde bylo poranění ledviny s ohledem na trajektorii rázové vlny nepravděpodobné. BMI a celkově užitá energetická dávka (Edose) měli v naší studii vliv na výslednou efektivitu i bezpečnost výkonu. Předchozí infekce ledvin a stenting močových cest, se zdá, mají tento vliv také.
Závěr:
Prokázali jsme dobrou efektivitu LERV (litototrypse extrakorporální rázovou vlnou) a zároveň jsme potvrdili předpoklad, že incidence poškození ledvin je vyšší než byl předpoklad v minulosti. Zásadní pro účinnost i bezpečnost je užitá energetická dávka. S ohledem na absenci jasných doporučení doporučujeme každému pracovišti sledovat své výsledky a optimalizovat energetické dávky na konkrétním přístroji. Dále doporučujeme zavedení koeficientu bezpečné účinnosti ESQ (efficaccy safety quotient) a nadále analyzovat faktory ovlivňující jak efektivitu, tak bezpečnost. Zejména přístup k periferní nefrolitiáze a litiáze dolního kalichu pak zůstává problematický.
Klíčová slova:
Litotrypse extrakorporální rázovou vlnou, stone free rate, koeficient účinnosti, energetická dávka, koeficient bezpečné účinnosti.
ÚVOD
Aktuální moderní léčba urolitiázy v sobě zahrnuje komplexní přístup, kombinaci metod, snahu o definitivní řešení. Zejména zavedení flexibilních metod a mini‑invazivních přístupů vede v posledních letech k poklesu úlohy LERV. I přes tento fakt je stále více než 50 % urolitiáz řešeno tímto přístupem (1). Navíc je urolitiáza nejčastěji operačně řešenou diagnózou oboru urologie. Obecně lze přijmout realitu, že se zájem o extrakorporální litotrypsi po více než třiceti letech od sestrojení prvního přístroje přesunul spíše do řad výrobců. Produkce nových a nových generací přístrojů však nepřináší významně lepší výsledky, naopak se v klinické praxi objevuje řada nezodpovězených otázek. Obecně neexistuje žádné souhrnné srovnání mezi jednotlivými výrobci, hodnocení výsledků provádí různá klinická pracoviště na základě nejednotných metod, následně chybí standardní zpracování analýz a nezávislé instituce pro zpracování dat.
Zavedení parametrů jako stone free rate (SFR) či koeficientu účinnosti (EQ) do klinické praxe byl jen částečnou snahou, jak tento problém zlepšit. I nadále lze očekávat nejednotné postupy v hodnocení výsledků, kdy do současné doby neexistuje ani jasný konsensus na definici SFR. V metaanalýze 249 publikací bylo nalezeno hned sedm různých definic SFR (2), kdy někteří autoři klasifikovali pacienty jako „SFR“ s reziduální litiázou pod 1 mm, jiní pod 2 mm nebo pod 3 mm či 4 mm. Zároveň byly k hodnocení SFR užity různé metody jako UZ, rtg či nativní SCT. Přibližně třetina publikací zabývajících se výsledky po ošetření litiázy neposkytuje žádné informace o SFR. Zásadní také zůstává, jakou metodu jsme k dosažení SFR zvolili.
Obecně přijatelný výsledek SFR po LERV při reziduálním fragmentu <2 mm nemusí být přijatelný pro pacienty léčené metodou flexibilní ureterorenoskopie. Moderní definice se tak dnes snaží užívat nových skórovacích systémů zohledňujících nejen užité metody při odstranění litiázy, ale i zobrazovací metody užité při hodnocení SFR. Snaha porovnat efektivitu jednotlivých přístrojů pomocí parametru EQ pak není také dokonalá, kdy aktuálně máme k dispozici hned dvě rovnice dle Denstedta a Claymana (3, 4) nebo rovnici dle Rassweilera (5), která zohledňuje mimo auxiliární procedury po výkonu i procedury před výkonem.
Z fyzikálního hlediska úspěšnost fragmentace konkrementu nekoreluje s hodnotami tlaku v ohnisku (6), ale úzce koresponduje s energií rázové vlny dodávané do ohniskové zóny (7, 8, 9). Vznikla tak nová snaha a byl definován koncept energetické dávky (10). Tento koncept bohužel naráží na realitu, kdy různí výrobci užívají k hodnocení užité energetické dávky různé jednotky, mimo jouly (J) i milivolty (mV). Navíc při srovnání užitých energetických dávek jednotlivými autory se tyto hodnoty často zásadně liší (10, 11, 12, 13, 14, 15). Částečným zdůvodněním užití širokého rozsahu energetických dávek můžou být práce zabývající se vlivem couplingu na ztrátu energie během transportu rázové vlny (16, 17, 18, 19), kdy coupling obecně jako mechanické spojení zajišťuje optimální přenos rázové vlny od jejího zdroje do ohniska. Tento transport musí probíhat v prostředí s minimálními rozdíly akustické impedance, aby nedocházelo ke ztrátám energie během transportu, kdy například na rozhraní prostředí voda‑vzduch dochází ke ztrátě až 99,9 % energie rázové vlny. Jiné práce pak prokazující například negativní vliv stentingu na dezintegraci litiázy (20, 21). Přes všechny aspekty zůstávají nejednoznačně definované energetické dávky po více než 30 letech praxe extrakorporální litotrypse do jisté míry překvapením (15). Odborná doporučení guidelines EAU (22) týkající se doporučených energetických dávek pro extrakorporální litotrypsi jsou pak jen obecná a prakticky vlastní dávky neřeší.
METODIKA
V období od prosince 2012 do října 2015 jsme prospektivně zhodnotili léčbu urolitiázy u celkem 250 pacientů, u kterých jsme provedli celkem 301 výkonů extrakorporální litotrypse. Průměrný věk pacientů ve sledovaném souboru byl 58 let, mužů bylo v souboru 225 a žen pouze 76, ve 138 případech (45,8 %) jsme provedli výkon na zavedeném stentu. Periferní nefrolitiázu jsme ve sledovaném souboru řešili v 73 případech, pyelolitiázu ve 130 případech, subrenální ureterolitiázu ve 41 případech a ostatní ureterolitázu (abdominální a lumbální) v 57 případech. Ve sledovaném souboru jsme zaznamenali podváhu (BMI pod 18,5) u 0,7 % pacientů, normální váhu (BMI 18,5–24,9) u 26,2 % pacientů, nadváhu (BMI 25–29,9) u 42 % pacientů a obezitu (BMI nad 30) u 31,1 % pacientů.
Výkony jsme provedli v analgosedaci pomocí elektromagnetického zdroje EMSE 140f přístroje Dornier Compact Sigma na základě předem určených aplikačních schémat, ve kterých jsme zohlednili velikost a lokalizaci litiázy. Vždy jsme použili schéma postupného navyšovaní energetické hladiny 1–5. Během výkonu jsme užili frekvenci 60 nebo 80 rázů za minutu a coupling byl během výkonu optimálně na hodnotě 3 z možného rozsahu 0–5. Předčasný konec trypse jsme metodicky definovali jako časnou dezintegraci, kdy litiáza nebyla na skiaskopii dále patrna. Dalším důvodem předčasného ukončení výkonu byla špatná tolerance výkonu. Podmínkou provedení výkonu byla schopnost skiaskopického zaměření litiázy – fokusace, kdy jsme následně průběžně po celou dobu výkonu kontrolovali polohu konkrementu a kvalitu couplingu, aby nedocházelo ke ztrátám aplikované energie špatným přenosem či nekvalitní fokusací. Do 24 hodin po výkonu jsme vždy provedli sonografickou kontrolu a při podezření na poranění parenchymu ledviny jsme doplnili nativní CT vyšetření. Definitivní zhodnocení výsledků jsme provedli za tři měsíce od výkonu pomocí nativního nefrogramu, sonograficky nebo pomocí CT. Výpočet aplikované energetické dávky (Edose) jsme stanovili na základě konceptu energetické dávky:
Edose = n1 * Eeff1 + n2 * Eeff2 + n3 * Eeff3
V souboru jsme hodnotili efektivitu pomocí koeficientu účinnosti (EQ) a stone free rate (SFR). Efektivitu jsme následně posoudili ve vztahu k BMI, lokalizaci, velikosti litiázy a užité celkové energetické dávce (Edose). Pro výpočet EQ jsme použili rovnici dle Denstedta a Claymana:
Z hodnocení posuzující poranění ledvin jsme vyloučili pacienty s ureterolitiázou, kde bylo poranění ledviny s ohledem na trajektorii rázové vlny nepravděpodobné. Následně jsme porovnali data pacientů s poraněním parenchymu ledviny a pacientů bez poranění. Při srovnání obou skupin jsme se pokusili analyzovat možné rizikové faktory poranění ledvin. Závěrem jsme definovali zcela nový parametr, který hodnotí současně efektivitu i bezpečnost extrakorporální litotrypse. Tento parametr jsme nazvali koeficient bezpečné účinnosti – ESQ (efficaccy safety quotient) a vyjadřuje procento úspěšně vyřešených případů bez poranění ledviny.
VÝSLEDKY
V souboru 250 pacientů jsme dosáhli SFR v 78,6 %, celkem jsme provedli 301 výkonů a EQ generátoru EMSE 140f dosáhl v daném souboru 56,6 %.
V souboru 301 výkonů jsme zaznamenali výskyt hematomu ledviny v 11 případech (4,5 %), z toho u třech pacientů byl hematom symptomatický (1,23 %). Z hodnocení jsme vyřadili pacienty s ureterolitázou, kde bylo poranění ledviny s ohledem na trajektorii rázové vlny nepravděpodobné (celkem 57 případů ureterolitiázy). Poranění parenchymu ledvin jsme klasifikovali jako subkapsulární hematom grade I dle A.A.S.T. (American Association for Surgery of Trauma). Deset případů jsme řešili konzervativně a pouze v jednom případě byla nutná selektivní embolizace segmentární arterie. S odstupem jsme zhodnotili všechny případy, kdy finálně došlo ke zhojení všech nálezů.
Celkem 19 pacientů obdrželo energetickou dávku Edose nad 100 J. Z těchto 19 pacientů hned u třech pacientů došlo k poranění parenchymu ledviny a verifikaci subkapsulárního hematomu (15,8 %). Dalších 225 pacientů obdrželo dávku pod 100 J a výskyt hematomu ledviny byl v tomto souboru celkem u osmi pacientů (3,6 %) (graf 1). Dva ze tří pacientů, kteří měli symptomatický hematom ledvin, pak obdrželi dávku nad 100 J.

Jinak průměrně aplikovaná energetická dávka Edose ve skupině pacientů bez poranění parenchymu ledviny byla 73,6 J a průměrně aplikovaná dávka ve skupině pacientů s diagnostikovaným subkapsulárním hematomem ledviny byla 86,1 J (graf 2).

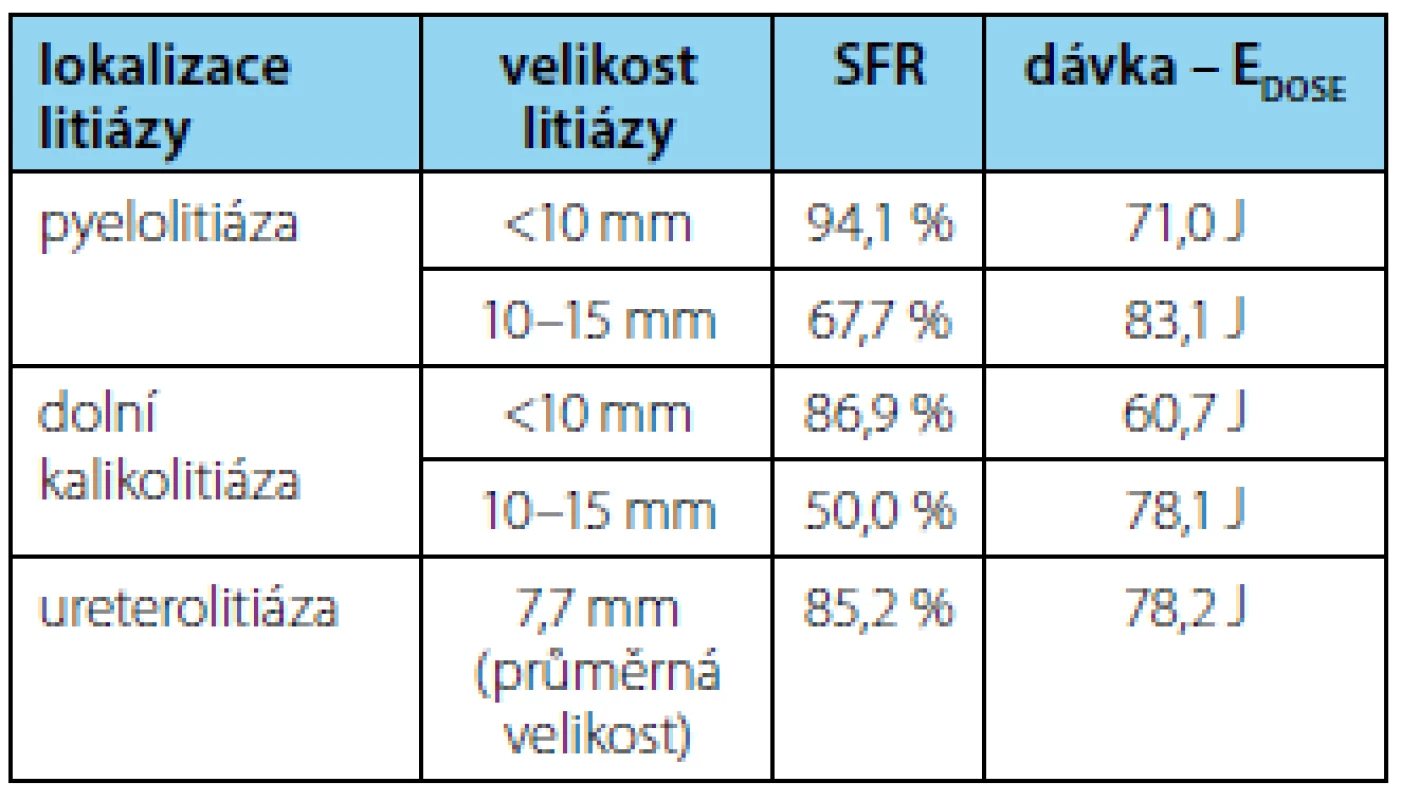
Ve sledovaném souboru jsme dále zhodnotili vztah lokalizace, velikosti litiázy a aplikované energetické dávky k dosaženému SFR. V případě pyelolitiázy do 10 mm jsme při průměrně aplikované energetické dávce 71,0 J dosáhli SFR až u 94,1 % pacientů, v případě pyelolitiázy velikosti 10–15 mm jsme i přes vyšší průměrně aplikovanou energii 83,1 J zaznamenali SFR jen u 67,7 % pacientů. V případě ureterolitiázy jsme při průměrné velikosti litiázy 7,7 mm a průměrné aplikované energetické dávce 78,2 J dosáhli SFR až u 85,2 % pacientů.
Nejnižší SFR a zároveň nejvyšší procento poranění parenchymu jsme zaznamenali při řešení litiázy dolního kalichu. Celkem jsme provedli 61 výkonů u 52 pacientů s lokalizací litiázy v dolním kalichu. Celkový SFR byl u této skupiny pacientů nižší v porovnání s celkově dosaženým SFR a dosahoval jen 71,4 %. Navíc v případě litiázy 10–15 mm jsme zaznamenali SFR jen u 50 % pacientů při průměrně aplikované energetické dávce 78,1 J. Ve skupině litiázy do 10 mm jsme pak zaznamenali SFR až 86,9 % a to jen při průměrně aplikované energetické dávce 60,7 J. Mimo užitou energetickou dávku je tak pro pasáž litiázy a dobré výsledky rozhodující i lokalizace a velikost litiázy (tabulka 1).
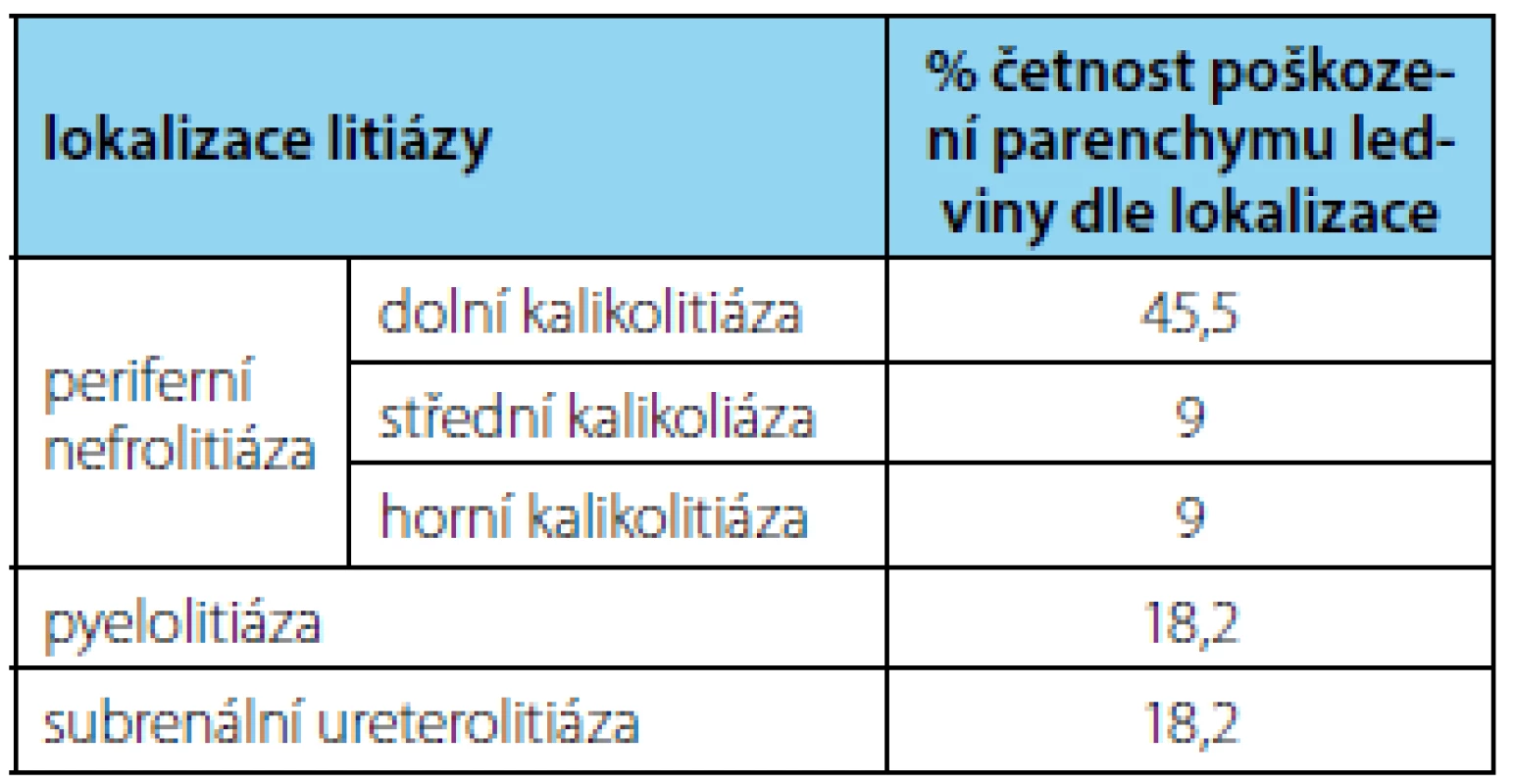
Řešení periferní litiázy pak bylo nejčastější lokalizací pro možné poranění parenchymu ledviny. V souboru 11 pacientů jsme zaznamenali rozvoj subkapsulárního hematomu ledviny hned v pěti případech při řešení litiázy dolního kalichu (45,5 %), jeden případ pak při řešení litiázy středního kalichu (9 %) a jeden při litotrypsi horního kalichu (9 %). Po dvou případech došlo k rozvoji hematomu při řešení pylelolitiázy (18,2 %) a subrenální litiázy (18,2 %) (tabulka 2). Navíc reálné zastoupení pacientů s periferní litiázou bylo v hodnoceném souboru (244 výkonů) jen 29,9 %. Četnost výskytu poranění parenchymu ledviny po extrakorporální litotrypsi periferní nefrolitiázy tak byla více než 2x vyšší než její reálné zastoupení s ohledem na lokalizaci.
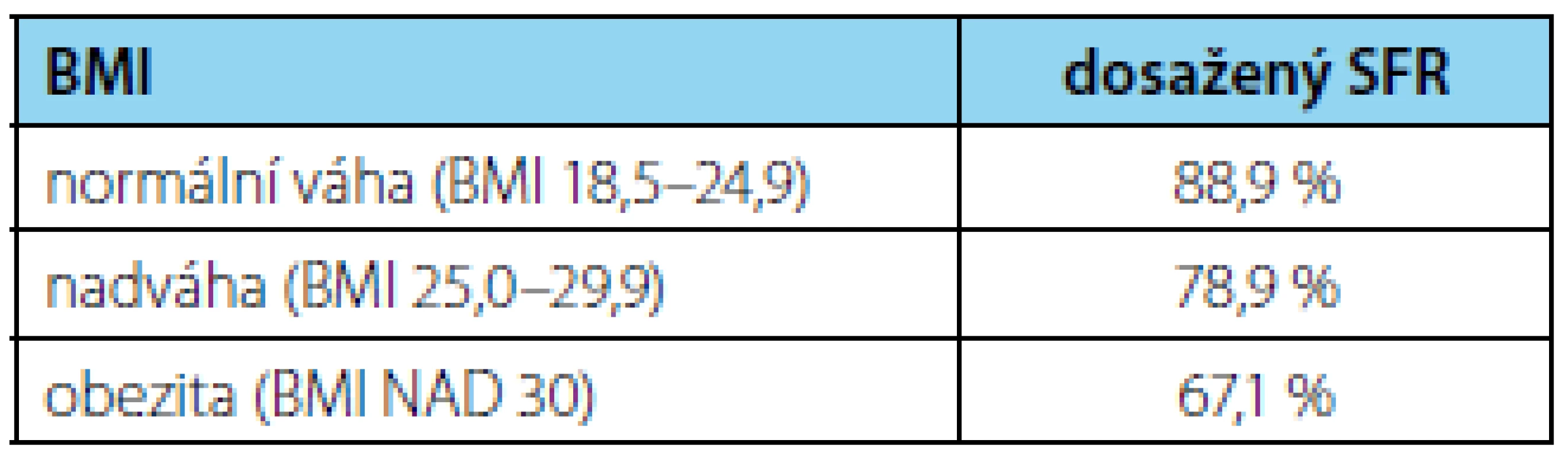
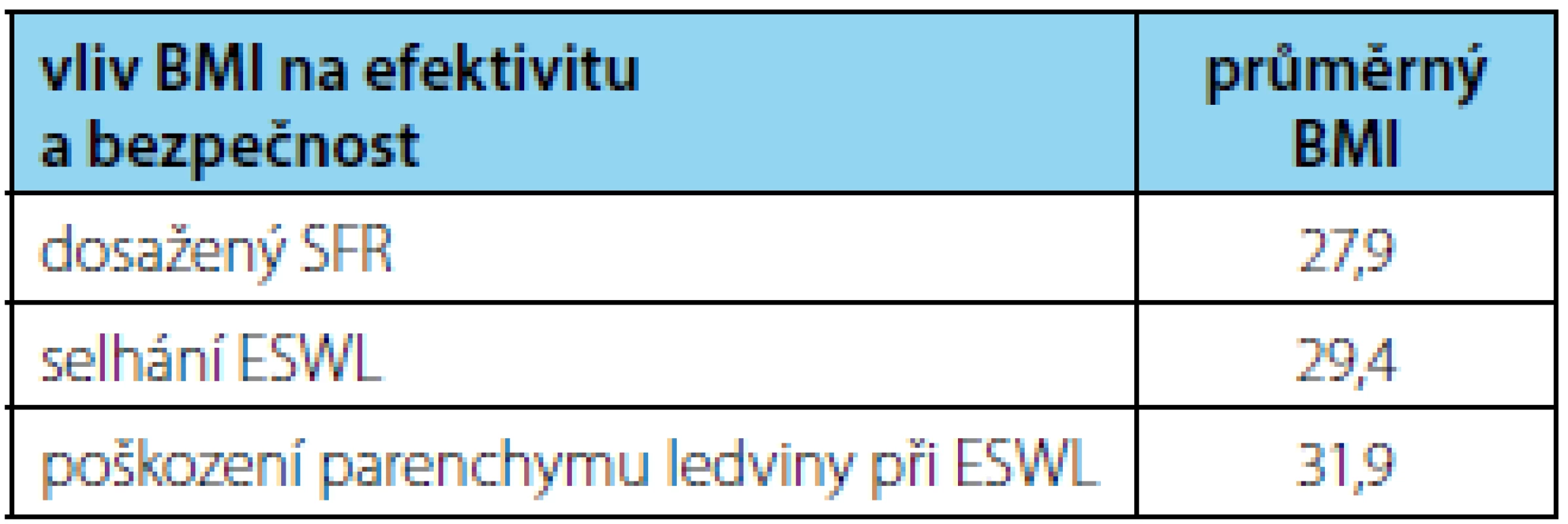
BMI ve sledovaném souboru ovlivňoval jak bezpečnost, tak efektivitu. Ve skupině pacientů s normální váhou (BMI 18,5–24,9) jsme dosáhli SFR u 88,9 % pacientů, u pacientů s nadváhou (BMI 25,0–29,9) jsme zaznamenali SFR jen v 78,9 % a u pacientů s obezitou (BMI nad 30) dokonce jen 67,1 % (tabulka 3). Průměrný BMI byl ve skupině pacientů s úspěšným SFR 27,9 oproti BMI 29,4 ve skupině pacientů, kde jsme SFR nedosáhli. Ve vztahu k bezpečnosti byl pak průměrný BMI ve skupině pacientů s poraněním ledviny nadprůměrný a dosahoval hodnoty až 31,9 (tabulka 4).
Při další analýze rizikových faktorů jsme ve sledovaném souboru zaznamenali, že 45,5 % pacientů s poraněním parenchymu ledviny mělo před výkonem anamnézu předchozího zánětu ledviny. Pacienti bez poranění parenchymu ledviny měli anamnézu předchozího zánětu jen v 11,6 % případů. Celkem devět pacientů z 11 s poraněním ledviny pak mělo zavedený stent. Jinak jsme ve sledovaném souboru nezaznamenali vliv hypertenze či předchozí anamnézy užití antiagregační terapie na rozvoj hematomu ledviny v důsledku LERV.
ESQ dosáhl v našem souboru 75,2 %.
DISKUZE
V rozvoji extrakorporální litotrypse byl na prvním místě kladen důraz na efektivitu. Přes obecné pravdy, že míra úspěšnosti LERV závisí na výkonnosti litotryptoru, velikosti, lokalizaci, tvrdosti konkrementu, celkovém habitu pacienta a zkušenosti operatéra (23), stále neznáme jednoznačné odpovědi na bezpečný počet rázových vln, výběr energie rázové vlny, frekvenci.
Snižovaní frekvencí rázové vlny z původních 120 rázů na 60–90 rázů za minutu sice zlepšuje SFR (24–29), ale jak ukazují nejnovější publikace, neustálé snižování frekvence není také jasným receptem. Hnilicka et al. v prospektivní randomizované studii na souboru 240 pacientů prokázali lepší účinnost užití frekvence 90 Hz než užití frekvence 60 Hz při řešení ureterolitiázy (SFR 91,2 % vs. 79,5 %; p=0,012) (30).
Ve vztahu ke složení litiázy se prediktivním faktorem úspěšnosti LERV stala denzita konkrementu na CT. Odolná litiáza (kalcium oxalát monohydrát, brushite, cystinová litiáza) dosahuje denzit až nad 1 000 HU (Hounsfieldových jednotek), úspěšnost fragmentace je u této litiázy asi jen 55 %, riziko opakované léčby je u litiázy s denzitou nad 750 HU až 10× vyšší než u litiázy s nižší denzitou (31, 32). Při velikosti do 1 cm má pak nefrolitiáza řešená LERV jen 75% šanci na SFR oproti 100% šanci při perkutánní extrakci konkrementu (PEK). U litiázy nad 1 cm se tento poměr ještě více prohlubuje v poměru 52 % při ESWL vs. 90 % při užití PEK (33).
Dalším faktorem úspěšnosti terapie je habitus pacienta, kdy pacienti s BMI nad 30 mají významně nižší šanci na fragmentaci litiázy (32). Navíc dle našich výsledků pacienti s průměrně vyšším BMI měli i vyšší riziko poškození parenchymu ledvin po LERV, jak potvrzuje Nussberger et al. v recentní publikaci hodnotící soubor 418 pacientů s výskytem hematomu ledviny po LERV u 9 % pacientů (34). Riziko poranění parenchymu ledvin pak měli ve sledovaném souboru nejen pacienti s vysokým BMI (>30), ale i pacienti s nízkým BMI (<21,5) (p=0,001).
Samostatnou skupinu ve vztahu k lokalizaci tvoří problematika nefrolitiázy v dolním kalichu, jejíž řešení je zatíženo nejnižším SFR a současně je její řešení dle našich zjištění zatíženo nejvyšším procentem komplikací. Nedostatečný efekt je popisován až u 35 % (35) a dle literárně dostupných dat je riziko rozvoje hematomu při řešení periferní nefrolitiázy až dvojnásobné oproti řešení pyelolitiázy (36). Dle některých autorů jsou pak nepříznivými faktory úspěšné terapie litiázy dolního kalichu ostrý infundibulo‑pelvický úhel nad 45 stupňů, dlouhý kalich nad 10 mm nebo úzký krček pod 5 mm (37, 38). Některé prospektivní randomizované studie se sledováním delším než dva roky ukazují, že není signifikantního rozdílu mezi LERV a observací při srovnání periferní nefrolitiázy do 15 mm z pohledu SFR, symptomů, požadavků na následnou léčbu, kvalitu života, funkci ledvin či hospitalizaci (39).
Dále více než pětileté sledování ukazuje, že pacienti s malým reziduem po LERV potřebují ve 25 % další léčbu (40, 41). S ohledem na možné aspekty léčby včetně komplikací by mělo být (mimo jasných indikací) aktivní řešení asymptomatické drobné periferní nefrolitiázy důsledně zváženo a to i s ohledem na věk a komorbidity pacienta.
Koncem osmdesátých let reportovali Chaussy et al. incidenci hematomů po LERV 0,6 % (42), ostatní autoři pak udávali výskyt hematomů od 0,2 % až 1,5 % (43, 44, 45, 46). Ve vztahu k bezpečnosti však aktuální data ukazují, že procento poškození ledvin v souvislosti s užitím extrakorporální litotrypse je výrazně vyšší než byl původní předpoklad. Možným důvodem může být častější užití CT v diagnostice po LERV a tedy i vyšší záchyt poranění, která mohla být v minulosti přehlédnuta při pouhém užití sonografie. Tailly udává, že záchyt subkapsulárního či perirenálního hematomu je při užití sonografie jen 0,24–0,66 %, kdežto při užití CT nebo MRI roste až na 25–30 % (47). Na tuto realitu upozorňovali již některé rané práce koncem osmdesátých let, které udávaly výskyt hematomů při užití CT či MRI od 20 do 25 % (48, 49, 50). Zásadní zůstává poznatek, že klinicky symptomatických hematomů je minimum a to <1 % při dnes akceptované celkové incidenci 4–19 % hematomů po extrakorporální litotrypsi (36).
Kromě kvalitnější diagnostiky může být další příčinou vyššího výskytu i užití různých generací přístrojů, které byly vyvinuty ne vždy v souladu s fyzikálními principy vlastností rázové vlny. Zejména navyšování maximálních tlaků v ohnisku za cenu zvýšení výkonů nebylo u některých přístrojů šťastným řešením (51). Rovněž tlak výrobců přesunout extrakorporální litotrypsi do ambulantní péče, upřednostnit komfort pacienta záměnou „mokrého konceptu“ za „suchý“, nebyl zcela optimální. Obtížně definované ztráty energie při transportu rázové vlny a neoptimální coupling mohou být příčinou širšího užití energetických dávek (16). Tento fakt se může zásadním způsobem podílet na výsledné efektivitě, ale i bezpečnosti.
Pro výsledky jsou jednoznačně zásadní dostatečné zkušenosti provádějícího centra včetně zkušeností s daným typem přístroje. Rizikové faktory poškození ledvin tak byly obecně rozděleny na faktory vyplývající z typu užitého přístroje (fokální zóna, energetické nastavení), faktory vztahující se ke zkušenostem operatéra (pečlivá fokusace, pečlivý dohled při terapii, zbytečný overtreatment) a na vlastní faktory vztahující se přímo k pacientovi (hypertenze, porucha koagulace, chronické užívání antikoagulační či antiagregační terapie, ateroskleróza, ischemická choroba srdeční, obezita a diabetes melitus) (47). Přes obecně definované rizikové faktory je jen málo randomizovaných prací jednoznačně potvrzující vliv různých aspektů na poškození ledvin. Například práce amerických kolegů analyzující rizikové faktory rozvoje subkapsulárního hematomu ledvin při užití elektromagnetického zdroje prokazuje jako statisticky významný jen věk pacienta. Celkem analyzovali 415 výkonů v souboru 317 pacientů s nefrolitiázou, kdy výskyt hematomu ledvin zaznamenali u 4,1 % případů. (36). Vliv hypertenze na rozdíl od původních prací z osmdesátých let (44, 45, 52) neprokázali. Naopak Lee at al. prezentují v retrospektivně hodnoceném souboru 6 177 pacientů vliv hypertenze na rozvoj hematomu po LERV jako statisticky významný (p=0,022), kdy incidence hematomu byla v souboru pacientů s historií hypertenze 20 % oproti kontrolní skupině pacientů bez hypertenze, kdy byla incidence jen 8 % (53). Schnabel et al. hodnotící soubor 857 pacientů po LERV (incidence hematomu 0,53 %) doporučují v případě krevního tlaku, který překročí 160/100 mmHg, výkon odložit (54).
Vliv energie na poranění ledvin prezentovali Skuginna et al. v prospektivní randomizované studii. V souboru 418 pacientů porovnali dvě skupiny pacientů, v první skupině 213 pacientů byla během výkonu energetická dávka postupně navyšována, ve druhé skupině 205 pacientů byla dávka podána na fixní hladině. U pacientů v první skupině bylo prokázáno poranění ledvin jen ve 12 případech oproti druhé skupině, kde poranění parenchymu ledvin bylo zaznamenáno až ve 27 případech. (p=0,0184) (55). Obecně pak užití nižší frekvence působí protektivně na parenchym ledviny.
Prakticky 30letitá snaha zvyšovat efektivitu vedla k zavedení parametrů, jako je SFR či EQ, na druhé straně doposud nemáme žádný parametr hodnotící bezpečnost extrakorporální litotrypse, přitom navyšovaní energetických dávek vedoucí k lepší efektivitě je úměrné vyššímu riziku poranění ledvin. Pro lepší porovnání nejen efektivity, ale i bezpečnosti navrhujeme v klinické praxi používat nový parametr – koeficient bezpečné účinnosti ESQ (efficaccy safety quotient):
ESQ de facto vyjadřuje procento úspěšně vyřešených případů bez poškození ledviny. Doposud používaný parametr EQ či SFR vyjadřuje procento vyřešených případů včetně případů, ve kterých došlo k poranění ledviny.
ZÁVĚR
Prokázali jsme dobrou účinnost extrakorporální litotrypse a dosáhli jsme SFR v 78,6 %. Efektivita LERV byla ovlivněna velikostí a lokalizací litiázy, BMI pacienta a užitou energetickou dávkou. Incidence renálního hematomu po elektromagnetické litotrypsi dosahuje v našem souboru 4,5 %, kdy symptomatických pacientů bylo pouze 1,23 %. Potvrdili jsme tak, že incidence poškození parenchymu ledvin je vyšší, než byl předpoklad v minulosti.
Ve vztahu k lokalizaci a velikosti je nejvíce problematické řešení litiázy dolního kalichu a to jak stran SFR, tak s ohledem na bezpečnost. Doporučujeme tedy důsledně zvažovat aktivní přístup při řešení asymptomatické periferní litiázy.
Zaznamenali jsme vyšší výskyt poranění parenchymu ledvinu u pacientů se zavedeným stentem, a to zejména u pacientů s anamnézou předchozí infekce ledviny. V takových případech doporučujeme zvážit podání antibiotické profylaxe před výkonem a řešení litiázy naplánovat v optimálním časovém odstupu po vyléčení zánětu.
Zásadní pro účinnost i bezpečnost zůstává užitá energetická dávka. S ohledem na absenci jasných doporučení energetických dávek doporučujeme každému klinickému pracovišti sledovat své výsledky a následně se snažit na konkrétním přístroji energetické dávky optimalizovat.
Závěrem doporučujeme zavést do praxe koeficient bezpečné účinnosti ESQ, který umožní porovnání nejen efektivity, ale i bezpečnosti mezi jednotlivými přístroji. Další souhrnné analýzy dat pak můžou zlepšit naši klinickou praxi.
Došlo: 26. 4. 2017
Přijato: 28. 5. 2017
Střet zájmů: žádný
Prohlášení o podpoře: Autor prohlašuje, že zpracování článku nebylo podpořeno farmaceutickou firmou. Práce vznikla s finanční podporou Vědecké rady Krajské nemocnice Liberec, a.s.
Kontaktní adresa:
MUDr. Vít Paldus
Urologické oddělení,
Krajská nemocnice Liberec, a. s.
Husova 10, 460 63 Liberec
e‑mail: vit.paldus@nemlib.cz
Sources
1. Petřík A, Horáková J, Tolinger J. Trendy v terapii urolitiázy v létech 1990–2015. 62. Výroční konference české urologické společnosti ČLS JEP. Poster.
2. Deters LA, Jumper CM, Steinberg PL, et al. Evaluating the definition of „stone‑free status“ in contemporary urologic literature. Clin Nephrol 2011; 76(5): 354–357.
3. Denstedt JD, Clayman RV, Preminger GM. Efficacy quotient as a means of comparing lithotripters. J Endourol 1990; (3): 100.
4. Clayman RV, MCLennan BL, Garvin TJ, Denstedt JD, Andriole GL. Lithostar: an electromagnetic acoustic shock wave unit for extracorporeal lithotripsy. J Endourol 1989; 3 : 307–313.
5. Rassweiler J, Köhrmann J, Jünemann KP, Alken P. Use of electromagnetic technology. In Smith AD. Controversies in endourology, Philadelphia: WB Saunders Co 1995 : 95–106.
6. Kerbl K, Rehman J, Landman J, et al. Current management of urolithiasis: progress or regress? J Endourol 2002; 16 : 281–288.
7. Granz B, Köhler G. What makes a shock wave efficient in lithotripsy stones disease 1992; 4 : 123–128.
8. Rassweiler JJ, Bergsdorf T, Ginter S, et al. Progress in lithotripter technology. In: Chassy C, Haupt G, Jocham D, Köhrmann KU, Wilbert D (eds.) Therapeutic energy applications in urology. Standards and recent developments. Thieme Stuttgart – New York 2005 : 3–15.
9. Rassweiler JJ, Tailly GG, Chaussy C. Progress in lithotriptor technology. EAU Update Series 2005 : 17–36.
10. Chaussy C, Haupt G, Jocham D, Köhrmann KU. Consensus: shock wave technology and application – state of the art in 2010. Therapeutic Energy Applications in Urology II 2010; 2 : 37–52.
11. Sheir KZ, Madbouly K, Elsobky E. Prospective randomized comparative study of the effectiveness and safety of electrohydraulic and electromagnetic extracorporeal shock wave lithotripters. J Urol 2003; 170 : 389–392.
12. Koser M, Rhein A, Haecker M, Rabs U. Extracorporeal shock wave lithotripsy (ESWL) of urinary calculi – effect of shock wave frequency on fragmentation success: preliminary result of prospective study. Eur Urol 2001; 39(Suppl): 58.
13. Sorensen C, Chandhoke P, Moore M, Wolf C, Sarram A. Comparison of intravenous sedation versus general anesthesia on the efficacy of the Doli 50 lithotriptor. J urol 2002; 168 : 35–37.
14. Rassweiler J, Knoll T, Köhrmann K, et al. Shock wave technology and application: an update. Eur Urol May 2011; 59(5): 784–796.
15. Paldus V, Šámal V, Mečl J, Pírek J. Zhodnocení účinnosti extrakorporální litotrypse elektromagnetického generátoru EMSE 140f Dornier Compact Sigma a stanovení efektivní energetické dávky. Ces Urol 2014; 18(4): 316–323.
16. Guanqyan L, James WC Jr, Pischalnikov YA, Ziyue L, McAteer JA. Size and Location of Defects at the Coupling Interface Affect Lithotripter Performance. BJU Int. Dec 2012; 110: E871–E877.
17. Bohris C, Roosen A, Dickmann M, et al. Monitoring the coupling of the lithotripter therapy head with skin during routine shock wave lithotripsy with a surveillance camera. J Urol. 2012 Jan; 187 : 157–163.
18. Tailly GG. Optical coupling control in ESWL: first clinical experience. Poster.
19. Pishchalnikov YA, Neucks JS, VonDerHaar RJ, Pishchalnikova IV, Williams Jr JC, MCAteer JA. Air pockets trapped during routine coupling in dry head lithotripsy can significantly decrease the delivery of shock wave energy. J Urol 2006; 176 : 2706–2710.
20. Petřík A, Záťura F, Beneš J. Vliv stentingu na dezintegraci ureterolitiázy in vitro. Ces Urol 2004; 8(3): 46–48.
21. Petřík A, Alterová E, Fiala M, Novák J, Záťura F. Vliv stentingu na dezintegraci ureterolitázy in vivo. Ces Urol 2006; 10(1): 59–63.
22. Turk C, Petrik A, Sarica K, Seitz C, Skolarikos A, Straub M, et al. EAU Guidelines on Interventional Treatment for Urolithiasis. Eur Urol. 2016; 69(3): 475–482.
23. Logarakis NF, Jewett MA, Luymes J, et al. Variation in clinical outcome following shock wave lithotripsy. J urol 2000; 163(3): 721–725
24. Li WM, Wu WJ, Chou YH, et al. Clinical predictors of stone fragmentation using slow‑rate shock wave lithotripsy. Urol Int 2007; 79 : 124.
25. Yilmaz E, Batislam E, Basar M, Tuglu D, Mert C, Basar H. Optimal frequency in extracorporeal shock wave lithotripsy: prospective randomized study. Urology 2005; 66 : 1160.
26. Pace KT, Ghiculete D, Harju M, Honey JDA. Shock wave lithotripsy at 60 or 120 shocks per minute: a randomized, double‑blind trial. J Urol 2005; 174 : 595.
27. Madbouly K, El-Tiraifi AM, Seida M, El_Faqih SR, Atassi R, Talic RF. Slow versus fast shock wave lithotripsy rate for urolithiasis: a prospective randomized study. J Urol 2005; 173 : 127.
28. Semins MJ, Trock BJ, Matlaga BR. The effect of shock wave rate on the outcome of shock wave lithotripsy: a meta‑analysis. J Urol 2008; 179 : 194.
29. Li K, Lin T, Zhang C, et al. Optimal frequency of shock wave lithotripsy in urolithiasis treatment: a systematic review and meta‑analysis of randomized controlled trials. J Urol 2013; 190 : 1260.
30. Hnilicka S, Nguyen DP, Schmutz R, et al. Optimising parameters of extracorporeal shock wave lithotripsy (ESWL) for ureteral stones results in excellent treatment outcomes. Results of prospective, randomised trial. Annual EAU Congres 2015, Madrid. Abstr. 92.
31. Choi JW, Song PH, Kim HT. Kim predictive factors of the outcome of extracorporeal shockwave lithotripsy for ureteral stones. Korean J Urol 2012; 53(6): 424–430.
32. Pareek G, Armenakas NA, Panagopoulos G, Bruno JJ, Fracchia JA. Extracorporeal shock wave lithotripsy success based on body mass index and Hounsfield units. Urology 2005; 65 : 33–36.
33. Lingeman JE, Siegel YI, Steele B, et al. Management of lower pole nephrolithiasis: a critical analysis. J Urol 1994; 151 : 663–667.
34. Nussberger F, Roth B, Metzger T, Kiss B, Thalmann GN, Seiler R. A low or high BMI is a risk factor for renal hematoma after extracorporeal shock wave lithotripsy for kidney stones. Urolithiasis 2016; 30 : 30.
35. Cambell‑Walsh Urology. Philadelphia: Elsevier Souders, Tenth edition 2012; 1356–1408.
36. Dhar NB, Bailey MR, Paun M, et al. A multivariate analysis of risk factors associated with subcapsular hematoma formation following electromagnetic shock wave lithotripsy. J Urol 2004; 172 : 2271.
37. Handa RK, Bailey MR, Paun M, et al. Pretreatment with low‑energy shock wave induces renal vasoconstriction during standard shock wave lithotripsy (SWL): a treatment protocol known to reduce SWL‑induced renal injury. BJU Int 2009; 103(9): 1270–1274.
38. Manikandan R, Gall Z, Gunendran T, et al. Do anatomic factors pose a significant risk in the formation of lower pole stones? Urology 2007; 69(4): 620–624.
39. Keeley FX Jr, Tilling K, Elves A, et al. Preliminary results of a randomized controlled trial of prophylactic shock wave lithotripsy for small asymptomatic renal calyceal stones. BJU Int 2001; 87 : 1.
40. Osman MM, Alfano Y, Kamp S, et al. 5-year‑follow‑up of patients with clinically insignificant residual fragments after extracorporeal shockwave lithotripsy. Eur Urol 2005; 47 : 860.
41. Rebuck DA, Macejko A, Bhalani V, Ramos P, Nadler RB. The natural history of renal stone fragments following ureteroscopy. Urology 2011. 77 : 564.
42. Chaussy C, Schuller J, Schmiedt E, Brandl H, Jocham D, Liedl B. Extracorporeal shock‑wave lithotripsy (ESWL) for treatment of urolithiasis. Urology 1984; 23 : 59.
43. Roth RA, Beckmann CF. Complications of extracorporeal shock‑wave lithotripsy and percutaneous nephrolithotomy. Urol Clin North Am 1900; 15 : 155.
44. Knapp PM, Kulb TB, Lingeman JE, et al. Extracorporeal shock wave lithotripsy‑induced peri‑renal hematomas. J Urol 1988; 139 : 700.
45. Newman LH, Saltzman B. Identifying risk factors in development of clinically significant post‑shock‑wave lithotripsy subcapsular hematomas. Urology 1991; 38 : 35.
46. Tillotson CL, Deluca SA. Complications of extracorporeal shock wave lithotripsy. Am Fam Physician 1988; 38 : 161.
47. Tailly GG. Management of acute post ESWL complications. Ces Urol 2000, 4(2): 5–8.
48. Kaude JV, Williams CM, Millner MR, Scott KN, Finlayson B. Renal morphology and function immediately after extracorporeal shock‑wave lithotripsy. Am J Roentgenol 1985; 145 : 305.
49. Rubin JI, Arger PH, Pollack HM, et al. Kidney changes after extracorporeal shock wavelithotripsy: CT evaluation. Radiology 1987; 162 : 21.
50. Baumgartner BR, Dickey KW, Ambrose SS, Walton KN, Nelson RC, Bernardino ME. Kidney changes after extracorporeal shock wave lithotripsy: appearance on MR imaging. Radiology 1987; 163 : 531.
51. Matin SF, Yost A, Streem SB. Extracorporeal shockwavelithotripsy: a comparative study of electrohydraulic and electromagnetic units. J Urol 2001; 166 : 2053.
52. Coptcoat MJ, Webb DR, Kellett MJ, et al. The complications of extracorporeal shockwave lithotripsy: management and prevention. Br J Urol 1986; 58 : 578
53. Lee HY, Yang YH, Shen JT, et al. Risk factors survey for extracorporeal shockwave lithotripsy‑induced renal hematoma. J Endourol 2013; 27(6): 763–767.
54. Schnabel MJ, Gierth M, Chaussy CG, Dotzer K, Burger M, Fritsche HM. Incidence and risk factors of renal hematoma: a prospective study of 1,300 SWL treatments. Urolithiasis. 2014.
55. Skuginna V, Nguyen DP, Seiler R, et al. Does a step‑wise voltage ramping protect the kidney from injury during extracorporeal shock wave lithotripsy (ESWL)? Results of the prospective randomized trial. Annual EAU Congres 2015, Madrid. Abstr. 90.
Labels
Paediatric urologist Nephrology UrologyArticle was published in
Czech Urology

2017 Issue 2
-
All articles in this issue
- Využití flexibilní nefroskopie k extrakci urolitiázy při laparoskopické a roboticky asistované pyeloplastice
- Intravezikální chemoterapie s využitím tepelné energie u pacientů s uroteliálním karcinomem močového měchýře bez invaze svaloviny
- Dysfunkce mikce u pacientů s posttraumatickou míšní lézí - úloha urologa
- Trombóza povrchové dorzální žíly penisu (Penilní Mondorova choroba)
- Zpráva o proběhlém 5. ročníku Video‑semináře Tipy a triky v Urologické operativně
- Zpráva z workshopu Sekce urodynamiky, neurourologie a urogynekologie ČUS ČLS JEP: Funkční urologie - Novinky 2017
- 2. ročník konference KNOU, pohled mladého lékaře
- ASSOC. PROF. ROMAN ZACHOVAL, M.D., PH.D., MBA, CELEBRATED HIS 50TH BIRTHDAY
- Sledování a léčba pacientů po radikální prostatektomii s pozitivními okraji preparátu
- Funkční výsledky pyeloplastiky provedené v kojeneckém věku
- Nefrometrická skóre první a druhé generace pro predikci peri- a pooperačních výsledků resekcí ledvin
- Efficacy and safety of extracorporeal shock wave lithotripsy in the 21th century – controversy and clinical practice.
- Spontánní ruptura renálního angiomyolipomu
- Czech Urology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Trombóza povrchové dorzální žíly penisu (Penilní Mondorova choroba)
- Dysfunkce mikce u pacientů s posttraumatickou míšní lézí - úloha urologa
- Sledování a léčba pacientů po radikální prostatektomii s pozitivními okraji preparátu
- ASSOC. PROF. ROMAN ZACHOVAL, M.D., PH.D., MBA, CELEBRATED HIS 50TH BIRTHDAY




