Nefrometrická skóre první a druhé generace pro predikci peri- a pooperačních výsledků resekcí ledvin
First and second generation nephrometry scores for predicting peri - and post-operative results of kidney resection
Introduction:
Assessment of the first and the second generation nephrometric scores (NS) and their relationship with selected peri - and postoperative results of partial nephrectomies. We tested the correlation of NS with duration of warm ischemia (WI) and estimated glomerular filtration rate (eGF) change in per cent.
Patients and methods:
Prospective assessment of patients undergoing PN between 11/2015 and 6/2016. Tumor size, RENAL, PADUA, DAP scores and C-index as the first-generation NS and NePhRO, SARR a Tobert score as the second-generation NS were tested for correlation with duration of WI and per cent change of eGF.
Results:
We evaluated 35 patients, of which 21 had laparoscopic and 14 open PN. Median and interquartile ranges (IQR) were: age 65 (IQR 52–72), tumor size 35 mm (27–48), RENAL 8 (6–9), PADUA 9 (7–10), DAP 6 (5–7), C index 2.3 (1.6–2.6), NePhRO 9 (7–10), SARR 8 (7–11), Tobert score 7 (3–8), duration of WI 16 min (10–18), per cent change of eGF -5.3 % (-19.1 to -1.5). Duration of WI correlated significantly with tumor size and RENAL, PADUA, DAP, NePhRO, SARR, Tobert scores, and significantly, but inversely with C index. Correlation strength was mild to moderate. In contrast, per cent eGF change correlated significantly with RENAL, PADUA, DAP, NePhRO and SARR scores and tumor size, but not with C-index.
Conclusions:
WI correlated with tumor size and all NS used, but its strength was moderate at best. However, per cent change of eGF, did not correlated with C-index and Tobert score. This is in line with published data about estimated PN difficulty (with WI as surrogate marker), however our data and literature diverge in opinion on functional results. The difference might be due to small cohort size. The main impact of PN scoring systems is in the mutual comparison of PN data and gives us information we may use during counselling.
KEY WORDS:
Partial nephrectomy, nephrometric scores, warm ischemia, estimated glomerular filtration rate.
Authors:
Petr Macek; Maria Stevens; Květoslav Novák; Michael Pešl; Tomáš Hanuš
Authors‘ workplace:
Urologická klinika 1. LF UK a VFN v Praze
Published in:
Ces Urol 2017; 21(2): 154-160
Category:
Original Articles
Overview
Úvod:
Cílem práce je zhodnocení souvislosti nefrometrických skóre (NS) první a druhé generace s vybranými peri - a pooperačními výsledky resekcí ledvin (RL). Posuzována je korelace NS a doby teplé ischemie (TI) a procentuální změny glomerulární filtrace (GF).
Soubor a metodika:
Prospektivní hodnocení pacientů podstupujících RL v období 11/2015 až 6/2016. Hodnocena byla velikost tumoru, NS první generace RENAL, PADUA, DAP, C index a NS druhé generace NePhRO, SARR a Tobertovo skóre. Jejich hodnoty byly hodnoceny ve vztahu k délce TI a procentuální změně GF.
Výsledky:
Hodnoceno bylo 35 pacientů, 21 laparoskopických RL a 14 otevřených. Medián a mezikvartilové rozpětí (IQR) byly: věk 65 (IQR 52–72), velikost tumoru 35 mm (27–48), RENAL 8 (6–9), PADUA 9 (7–10), DAP 6 (5–7), C index 2,3 (1,6–2,6), NePhRO 9 (7–10), SARR 8 (7–11), Tobertovo sk. 7 (3–8), délka ischemie 16 min (10–18), změna GF -5,3 % (-19,1 až -1,5). Délka TI významně korelovala pozitivně s velikostí tumoru a skóre RENAL, PADUA, DAP, NePhRO, SARR a Tobertovým skóre, a negativně s indexem centrality. Míra korelace byla nízká nebo středně významná. Proti tomu % změna GF významně korelovala se skóre RENAL, PADUA, DAP, NePhRO a SARR. Nebyla zjištěna korelace % změny GF s indexem centrality a Tobertovým skóre.
Závěr:
Teplá ischemie souvisela s velikostí tumoru a korelovala se všemi sledovanými NS, míra korelace byla maximálně střední. Proti tomu procentuální změna GF nesouvisela s C‑indexem a Tobertovým skóre, ale souvisela s ostatními NS. To je v souladu s literárními údaji v odhadu komplexity výkonu (zastoupené délkou TI), při hodnocení komplikací naše údaje potvrdily souvislost s funkčním dopadem RL jen u některých NS, s výjimkou C‑indexu a Tobertova skóre, kde se rozchází s literárními výsledky. Rozdíl může být dán posuzováním menšího souboru. Hlavní význam NS však spočívá v možnosti vzájemného srovnání souborů a volbě informací komunikovaných s pacienty.
KLÍČOVÁ SLOVA:
Resekce ledviny, nefrometrické skóre, teplá ischemie, vypočtená glomerulární filtrace.
ÚVOD
Česká republika drží celosvětové prvenství ve výskytu nádorů ledvin (1). V roce 2014 byla incidence v České republice 30 případů na 100 000 osob, přičemž v čase jde o pomalý, ale trvalý nárůst. Mortalita na uvedené onemocnění v roce 2014 činila 11,1 na 100 000, nicméně v čase dochází k velmi mírnému poklesu setrvale od roku 2003. Maximum výskytu nádorů ledvin je mezi 70. a 80. rokem (2). Typicky jsou nádory ledvin zastiženy při provedení zobrazovacího vyšetření z jiné indikace. Podíl takto zjištěných lézí může činit až 70 % (3). Časně zjištěné tumory ledvin typicky patří do kategorie cT1, tj. menší než 7 cm. V této souvislosti se proto stalo standardem pokusit se o ledvinu šetřící přístup, je‑li to technicky proveditelné, nicméně je nutno přihlédnout k množství ponechaného zdravého parenchymu. Tato doporučení jsou obsažena v řadě mezinárodních doporučení a celosvětově je patrný nárůst ledvinu šetřících postupů (4, 5). Resekce ledviny je v narůstajících množstvích prováděna i v České republice (6, 7).
Při hodnocení, zda je určitý tumor ledviny vhodný k ledvinu zachovávajícímu výkonu, přihlížíme k řadě faktorů. Mezi ně patří: 1) faktory nádoru: počet, velikost, umístění, včetně vztahu ke kalichopánvičkovému systému (KPS)/močovodu a velkým cévám; 2) faktory pacienta: přidružená onemocnění (např. diabetes, ledvinná nedostatečnost apod.), předchozí operace ledvin či břicha, funkční a anatomická kondice ledvin, možné hereditární stavy; 3) zkušenosti operatéra a přístrojové vybavení.
Na základě toho je patrné, že každý tumor ledviny je unikátní, a tedy i výsledky záchovných výkonů se proto v jednotlivých souborech budou lišit. Urologická komunita tedy vyvíjí kontinuální snahu o standardizaci hodnocení komplexnosti nádorů za účelem lepší srovnatelnosti peri - a pooperačních výsledků nebo hodnocení komplikací. Výsledkem těchto snah jsou tzv. nefrometrická skóre (NS), kterých však postupně vznikla celá řada. Většina z nich hodnotí především velikost nádoru, jeho umístění z různého pohledu (zde je významná variabilita), hloubka jeho invaze a také vztah ke KPS. Nevýhodou velkého množství NS je roztříštěnost v hodnocení a ve většině případů také absence validace. Přestože je nepochybně dokumentováno, že na základě NS lze odhadovat pravděpodobnost určitých výsledků, jako jsou délka teplé ischemie, riziko krvácení či rozsah změny pooperační funkce, není však zatím zcela jasné, zda jsou některá NS významně lepší proti jiným. Ani u recentně dostupných skórovacích systémů druhé generace není tedy zřejmé, zda budou výhodnější z pohledu přesnosti predikce či uživatelské přívětivosti/ snadnosti.
Cílem naší práce bylo zhodnocení resekcí ledvin z pohledu několika vybraných skórovacích schémat první i druhé generace.
METODIKA A SOUBOR
Hodnocení bylo provedeno u souboru prospektivně vytvářené klinické databáze. NS první generace (NS1G) jsou v databázi aplikována od roku 2013 a NS druhé generace (NS2G) od roku 2015.
Hodnotili jsme výsledky pacientů podstupujících resekci ledviny v období 11/2015 až 6/2016. Sledovanými parametry byly: velikost tumoru (v milimetrech), NS1G: RENAL (Radius – Endo/ exophytic – Neareness – Anterior/posterior – Localization) (8), PADUA (Perioperative Aspects and Dimensions Used for Anatomical classification) (9), DAP (Diameter‑Axial‑Polar) (10), C (=Centrality) index (11), NS2G: NePhRO (Nearness to collecting system, Physical location of the tumor, Radius, Organization) (12), SARR (Surgical Approach Rrenal Ranking) (13) a Tobertovo skóre (14). Jejich hodnoty byly hodnoceny ve vztahu k délce teplé ischemie (TI) v minutách a procentuální změně vypočtené glomerulární filtrace (GF). Pokud nebyla teplá ischemie použita, pak byla hodnocena jako 0 minut. Výpočet GF byl prováděn dle rovnice Lund‑Malmö (LM) s korekcí na beztukovou tělesnou hmotu (lean body mass = LBM), protože tato rovnice vytvořená švédskými autory nejvíce odpovídá evropské populaci (15). GF byla hodnocena dle kreatininémie před operací a při dimisi. Hodnoceni byli pouze pacienti s kompletními perioperačními výsledky a všemi vybranými skórovacími systémy. Poklady pro skórování vycházely z počítačové tomografie (CT) 31x, z PET‑CT vyšetření 2x a z magnetické rezonance 2x. Všechna skóre byla vyhodnocena jednou osobou, urologem. Dosažené skóre nemělo vliv na volbu přístupu (laparoskopicky vs. otevřeně). Celkový stav osob byl hodnocen dle Charlesonové indexu komorbidit (http://touchcalc.com/calculators/ cci_js). Statistické zhodnocení bylo provedeno s pomocí softwaru SPSS ver. 22. Hladina významnosti 0,05 a s ohledem na charakteristiky souboru byly použity neparametrické testy.
VÝSLEDKY
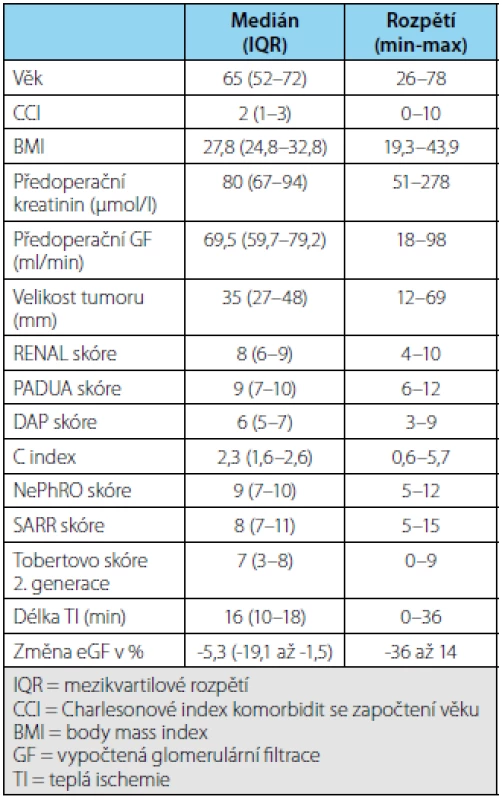
Všechna NS byla dostupná u 42 pacientů, nicméně z hodnocení byly vyloučeny osoby s nekompletními údaji o perioperačních výsledcích nebo funkci, pacienti s vícenásobnou nebo bilaterálně provedenou resekcí ledviny. Hodnoceno tedy bylo 35 pacientů, z toho dvě osoby měly provedenou resekci solitární ledviny. Charakteristiky souboru jsou shrnuty v tabulce 1. Osm RL (8/35, tj. 23 %) bylo provedeno bez ischemie. Výkon byl proveden u 21 (60 %) pacientů laparoskopicky, u 14 (40 %) otevřeně.
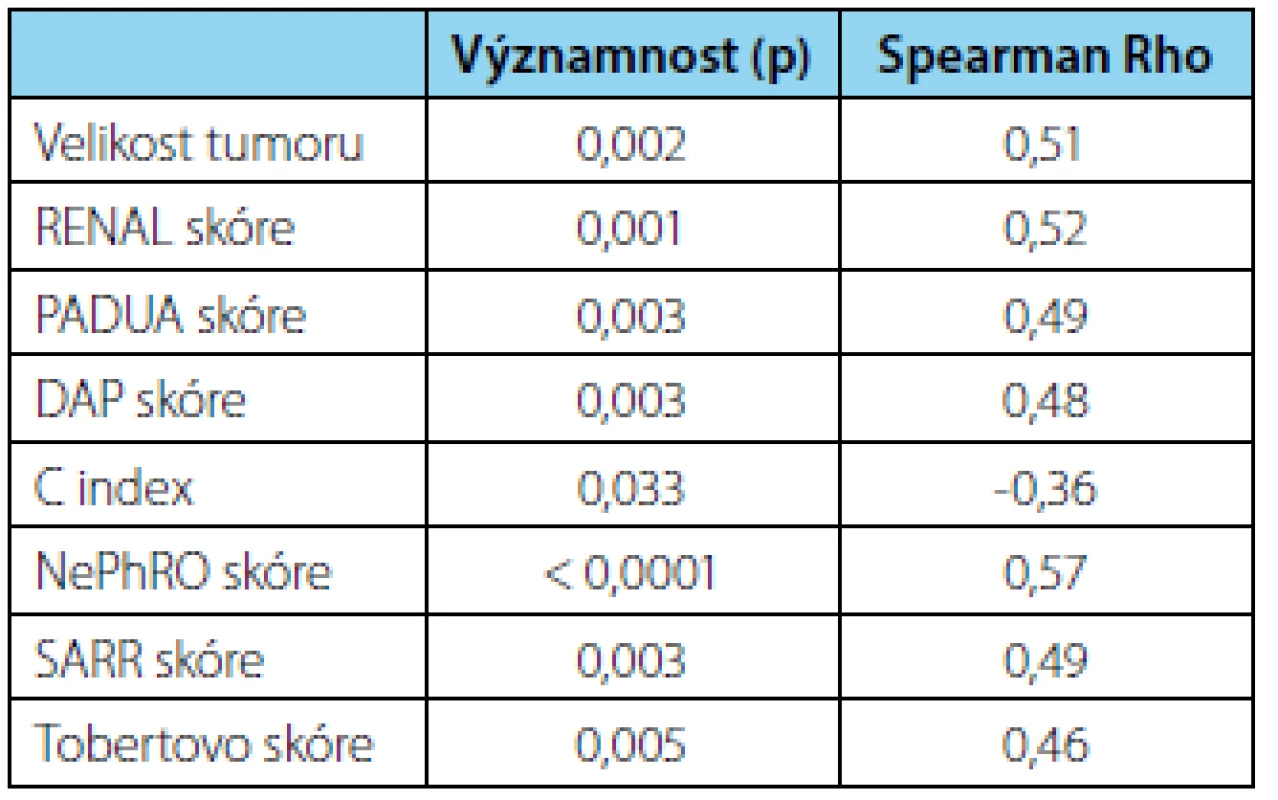
Délka TI měla souvislost s předoperační velikostí tumoru, ale také se všemi hodnocenými NS. Míra korelace byla nízká (Spearmanův koeficient 0,3–0,5) nebo středně významná (Spearman 0,5–0,7) (16). Souhrn vztahů TI k hodnoceným NS je uveden v tabulce 2.
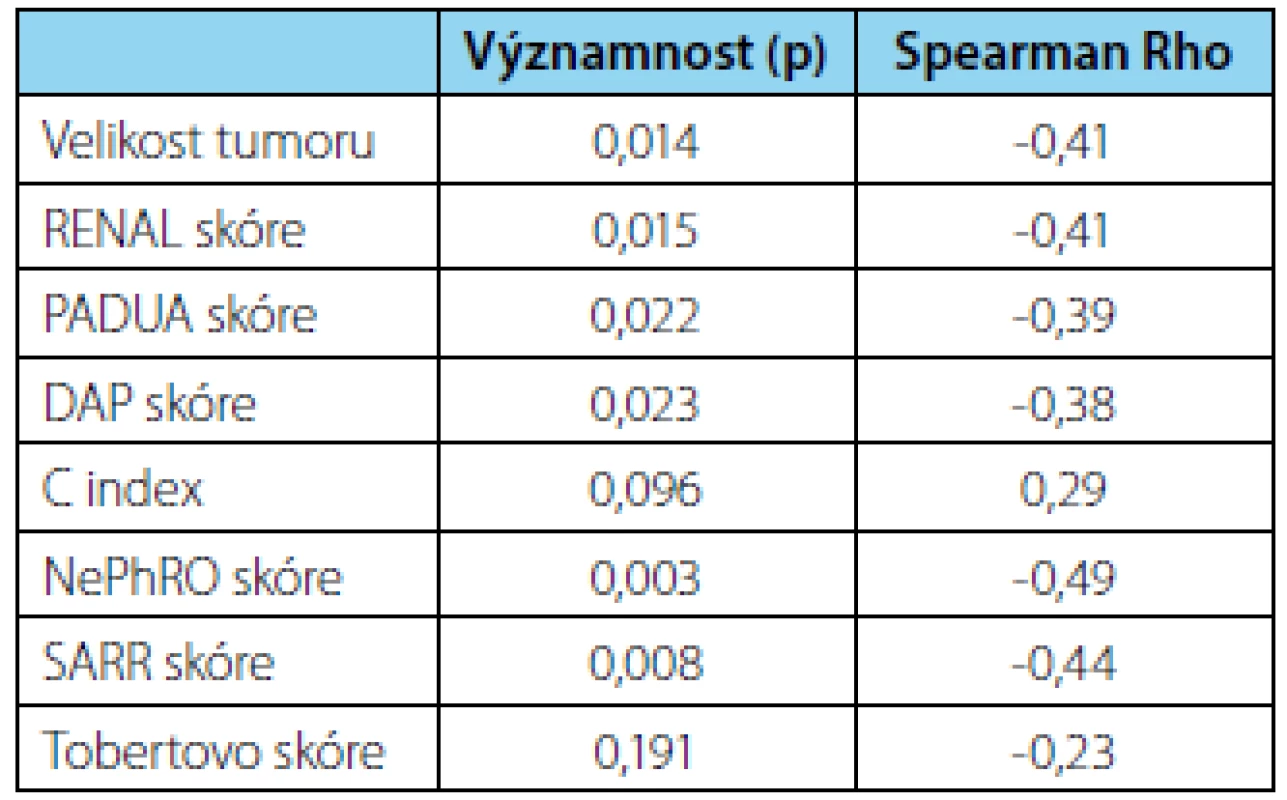
Ve vztahu k procentuální změně GF byla zjištěna významná korelace s velikostí nádoru, skóre RENAL, PADUA, DAP, NePhRO a SARR (hladina významnosti v tabulce 3). Naopak nebyla zjištěna významná souvislost procentuální změny GF s C‑indexem a Tobertovým skóre 2. generace. Míra korelace u všech zjištěných souvislostí byla taktéž nízká nebo středně silná. Souhrn relací vztahujících se k procentuální změně GF včetně je uveden v tabulce 3.
DISKUZE
Současný trend v léčbě nádorů ledvin je spojen s pozvolným posouváním hranic jednotlivých výkonů. Důvodů je celá řada – počínaje rozšiřujícími se znalostmi o funkci solitární ledviny a metabolických dopadech renální insuficience, přes prohlubující se znalosti a zkušenosti ve vztahu k minimalizaci dopadu na zdravý parenchym včetně zkrácení doby ischemie a v neposlední řadě také požadavky pacientů a odbornými doporučeními.
I když připustíme, že každá expanze ledviny je specifická, nelze opomenout, že se mohou výsledky RL značně lišit. Je to dáno jistě výběrem pacientů k záchovným výkonům, k nimž přispívá zkušenost operatérů/pracovišť. Abychom byli schopni onkologické i funkční výsledky jednotlivých pracovišť porovnat, je nutná standardizace hodnocení vstupních parametrů – 1) pacientů (např. ASA klasifikace nebo index Charlesonové) a 2) tumorů. V druhém případě jsou k dispozici nefrometrická skórovací schémata. K dispozici jich je celá řada a stále přibývají. Úlohou NS je však také rozpoznání komplexnosti expanze a dle toho pak plánování průběhu výkonu (přístup, užití ischemie, případně doplňkové manipulace).
Většina NS typicky hodnotí velikost nádoru, hloubku invaze a jeho vztah ke KPS systému a případně jeho umístění ve vztahu k orientačním bodům na ledvině (např. hranice sinu, hranice KPS nebo jiné) (8, 10, 12).
Nicméně jednotlivá NS jsou konstruována odlišně a jejich výkonnost v predikci nemusí být identická. Některá NS jsou lepší pro predikci komplikací (v návaznosti na komplexnost léze) (8, 9, 12, 13, 14), jiná jsou spíše zaměřená na odhad pooperačního funkčního výsledku (10, 17, 18, 19), další jsou pak zaměřena relativně specificky např. na riziko otevření KPS (20) nebo na komplexní algoritmus hodnotící obecný perioperační průběh v případě RoSCO hodnocení (21).
Množství dostupných NS je spíše nevýhodou vedoucí k roztříštěnosti výsledků, protože některá pracoviště mohou tvrdošíjně prosazovat „své“ NS. V současnosti jsou proto nejen dostupná již validovaná NS první generace, jakou jsou RENAL (17) a PADUA (22) skóre, případně Arterial‑Based‑Classification (ABC) (23), ale jsou také vytvořená NS druhé generace, která využívají již etablovaných parametrů, ale přidávají také zkušenosti např. s odlišnou komplexností tumorů uložených v různých částech ledviny, např. NePhRO, SARR, Toberovo a ABCD skóre (12, 13, 14, 23). Nicméně z důvodu absence přímých srovnání není dosud jasné, zda jsou NS2G obecně lepší než NS1G, nebo zda jsou rozdíly jen v určitých oblastech hodnocení. Dosud byla porovnávána přepředevším skóre první generace, kde se RENAL, PADUA a DAP skóre jevily lepší než C‑index (24) a zatím izolované srovnání zahrnující také NePhRO skóre vychází podobně v jeho prospěch proti C‑indexu (25).
Pro budoucí užití bude podstatná nejen vypovídací hodnota NS, ale také snadnost jejich vyhotovení („výpočtu“) pro urology. Ukazuje se, že u zavedených (RENAL, PADUA) i nových (NePhRO) schémat je shoda mezi hodnotiteli (urolog vs. radiolog) přijatelná a není tedy problém, aby skórování prováděl sám urolog (25). Časová náročnost provedení jednoho skórování je individuální a závisí na zkušenostech se čtením CT či MR obrazové dokumentace. Zpočátku lze očekávat dobu asi pěti minut z důvodu opakovaného nahlížení na obrazový nález. Po odpovídajícím zapracování lze skórování jedním systémem u jednoho pacienta provést do jedné minuty, pokud není třeba přesného měření a opakovaného vracení se k obrazovému nálezu. Čas lze také zkrátit užitím více monitorů – jeden s obrazovým nálezem, druhý se skórovací dokumentací. Pro hodnocení subjektivní náročnosti jednotlivých schémat nejsou přímá srovnání. Nám se jako nejjednodušší (tedy asi s nejmenším rizikem vzniku chyby) jeví ABC skóre, protože nevyžaduje žádná měření, ani opakované vrácení se k obrazové dokumentaci. Na druhou stranu je dosti jednostranně zaměřeno a nemusí splňovat nároky na komplexní zhodnocení.
Bylo by to sice optimální, není to ale zřejmě reálné, aby postupem času vznikl konsenzus na určitém NS, které bude univerzálně užíváno.
Při porovnání zjištěných a literárních výsledků z pohledu míry korelace mezi jednotlivými NS a délkou TI je korelace v našem souboru podobný v případě RENAL skóre – Spearmanův koeficient 0,52, proti literární 0,31–0,39, podobně pak také u korelace velikosti nádoru a TI je Spearmanův koeficient 0,51, proti udávaným 0,35–0,58, a podobně i PADUA se Spearman koeficientem 0,49, proti publikovaným 0,25–0,5, naopak mírně horší u C‑indexu Spearmanův koeficient -0,36, proti literárním -0,44 až -0,61 (26). Při srovnání s literárními údaji o korelaci mezi NS a procentuální změnou GF jsme dosáhli příznivější shody ve skóre RENAL Spearmanův koeficient náš soubor -0,41, proti -0,30, PADUA Spearman -0,39, proti -0,20 (ve všech případech se jednalo o statisticky významný vztah p<0,05) (27). V případě DAP skóre jsme zjistili lepší korelaci než literatura, Spearmanův koeficient našeho souboru -0,38, proti -0,16 (v obou případech p<0,05) (28). Srovnatelné výsledky byly v případě C‑indexu Spearman 0,29 (bez statistické významnosti p=0,096), proti 0,30 (při p<0,01) (27).
NS2G jsou v literatuře hodnoceny mírně odlišnými jinými statistickými testy a i přes obecně publikovaná vyjádření o korelaci výsledků s těmito NS, nelze provést přímé srovnání s našimi výsledky.
ZÁVĚR
Na vybrané skupině našich pacientů jsme prokázali souvislost některých dílčích perioperačních (nutno užití a délky teplé ischemie) a pooperačních (funkční dopad vyjádření procentuální změnou glomerulární filtrace) výsledků resekcí ledviny, které jsou srovnatelné s literárními údaji v případě NS1G a pravděpodobně i NS2G (zde není možnost porovnání pro absenci srovnatelných statistických metod). V ČR jde o pilotní projekt. Byť se jedná o menší soubor a uvedené výsledky přímo nazvat validací, lze konstatovat, že i v rámci české populace lze hodnocená schémata použít pro předoperační odhad komplexity záchovných výkonů ledvin a pro odhad peri - a pooperačních výsledků. Hodnocení souboru prostřednictvím NS (bez ohledu na typ) může sloužit ke vzájemné porovnatelnosti vstupních charakteristik souborů a v neposlední řadě také ke komunikaci odpovídajících informací s pacienty v rámci konzultace při plánování odpovídajícího typu intervence.
Došlo: 25. 1. 2017
Přijato: 28. 3. 2017
Střet zájmů: žádný
Prohlášení o podpoře: Autor prohlašuje, že zpracování článku nebylo podpořeno farmaceutickou firmou.
Kontaktní adresa:
MUDr. Petr Macek, Ph.D., FEBU
Urologická klinika 1. LF UK a VFN v Praze
Ke Karlovu 6, 128 08 Praha 2
e-mail: macekp@gentlemail.com
Sources
1. Znaor A, Lortet-Tieulent J, Laversanne M, Jemal A, Bray F. International variations and trends in renal cell carcinoma incidence and mortality. Eur Urol. 2015; 67(3): 519–530.
2. www.svod.cz, přístup 18. 2. 2017
3. Capitanio U, Montorsi F. Renal cancer. The Lancet 387(10021): 894–906.
4. Ljungberg B, Bensalah K, Canfield S, et al. EAU guidelines on renal cell carcinoma: 2014 update. Eur Urol. 2015; 67(5): 913–924.
5. Vigneswaran HT, Lec P, Brito J, et al. Partial nephrectomy for small renal masses: do teaching and nonteaching institutions adhere to guidelines equally? J Endourol. 2016; 30(6): 714–721.
6. Novák K. Laparoskopická resekce ledviny. Urol List. 2010; 8(1): 39–42.
7. Stránský P, Hora M, Hrbáček J, et al. Ischemie ledviny při resekcích ledvin a možnosti jejího ovlivnění. Ces Urol 2015; 19(2): 118–130.
8. Kutikov A, Uzzo RG. The R.E.N.A.L. nephrometry score: a comprehensive standardized system for quantitating renal tumor size, location and depth. J Urol. 2009; 182(3): 844–853.
9. Ficarra V, Novara G, Secco S, et al. Preoperative aspects and dimensions used for an anatomical (PADUA) classification of renal tumours in patients who are candidates for nephron-sparing surgery. Eur Urol. 2009; 56(5): 786–793.
10. Simmons MN, Hillyer SP, Lee BH, et al. Diameter-axial-polar nephrometry: integration and optimization of R.E.N.A.L. and centrality index scoring systems. J Urol. 2012; 188(2): 384–390.
11. Simmons MN, Ching CB, Samplaski MK, Park CH, Gill IS. Kidney tumor location measurement using the C index method. J Urol. 2010; 183(5): 1708–1713.
12. Hakky TS, Baumgarten AS, Allen B, et al. Zonal NePhRO scoring system: a superior renal tumor complexity classification model. Clin Genitourin Cancer 2014; 12(1): e13–18.
13. Tannus M, Goldman SM, Andreoni C. Practical and intuitive surgical approach renal ranking to predict outcomes in the management of renal tumors: a novel score tool. J Endourol. 2014; 28(4): 487–492.
14. Tobert CM, Shoemaker A, Kahnoski RJ, Lane BR. Critical appraisal of first-generation renal tumor complexity scoring systems: Creation of a second-generation model of tumor complexity. Urol Oncol. 2015; 33(4): 167.e1–6.
15. Bjork J, Back SE, Sterner G, et al. Prediction of relative glomerular filtration rate in adults: new improved equations based on Swedish Caucasians and standardized plasma-creatinine assays. Scand J Clin Lab Inv. 2007; 67(7): 678–695.
16. Mukaka MM. Statistics corner: a guide to appropriate use of correlation coefficient in medical research. Malawi Med J. 2012; 24(3): 69–71.
17. Shin TY, Komninos C, Kim DW, et al. A novel mathematical model to predict the severity of postoperative functional reduction before partial nephrectomy: the importance of calculating resected and ischemic volume. J Urol. 2015; 193(2): 423–429.
18. Zhou L, Cao Y, Bian T, et al. Number of renal columns invaded by tumor: a novel parameter for predicting complexity and outcomes of off-clamp open partial nephrectomy. J Am Coll Surg. 2015; 221(2): 539–49.e1.
19. Leslie S, Gill IS, de Castro Abreu AL, et al. Renal tumor contact surface area: a novel parameter for predicting complexity and outcomes of partial nephrectomy. Eur Urol. 2014; 66(5): 884–893.
20. Tomaszewski JJ, Cung B, Smaldone MC, et al. Renal pelvic anatomy is associated with incidence, grade, and need for intervention for urine leak following partial nephrectomy. Eur Urol. 2014; 66(5): 949–955.
21. Roscigno M, Ceresoli F, Naspro R, et al. Predictive accuracy of nephrometric scores can be improved by adding clinical patient characteristics: a novel algorithm combining anatomic tumour complexity, body mass index, and Charlson comorbidity index to depict perioperative complications after nephron-sparing surgery. Eur Urol. 2014; 65(1): 259–262.
22. Minervini A, Vittori G, Salvi M, et al. Analysis of surgical complications of renal tumor enucleation with standardized instruments and external validation of PADUA classification. Ann Surg Oncol. 2013; 20(5): 1729–1736.
23. Kriegmair MC, Hetjens S, Mandel P, et al. Tumor size and invasiveness matters for partial nephrectomy: external validation and modification of the arterial based complexity score. J Surg Oncol. 2017; doi: 10.1002/jso.24565.
24. Borgmann H, Reiss AK, Kurosch M, et al. R.E.N.A.L. score outperforms PADUA score, C-Index and DAP score for outcome prediction of nephron sparing surgery in a selected cohort. J Urol. 2016; 196(3): 664–671.
25. Kriegmair MC, Mandel P, Moses A, et al. Defining renal masses: comprehensive comparison of RENAL, PADUA, NePhRO, and C-Index score. Clin Genitourin Cancer. 2016; pii: S1558–7673(16)30233–6.
26. Hou W, Yan W, Ji Z. Anatomic features involved in technical complexity of partial nephrectomy. Urol. 2015; 85(1): 1–7.
27. Kwon T, Jeong IG, Ryu J, et al. Renal function is associated with nephrometry score after partial nephrectomy: a study using Diethylene Triamine Penta-Acetic Acid (DTPA) renal scanning. Ann Surg Oncol. 2015; 22 Suppl 3: S1594–600.
28. Li M, Gao Y, Cheng J, et al. Diameter-axial-polar nephrometry is predictive of surgical outcomes following partial nephrectomy. Medicine. 2015; 94(30): e1228.
Labels
Paediatric urologist Nephrology UrologyArticle was published in
Czech Urology

2017 Issue 2
-
All articles in this issue
- Využití flexibilní nefroskopie k extrakci urolitiázy při laparoskopické a roboticky asistované pyeloplastice
- Intravezikální chemoterapie s využitím tepelné energie u pacientů s uroteliálním karcinomem močového měchýře bez invaze svaloviny
- Dysfunkce mikce u pacientů s posttraumatickou míšní lézí - úloha urologa
- Trombóza povrchové dorzální žíly penisu (Penilní Mondorova choroba)
- Zpráva o proběhlém 5. ročníku Video‑semináře Tipy a triky v Urologické operativně
- Zpráva z workshopu Sekce urodynamiky, neurourologie a urogynekologie ČUS ČLS JEP: Funkční urologie - Novinky 2017
- 2. ročník konference KNOU, pohled mladého lékaře
- ASSOC. PROF. ROMAN ZACHOVAL, M.D., PH.D., MBA, CELEBRATED HIS 50TH BIRTHDAY
- Sledování a léčba pacientů po radikální prostatektomii s pozitivními okraji preparátu
- Funkční výsledky pyeloplastiky provedené v kojeneckém věku
- Nefrometrická skóre první a druhé generace pro predikci peri- a pooperačních výsledků resekcí ledvin
- Efficacy and safety of extracorporeal shock wave lithotripsy in the 21th century – controversy and clinical practice.
- Spontánní ruptura renálního angiomyolipomu
- Czech Urology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Trombóza povrchové dorzální žíly penisu (Penilní Mondorova choroba)
- Dysfunkce mikce u pacientů s posttraumatickou míšní lézí - úloha urologa
- Sledování a léčba pacientů po radikální prostatektomii s pozitivními okraji preparátu
- ASSOC. PROF. ROMAN ZACHOVAL, M.D., PH.D., MBA, CELEBRATED HIS 50TH BIRTHDAY
