Intravezikální chemoterapie s využitím tepelné energie u pacientů s uroteliálním karcinomem močového měchýře bez invaze svaloviny
Intravesical chemotherapy using heat energy in patiens with urothelial carcinoma of the urinary bladder
Major statement:
The authors present an overview on intravesical termotherapy using heat energy in treatment of patients with non-muscle invasive bladder cancer. Furthermore, their own experience with this method is presented.
Intravesical chemotherapy currently represents an alternative treatment in patiens with high risk non-muscle invasive urothelial carcinoma failing other intravesical treatment or refusing radical cystectomy. Substitution of BCG instillation during BCG shortage represents another indication. Currently, there are long-term data on chemohyperthermia Synergo available (heat energy applied to bladder wall using radiofrequency). Termotherapy is a new method connecting warming up of the chemotherapy agent and its recirculation inside the bladder. Better cell penetration is achieved in both systems. Both methods have not become standard clinical practice yet. In this overview article, a single site experience with both procedures is presented.
KEY WORDS:
Urinary bladder carcinoma, non-muscle-invasive bladder cancer, intravesical chemotherapy, termotherapy, chemohyperthermy.
Authors:
Antonín Brisuda; Marek Babjuk; Jozef Stolz
Authors‘ workplace:
Urologická klinika 2. LF UK a FN Motol, Praha
Published in:
Ces Urol 2017; 21(2): 122-128
Category:
Review article
Overview
Hlavní stanovisko práce:
Autoři předkládají přehledový článek o intravezikální chemoterapii za použití tepelné energie při léčbě svalovinu neinfiltrujících nádorů močového měchýře a vlastní zkušenosti s touto léčbou.
Intravezikální chemoterapie s využitím tepelné energie představuje v současné době alternativní léčebný postup u pacientů s rizikovým svalovinu neinfiltrujícím uroteliálním karcinomem močového měchýře, u kterých selhala jiná instilační léčba a odmítají radikální cystektomii. Další indikací je substituce BCG terapie při absenci vakcíny. V současné době již existují data z dlouhodobějších zkušeností s chemohypertermií Synergo (tepelná energie dodávaná do stěny měchýře pomocí radiofrekvence). Termoterapie je nová metoda spočívající v zahřátí instilovaného chemoterapeutika a jeho recirkulaci v měchýři. V obou případech je umožněna jeho lepší penetrace do buněk. Obě metody zatím nejsou v klinické praxi standardem. V přehledovém článku jsou uvedeny zkušenosti našeho pracoviště s oběma metodami.
KLÍČOVÁ SLOVA:
Karcinom močového měchýře, svalovinu neinfiltrující nádor, intravezikální chemoterapie, termoterapie, chemohypertermie.
ÚVOD
Nádory močového měchýře (NMM) představovaly v České republice (ČR) k 31. 12. 2014 po nádorech ledvin druhou nejčastější malignitu močového ústrojí a odečteme‑li kožní nádory, tak sedmou nejčastější malignitu vůbec (1). Jejich incidence v ČR v posledních deseti letech stagnuje zhruba na hodnotě 21 případů na 100 000 obyvatel, přičemž u mužů je přibližně trojnásobná než u žen (1). Převážnou většinu NMM tvoří uroteliální karcinom (UK) (90 %) (2). Uroteliální karcinom má velmi variabilní průběh i prognózu (3). Pro vysoké riziko recidivy je u svalovinu neinfiltrujících nádorů (NMIBC) doporučena adjuvantní instilační léčba (4). Jednorázová instilace po transuretrální resekci (TUR) je dostatečnou léčbou u nádorů s nízkým rizikem (5). U nádorů se středním a vysokým rizikem je doporučena ambulantní intravezikální chemoterapie (CHT), respektive BCG instilace, která je v prevenci recidiv účinnější (6). Karcinom in situ (CIS) nelze pomocí TUR eradikovat a instilace BCG je plně indikována (7). Pacienti recidivující po intravezikální chemoterapii mohou profitovat též z instilací BCG (8). Problém ovšem představují pacienti, u kterých je diagnostikována recidiva o nízkém stupni diferenciace (HG) po BCG instilacích. Přehled a definice „BCG selhání“ je uvedena v doporučení EAU (4).
Jedinou onkologicky bezpečnou alternativou léčby těchto pacientů zůstává radikální cystektomie, kterou někteří pacienti nejsou ochotni akceptovat nebo pro ně pro vysoký věk či komorbidity představuje neúnosně vysoké riziko. Dalším aspektem posledních let je nízká dostupnost BCG vakcíny v ČR. Za uvedené situace se do popředí dostávají alternativní měchýř šetřící postupy, kde základem léčby nadále zůstává intravezikální CHT, snahou je však zefektivnění jejího účinku.Došlo: 9. 1. 2017
CHEMOHYPERTERMIE SYNERGO
Princip
Kombinace intravezikální CHT a hypertermie je známá již téměř 15 let, nicméně klinické zkušenosti jsou chudé. Dostupných dat není mnoho, což je dáno nákladností systému jako takového včetně originálních setů, které jsou použitelné pouze jednou. První prospektivní studie byla publikována již v roce 2003, kdy při sledování 24 měsíců byl prokázán jednoznačný benefit chemohypertermie (C‑HT) ve smyslu délky přežití bez recidivy a pravděpodobnosti recidivy (9). Tyto výsledky byly potvrzeny stejnými autory i při desetiletém sledování (10). Chemohypertermie Synergo je založena na současném působení tří faktorů: radiofrekvenční energie (mikrovlnné záření) (RF), hypertermie a CHT. Při klasické studené intravezikální chemoterapii dochází k pasivní difuzi terapeutického agens do buněk urotelu. Zlepšení efektivity lze dosáhnout např. restrikcí tekutin v den instilace nebo optimalizací pH moči (a tím stabilizací chemoterapeutika). Při mikrovlnné hypertermii dochází ke specifickým změnám v nádorových buňkách: tvorba mikropórů v membráně = zvýšené vychytávání MMC; zvýšení mobility léčiva = aktivní difuze do buněk; ohřev tkání = vazodilatace = lepší průnik CHT do stěny měchýře a uvolnění nádorových buněk ze spojů (11). Systém Synergo má zabudovaný vlastní počítač a software (Obr. 1). Jedná se o intravezikální irigační systém a jednotku, která dodává do tkáně energii. Systém zahrnuje RF generátor, který dodává RF energii o kmitočtu 915 MHz, recirkulační jednotku, mikroprocesor a software. Ovládání probíhá na dotykové obrazovce, kde jsou po celou dobu zobrazeny všechny aktuální parametry a průběh instilace lze dle potřeby modifikovat. Speciální katétr obsahuje několik sond, které se po zavedení do měchýře rozvinou a měří aktuální teplotu stěny měchýře na několika místech, včetně prostatické uretry. Roztok s chemoterapeutikem recirkuluje přes močový měchýř a je, na rozdíl od prosté termoterapie (viz dále), průběžně chlazen. Udržuje se tak konstantní teplota 42 °C (+/ - 2 °C). Rychlost recirkulace lze průběžně měnit dle aktuální teploty stěny měchýře, stejně tak i množství dodané energie. Ve srovnání s termoterapií se jedná o složitější, časově náročnější a dražší systém, nicméně vzhledem k možnosti individuálního nastavení u konkrétního pacienta (dle typu tkáně, např. jizvy po TUR, vazodilatace apod.) sofistikovanější. Dle doporučení výrobce (Medical Enterprises Europe B.V., Nizozemsko) existují dva léčebné protokoly, a to profylaktický a ablační, nicméně optimální schéma zhotovené na základě klinických dat zatím není k dispozici. Profylaktický protokol je doporučen k prevenci vzniku recidivy u pacientů se středním a vysokým rizikem. V indukční fázi se aplikuje 2x20 mg Mitomycinu C (MMC) á 30 minut v šesti týdenních intervalech. Udržovací fáze zahrnuje instilace á šest týdnů po dobu jednoho roku a instilace á osm týdnů v dalším roce. Pro tumory s vysokým rizikem je vhodný ablační protokol. Ablační (neoadjuvatní) je indikován u pacientů, kde není možná kompletní resekce, měli CIS v poslední TUR, jsou neúnosní anestezie nebo dle uvážení urologa (rychle recidivující nádory s vysokým rizikem progrese apod.). Schéma spočívá v instilaci 2x 40 mg MMC á 30 minut v osmi týdenních intervalech a v udržovací fázi stejné jako v profylaktickém protokolu. U velmi rizikových nádorů se hodnotí efekt léčby po čtyřech týdnech pomocí cystoskopie a cytologie moči (CSK), eventuálně TUR biopsie. V průběhu léčby jsou pacienti dispenzarizováni běžným způsobem.

Dostupná data
V systematické metaanalýze bylo v roce 2011 zhodnoceno 22 relevantních studií srovnávajících C‑HT a „studenou“ intravezikální chemoterapii s MMC. Primární cíl byl čas do recidivy a sekundární cíle – čas do progrese, míra zachování měchýře a nežádoucí vedlejší účinky léčby (12). Recidiva byla pozorována u méně pacientů s C‑HT než s CHT (o 59 %). Vzhledem ke krátkému sledování nebylo možno relevantně zhodnotit čas do recidivy a progrese. Celková míra zachování měchýře byla u C‑HC 87,6 %, což je více než u pacientů po CHT, nicméně validní srovnávací studie schází. Vedlejší nežádoucí účinky byly u C‑HC častější než u CHT, ale nevýznamně. Jednalo se nejčastěji o spazmy měchýře a cystalgie (21,6 % resp. 17,5 %). Bezprostřední komplikace léčby byly polakisurie, dysurie, nykturie a hematurie, vyskytly se u 25,6 %, nicméně byly hodnoceny jako mírné a přechodné. Nespecifická kožní vyrážka se objevila u 7,5 % pacientů, což je srovnatelné s CHT (13). Vzácné závažné komplikace ve smyslu svraštělého měchýře a těžké inkontinence byly publikovány ve dvou studiích (14). Prospektivní multicentrická randomizovaná nezaslepená studie srovnávající C‑HT a BCG u pacientů s NMIBC se středním a vysokým rizikem byla publikována nedávno (15). Celkem 190 pacientů bylo randomizováno do C‑HT ramene (šest týdenních instilací a šest udržovacích) a do BCG ramene (Moralesovo schéma s udržovací léčbou do 12. měsíce). Primárním cílem studie bylo přežití bez recidivy (RFS) během 24 měsíců sledování v intention‑to‑treat a per‑protocol analýze. Přežití bez recidivy ve skupině C‑HT bylo 78,1 % a ve skupině BCG 64,8 % (p=0,08), nicméně v per‑protocol analýze bylo dosaženo signifikantního rozdílu (p=0,02). Míra progrese byla <2 % v obou skupinách. Vedlejší účinky byly obdobné. Limitací studie byl fakt, že byla uzavřena předčasně a nebyla statisticky dostatečně silná. Autoři uzavírají, že léčba pomocí C‑HT je bezpečná a v prevenci recidiv je u rizikové skupiny NMIBC při 24měsíčním sledování účinnějsí než BCG.
Naše zkušenosti
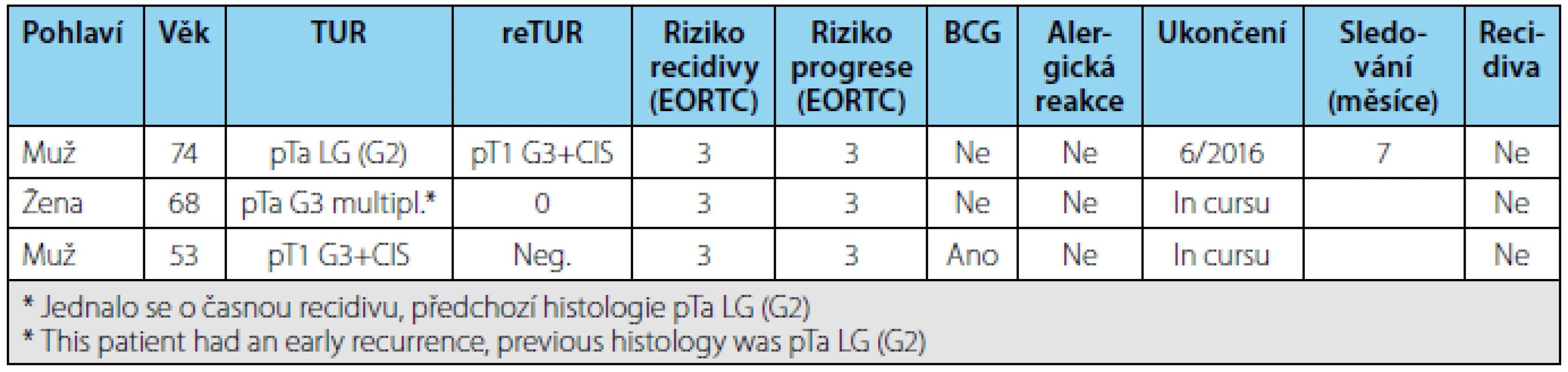
Na našem pracovišti máme k dispozici systém Synergo (Medical Enterprises Europe B.V., Amstelveen, Nizozemsko; model 2001) od 12/2015. Zatím léčba proběhla/probíhá u 3 pacientů (Tab. 1). U jednoho pacienta byla léčba časně ukončena pro netoleranci náplně měchýře a u dalšího léčba začíná. Všichni pacienti měli vysoké riziko recidivy i progrese, u jednoho se jednalo u HG recidivu po BCG léčbě. U všech bylo indikováno ablační schéma. U jednoho pacienta (muž, 53 let) byla těsně před iniciací provedena kontrolní flexibilní CSK s nálezem drobného tumoru v předchozí resekční ploše. Při kontrolní CSK po indukční fázi léčby byl měchýř bez tumoru. Všichni pacienti pokračují v udržovací fázi léčby a jsou bez recidivy. U jednoho pacienta (muž, 74 let) se po třetí instilaci v rámci udržovací fáze objevila těžká inkontinence. Léčba byla ukončena. Při urgentní CSK a TUR byl zjištěn malokapacitní měchýř s oboustranným refluxem. Měchýř byl histologicky bez recidivy. Kapacita měchýře je kolem 100 ml a nemocný trpí na recidivující cystitidy s intermitentním městnáním a intermitentně zaváděným permanentním katétrem. Má mírnou renální insuficienci, je kontinentní, nicméně pro pokračující intramurální fibrózu mu byly oboustranně zavedeny pig‑tail katétry. Další dva pacienti nemají závažnější komplikace, pouze několik dní po instilaci mírné a rychle ustupující dysurie a cystalgie.
INTRAVEZIKÁLNÍ TERMOTERAPIE
Intravezikální termoterapie je relativně nová metoda spočívající v prostém ohřátí chemofarmaka na konstantní teplotu u každého pacienta bez rozdílu (16). V současnosti jsou v ČR dostupné minimálně dva systémy, a to Pelvix TT (Archie Samuel) a Combat BRS (Combat Medical). Princip HIVEC (Hyperthermic Intra‑VEsical Chemotherapy) je vcelku jednoduchý. Jedná se o uzavřený, suchý, zevní systém, který ohřívá roztok MMC a za stálého tlaku jej recirkuluje přes močový měchýř. Teplota se udržuje konstantní 43 °C, průtok je 200 ml/min přes trojcestný katétr. Výměnný set u systému Combat BRS (neresterilizovatelný) se skládá z aluminiového výměníku tepla, teplotní sondy, hadic a trojcestného silikonového katétru o kalibru 16 F. Na konci každé instilace je obsah měchýře a celého setu vypuštěn přímo do sběrného sáčku, což minimalizuje kontakt obsluhy a pacienta s chemoterapeutikem (Obr. 2). V současné době nejsou k dispozici silná data, která by prokázala vliv termoterapie MMC na míru vzniku recidiv u pacientů po TUR NMIBC. V roce 2017 by měly být k dispozici první výsledky dvou prospektivních randomizovaných studií (HIVEC I a HIVEC II) a další jsou v běhu. Jedná se o pacienty se středním rizikem po TUR a jednorázové pooperační instilaci MMC. V HIVEC I jsou tři léčebná ramena (vždy MMC 40 mg, v jednom rameni navíc 30 minut termoterapie, v dalším 60 minut), schéma jsou čtyři instilace v týdenních intervalech a další tři instilace v měsíčních intervalech. V HIVEC II jsou dvě léčebná ramena (MMC 40 mg + 60 minut termoterapie, respektive MMC bez termoterapie), schéma je šest instilací v týdenních intervalech. Primární cíle jsou u obou projektů stejné, a to přežití bez recidivy během 24 měsíců sledování. Sekundární cíle jsou míra vzniku recidiv, tolerance léčby a kvalita života.

Naše zkušenosti
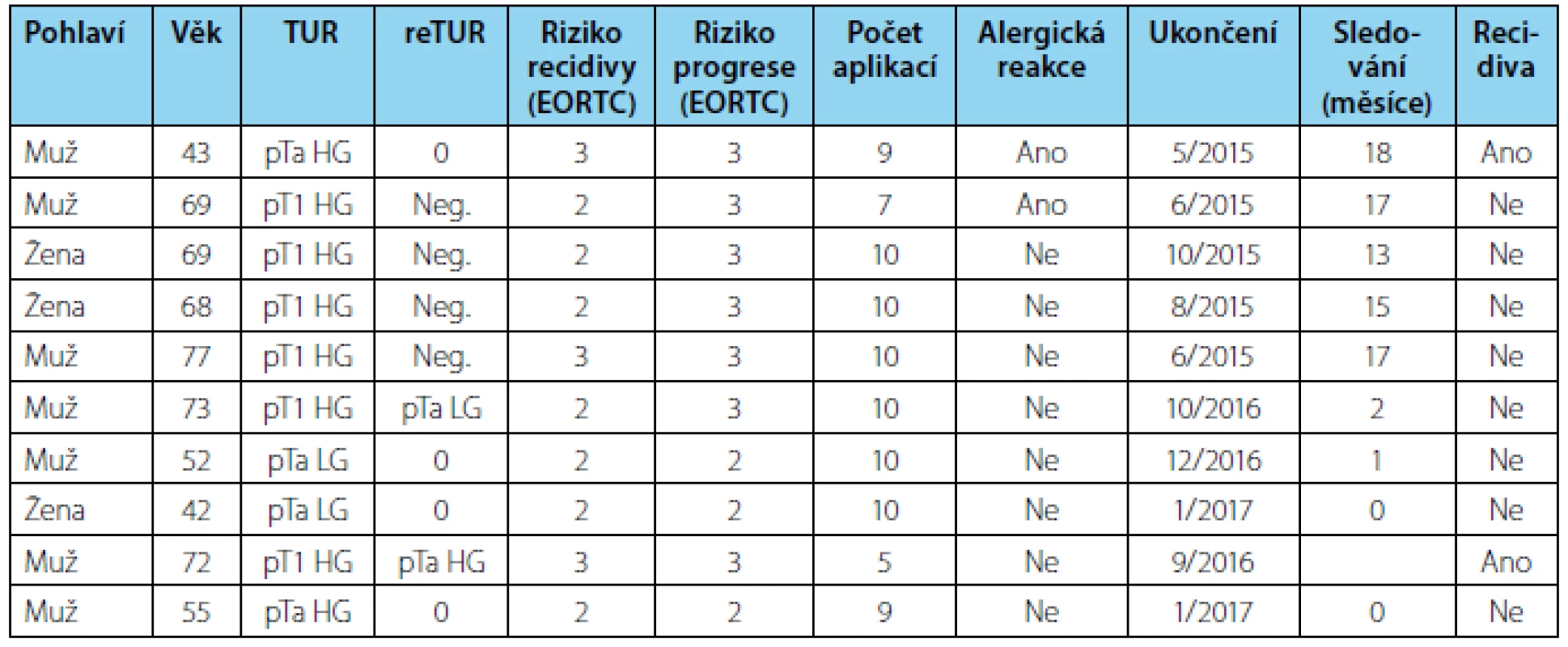
Na našem pracovišti máme v současné době k dispozici systém Combat BRS, prvních pět pacientů bylo však léčeno pomocí systému Pelvix TT. Princip i nastavení jsou u obou systémů obdobné. Léčebné schéma je u všech pacientů totožné: čtyři aplikace 40 mg MMC v týdenních intervalech a dále šest aplikací v měsíčních intervalech, každá aplikace trvá vždy 60 minut. S léčbou se začalo v 12/2014. V současné době je léčba ukončena u téměř deseti pacientů (Tab. 2). Dalších šest pacientů je rozléčeno nebo léčba rozplánována. První dva pacienti měli po deváté respektive sedmé aplikaci silnou kožní alergickou reakci, kvůli které byla léčba ukončena. První z nich měl hned při první kontrolní CSK LG recidivu. Nyní má opět recidivu po ukončení šesti úvodních aplikací BCG a je u něj zvažována radikální cystektomie. Další pacient měl recidivu po pěti aplikacích a také byl indikován k BCG léčbě, která v současné době probíhá. U zhruba 50 % pacientů se vyskytly přechodně dysurie mírného stupně nebo cystitidy, které byly bez problémů zvládnuty symptomaticky nebo pomocí ATB a nebyly důvodem přerušení či ukončení léčby. U některých nemocných se objevují v průběhu recirkulace urgence a systém je pak potřeba opakovaně zapínat po přechodném upuštění náplně z měchýře tak, aby bylo dosaženo požadovaných 60 minut recirkulace.
ZÁVĚR
Alternativní měchýř šetřící postupy při léčbě rizikových NMIBC se dostávají do popředí zájmu v situaci nedostatku BCG vakcíny a zejména při selhání BCG nebo klasické intravezikální CHT. Využití tepelné energie při instilaci chemoterapeutika a tedy zvýšení jeho efektivity tímto způsobem je jedna z možností. Dle dostupných dat je C‑HT Synergo metodou volby u nejrizikovějších forem NMIBC, nicméně je nutno vzít v potaz vyšší náklady na pořízení setu a relativně vyšší invazivita při zavádění speciálního katétru s teplotními čidly. U jednoho ze tří našich pacientů se navíc vyskytla závažná komplikace ve formě malokapacitního měchýře s oboustranným městnáním a renální insuficiencí, nicméně tato komplikace je v literatuře popsána vzácně. Termoterapie je technicky, časově i finančně méně náročná, zavádí se tenčí silikonový katétr školenou sestrou a není ani významně zatěžující pro obsluhující personál. Dostupná data jsou zatím sporá. V nejbližších letech by měly být k dispozici výsledky z prospektivních randomirandomizovaných studií ohledně účinnosti intravezikální termoterapie. Podstatný je fakt, že ani jedna z obou metod zatím nebyla doporučena a schválena v ČR odbornou společností jako standard a není tedy hrazena plátcem zdravotní péče (kromě MMC).
Přijato: 21. 3. 2017
Střet zájmů: žádný
Prohlášení o podpoře: Podpořeno projektem koncepčního rozvoje výzkumné organizace 00064203.
Kontaktní adresa:
MUDr. Antonín Brisuda, FEBU
Urologická klinika 2. LF UK a FN Motol
V Úvalu 84, 150 06 Praha 5
e‑mail: antonin.brisuda@fnmotol.cz
Sources
1. Mužík J, Dušek L, Babjuk M, et al. Uroweb – webový portál pro analýzu a vizualizaci epidemiologie, diagnostiky a léčby urologických malignit [online]. Masarykova univerzita, Brno, 2017. [cit. 2017–02–16]. Dostupný z WWW: http://www.uroweb.cz. ISSN 1804–6371. Verze 1.6d.
2. Pešl M, Soukup V, Babjuk M, et al. Hodnocení významu klinicko-patologických prognostických faktorů u nádorů močového měchýře neinfiltrujících svalovinu. Ces Urol 2011; 15(4): 222–228.
3. Dvořáček J, Babjuk M. Onkourologie. Praha: Galén, Karolinum 2005, 589 s., ISBN 80–7262–349–4 (Galén), 80–246–1108–2 (Karolinum).
4. Babjuk M, Burger M, Compérat E, et al. EAU Guidelines on non-muscle-invasive urothelial carcinoma of the bladder: Update 2016. Eur Urol. 2017 Mar; 71(3): 447–461.
5. Sylvester RJ, Oosterlinck W, Holmang S, et al. Systematic review and individual patient data meta‑analysis of randomized trials comparing a single immediate instillation of chemotherapy after transurethral resection with transurethral resection alone in patients with stage pTa‑pT1 urothelial carcinoma of the bladder: which patients benefit from the instillation? Eur Urol. 2016 Feb; 69(2): 231–244.
6. Järvinen R, Kaasinen E, Sankila A, Rintala E. FinnBladder Group. Long‑term efficacy of maintenance bacillus Calmette‑Guerin versus maintenance mitomycin C instillation therapy in frequently recurrent TaT1 tumours without carcinoma in situ: a subgroup analysis of the prospective, randomised FinnBladder I study with a 20-year follow‑up. Eur Urol, 2009; 56 : 260.
7. Sylvester RJ, van der Meijden AP, Witjes JA, Kurth K. Bacillus calmette.guerin versus chemotherapy for the intravesical treatment of patients with carcinoma in situ of the bladder: a meta.analysis of the published results of randomized clinical trials. J Urol. 2005; 174 : 86.
8. Malmstrom PU, Sylvester RJ, Crawford DE, et al. An individual patient data meta.analysis of the long.term outcome of randomised studies comparing intravesical mitomycin C versus bacillus Calmette.Guerin for non.muscle.invasive bladder cancer. Eur Urol 2009; 56 : 247.
9. Colombo R1, Da Pozzo LF, Salonia A, et al. Multicentric study comparing intravesical chemotherapy alone and with local microwave hyperthermia for prophylaxis of recurrence of superficial transitional cell carcinoma. J Clin Oncol. 2003 Dec 1; 21(23): 4270.4276.
10. Colombo R, Salonia A, Leib Z, Pavone.Macaluso M, Engelstein D. Long.term outcomes of a randomized controlled trial comparing thermochemotherapy with mitomycin.C alone as adjuvant treatment for non.muscle.invasive bladder cancer (NMIBC). BJU Int. 2011; 107 : 912.918.
11. Internetovy portal www.synergo.medical. com.
12. Lammers RJ, Witjes JA, Inman BA, et al. The role of a combined regimen with intrave sical chemotherapy and hyperthermia in the management of non.muscle.invasive bladder cancer: a systematic review. Eur Urol. 2011; 60 : 81.93.
13. Halachmi S, Moskovitz B, Maffezzini M, et al. Intravesical mitomycin C combined with hyperthermia for patients with T1G3 transitional cell carcinoma of the bladder. Urol Oncol. 2011 May.Jun; 29(3): 259.264.
14. Colombo R, Da Pozzo LF, Lev A, et al. Local microwave hyperthermia and intravesical chemotherapy as bladder sparing treatment for select multifocal and unresectable superficial bladder tumors. J Urol. 1998; 159 : 783.787.
15. Arends TJ, Nativ O, Maffezzini M, et al. Results of a randomised controlled trial comparing intravesical chemohyperthermia with Mitomycin C versus Bacillus Calmette.Guerin for adjuvant treatment of patients with intermediate - and high.risk non.muscle.invasive bladder cancer. Eur Urol. 2016 Jun; 69(6): 1046.1052.
16. Sousa A, Pineiro I, Rodriguez S, et al. Recirculant hyperthermic IntraVEsical chemotherapy (HIVEC) in intermediate.high.risk non.muscle.invasive bladder cancer. Int J Hyperthermia. 2016 Jun; 32(4): 374.380.
Labels
Paediatric urologist Nephrology UrologyArticle was published in
Czech Urology

2017 Issue 2
-
All articles in this issue
- Využití flexibilní nefroskopie k extrakci urolitiázy při laparoskopické a roboticky asistované pyeloplastice
- Intravezikální chemoterapie s využitím tepelné energie u pacientů s uroteliálním karcinomem močového měchýře bez invaze svaloviny
- Dysfunkce mikce u pacientů s posttraumatickou míšní lézí - úloha urologa
- Trombóza povrchové dorzální žíly penisu (Penilní Mondorova choroba)
- Zpráva o proběhlém 5. ročníku Video‑semináře Tipy a triky v Urologické operativně
- Zpráva z workshopu Sekce urodynamiky, neurourologie a urogynekologie ČUS ČLS JEP: Funkční urologie - Novinky 2017
- 2. ročník konference KNOU, pohled mladého lékaře
- ASSOC. PROF. ROMAN ZACHOVAL, M.D., PH.D., MBA, CELEBRATED HIS 50TH BIRTHDAY
- Sledování a léčba pacientů po radikální prostatektomii s pozitivními okraji preparátu
- Funkční výsledky pyeloplastiky provedené v kojeneckém věku
- Nefrometrická skóre první a druhé generace pro predikci peri- a pooperačních výsledků resekcí ledvin
- Efficacy and safety of extracorporeal shock wave lithotripsy in the 21th century – controversy and clinical practice.
- Spontánní ruptura renálního angiomyolipomu
- Czech Urology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Trombóza povrchové dorzální žíly penisu (Penilní Mondorova choroba)
- Dysfunkce mikce u pacientů s posttraumatickou míšní lézí - úloha urologa
- Sledování a léčba pacientů po radikální prostatektomii s pozitivními okraji preparátu
- ASSOC. PROF. ROMAN ZACHOVAL, M.D., PH.D., MBA, CELEBRATED HIS 50TH BIRTHDAY
