Primární vaskulitidy – současná diagnostika a léčba
Primary vasculitides – current diagnostics and therapy
By term „vasculitis“ inflammatory disease of blood vessels is designated that leads to vessel wall destruction followed by proliferation and occlusion of their lumina. Basic condition for this diagnosis is that vessel wall is a primary site of the pathological process. Clinical syndromes are a consequence of this process resulting into ischaemia of tissues supplied by the affected vessels and with constitutional symptoms associated to the inflammatory disease. Vasculitis can occur de novo as a primary involvement of vessel wall of unknown aetiology or it develops secondary to other diseases. The diagnosis of vasculitis is usually based on pathological findings from biopsy or abnormalities detected by imaging methods. This review describes the common primary vasculitides, their diagnostics and management.
Keywords:
vasculitis – arteritis – angiogramy – Biopsy – immunosuppression
Authors:
Radim Bečvář
Authors‘ workplace:
Revmatologický ústav a Revmatologická klinika 1. LF UK, Praha
Published in:
Čes.-slov. Patol., 56, 2020, No. 2, p. 74-82
Category:
Reviews Article
Overview
Termín „vaskulitida“ označuje zánětlivé onemocnění cév vedoucí k destrukci cévní stěny, následné proliferaci a k jejich uzávěru. Podmínkou pro stanovení diagnózy je, aby cévní stěna byla primárním místem patologického procesu. Jako důsledek vznikají klinické syndromy na podkladě ischémie tkání zásobovaných poškozenými cévami a celkových projevů, které provázejí zánětlivé onemocnění. Vaskulitida může vzniknout de novo jako primární postižení cévní stěny neznámé etiologie nebo provázet jiné choroby. Diagnóza vaskulitidy je dána především histopatologickým nálezem z biopsie a někdy patologickými změnami, které prokážeme zobrazovacími metodami. Tento přehledný článek je věnován častějším primárním vaskulitidám, jejich diagnostice a léčbě.
Klíčová slova:
vaskulitida – arteriitida – Biopsie – angiografie – imunosuprese
Termín „vaskulitida“ označuje zánětlivé onemocnění cév vedoucí k destrukci cévní stěny, následné proliferaci a k jejich uzávěru. Podmínkou pro stanovení diagnózy je, aby cévní stěna byla primárním místem patologického procesu (1). Jako důsledek vznikají klinické syndromy na podkladě ischémie tkání zásobovaných poškozenými cévami a celkových projevů, které provázejí zánětlivé onemocnění (horečka, úbytek hmotnosti, anorexie).
Vaskulitida může vzniknout de novo jako primární postižení cévní stěny neznámé etiologie, nebo se objeví sekundárně při některých infekčních onemocněních, nádorech a jiných procesech. Také některá difúzní onemocnění pojiva jako revmatoidní artritida, systémový lupus erytematodes, systémová sklerodermie, dětská dermatomyozitida mohou být provázena vaskulitidou. Tyto manifestace se liší svým původem, rozsahem a kalibrem postižených cév (2).
KLASIFIKACE VASKULITID
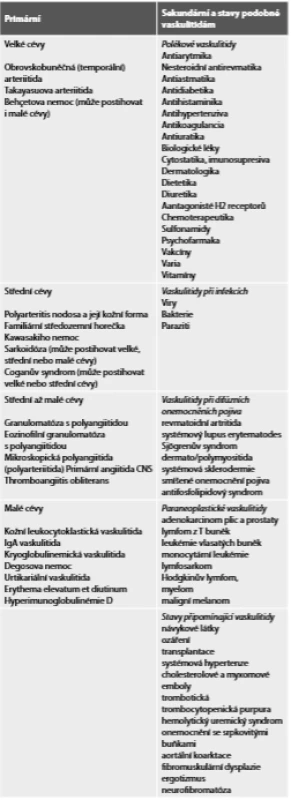
Klasifikace vaskulitid je složitý problém, neboť příčina je většinou neznámá a klinické obrazy jsou velmi variabilní a mohou se překrývat. Konečná diagnóza je zpravidla dána histopatologickým nálezem z biopsie, v některých případech stačí změny ze zobrazovací metody. V posledních desetiletích vzniklo několik klasifikací vytvořených v American College of Rheumatology (ACR). Nejnovější klasifikace Balla upravená Fesslerem je kombinací klasifikace ACR a závěrů konference v Chapel Hill. Zahrnuje primární a sekundární vaskulitidy a stavy připomínající vaskulitidy (Tab. 1) (3).
Vaskulitidy velkých tepen
Obrovskobuněčná (Hortonova, temporální) arteriitida
Obrovskobuněčná arteriitida (OBA) je vaskulitida neznámého původu postihující větve zevní i vnitřní karotidy u osob středního a vyššího věku. OBA postihuje téměř výhradně jedince bílé rasy starší 50 let s převahou žen. Jsou značné rozdíly v incidenci podle geografických oblastí. Nejvyšší počty byly zjištěny na severu USA a v severní Evropě.
Příčina vzniku OBA je dosud nejasná. Výskyt omezený na osoby starší 50 let by ukazoval na souvislost s procesem stárnutí, ale mechanismus vzniku je předmětem hypotéz. Stále se uvažuje o genetické predispozici k této nemoci, neboť u těchto nemocných byla zjištěna zvýšená incidence antigenu HLA-DR4 a zejména alel DRB1. Uvažuje se také o roli infekce, protože u části nemocných byly nalezeny zvýšené protilátky proti viru parainfluenzy. Spouštěcím agens by mohly být infekce Mycoplasma pneumoniae, Chlamydia pneumoniae nebo parvovirem B19 (4). Imunologické procesy se nepochybně účastní patogeneze OBA. Zásadní význam mají změny buněčné imunity zejména cirkulující aktivované monocyty, které secernují prozánětlivé cytokiny. Ve stěně arteria temporalis byly nalezeny CD4+ T lymfocyty a aktivované makrofágy, dále depozita imunoglobulinů a složek komplementu, která mohou představovat buď protilátky proti stěně tepny, nebo cirkulující imunitní komplexy.
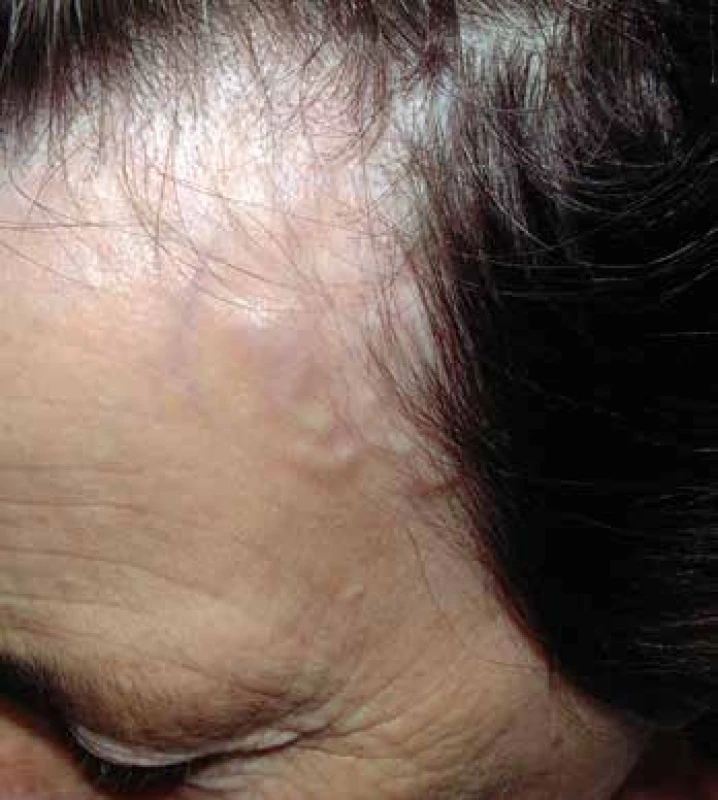
Začátek onemocnění je většinou postupný s rozvojem celkových příznaků - slabost, horečka, hubnutí, může mít však i akutní průběh. Někdy jsou tyto příznaky přičítány depresi, stárnutí nebo malignitě. Je třeba zdůraznit, že příznaky značně v průběhu doby kolísají i bez léčby. To se týká především bolestí hlavy, čelistních klaudikací a horečky. Nicméně ztráta zraku a jiné důsledky uzávěru cév jsou trvalé. Nejběžnějším příznakem OBA je někdy až úporná cefalea. Lokalizuje se do jednoho nebo více míst, může být intermitentní, ale častěji se objevuje denně. Polymyalgia rheumatica (PMR) může být jedním z počátečních příznaků. Čelistní klaudikace je typickým příznakem, může postihovat musculus masseter nebo temporální svaly, bývá často oboustranná. Objevuje se při žvýkání tuhých soust. Tyto klaudikace mohou postihnout jazyk a polykací svaly. Někdy může dojít ke spazmu žvýkacího svalstva, což zabrání nemocnému v příjmu potravy. Oslabení pulzu a palpační citlivost spánkových tepen se vyskytuje asi u poloviny postižených. Je třeba rozlišit, zda se jedná o citlivost pokožky hlavy a větví arteria temporalis nebo svalů a jejich úponů. Zduřelé, uzlovité nebo jen ztluštělé větve spánkové tepny (Obr. 1) jsou jasným příznakem arteriitidy. Segmentální oslabení pulzu spánkové tepny svědčí pro vaskulitidu, kdežto celkové oslabení pulzu proximální části karotidy bývá důsledkem aterosklerotického zúžení. Oční příznaky jsou časté – amaurosis fugax, jiskřící skotomy a diplopie. Přechodná porucha vidění bez adekvátní terapie často přechází do trvalé slepoty. Asi 10% nemocných má příznaky postižení velkých tepen končetin manifestující se oslabením pulzu a klaudikacemi zejména horních končetin nezřídka i Raynaudovým fenoménem. Protože se uzávěry velkých tepen vyvíjejí pomalu, kolaterální oběh může včas zabránit těžké ischémii. Artritida se popisuje asi u 15% nemocných. Synovitida bývá lehká a postihuje hlavně kolena a kotníky, méně často zápěstí. Neurologické příznaky jsou pestré – nejčastěji mononeuropatie nebo periferní polyneuropatie. Vzácné není ani mozkové krvácení v povodí arteria carotis interna nebo arteria basilaris. Dále se objevuje tinnitus, vertigo a jednostranné poruchy sluchu.
Při nejasném obraze diagnózu OBA potvrdí histopatologický nález z biopsie větve arteria temporalis. Pokud není tepna jasně makroskopicky postižena, je vhodné odebrat delší úsek (4-6 cm). Pokud se v prvním vzorku neprokáží patologické změny a trvá klinické podezření, je vhodné provést biopsii na druhé straně. Z neinvazivních vyšetření se užívá Dopplerovo měření průtoku, které může učit místo vhodné pro biopsii při nevýrazném klinickém nálezu. Další metodou je oční pneumopletysmografie, kterou lze ověřit snížení průtoku arteria centralis retinae, které může včas odhalit riziko poruchy zraku. Pro stanovení diagnózy OBA byla ACR v roce 1990 vypracována klasifikační kritéria (Tab. 2) (5).

Při přítomnosti tří kritérií z pěti je senzitivita 93,5% a specificita 91,2%. Většina nemocných OBA má mírnou hypochromní nebo normochromní anémii. Sérová hladina železa a saturace transferinu bývají snížené. Počet leukocytů je obvykle v normě, počet destiček spíše vyšší. Typické jsou vysoké hodnoty reaktantů zánětu a asi ve čtvrtině případů nacházíme zvýšení jaterních testů, kdy biopticky se zjišťuje steatóza až lehká fibróza. Orgánově nespecifické autoprotilátky bývají negativní. Histopatologický nález ve svém klasickém obraze ukazuje infiltraci lymfocyty s fragmentací lamina elastica interna, dále granulomatózní zánět s histiocyty a mnohojadernými obrovskými buňkami. Nacházíme T-lymfocyty typu CD4+ a příměs B lymfocytů. Zmnožené retikulocyty jsou důkazem imunitní reakce probíhající v cévní stěně.
V diferenciální diagnóze obvykle není obtížně odlišit OBA od jiných typů vaskulitid díky charakteristickému klinickému obrazu, typické histologii a orgánovému postižení. Jiné nekrotizující vaskulitidy jen zřídka postihují větve arteria carotis externa. Podobný morfologický obraz je možné pozorovat u Takayasuovy arteriitidy, avšak ta mívá jinou distribuci změn a je v Evropě mnohem vzácnější (6).
Lékem volby OBA jsou kortikosteroidy (KS) a léčbu je třeba zahájit co nejdříve, abychom předešli rozvoji cévní mozkové příhody nebo ztrátě zraku. V současnosti je snaha podávat u OBA biologickou léčbu (7).
Prognóza OBA, co se týče přežívání, je všeobecně dobrá. U neléčených však až u poloviny nemocných může dojít ke ztrátě zraku nebo cévní mozkové příhodě až smrti.
Takayasuova arteriitida
Takayasuova arteriitida (TA) je chronické zánětlivé onemocnění postihující velké tepny, především aortu a její hlavní větve. TA postihuje nejčastěji mladé ženy až 9-krát častěji než muže. Vyskytuje se zejména v Asii a Jižní Americe
Etiologie nemoci je neznámá. Soudí se na souvislosti se streptokokovou infekcí, byla popsána hypersenzitivita na tuberkulinový test. Dále jsou zmínky o možné roli cirkulujících imunitních komplexů (CIK). Také byly popsány cirkulující protilátky proti složkám stěny tepen, zejména antiendoteliální protilátky. Imunogenetické studie ukazují na asociace s haplotypem BW52 a DR4 (8).
Klinický průběh mívá dvě fáze. V první akutní fázi jsou časté artralgie, někdy se objeví synovitida na dolních končetinách, případně symetrická polyartritida. Myalgie jsou časté a mohou být zavádějící. Tato fáze nemoci může trvat řadu měsíců. Nemocní bývají léčeni pro „horečku neznámého původu“ několik let. Poté dojde k rozvoji druhé chronické fáze s příznaky cévní insuficience. Ty se objevují zejména na horních končetinách, kde se popisují jako klaudikace paží nebo pocit tuposti. Dále zachycujeme šelesty a oslabení nebo chybění pulsu nejčastěji nad karotidami a břišní aortou, řidčeji nad podklíčkovými a stehenními tepnami. Často naměříme tlakový rozdíl mezi horními končetinami větší než 30 mm Hg. Posturální nevolnost je příznakem okluze karotid a/nebo vertebrobazilárního řečiště. Tento typ postižení může vyvolávat typické držení částečné flexe krční páteře. Zrakové poruchy mívají formu mlhavého vidění, diplopie nebo přechodné jednostranné amaurózy. Běžný je nález hypertonické retinopatie. Mikroaneuryzmata, dilatace žil a krvácení připomínají diabetickou retinopatii. Pozdními následky jsou atrofie nervus opticus, amoce sítnice a krvácení do sklivce. Kožní léze mívají formu erythema nodosum a bércových vředů. Kardiální postižení spočívá v insuficienci aortální chlopně a změnách ústí koronárních artérií, nebo jejich proximálních úseků. Srdeční selhání je nejčastěji způsobeno touto vadou nebo systémovou hypertenzí, biopsií myokardu byla prokázána i myokarditida (9). Dále bývají postiženy plicní tepny velkého a středního kalibru, což vede ke vzniku plicní hypertenze často bez klinických příznaků. Může se objevit i mezangioproliferativní glomerulonefritida. Opakovaně byla popsána amyloidóza ledvin. Pozánětlivé stenózy renální tepny mohou být mnohočetné i bilaterální a projevují se systémovou hypertenzí.
V laboratorních vyšetřeních u většiny nemocných bývá zrychlená FW, mírná anémie a leukocytóza a zvýšená koncentrace CRP. Zjišťujeme také zvýšení všech tříd imunoglobulinů, ale běžné autoprotilátky bývají negativní.
Z pomocných vyšetření v časné zánětlivé fázi je významným přínosem vyšetření pomocí pozitronové emisní tomografie pomocí 18F-deoxyglukózy (PET). Tato metoda zobrazí metabolicky aktivní buňky, tedy lokalizaci zánětu ve stěně tepen a slouží i k monitorování efektu léčby. Pozdější morfologické změny zobrazí angiografické vyšetření se zaměřením na všechny větve aorty. Další arteriografie se řídí klinickým obrazem, dnes se zpravidla provádí digitální subtrakční angiografie. Podle lokalizace změn se TA klasifikuje do několika typů (Tab. 3).

CT nebo MRI aortální stěny dobře znázorňuje tloušťku cévní stěny a její změny v závislosti na terapii. Přínosně také bývá ultrasonografické vyšetření karotid. Případnou aortální insuficienci a změny na srdci je třeba ověřit echokardiograficky. V histopatologickém obraze granulomatózní fáze v období aktivního zánětu nacházíme změny na médii a adventicii se smíšeným buněčným infiltrátem lymfocytů, plazmocytů a histiocytů spolu s typickými obrovskými buňkami. Pozdní stadium choroby je vyjádřeno mírnou vazivovou hyperplazií intimy, degenerací médie a fibrózou adventicie.
Diagnóza TA vychází z typické distribuce změn na aortě a jejích hlavních větvích, především levé arteria subclaviae, horní mezenterické tepny a dalších větvích břišní aorty. Asi u 85% nemocných se nacházejí pouze stenózy a u zbylých kombinované změny. Ke stanovení diagnózy byla v roce 1990 vytvořena klasifikační kritéria (Tab. 4) (10). V diferenciální diagnóze je třeba především odlišit aterosklerózu, která se nevyskytuje u mladších jedinců bez rizikových faktorů tohoto onemocnění. Dále pak vylučujeme systémový lupus erytematodes (SLE), Behçetovu nemoc (BN), aortitidu při ankylozující spondylitidě, revmatické horečce, Crohnově chorobě a syfilitickou aortitidu. TA může také připomínat OBA, vrozenou koarktaci, ergotizmus a trombangiitis obliterans.

V terapii TA jsou lékem volby KS. Pokud se nedaří snížit dávku KS, je na místě cytotoxická terapie, případně blokátory faktoru nekrózy tumoru alfa (anti TNF-alfa). Chirurgická léčba je vyhrazena pro případy ve fázi, kdy je onemocnění pod kontrolou (11).
Prognóza je dána přítomností specifických projevů (Takayasuova retinopatie, sekundární hypertenze, aortální insuficience, aortální a arteriální aneuryzmata). Pacienti se stabilizovaným onemocněním přežívají 6 let v 98%. Hlavními příčinami úmrtí jsou srdeční selhání, cévní mozkové příhody a multiorgánové selhání.
Vaskulitidy středních cév
Polyarteritis nodosa
Primární polyarteritis nodosa (PAN) je vzácné onemocnění převážně středních artérií charakterizované postižením všech tří vrstev stěny cév vedoucí ke vzniku mnohočetných aneuryzmat, trombů a infarzací. Sekundární PAN může provázet revmatoidní artritidu (RA), systémovou sklerodermii (SSc) a další difúzní onemocnění pojiva. PAN postihuje všechny etnické skupiny bez rozdílu. Vyskytuje se v každém věku, nejčastěji mezi 40. a 60. rokem bez rozdílu pohlaví.
Etiologie nemoci je neznámá. V patogeneze se zřejmě uplatňují viry hepatitidy především B, méně často C, HIV a cytomegalovirus a snad i parvoviry. Nejasná je role ANCA protilátek a hypersenzitivní reakce. Při rozvoji nemoci hrají nespornou úlohu imunitní komplexy, které se ukládají v různých tkáních (12).
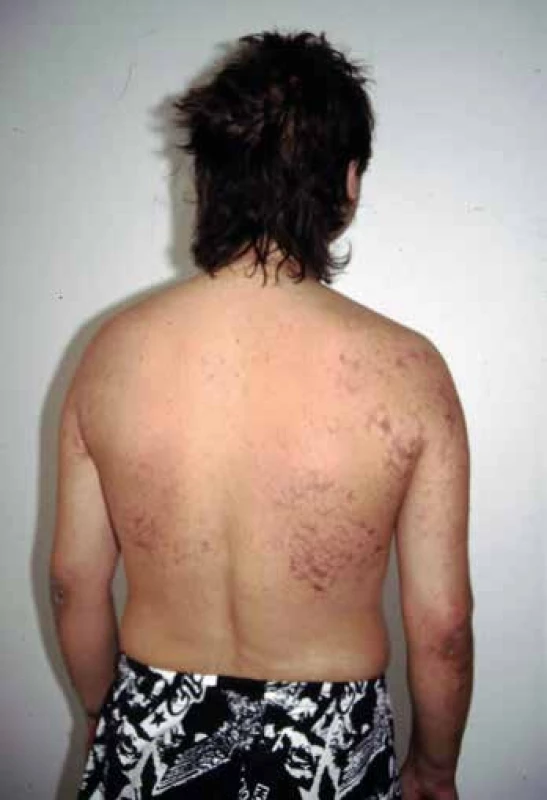
Existuje celé spektrum závažnosti od omezeného onemocnění až po rychle progredující s fatálním koncem. Většina nemocných má celkové příznaky jako horečka, slabost, úbytek hmotnosti a někteří i rash, periferní neuropatie a polyartritidu. Kožní projevy mívají formu ulcerací, livedo reticularis (Obr. 2), nekrotizující purpury a trofických ischemických změn na distálních falangách. Při rupturách cév se objevují sufúze a ekchymózy. Kloubní postižení představují artralgie nebo artritidy. Může se objevit i syndrom PMR. Myalgie vyvolává difúzní postižení svalových tepen, někdy se projevuje jako intermitentní klaudikace. Neurologické příznaky bývají ve formě periferní neuropatie (13). Začátek může být náhlý – bolest a parestezie vyzařující v průběhu periferního nervu, následované motorickým výpadkem. Postupné postižení nervů může skončit jako symetrická polyneuropatie. Renální postižení je méně časté, projevuje se proteinurií, časněji se objevuje hematurie. Hypertenze bývá důsledkem postižení renálních artérií nebo glomerulů. Postižení gastrointestinálního traktu (GIT) se manifestuje bolestmi břicha, které svou lokalizací odpovídají postiženému orgánu. Při difúzních bolestech je třeba myslet na trombózu mezenterických tepen. Ta vyvolává také distenzi břicha, někdy i s peritonitidou. Vzácné není ani krvácení z GIT. Kardiální postižení představuje srdeční selhání způsobené koronární insuficiencí nebo hypertenzí. Při postižení očí nalézáme exsudativní amoci sítnice a toxickou retinopatii. Pro PAN je charakteristická jednostranná orchitida. Někdy je postižen pouze jediný orgán, např. kůže, periferní nervy, GIT nebo ledviny. Tato lokalizovaná forma PAN je vzácná s výjimkou izolované kožní manifestace.
V laboratorním obraze zaznamenáváme zrychlenou FW, vyšší CRP, leukocytózu, normochromní anémii, trombocytózu a sníženou hladinu sérového albuminu. Až 40 % případů má pozitivní HBsAg. Známkou aktivity je pokles hladin komplementu a zvýšené CIK.
Z pomocných vyšetření má velký přínos má arteriografie. Popisují se vakovitá nebo vřetenovitá aneuryzmata nebo postupné zužování tepen do špičky. Aneuryzmata se nacházejí v renálních, jaterních, mezenterických, mozkových, lumbálních, interkostálních, dolních frenických, hypogastrických a gastroduodenálních artériích. Běžně se provádí biopsie kůže, kosterních svalů, nervus suralis a testes. V histopatologickém obraze nalézáme postižení artérií středního kalibru s predilekcí v místě větvení. Typická je fibrinoidní přeměna a masivní infiltrace všech tří vrstev cévní stěny polymorfonukleáry a eozinofily. V místech změn se objevují trombózy a aneuryzmata. Zánětlivá ložiska se hojí vazivovou tkání, což vede k uzávěrům cév. Glomerulonefritida je většinou segmentální a proliferativní.
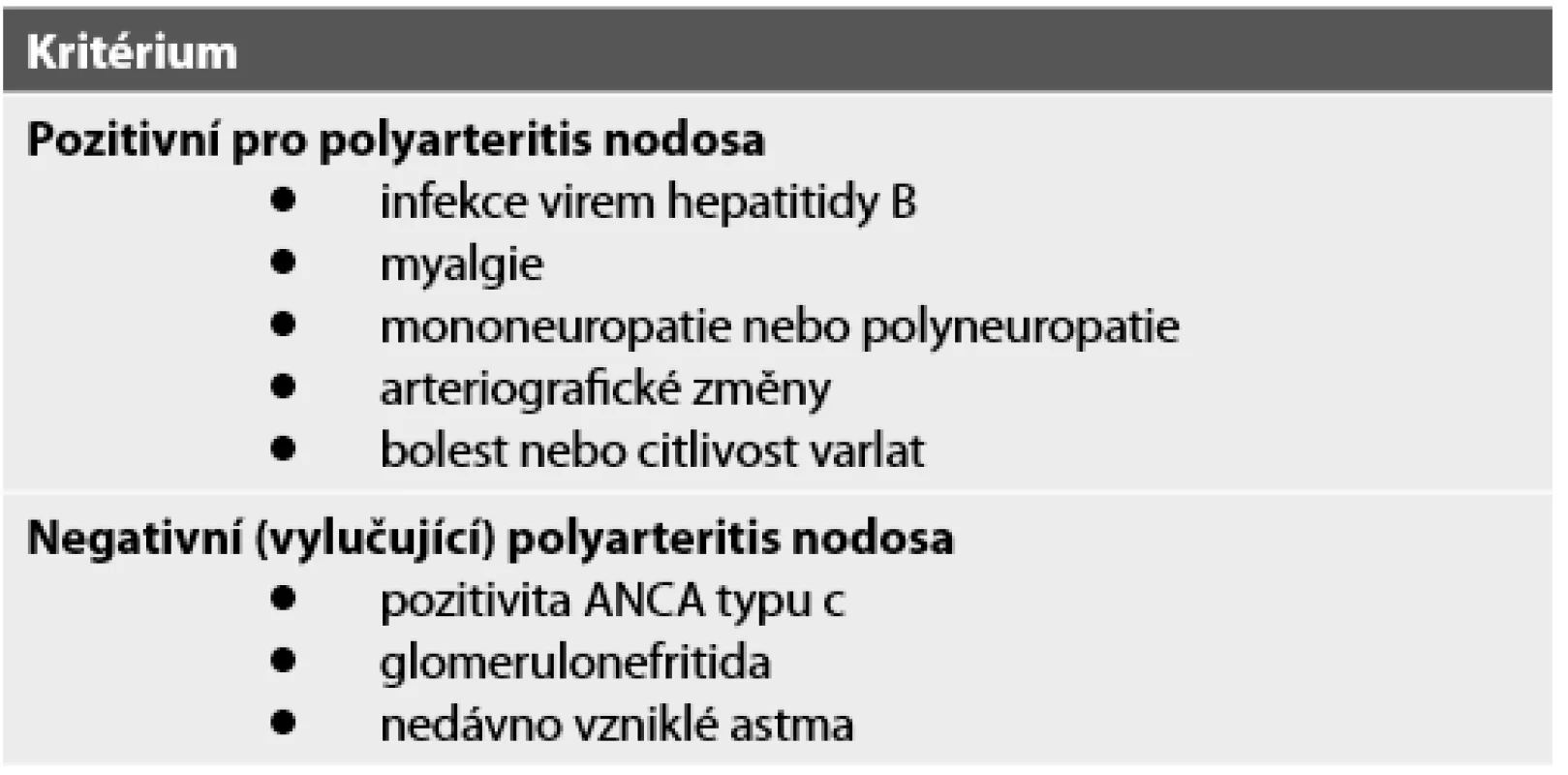
Diagnózu je třeba vždy ověřit biopsií, pokud je postižený orgán dostupný. Může ji nahradit arteriografie s nálezem typických aneuryzmat. Vzhledem k velmi pestrému obrazu PAN byla navržena diagnostická kritéria, jak uvedeno v tabulce 5 (14).
V diferenciální diagnóze je třeba odlišit mikroskopickou polyangiitidu (MPA), IgA vaskulitidu (IGV) a anti-GBM nefritidu. Nález z renální biopsie může být identický s granulomatózou s polyangiitidou (GPA) a eozinofilní granulomatózou s polyangiitidou (EGPA). Pokud se jasně nezobrazí aneuryzmata, podobný angiografický obraz má GPA, vaskulitida při SLE, dále trombotická trombocytopenická purpura, infekční endokarditida, tumory metastazující na peritoneum. Problémem jsou také disekující aneuryzmata artérií.
Všem nemocným PAN se podávají KS. Při extenzívním viscerálním postižením s rychlou progresí je nutné přidat cytotoxické léky. Lokalizované kožní formy dobře reagují na kolchicin v kombinaci s topickými KS (15).
Prognóza závisí na rozsahu postižení životně důležitých orgánů. K úmrtí dochází v důsledku nezvládnutelné vaskulitidy (srdeční a mozkové příhody) nebo infekčních komplikací při imunosupresivní léčbě.
Vaskulitidy malých cév
Vaskulitidy s pozitivitou autoprotilátek proti cytoplazmě neutrofilních leukocytů
Granulomatóza s polyangiitidou
GPA je chronická nekrotizující vaskulitida neznámého původu charakterizovaná granulomatózními lézemi. Plně rozvinutý obraz může být život ohrožující s typickým pulmorenálním syndromem (16). Prevalence je 3-6 pacientů na 100 000 obyvatel a roční incidence činí 7 případů na 100 000 obyvatel. GPA postihuje častěji muže obvykle mezi 40. a 60. rokem života.
Etiologie je neznámá. Byla zjištěna významná imunogenetická asociace s alelami HLA-DRB1*04 a DRB*13. V patogeneze se uplatňuje geneticky podmíněná nebo získaná nerovnováha proteáza/antiproteáza, kdy u GPA se jedná o proteinázu 3 (PR3). Proti tomuto enzymu se tvoří autoprotilátky s cytoplazmatickým typem imunofluorescence (cANCA) (17). Z faktorů zevního prostředí určitou roli může hrát hypersenzitivita na blíže neurčený alergen zejména inhalované substance. Z bakteriálních agens se jedná o Staphylococcus aureus a z virových parvovirus B19 (18). Expozice křemíku nebo silikonu zřejmě souvisí s rychle progredující glomerulonefritidou při GPA.
Z klinických projevů jsou časté celkové příznaky – únava, slabost, hubnutí a febrilie. Postižení horních dýchacích cest se projevuje ucpaným nosem, epistaxí, chronickou rýmou a sinusitidou. Granulomatózní zánět může mít destruktivní charakter a vést ke vzniku sedlovité deformity nosu. Popisuje se také ulcerózní stomatitida a hyperplastická gingivitida. Časté jsou záněty zevního zvukovodu – chondritida středouší a převodní porucha sluchu. Při postižení trachey může vzniknout subglotická stenóza. Postižení dolních dýchacích cest signalizuje kašel, hemoptýza či bolest na hrudi. Granulomy se mohou provalit do pleurální dutiny a způsobit ventilový pneumotorax. Postižení ledvin je časté pod obrazem rychle progredující glomerulonefritidy někdy až s rozvojem k renální insuficience (19). Oční symptomatologie je pestrá – konjunktivitida, episkleritida, korneální vředy, retinální vaskulitida, neuropatie nervus opticus až protruze bulbu. Postižení periferních nervů se projevuje nejčastěji jako mononeuritis multiplex. Méně časté je postižení GIT – průjmy, krvácení a bolesti břicha, někdy perforace střeva. Vídáme také artralgie a myalgie, vzácně erozivní artritidy.
Při laboratorním vyšetření zjišťujeme normochromní normocytární anémii, leukocytózu s lehkou eozinofilií, často trombocytémii. Zpravidla je zrychlená FW, vyšší CRP a mírná hypergamaglobulinémie, zejména zvýšení IgA. V časné fázi je obvyklá mikroskopická glomerulární erytrocyturie s malou či střední proteinurií. Renální funkce mohou být snížené. Někdy se prokáže revmatoidní faktor a zvýšené CIK. Vždy vyšetřujeme autoprotilátky ANCA. Nejprve se provádí imunofluorescenční vyšetření a při jeho pozitivitě doplňujeme test komerční soupravou ELISA proti PR3 a myeloperoxidáze (20).
Z pomocných vyšetření je vhodné provést MRI hlavy, které může prokázat přítomnost granulomů v horních dýchacích cestách, vedlejších dutinách, orbitě (Obr. 3) a mozku. Biopsie sliznice hroních cest slouží k detekci granulomů, častěji však nacházíme nekrózu se sekundární infekcí. Na skiagramu snímku hrudníku bývá charakteristické motýlovité zastření, pro přesnější obraz je nutné doplnit HRCT. Vedle prchavých infiltrátů lze někdy v alveolech také pozorovat rozsáhlé granulomy s centrálním rozpadem. Angiografické vyšetření může být přínosné při postižení tepen středního kalibru, protože pomůže odlišit vaskulitické a aterosklerotické léze při ischémii střev nebo hypoperfúzi končetin. Někteří autoři doporučují i bronchoskopii s bronchoalveolární laváží a cytologické vyšetření získané tekutiny. Při renální biopsii se popisuje fokální až difúzní segmentální nekrotizující glomerulonefritida. Někdy lze zachytit vaskulitidu drobných cév.
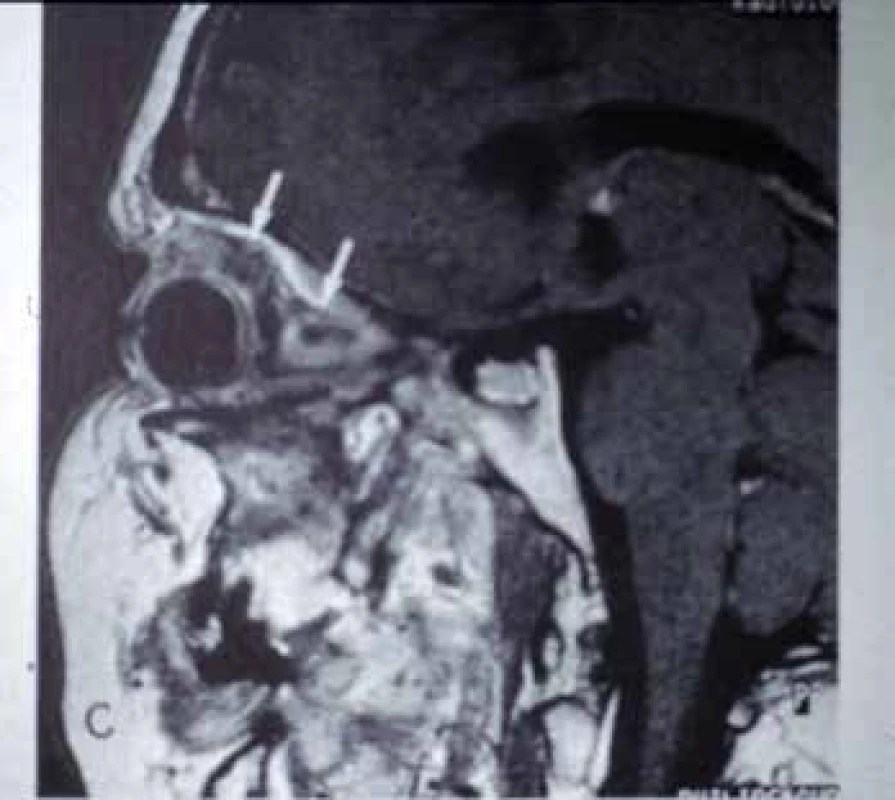
Diagnóza se opírá o typický klinický obraz celkových příznaků, postižení horních a dolních dýchacích cest s granulomy, postižení očí a v pozdějších fázích i ledvin. Svůj význam má průkaz cANCA protilátek, jejich nepřítomnost často svědčí pro limitovanou formu onemocnění. V diferenciální diagnóze je třeba odlišit jiná pulmorenální onemocnění – zejména Goodpastureův syndrom na základě imunofluorescenčního vyšetření vzorků z renální biopsie, kde u tohoto syndromu nacházíme lineární depozita imunoglobulinů na bazální membráně glomerulů. Pro EGPA je příznačné astma bronchiale, krevní a tkáňová eozinofilie. U PAN je postižení plic mnohem vzácnější než u ANCA asociovaných vaskulitid.
V léčbě se k navození remise se užívá prednison s cyklofosfamidem nebo metotrexátem. Lokalizované granulomatózní formy lze léčit kombinovaným preparátem trimetoprimum/sulfametoxazol. U refrakterních forem se ukázal jako účinný blokátor CD20 rituximab (21).
Prognóza závisí na míře postižení ledvin a výskytu oportunní infekce. Z akutních příčin úmrtí to bývá masivní plicní krvácení. Relapsy se objevují až u 50% nemocných i několik let od stanovení diagnózy, často ve vazbě na infekci či po snížení dávek imunospresiv. Autoprotilátky ANCA jsou užitečným parametrem, který může upozornit na hrozící relaps.
Eozinofilní granulomatóza s polyangiitidou
EGPA je nekrotizující vaskulitida s astmatem, periferní eozinofilií, extravaskulárními nekrotizujícími granulomy a s eozinofilními infiltráty ve stěně cév a perivaskulární tkáni. Nemoc postihuje poněkud častěji muže než ženy a začíná obvykle ve středním věku. Jedná se o vzácné onemocnění – roční incidence se odhaduje 1-3 případy na milion obyvatel.
Etiologie je neznámá. Podíl ANCA protilátek na patogeneze onemocnění je zřejmý podle bohatší manifestace choroby u ANCA pozitivních nemocných. Role eozinofilů a polymorfonukleárů v poškození cévní stěny není jasná. Diskutuje se působení antagonistů receptorů pro leukotrieny (22).
Nemoc se obvykle projeví nejdříve postižením respiračního traktu, které může předcházet projevům mimoplicní vaskulitidy až o několik let nejčastěji ve formě astma bronchiale. U části nemocných je v anamnéze alergie, zejména sezónní pylové alergie nebo jiné prokázané alergie na potraviny. Na radiogramu hrudníku nalézáme infiltráty prchavého či migrujícího charakteru a pleurální výpotek obsahující značné množství eozinofilů. Postižení horních cest dýchacích bývá ve formě alergické rýmy či nosních polypů. Dále bývají postiženy: srdce (myokard a endokard), kůže, střevo, svaly a nervová tkáň. Mononeuritidy se popisují až u dvou třetin případů, méně časté je postižení CNS. Postižení ledvin nalézáme asi u třetiny nemocných – dominujícím nálezem bývá fokálně segmentální glomerulonefritida. Frekvence výskytu orgánových manifestací a klinických projevů je uvedena v tabulce 6.
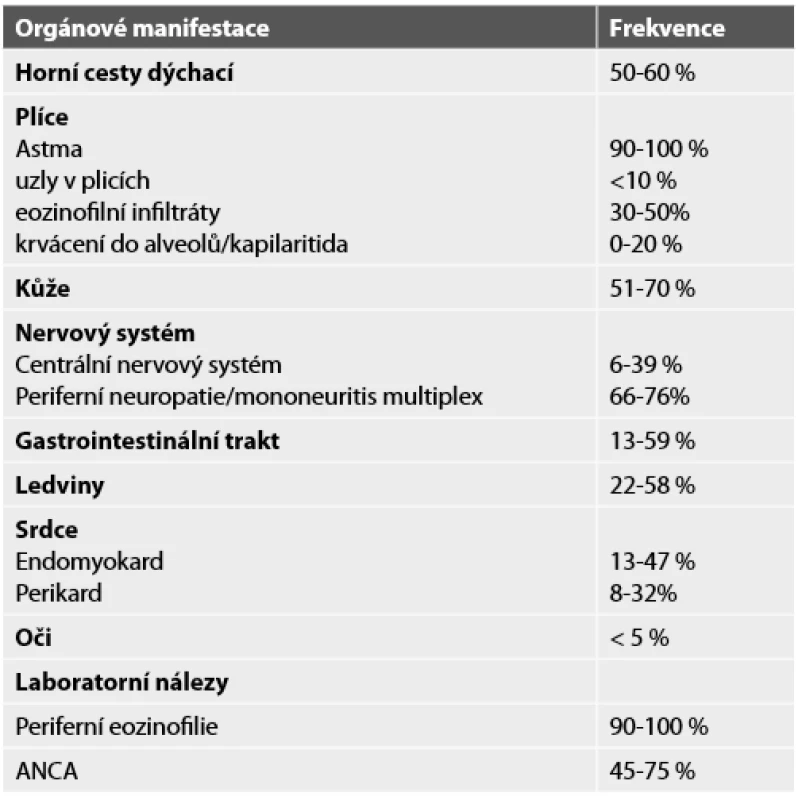
V laboratorních testech nacházíme zrychlenou FW, vysoké CRP, anémii a zvýšené sérové hladiny IgE. Počet eozinofilních leukocytů v periferní krvi přesahuje 1,5x109/l, může však dosáhnout až 8,5x109/l. Typickým laboratorním nálezem je přítomnost autoprotilátek ANCA. Zjišťován bývá cytoplazmatický i perinukleární typ imunofluorescence, antimyeloperoxidázová aktivita bývá častější (23). Průkaz ANCA u plicních onemocnění nás vždy nutí pomýšlet na systémovou vaskulitidu. Renální postižení se projeví mikroskopickou hematurií, popřípadě proteinurií do 2 g/24 h a vyššími hodnotami kreatininu a močoviny.
Z pomocných vyšetření je nutné podrobné vyšetření plic – skiagram a HRCT, vyšetření plicních funkcí potvrdí závažnost astmatu. Vhodná je též bronchoskopie s laváží a cytologickým vyšetřením získané tekutiny. Z kožní biopsie je zásadní nález nekrotizujících granulomů a vaskulitida postihující malé artérie a venuly. Granulomy mívají průměr 1 mm i více a jsou lokalizovány v okolí malých tepen. Jejich centrum bývá složené z eozinofilů a obklopené makrofágy a epiteloidními obrovskými buňkami.
Diagnóza se opírá především o anamnézu astma bronchiale a atopie, přítomnost typických infiltrátů v plicích a vysoké cirkulační eozinofilie. V diferenciální diagnóze je nutno vyloučit parazitární infekce a polékové reakce. EGPA mohou připomínat některá alergická onemocnění s astmatem, akutní a chronické eozinofilní pneumonie a hyperenozinofilní syndrom. Při pozitivitě ANCA je třeba odlišit GPA a MPA. U těchto nemocí nebývá v anamnéze astma a naopak u EGPA zpravidla nenacházíme ulcerace v horních dýchacích cestách (22).
Lékem volby u lehčích forem onemocnění jsou KS. U perzistentních projevů se přidává cyklofosfamid nebo azathioprin (24). Pětileté přežití je běžné u více než 60% nemocných i při prokázaném postižení ledvin. Nejčastější příčinou smrti je srdeční selhání.
Behçetova nemoc
BN je chronický relabující zánětlivý proces postihující řadu tkání a orgánů. Podkladem je vaskulitida drobných tepen, ale postižení velkých tepen i žil je také možné. BN se nejčastěji vyskytuje v Japonsku, východním Středomoří, v USA a na středním Východě. V jihovýchodní Asii a Turecku je častější výskyt a závažnost uveitidy. Onemocnění postihuje stejně často muže i ženy (25).
Etiologie a patogeneze BN jsou neznámé. Incidence HLA-B5 a subtypu B51 je u nemocných BN 3-6krát vyšší než u zdravých jedinců. Zvláště přítomnost subtypu B51 může být předzvěstí těžkého průběhu choroby. Je jasné, že imunologické mechanizmy spouštějí vaskulitický proces, ale nemáme žádné doklady, že se u BN jedná o autoimunitní proces. Dlouho se pátralo po mikrobiálních agens, zejména virech, které by aktivovali T lymfocyty a jejich subpopulaci Th1.
K hlavním klinickým příznakům patří léze na bukální sliznici a genitálu o průměru 3-15 mm oválného nebo okrouhlého tvaru. Orální léze mají ostře ohraničené okraje a jsou provázeny houbovitými papilami na jazyku, plakovitými lézemi na faryngu a fetorem z úst. Ulcerativní změny na penisu a skrótu bývají bolestivé, na vulvě (Obr. 4) a vagině většinou nebolestivé, takže mohou zůstat nepovšimnuty. Běžné jsou kožní projevy – pyoderma s pustulami, erythema nodosum a gangrény. Postižení GIT má charakter aft až ulcerací zejména v tlustém střevě. Klasickým očním příznakem je iritida s hypopyonem. Také se objevuje episkleritida, konjuktivitida, keratitida, iridocyklitida, retinální tromboflebitida, edém papily až atrofie nervus opticus, která u neléčených může vést k oslepnutí. Závažné bývá postižení CNS, zejména meningitida, myelitida a syndrom mozkového kmene. Klinicky bývá neurologické postižení vyjádřeno spastickou hemi - nebo kvadruparézou často s cerebelární ataxií. Trombóza horní a dolní duté žíly, povrchních a hlubokých žil končetin se popisují v 7-37% případů. Uzávěr intrakraniálního kavernózního sinu se manifestuje chronickou cefaleou a mlhavým viděním. Aneuryzmata a uzávěry velkých tepen byly popsány v pitevním materiálu až u 37 % pacientů. Uzávěry byly často způsobeny emboly z endokardu mitrální chlopně. Postižení plicních tepen aneuryzmaty, která komunikují s bronchy, se projevuje masivní hemoptýzou. Kloubní postižení bývá ve formě artralgií, nejčastěji jsou postiženy kolena, hlezna, zápěstí a sakroiliakální klouby (25).
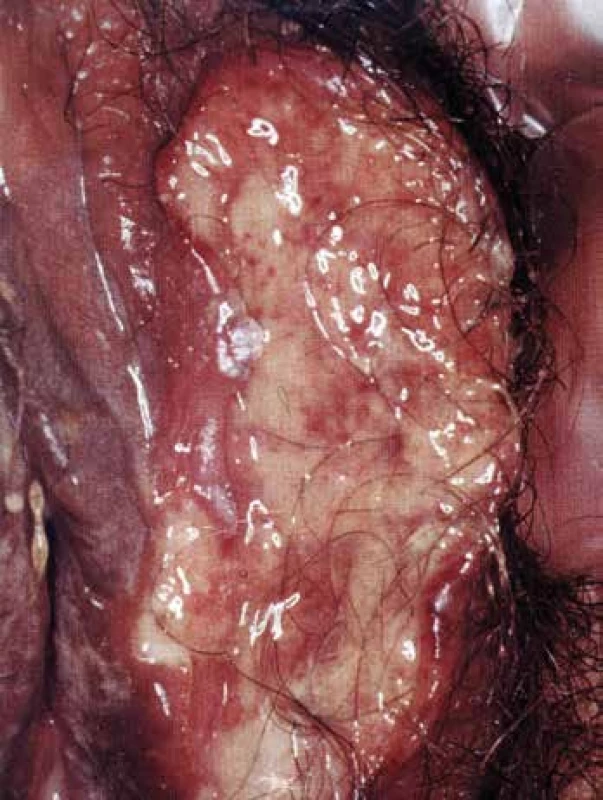
V akutní fázi onemocnění bývají zvýšené hodnoty reaktantů akutní fáze, anémie a typická je polyklonální gamapatie. Z imunologických testů zjišťujeme pouze nespecifické zvýšení hladiny CIK a přítomnost kryoglobulinů až u 25% nemocných.
Z pomocných vyšetření se provádí biopsie sliznice úst nebo genitálu a histopatologický obraz lézí je charakterizován infiltrací lymfocyty a plazmocyty s depozity IgM a C3 v cévách a perivaskulitidou, někdy se prokáže leukocytoklastická vaskulitida. Při neurologických projevech je indikováno CT a MR vyšetření mozku. Trombózy se prokazují flebograficky, diagnózu postižení tepen lze nejsnáze potvrdit digitální subtrakční angiografií. Diagnostickým vyšetřením postižení plicních tepen je také arteriografie. Pyoderma lze prokázat testem patergity – intradermální vpich sterilní jehly, kdy se objeví papula či pustula za 24–48 h (25).
Pro stanovení diagnózy vypracovali v roce 1990 členové International Study Group for Behçets disease kritéria uvedená v tabulce 7 (26).

Diagnóza je splněna, je-li přítomno hlavní kritérium a dvě vedlejší kritéria.
V diferenciální diagnóze BN je třeba si uvědomit, že se často vyskytují inkompletní formy s recidivujícími afty a postižením jen některého orgánu. U reaktivní artritidy se vyskytují orální a genitální ulcerace, avšak u BN jsou lokalizovány spíše na skrotu než na glans penis. Navíc u BN nebývá uretritida. SLE se sekundárním antifosfolipidovým syndromem nemívá výrazné slizniční projevy. Někdy se také u colitis ulcerosa objevují slizniční a kožní léze a episkleritida, které nelze odlišit od BN. Některé neurologické příznaky BN mohou připomínat sclerosis multiplex.
Terapie KS má u BN spíše paliativní účinek, uplatňují se více v topické formě na mukokutánní projevy nemoci. K léčbě očních manifestací se podává v kombinaci KS s azathioprinem případně cyklosporinem A. Z biologických léků se osvědčily interferon-alfa a infliximab (27).
I když BN výrazně nezkracuje život, varující jsou vždy neurologické příznaky a postižení velkých cév. U těchto manifestací se popisuje zvýšená mortalita zejména u mladých mužů.
IgA vaskulitida
IGV je vaskulitida drobných tepen vyskytující se v dětském a pubertálním věku a často navazuje na prodělané infekční onemocnění. Roční incidence podle literárních údajů činí 100-200 nemocných na milion obyvatel. Původ nemoci je neznámý. U nemocných IGV byl zjištěn zvýšený výskyt alel HLA-DRB1*01 a HLA-DRB1*11 (28). Úloha interkurentní infekce je nepochybná, žádné infekční agens však nebylo prokázáno jako etiologické. Zejména se zvažuje vliv respiračních infekcí. Obecně infekce často předchází rozvoji nemoci a byla nejčastěji prokázána tato agens: streptokoky, Staphylococcus aureus, Escherichia coli, Mycobacterium tuberculosis, Yersinia species, Legionella species, Mycoplasma pneumoniae, virus Epsteina-Barrové, virus hepatitidy B, varicella, adenoviry, cytomegaloviry a parvovirus B19. Nemoc také byla vyvolána očkováním proti tyfu, paratyfu, choleře, žluté horečce a spalničkám. Obdobnou provokující roli může hrát léková či potravinová alergie.
Artralgie až oligoartritidy často předcházejí kožní projevy a postihují drobné nožní klouby, kotníky nebo kolena. Exantém začíná jako urtikariální eflorescence na extenzorových stranách končetin, okolo kotníků, loktů a na hýždích, méně často na trupu a obličeji. Během dvou dnů dochází k vývoji typické prominující purpury (Obr. 5), která může splývat v ekchymózy. Abdominální symptomatologie mívá charakter intenzivní kolikovité bolesti, někdy nauzey a zvracení, vzácně akutní intususcepce. Gastrointestinální krvácení bývá jen okultní, výjimečně masivní. Bolesti a otok skróta a chámovodu mohou vést k diagnóze testikulární torze. Postižení ledvin se manifestuje proteinurií s hematurií, někdy hypertenzí a oligurií s poklesem renálních funkcí až ledvinnou nedostatečností. Neurologické symptomy zahrnují bolesti hlavy, vzácněji poruchy chování a křeče.
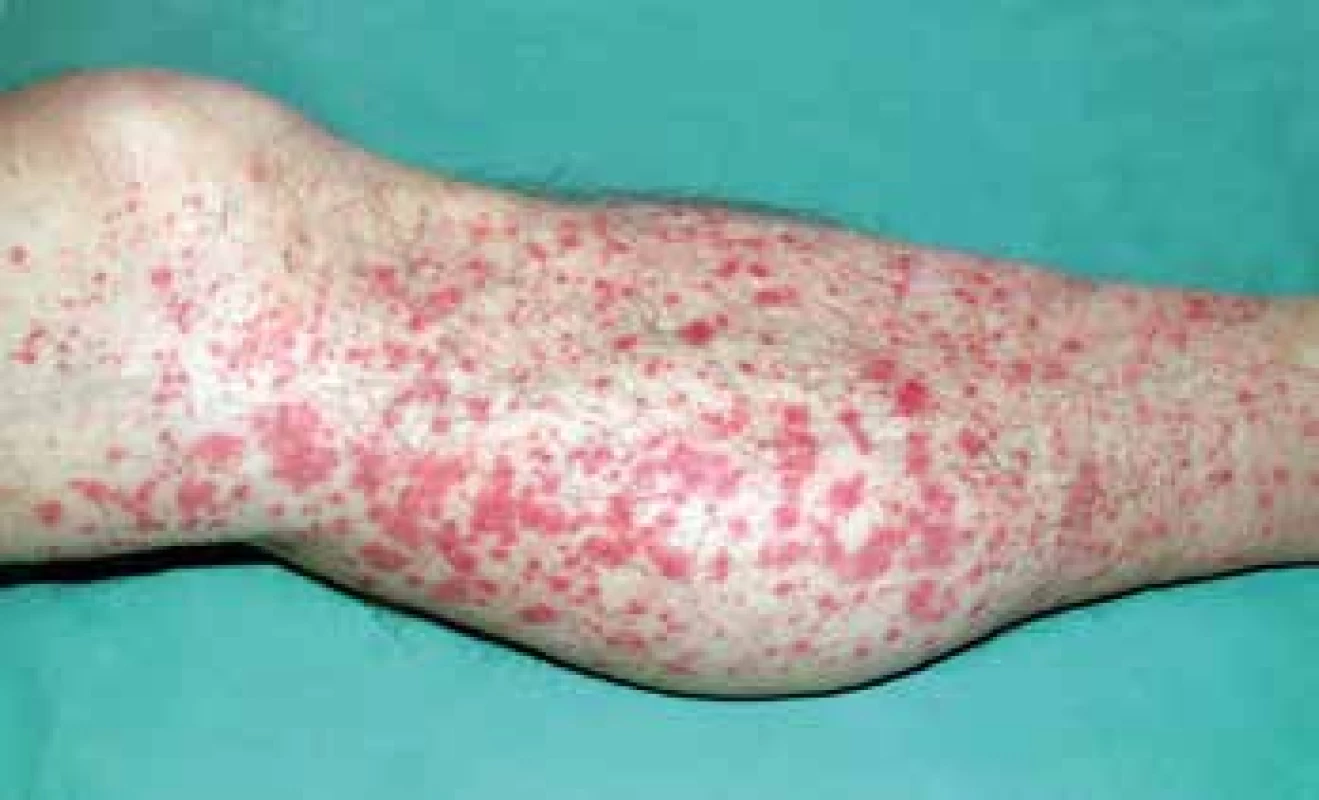
V laboratorním obraze zaznamenáváme zvýšení reaktantů akutní fáze, normochromní normocytární anémii, mírnou leukocytózu a trombocytózu. Hematurie s nálezem válců v sedimentu a proteinurií je indikací k biopsii ledvin. U některých nemocných byly prokázány vysoké titry revmatoidního faktoru ve třídě IgA. Hodnoty C3, C4 a CH50 bývají snížené. Z kožní biopsie nacházíme histologicky leukocytoklastickou vaskulitidu s perivaskulární akumulací polymorfonukleárů v okolí kapilár a venul koria. Imunofluorescenčně lze prokázat IgA, C3 a fibrin. Renální biopsie mívá typický obraz fokálně segmentální proliferativní glomerulonefritidy s proliferací mesangiálních buněk. U starších lézí může být přítomen i různý stupeň glomerulosklerózy. Při hemateméze se provádí gastroskopie, kdy nacházíme na sliznici petechie, eroze i ulcerace. Při kolikách je indikována ultrasonografie a CT břicha (29).
Diagnóza se stanoví na základě typického exantému s histopatologickým nálezem leukocytoklastické vaskulitidy, bolestí břicha a postižením ledvin. V diferenciální diagnostice je zásadní otázkou, zda se jedná o samotný kožní projev nebo součást celkového onemocnění. Je třeba odlišit GPA a MPA, kde bývají pozitivní ANCA protilátky. SLE odliší pozitivita antinukleárních protilátek a autoprotilátek pro dvouvláknové DNK. Purpura je jinak průvodním příznakem mnoha infekčních chorob a polékových reakcí, nebývá však hmatná.
Celkově lékem volby jsou KS. Bolesti a otoky kloubů tlumíme nesteroidními antirevmatiky. Při multiorgánovém postižení je indikována kombinace KS s cyklofosfamidem nebo azathioprinem (30). Prognóza je příznivá a je dána závažností renálního postižení, avšak pouze 3 % nemocných progreduje do terminální renální insuficience.
ZÁVĚR
Obecně platí, že vyšetření, stanovení diagnózy vaskulitidy a léčení těchto nemocných představuje pro většinu lékařů určitou „výzvu“, protože tyto vzácné choroby mohou vést k nevratnému poškození orgánů a v některých případech jsou i život ohrožující. Vždy je nutno nemocného s podezřením na vaskulitidu odeslat k revmatologovi. Pro stanovení diagnózy stále platí, že „zlatým standardem“ je histopatologický nález z biopsie postižené tkáně nebo orgánu, pro některé jednotky stačí kvalitní zobrazovací metoda. Nutnou podmínkou kvalitní péče o tyto pacienty je mezioborová interní spolupráce s kardiologem, angiologem, nefrologem, pneumologem, hematologem a někdy také s klinickým imunologem. Dále jsou často zapotřebí konzultace dermatologa, otorinolaryngologa, infekcionisty, neurologa, oftalmologa a specialistů na zobrazovací metody.
PROHLÁŠENÍ
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
∗ Adresa pro korespondenci:
Doc. MUDr. Radim Bečvář, CSc.
Revmatologický ústav a Revmatologická klinika 1. LF UK,
12850 Praha 2, Na Slupi 4
e-mail: becvar@revma.cz
Sources
- Bečvář R, Tesař V, Rychlík I. Vaskulitidy v klinické praxi - diagnostika a terapie. (1. vyd) Praha: Medprint; 1994, 8-9.
- Ansell BM, Bacon PA, Lie JT, Yazici H. The vasculitides. Science and practice (1st ed). London: Chapman&Hall Medical; 1996 : 267-269.
- Fessler BJ. Approach to the diagnosis of vasculitis in adult patients. In: Ball GV, Louis Bridge S Jr, eds. Vasculitis (2nd ed). Oxford: Oxford University Press; 2008 : 277-284.
- Alvarez-Lafuente R, Fernández-Gutiérrez B, Jover JA et al. Human parvovirus B19, varicella zoster virus, and human herpes virus 6 in temporal artery biopsy specimens of patients with giant cell arteritis: analysis with quantitative real time polymerase chain reaction. Ann Rheum Dis 2005; 64 : 780-782.
- Hunder GG, Bloch DA, Michel BA et al. The American College of Rheumatology 1990 revised criteria for the classification of giant cell arteritis. Arthritis Rheum 1990; 33 : 1122-1128.
- Dejaco C, Duftner C, Buttgereit F, Matteson EL, Dasgupta B. The spectrum of giant cell arteritis and polymyalgia rheumatica: revisiting the concept of the disease. Rheumatology (Oxford) 2017; 56 : 506-515.
- Mukhtyar C, Guillevin, Cid MC et al. EULAR recommendations for the management of large vessel vasculitis. Ann Rheum Dis 2009; 68 : 318-323.
- Hall S, Buchbinder R. Takayasu‘s arteritis. Rheum Dis Clin North Amer 1990; 16 : 411-422.
- Kobayashi Y. Takayasu‘s arteritis. In: Ball GV, Louis Bridges S Jr, eds. Vasculitis (2nd ed). Oxford: Oxford University Press; 2008 : 325-327.
- Hunder GG, Bloch DA, Michel BA et al. The American College of Rheumatology 1990 criteria for the classification of Takayasu‘s arteritis. Arthritis Rheum 1990; 33 : 1129-1134.
- Hellmich B, Agueda A, Monti S et al. 2018 Update of the EULAR recommendations for the management of large vessel vasculitis. Ann Rheum Dis 2019 Jul 3. pii: annrheumdis-2019-215672. doi: 10.1136/annrheumdis-2019-215672. [Epub ahead of print].
- De Virgilio A, Greco A, Magliulo G et al. Polyarteritis nodosa: A contemporary overview. Autoimmun Rev 2016; 15 : 564-570.
- Pagnoux C, Seror R, Henegar C for the French Vasculitis Study Group. Clinical Features and Outcomes in 348 Patients With Polyarteritis Nodosa A Systematic Retrospective Study of Patients Diagnosed Between 1963 and 2005 and Entered Into the French Vasculitis Study Group Database. Arthritis Rheum 2010; 62 : 616–662.
- Henegar C, Pagnoux C, Puéchal X for the French Vasculitis Study Group. A paradigm of diagnostic criteria for polyarteritis nodosa: analysis of a series of 949 patients with vasculitides. Arthritis Rheum 2008; 58 : 1528-1538.
- Guillevin L, Pagnoux C, Teixeira L. Treatment of PAN. In: Ball GV, Louis Bridges S Jr, eds. Vasculitis (2nd ed). Oxford: Oxford University Press; 2008 : 347-349
- Hoffman GS, Weyand CM et al. Inflammatory diseases of blood vessels. (1st ed.). New York: Marcel Dekker, Inc, 2002 : 306-368.
- Clain JM, Hummel AM, Stone JH et al. Immunoglobulin (Ig)M antibodies to proteinase 3 in granulomatosis with polyangiitis and microscopic polyangiitis. Clin Exp Immunol 2017; 188 : 174-181.
- Nikkari RA, Vainionpää R, Toivanen P et al. Wegener‘s granulomatosis and parvovirus B19 infection. Arthritis Rheum 1995; 38 : 1175-1176.
- Hoffman GS, Kerr GS, Leavitt RY et al. Wegener granulomatosis: an analysis of 158 patients. Ann Intern Med 1992; 116 : 488–498.
- Csernok E, Holle J, Hellmich B et al. Evaluation of capture ELISA for detection of neutrophil cytoplasmic antibodies directed against proteinase 3 in Wegeners granulomatosis: first results from a multicenter study. Rheumatology (Oxford) 2004; 43 : 174-180.
- Smith RM, Jones RB, Jayne DR. Progress in treatment of ANCA-associated vasculitis. Arthritis Res Ther 2012; 4 : 210-213.
- Specks U. Churg-Strauss syndrome In: Ball GV, Louis Bridges S Jr, eds. Vasculitis (2nd ed). Oxford: Oxford University Press; 2008 : 429-438.
- Zhou XL, Zheng MJ, Shuai ZW et al. The significances of peripheral neutrophils CD(55) and myeloperoxidase expression in patients with myeloperoxidase-specific anti-neutrophil cytoplasmic antibody associated vasculitis. Zhonghua Nei Ke Za Zhi 2017; 56 : 427-432.
- Bečvář R. Moderní terapie ANCA pozitivních vaskulitid. Acta medicinae 2013; 2 : 76-79.
- Fresko I, Melikoglu M, Kural-Seyahi E et al. Behçet’syndrome: pathogenesis, clinical manifestations, and treatment. In: Ball GV, Louis Bridges S Jr, eds. Vasculitis (2nd ed). Oxford: Oxford University Press; 2008 : 461-474.
- International Study Group for Behçets disease. Criteria for diagnosis of Behcet‘s disease. Lancet 1990; 335 : 1078-1080.
- Hatemi G, Silman A, Bang D and EULAR Expert Committee. EULAR recommendations for the management of Behçet disease. Ann Rheum Dis 2008; 67 : 1656-1662.
- Calvino MC, Llorca J, Garcia-Porrú AC et al. Henoch-Schönlein purpura in childern in north western Spain: a 20-year epidemiologic and clinical study. Medicine (Baltimore) 2001; 80 : 279-290.
- Ozen S, Marks SD, Brogan P et al. European consensus-based recommendations for diagnosis and treatment of immunoglobulin A vasculitis-the SHARE initiative. Rheumatology (Oxford). 2019; 58 : 1607-1616.
- Bogdanović R. Henoch-Schönlein purpura nephritis in children: risk factors, prevention and treatment. Acta Paediatr 2009; 98 : 1882-1889.
Labels
Anatomical pathology Forensic medical examiner ToxicologyArticle was published in
Czecho-Slovak Pathology

2020 Issue 2
-
All articles in this issue
- Úvod do diagnostiky vaskulitid – „pattern based“ přístup a diferenciální diagnostika z pohledu morfologie
- Editorial
- Už asi není udržitelné fungovat bez subspecializací
- Monitor aneb nemělo by Vám uniknout, že...
- Pathophysiology of ANCA-associated vasculitis
- How to improve the histopathological diagnosis of systemic vasculitides in daily practice?
- Primary vasculitides – current diagnostics and therapy
- Secondary vasculitis – omitted manifestation of many diseases
- Dermatofibrosarcoma protuberans with fibrosarcomatous transformation: a case report
- Jaká je vaše diagnóza?
- Jaká je vaše diagnóza? Odpověď: Mukozálny hamartóm zo Schwannovych buniek pripomínajúci taktilné Wagnerove-Meissnerove telieska
- A case of amoebic colitis with Crohn-like endoscopic and histopathological features
- Czecho-Slovak Pathology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Primary vasculitides – current diagnostics and therapy
- Secondary vasculitis – omitted manifestation of many diseases
- Dermatofibrosarcoma protuberans with fibrosarcomatous transformation: a case report
- Pathophysiology of ANCA-associated vasculitis
