Pacient – diabetik s periférnym artériovým ochorením
A diabetic patient with peripheral arterial disease
Diabetes mellitus and peripheral arterial disease frequently occur particularly at older age. Their simultaneous course presents a significant risk of vascular complications. The authors deal with a mutual relationship of the two diseases, the incidence of complications and ongoing pathophysiological changes as well as diagnostic possibilities. The treatment places emphasis primarily on influencing the risk factors of both diseases – ban on smoking, normalization of blood pressure, the lipid spectrum values, a rigorous control of blood glucose. The specific treatment for the peripheral arterial disease is always based on movement therapy, as to medication antiplatelet drugs are indicated for symptomatic patients, as to vasoactive drugs prostanoids or possibly cilostazol or naftidrofuryl are administered to a selected group of patients. Revascularization is justified in patients with life-limiting claudications with an insufficient response to conservative treatment.
Key words:
diabetes mellitus, diagnostics PAD, pathogenesis PAD, peripheral arterial disease (PAD), treatment PAD
Received:
28. 2. 2018
Accepted:
7. 3. 2018
Authors:
Tomáš Petrovič; Peter Jackuliak; Juraj Payer
Authors‘ workplace:
V. interná klinika LF UK a UNB, Nemocnica Ružinov, Bratislava
Published in:
Forum Diab 2018; 7(1): 34-39
Category:
Overview
Diabetes mellitus a periférne artériové ochorenie sú častými ochoreniami najmä vo vyššom veku. Ich súbežný priebeh predstavuje významné riziko cievnych komplikácií. Autori sa v texte zaoberajú vzájomným vzťahom týchto dvoch ochorení, výskytom komplikácií ako aj prebiehajúcimi patofyziologickými zmenami a diagnostickými možnosťami. Z hľadiska liečby sa kladie dôraz predovšetkým na ovplyvňovanie rizikových faktorov oboch ochorení – zákaz fajčenia, normalizácia tlaku krvi, hodnôt lipidového spektra, prísna kontrola glykémií. Z hľadiska špecifickej liečby periférneho artériového ochorenia je základom vždy pohybová liečba, z medikamentóznej liečby je indikovaná protidoštičková liečba u symptomatických pacientov, z vazoaktívnych liekov u vybranej skupiny pacientov prostanoidy, prípadne cilostazol či naftidrofuryl. Revaskularizácia je odôvodnená u pacientov s život limitujúcimi klaudikáciami s nedostatočnou odpoveďou na konzervatívnu liečbu.
Kľúčové slová:
diabetes mellitus, diagnostika PAO, liečba PAO, patogenéza PAO, periférne artériové ochorenie (PAO)
Úvod
Diabetes mellitus (DM) je ochorenie s veľkou incidenciou. Podľa svetovej zdravotníckej organizácie sa celosvetovo vyskytuje asi u 150 miliónov ľudí [1]. ADA (American Diabetes Association ) uvádza výskyt diabetes mellitus v Spojených štátoch v roku 2015 u 30,3 milióna Američanov, čo predstavuje 9,4 % americkej populácie. Rovnako periférne artériové ochorenie je tiež veľmi časté a jeho incidencia a prevalencia stúpa s vekom na viac ako 10 % populácie u 60 až 70-ročných [3]. Z hľadiska terminológie sa vo svetovom písomníctve pre ochorenia periférnych tepien končiace ischémiou používa názov peripheral arterial disease (PAD) – periférne artériové ochorenie (PAO). Termín PAO teda nezahrňuje len ochorenia končatinových artérií, ale aj ochorenia iných tepnových riečísk, s výnimkou koronárnych artérií [4]. Hoci je aj v odbornej verejnosti pojem PAO ešte stále vnímaný skôr ako ochorenie tepnového riečiska dolných končatín, pre toto ochorenie v anglosaskej literatúre poznáme aj pojem lower extremity artery disease (LEAD), čiže artériové ochorenie dolných končatín. V slovenskej literatúre sa stretneme s pojmom periférne artériové ochorenie dolných končatín (PAO DK). V nasledujúcom texte sa budeme zaoberať práve týmto ochorením (PAO DK).
Vzťah diabetes mellitus a PAO DK
Diabetes mellitus je rizikový faktor aterosklerotického postihnutia ciev vedúceho k zvýšenej kardiovaskulárnej morbidite a mortalite [5]. U pacientov s DM je vyššia nie len samotná incidencia aterosklerózy, ale proces jej vzniku je akcelerovaný a pozorujeme ho u mladších vekových kategórií než v populácii bez DM. Ateroskleróza potom u pacientov s DM zvyšuje mortalitu o 44 % [6]. S DM asociovaná progresia aterosklerózy postihuje cievy všetkých diametrov, vrátane koronárnych artérií, karotíd a artérií dolných končatín [7]. Diabetes mellitus patrí teda popri fajčení ( pomer šancí – odds ratio – OR 1,88) medzi najzávažnejší rizikový faktor PAO DK (OR 2,72) [8]. Preto neprekvapuje, že sa vo svetovom písomníctve udáva až 20–30% výskyt diabetes mellitus u pacientov s PAO DK [6]. Uvedený vzťah platí aj opačne, napríklad podľa Faglia u 22 % novodiagnostikovaných pacientov s DM 2. typu (DM2T) sa vyskytuje PAO DK [9]. U pacientov s diabetickou nohou a vredom je výskyt PAO DK viac ako 50% [10]. Vek, trvanie DM a periférna neuropatia sú asociované s vyšším rizikom PAO u pacientov s preexistujuúcim DM [8]. Známa UKPDS štúdia (United Kingdom Prospective Diabetes Study) ukázala, že každé zvýšenie glykovaného hemoglobínu o 1 % korelovalo s 28% nárastom incidencie PAO, vyššou mierou úmrtia, mikrovaskulárnych komplikácií a amputácií [11]. Táto korelácia bola vyjadrená hlavne u mužov s hypertenziou a anamnézou fajčenia. Diabetici s PAO zvyčajne ostávajú aj dlhšie hospitalizovaní, vyžadujú zvýšené náklady na komplexnú liečbu a sú aj častejšie rehospitalizovaní v porovnaní s pacientami s PAO ale bez DM. Diabetes mellitus je asociovaný so závažnejším postihnutím ciev predkolenia, zatiaľ čo fajčenie je asociované skôr s postihnutím proximálnych artérií v aorto-femorálnom úseku [11]. Súbeh oboch rizikových faktorov môže predstavovať pre pacientov reálne riziko nepriaznivého vývoja. V práci Dicka u pacientov kritickou končatinovou ischémiou sa preukázal u fajčiarov až 50% výskyt DM alebo poruchy glukózovej tolerancie [12]. Pacienti s PAO majú aj vyšší výskyt iných kardiovaskulárnych ochorení, alebo priebeh a prognózu iných kardiovaskulárnych ochorení zhoršujú [13]. Anatomická distribúcia PAO DK sa líši medzi diabetikmi a nediabetikmi. U diabetikov častejšie postihuje podkolenné tepny, býva symetrické a multisegmentálne, pričom kolaterálne tepenné riečisko môže byť tiež postihnuté stenózami. Závažnosť sa u uvedených dvoch populácií tiež líši, diabetici mávajú väčší počet stenóz/obliterácií v hĺbkovej femorálnej, popliteálnej, peroneálnej, prednej a zadnej tibiálnej artérii, či dokonca na plantárnych tepnách [14]. Základný a najčastejší klinický príznak – intermitentné klaudikácie (claudicatio intermitens) býva u pacienta s DM zriedkavejší, čo predlžuje čas do stanovenia diagnózy a častokrát sa zistí PAO až vo výrazne pokročilom štádiu. Príčinou býva diabetická neuropatia v dôsledku poruchy percepcie (hlavne nocicepcie). To predisponuje k vzniku závažných štádií PAO v zmysle vzniku ischemického ulkusu alebo gangrény. Taktiež prevalencia amputácií je u pacientov s PAO s koincidujúcim DM 5 až 15-krát vyššia než u nediabetickej populácie [15].
Patofyziológia periférneho artériového ochorenia u pacientov s diabetes mellitus
DM je charakterizovaný hyperglykémiou, dyslipidémiou, zvýšenou produkciou voľných mastných kyselín a inzulínovou rezistenciou. Tieto patologické stavy vedú následne cez komplex mechanizmov (tab. 1) k vzniku a progresii PAO [16]. Periférne artériové ochorenie je teda u diabetikov sytémové, obštrukčné aterosklerotické ochorenie s niektorými histopatologickými odchýlkami, najmä so zvýšenou incidenciou cievnych kalcifikácií.
![Patomechanizmy vzniku PAO u pacientov s DM. Upravené podľa [16]](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/ab9ed9b17393744c733f8be4f479f106.jpg)
Diagnostika
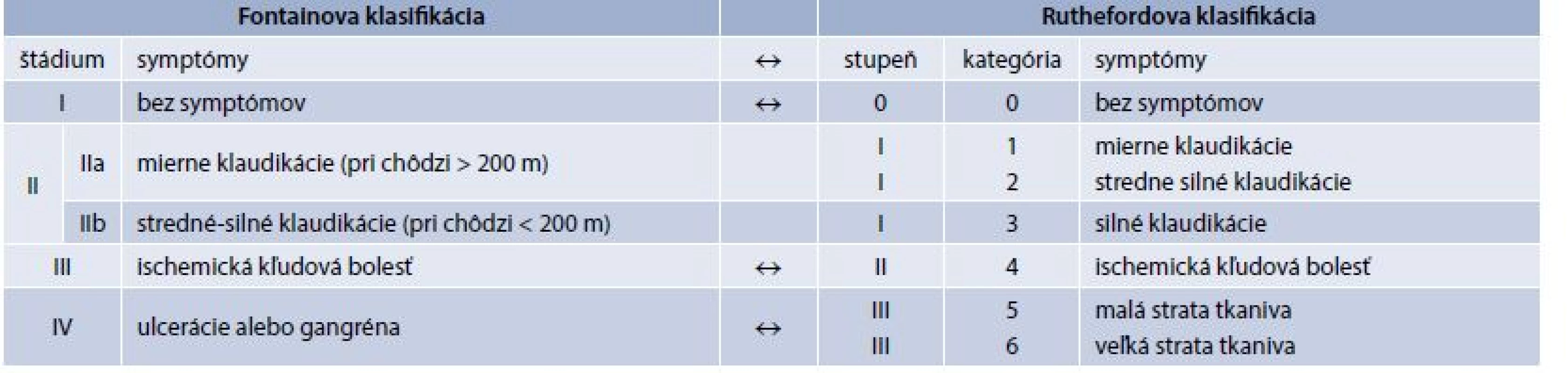
Samozrejme prvým krokom je vždy odber anamnézy, u ktorej sa zameriavame na všeobecné údaje ohľadom rizikových faktorov aterosklerózy, ohľadom prejavov obštrukcií iných častí riečiska (napr. koronárnej choroby) a prítomnosti DM. Z hľadiska PAO DK je najtypickejším prejavom claudicatio intermitens, a preto sa v anamnéze sústredíme najmä na zhodnotenie bolestí dolných končatín. Na základe okolností ich vzniku, či ich prítomnosti, potom pacientov klasifikujeme, najčastejšie podľa Fontaina alebo Rutheforda (tab. 2.). Treba si uvedomiť, že u niektorých pacientov, najmä diabetikov a starých ľudí s mnohými komorbiditami, je nezriedka prvým príznakom infekcia, alebo aj nekróza po banálnom poranení (napríklad po agresívnom strihaní nechtov). Pri fyzikálnom vyšetrení sa najmä dôsledne snažíme vyšetriť palpačne pulz na periférnych artériách, všímame si rôzne kožné zmeny, poranenia, či nekrózy.
ABI index (ankle-brachial index/členkovo-brachiálny index) je základné, jednoduché a lacné vyšetrenie s relatívne vysokou výpovednou a prediktívnou hodnotou. Abnormálne hodnoty ABI v pokoji sú ≤ 0,90, hraničné 0,91–0,99, normálne 1,0–1,4 a hodnoty ABI >1,40 hodnotíme ako non-kompresibilné. ABI ≤ 0,9 má 75% senzitivitu a 86% špecificitu pre PAO DK, jeho senzitivita však klesá u pacientov s DM a v pokročilých štádiách chronického obličkového ochorenia vzhľadom na prítomnú mediokalcinózu [17]. ABI index > 1,40 poukazuje na to, že artérie sú ťažšie kompresibilné v dôsledku extenzívnej kalcifikácie cievnej steny. Normálne hodnoty ABI však nevylučujú PAO DK. V prípade klinických pochybností môžeme doplniť pozáťažové vyšetrenie ABI alebo duplexné USG vyšetrenie artérií (DUS). V prípade pacientov s ABI ≥ 1,4 dopĺňame tzv. TBI (toe-brachial index/palcovo-brachiány index), ktorý meria rozdiel medzi brachiálnym TK a systolickým tlakom v úrovni palca, pretože tieto cievy sú zvyčajne bez kalcifikácií [18]. Za normálnych podmienok tlak v oblasti palca je asi o 30 mm Hg nižší než v oblasti členka a normálne TBI je > 0,71. Hodnota TBI of < 0,71 je indikátorom PAO. Absolútna hodnota tlaku v oblasti palca > 50 mm Hg indikuje suficientnú perfúziu a úspešnosť hojenia defektov. Naopak tlak < 50 mm Hg (TBI < 0,3) indikuje kritickú končatinovú ischémiu [19]. Aj vzhľadom na uvedené meranie TBI sa stalo súčasťou štandardných liečebných postupov u pacientov s ABI ≥ 1,4 (trieda odporúčania I, úroveň dôkazu B) [20].
Ďalšou diagnostickou možnosťou je aj využitie bežeckého pásu (treadmill test), ktorý nám môže demaskovať napríklad stredne závažné stenózy. Pozáťažový pokles členkového systolického tlaku o > 30 mm Hg alebo pokles ABI o > 20 % sú diagnostické pre PAO DK [17].
Duplexná ultrasonografia umožňuje posúdenie morfologických a funkčných zmien cievneho stromu s 85–90% senzitivitou a > 95% špecificitou pre stenózy > 50 % [21]. Podľa niektorých autorov DUS predstavuje dostačujúce vyšetrenie na určenie pacientov s nutnosťou revaskularizácie.
Medzi ďalšie diagnostické metódy patria predovšetkým CT angiografia a MR angiografia. CT angiografia má odhadovanú vysokú > 95% senzitivitu aj špecificitu pre aortoiliacké, resp. femoro-popliteálne stenózy. Jej výhodou býva aj vizualizácia rôznych anatomických špecifík (by-passy, klipy, stenty, aneuryzmy). Úskalím bývajú väčšie kalcifikácie, najmä v distálnom riečisku, brániace presnému zhodnoteniu stenóz [22]. Výhodou MR angiografie býva presnejšie zhodnotenie distálnych artérií.
Digitálna subtrakčná angiografia je dnes často potrebná pri periférnych intervenciách, alebo pre znázornenie podkolenných artérií najmä u pacientov s chronickou končatinu ohrozujúcou ischémiou vzhľadom na problémy pri zobrazení distálneho artériového riečiska inými modalitami [21].
Liečba
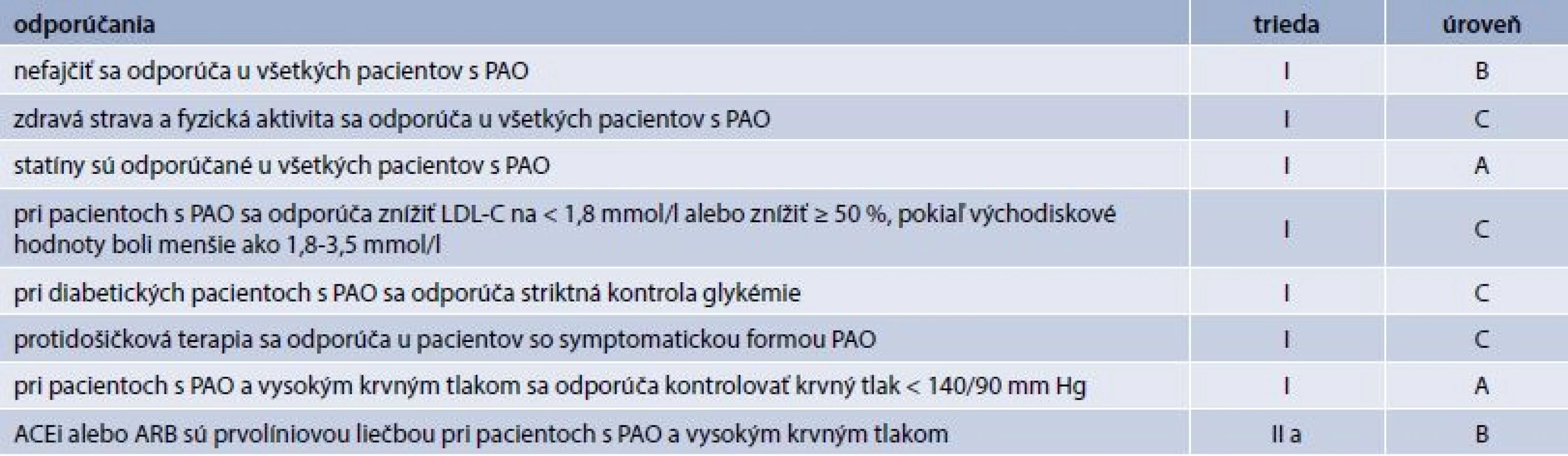
U všetkých pacientov s periférnym artériovým ochorením je indikované dodržiavanie „nešpecifických“ opatrení ako kontrola glykémie, lipidémie, hodnôt tlaku krvi. Je známe, že neuspokojivá metabolická kompenzácia je asociovaná s vyššou prevalenciou PAO a komplikácií s tým súvisiacich (amputácie, by-pass, úmrtie) [23]. Zlá metabolická kompenzácia cukrovky taktiež zhoršuje výsledky angiochirurgických zákrokov. Vzhľadom na uvedené je základom manažmentu dosiahnutie optimálnej glykemickej kompenzácie. Súčasťou sú samozrejme aj režimové opatrenia ako absolútny zákaz fajčenia, redukcia hmotnosti, nízkotuková diéta. Veľmi významnou liečebnou modalitou je záťažová liečba, preferenčne pod dohľadom odborného pracovníka. Už len pravidelný tréning dokáže predĺžiť klaudikačný interval a zvýšiť kvalitu života [24]. Z hľadiska špecifickej medikamentóznej liečby PAO DK je potrebné spomenúť protidoštičkovú a vazodilatačnú liečbu. V rámci sekundárnej prevencie sa u symptomatických pacientov s DM a PAO odporúča kyselina acetylsylicylová (75–100 mg denne) alebo klopidogrel (75 mg denne). Duálna protidoštičková terapia nie je bežne odporúčaná. U asymptomatických pacientov s PAO nie je protidoštičková liečba podľa európskych odporúčaní indikovaná [21], hoci ostatné americké odporúčania [20] považujú takúto liečbu za racionálnu pri redukcii rizika infarktu myokardu, mozgovej porážky a vaskulárnej smrti (trieda odporúčania IIa, úroveň dôkazu C). Duálna protidoštičková liečba sa odporúča len u pacientov po intervencii v trvaní 1 mesiac. U pacientov vyžadujúcich antikoagulačnú liečbu (napr. pacienti s fibriláciou predsiení alebo pacienti s venóznym tromboembolizmom) sa protidoštičková liečba pridáva ku antikoagulanciám len u pacientov s nízkym rizikom krvácania po perkutánnej intervencii spravidla na jeden mesiac [21]. Prostanoidy (napr. intravenózna infúzia prostacyklínu PGI2) by nemali byť alternatívou k revaskularizačnému výkonu pacientov diabetikov s PAO. Podľa systematickej metaanalýzy Lanea prostaoidy nemajú zmysluplný dlhotrvajúci klinický prospech pacientov s kritickou končatinovou ischémiou [24]. Avšak ovplyvnenie bolesti v období pred revaskularizáciou a zlepšenie postrevaskularizačnej ischémie sú indikácie na ich podávanie [25]. V americkom písomníctve sa odporúča cilostazol ako účinný preparát na zlepšenie symptómov a predĺženie klaudikačného intervalu (trieda odporúčania I, úroveň dôkazu A) [20]. Medzi ďalšie študované molekuly patria naftidrofuryl, pentoxifylín, buflomedil, karnitín, propionyl-L-karnitín, u ktorých máme len limitované dáta o ich vplyve na priebeh ochorenia. Všeobecné odporúčania pre liečbu POA podľa Európskej kardiologickej spoločnosti z roku 2017 sú prehľadne uvedené v tab. 3.
Revaskularizačná liečba
Všeobecne možno povedať, že revaskularizácia je odôvodnená u pacientov s život limitujúcimi klaudikáciami s nedostatočnou odpoveďou na konzervatívnu liečbu. Rovnako u každého pacienta s kritickou končatinovou ischémiou by sa mala revaskularizácia realizovať vždy, keď je to možné [21]. V zásade sa používajú jednak endovaskulárne, chirurgické alebo hybridné techniky. Problematika rervaskularizácií presahuje túto prácu, schématické odporúčania na revaskulirazáciu u pacientov s PAO sú na schéme 1. a schéme 2.
![Schéma 1 | Postup u pacientov s claudicatio intermitens. Upravené podľa [21]](https://pl-master.mdcdn.cz/media/image/82e2c6289b78b2b0ac39ce50b4c8fc89.jpg?version=1537794950)
![Schéma 2 | Revaskulizačná stratégia u diabetických pacientov s kritickou končatinovou ischémiou pri extenzívnom postihu femoropopliteálnej oblasti alebo infrapopliteálnych ciev. Upravené podľa [14]](https://pl-master.mdcdn.cz/media/image/a124b0530a2edb7b9f704be0d94c83d2.jpg?version=1537795641)
Záver
Diabetes mellitus je asociovaný s častejším výskytom a závažnejšou formou PAO. Tento výskyt koreluje s vyššou kardiovaskulárnou morbiditou a mortalitou diabetikov, skracujúcich očakávanú dĺžku života a zhoršujúcu celkovú kvalitu života. Mechanizmy vzniku PAO sú multifaktoriálne, významnú negatívnu úlohu tu hrá zlá metabolická kompenzácia diabetika.
Doručené do redakcie: 28. 2. 2018
Prijaté po recenzii: 7. 3. 2018
MUDr. Tomáš Petrovič, PhD.
Sources
1. Diabetes mellitus. [WHO]. Dostupné z WWW: <http://www.who.int/mediacentre/factsheets/fs138/en/>.
2. Statistics About Diabetes. [American Diabetes Association]. Dostupné z WWW: <http://www.diabetes.org/diabetes-basics/statistics/>.
3. Criqui MH, Aboyans V. Epidemiology of peripheral artery disease. Circ Res 2015; 116(9): 1509–1526. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCRESAHA.116.303849>. Erratum in Correction. [Circ Res. 2015].
4. Stvrtinová V, Sefránek V, Murín J et al. Peripheral arterial disease of extremities – guidelines for diagnostic and treatment. Vnitr Lek 2008; 54(2): 195–202.
5. Armstrong EJ, Rutledge JC, Rogers JH. Coronary artery revascularization in patients with diabetes mellitus. Circulation. 2013;128(15): 1675–1685. Dostupné z DOI <http://dx.doi.org/10.1161/CIRCULATIONAHA.113.002114>.
6. Marso SP, Hiatt WR. Peripheral arterial disease in patients with diabetes. J Am Coll Cardiol 2006; 47(5): 921–929. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2005.09.065>.
7. Forbang NI, McDermott MM, Liao Y et al. Associations of diabetes mellitus and other cardiovascular disease risk factors with decline in the ankle-brachial index. Vasc Med 2014; 19(6): 465–472. Dostupné z DOI: <http://dx.doi.org/10.1177/1358863X14554033>.
8. Fowkes FG, Rudan D, Rudan I et al. Comparison of global estimates of prevalence and risk factors for peripheral artery disease in 2000 and 2010: a systematic review and analysis. Lancet 2013; 382(9901): 1329–1340. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(13)61249–0>.
9. Faglia E, Caravaggi C, Marchetti R, et al. Screening for peripheral arterial disease by means of the ankle-brachial index in newly diagnosed Type 2 diabetic patients. Diabet Med 2005; 22(10): 1310–1314. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1464–5491.2005.01612.x>.
10. Prompers L, Schaper N, Apelqvist J, Edmonds M, Jude E, Mauricio D, et al. Prediction of outcome in individuals with diabetic foot ulcers: focus on the differences between individuals with and without peripheral arterial disease. The EURODIALE Study. Diabetologia 2008; 51(5): 747–755. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–008–0940–0>.
11. Jude EB, Eleftheriadou I, Tentolouris N. Peripheral arterial disease in diabetes--a review. Diabet Med 2010; 27(1): 4–14. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1464–5491.2009.02866.x>.
12. Dick F, Diehm N, Galimanis A et al. Surgical or endovascular revascularization in patients with critical limb ischemia: influence of diabetes mellitus on clinical outcome. J Vasc Surg 2007; 45(4): 751–761. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jvs.2006.12.022>.
13. Grenon SM, Vittinghoff E, Owens CD et al. Peripheral artery disease and risk of cardiovascular events in patients with coronary artery disease: Insights from the Heart and Soul Study. Vasc Med 2013; 18(4): 176–184. Dostupné z DOI: <http://dx.doi.org/10.1177/1358863X13493825>.
14. Aiello A, Anichini R, Brocco E et al. Treatment of peripheral arterial disease in diabetes: a consensus of the Italian Societies of Diabetes (SID, AMD), Radiology (SIRM) and Vascular Endovascular Surgery (SICVE). Nutr Metab Cardiovasc Dis 2014; 24(4): 355–369. Dostupné z DOI: <http://dx.doi.org/10.1016/j.numecd.2013.12.007>.
15. Selvin E, Marinopoulos S, Berkenblit G et al. Meta-analysis: glycosylated hemoglobin and cardiovascular disease in diabetes mellitus. Ann Intern Med 2004; 141(6): 421–431.
16. Paneni F, Beckman JA, Creager MA et al. Diabetes and vascular disease: pathophysiology, clinical consequences, and medical therapy: part I. Eur Heart J 2013; 34(31): 2436–2443. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/eht149>.
17. Aboyans V, Criqui MH, Abraham P,et al. Measurement and interpretation of the ankle-brachial index: a scientific statement from the American Heart Association. Circulation 2012; 126(24): 2890–2909.
18. Park SC, Choi CY, Ha YI et al. Utility of Toe-brachial Index for Diagnosis of Peripheral Artery Disease. Arch Plast Surg 2012; 39(3): 227–231. Dostupné z DOI: <http://dx.doi.org/10.5999/aps.2012.39.3.227>.
19. Hoyer C, Sandermann J, Petersen LJ. The toe-brachial index in the diagnosis of peripheral arterial disease. J Vasc Surg 2013; 58(1): 231–238. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jvs.2013.03.044>.
20. Gerhard-Herman MD, Gornik HL, Barrett C et al. 2016 AHA/ACC Guideline on the Management of Patients With Lower Extremity Peripheral Artery Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation 2017; 135(12): e726-e779. Dostupné z DOI: <http://dx.doi.org/10.1161/CIR.0000000000000471>. Erratum in Correction to: 2016 AHA/ACC Guideline on the Management of Patients With Lower Extremity Peripheral Artery Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. [Circulation. 2017].
21. Aboyans V, Ricco JB, Bartelink M-L EL et al. 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS): Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteriesEndorsed by: the European Stroke Organization (ESO)The Task Force for the Diagnosis and Treatment of Peripheral Arterial Diseases of the European Society of Cardiology (ESC) and of the European Society for Vascular Surgery (ESVS). Eur Heart J 2017; 39(9): 720–729. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehx095>.
22. Met R, Bipat S, Legemate DA et al. Diagnostic performance of computed tomography angiography in peripheral arterial disease: a systematic review and meta-analysis. JAMA 2009; 301(4): 415–424. Dostupné z DOI: <http://dx.doi.org/10.1001/jama.301.4.415>.
23. Singh S, Armstrong EJ, Sherif W et al. Association of elevated fasting glucose with lower patency and increased major adverse limb events among patients with diabetes undergoing infrapopliteal balloon angioplasty. Vasc Med 2014;19(4):307–314. Dostupné z DOI: <http://dx.doi.org/10.1177/1358863X14538330>.
24. Lane R, Ellis B, Watson L et al. Exercise for intermittent claudication. Cochrane Database Syst Rev 2014; (7): CD000990. Dostupné z DOI: <http://dx.doi.org/10.1002/14651858.CD000990.pub3>.
25. Ruffolo AJ, Romano M, Ciapponi A. Prostanoids for critical limb ischaemia. Cochrane Database Syst Rev 2010; 1: CD006544. Dostupné z DOI: <http://dx.doi.org/10.1002/14651858.CD006544.pub2>. Update in Prostanoids for critical limb ischaemia. [Cochrane Database Syst Rev 2018].
26. Piaggesi A, Vallini V, Iacopi E et al. Iloprost in the management of peripheral arterial disease in patients with diabetes mellitus. Minerva Cardioangiol 2011; 59(1): 101–108.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Forum Diabetologicum

2018 Issue 1
-
All articles in this issue
- Komplexný prístup v manažmente pacienta s diabezitou
- Manažment pacienta s diabetes mellitus a hypertenziou
- Manažment kardiovaskulárneho rizika u diabetikov v svetle aktuálnych odporúčaní
- Komplexná starostlivosť o diabetika pri kardiovaskulárnych ochoreniach
- Pacient – diabetik s periférnym artériovým ochorením
- Komplexná starostlivosť o diabetikov s končatinovocievnou artériovou chorobou
- Inhibítory PCSK9 a postavenie evolokumabu v liečbe pacientov s hyperlipoproteinémiou
- Konsenzuálne terapeutické odporúčanie Slovenskej diabetologickej spoločnosti pre diabetes mellitus 2. typu (2018)
- Vildagliptin: zkušenosti a perspektivy
- Forum Diabetologicum
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Inhibítory PCSK9 a postavenie evolokumabu v liečbe pacientov s hyperlipoproteinémiou
- Vildagliptin: zkušenosti a perspektivy
- Konsenzuálne terapeutické odporúčanie Slovenskej diabetologickej spoločnosti pre diabetes mellitus 2. typu (2018)
- Komplexný prístup v manažmente pacienta s diabezitou
