Farmakoterapie po srdečním infarktu
Pharmacotherapy following myocardial infarction
Early reperfusion is the treatment of choice for acute coronary syndrome. In the Czech Republic, reperfusion therapy is well accessible thanks to the network of 22 catheterization centres. Every year, 28,000 patients are treated using this technique. Successful reperfusion should be followed by life style changes – smoking cessation, maintenance of appropriate body weight etc. These steps than has to be accompanied by effective pharmacotherapy to prevent remodelling of the left ventricle, re-stenosis of the coronary artery, re-thrombosis and arrhythmias. Four drug groups provide the desired effects – renin-angiotensin-aldosterone system blockers, beta--blockers, antiplatelet agents and statins.
Key words:
myocardial infarction – pharmacotherapy
Authors:
L. Špinarová 1; J. Špinar 2; J. Vítovec 1
Authors‘ workplace:
I. interní kardio-angiologická klinika Lékařské fakulty MU a FN u sv. Anny Brno, přednosta prof. MUDr. Jiří Vítovec, CSc., FESC
1; Interní kardiologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Jindřich Špinar, CSc., FESC
2
Published in:
Vnitř Lék 2011; 57(11): 966-969
Category:
Birthday
Overview
Základem léčby akutního koronárního syndromu je dnes včasná reperfuze. Česká republika patří díky síti 22 katetrizačních center mezi země s vysokou dostupností reperfuzní léčby. Ročně je takto ošetřeno asi 28 000 nemocných. Po úspěšné reperfuzi musí následovat režimová opatření – nekouřit, udržovat vhodnou hmotnost atd. Vše musí být doplněno účinnou farmakoterapií, která má za úkol zabránit remodelaci levé komory, restenóze koronární tepny, retrombóze a arytmiím. K tomu slouží 4 lékové skupiny – blokátory systému renin-angiotenzin-aldosteron, beta-blokátory, antiagregancia a statiny.
Klíčová slova:
srdeční infarkt – farmakoterapie
Kardiovaskulární nemoci jsou v rozvinutých zemích hlavní příčinou úmrtí, výrazně se podílejí na invaliditě a nemocnosti populace a ve stále větší míře na rostoucích nákladech zdravotní péče [1]. Světová zdravotnická organizace (WHO) uvádí, že kardiovaskulární onemocnění jsou zodpovědná asi za 30 % celosvětové mortality [2].
Od roku 1980 do roku 2005 se průměrná délka lidského života prodloužila o 6 let: ze 72 na 78 let. Na těchto 6 letech se kardiovaskulární onemocnění podílejí 5 lety.
Je to právě zlepšená péče o pacienty s akutním infarktem myokardu, která k tomu přispěla.
Dochází k enormnímu rozvoji invazivní kardiologie: provádění angioplastik a využívání stentů. U akutního koronárního syndromu je časná perkutánní koronární intervence (PCI) preferovanou formou revaskularizace, která zlepšuje prognózu nemocných [3].
Oproti roku 1992 došlo v roce 2009 k 37násobnému nárůstu počtu angioplastik: ze 60/1 milion obyvatel na 2 250/1 milion obyvatel. V oblasti implantace stentů je situace ještě dynamičtější: 5/1 milion obyvatel v roce 1992 a 2 850/1 milion obyvatel v roce 2009.
Navzdory úspěchům v intervenční kardiologii a pokrokům ve farmakoterapii dochází u části pacientů po srdečním infarktu k vývoji srdečního selhání. Ve švédském národním registru, který sleduje hospitalizace pacientů po srdečním infarktu, byla provedena analýza dat celkem u 175 216 osob. Od sledovaného období let 1993–1995 ve srovnání s lety 2002–2004 se výskyt srdečního selhání po více než 3 letech po IM snížil z 31,49 % na 27,96 %. Přesto je toto číslo vysoké, protože přesahuje více než 1/4 pacientů (tab. 1) [4].
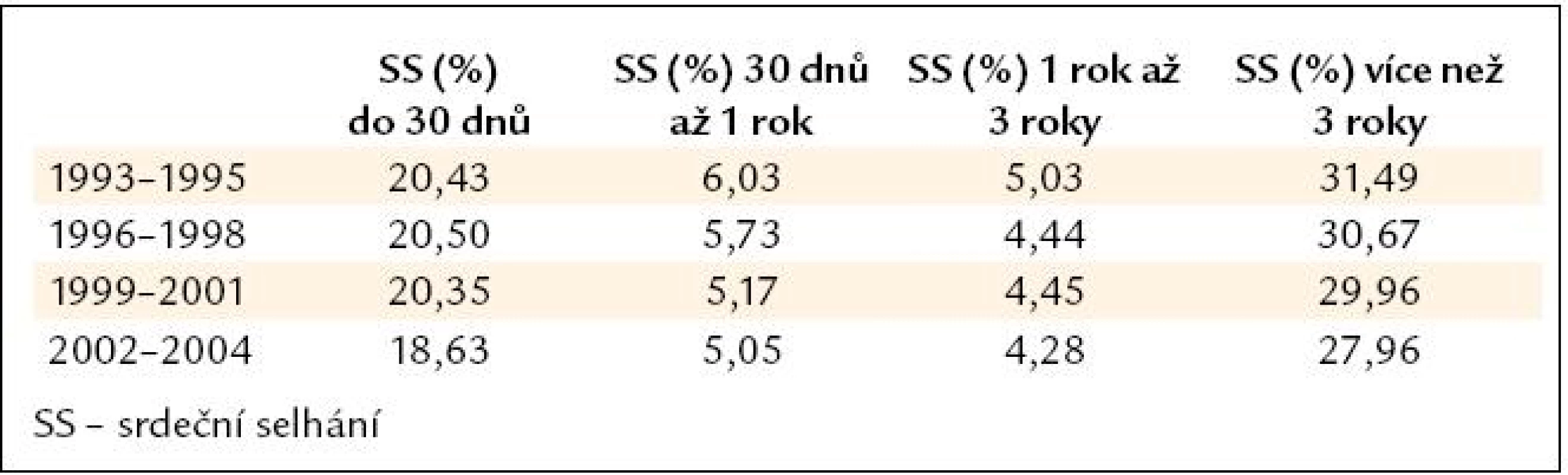
Mezi základní postupy léčby po infarktu myokardu patří:
- reperfuze,
- zábrana remodelace,
- zábrana restenózy,
- zábrana retrombózy.
Mezi základní léky po infarktu myokardu patří:
- blokáda systému renin-angiotenzin-aldosteron – inhibitory konvertujícího enzymu (ACEI) a/nebo blokátory receptoru 1 pro angiotenzin II (ARB). Ve fázi klinického zkoušení jsou přímé blokátory reninu. Základem jsou ACE inhibitory, blokátory receptoru 1 jsou vhodné při intoleranci ACEI. Na základě studií ONTARGET a VALIANT není doporučeno tyto lékové skupiny kombinovat [5–7]. U nemocných se srdečním selháním je doporučeno přidat blokátory aldosteronu.
- Beta-blokátory – jsou doporučovány všem nemocným, kteří nemají kontraindikace. Podle výsledku studie INVEST je alternativou verapamil, který je ovšem kontraindikován u nemocných se srdečním selháním [8].
- Hypolipidemika – především statiny s cílem dosáhnout hodnot cholesterolu pod 4,5 mmol/l [9]. Fibráty mortalitní data nemají, s ezetimibem mortalitní studie probíhají, kyselina nikotinová mortalitní studie nemá.
- Antiagregace – základem je kyselina acetylsalicylová, ke které se po angioplastice či stentu přidává na několik měsíců (většinou 12) clopidogrel. Ve 4. fázi klinického zkoušení jsou nové antiagregační léky jako prasugrel či ticagrelol [10,11].
Tyto lékové skupiny mají prokazatelná data na snížení mortality:
Antiagregancia. Kyselinu acetylsalicylovou (ASA) 75–100 mg denně, která snižuje riziko reinfarktu nebo úmrtí až o 25 %, podáváme trvale. Clopidogrel v dávce 75 mg/den přidaný k ASA, nebo samostatně při alergii na ASA, je indikován po dobu 1 roku u pacientů se STEMI bez ohledu na to, zda podstoupili nebo nepodstoupili reperfuzní léčbu. V dnešní době přicházejí modernější přípravky, prasugrel a ticagrelol, které vykázaly vyšší antiagregační účinnost [10,11].
Beta-blokátory. Mechanizmus působení beta-blokátorů (BB) zahrnuje více kardiovaskulárních účinků, mezi něž patří: negativně chronotropní a dromotropní efekt, snížení aktivity centrálního i periferního tonu sympatiku, snížení spotřeby kyslíku v myokardu, změna citlivosti baroreceptorů, snížení uvolňování noradrenalinu, snížení sekrece reninu, snížení presorické odpovědi na katecholaminy při námaze, antiischemický a antiarytmický vliv. V léčbě nemocných po IM jsou jednoznačně indikovány a pouze absolutní kontraindikace nebo jednoznačná nesnášenlivost jsou důvodem pro jejich nepodání. Dávku bychom také měli postupně titrovat na základě snášenlivosti do maximálně doporučených dávek (např. metoprolol 200 mg, bisoprolol 10 mg, carvedilol 2krát 25 mg). Pro dávkování beta-blokátorů bychom měli sledovat i tepovou frekvenci, která by u nemocných se sinusovým rytmem neměla být vyšší než 70 tepů/min [12].
Studie CRUSADE sledovala význam tepové frekvence u nemocných s nonST akutním koronárním syndromem u 139 194 nemocných. Vyloučeni byli nemocní se systolickým krevním tlakem < 90 mm Hg, aby se zamezilo zkreslení kardiogenním šokem. Nejnižší výskyt primárního cíle (mortalita, nefatální infarkt myokardu a nefatální cévní mozková příhoda) byl při tepové frekvenci 60–69 tepů/min, se stoupající i s klesající tepovou frekvencí výskyt stoupal [13].
ACE inhibitory a blokátory receptorů pro angiotenzin II (sartany). Inhibitory angiotenzinkonvertujícího enzymu jsou obecně uznávanou indikací v léčbě srdečního selhání a hypertenze. U nemocných po srdečním infarktu brání remodelaci levé komory srdeční, sníží výskyt reinfarktů či nového diabetes mellitus a vedou k oddálení manifestace srdečního selhání. ACE inhibitory snižují při dlouhodobém sledování mortalitu přibližně o 20 %. Léčba ACE inhibitory je u nemocných se systolickou dysfunkcí účinná bez ohledu na to, zda nemocní mají nebo nemají potíže či normální krevní tlak. Základní účinky spočívají v tom, že zlepšují životní prognózu, snižují počet hospitalizací, zpomalují progresi onemocnění, zlepšují symptomatologii, brání remodelaci srdeční, snižují výskyt infarktu myokardu a snižují výskyt nestabilní AP. V roce 2004 publikovali Pilote et al práci z registru pojišťovny v Ontariu, kde ukázali u nemocných po infarktu myokardu rozdílnou mortalitu podle typu ACEI, který užívají [14]. Nejmenší mortalitu měli nemocní užívající ramipril a perindopril, naopak nemocní užívající např. captopril, enalapril či quinapril měli statisticky významně vyšší mortalitu (tito nemocní měli ale také nejčastěji nízkou dávku ACEI). Tuto práci nepotvrdili Hansen et al na populaci více než 16 000 nemocných po infarktu myokardu v Dánsku, kde měli nemocní, pokud užívali doporučené dávky ACEI, stejnou prognózu [15]. V této práci byl referenční ACE inhibitor trandolapril. Na základě těchto výsledků se zohledněním pohodlí pacienta pro podávání léku 1krát denně můžeme uzavřít, že ověřené a doporučené ACEI jsou perindopril, ramipril a trandolapril ve vysokých dávkách, tedy 10 mg pro perindopril a ramipril a 4 mg pro trandolapril.
Sartany doporučujeme těm nemocným po infarktu myokardu, u kterých je indikováno podávání ACE inhibitorů, nemocný je však netoleruje pro suchý kašel. Jejich kombinace s ACE inhibitory nepřináší větší prospěch nemocným, pouze více nežádoucích účinků. Opět je třeba zachovat dávkování maximálně tolerované stran krevního tlaku a renálních funkcí [16–18].
Hypolipidemická léčba. Statiny mají, kromě snížení LDL-cholesterolu, vliv na skladbu a funkci buněčných membrán, ovlivňují hemokoagulaci a vnitřní trombolytickou aktivitu, zlepšují funkci endoteliálních buněk, omezují proliferaci a aktivitu buněk hladkého svalstva a řadu dalších. Hypolipidemická léčba vede ke stabilizaci sklerotických plátů, snižuje obsah lipidů v těchto plátech a vede k jejich přeměně na pláty stabilní, které jsou méně náchylné k prasknutí a ke vzniku akutní trombózy. Je prokázáno a doporučeno podávat vysoké dávky statinu (atorvastatin 40–80 mg, rosuvastatin 20–40 mg), a to již od 1. dne vzniku akutního koronárního syndromu, s postupným dosažením hodnoty celkového cholesterolu pod 4,5 mmol/l a LDL-cholesterolu pod 2,5 mmol/l [19,20].
Studie TNT zavzala 10 001 pacientů se stabilizovanou ischemickou chorobou srdeční, kteří byli randomizováni k léčbě atorvastatinem 10 mg oproti 80 mg a sledováni průměrně 4,9 let. Léčba vysokou dávkou statinu snížila riziko vzniku srdečního infarktu či cévní mozkové příhody o 22 % (p < 0,001) [21].
Blokátory aldosteronu. U nemocných po IM s dysfunkcí levé komory se prokázal jako příznivý vliv antagonistů aldosteronu, které inhibují směnu sodíku za draslík a kromě malého diuretického efektu mají i podstatný vliv na zpomalení tvorby fibrózní tkáně v myokardu a příznivý vliv na remodelaci komory. Patří sem spironolakton v dávce 25 mg a novější eplerenon s nižším výskytem nežádoucích účinků, který byl sledován ve studii EPHESUS [22].
Doporučená farmakoterapie v sekundární prevenci po IM je uvedena v tab. 2.
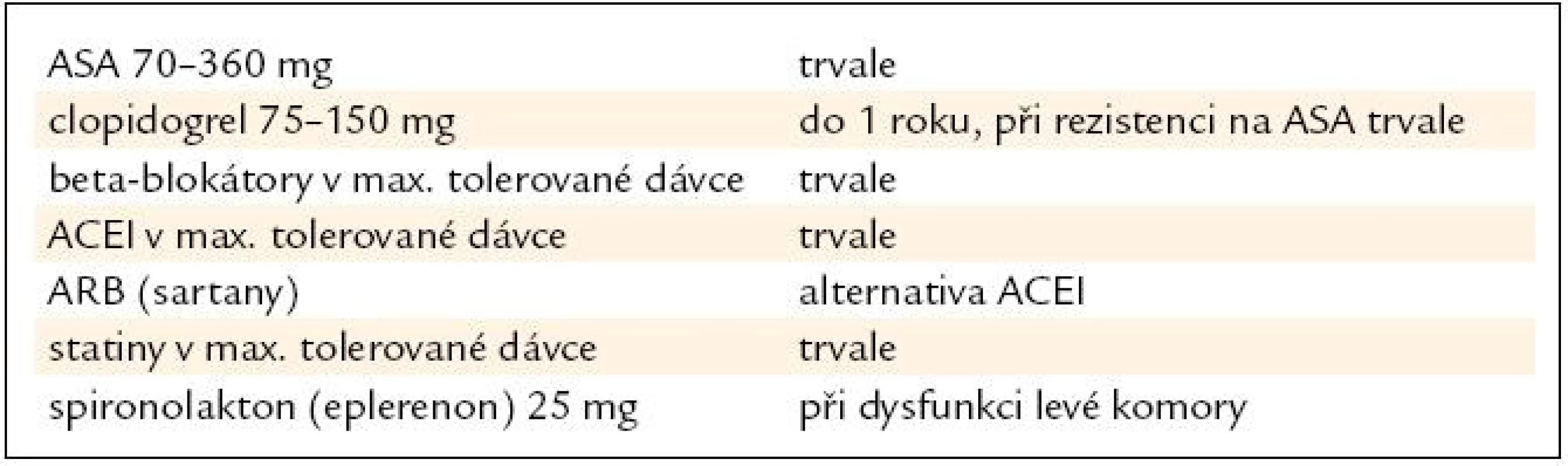
Všechny tyto poznatky se již dostaly do klinické praxe, což potvrzují výsledky studií EUROASPIRE I, II, III [23,24]. Tyto epidemiologické studie v různých zemích Evropy (8 zemí, za Českou republiku FN Plzeň a IKEM Praha) sledovaly farmakoterapii nemocných po infarktu myokardu (minimálně 6 měsíců) v letech 1996, 2001 a 2006. Data z České republiky jsou velmi povzbuzující a ukazují obrovský nárůst ve všech lékových skupinách, takže procento pacientů na každé doporučené lékové skupině přesahuje 75 % (tab. 3).
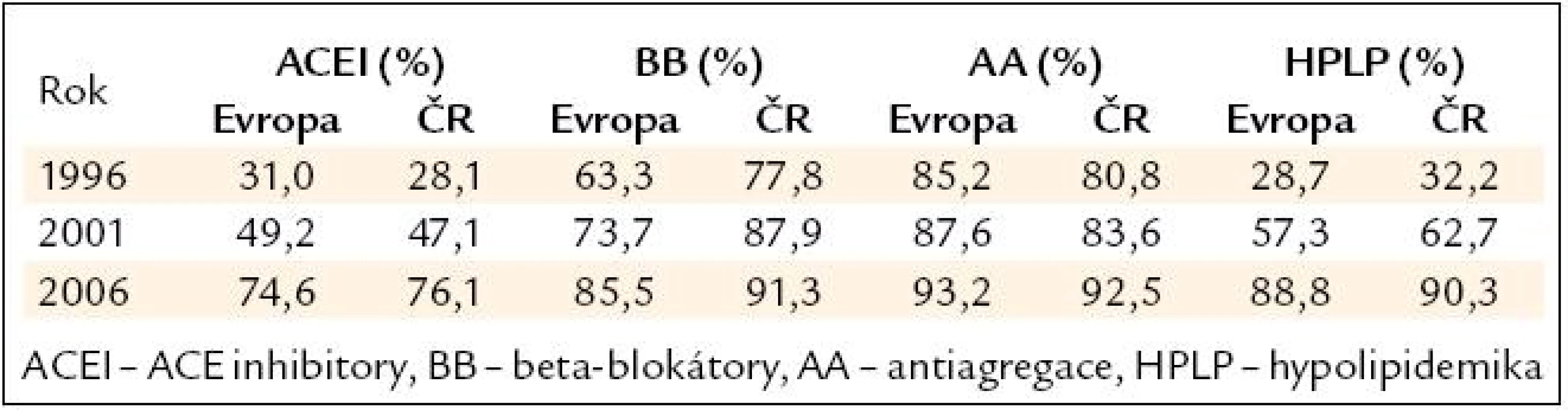
Z EUROASPIRE III (rok 2006) vyplynuly ještě 2 důležité poznatky, a to, že krevní tlak > 140/90 mm Hg mělo 62,5 % nemocných v ČR a 55,2 % v Evropě a cholesterol > 5,0 mmol/l 28,1 % nemocných v ČR a 28,5 % v Evropě. Z pohledu léčby hypertenze nebyl mezi roky zásadní rozdíl a procento nedostatečně kontrolovaných nemocných bylo podobné, z pohledu léčby dyslipidemie došlo ale k zásadní změně, protože v roce 1996 mělo v Evropě 87,0 % a v České republice 89,2 % nemocných cholesterol > 5,0 mmol/l, zatímco v roce 2006 to bylo již pouze 28,5 % v Evropě a 28,1 % v ČR. Data ze studií EUROASPIRE neobsahují údaj o dávce, a tak se domníváme, že přestože zastoupení jednotlivých lékových skupin je dobré, dochází k poddávkovávání nemocných, především u ACE inhibitorů a statinů, jinak si neumíme vysvětlit špatnou kontrolu tlaku i cholesterolu.
Trend k dalšímu zlepšení byl popsán v registru FARIM, který je právě nyní odeslán k publikaci. Popisuje 2 500 nemocných v ČR s anamnézou infarktu myokardu před > 1 měsícem, kteří navštívili ambulanci praktického lékaře, internisty či kardiologa v době od 1. 9. 2009 do 31. 3. 2010. Lékaři pomocí internetového portálu zadávali údaje o nemocných, jejich obtíže, léčbu, krevní tlak, tepovou frekvenci a základní biochemické parametry.
Průměrný krevní tlak byl 132//79 mm Hg, bez významného rozdílu mezi pohlavími, naopak se signifikantním rozdílem podle věku (do 70 let 131/79 mm Hg, nad 70 let 134/78 mm Hg, p < 0,001).
Hladina celkového cholesterolu byla 4,55 mmol/l, velmi signifikantně (p < 0,001) nižší u mužů (4,50) než u žen (4,68) a mírně signifikantně (p < 0,05) vyšší u osob do 70 let (4,60) než u starších 70 let (4,47).
Sledujeme-li kombinace uvedených 4 skupin léčiv (RAAS, BB, statiny, AA), pak 66 % pacientů užívá všechny tyto skupiny, 26 % tři z nich (přitom nejčastěji chybí BB), 7 % pouze dvě (nejčastěji jde o statin + RAAS) a pouze 2 % užívá lék pouze z 1 skupiny (nejčastěji AA).
Preskripce lékových skupin se neodlišovala mezi praktiky, internisty či kardiology [25].
Ve studii BRNO, která zahrnula 850 pacientů s anamnézou infarktu myokardu, kteří prošli ambulancemi Interní kardiologické kliniky v Brně, byla situace obdobná. 75,8 % nemocných užívalo všechny doporučené lékové skupiny dle guidelines (blokátory RAAS, beta-blokátory, statiny, antiagregancia) a každá léková skupina jednotlivě byla zastoupena u > 90 % nemocných. Nebyly rozdíly mezi muži a ženami ani staršími a mladšími. Nedostatečně byly podávány doporučené (vysoké) dávky ACE inhibitorů a statinů.
Krevní tlak < 140/90 mm Hg mělo 60,1 % nemocných, cholesterol < 5 mmol/l mělo 75 % mužů a 65 % žen a > 50 % nemocných mělo cholesterol < 4,5 mmol/l. Metabolický syndrom měla asi 1/2 nemocných a kouření přiznalo 12,5 % nemocných [26].
Závěr
Závěrem lze říci, že pokud pacient užívá všechny 4 doporučené lékové skupiny, snižuje se kumulativní 5leté riziko kardiovaskulární příhody o 70 %: z 20 % rizika při neužívání žádné lékové skupiny na 5,9 % při užívání všech 4 skupin. Počet pacientů, které je takto v následujících 5 letech potřeba léčit, aby se zabránilo vzniku jedné kardiovaskulární příhody, je 7.
Práce byla podpořena výzkumným záměrem MŠMT 0021622402.
prof. MUDr. Lenka Špinarová, Ph.D., FESC
www.fnusa.cz
e-mail: lenka.spinarova@fnusa.cz
Doručeno do redakce: 23. 8. 2011
Sources
1. Šimon J et al. Epidemiologie a prevence ischemické choroby srdeční. Praha: Grada Publishing 2001.
2. Špinar J, Vítovec J et al. Ischemická choroba srdeční. Praha: Grada Publishing 2003.
3. Groch L. Co způsobuje pokles úmrtnosti na ischemickou chorobu srdeční? – editorial. Vnitř Lék 2011; 57 : 437–438.
4. Shafazand S, Rosengren A, Lampas G et al. Decreasing trends in the incidence of heart failure after acute myocardial infarction from 1993–2004: a study of 175,216 patients with a first acute myocardial infarction in Sweden. Eur J Heart Fail 2011; 13 : 135–141.
5. ONTARGET study investigators. Yusuf S, Teo KK, Pogue J et al. Telmisartan, ramipril or both in patients at high risk for vascular events. N Engl J Med 2008; 358 : 1547–1559.
6. Pfeffer MA, McMurray JJ, Velazquez EJ et al. VALIANT Investigators. Valsartan, Captopril, or Both in Myocardial Infarction Complicated by Heart Failure, Left Ventricular Dysfunction, or Both. N Engl J Med 2003; 349 : 1893–1906.
7. Vítovec J, Špinar J. Je kombinace inhibitorů ACE a blokátorů receptorů pro angiotenzin II v léčbě kardiovaskulárních onemocnění indikovaná? Remedia 2009; 19 : 149–152.
8. Pepine CJ. INVEST group. Outcomes from randomised trial of calcium antagonist and non calcium antagonist blood pressure treatment strategy in patients with coronary artery disease. JAMA 2003; 290 : 2859–2816.
9. Vaverková H, Soška V, Rosolová H et al. Doporučení pro diagnostiku a léčbu dyslipidémií v dospělosti, vypracované výborem České společnosti pro aterosklerózu. Vnitř Lék 2007; 53 : 181–197.
10. Walentin L, Becker RC, Budaj A et al. PLATO Investigators. Ticagrelor versus clopidogrel in patients with acute coronary syndroms. N Engl J Med 2009; 361 : 1045–1057.
11. Wiviott SD, Braunwald E, McCabe CH et al. TRITON-TIMI 38 Investigators. Prasugrel versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2007; 357 : 2001–2015.
12. Borer JS. Heart rate: from risk marker to risk factor. Eur Heart J Suppl 2008; 10: F2–F6.
13. Bangalore S, Messerli FH, Ou F et al. CRUSADE Investigators. The association of admission heart rate and in-hospital cardiovascular events in patients with non--ST-segment elevation acute coronary syndromes: results from 135 164 patients in the CRUSADE quality improvement initiative. Eur Heart J 2010; 31 : 552–560.
14. Pilote L, Abrahamowitz M, Rodrigues E et al. Mortality rates in elderly patients who take different angiotensin-converting enzyme converting inhibitors after acute myocardial infarction: a class effect? Ann Intern Med 2004; 141 : 102–112.
15. Hansen ML, Gislason GH, Køber L et al. Different angiotensin-converting enzyme inhibitors have similar clinical efficacy after myocardial infarction. Br J Clin Pharm 2008; 65 : 217–223.
16. Yusuf S, Sleight P, Pogue J et al. The HOPE investigators. Effects of angiotensin-converting-enzyme inhibitor ramipril, on cardiovascular events in high-risk patients. N Engl J Med 2000; 342 : 145–153.
17. Fox KM. The EURopean Trial On reduction of cardiac events with Perindopril in stable coronary Artery disease Investigators. Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomised, double-blind, placebo-controlled, multicentre trial (the EUROPA study). Lancet 2003; 362 : 782–788.
18. Braunwald E, Domanski MJ, Fowler SE et al. The PEACE Trial Investigators. Angiotensin-converting-enzyme inhibition in stable coronary artery disease. N Engl J Med 2004; 351 : 2058–2068.
19. Pedersen TR, Faergeman O, Kastelein JJ et al. Incremental Decrease in End Points Through Aggressive Lipid-Lowering Study Group. High-dose atorvastatin versus usual-dose simvastatin for secondary prevention after myocardial infarction: the IDEAL study: a randomized controlled trial. JAMA 2006; 294 : 2437–2445.
20. Špinar J, Ludka O, Šenkyříková M et al. Hladiny cholesterolu v závislosti na věku. Vnitř Lék 2009; 55 : 724–729.
21. Waters DD, Guyton JR, Herrington DM et al. TNT Steering Committee Members and Investigators. Treating to New Targets (TNT) Study: does lowering low-density lipoprotein cholesterol levels below currently recommended guidelines yield incremental clinical benefit? Am J Cardiol 2004; 93 : 154–158.
22. Pitt B, Remme W, Zannad F et al. Eplerenone Post-Acute Myocardial Infarction Heart Failure Efficacy and Survival Study Investigators. Eplerenone, a selective aldosterone blocker, in patients with left ventricular dysfunction after myocardial infarction. N Engl J Med 2003; 348 : 1309–1321.
23. Kotseva K, Wood D, De Backer G et al. EUROASPIRE Study Group. Cardiovascular prevention guidelines in daily practice: a comparison of EUROASPIRE I, II, and III surveys in eight European countries. Lancet 2009; 373 : 929–940.
24. Mayer jr. O, Šimon J, Galovcová M et al. Úroveň sekundární prevence ischemické choroby srdeční u českách pacienců ve studii EUROASPIRE III. Cor Vasa 2008; 50 : 156–162.
25. Špinar J, Vítovec J, Špinarová L. FARIM. Farmakoterapie po infarktu myokardu. Vnitř Lék 2011; 57 : 778–784.
26. Špinar J, Ludka O, Sepši M et al v zastoupení řešitelů registru: Registr BRNO 2: farmakoterapie po infarktu myokardu. Vnitř Lék 2010; 56 : 533–540.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2011 Issue 11
-
All articles in this issue
- Aktuální a budoucí možnosti léčby osteoporózy
- Chronická pankreatitida v roce 2011
- Patofyziologické podklady inkretinové léčby: dokáže ještě více, než si myslíme?
- Jak se dívat na psychosomatickou medicínu
- Možnosti plnění mezinárodních doporučení terapie syndromu diabetické nohy v České republice
- Antibiotická léčba akutních bakteriálních infekcí
- Inkretiny změnily a dále mění strategii léčby diabetu 2. typu
- Moderní technologie v diabetologii. CSII (kontinuální subkutánní infuze inzulinu) a CGM (kontinuální glykemický monitoring) v klinické praxi
- Lze zpomalit rentgenovou progresi ankylozující spondylitidy?
- Inzulinová léčba v roce 2011
- Genetika monogénových foriem diabetu
- Terapie obezity – postupy, účinnost a perspektivy
- Patogeneze diabetes mellitus 1. a 2. typu v roce 2011 – jednotící model poruchy glykoregulace
- Nahlédnutí do budoucnosti farmakoterapie diabetes mellitus 2. typu
- Pharmacotherapy of chronic heart failure after the first decade of 21st century
- Farmakoterapie po srdečním infarktu
- Pokroky v metabolizmu a výživě 2011 a cesta k personalizované léčbě
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Antibiotická léčba akutních bakteriálních infekcí
- Moderní technologie v diabetologii. CSII (kontinuální subkutánní infuze inzulinu) a CGM (kontinuální glykemický monitoring) v klinické praxi
- Terapie obezity – postupy, účinnost a perspektivy
- Genetika monogénových foriem diabetu
