Senioři a kardiovaskulární medikace
Seniors and cardiovascular medications
Authors analyze the situation in the therapy of cardiovascular diseases – unsatisfactory situation especially from the dyslipidaemia point of view. Different groups of medications are discussed and their risks for elderly patients. Angiotensin converting enzyme blockers and their influence on the endothelial dysfunction, but the risk of hyperpotassemia are showed. The risk of gastrointestinal bleeding during the treatment with antiagregants and anticoagulants, the risk of bradycardia in beta-blockade, possible interactions with other medications lowering the heart rate are discussed. Attention is paid to calcium channel blockers, diuretics and digoxin. The table containing possible clinical symptoms of unwanted sideefect of most frequently used cardiovascular medications in elderly is added as the conclusion of the article.
Key words:
angiotensin converting enzyme inhibitors – antiagregants – beta-blockers – statins – calcium blockers – diuretics – digoxin – pharmacotherapy in elderly – unwanted side effects – interaction of medications
Authors:
H. Matějovská Kubešová; P. Weber; H. Meluzínová; J. Matějovský
Authors‘ workplace:
Klinika interní, geriatrie a praktického lékařství Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednostka prof. MUDr. Hana Matějovská Kubešová, CSc.
Published in:
Vnitř Lék 2011; 57(6): 561-570
Category:
Reviews
Overview
Autoři analyzují situaci v terapii kardiovaskulárních chorob starších nemocných, která není zcela uspokojivá, zvláště ve smyslu indikace hypolipidemik. Dále je v článku pojednáno o jednotlivých doporučovaných lékových skupinách a rizicích vyplývajících z nich pro straší nemocné – je rozebrána skupina inhibitorů angiotenzin-konvertujícího enzymu, příznivé ovlivnění endoteliální dysfunkce touto skupinou se zdůrazněním nebezpečí vzniku hyperkalemie, skupina antiagregačních preparátů, riziko gastrointestinálního i dalších druhů krvácení a možnosti využití dalších typů antiagregancií, skupina beta-blokátorů a jejich bradykardizující efekt a možnosti závažných interakcí s dalšími druhy podávané medikace, skupina statinů a jejich příznivý vliv na endoteliální dysfunkci s rizikem vzniku myopatií až rabdomyolýzy. Z dalších skupin kardiovaskulárních medikamentů je věnována pozornost blokátorům kalciového kanálu, diuretikům a digoxinu. V závěru článku je vypracována tabulka možných klinických projevů nežádoucích vedlejších účinků nejčastěji užívaných kardiovaskulárních medikamentů u starších nemocných.
Klíčová slova:
inhibitory angiotenzin-konvertujícího enzymu – antiagregancia – beta-blokátory – statiny – kalciové blokátory – diuretika – digoxin – farmakoterapie ve stáří – nežádoucí vedlejší účinky – lékové interakce
Úvod
Problematika polymorbidity, polyfarmakoterapie a specifických rysů medikace u seniorů je v našem i zahraničním písemnictví opakovaně rozebírána [1–6], včetně neuspokojivé situace v oblasti náležitosti terapie ordinované starším nemocným, kdy se ve snaze o respektování doporučení odborných společností můžeme za určitých okolností dostat do přímého rozporu s Beersovými kritérii [7,8] zahrnujícími léky potenciálně nevhodné pro nemocné vyššího věku.
Ze studie prováděné nedávno na našem pracovišti vyplynuly některé skutečnosti, které je možné hodnotit právě z těchto pohledů prakticky protichůdně.
Populace starších nemocných s různými formami ischemické choroby srdeční je léčena z poloviny kombinací medikamentů doporučovanou kardiologickými odbornými společnostmi, tedy inhibitory angiotenzin-konvertujícího enzymu, beta-blokátory a antiagregační terapií, nejčastěji v podobě kyseliny acetylsalicylové a při její nesnášenlivosti ticlopidinem či clopidogrelem. Hypolipidemiky je léčena jen asi 1/3 těchto nemocných. Významný podíl starších nemocných s ICHS užívá pravidelně diuretika, nitráty a blokátory kalciového kanálu. Pětina starších nemocných s ICHS je digitalizována, nutno ovšem přiznat, že ne vždy v souladu s doporučeními odborné společnosti. Warfarinizováno je asi 5% starší populace s ICHS. Analýzu složení medikace souboru 126 nemocných nad 75 let věku před přijetím na geriatrické oddělení pro akutní koronární syndrom ukazuje graf 1.
![Zastoupení lékových skupin v medikaci nemocných starších 75 let přijatých k hospitalizaci na geratrické oddělení pro akutní koronární syndrom – n = 126, převzato z [31]. ACEI – inhibitory angiotensin-konvertujícího enzymu, ARB – blokátory receptorů angiotenzinu, BB – beta-blokátory, ASA – kyselina acetylsalicylová.](https://pl-master.mdcdn.cz/media/image/ff447c64294278aab49e48f5174fb847.jpg?version=1537797825)
Při vyhodnocení podílu kardiovaskulární medikace v seniorské populaci bez rozdílu v základní diagnóze pacientů léčených v ordinacích praktických lékařů zjistíme, že téměř 60% seniorů pravidelně užívá ACEI nebo sartany, 40% seniorů užívá pravidelně beta-blokátory či diuretika a 1/3 seniorů má zavedenou terapií antiagregancii či hypolipidemiky [9] (graf 2). Při tomto vysokém zastoupení lékových skupin v populaci seniorů je nutné samozřejmě zvážit celkové počty a druhy užívaných léků, abychom mohli objektivně zhodnotit riziko pro konkrétního nemocného.

Jako další rizikový faktor se vzhledem ke starší populaci jeví rozmanitost farmaceutického trhu s desítkami firemních názvů jednoho generika a mnohdy praktická nečitelnost skutečného názvu generika pro nemocného s deficitem vizu.
Z těchto důvodů je nutné se zabývat problematikou užívaného lékového schématu u seniorů na všech úrovních zdravotnické péče a s prozíravou ostražitostí a za opakovaného důkladného vysvětlování schéma modifikovat, redukovat či jinak racionálně upravovat.
Inhibitory angiotenzin-konvertujícího enzymu (ACEI), blokátory receptorů angiotenzinu I
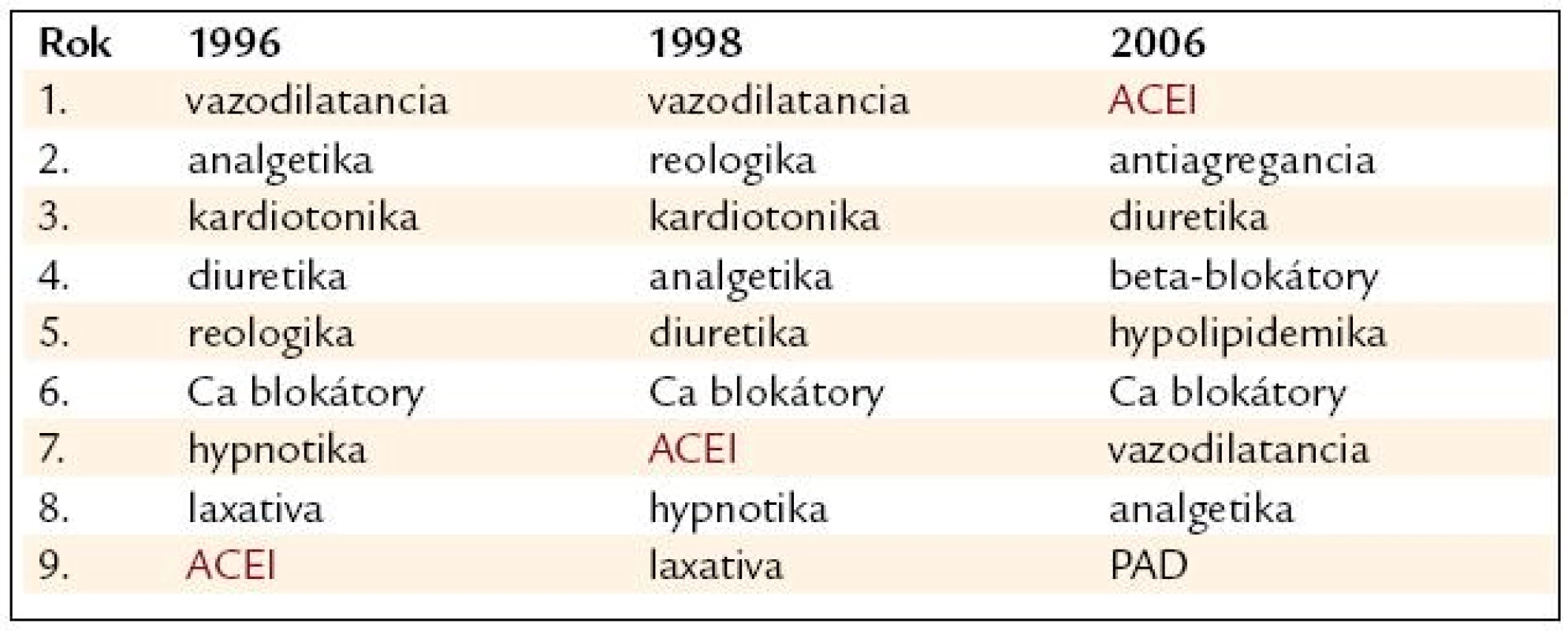
V současné době jsou vůbec nejčastěji podávanou lékovou skupinou u seniorů. Vzhledem k zastoupení nejčastějších chorob ve vyšším věku – ischemická choroba srdeční, hypertenze, diabetes mellitus – lze jejich podávání označit za velmi racionální, neboť jeden medikament, dnes již většinou v podání jednou denně, ovlivňuje rovnou 3 choroby staršího nemocného. V terénní praxi se tato užitečnost ACEI projevila v jasném trendu postupu v pořadí nejčastěji předepisovaných lékových skupin [4,9] – tab. 1. K podobným výsledkům dospěli ve svém sledování i kanadští autoři [10].
Souhrn údajů o přípravku uvádí jedinou kontraindikaci – angioneurotický edém, referuje v rámci nežádoucích účinků o známém dráždivém kašli, z hlediska starších nemocných je podstatný údaj o možném zhoršení renálních funkcí, o palpitacích a poruchách srdečního rytmu, možných závratích a synkopách a náhlém poklesu krevního tlaku při zahájení léčby, i když tzv. fenomén první dávky, jak jsme jej znali u periferních vazodilatancií, zvláště hydralazinových preparátů či prazosinu, není naštěstí tak výrazný a častý. Skupina ACEI je jmenována mezi léky způsobujícími závratě výrazně častěji než ostatní lékové skupiny u nemocných léčených na otorinolaryngologii [11].
Významné a bohužel často opomíjené jsou možné interakce s další kardiologickou, ale i nekardiologickou medikací. Právě podávání ACEI změnilo naše nazírání na hladinu kalia u kardiaků i hypertoniků. V dobách, kdy se pro terapii srdečního selhání užívala kombinace digoxinu a diuretik, byla naší hlavní obavou hypokalemie, která zvyšovala toxicitu digoxinu a pohotovost k arytmiím. Dbali jsme tedy na to, aby byla diuretická terapie buď v kombinaci s kalium šetřícím diuretikem, nebo suplementací kalia. V současné době řešíme opačný problém – ACEI již podstatou svého účinku mají tendenci způsobovat hyponatremii a hyperkalemii a v kombinaci s kalium šetřícími diuretiky, zvláště s antagonisty aldosteronu, mohou vyvolat u seniorů až hyperkalemii ohrožující život. Nejsou výjimkou sérové koncentrace kalia až 8,5 mmol/l [12]. Významná je z hlediska adekvátní péče o seniory polemika mezi dialyzačními středisky o indikaci hemodialýzy u farmakologicky indukované hyperkalemie.
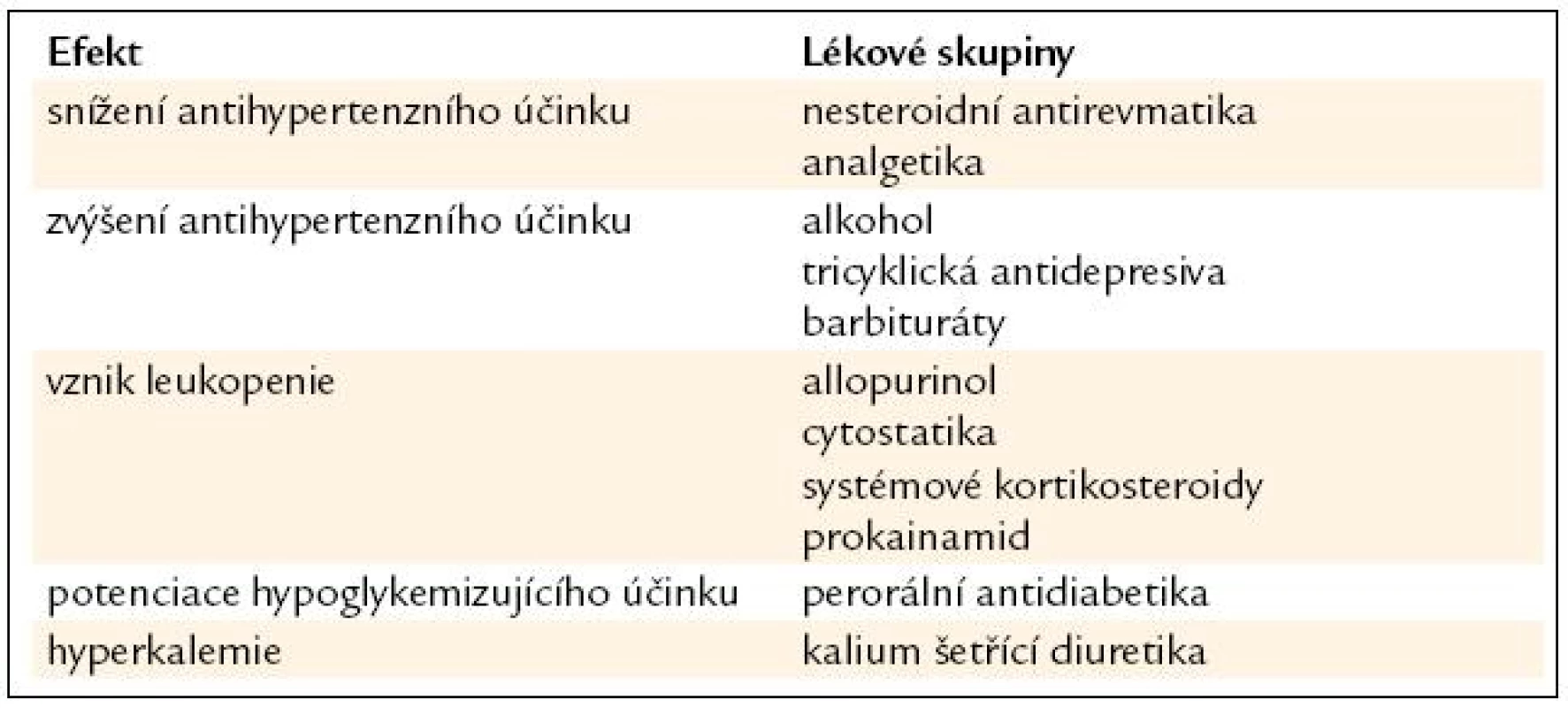
Interakce další medikace s ACEI ve smyslu ovlivnění antihypertenzního účinku a dalších efektů ukazuje tab. 2.
Z hlediska spektra předepisovaných ACEI je zřejmý trend obratu k preparátům, které je možné podávat v jedné denní dávce. Z preparátů s kratší účinnosti je captopril užíván dnes již prakticky výhradně pro řešení hypertenzní krize, enalapril si však zachovává ještě poměrně značné zastoupení – přibližně 7,5% klientů praktických lékařů [9] – a právě u seniorů je mnohdy podáván pouze v jedné denní dávce, tedy v dávkování, které velmi pravděpodobně nezaručí celodenní uspokojivé hodnoty krevního tlaku. Z hlediska indikace ACEI při chronickém srdečním selhání upozorňuje Pilote et al na výsledky studie porovnávající dlouhodobou mortalitu nemocných léčených captoprilem, enalaprilem a ramiprilem ve 3 kanadských provinciích. Nemocní léčení captoprilem a enalaprilem vykazovali o 10–15% vyšší 3letou mortalitu v porovnání s nemocnými léčenými ramiprilem. Design této studie však byl následně poněkud zpochybněn [13].
Relativně nová informace o jednom z možných nepříznivých efektů ACEI u starších nemocných byla publikována v Japonsku, kde dlouhodobá prospektivní studie, která běží již od roku 1958 v podobě 2letého pravidelného vyšetřování vzorku populace, prokázala v letech 1994–2004 průměrný roční pokles minerální kostní hmoty v krčku kosti stehenní o 1,14% u žen a 0,38% u mužů. Na tomto poklesu se dle analýzy autorů nejvíce podílely právě ACEI a v menší míře také benzodiazepiny [14].
Vliv ACEI na endoteliální funkce vychází z průběžné dlouholeté diskuze spíše pozitivně, nyní byla publikována dvojitě slepá randomizovaná studie potvrzující u nemocných s revmatoidní artritidou významný příznivý vliv ACEI přidaných k běžné terapii antirevmatiky na endoteliální funkce v podobě snížení oxidativního stresu a snížení aktivity zánětlivých markerů [15].
V diskuzích ohledně kombinovaného podání ACEI a ARB je oběma skupinám přiznáván prakticky identický příznivý vliv na endoteliální dysfunkci, nejsou však zatím k dispozici argumenty pro vzájemnou potenciaci tohoto efektu při kombinování obou. Stejně tak byl prokázán příznivý vliv obou skupin na kardiovaskulární morbiditu i mortalitu, kombinace obou skupin nevedla k dalšímu zlepšení, docházelo však ke kumulaci nežádoucích účinků. Jako jediná evidence-based indikace ke kombinaci ACEI a ARB zůstává chronické srdeční selhání s nedokonalou neuroendokrinní blokádou při podávání samotných ACEI [16]. Guidelines České kardiologické společnosti udávají jako indikaci kombinace ACEI a ARB nedostatečně kontrolovanou hypertenzi či výraznější proteinurii [17].
Antiagregační, antikoagulační terapie
Nejčastější látkou navozující antiagregační efekt u starších nemocných je v našich podmínkách kyselina acetylsalicylová (ASA). O příznivém vlivu antiagregace na morbiditu i mortalitu kardiovaskulárních chorob dnes již nikdo nepochybuje. Studie efektivity preventivních opatření kardiovaskulárních chorob prováděná v USA umístila podávání aspirinu na jedno z předních míst [18]. Byl prokázán i příznivý vliv ASA na hemoreologické vlastnosti, a tím na vývoj mikroangiopatických komplikací u diabetiků [19]. V naší seniorské populaci je ASA léčeno 35% klientů praktických lékařů a 50% klientů s ICHS, dalších 10% klientů užívá pro nesnášenlivost ASA jiné antiagregans – nejčastěji clopidogrel či ticlopidin.
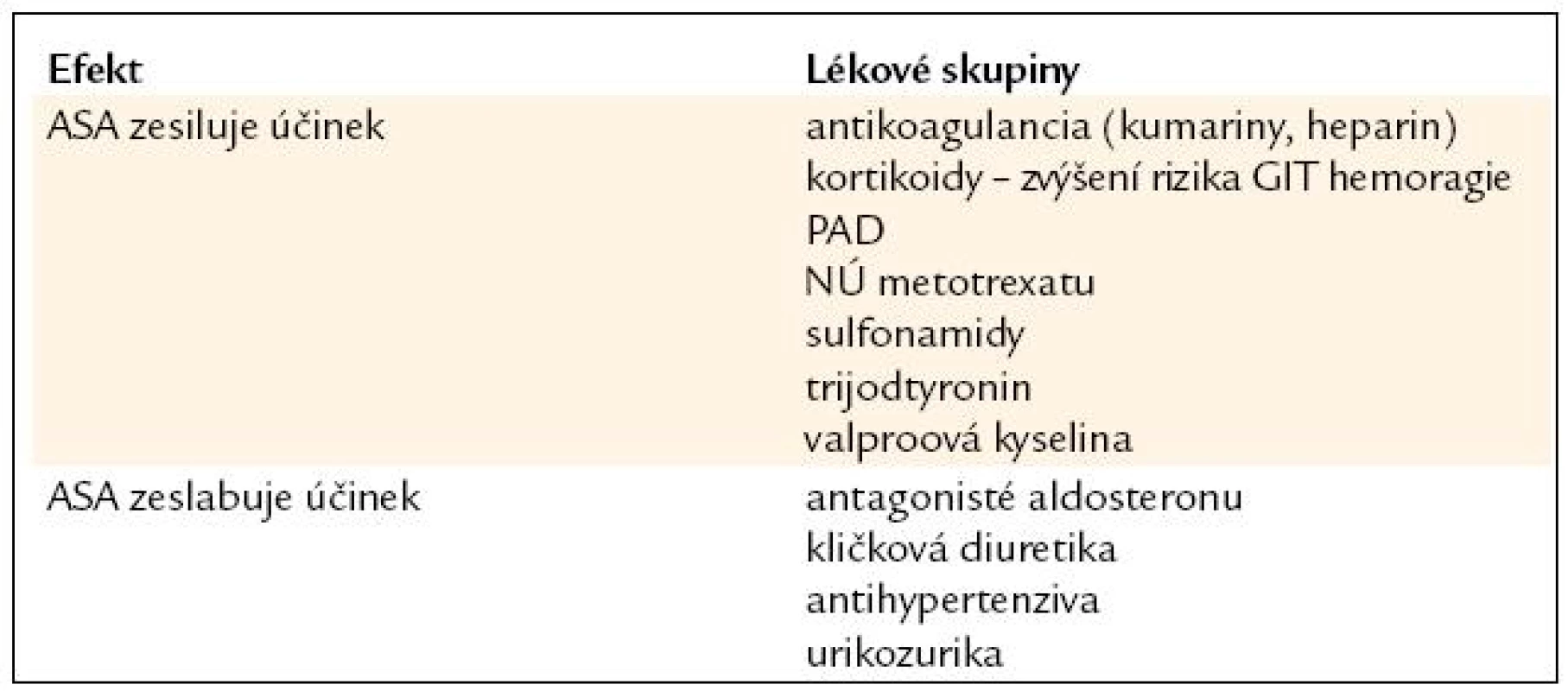
Souhrn farmaceutických údajů o ASA kontraindikuje její podání u vředové choroby gastroduodena a při patologickém sklonu ke krvácení, nabádá k opatrnosti u nemocných s bronchiálním astmatem, poškozením funkce jater a ledvin a s chronickými gastrointestinálními obtížemi. Interakce ASA s dalšími lékovými skupinami ukazuje tab. 3.
V běžné praxi nejčastěji narážíme na krvácivé komplikace, které sice vzniknou v době užívání ASA, jejich vznik je však často potencován vzhledem k vysokému výskytu onemocnění pohybového systému užíváním dalších nesteroidních antirevmatik. Alarmující byly výsledky šetření kanadských autorů prověřující účinnost Canadian guidelines – doporučení pro terapii nesteroidními antirevmatiky u seniorů. Souběžně s nesteroidními antirevmatiky byla ASA předepisována u 37% nemocných, cytoprotektivní terapie byla sice podávána 38% nemocných sledované skupiny, nicméně nerespektovala právě toto zvýšené riziko [20].
V případě nesnášenlivosti nebo omezené účinnosti či jiné kontraindikace podání nahrazujeme ASA jinými antiagregancii blokujícími reverzibilně či ireverzibilně agregační aktivity – clopidogrel, ticlopidin. Clopidogrel (Plavix) je podáván v prvních měsících po provedených invazivních výkonech na arteriích, především koronárních, některá pracoviště jej podávají v této indikaci i v kombinaci s ASA. Profylaktická efektivita ticlopidinu byla také opakovaně prokázána, pro starší nemocné je však tento preparát zařazen v seznamu potenciálně nevhodných léčiv ve stáří pro nebezpečí vzniku neutropenie a trombocytopenie [2,3]. Proto jsou po dobu jeho podávání nutné kontroly krevního obrazu. Jako další alternativa ASA bývá uváděn indobufen (Ibustrin), který má však zkříženou alergii s ASA. Další možným postupem je ovlivnění sérových srážecích faktorů a také zlepšení hemoreologických vlastností sulodexidem (Vessel due F).
Diskutovanou oblastí je možný podíl podávání ASA jako preparátu s antirevmatickými účinky na zpomalení vývoje Alzheimerovy demence (AD). Přítomnost sterilního zánětu v neuronech byla u AD opakovaně prokázána a nesteroidní antirevmatika byla opakovaně navrhována jako jedna z léčebných či podpůrných modalit, zvláště druhy antirevmatik s prokázanou selektivní aktivitou proti A-β(42). I v současné době je však možné nalézt rozdílné závěry studií. Dvanáctileté sledování 1 019 seniorů, z nichž 209 jevilo na počátku sledování počínající známky AD, neprokázalo závislost dalšího vývoje kognitivních funkcí na užívání nesteroidních antirevmatik včetně ASA [21]. Na druhé straně ukázala metaanalýza několika studií zahrnujících 13 000 nemocných, u nichž byly v 820 případech prokázány známky počínající AD, jednoznačný efekt nesteroidních antirevmatik včetně ASA na snížení výskytu AD, neprokázala ale závislost na druhu antirevmatika vzhledem k A-β(42) [22].
Jednou z nejdiskutovanějších otázek v klinické praxi u starších nemocných s kardiovaskulárním postižením je, zda má být dlouhodobou profylaxí mozkové příhody při fibrilaci síní u starších nemocných ASA či warfarin. Z praxe jsou známy argumenty pro podporu obou přístupů i proti ní, u mladších seniorů se jeví prospěšnější warfarin, nicméně jistě všichni máme zkušenost s jinak velmi zachovalým warfarinizovaným sedmdesátníkem a dramatickým průběhem jeho např. chirurgické komplikace či fatální mozkové hemoragie. Z tohoto pohledu byl studií RE-LY prokázán jako podstatně bezpečnější nový přípravek dabigatran [23].
Velká populační studie britských autorů zahrnující 41 900 nemocných konstatovala častější profylaxi ASA než warfarinem u seniorů s fibrilací síní ve věku nad 85 let ve srovnání se skupinou 40–65letých. Nejčastějším faktorem upřednostnění ASA byl kognitivní deficit a výskyt pádů. Po 6letém sledování překvapivě nebyl nalezen významný rozdíl ve výskytu kardioembolizačních příhod. Varovné však bylo zjištění, že roční perzistence profylaxe dosáhla pouze 70% u nemocných léčených warfarinem a 50% u nemocných léčených ASA. Autoři z tohoto faktu vyvozují, že v každodenní klinické praxi pravděpodobně není dosahováno všech efektů dané terapie, jak je ukazují výsledky klinických studií [24].
Nová doporučení Evropské kardiologické společnosti týkající se antikoagulační či antiagregační léčby u starších nemocných s fibrilací síní zahrnují stratifikaci nemocných podle možných rizik vyplývajících ze samotné arytmie a souběžných onemocnění (CHADS2 skóre – chronické srdeční selhání, hypertenze, věk nad 75 let, diabetes mellitus, mozková příhoda dříve proběhlá, CHADS2-VASC2 – vaskulární onemocnění, mužské pohlaví), ale také možných rizik vyplývajících z antikoagulační či antiagregační léčby (HAS-BLED skóre – hypertenze, abnormální renální funkce, mozková příhoda v anamnéze, krvácení v anamnéze, labilní INR, věk nad 65 let, abúzus léků nebo alkoholu) [25].
Beta-blokátory
Tato skupina léků prošla poměrně dlouhým vývojem, a to jak z hlediska chemického, tak i z hlediska klinického náhledu. Dnes je již zcela běžné ordinovat v klinické praxi cíleně beta-blokátory neselektivní a samozřejmě častěji selektivní, beta-blokátory s vnitřní sympatomimetickou aktivitou či bez ní. Beta-blokátory jsou v dnešní době jednou z mála lékových skupin se zcela nepochybně a opakovaně prokázaným příznivým vlivem na morbiditu i mortalitu ischemické choroby srdeční. Jsou upřednostňovány v terapii arytmií před ostatními antiarytmiky právě pro jejich dlouhodobý příznivý efekt oproti původním klasickým antiarytmikům. U starších hypertoniků, zvláště se systolickou hypertenzí, je vhodné využít blokády β-receptorů k ovlivnění systolického krevního tlaku. Relativně častou indikací podání ve vyšším věku je i hypertyreóza.
Z hlediska rizik u starších nemocných je nutno mít na paměti, že i nepatrná dávka může u citlivějších seniorů vyvolat závažnou bradykardii a poruchy atrioventrikulárního převodu až s klinickými projevy závratí a pádů s rizikem závažných poranění. Nejednou je možné zrušit u staršího nemocného s prokázanou atrioventrikulární blokádou plánovanou implantaci kardiostimulátoru, protože kontrolní Holterovo monitorování prokázalo po vysazení poslední minimální dávky beta-blokátoru vymizení blokády a zrychlení tepové frekvence na zcela přijatelné hodnoty. Tento efekt může být samozřejmě umocněn podáváním dalších medikamentů – nejdelší známý efekt má v tomto smyslu digoxin, v současné době se k němu přidává i relativně často předepisovaná skupina antidepresiv typu SSRI [26]. Opomíjeným vlivem potencujícím vznik AV blokády vyšších stupňů při terapii beta-blokátory je hypotyreóza.
Velká švédská studie zabývající se analýzou 61 788 nežádoucích účinků medikamentů za 15 let odhalila nejčastější příčinu torsades de pointes jako nežádoucího účinku sotalol a jako 3. nejčastější citalopram [27].
Velmi opatrně jsme zvyklí zavádět blokádu β-receptorů u starších nemocných s chronickou srdeční insuficiencí na hranici kompenzace pro možnost dalšího zhoršení kontraktility myokardu a manifestaci selhávání. Ještě závažnější je situace u nemocných s CHOPN a pravostranným selháváním. Dlouhodobé podávání nízkých dávek beta-blokátorů nemocným se srdečním selháním ve stabilizovaném stavu bylo opakovaně prokázáno jako jednoznačně příznivé. Poslední doporučení jsou však i pro starší nemocné poněkud razantnější – blokáda β-receptorů by měla být zavedena u všech nemocných NYHA II-III nejpozději 1 měsíc po dekompenzaci. Doporučovány jsou vysoce selektivní beta-blokátory bisoprolol nebo nebivolol. V případě nežádoucího poklesu krevního tlaku či tepové frekvence musí být beta-blokátory upřednostněny před ostatními antihypertenzivy nebo bradykardizujícími preparáty [28].
V této oblasti jsou v posledních letech hojně využívány blokátory α - i β-adrenergního účinku – vůbec poprvé proběhla multicentrická, dvojitě slepá, randomizovaná studie srovnávající u starších nemocných s chronickým srdečním selháním efekt vysoce kardioselektivního beta-blokátoru bisoprololu a alfa - i beta-blokátoru carvedilolu – CIBIS-ELD. Výsledky studie byly publikovány v roce 2009. Zahrnovala 800 nemocných průměrného věku 73 let a její výsledky ukázaly sice obtížnější titrovatelnost dávky beta-blokátorů u nemocných vyššího věku, nicméně podobnou tolerabilitu obou zkoumaných léčiv. Cílové dávky beta-blokátorů – tedy 50mg carvedilolu nebo 10mg bisoprololu – však dosáhlo bez nežádoucích vedlejších účinků pouze 25%, resp. 24% pacientů [29]. Známé jsou výsledky randomizované studie porovnávající efekt metoprololu a carvedilolu u celkem 25 000 amerických veteránů se srdečním selháním (first prescription). Výsledky studie ukazují, že starší nemocní byli po několika měsících léčeni dávkou nižší než 50% dávky obecně doporučované, hlavním důvodem snížení dávkování byl výskyt nežádoucích vedlejších účinků. V celkovém hodnocení vykazovali delší dobu přežití nemocní léčení metoprololem, autoři sami ale přiznávají přítomnost mnoha faktorů, které mohou interpretaci výsledků ovlivňovat [30].
U diabetiků starších i mladších podáváme beta-blokátory spíše méně často, a to vždy za důkladného zvážení rizika zastření příznaků hypoglykemie, případně vyvolání hypoglykemie u diabetiků léčených inzulinem či perorálními antidiabetiky. Dalším rizikem je zhoršení prokrvení končetin, zvláště u diabetiků s mikroangiopatií se vznikem periferních vazospazmů a urychlením vývoje diabetické nohy.
Další skupinou, u které nelze v léčbě ischemické choroby srdeční plně využít výhod blokády β-receptorů, jsou nemocní s CHOPN – i beta-blokátory prezentované jako vysoce β1-selektivní (bisoprolol), je obvykle možné podávat jen ve velmi nízkých dávkách.
Rizikovým obdobím u starších nemocných je ukončování terapie beta--blokátory či přerušení léčby z důvodu non-compliance samotného nemocného. V rámci rebound fenoménu známe ze zkušenosti i velmi závažné tachyarytmie – nejčastěji tachyfibrilaci či flutter síní s nízkým stupněm převodu na komory, závažné zhoršení anginy pectoris až vznik infarktu myokardu či vznik hypertenzní krize.
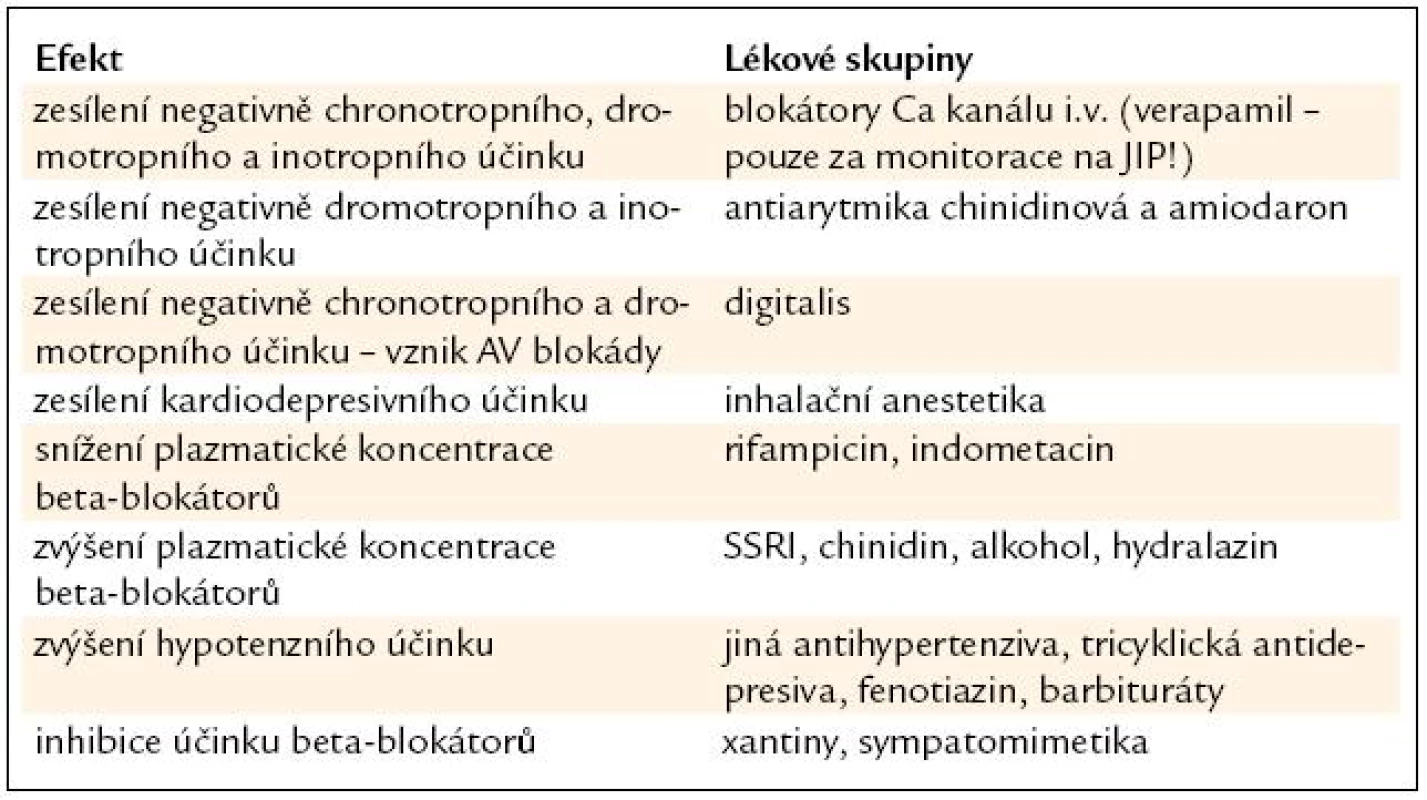
Nejvýznamnější lékové interakce beta-blokátorů jsou zachyceny v tab. 4.
Amiodaron
Po zveřejnění výsledků antiarytmických studií se amiodaron ocitá na jednom z čelních míst mezi doporučovanými antiarytmiky v akutním i dlouhodobém podávání. Časté zastoupení chronických supraventrikulárních arytmií ve vyšším věku znamená vysokou pravděpodobnost zařazení amiodaronu do lékového schématu. Zároveň však vzhledem k vysokému výskytu latentních tyreopatií v seniorské populaci a k vysokému obsahu jódu v molekule amiodaronu je třeba mít se na pozoru před klinickou manifestací až dekompenzací preexistující tyreopatie. V tomto směru přináší novou léčebnou modalitu dronedaron, jehož antiarytmické vlastnosti jsou srovnatelné s amiodaronem, dronedaron však neobsahuje jód. Lze očekávat, že v blízké budoucnosti bude v léčbě fibrilace síní, jako nejčastější arytmie seniorského věku, nahrazen amiodaron dronedaronem.
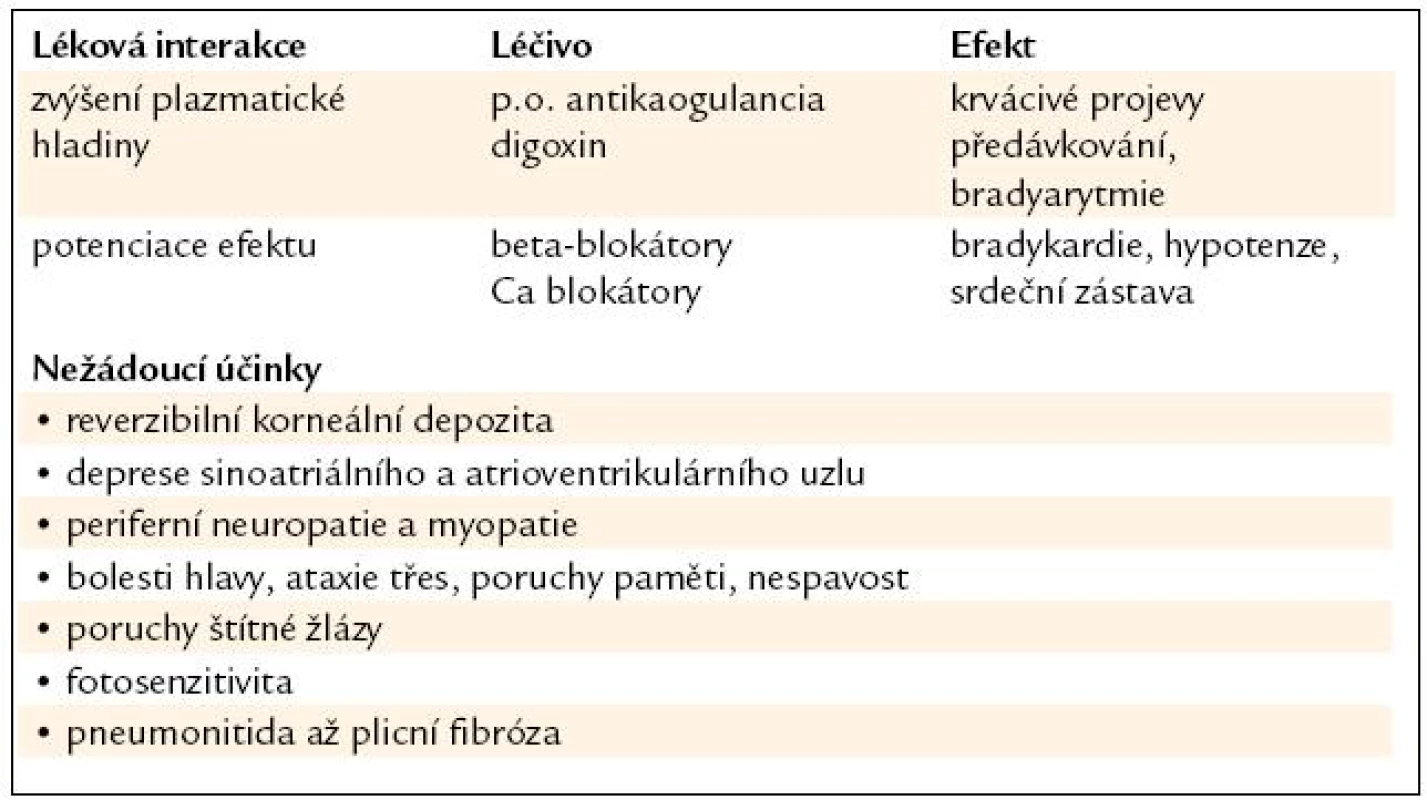
Riziko kumulace amiodaronu v rohovce, a z tohoto faktu vyplývající nutnost přerušovaného dávkování, je známa již od samotného počátku klinického užití amiodaronu v 80. letech minulého století stejně jako možnost vzniku periferní neuropatie, poruch spánku, poruch paměti a plicní fibrózy, tzv. amiodaronových plic. Nepříznivě se může kumulovat myopatie vyvolaná amiodaronem souběžně podávaným se statiny. Méně pozornosti je věnováno relativně časté hyperpigmentaci na nekrytých místech kůže, která také může signalizovat nežádoucí kumulaci preparátu [32].
Další možné interakce a nežádoucí účinky amiodaronu uvádí tab. 5.
Statiny
Statiny užívá přibližně 1/3 nemocných s diagnostikovanou ischemickou chorobou srdeční a polovina geriatrických nemocných po prodělané kardiovaskulární příhodě [29]. Tato hodnota je poměrně nízká vzhledem k přínosům, které snižování hladin krevních lipoproteinů, ale i vlastní aktivity statinů, např. na endoteliální dysfunkce znamenají. Podobná konstatování můžeme najít i v zahraničních literárních zdrojích [33,34].
V našich podmínkách byla preskripce statinů již poměrně dlouhou dobu uvolněna i pro praktické lékaře, nicméně jí nebyly přizpůsobeny limity zdravotních pojišťoven. Jen dostatečně vytrvalí nemocní si nakonec předepsání doporučeného statinu „vyběhali“. V současné době poklesů úhrad zdravotními pojišťovnami nebudou sice preskripcí statinů tak zatíženy sledované náklady praktických lékařů a ambulantních specialistů, finanční zatížení, které takto přejde na samotné nemocné, bude ale zcela jistě pro mnohé z nich limitující. Omezená perzistence statinů v terapeutické kombinaci byla konstatována i americkou analýzou průběhu léčby statiny. Nemocní s hyperlipidemií bez předchozí kardiovaskulární příhody užívali statiny 150–200 dní, nemocní v sekundární prevenci, tedy po kardiovaskulární příhodě, užívali statiny 200–250 dní, přičemž atorvastatin vykazoval významně delší perzistenci než simvastatin. Autoři sami upozornili na nedostatek použité databáze, a to že neobsahovala důvody ukončení terapie – cena, efektivita, vedlejší účinky apod. [35,36].
Objevují se také diskuze, ale i fakta ohledně možného podílu statinů na zpomalení vývoje Alzheimerovy choroby. Množí se důkazy pro přímé zapojení cholesterolu do produkce beta--amyloidu, na druhé straně jsou známa i konstatování, že hranice mezi vaskulární a Alzheimerovou demencí není, zvláště u starších nemocných, přesná, a tedy že se dyslipidemie mohou podílet na progresi úbytku kognitivních funkcí jako celku s možným příznivým podílem léčby statiny [37].
Poruchy metabolizmu lipidů i celý metabolický syndrom vyskytující se ve středním věku je dnes některými autory zařazován mezi rizikové faktory Alzheimerovy choroby jako nadcházejícího populačního problému a od intervence rizikových faktorů právě ve středním věku je očekáváno zpomalení vývoje a snížení výskytu AD ve stárnoucí populaci [38].
Nežádoucí vedlejší účinky statinů jsou všeobecně známy a u starších nemocných dochází k jejich častějšímu výskytu (dyspepsie, bolesti hlavy, nespavost, závratě, myalgie, parestezie, cholestatický ikterus, rabdomyolýza). Nová, ještě razantnější doporučení ohledně udržování hladin LDL-cholesterolu pod 1,8 mmol/l znamenají nutnost zvyšování dávek, samozřejmě s ještě vyšší pravděpodobností výskytu nežádoucích účinků. Proto je u starších nemocných doporučováno zvažovat doplňkovou terapii, např. snižující střevní absorpci cholesterolu – ezetrolem nebo fytosteroly [39].
Na novou, dosud neprobádanou oblast upozorňuje práce z května roku 2008 osvětlující vliv statinů na nárůst počtu T-lymfocytů s následným možným negativním ovlivněním obranyschopnosti vůči virovým onemocněním a neurodegenerativním onemocněním jako např. amyotrofická laterální skleróza, ale i vůči nádorům [40].
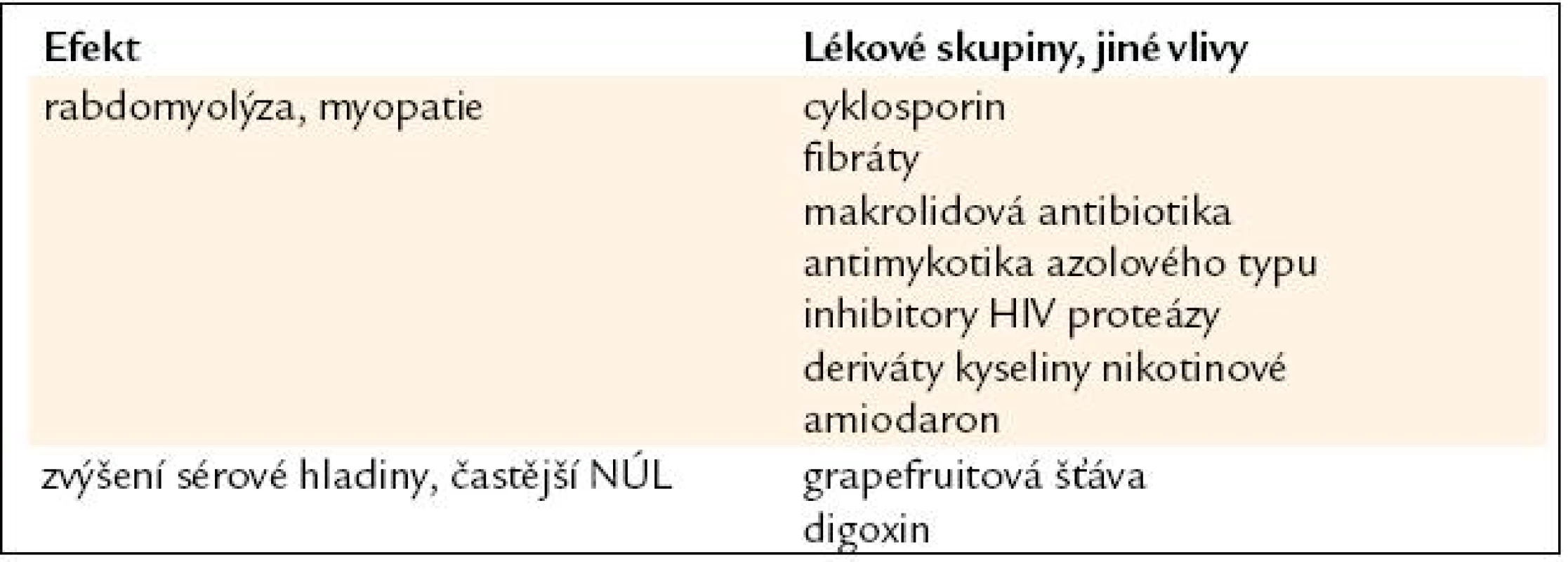
Nejčastější interakce statinů uvádí tab. 6.
Blokátory kalciového kanálu
Relaxace hladké arteriální svaloviny je nejvýraznějším účinkem této lékové skupiny – efektu se využívá při snaze o ovlivnění zejména epikardiální části koronárního řečiště, k terapii hypertenze, ke snížení periferní cévní rezistence při námahové angíně pectoris a při srdečním selhání – to vše při minimálním efektu inotropním a dromotropním.
U starších nemocných se obvykle uchylujeme k přidání těchto látek do kombinační léčby hypertenze, pokud dosavadní kombinací nebylo dosaženo požadovaného efektu, podobně je tomu i u anginy pectoris. Vzhledem k možným prudkým výkyvům krevního tlaku až s vývojem fatálních mozkových ischemií po podání kalciových blokátorů je u starších nemocných striktně doporučeno podávat pouze retardované formy preparátu. Nežádoucí účinek, poměrně častý u dříve podávaných neretardovaných forem – tedy zčervenání v obličeji s pocitem horkosti – je možné občas pozorovat u starších nemocných i po zavedení terapie preparátem retardovaným. U některých nemocných může dojít po zavedení terapie blokátory kalciového kanálu k rozvoji masivních otoků dolních končetin imitujících pravostranné kardiální selhání, ovšem bez doprovodné dušnosti – tento příznak není obvykle řešitelný jinak než vysazením preparátu. Podávání kalciových blokátorů novější generace vyvolává edémy podstatně řidčeji.
U starších nemocných jsou možnosti terapie kalciovými blokátory omezeny jejich relativní kontraindikací u stenotických vad – zvláště aortální stenóza aterosklerotického původu různé závažnosti se podle zkušenosti vyskytuje až u 1/5 nemocných. Dosud nebyly zjištěny známky obdobného působení blokátorů kalciového kanálu na arteriální endotel podobně jako u ACEI [41].
Blokátory kalciového kanálu je možné bezpečně kombinovat se všemi běžně doporučovanými antihypertenzivy a antianginózními preparáty, antibiotiky i perorálními antidiabetiky.
Diuretika
Nejčastěji jsou předepisována diuretika kličková a thiazidová, chlortalidon je v monoterapii pokládán u seniorů za nevhodný, protože může způsobovat hypokalemii a interindividuálně rozdílné, ne vždy předvídatelné ztráty tekutin.
Furosemid může, jako kličkové diuretikum, způsobovat ztráty kalia, kalcia, magnezia a natria – podáván dlouhou dobu (měsíce) bez kontroly sérových hladin minerálů může vést zpočátku ke zvýšené nervosvalové dráždivosti, křečím nebo arytmiím, hypomagnezemie způsobuje častější a těžší záchvaty anginy pectoris, později dochází až k těžkému, život ohrožujícímu minerálnímu rozvratu.
V terapii srdečního selhání je nyní s výhodnými účinky kombinován s ACEI, je však nutno mít na paměti vzájemný potencující vliv na vznik hyponatremie – v současné době nejčastější minerální poruchy u geriatrických nemocných [1].
Thiazidová diuretika jsou indikována častěji při terapii hypertenze, u starších nemocných je však jejich preskripce limitována jejich praktickou neúčinnost při snížené funkci ledvin (pokles GF pod 0,5ml/s), dále by neměla být podávána diabetikům pro riziko zhoršení ledvinných funkci při diabetické nefropatii a pro zhoršení kompenzace diabetu. Podávání thiazidových diuretik vede k retenci kyseliny močové až po riziko vyvolání dnavého záchvatu.
U starších nemocných by optimální podávaná dávka hydrochlorothiazidu měla být 12,5mg a neměla by překročit 25 mg denně – tedy 1 tbl. u nás dostupného Hydrochlorothiazidu, v kombinovaných preparátech (Moduretic, Rhefluin, Loradur mite) je dávka hydrochlorothiazidu dvojnásobná, tedy 50mg. Podávání malých dávek thiazidových diuretik k antihypertenzní terapii je prospěšné z hlediska kompenzace izolované systolické hypertenze a významně neovlivňuje metabolizmus, včetně kompenzace diabetu [42]. Tento postup je doporučován také guidelines ESH/ESC, je však stále nutno mít na paměti dlouhodobou subklinickou dehydrataci většiny starších nemocných, tedy to, že při jakékoli komplikaci zvyšující pravděpodobnost prohloubení dehydratace, jako je horečka, zvracení či průjem, mohou diuretika významným způsobem stav nemocného dále zhoršit.
Obecně je nutno na staršího nemocného léčeného diuretiky pohlížet při jakékoli i nepříliš velké ztrátě tekutin jako na ohroženého akutním vznikem dehydratace se všemi důsledky včetně prerenálního selhání ledvin a mozkové dysfunkce s delirantním stavem.
Z hlediska režimu podávání diuretik je samozřejmě nutné respektovat podání v ranních hodinách, aby se nezvyšoval počet nočních mikcí a nezhoršovala se compliance nemocného. Dalším úskalím v diuretické terapii seniorů je inkontinence – po zavedení diuretické terapie se mohou příznaky inkontinence zhoršit, zvýší se spotřeba příslušných pomůcek a nemocný diuretickou terapii spontánně vynechává, což je obvyklou příčinou četných rehospitalizací nemocných s chronickým srdečním selháním.
Podle aktualizace doporučení pro terapii hypertenze se ustupuje od dříve doporučované kombinace beta-blokátoru a diuretika jako první volby [43].
Digoxin
Jedinou evidence based indikací digoxinu je fibrilace síní s rychlou odpovědí komor, procento starších nemocných užívajících digoxin se tedy snižuje – tab. 1. V současné době již digoxin není mezi prvními 9 nejčastěji užívanými léky mezi seniory.
Nicméně stále je nutné mít na paměti jeho poměrně úzké terapeutické rozmezí i malý distribuční prostor, a tedy možnost snadného předávkování s nutností kontrolovat hladinu digoxinu a hladiny minerálů, zvláště kalia. U některých starších nemocných má digoxin i v terapeutické hladině výrazně bradykardizující efekt až po hodnoty TF pod 40/min či až do vývoje AV blokády vyšších stupňů.
Předávkování digoxinem je jednou z častých příčin vážných dyspeptických obtíží nemocného s nechutenstvím, nauzeou a zvracením, které vedou k další dehydrataci, dalšímu zmenšení distribučního prostoru a k dalšímu zvýšení toxické hladiny obvykle dále poctivě užívaného digoxinu. Z těchto důvodů je doporučováno nepřekračovat u seniorů dávku 125mg za den, a to i při normálních renálních funkcích – viz Beersova kritéria [3].
Závěry pro praxi
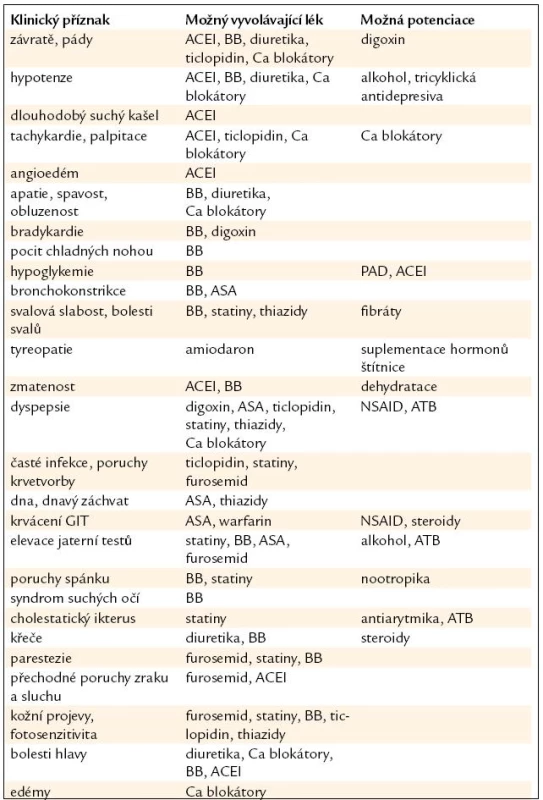
Léčebné ovlivnění kardiovaskulárního postižení se u většiny seniorů přičítá k účinkům mnoha dalších preparátů užívaných pro jiné choroby včetně působení volně dostupných medikamentů. Narůstá riziko snížené compliance a zvýšeného výskytu nežádoucích vedlejších účinků i lékových interakcí (tab. 7).
Dávkování obvyklé u mladší populace je u starších nemocných nutno s ohledem na aktuální eliminační kapacitu individuálně přizpůsobovat.
U seniorské populace je nutno při podávání kardiovaskulární medikace očekávat výskyt i těch nežádoucích vedlejších účinků, které jsou u mladších nemocných spíše výjimečné či s podstatně menšími projevy.
U starších multimorbidních nemocných je třeba mít na paměti nejen interakce podávaných léčiv mezi sebou, ale i možné interakce léčiv a souběžných chorob či interakce léčiva a stravy.
Podávání retardovaných léčiv, prospěšné u seniorů z hlediska možné redukce počtu užívaných tablet, s sebou může nést riziko kumulace léčiva, nebo naopak trvání účinku, které nepokrývá celou předpokládanou dobu účinnosti.
Podpořeno grantem IGA MZ č. NS/10029–4 „Zvýšení kvality preskripce seniorům – validace nástrojů lékové politiky v ČR“.
prof.
MUDr. Hana Kubešová Matějovská, CSc.
www.fnbrno.cz
e-mail: hkubes@med.muni.cz
Sources
1. Kalvach Z, Zadák Z, Jirák R et al. Geriatrie a gerontologie. 1. vyd. Praha: Grada 2004.
2. Topinková E. Geriatrie pro praxi. Praha: Galén 2005.
3. Fialová D, Topinková E, Gambassi G et al. Potentially Inappropriate Medication Use Among Elderly Home Care Patients in Europe. JAMA 2005; 293 : 1348–1358.
4. Kubešová H, Holík J, Šipr K et al. Odraz vědeckých poznatků v preskripci praktického lékaře. Prakt Lék 2000; 80 : 509–513.
5. Kubešová H, Holík J, Weber P et al. Spotřeba léčiv v seniorské populaci a rizika polyfarmakoterapie ve stáří. Čas Lék Čes 2006; 9 : 708–712.
6. Zed PJ, Abu-Laban RJ, Balen RM. Incidence, severity and preventability of medication-related visits to emergency department: a prospective study. CMAJ 2008; 178 : 1563–1569.
7. Beers MH, Ouslander JG, Rollingher Iet al. Explicit criteria for determining inappropriate medication use in nursing home residents. UCLA Division of Geriatric Medicine. Arch Intern Med 1991; 151 : 1825–1832.
8. Beers MH. Explicit criteria for determining potentially inappropriate medication use by the elderly: an update. Arch Intern Med 1997; 157 : 1531–1536.
9. Matějovský J. Komplexní pohled na funkční a zdravotní stav seniorů žijících ve svém vlastním prostředí. Diplomová práce, Lékařská fakulta, Masarykova univerzita 2007.
10. Hemmelgarn BR, Chen G, Walker R et al. Trends in antihypertensive drug prescriptions and physician visits in Canada between 1996 and 2006. Can J Cardiol 2008; 24 : 507–512.
11. Blakley BW, Gulati H. Identifying drugs that cause dizziness. J Otolaryngol 2008; 37 : 11–15.
12. Konopa J, Bullo B, Rutkowski B. Life threatening drug-induced hyperkaliemia – case report. Pol Arch Med Wewm 2006; 115 : 238–242.
13. Pilote L, Abrahamovicz M, Eisenberg M et al. Effect of different angiotensin-converting enzyme inhibitors on mortality among elderly patients with congestive heart failure. CMAJ 2008; 178 : 1303–1311.
14. Masunari N, Fujiwara S, Nakata Y et al. Effect of angiotensin converting enzyme inhibitor and benzodiazepine intake on bone loss in older Japanese. Hiroshima J Med Sci 2008; 57 : 17–25.
15. Flammer AJ, Sudano I, Hermann F et al. Angiotensin converting enzyme inhibition improves vascular function in rheumatoid artritis. Circulation 2008; 117 : 2262–2269.
16. Werner C, Baumhäkel M, Teo KK et al. RAS blockade with ARB and ACE inhibitors: current perspective on rationale and patients selection. Clin Res Cardiol 2008; 97 : 481–431.
17. Doporučení České kardiologické společnosti pro diagnostiku a léčbu srdečního selhání ČKS 2006. Cor et Vasa 2007; 49: K5–K34.
18. Kahn R, Robertson RM, Smith R et al. The impact of prevention on reducing the burden of cardiovasculat disease. Circulation 2008; 118 : 576–585.
19. Vekasi J, Koltai K, Gaal V et al. The effect of aspirin on hemoreological parameters of patients with diabetic retinopathy. Clin Hemorheol Microcirc 2008; 39 : 385–389.
20. Juby AG, Davis P. Utility of published guidelines on the use of nonsteroidal anti-inflammatory drugs in the elderly. Clin Rheumatol 2008; 27 : 1191–1194.
21. Arvanitakis Z, Grodstein F, Bienias JL et al. Relation of NSAIDs to incident AD, change in cognitive function, and AD patology. Neurology 2008; 70 : 2219–2225.
22. Szekely CA, Green RC, Breitner JC et al. No advantage of A beta 42-lowering NSAIDs for prevention of Alzheimer dementia in six pooled cohort studies. Neurology 2008; 70 : 2291–2298.
23. Vojáček J. Výsledky stuide RE-LY slibují účinnější, bezpečnější a jednodušší prevenci embolických komplikací u nemocných s nevalvulární fibrilací síní. Vnitř Lék 2009; 55 : 1085–1088.
24. Gallagher AM, Rietbrock S, Plomb J et al. Initiation and persistence of warfarin or aspirin in patients with chronic atrial fibrillation in general practice: do the appropriate patients receive stroke prophylaxis? J Throm Haemost 2008; 6 : 1500–1506.
25. European Heart Rhythm Association; European Association for Cardio-Thoracic Surgery, Camm AJ, Kirchhof P, Lip GY et al. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010; 31 : 2369–2429.
26. Onalan O, Cumurcu BE, Bekar L et al. Complete atrioventricular block associated with concomitant use of metoprolol and paroxetine. Mayo Clin Proc 2008; 83 : 595–599.
27. Aströlm-Lilja C, Odeberg JM, Ekman E et al. Drug-induces torsades de pointes: a review of the Swedish pharmacovigilance database. Pharmacoepidemiol Drug Saf 2008; 17 : 587–592.
28. Galinier M, Emeriau JP. Prescribing beta blockers in elderly patients with heart failure. Presse Med 2008; 37 : 1047–1054.
29. Cleland JG, Coletta AP, Torabi A et al. Clinical trials update from the European Society of Cardiology heart failure meeting 2009: CHANCE, B-Convinced, CHAT, CIBIS-ELD and Signal HF. Eur J Heart Fail 2009; 11 : 802–805.
30. Rector TS, Anand IS, Nelson DB et al. Carvedilol versus controlled-release metoprolol for elderly veterans with heart failure. J Am Geriatr Soc 2008; 56 : 1021–1027.
31. Kubešová H, Weber P, Kala P et al. Akutní koronární syndrom u seniorů. Čes Ger Rev 2008; 6 : 41–46.
32. Zgažarová S, Jedličková H, Vašků V. Nežádoucí účinky amiodaronu na kůži. Vnitř Lék 2009; 55 : 976–980.
33. Manderbacka K, Keskimäki I, Reunanen A et al. Equity in the use of antithrombotic drugs, beta-blockers and statins among Finnish coronary patients. Int J Equity Health 2008; 7 : 16–20.
34. Pretnar-Oblak J, Sebestjen M, Sabovic M. Statin treatment improves cerebral more than systemic endothelial dysfunction in patients with arterial hypertension. Am J Hypertens 2008; 21 : 674–678.
35. Foody JM, Joyce AT, Rudolph AE et al. Persistence of atorvastatin and simvastatin among patients with and without prior cardiovascular diseases: a US managed care study. Curr Med Res Opin 2008; 24 : 1987–2000.
36. Pella D. Statínová myopatia – rarita, alebo realita? Vnitř Lék 2010; 9 : 972–976.
37. Pregelj P. Involvement of cholesterol in the pathogenesis of Alzheimer’s disease: Role of statins. Psychiatr Danub 2008; 20 : 162–167.
38. Duron E, Hanon O. Vascular risk factors, cognitive decline and dementia. Vasc Health Risk Manag 2008; 4 : 363–381.
39. Kevelaitiene S, Slapikas R. A new approach to the treatment of dyslipidemia. Medicina (Kaunas) 2008; 44 : 407–413.
40. Goldstein MR, Mascitelli L, Pezzeta F. The double-edged sword of statin immunomodulation. Int J Cardiol 2008; 5 : 432–436.
41. Hirooka Y, Kimura Y, Sagara Y et al. Effects of valsartan or amlodipine on endothelial function and oxidative stress after one year follow-up in patients with essential hypertension. Clin Exp Hypertens 2008; 30 : 267–276.
42. Kudoh T, Nagawaga T, Nawaga I. Additional small amounts of diuretics improve blood pressure control at low cost without disadvantages in blood sugar metabolism. Hypertens Res 2008; 31 : 455–462.
43. Špinar J, Souček M. Přehodnocení doporučení pro diagnostiku a léčbu hypertenze. Vnitř Lék 2010; 56 : 157–161.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2011 Issue 6
-
All articles in this issue
- Vplyv dlhodobej glykemickej kompenzácie na zmeny v lipidovom profile detí a adolescentov s diabetes mellitus 1. typu
- Účinnost a bezpečnost podávání moxonidinu u pacientů s metabolickým syndromem (klinické hodnocení O.B.E.Z.I.T.A.)
- Dlouhodobé výsledky katetrizační ablační léčby u supraventrikulárních tachyarytmií
- Brugada syndrom
- Senioři a kardiovaskulární medikace
- Infekční endokarditida – klíčová včasná diagnóza
- Úspěšná léčba Erdheimovy-Chesterovy nemoci chemoterapií obsahující 2-chlorodeoxyadenozin. Popis dvou případů a přehled literatury
- Primární jaterní karcinoid
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Brugada syndrom
- Primární jaterní karcinoid
- Senioři a kardiovaskulární medikace
- Dlouhodobé výsledky katetrizační ablační léčby u supraventrikulárních tachyarytmií
