Diagnostika sekundární hypertenze v ambulantní praxi
Diagnostic of secondary hypertension in clinical practice
Arterial hypertension is a common worldwide disease with a prevalence of approximately 26%. Secondary cause is known in 5–10% of patients with hypertension. We should think of secondary hypertension in all patients with resistant hypertension, in patients with sudden deterioration in the control of hypertension and in patients with laboratory and clinical signs of diseases associated with secondary hypertension. It is important to distinguish between secondary hypertension and pseudo-resistance (noncompliance to treatment, white coat syndrome). Secondary causes of hypertension can be divided into endocrine (primary aldosteronism, pheochromocytoma, hypercortisolism, hyperparathyreoidism), renal – renovascular and renal parenchymal hypertension, and other causes as sleep apnoe syndrome, hypertension in pregnancy, coarctation of the aorta and intracranial tumors.
Key words:
secondary hypertension – primary aldosteronism – renovascular and renal parenchymal hypertension – pheochromocytoma – hypercortisolism – sleep apnoe syndrome – hypertension in pregnancy – coarctation of the aorta
Authors:
Z. Šomlóová; J. Rosa; O. Petrák; B. Štrauch; T. Zelinka; R. Holaj; J. Widimský jr.
Authors‘ workplace:
III. interní klinika 1. lékařské fakulty UK a VFN Praha, přednosta prof. MUDr. Štěpán Svačina, DrSc., MBA
Published in:
Vnitř Lék 2011; 57(9): 772-776
Category:
65th birthday Mudr. Jany Laciné and and 60th birthday Milana Tržila
Overview
Arteriální hypertenze je celosvětově časté onemocnění s prevalencí kolem 26 %. Z toho u 5–10 % pacientů můžeme prokázat sekundární příčinu hypertenze. Na sekundární hypertenzi bychom měli pomýšlet u všech pacientů s rezistentní hypertenzí, u pacientů s náhlým zhoršením kontroly hypertenze a u pacientů s laboratorními nebo klinickými příznaky chorob spojených se sekundární hypertenzí. Od sekundární hypertenze je nutné odlišit stavy tzv. pseudorezistence (non-compliance k léčbě, syndrom bílého pláště). Mezi sekundární příčiny hypertenze patří endokrinní příčiny (primární hyperaldosteronizmus, feochromocytom, hyperkortizolizmus, hyperparatyreóza), renální – renoparenchymatózní a renovaskulární hypertenze, dále syndrom spánkové apnoe, hypertenze v těhotenství, koarktace aorty a intrakraniální tumory.
Klíčová slova:
sekundární hypertenze – primární hyperaldosteronizmus – renovaskulární a renoparenchymatózní hypertenze – feochromocytom – hyperkortizolizmus – syndrom spánkové apnoe – hypertenze v těhotenství – koarktace aorty
Úvod
Arteriální hypertenze je časté a komplexní onemocnění s celosvětově významnou mortalitou a morbiditou. Prevalence v celosvětové populaci je asi 26 % [1]. Přibližně u 5–10 % pacientů se jedná o sekundární hypertenzi, kdy je identifikovatelná konkrétní, potenciálně odstranitelná vyvolávající příčina. Na sekundární hypertenzi bychom měli pomýšlet u všech pacientů s rezistentní hypertenzí, kdy i přes 3kombinaci antihypertenziv různých tříd, z nichž jedno by mělo být diuretikum, nedochází k poklesu TK pod 140/90 mm Hg, u pacientů s náhlým zhoršením kontroly hypertenze a u pacientů s laboratorními nebo klinickými příznaky chorob spojených se sekundární hypertenzí [2,3]. Od tzv. „true resistant“ hypertenze je nutné odlišit stavy tzv. pseudorezistence, kam patří non-compliance k léčbě (možnost potvrzení pomocí kvantitativního stanovení antihypertenziv v krvi) a syndrom bílého pláště (vysoký TK v ordinaci v kontrastu s normálním nebo mnohem nižším TK v domácím prostředí), který se vyskytuje asi ve 20–30 % pacientů s tzv. rezistentní hypertenzí [4,5]. Dále je důležitá i informace o přísunu soli v dietě, abúzu alkoholu, drog, přítomnost chronické bolesti a užívání určitých léků, které mohou zvyšovat TK (nesteroidní analgetika, steroidy, hormonální antikoncepce, hormonální substituční terapie, sympatomimetika, psychostimulancia, cyklosporin, erytropoetin). K vyšetření eventuální sekundární hypertenze bychom měli přistoupit až po vyloučení pseudorezistence nebo po potvrzení těžší formy hypertenze za pomoci 24hodinového ambulantního monitorování TK.
Sekundární příčiny hypertenze můžeme rozdělit na časté, jako je primární hyperaldosteronizmus, renoparenchymatózní a renovaskulární hypertenze, syndrom spánkové apnoe [6], léky indukovaná hypertenze či hypertenze v těhotenství, a na méně časté jako feochromocytom, hyperkortizolizmus, hyperparatyreóza, koarktace aorty, intrakraniální tumory [6].
Primární hyperaldosteronizmus
Patří mezi nejčastější formy sekundární hypertenze, je vyvolán autonomní nadprodukcí aldosteronu z kůry nadledvin. Jeho prevalence je v neselektované populaci hypertoniků kolem 5–13 % [7], zatímco u pacientů s rezistentní hypertenzí až 20 % [8].
Pacienti s primárním hyperaldosteronizmem mají vyšší výskyt CMP, fibrilace síní, IM [9], mikroalbuminurie [10], hypertrofie levé komory [11] a metabolického syndromu [12], dále mají i vyšší tuhost cévní stěny [13] a významnější změny karotického řečiště [14] než pacienti s esenciální hypertenzí.
K nejčastějším formám primárního hyperaldosteronizmu patří idiopatický hyperaldosteronizmus na podkladě bilaterální hyperplazie nadledvin (60 %) a aldosteron produkující adenom (35 %), méně časté formy jsou unilaterální hyperplazie (2 %), familiární hyperaldosteronizmus I. a II. typu nebo karcinom kůry nadledvin [7].
Primární hyperaldosteronizmus je nejčastěji diagnostikován u osob mezi 30. a 60. rokem života [7]. Arteriální hypertenze se vyskytuje ve 100 % případů primárního hyperaldosteronizmu a nejčastěji je středně těžká až těžká nebo rezistentní [15]. Hypokalemie a příznaky s ní spojené (svalová slabost a křeče, bolesti hlavy, palpitace, polydipsie, polyurie, metabolická alkalóza, hypernatremie) se vyskytují jen v 50–60 % případů, většinou u těžších forem [7,16]. Hypokalemie se však může někdy projevit až při terapii diuretiky [7].
Základem diagnózy primárního hyperaldosteronizmu je zvýšený poměr plazmatického aldosteronu (ng/dl)//plazmatické reninové aktivity (ng//ml/hod) nad 30 (ng/dl/ng/ml/hod), avšak hodnota plazmatického aldosteronu by měla být alespoň na horní hranici normy (15 ng/dl). K definitivnímu potvrzení diagnózy pak slouží supresní testy, u nás nejčastěji test s náloží fyziologického roztoku (2 l za 4 hod), kde nedostatečná suprese plazmatického aldosteronu (nad 7,5 ng/dl) potvrzuje diagnózu primárního hyperaldosteronizmu. K správné diagnóze primárního hyperaldosteronizmu je nutná změna chronické antihypertenzní terapie. Z medikace je nutné vysadit léky ovlivňující systém RAAS nejméně 14 dní před vyšetřením, spironolakton 6 týdnů, a do terapie přechodně zavést kombinaci α1-blokátoru a blokátoru kalciového kanálu – verapamilu, které neovlivňují stanovení hladin aldosteronu a reninu. Dále je vhodné vysadit hormonální antikoncepci a hormonální substituční terapii, jež mohou také ovlivňovat stanovení [17].
Po laboratorním potvrzení primárního hyperaldosteronizmu přistupujeme k morfologickému vyšetřování pomocí CT nebo MR, a to i u pacientů, kteří si nepřejí operační řešení, neboť může být vzácně příčinou nadprodukce aldosteronu i karcinom kůry nadledvin. U pacientů, kteří souhlasí s operací, pak k definitivnímu stanovení podtypu provádíme separované odběry z nadledvinových žil, kde posuzujeme stranovou nadprodukci aldosteronu (výjimečně u mladých lidí s jednoznačným CT nálezem můžeme přistoupit přímo k operaci). V případě potvrzené jednostranné nadprodukce je léčba chirurgická. Po adrenalektomii dochází k poklesu krevního tlaku prakticky u všech pacientů a normotenze přetrvává přibližně ve 30–72 % případů [18,19]. Rozhodující je věk pacienta, délka trvání hypertenze, menší počet antihypertenziv, stav renálních funkcí a pozitivní odpověď na léčbu spironolaktonem [2]. V ostatních případech přistupujeme k farmakologické léčbě blokátorem mineralokortikoidního receptoru – spironolaktonem. Dávka je individuální kolem 50–100 mg denně, plný účinek se dostaví za 4–6 týdnů, ale často jsme limitováni nežádoucími účinky spironolaktonu. I přes snížení TK je většinou nutné spironolakton kombinovat s jinými antihypertenzivy, nejlépe thiazidovými diuretiky a blokátory kalciových kanálů. V případě nežádoucích účinků je možná terapie selektivním antagonistou mineralokortikoidních receptorů eplerenonem. Terapii spironolaktonem je možné použít i jako terapeutický test – v případě dobré odpovědi na léčbu je diagnóza primárního hyperaldosteronizmu pravděpodobnější.
Renoparenchymatózní hypertenze
Prevalence renální hypertenze je asi 5–6 % [20]. Renoparenchymatózní hypertenze se vyskytuje u různých onemocnění ledvinného parenchymu (primární glomerulonefritidy, diabetická nefropatie, vaskulitidy, chronické tubulointersticiální nefritidy, polycystické ledviny, jednostranná malá ledvina, vrozené abnormality – jednostranná ageneze, ektopická ledvina, hydronefróza). Její závažnost závisí na věku nemocného, tělesné hmotnosti, typu a trvání ledvinného onemocnění a rozsahu poruchy renálních funkcí [20,21]. Důvodem horší kontroly hypertenze u těchto pacientů je především zvýšená retence sodíku a tekutin vedoucí k expanzi intravaskulárního volumu [6]. Cílové hodnoty TK jsou u těchto pacientů pod 130/80 mm Hg. Léčbu zahajujeme inhibitorem ACE nebo AT1-blokátory nebo jejich kombinací, dále přidáváme diuretika (při poklesu glomerulární filtrace pod 60 ml/min/1,73m2 nebo pod 1,3 ml/s//1,73m2 jsou thiazidová diuretika často neúčinná, a proto je nutné použít kličkové diuretika), při nedostatečném účinku a absenci převodnění kombinujeme s dlouhodobě působícím blokátorem kalciových kanálů, v případě nadále nedostatečné kompenzace TK přidáváme beta-blokátor nebo centrálně působící antihypertenzivum. U rezistentních pacientů je možné přidat do terapie i blokátory periferních α-receptorů [3,20].
Renovaskulární hypertenze
Příčinou je hemodynamicky významné zúžení renální tepny. Vyskytuje se asi u 2–5 % hypertoniků [20]. Za významnou se považuje víc než 60% redukce průsvitu tepny s předpokladem vzniku tlakového gradientu víc než 15–20 mm Hg [22]. Nález stenózy renální tepny je však docela častým nálezem u hypertoniků podstupujících koronarografii, víc než 20 % pacientů má unilaterální nebo bilaterální stenózu větší než 70 % [23]. Ukazuje se, že nález stenózy ještě nemusí ukazovat na příčinu hypertenze, randomizované studie – aktivní vs konzervativní přístup – zatím neprokázaly zlepšení hodnot TK nebo renálních funkcí ve prospěch aktivního přístupu [6]. Nejčastější příčinou je ve více než 90 % případů ateroskleróza, vyskytuje se častěji u starších pacientů, kuřáků, u pacientů se známou aterosklerózou, např. ICHDK. Na stenózu renální tepny bychom měli myslet u pacientů s nevysvětlenou renální insuficiencí, u pacientů s náhlým nebo opakujícím se plicním edémem při dobré systolické funkci [6] a u pacientů s nálezem sekundárního hyperaldosteronizmu (vyšší poměr aldosteron/renin při vysokých hodnotách reninu i aldosteronu). Zbylých 10 % tvoří fibromuskulární dysplazie vyskytující se častěji u žen pod 50 let [6]. V diagnostice stenózy renálních tepen využíváme CT/MR angiografii, u hubených jedinců lze použít i duplexní sonografii renálních tepen, avšak za zlatý standard je považována angiografie renálních tepen s možností intervence. Profit z léčby budou mít mladí pacienti nebo pacienti s bilaterální stenózou renálních tepen a recidivujícími plicními edémy, jinak je rozhodnutí o konzervativní nebo invazivní terapii zcela individuální [2]. Ve farmakologické terapii volíme ACE inhibitory nebo AT1-blokátory, které jsou však v případě bilaterální stenózy kontraindikované, v kombinaci s jinými antihypertenzivy a nezapomínáme na intervenci rizikových faktorů aterosklerózy [24].
Syndrom spánkové apnoe
Syndrom spánkové apnoe je charakterizován opakovaným přerušením dýchání během spánku způsobeným kolapsem horních cest dýchacích. Je častý u pacientů s rezistentní hypertenzí a vyskytuje se víc u mužů než u žen. Intermitentní hypoxie a vyšší rezistence horních cest dýchacích indukují zvýšenou sympatickou aktivitu, ta vede ke zvýšení krevního tlaku, a to zvýšením srdečního výdeje a periferní rezistence a také zvýšenou retencí tekutin [6]. Na diagnózu bychom měli pomýšlet u lidí s dokumentovanými apnoickými pauzami, rušivým chrápáním, obézních a u lidí s výraznou denní únavností nebo usínáním [25]. Diagnostikuje se ve spánkové laboratoři pomocí polysomnografie (simultánní měření EEG, EMG, elektrookulogramu, respirace – průtok a úsilí, saturace O2 a chrápání). Diagnóza je potvrzena, když je index apnoe-hypopnoe větší než 5 (počet apnoických pauz a hypopnoí za hodinu spánku) a pacient trpí nadměrným denním spánkem nebo jsou přítomny alespoň 2 z následujících symptomů: dusivé nebo lapavé dechy ve spánku, opakované probouzení se ze spánku, neosvěžující spánek, denní únava, porucha koncentrace (a dané poruchy nelze vysvětlit jinými příčinami) [25]. Proto bychom neměli zapomínat na anamnézu kvality spánku u pacientů s rezistentní hypertenzí, obézních a u pacientů s vyššími hodnotami TK v nočních hodinách. V terapii se uplatňuje úprava životního stylu – redukce hmotnosti, chirurgická korekce v oblasti měkkého patra a dýchání kontinuálním přetlakem – CPAP.
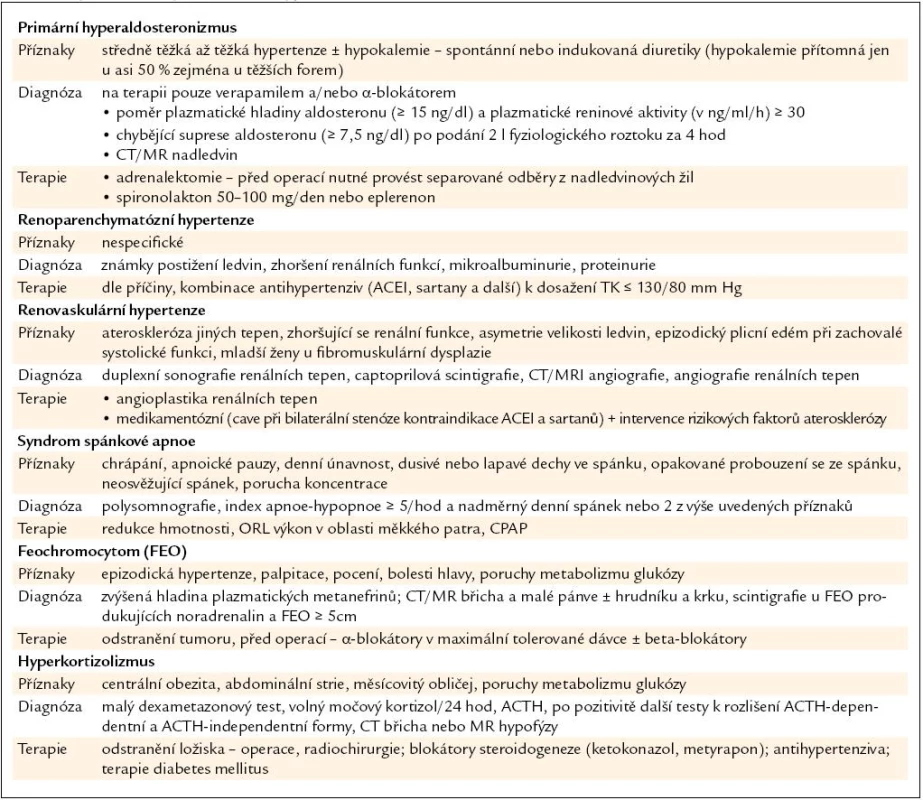
Feochromocytom
Feochromocytom a funkční paragangliom jsou vzácné nádory vycházející z chromafinních buněk sympatického nervového systému (nadledviny – feochromocytom, sympatické ganglia – paragangliom) produkující katecholaminy, nejčastěji noradrenalin. Příznaky onemocnění jsou různorodé a vycházejí s nadprodukce katecholaminů. Arteriální hypertenze se vyskytuje asi u 95 % pacientů, ale jen u 50 % je trvalá, nejčastěji se vyskytuje v kombinaci s bolestmi hlavy, palpitacemi či zvýšeným pocením a příznaky se objevují většinou epizodicky. K vyšetřením s nejvyšší senzitivitou a specificitou patří stanovení hladin plazmatických metanefrinů [6]. Po stanovení diagnózy se přistupuje k morfologickému vyšetření pomocí CT, MR a v případě noradrenergní nadprodukce nebo většího tumoru je vhodné doplnit i scintigrafické vyšetření k vyloučení mnohočetného metastatického postižení. Terapie spočívá v chirurgické léčbě po předchozí přípravě α1-blokátory v postupně se zvyšující dávce do maximálně tolerované nejméně 10–14 dní před operací. Beta-blokátory přidáváme pouze při tachykardii. I po úspěšné operaci je nutné dlouhodobé sledování pacientů pro možnost recidivy tumoru [2].
Cushingův syndrom – hyperkortizolizmus
Je způsoben zvýšenými hladinami kortizolu, a to buď endogenní nadprodukcí, nebo zvýšením přívodu kortizolu – iatrogenní hyperkortizolizmus. Hyperkortizolizmus rozdělujeme na ACTH-dependentní (adenom hypofýzy, nadprodukce CRH nebo ektopická nadprodukce ACTH z jiných tumorů) a na ACTH-independentní (adenom nebo karcinom nadledvin, hyperplazie nadledvin) [2]. Hypertenze je přítomna u 70–90 % pacientů [6]. Je způsobena zvýšenými koncentracemi kortizolu v plazmě, které vedou k retenci Na+ a zvýšené citlivosti cévní stěny na další vazopresorické působky [16]. K základním screeningovým vyšetřením patří především stanovení ranního kortizolu po večerním podání 1 mg dexametazonu ve 23 hod (plazmatický kortizol pod 50 nmol/l prakticky vylučuje hyperkortizolizmus) a stanovení volného močového kortizolu za 24 hod, případně stanovení diurnálního rytmu kortizolu. Vhodnější je provést více testů najednou a při nejasném výsledku testy zopakovat vzhledem k možnému intermitentnímu zvýšení kortizolu. Po potvrzení hyperkortizolizmu přistupujeme k další diagnostice pomocí stanovení hladiny ACTH (nízká hodnota ukazuje na ACTH-independentní, vysoká hodnota na ACTH-dependentní hyperkortizolizmus), doplňujeme zobrazovací metody a k bližší specifikaci můžeme doplnit velký dexametazonový test, kortikoliberinový test, dezmopresinový test nebo katetrizaci petrózních splavů. Terapie je chirurgická, farmakoterapie je vyhrazena jen pro inoperabilní adenomy/karcinomy [2,16].
Léky indukovaná hypertenze
Existuje velké množství léků a různých látek s vazopresorickým účinkem, které při dlouhodobém užívání mohou vyvolat vznik hypertenze. U těchto léků je proto vhodné pravidelné monitorování hodnot TK. Při opatrném dávkování a pravidelných kontrolách TK je riziko vzniku trvalé hypertenze minimální [2]. Mezi látky nejčastěji zvyšující krevní tlak patří:
- sympatomimetika (kofein, kokain, efedrin, metylendioxymetamfetamin – extáze, nikotin),
- glukokortikoidy, mineralokortikoidy,
- nesteroidní antirevmatika,
- cyklosporin, tacrolimus,
- erytropoetin,
- hormonální antikoncepce, hormonální substituční terapie,
- interakce s MAO inhibitory – potraviny s vyšším obsahem tyraminu,
- ergotamin,
- agonisté dopaminových receptorů – bromocriptin,
- tricyklická antidepresiva,
- alkohol,
- analoga oktreotidu [16].
Hypertenze v těhotenství
V těhotenství je důležité rozlišit, zda hypertenze předchází těhotenství (tzv. preexistující hypertenze), nebo zda se jedná o stav specifický pro těhotenství (tzv. gestační hypertenze). Preexistující hypertenze je diagnostikována buď skutečně před těhotenstvím, nebo do 20. týdne těhotenství. Zatímco gestační hypertenze vzniká v průběhu těhotenství, nejčastěji po 20. týdnu, a ve většině případů vymizí do 42 dnů po porodu. Nefarmakologickou léčbu hypertenze – omezení aktivit, klid na lůžku – zvažujeme u těhotných žen se systolickým TK (sTK) 140–150 mm Hg nebo diastolickým TK (dTK) 90–99 mm Hg. Antihypertenzní léčbu před 28. týdnem těhotenství zahajujeme při hodnotách sTK ≥ 140 mm Hg nebo dTK ≥ 90 mm Hg u žen s gestační hypertenzí bez proteinurie nebo s preexistující hypertenzí. Při stejných prahových hodnotách zahajujeme terapii kdykoli v průběhu těhotenství u žen s gestační hypertenzí a proteinurií nebo při výskytu symptomů preeklampsie, u preexistující hypertenze za přítomnosti doprovodných onemocnění nebo při orgánovém postižení a u preexistující hypertenze s „naroubovanou“ gestační hypertenzí. V ostatních případech se doporučuje zahajovat medikamentózní léčbu hypertenze při hodnotách sTK ≥ 150 mm Hg nebo dTK ≥ 95 mm Hg. Pokud se nejedná o závažnou hypertenzi, za léky volby považujeme metyldopu, labetalol a blokátory kalciových kanálů. Inhibitory ACE a AT1-blokátory jsou v těhotenství kontraindikovány [2].
Koarktace aorty
Jedná se o vrozenou stenózu aorty nejčastěji za odstupem levé podklíčkové tepny. Typickým projevem je hypertenze na horních končetinách s oslabenými či vymizelými pulzacemi na dolních končetinách, šelest mezi lopatkami, EKG známky hypertrofie levé komory. K diagnostice nám pomůže ECHO, kde je nález tlakových gradientů v oblasti descendentní aorty a CT nebo MR angiografie. Léčba je buď chirurgická, nebo pomocí angioplastiky [2].
MUDr. Zuzana Šomlóová
www.vfn.cz
e-mail: zsomloova@seznam.cz
Doručeno do redakce: 19. 4. 2011
Sources
1. Kearney PM, Whelton M, Reynolds K et al. Global burden of hypertension: analysis of worldwide data. Lancet 2005; 365 : 217–223.
2. Widimský J. Hypertenze. 3. vyd. Praha: Triton 2008.
3. Mancia G, De Backer G, Dominiczak A et al. ESH-ESC Task Force on the Management of Arterial Hypertension. 2007 ESH-ESC Practice Guidelines for the Management of Arterial Hypertension: ESH-ESC Task Force on the Management of Arterial Hypertension. J Hypertens 2007; 25 : 1751–1762.
4. Brown MA, Buddle ML, Martin A. Is resistant hypertension really resistant? Am J Hypertens 2001; 14 : 1263–1269.
5. Hermida RC, Ayala DE, Calvo C et al. Effects of time of day of treatment on ambulatory blood pressure pattern of patients with resistant hypertension. Hypertension 2005; 46 : 1053–1059.
6. Calhoun DA, Jones D, Textor S et al. American Heart Association Professional Education Committee. Resistant hypertension: diagnosis, evaluation, and treatment: a scientific statement from the American Heart Association Professional Education Committee of the Council for High Blood Pressure Research. Circulation 2008; 117: e510–e526.
7. Young WF. Primary aldosteronism: renaissance of a syndrome. Clin Endocrinol (Oxf) 2007; 66 : 607–618.
8. Štrauch B, Zelinka T, Hampf M et al. Prevalence of primary hyperaldosteronism in moderate to severe hypertension in the Central Europe region. J Hum Hypertens 2003; 17 : 349–352.
9. Milliez P, Girerd X, Plouin PF et al. Evidence for an increased rate of cardiovascular events in patients with primary aldosteronism. J Am Coll Cardiol 2005; 45 : 1243–1248.
10. Rossi GP, Bernini G, Desideri G et al. PAPY Study Participants. Renal damage in primary aldosteronism: results of the PAPY Study. Hypertension 2006; 48 : 232–238.
11. Tanabe A, Naruse M, Naruse K et al. Left ventricular hypertrophy is more prominent in patients with primary aldosteronism than in patients with other types of secondary hypertension. Hypertens Res 1997; 20 : 85–90.
12. Fallo F, Veglio F, Bertello C et al. Prevalence and Characteristics of the Metabolic Syndrome in Primary Aldosteronism. J Clin Endocrinol Metab 2006; 91 : 454–459.
13. Strauch B, Petrák O, Wichterle D et al. Increased arterial wall stiffness in primary aldosteronism in comparison with essential hypertension. Am J Hypertens 2006; 19 : 909–914.
14. Holaj R, Zelinka T, Wichterle D et al. Increased intima-media thickness of the common carotid artery in primary aldosteronism in comparison with essential hypertension. J Hypertens 2007; 25 : 1451–1457.
15. Young WF Jr, Klee GG. Primary aldosteronism. Diagnostic evaluation. Endocrinol Metab Clin North Am 1988; 17 : 367–395.
16. Widimský J jr. Sekundární hypertenze. 1. vyd. Praha: Triton 2003.
17. Funder JW, Carey RM, Fardella C et al. Endocrine Society. Case detection, diagnosis, and treatment of patients with primary aldosteronism: an endocrine society clinical practice guideline. J Clin Endocrinol Metab 2008; 93 : 3266–3281.
18. Celen O, O’Brien MJ, Melby JC et al. Factors influencing outcome of surgery for primary aldosteronism. Arch Surg 1996; 131 : 646–650.
19. Lumachi F, Ermani M, Basso SM et al. Long-term results of adrenalectomy in patients with aldosterone-producing adenomas: multivariate analysis of factors affecting unresolved hypertension and review of the literature. Am Surg 2005; 71 : 864–869.
20. Monhart V. Hypertenze a ledviny. Praha: Triton 2004.
21. Buckalew VM Jr, Berg RL, Wang SR et al. Prevalence of hypertension in 1,795 subjects with chronic renal disease: the modification of diet in renal disease study baseline cohort. Modification of Diet in Renal Disease Study Group. Am J Kidney Dis 1996; 28 : 811–821.
22. Conlon PJ, O’Riordan E, Kalra PA. New insights into the epidemiologic and clinical manifestations of atherosclerotic renovascular disease. Am J Kidney Dis 2000; 35 : 573–587.
23. Aqel RA, Zoghbi GJ, Baldwin SA et al. Prevalence of renal artery stenosis in high-risk veterans referred to cardiac catheterization. J Hypertens 2003; 21 : 1157–1162.
24. Hackam DG, Spence JD, Garg AX et al. Role of renin-angiotensin system blockade in atherosclerotic renal artery stenosis and renovascular hypertension. Hypertension 2007; 50 : 998–1003.
25. Somers VK, White DP, Amin R et al. American Heart Association Council for High Blood Pressure Research Professional Education Committee, Council on Clinical Cardiology; American Heart Association Stroke Council; American Heart Association Council on Cardiovascular Nursing; American College of Cardiology Foundation. Sleep Apnea and Cardiovascular Disease: An American Heart Association//American College of Cardiology Foundation Scientific Statement From the American Heart Association Council for High Blood Pressure Research Professional Education Committee, Council on Clinical Cardiology, Stroke Council, and Council on Cardiovascular Nursing In Collaboration With the National Heart, Lung, and Blood Institute National Center on Sleep Disorders Research (National Institutes of Health). Circulation 2008; 118 : 1080–1111.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2011 Issue 9
-
All articles in this issue
- Předoperační vyšetření u nemocných před nekardiálním chirurgickým výkonem
- Současný pohled na léčbu hypertenze v těhotenství
- Nová antitrombotika v prevenci žilní tromboembolie a nové protidestičkové léky
- Cílená biologická léčba solidních nádorů
- Proteinurie v ambulantní praxi
- Význam antihypertenzní léčby u subklinického poškození mozku
- Polypragmazie a lékové interakce
- Existuje vztah mezi léčbou diabetu a vznikem nádorů?
- Kombinovaný trénink u mužů s metabolickým syndromem po akutní koronární příhodě
- Diagnostika sekundární hypertenze v ambulantní praxi
- FARIM – FARmakoterapie po Infarktu Myokardu
- Tyreopatie v ambulantní praxi
- Česká angiologie a její proměny
- Dráždivý tračník
- Biologická léčba v dermatologii – psoriáza
- Prokinetika – jejich přínos v klinické praxi gastroenterologické
- Nemoci jater v interní ambulanci
- Arytmologie dnes: rizika antiarytmické terapie v interní ambulanci
- Terapie stabilní chronické obstrukční plicní nemoci (CHOPN) a její případná kardiovaskulární rizika (základní přehled)
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Proteinurie v ambulantní praxi
- Prokinetika – jejich přínos v klinické praxi gastroenterologické
- Polypragmazie a lékové interakce
- Tyreopatie v ambulantní praxi
