Povrchová tromboflebitida, neprávem podceňovaná choroba – je čas změnit názor?
Superficial thrombophlebitis, unjustly underestimated disease – has the time come to change our view?
Superficial thrombophlebites represent a very heterogeneous group of diseases which is caused by the difference between two basic forms of ST – varicophlebitis and thrombophlebitis of a “healthy” vein, as well as by other factors – the ratio of thrombotic and inflammatory process, the location and extent of thrombosis in superficial venous system, the distance from deep venous system, the stage of venous insufficiency and the general thrombotic risk of a patient. ST shares many common features with deep vein thrombosis (clinical risk factors, thrombophilic disorders), both diseases often coincide or follow one another. Some authors suggest considering ST as a part of venous thromboembolism in a broader sense. There are ensuing unresolved questions regarding ST management. So far, no evidence-based treatment has been clearly defined. Anticoagulation is recommended in more serious cases but no consensus about dosing and duration has been reached. The CALISTO trial confirmed a benefit of fondaparinux in prophylactic dose in the therapy of isolated ST and the results have been reflected in recent guidelines of expert groups. Further studies to improve our knowledge of ST and to earn more evidence about its management are definitely needed.
Key words:
superficial thrombophlebitis – deep vein thrombosis – thrombophilic disorders – anticoagulation therapy
Authors:
J. Hirmerová
Authors‘ workplace:
II. interní klinika Lékařské fakulty UK a FN Plzeň, přednosta prof. MUDr. Jan Filipovský, CSc.
Published in:
Vnitř Lék 2012; 58(9): 647-653
Category:
Reviews
Overview
Povrchové (superficiální) tromboflebitidy (ST) představují dosti heterogenní skupinu onemocnění, což je dáno jednak rozdílností dvou základních forem ST – varikoflebitidy a tromboflebitidy „zdravé“ žíly, jednak i dalšími faktory – podílem trombotického a zánětlivého procesu, lokalizací a rozsahem trombózy v povrchovém žilním systému, vzdáleností od hlubokého žilního systému, stupněm žilní insuficience i celkovým trombotickým rizikem pacienta. ST sdílí mnoho společných rysů s hlubokou žilní trombózou (klinické rizikové faktory, trombofilní stavy), obě choroby se často vyskytují společně či jedna následuje druhou. Podle některých autorů by měla být ST chápána jako součást žilní tromboembolické nemoci v širším slova smyslu. Se změnou pohledu na ST souvisí však i další nedořešené otázky týkající se diagnostiky a léčby ST. Dosud není stanoven optimální způsob léčby založený na důkazech. V závažnějších případech ST je doporučována antikoagulační léčba, zatím však nebyl dosažen odborný konsenzus ohledně jejího dávkování a délky. Studie CALISTO potvrdila benefit fondaparinuxu v profylaktických dávkách v léčbě izolované ST a její výsledky se promítly i do nových doporučení odborných společností. Další studie k rozšíření našich znalostí o ST a k získání důkazů o účinné léčbě jsou velmi zapotřebí.
Klíčová slova:
povrchová tromboflebitida – hluboká žilní trombóza – trombofilní stavy – antikoagulační léčba
Úvod
Povrchová (superficiální) tromboflebitida (ST) byla a je považována za zcela nezávažné onemocnění, jednoduše diagnostikovatelné a nevyžadující zvláštní opatření kromě symptomatické léčby. ST je lékařům známa již velmi dlouhou dobu, historicky se do její léčby zapojovali spíše chirurgové, nemoc stála mimo zájem internistů či hematologů a v odborné literatuře jí byla věnována jen omezená pozornost. Nicméně možnost komplikace ST plicní embolií (PE) si uvědomoval již Virchow a jeho současníci [1–3].
Zvýšení zájmu o ST podnítil až nástup sonografie do cévní medicíny. S narůstajícím využitím ultrazvukového vyšetření žil byly zjištěny dosti překvapivé a znepokojivé nálezy – jednak tromby v povrchovém žilním systému jsou mnohdy většího rozsahu, než by se pouhým fyzikálním vyšetřením zdálo, jednak poměrně často přecházejí do hlubokého žilního systému [3].
Definice, rozdělení
ST lze definovat jako zánětlivé postižení segmentu epifasciálního žilního systému, obvykle provázené trombózou příslušného segmentu, s velmi variabilním vzájemným poměrem zánětlivého a trombotického procesu [4]. Z toho zřejmě vyplývá i historické učebnicové členění ST na „tromboflebitidu“, tj. primární zánět žilní stěny vedoucí k trombóze, a „povrchovou flebotrombózu“ – primární trombózu způsobující následně zánět. Tyto termíny se však dnes jeví jako poněkud vágní a uvedené dělení by mělo být opuštěno [2].
Nejednotu v názorech na závažnost a léčbu ST ovlivňuje mimo jiné fakt, že touto diagnózou bývají označovány i některé zvláštní formy flebitidy povrchových žil, které se opravdu etiopatogeneticky odlišují a obvykle vyžadují i poněkud jiný léčebný přístup (tab. 1).
![Zvláštní formy flebitidy [1,3,4].DUSG – duplexní ultrasonografie, NSAID – nesteroidní antiflogistika](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/1f80f5257dc29f3149d698891e57b85a.png)
I po vyčlenění těchto odlišných forem představuje ST dosti heterogenní skupinu onemocnění. Jako 2 základní jednotky (rozdílné etiopatogeneticky, histologicky i klinickým průběhem) je třeba chápat ST na varikózně změněné žíle, často nazývanou jako varikoflebitidu, a ST na žíle „zdravé“. Varikoflebitida se vyskytuje zhruba 10krát častěji než ST na nevarikózní žíle [3].
Patofyziologie
Stejně jako u hluboké žilní trombózy (HŽT) se v patogenezi ST uplatňuje klasická Virchowova trias, a to s variabilním zastoupením jejích jednotlivých součástí – různou měrou se zapojují hemostatické a zánětlivé děje a alterace krevního toku. Je známo, že svou roli v patofyziologii ST hrají některé mediátory, např. trombin, interleukiny, tumor necrosis factor a jiné, avšak přesněji zatím jejich vzájemné působení vysvětleno nebylo.
Varikoflebitida (varikotrombóza) obvykle není primárním onemocněním cévní stěny, ale je způsobena především poruchou krevního toku v souvislosti s insuficiencí žilních chlopní a dilatací žíly s následným ovlivněním interakce solubilních a buněčných složek krve a endotelu a výsledným selháním lokálních antitrombotických mechanizmů.
K ST dochází velmi často v terénu chronické žilní insuficience – ST totiž může být jak příčinou, tak i následkem kožních změn. Trombóza v tomto terénu může nastat ve velkých varikózních žilách a bývá spojena s hypodermatitidou a lipodermatosklerózou, nebo se jedná o trombózu v malých žilách, která ani není klinicky patrná, avšak postupně vede k velmi bolestivým změnám a vzniku tzv. bílé atrofie. ST také často nastává v terénu potrombotického syndromu [3–5].
Faktory ovlivňující klinickou závažnost povrchové tromboflebitidy
Kromě základního rozlišení na varikoflebitidu a „nevarikózní“ povrchovou tromboflebitidu je možno uvést ještě řadu dalších faktorů, které způsobují značnou heterogenitu ST, resp. přispívají k podstatným rozdílům v klinickém průběhu a závažnosti jednotlivých případů onemocnění:
- variabilní podíl zánětlivého a trombotického procesu,
- lokalizace;
v literatuře je uváděno zjednodušené rozdělení:
- ST nad kolenem,
- ST pod kolenem,
- ST nad i pod kolenem.
Dle lokalizace v konkrétní povrchové žíle lze pak rozlišovat:
- ST na velké saféně (kmeni či varixech v povodí). Jako samostatná jednotka bývá někdy uváděna tzv. ascendentní tromboflebitida velké safény (ta nemusí být vždy provázena výraznější periflebitidou, zato ale pacienta ohrožuje rychlou proximální ascenzí a proniknutím do hlubokého žilního systému s příslušnými závažnými následky).
- ST na malé saféně – ta mívá poněkud odlišné projevy, díky umístění žíly v duplikatuře krurální fascie často vede k citlivosti lýtka, podobně jako HŽT.
- ST v ostatních povrchových žilách.
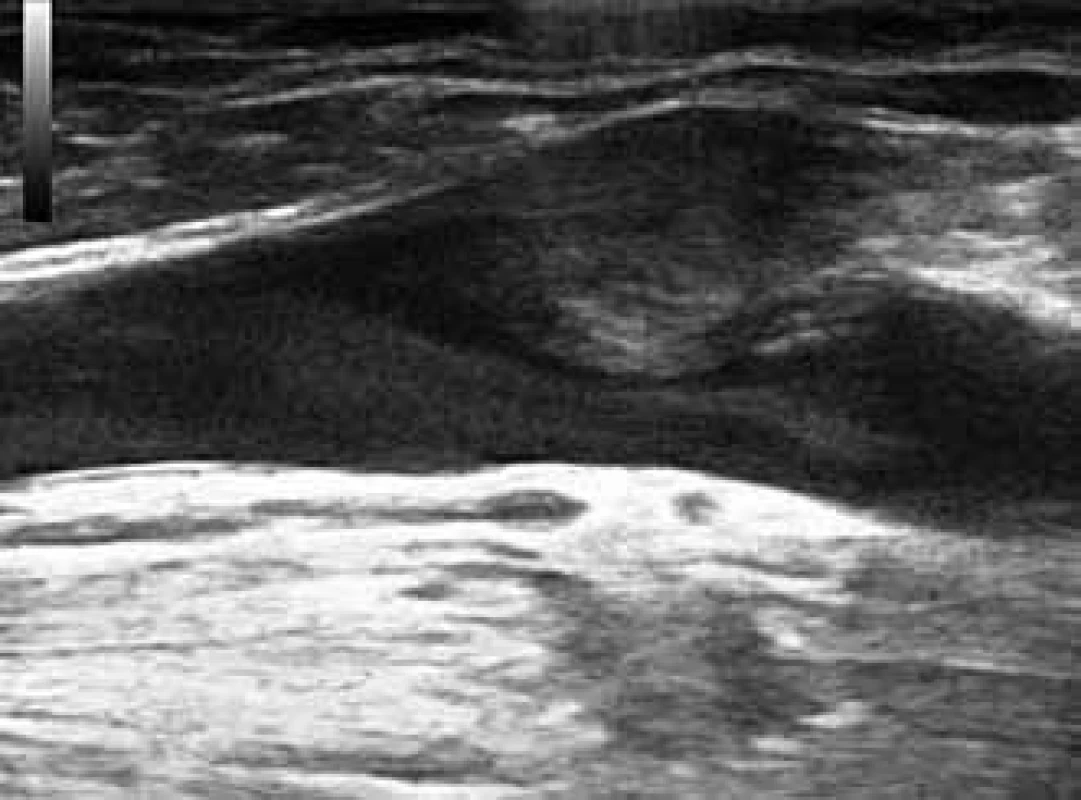
- celkový rozsah ST – ten souvisí i s lokalizací – nejrozsáhlejší je samozřejmě postižení celého kmene velké safény (někdy jde o trombus značných rozměrů – obr. 1, 2); naopak mnohdy je ST jen velmi malého rozsahu, např. omezena jen na jeden varix,
- stupeň žilní insuficience,
- vzdálenost od spojení s hlubokým žilním systémem (safénofemorální či safénopopliteální junkce, případně perforátory). Přesah trombu z velké safény do safénofemorální junkce je patrný na obr. 3,
- další rizikové faktory pacienta – přidružené choroby; trombofilní stavy; situace rizikové z hlediska tromboembolických komplikací [3,6,7].

Studie povrchové tromboflebitidy – metodologické rozdíly
Ačkoli ST byla donedávna lékařským výzkumem dosti opomíjena, přesto lze najít studie zabývající se její epidemiologií, průběhem a léčbou. Jejich výsledky jsou však často nejednoznačné či dokonce rozporné. Při hlubším zkoumání lze zjistit značné metodologické rozdíly v designu těchto studií:
- Byly použity různé definice ST (varikoflebitida, flebitida nevarikózní či obojí bez zvláštního rozlišení). Obecně je (vzhledem k nižší incidenci) mnohem méně údajů o tromboflebitidě nevarikózní.
- Byly zahrnuty rozdílné skupiny pacientů, mnohdy dosti selektované, takže jde velmi pravděpodobně o selekční „bias“ – a to jak ve smyslu vyřazení příliš rizikových pacientů z některých studií (s vylučovacími kritérii, jako trombofilie, gravidita, malignita, kardiovaskulární onemocnění, obezita), tak i naopak ve smyslu studií zahrnujících spíše závažnější a rizikovější případy, soustředěné do specializovaných center. V obou případech potom výsledky zřejmě neodpovídají přesně realitě.
- Byly použity rozličné léčebné postupy či jejich kombinace (různé typy antikoagulační léčby v různých dávkách, kompresní léčba, lokální léčba, chirurgická léčba, nesteroidní antiflogistika).
- V jednotlivých studiích byly sledovány nestejné cíle (ústup potíží, zábrana extenze či recidivy ST, prevence tromboembolických komplikací).
- Při sledování incidence konkomitantní či následné HŽT byl v některých studiích hodnocen jen výskyt symptomatické HŽT, v jiných i asymptomatické; navíc někteří autoři považovali za komplikaci jen proximální HŽT, zatímco jiní brali v úvahu i trombózu distální či dokonce trombózu svalových žil.
- Další možnou námitkou je malý počet pacientů ve většině studií a převládající retrospektivní charakter studií.
Povrchová tromboflebitida jako součást tromboembolické nemoci?
I přes nedostatek metodologicky kvalitních studií přibývají poznatky, které mění pohled lékařské veřejnosti (či snad alespoň její části) na ST. ST byla dosud podceňována, považována za nesrovnatelnou s HŽT a v učebnicích uváděná odděleně od žilní tromboembolické nemoci (TEN). Do pojmu TEN je však v širším smyslu zahrnována nejen HŽT na dolních končetinách a PE, ale také HŽT na horních končetinách a trombózy v netypických lokalizacích – cerebrální, hepatické, renální, splenické, portální, mezenterické a ovariální. Z tohoto hlediska by i ST měla být posuzována jako určitá lokální forma TEN. V literatuře jsou na podporu tohoto tvrzení uváděny následující argumenty [2]:
- ST a TEN sdílejí řadu společných klinických rizikových faktorů – úraz, operace, gravidita, hormonální antikoncepce, hormonální substituční léčba, dlouhodobá imobilizace, dlouhý let, obezita, vyšší věk, malignita (historicky je asociace ST a malignity známa již od dob Armanda Trousseaua; v novějších publikacích je uváděna souvislost ST s tumory prsu, tlustého střeva, pankreatu, ovarií, kůže a hematoonkologickými chorobami), autoimunitní onemocnění [2,5,8–18].
- U pacientů se ST i s TEN je vyšší výskyt trombofilních stavů. U ST jsou trombofilní stavy nalézány výrazně častěji v případě ST na „zdravé“ žíle, avšak i u varikoflebitid je jejich prevalence vyšší než u kontrolních souborů [17,18]. První příhoda ST byla spojena s leidenskou mutací v genu pro faktor V, s mutací v genu pro protrombin G20210A, deficitem antitrombinu, deficitem proteinu C a S [11,19–20]. U recidivujících ST byl zjištěn častější výskyt antikardiolipinových protilátek, vysoká hladina koagulačního faktoru VIII a deficit proteinu S [21–24].
- Koexistence ST a TEN, resp. zjištění HŽT, ev. PE současně s diagnózou ST. Rozsáhlejší literární rešerše z roku 2005 popsala koexistenci ST a HŽT v 6–53 %, ST a PE v 0–33,3 %. Autoři sami uvádějí, že většina hodnocených studií byla retrospektivních a zahrnovala jen malý počet nemocných (vyřadili pouze studie s méně než 20 pacienty). Nevylučují ani, že průběh šíření trombotického procesu mohl být z hlubokého do povrchového systému, což však nebylo v žádné studii specificky zkoumáno [5]. Dvě novější francouzské studie zahrnovaly již větší počet pacientů se symptomatickou ST – studie POST 844 a studie OPTIMEV (resp. její podstudie zaměřená na ST) 788 nemocných [25,26]. Současná HŽT či PE byla zjištěna u 24,9 % (POST), resp. 28,8 % (OPTIMEV).
- Progrese ST do HŽT, resp. vývoj HŽT či PE následně po ST. I v případě sonograficky potvrzené „izolované“ ST může dojít v následném kratším časovém intervalu k extenzi trombotického procesu do hlubokých žil. Několik studií hodnotilo incidenci následné tromboembolické komplikace pomocí opakovaných ultrazvukových vyšetření. Z důvodů uvedených výše (zejména užití různých způsobů léčby a také různé definice HŽT) jsou jejich výsledky rozmanité a kolísají ve starších studiích od 5,6 % do 15 % [27–30]. Ve studii POST [25] došlo během 3měsíčního sledování nemocných s izolovanou ST k vývoji HŽT v 2,8 % a symptomatické PE v 0,5 %, k vývoji tromboembolických komplikací v širším smyslu (nejen HŽT a PE, ale i recidivy ST či její extenze) v 8,3 % – navzdory faktu, že více než 90 % nemocných bylo léčeno antikoagulační léčbou (nikoli však standardizovanou – volba léčby byla ponechána na rozhodnutí ošetřujícího specialisty).
- Prodělaná TEN je rizikovým faktorem pro vznik ST v budoucnosti [21].
- Prodělaná ST je rizikovým faktorem pro vznik TEN v budoucnosti [21,31,32] – udávané „odds ratio“ – poměr šancí 4,3 [31] či dokonce 6,8 [32].
- ST není zcela benigní chorobou. Ve srovnání s HŽT je ST jistě méně závažnou chorobou (nižší komorbidita, nižší mortalita), přesto z výše uvedených faktů vyplývá, že ST nelze podceňovat a že její následky mohou být závažné [33].
- Zatím neexistuje přijatelná teorie, která by zdůvodnila, proč posuzovat ST jako zcela odlišnou jednotku od systémové TEN.
Nový přístup k povrchové tromboflebitidě v klinické praxi i ve výzkumu – nedořešené otázky
Měl by být dosažen konsenzus ohledně terminologie a klasifikace ST. Při stanovení této diagnózy by bylo vhodné vždy upřesnit lokalizaci a rozsah ST. Mělo by být uvedeno, jedná-li se o varikoflebitidu či tromboflebitidu na nevarikózní žíle a zcela odděleny by zřejmě měly být zvláštní formy flebitidy (tab. 1).
Je třeba sjednotit také diagnostický přístup k ST. Ve většině případů postačí k diagnóze ST jen fyzikální nález. Přesto by bylo vhodné rozšířit využití duplexní sonografie (DUSG) v diagnostice. DUSG jednak potvrdí diagnózu ST v případě ne zcela jasného fyzikálního nálezu, jednak upřesní rozsah trombotických hmot v povrchové žíle či žilách. Trombus totiž velmi často bývá mnohem větší, než by se pouhým pohledem či pohmatem mohlo zdát. Snad nejdůležitější role DUSG ale spočívá ve vyloučení ev. současné HŽT. Protokol sonografického vyšetření by měl zahrnovat vyšetření hlubokých žil oboustranně (v literatuře totiž bývá popisována i tzv. distanční trombóza, tj. nesouvisející přímo se ST, např. i na druhostranné končetině). Vlastní sonografický popis ST by pak měl uvádět lokalizaci a délku nálezu (v některých případech však délku nelze spolehlivě změřit, např. jde-li o postižení konvolutu varixů), vzdálenost od safénofemorální či safénopopliteální junkce (při postižení velké či malé safény). Často je nutné i opakování DUSG ke sledování vývoje ST [5,34].
Zatím nebylo dosaženo konsenzu ohledně vyšetřování trombofilních stavů u ST. Někteří autoři je navrhují v případě „nevarikózní“ ST či recidivující ST, případně při pozitivní rodinné či osobní anamnéze TEN [5,7].
Další otázkou je event. onkologický screening u pacientů se ST – ten je některými autory navrhován zejména u „nevarikózní“ ST [5–7]. Otázka onkologického screeningu však není jednoznačně dořešena ani u pacientů s HŽT, přestože u nich byla mnohem více studována. Není totiž jasně prokázáno, zdali časná detekce skryté malignity u nemocných s žilním tromboembolizmem zlepší jejich prognózu [16].
Ještě naléhavější je potřeba dosáhnout alespoň základního konsenzu ohledně léčby ST. V praxi bývá ST léčena nejspíše někdy i samotným nemocným bez návštěvy lékaře, dosti často praktickým lékařem, dále dermatologem, angiologem či chirurgem. Volba léčby pak závisí na odbornosti a zkušenosti lékaře, možnostech a zvyklostech pracoviště, bývá tedy značně rozmanitá a zároveň je i zdrojem kontroverzí mezi jednotlivými odborníky. Zatím však nebyl stanoven optimální způsob léčby založený na důkazech.
Doporučována je mobilizace pacienta, kompresní léčba, k symptomatické úlevě také vede lokální léčba přípravky s obsahem nesteroidních antiflogistik (NSAID), heparinu či heparinoidů anebo celková léčba NSAID.
Antibiotika, ač v praxi stále často používaná, nejsou ve většině případů tromboflebitidy indikována [2,3,5,35].
Na některých pracovištích je prováděna léčba chirurgická – lokální excize s vybavením trombu; trombektomie s následnou ligací safény nebo strippingem v případě ascendentní tromboflebitidy velké safény [3].
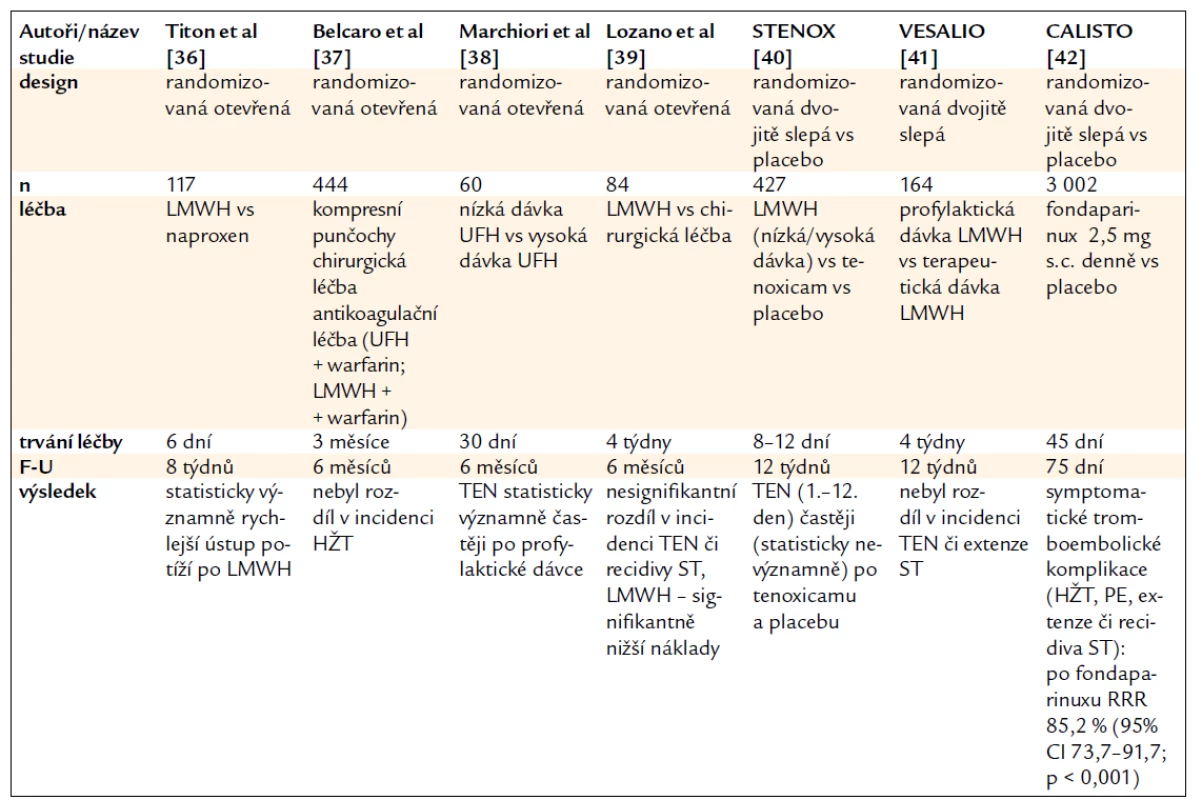
Stále větší příklon je k léčbě antikoagulační – výsledky studií jsou uvedeny v tab. 2 [36–42]. Dosud není zcela jasná volba typu antikoagulancia, dávky a délky podávání, avšak s postupným přibýváním dat lze sledovat i vývoj odborných doporučení.
Autoři systematického přehledu Cochranovy databáze z roku 2007 shrnuli, že LMWH i NSAID významně snižují riziko extenze či recidivy ST oproti placebu (o 70 %), zatímco chirurgická léčba zlepšuje lokální symptomy [43].
Soubor doporučení antitrombotické léčby tzv. American College of Chest Physicians (ACCP) ve svém předposledním vydání z roku 2008 se zmiňoval o ST jen velmi stručně – v případě „spontánní“ ST byla navrhována léčba středními dávkami heparinu či nízkomolekulárního heparinu (LMWH) po dobu minimálně 4 týdnů – s dovětkem, že úroveň dostupných důkazů je poměrně nízká – „2B“ [44].
Doporučení evropských národních expertních skupin kolísají od návrhů pouhého pečlivého sledování po antikoagulační léčbu po dobu 6–12 týdnů v rozmezí od profylaktické do plné léčebné dávky [35]. Konsenzus slovenských odborných společností z roku 2009 doporučuje LMWH ve všech případech ST s výjimkou ST velmi malého rozsahu (tj. délky pod 5 cm) v dostatečné vzdálenosti od safénofemorální junkce (tj. nad 10 cm), a to po dobu 4 týdnů v dávce adjustované rozsahu ST a komorbiditám [45].
Jedinou velkou randomizovanou, placebem kontrolovanou studií antikoagulační léčby ST je CALISTO (tab. 2). V ní byl použit fondaparinux v profylaktické dávce po dobu 45 dní u nemocných s izolovanou ST o délce alespoň 5 cm, ve vzdálenosti nad 3 cm od safénofemorální junkce [42]. Výsledky byly publikovány poměrně nedávno a potvrdily benefit uvedené antikoagulační léčby u ST.
Zvýšení odborného zájmu o ST dokumentuje i poměrně rychlý nárůst počtu publikací na toto téma. Nejnovější analýzy a doporučení již reflektují i výsledky zmiňovaných nedávných studií (POST, OPTIMEV, CALISTO).
Nově publikovaný systematický přehled Cochranovy databáze z roku 2012 uvádí pro ST jako validní terapeutickou možnost podávání profylaktické dávky fondaparinuxu po dobu 6 týdnů. Autoři zdůrazňují nutnost dalších kvalitních studií k upřesnění úlohy nových antikoagulancií, LMWH, NSAID, chirurgické i lokální léčby [46].
Poslední verze doporučení ACCP z roku 2012 pak upřesňuje indikaci k antikoagulační léčbě – pro ST o délce alespoň 5 cm navrhuje profylaktickou dávku fondaparinuxu či LMWH po dobu 45 dní. Úroveň důkazů je však stále hodnocena jako poměrně nízká – „2B“ [47].
Objevují se ale i publikace argumentující proti rutinnímu používání antikoagulační léčby u izolované ST. Autoři zdůrazňují, že v placebové větvi studie CALISTO byla velmi nízká incidence závažných tromboembolických komplikací, tj. HŽT a PE (1,3 %) a extrémně nízká mortalita a zpochybňují „cost-effectiveness“, resp. účinnost vynaložených nákladů při užívání antikoagulační léčby ve všech případech izolované ST [48,49].
Zásadním úkolem bude tedy zřejmě jakási stratifikace ST dle závažnosti a definice jednak těch případů ST, v nichž je antikoagulační léčba nezbytná, jednak těch případů, v nichž naopak není nutná. Podle některých autorů by léčba ST měla být individualizována, přičemž za případy s vysokým rizikem (a tedy s indikací antikoagulační léčby) lze považovat nemocné s postižením kmene velké či malé safény, s trombem blížícím se safénofemorální junkci, s nevarikózní tromboflebitidou a s rizikovými faktory TEN [50,51].
Podobné závěry vyplynuly i z nedávné souhrnné analýzy observačních studií POST a OPTIMEV zaměřené na určení prediktorů recidivy TEN (definované jako HŽT, PE či nová ST) u nemocných se symptomatickou ST. Vysoké riziko recidivy TEN měli pacienti s maligním onemocněním a s postižením safénofemorální junkce – v univariátní analýze statisticky významně zvýšené riziko, v multivariátní analýze těsně pod hranicí statistické významnosti (p = 0,06). Jediným významným a nezávislým prediktorem recidivy TEN pak bylo mužské pohlaví. Dalším zajímavým zjištěním této analýzy bylo nízké riziko recidivy TEN u pacientů s ST, kteří nebyli antikogulačně léčeni (byli tedy a priori považováni investigátory za „nízce rizikové“). Autoři takto dokládají, že určitá část případů ST skutečně antikoagulační léčbu nevyžaduje [52].
Dále je třeba zdůraznit i roli ST v anamnéze osobní, případně rodinné. Ačkoli prodělaná ST je rizikovým faktorem následné HŽT, často bývá ST v anamnéze opomíjena, resp. lékaři se na ni aktivně nevyptávají. Takový údaj by přitom mohl hrát roli např. při doporučeních perioperační tromboprofylaxe v rámci předoperačních vyšetření, dále při rozhodování o vhodnosti testování trombofilních stavů v trombotických centrech nebo např. při zvažování předpisu hormonální antikoncepce či hormonální substituční léčby v ambulanci gynekologa.
Výskyt ST by také neměl být opomíjen ve výzkumu, resp. ve studiích zkoumajících rizikové faktory, incidenci, komplikace či účinnost prevence a léčby TEN. V některých genetických studiích trombofilních stavů byla do projevů TEN zahrnuta i ST [53], v jiných nikoli [54].
Závěrečná doporučení
Zatím nelze vyvodit jednotné doporučení k diagnostice a léčbě ST. V praxi je nutno vycházet nejen z dostupných fakt a důkazů, ale také z konkrétních možností, resp. z dostupnosti určitých léků a postoje zdravotních pojišťoven. Velkou roli jistě hraje zkušenost a odborné znalosti ošetřujícího lékaře a jeho postoj k dané problematice. Lékař prvního kontaktu by měl zhodnotit, vyžaduje-li určitý případ ST specializované vyšetření. U nejméně rizikových případů (tj. pacientů se ST na varikózní žíle, o délce pod 5 cm, v dostatečné vzdálenosti od safénofemorální či safénopopliteální junkce, bez dalších rizikových faktorů TEN a bez pokročilé žilní insuficience) by postačovala kompresní a lokální léčba, případně celkově NSAID. V ostatních případech by měl další diagnostiku a léčbu řídit pokud možno cévní specialista. Ten by měl provést DUSG žil obou dolních končetin, u nemocných s nevarikózní ST a s osobní či rodinnou anamnézou TEN zvážit vyšetření na trombofilní stav (případně po poradě s hematologem), v případech nevarikózní ST a při klinickém podezření na malignitu provést či doporučit i onkologický screening. Podle odhadu pacientova individuálního rizika TEN, ale i rizika krvácivých komplikací by pak měl rozhodnout o antikoagulační terapii – nejspíše formou ambulantní léčby profylaktickou dávkou LMWH či fondaparinuxu. Léčba by podle doporučení ACCP měla trvat 6 týdnů, podle klinického nálezu či sonografické kontroly lze někdy rozhodnout o jejím zkrácení či prodloužení. U nejrizikovějších případů (přesah do safénofemorální junkce, velký rozsah ST či její extenze, přídatná rizika TEN apod.) je pak nutno zvážit vyšší dávky antikoagulační léčby.
Nejistoty a rozepře kolem ST ještě budou pravděpodobně přetrvávat. Jisté však je, že bychom měli začít tuto chorobu brát vážněji než dosud a případné odborné spory by měly mít pokud možno konstruktivní charakter. Nutná je i důkladná edukace zaměřená na nové poznatky o ST a určená nejen pro zdravotníky, ale i pro veřejnost. Velmi potřebné jsou další studie k rozšíření našich znalostí o ST i k získání důkazů o její optimální léčbě.
Práce byla podpořena Programem rozvoje vědních oblastí na Univerzitě Karlově (PRVOUK) Lékařské fakulty v Plzni.
MUDr. Jana Hirmerová, Ph.D.
www.fnplzen.cz
e-mail: hirmerova@fnplzen.cz
Doručeno do redakce: 29. 1. 2012
Přijato po recenzi: 9. 4. 2012
Sources
1. Hingorani A, Ascher E. Superficial venous thrombophlebitis. In: Handbook of Venous Disorders. 3rd Ed. London, UK: Hodder Arnold 2009 : 314–319.
2. Kitchens CS. How I treat superficial venous thrombosis. Blood 2011; 117 : 39–44.
3. Blättler W, Schwarzenbach B, Largiadèr J. Superficial vein thrombophlebitis – serious concern or much ado about little? Vasa2008; 37 : 31–38.
4. Schellong S, Schwarz T. Phlebitis. Peripheral Venous Diseases: Nonsurgical Approach. In: Lanzer P, Topol EJ (eds). PanVascular Medicine. Berlin Heidelberg, Germany: Springer-Verlag 2002 : 1505–1506.
5. Leon L, Giannoukas AD, Dodd D et al. Clinical significance of superficial vein thrombosis. Eur J Vasc Endovasc Surg 2005; 29 : 10–17.
6. Haire WD. Deep Venous Thrombosis and Pulmonary Embolus. In: Kitchens, Alving, Kessler. Consultative Hemostasis and Thrombosis. Elsevier Science 2002 : 211–212.
7. Perrin M, Gillet JL. A review of superficial thrombophlebitis of the lower limbs. Phlebolymphology 2002; 38 : 69–73.
8. Litzendorf MA, Satiani B. Superficial venous thrombosis: disease progression and evolving treatment approaches. Vasc Health Risk Manag 2011; 7 : 569–575.
9. McColl MD, Ramsay JE, Tait RC et al. Superficial vein thrombosis: incidence in association with pregnancy and prevalence of thrombophilic defects. Thromb Haemost 1998; 79 : 741–742.
10. deSancho MT, Dorff T, Rand JH. Thrombophilia and the risk of thromboembolic events in women on oral contraceptives and hormone replacement therapy. Blood Coagul Fibrinolysis 2010; 21 : 534–538.
11. de Moerloose P, Wutschert R, Heinzmann M et al. Superficial vein thrombosis of lower limbs: influence of factor V Leiden, factor II G20210A and overweight. Thromb Haemost 1998; 80 : 239–241.
12. Trousseau A. Plegmasia alba dolens. Lectures on clinical medicine, delivered at the Hotel-Dieu, Paris 1865; 5 : 281–332.
13. Mouton WG, Kienle Y, Muggli B et al. Tumors associated with superficial thrombophlebitis. Vasa 2009; 38 : 167–170.
14. Leon LR Jr, Labropoulos N. Superficial vein thrombosis and hypercoagulable states: the evidence. Perspect Vasc Surg Endovasc Ther 2005; 17 : 43–46.
15. Wichers IM, Haighton M, Büller HR et al. A retrospective analysis of patients treated for superficial vein thrombosis. Neth J Med 2008; 66 : 423–427.
16. Sørensen HT, Sværke C, Farkas DK et al. Superficial and deep venous thrombosis, pulmonary embolism and subsequent risk of cancer. Eur J Cancer 2012; 48 : 586–593.
17. Karathanos C, Sfyroeras G, Drakou A et al. Superficial vein thrombosis in patients with varicose veins: role of thrombophilia factors, age and body mass. Eur J Vasc Endovasc Surg 2012; 43 : 355–358.
18. Milio G, Siragusa S, Minà C et al. Superficial venous thrombosis: prevalence of common genetic risk factors and their role on spreading to deep veins. Thromb Res 2008; 123 : 194–199.
19. Hanson JN, Ascher E, DePippo P et al. Saphenous vein thrombophlebitis (SVT): a deceptively benign disease. J Vasc Surg 1998; 27 : 677–680.
20. Martinelli I, Cattaneo M, Taioli E et al. Genetic risk factors for superficial vein thrombosis. Thromb Haemost 1999; 82 : 1215–1217.
21. Schönauer V, Kyrle PA, Weltermann A et al. Superficial thrombophlebitis and risk for recurrent venous thromboembolism. J Vasc Surg 2003; 37 : 834–838.
22. de Godoy JM, Batigália F, Braile DM. Superficial thrombophlebitis and anticardiolipin antibodies – report of association. Angiology 2001; 52 : 127–129.
23. de Godoy JM, Braile DM. Protein S deficiency in repetitive superficial thrombophlebitis. Clin Appl Thromb Hemost 2003; 9 : 61–62.
24. Pabinger I, Schneider B. Thrombotic risk in hereditary antithrombin III, protein C, or protein S deficiency. A cooperative, retrospective study. Gesellschaft fur Thrombose - und Hamostaseforschung (GTH) Study Group on Natural Inhibitors. Arterioscler Thromb Vasc Biol 1996; 16 : 742–748.
25. Decousus H, Quéré I, Presles E et al. POST (ProspectiveObservational Superficial Thrombophlebitis) Study Group. Superficial Venous Thrombosis and Venous Thromboembolism. A Large, Prospective Epidemiologic Study. Ann Intern Med 2010; 152 : 218–224.
26. Galanaud JP, Genty C, Sevestre MA et al. OPTIMEV SFMV investigators. Predictive factors for concurrent deep-vein thrombosis and symptomatic venous thromboembolic recurrence in case of superficial venous thrombosis. The OPTIMEV study. Thromb Haemost 2011; 105 : 31–39.
27. Blumenberg RM, Barton E, Gelfand ML et al. Occult deep venous thrombosis complicating superficial thrombophlebitis. J Vasc Surg 1998; 27 : 338–343.
28. Bounameaux H, Reber-Wasem MA. Superficial thrombophlebitis and deep vein thrombosis. A controversial association. Arch Intern Med 1997; 157 : 1822–1824.
29. Pulliam CW, Barr SL, Ewing AB. Venous duplex scanning in the diagnosis and treatment of progressive superficial thrombophlebitis. Ann Vasc Surg 1991; 5 : 190–195.
30. Chengelis DL, Bendick PJ, Glover JL et al. Progression of superficial venous thrombosis to deep vein thrombosis. J Vasc Surg 1996; 24 : 745–749.
31. Heit JA, Silverstein MD, Mohr DN et al. Risk factors for deep vein thrombosis and pulmonary embolism: a population-based case-control study. Arch Intern Med 2000; 160 : 809–815.
32. Tosetto A, Frezzato M, Rodeghiero F. Prevalence and risk factors of non-fatal venous thromboembolism in the active population of the VITA Project. J Thromb Haemost 2003; 1 : 1724–1729.
33. Decousus H, Leizorovicz A. Superficial thrombophlebitis of the legs: still a lot to learn. J Thromb Haemost 2005; 3 : 1149–1151.
34. Vítovec M, Pecháček V. Doporučení pro duplexní ultrazvukové vyšetření končetinových žil. Vnitř Lék 2009; 55 : 136–146.
35. Décousus H, Bertoletti L, Frappé P et al. Recent findings in the epidemiology, diagnosis and treatment of superficial-vein thrombosis. Thromb Res 2011; 127 (Suppl 3): S81–S85.
36. Titon JP, Auger D, Grange P et al. Traitement curatif des thromboses veineuses superficielles par nadroparine calcique. Recherche posologique et comparaison à un anti-inflammatoire non stéroïdien. Ann Cardiol Angeiol (Paris) 1994; 43 : 160–166.
37. Belcaro G, Nicolaides AN, Errichi BM et al. Superficial thrombophlebitis of the legs: a randomized, controlled, follow-up study. Angiology 1999; 50 : 523–529.
38. Marchiori A, Verlato F, Sabbion P et al. High versus low doses of unfractionated heparin for the treatment of superficial thrombophlebitis of the leg. A prospective, controlled, randomized study. Haematologica 2002; 87 : 523–527.
39. Lozano FS, Almazan A. Low-molecular-weight heparin versus saphenofemoral disconnection for the treatment of above-knee greater saphenous thrombophlebitis: a prospective study. Vasc Endovascular Surg 2003; 37 : 415–420.
40. Superficial Thrombophlebitis Treated By Enoxaparin Study Group. A pilot randomized double-blind comparison of a low-molecular-weight heparin, a nonsteroidal anti-inflammatory agent, and placebo in the treatment of superficial vein thrombosis. Arch Intern Med 2003; 163 : 1657–1663.
41. Prandoni P, Tormene D, Pesavento R. Vesalio Investigators Group. High vs. low doses of low-molecular-weight heparin for the treatment of superficial vein thrombosis of the legs: a double-blind, randomized trial. J Thromb Haemost 2005; 3 : 1152–1157.
42. Decousus H, Prandoni P, Mismetti P et al. CALISTO Study Group. Fondaparinux for the Treatment of Superficial-Vein Thrombosis in the Legs. N Engl J Med 2010; 363 : 1222–1232.
43. Di Nisio M, Wichers IM, Middeldorp S. Treatment for superficial thrombophlebitis of the leg. Cochrane Database Syst Rev 2007; 2: CD004982.
44. Kearon C, Kahn SR, Agnelli G et al. American College of Chest Physicians. Antithrombotic therapy for venous thromboembolic disease: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th Ed). Chest 2008; 133 (6 Suppl): 454S–545S.
45. Štvrtinová V, Dukát A, Frankovičová M et al. Povrchová tromboflebitída – diagnostika a liečba. Vnitř Lék 2009; 55 : 131–135.
46. Di Nisio M, Wichers IM, Middeldorp S. Treatment for superficial thrombophlebitis of the leg. Cochrane Database Syst Rev 2012; 3: CD004982.
47. Kearon C, Akl EA, Comerota AJ et al. AmericanCollege of Chest Physicians. Antithrombotic therapy for VTE disease: Antithrombotic Therapy and Prevention of Thrombosis (9th Ed): American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141 (2 Suppl): e419S–e494S.
48. Goldman L, Ginsberg J. Superficial phlebitis and phase 3.5 trials. N Engl J Med 2010; 363 : 1278–1280.
49. Blondon M, Righini M, Bounameaux H et al. Fondaparinux for isolated superficial-vein thrombosis of the legs: a cost-effectiveness analysis. Chest 2012; 141 : 321–329.
50. Carnero-Vidal LG, Rathbun S, Wakefield TW. Anticoagulant treatment for superficial venous thrombosis. Dis Mon 2010; 56 : 574–581.
51. Dalsing MC. The case against anticoagulation for superficial venous thrombosis. Dis Mon 2010; 56 : 582–589.
52. Galanaud JP, Bosson JL, Genty C. Superficial vein thrombosis and recurrent venous thromboembolism: a pooled analysis of two observational studies. J Thromb Haemost 2012; doi: 10.1111/j.1538-7836.2012.04704.x. (Epub ahead of print).
53. Souto JC, Almasy L, Borrell M et al. Genetic susceptibility to thrombosis and its relationship to physiological risk factors: the GAIT study. Genetic Analysis of Idiopathic Thrombophilia. Am J Hum Genet 2000; 67 : 1452–1459.
54. Severinsen MT, Overvad K, Johnsen SP et al. Genetic susceptibility, smoking, obesity and risk of venous thromboembolism. Br J Haematol 2010; 149 : 273–279.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2012 Issue 9
-
All articles in this issue
- Srovnání dvou metod dlouhodobého externího telemonitorování EKG po ablaci fibrilace síní
- Časný pohybový režim snižuje asymetrický dimetylarginin po transplantaci ledviny
- Povrchová tromboflebitida, neprávem podceňovaná choroba – je čas změnit názor?
- Léková compliance – úskalí terapie revmatoidní artritidy?
- Peripartální život ohrožující krvácení – mezioborové konsenzuální stanovisko
- Upozornění na nebezpečí invazivních infekcí u splenektomovaných pacientů. Zkušenosti z FN Brno 2011
- Morbus Weil – kazuistika a princípy
- Nádor srdce manifestující se náhlou srdeční smrtí
- Naše zkušenosti s léčbou multicentrické plazmocelulární Castlemanovy choroby s projevy vaskulitidy – popis případu a přehled literatury
- Hyperventilační echokardiografie v diagnostice vazospastické anginy pectoris
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Povrchová tromboflebitida, neprávem podceňovaná choroba – je čas změnit názor?
- Upozornění na nebezpečí invazivních infekcí u splenektomovaných pacientů. Zkušenosti z FN Brno 2011
- Morbus Weil – kazuistika a princípy
- Hyperventilační echokardiografie v diagnostice vazospastické anginy pectoris

