Aortální regurgitace
Aortic regurgitation
This paper focuses on aortic regurgitation. It covers the findings related to etiopathogenesis, clinical signs, echocardiographic and catheter examination. It analyses the treatment criteria with a focus on cardiac surgery.
Key words:
aortic regurgitation – aortic valve replacement – left ventricular volume overload – echocardiography and aortic regurgitation
:
P. Gregor; H. Línková
:
Kardiocentrum III. interní - kardiologická klinika 3. lékařské fakulty UK a FN Královské Vinohrady Praha, přednosta prof. MUDr. Petr Widimský, DrSc., FESC
:
Vnitř Lék 2013; 59(2): 99-104
:
Review
Práce se zabývá problematikou aortální regurgitace. Zahrnuje poznatky týkající se etiopatogeneze, klinických známek, echokardiografického a katetrizačního vyšetření. Rozebírá kritéria léčby, zvláště kardiochirurgické.
Klíčová slova:
aortální regurgitace – náhrada aortální chlopně – objemové přetížení levé komory – echokardiografie u aortální regurgitace
Úvod
Aortální regurgitace (AR) je vadou, která je známa již velmi dlouho. Původ vady, její etiologie a způsoby řešení se však v posledních desítiletích změnily, proto rekapitulace znalostí o této vadě by mohla být zajímavá kromě kardiologů i pro praktické lékaře a internisty tím spíše, že zdaleka nejde o nejčastější vadu a zkušenosti s ní nemusejí být v běžné praxi lékařů tak bohaté jako u některých častějších vad.
V učebnici interny, z níž se učila naše generace k různým zkouškám a atestacím [1], začíná kapitola o AR takto: „Většina čistých aortálních insuficiencí nebo kombinovaných se stenózou je revmatického původu… Vzácnější příčiny jsou bakteriální endokarditida, vrozená anomálie, disekující aneurysma v kořenu aorty, Marfanův syndrom a luetická aortitida“. Z uvedené ukázky vyplývá, jak se jen v průběhu necelého čtvrtstoletí, které uplynulo od vydání uvedené učebnice, situace změnila. Porevmatická etiologie je dnes již velmi vzácná, luetická mesaortitida téměř neexistuje, mezi nejčastější naopak patří degenerativní a vrozené bikuspidální aortální vady, kdy degenerativní nejsou ve výše uvedeném výňatku vůbec uvedeny.
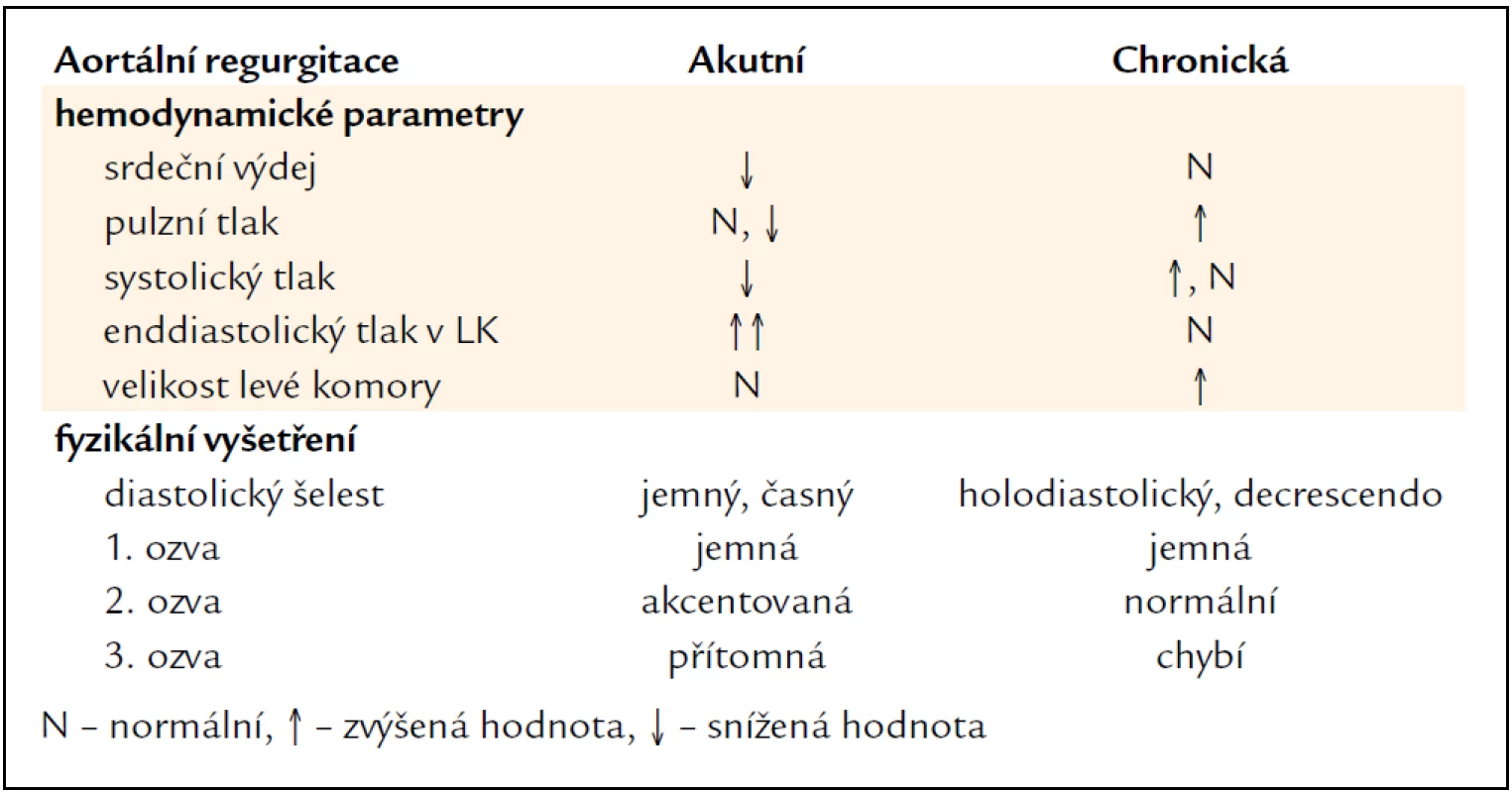
V celkovém počtu operovaných vad zaujímají podle Čerbáka první dvě místa stenóza aorty (více než 50 %) a mitrální regurgitace (přes 20 %). AR je v počtu operovaných vad na třetím místě a v porovnání se stenózou aorty toto číslo představuje 1/5, tedy zhruba 10 % [2].
AR je vada spojená s regurgitací krve na aortálním ústí do levé komory. Její etiologii lze nyní shrnout do dvou kategorií, a to na postižení samotných cípů a na postižení prstence a kořene aorty (tab. 1). Jako zvláštní skupina se vyčleňuje akutní aortální regurgitace, která se liší od chronické etiologií, hemodynamikou i terapií (viz dále). Degenerativní původ je v současnosti nejčastější u chronické AR.

Z hlediska patofyziologie dochází ke třem hlavním dějům a kompenzačním mechanizmům:
- Především se zvyšuje objem levé komory o regurgitující část krve. Levá komora trpí objemovým přetížením, které se dříve nebo později projeví její dilatací – zvyšuje se enddiastolický objem (vznik excentrické hypertrofie se zvýšením hmotnosti levé komory) – tato dilatace je podle Frank-Starlingova zákona základním kompenzačním mechanizmem, vedoucím k zvýšení kontrakcí (ejekční frakce se zvyšuje). Vzhledem k tomu, že krev přichází do levé komory pod vysokým (arteriálním) tlakem, uplatňuje se u AR kromě objemového i složka tlakového přetížení se zbytněním myokardu levé komory.
- Dalším významným kompenzačním mechanizmem je pokles periferní cévní rezistence, díky níž se regurgitační frakce snižuje.
- Třetím významným kompenzačním dějem je tachykardie, která vede ke zkrácení diastoly, a tím i ke zmenšení regurgitovaného množství krve.
Při delším trvání vady narůstá endsystolický objem, prohlubuje se dilatace a remodelace levé komory, posléze dojde i k jejímu systolickému selhávání s poklesem ejekční frakce.
Klinický obraz
Vada probíhá dlouho asymptomaticky, nemocní mohou pozorovat pouze občasné palpitace, a to někdy i v době, kdy je již vyjádřena dysfunkce levé komory. Při projevech dekompenzace se objevuje dušnost – vada však již v té době bývá ve stadiu vyšší pokročilosti s horší prognózou. Stenokardie jsou zde – na rozdíl od aortální stenózy – vzácné.
Při fyzikálním vyšetření je nejnápadnějším nálezem diastolický vysokofrekventní decrescendový šelest s maximem v Erbově bodě (3. mezižebří vlevo u sterna), který se propaguje pásovitě podél levého okraje sterna dolů a začíná hned po II. ozvě. Zesiluje se vsedě. Vzácně lze nalézt i diastolický šelest nad mitrálním ústím, tzv. Austinův--Flintův šelest, jehož podkladem je vznik jakési funkční mitrální stenózy tím, jak regurgitující krev z aorty dopadá na přední mitrální cíp (nikdy zde však nebývá mitrální otevírací zvuk) [3,4].
Při pokročilé aortální regurgitaci je nápadná velká tlaková amplituda (zvýšení systolického a snížení diastolického TK). Stejnou příčinu má i typický mrštný Corriganův pulz s rychlým vzestupem pulzové vlny (pulsus magnus, frequens et celer) a řada dalších známek. Z nich jsou nejznámější příznaky Mussetův (otřásání hlavou synchronně s tepem), Quinckeho (pulzace okraje lunuly při lehkém stlačení nehtu), Traubeův (2 ozvy při poslechu nad a. femoralis), Duroziezův (po přitlačení fonendoskopu slyšitelné 2 šelesty), Müllerův (pulzace uvuly). Tyto příznaky však mají význam spíše historický, neboť jde o pozdní příznaky pokročilé AR a dnes je většina nemocných operována dříve, než se tyto příznaky rozvinou [4].
EKG odhalí známky hypertrofie levé komory. Zátěžové EKG slouží k objektivizaci symptomů a k posouzení dlouhodobého vývoje fyzické výkonnosti u málo symptomatických, ale významných regurgitací [5]. Může být užito i před těhotenstvím, k vyloučení arytmií, u sportovců, ale i u osob se sedavým způsobem života k objektivizaci symptomů [5].
Echokardiograficky se prokáže regurgitační jet, který je velice dobře vidět především při barevném dopplerovském mapování (obr. 1). Obraz je velmi přesvědčivý a svádí k přesné kvantifikaci AR, ta však pomocí této metody nemusí být přesná (regurgitační jet může být excentrický, s neostrými okraji, mísí se s mitrálním vtokem, rozhoduje i nastavení ovládacích prvků). Cenné je měření v. contracta (nejužší místo proximálního regurgitačního proudu z barevného mapování – obr. 1a a 1b), která přesahuje u těžších regurgitací 6 mm. Svůj význam má hodnocení šíře regurgitačního toku, která u významnějších vad přesahuje 60 % šíře výtokového traktu levé komory (analogicky lze kvantifikovat i odpovídající plochy) (tab. 2). Tlak v levé komoře poklesá velmi rychle, což lze kontinuální dopplerovskou echokardiografií dobře kvantifikovat jednak strmým poklesem tlakového spádu (bývá spíše u akutní AR), jednak zvýšením deceleračního sklonu (tab.2). Oba posledně uvedené parametry však mohou být ovlivněny celou řadou dalších aktuálních hemodynamických situací (např. systémovou cévní rezistencí). Výpočet regurgitačního objemu a regurgitační frakce vychází ze skutečnosti, že dopředný aortální tepový objem je zvětšen oproti pulmonálnímu ústí o regurgitační objem. Ten lze tedy spočítat jako rozdíl tepového objemu stanoveného v aortě a v plícnici [6]. Dopředný aortální průtok je součinem systolického rychlostního integrálu a průřezové plochy v aortě, analogicky pak v plícnici změříme skutečný tepový objem.
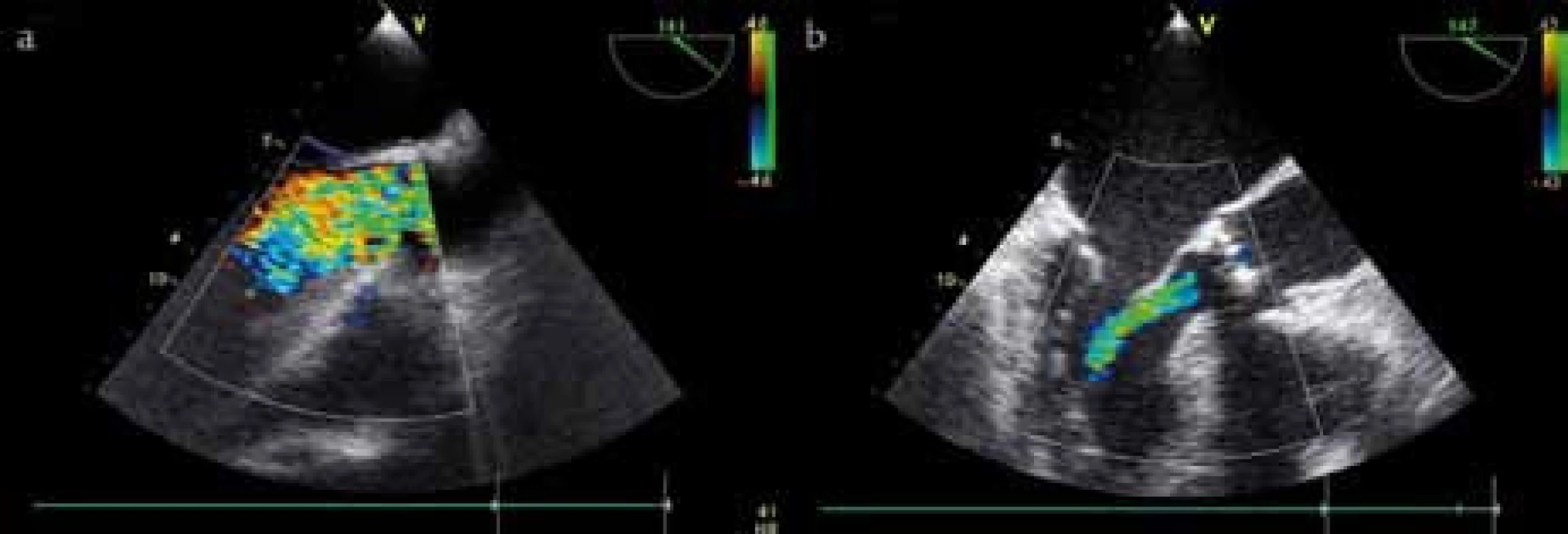
![Kvantifikace významnosti chronické aortální regurgitace (podle [5]).](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/1c0070c7b38f56481fcf3d1da3a44991.png)
Průtoková křivka na začátku descendentní aorty vykazuje normálně pouze systolické proudění. U AR však lze detekovat i reverzní diastolické proudění, jehož rozsah závisí na tíži vady (holodiastolické proudění, zejména v břišní aortě, svědčí pro významnou vadu). Pomocí metody PISA (Proximal Isovelocity Surface Area) lze stanovit plochu efektivního regurgitačního ústí – ERO, u závažnějších regurgitací přesahuje 0,3 cm2. Ostatní parametry pro posouzení AR jsou zachyceny v tab. 2, v zájmu přesnější kvantifikace AR by se mělo kombinovat vždy více parametrů současně.
Echokardiografie dvourozměrná umožní přesně popsat zodpovědnou patologii aortální chlopně nebo vzestupné aorty, detailně lze posoudit stupeň excentrické hypertrofie levé komory a její funkce. Ejekční frakce bývá pro objemové přetížení levé komory obvykle zvýšená, u déletrvající vady se však snižuje.
Sledování nemocných s lehčí až středně těžkou vadou se doporučuje jednou ročně, u těžkých vad – pokud se neoperují – je tento interval 6 měsíců (ESC).
Zátěžové echokardiografické vyšetření s nízkou dávkou dobutaminu lze užít k zhodnocení kontraktilní rezervy u pokročilých AR s těžkou dysfunkcí levé komory [5], zátěžové echo na sklopném ergometru používáme spíše k objektivizaci symptomů a zhodnocení kondice pacientů.
RTG odhalí aortální konfiguraci srdce (zaoblení levé hranice a prohloubení zářezu v levém kardiofrenickém úhlu), rozšíření srdečního stínu doleva (není u akutních), případně dilataci aorty a městnání na plicích.
CT vyšetření s kontrastem je výhodné k zobrazení anatomie hrudní aorty (šíře, struktura, odstupy velkých cév) především tam, kde se uvažuje o výkonu na hrudní aortě a kde není situace zcela jasná z echokardiografie a/nebo aortografie.
Katetrizace se provádí obvykle u nemocných starších 40 (event. 45) let, kdy je nutno koronarograficky vyloučit ICHS, u mladších pak tam, kde je podezření na ICHS z hlediska anamnézy, kumulace rizikových faktorů apod. Katetrizace srdeční oboustranná je indikována tam, kde je patrný rozpor mezi klinickými a echokardiografickými daty ve smyslu významnosti AR či jiných konkomitujících vad i u podezření na plicní hypertenzi [3,5]. Nachází se při ní obvykle vyšší enddiastolický tlak v levé komoře (zejména se to však týká akutních regurgitací), vyrovnaný tlak v aortě a levé komoře na konci diastoly (aortální chlopeň „netěsní“), může být přítomen i menší systolický tlakový gradient (do 25 mm Hg), který je dán vyšším tepovým objemem, a tím vyšším množstvím krve proudící přes aortální ústí [3]. S pomocí aortografie lze kvantifikovat regurgitaci do 4 stupňů (tab. 3). Lze spočítat i regurgitační frakci (RF) podle vzorce

Podle tohoto vzorce lze kvantifikovat AR na těžkou (RF > 55 %), střední (20–55 %) a lehkou (RF < 20 %), toto stanovení je však složité a nepřesné, především pro nutnost výpočtu jednotlivých parametrů z různých metod (SVangio = tepový objem stanovený angiograficky, SVefekt = efektivní tepový objem zjištěný Fickovou metodou či dilučně).
Pravostranná katetrizace je vhodná před plánovanou operací u pokročilých AR s dysfunkcí levé komory nebo u kombinovaných vad s těžší plicní hypertenzí [5].
Průběh a prognóza
Prognózu u AR určují symptomy, velikost a funkce levé komory. Asymptomatická AR s normální funkcí má prognózu velmi dobrou, jakmile se však objeví symptomy, mortalita pacientů prudce narůstá. Rozvoj symptomů zvyšuje riziko náhlé smrti na 10 %/rok, rozvoj dysfunkce levé komory až na 20 % [5,7]. Kromě symptomů a funkce levé komory je velikost levé komory třetím parametrem ovlivňujícím prognózu. Týká se to endsystolického rozměru, jehož zvýšení nad 50 mm zvyšuje riziko symptomů, úmrtí a dysfunkce levé komory na 19 % za rok, u endsystolického rozměru v pásmu 40–50 mm činí toto riziko 6 %, pod 40 mm je zanedbatelné [5,8].
Pokud jde o šíři vzestupné aorty, nejjednoznačnější jsou data u Marfanova syndromu. Úmrtí závisí na rozměru aortálního kořene a rodinné anamnéze náhlých kardiovaskulárních příhod (disekce aorty, náhlá smrt) [9].
Léčba aortální insuficience
Medikamentózní terapie nemá u AR smysl, může sloužit nanejvýše ke zlepšení stavu nemocných se srdečním selháváním před operací. Od podávání vazodilatancií, dříve doporučované, si lze nanejvýše slibovat snížení hodnot krevního tlaku u systolické hypertenze, na progresi vady samotné však nemá žádný vliv. Smysl má pouze kardiochirurgická léčba, vazodilatancia (zvláště inhibitory ACE) se mohou použít u nemocných, u nichž nelze operaci provést. Beta-blokátory se doporučují u nemocných s Marfanovým syndromem (zpomalení rozvoje dilatace aorty, snížení rizika různých komplikací, jejich podávání se doporučuje před operací i po ní) [9,10], jejich negativně chronotropní efekt s výraznějším zpomalením srdeční frekvence však není výhodný a u velmi těžkých AR by se spíše užívat neměla (zvětšení regurgitační frakce po zpomalení srdeční akce). Podávání blokátorů vápníkového kanálu u nemocných s AR jindy než u konkomitující hypertenze se pokládá za neprokázané [12]. U AR by měla být prováděna antibiotická profylaxe infekční endokarditidy podle doporučených zásad [13].
Kardiochirurgický zákrok spočívá nejčastěji v náhradě aortální chlopně. V posledních 20 letech však byly vyvinuty techniky korekce nativní chlopně, které se užívají u více než 15 % operovaných AR – volí se zejména u postižení aortálního kořene při zachovalých cípech, zvláště u mladých pacientů s bikuspidální aortální chlopní, prolapsem nebo perforací chlopně [12]. Pokud je současně přítomno i aneuryzma aortálního kořene (obr. 2), provádí se obvykle i náhrada vzestupné aorty spojená s reimplantací koronárních tepen (Bentallova operace). Operovat je nutno i další závažné přidružené abnormality, např. aneuryzma Valsalvova sinu (obr. 3). V úvahu přichází i Rossova operace, kdy se aortální chlopeň nahradí chlopní pulmonální a místo ní se pak všije homograft (používá se spíše u dětí, u dospělých však zcela výjimečně).
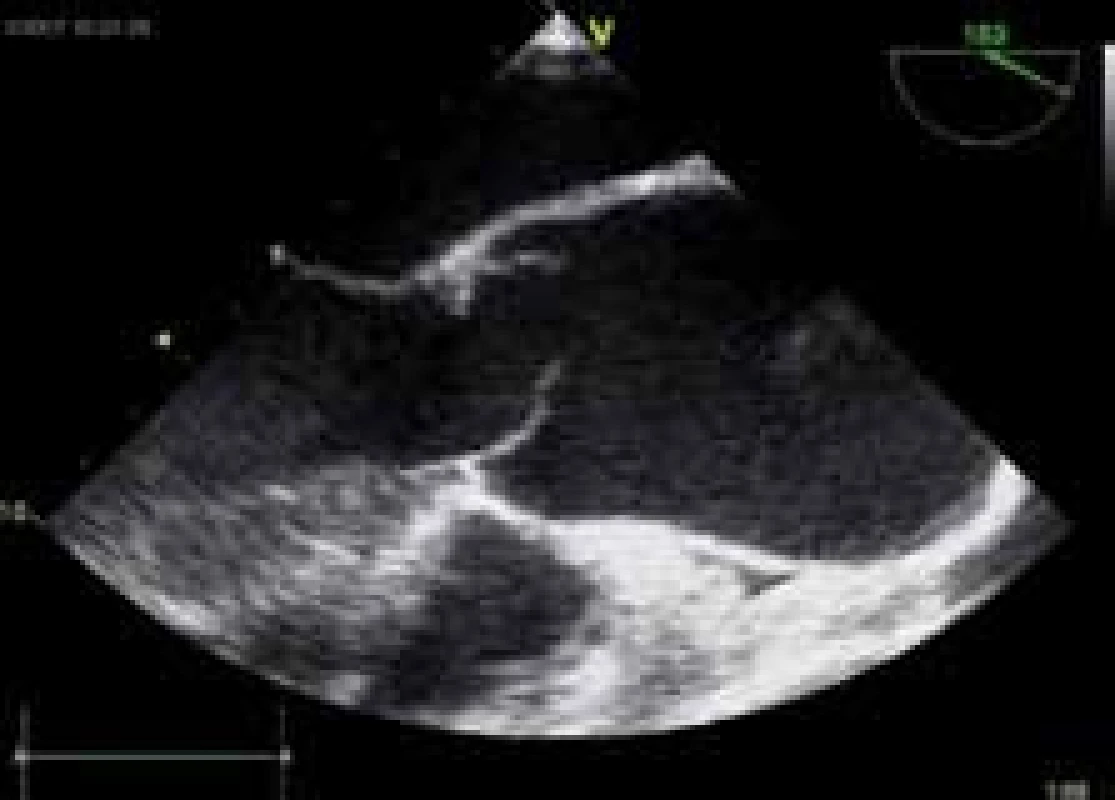
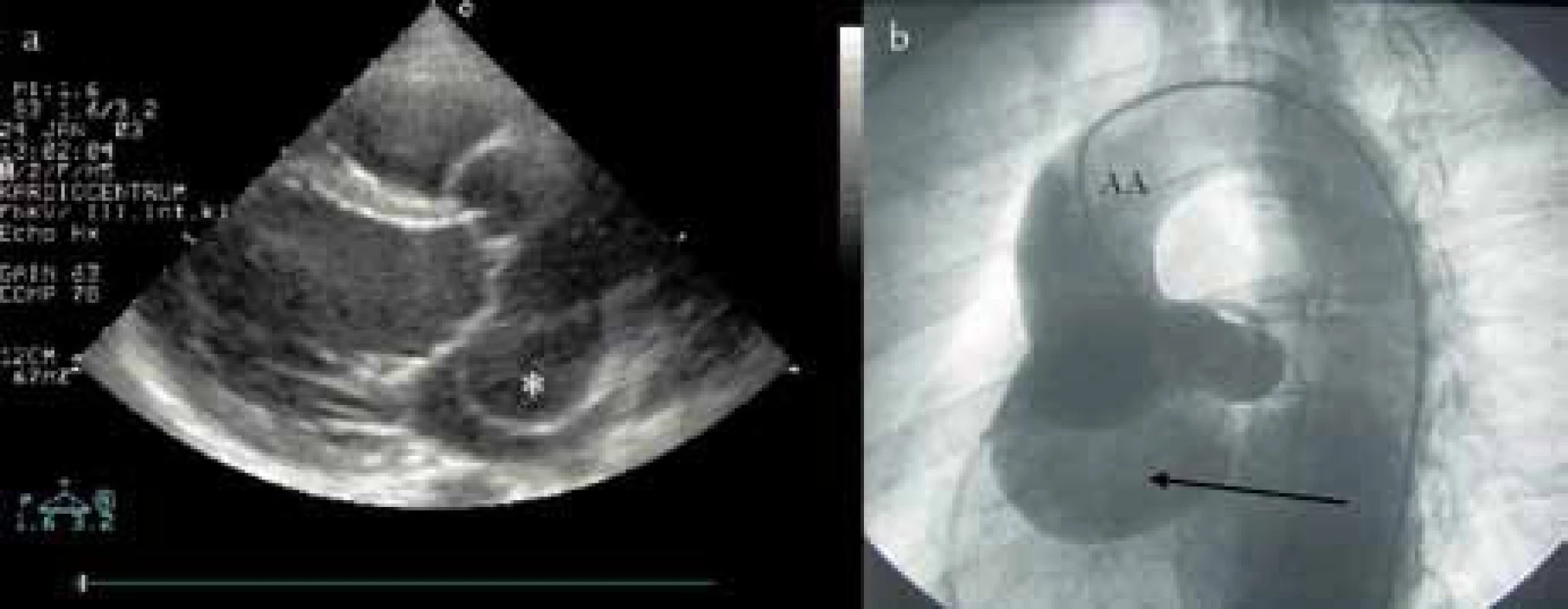
K operaci indikujeme všechny symptomatické nemocné (od NYHA II) s významnou AR (tab. 4). U asymptomatických s těžkou AR volíme operaci při klidové dysfunkci levé komory (EF < 50 %) nebo při poklesu ejekční frakce při zátěži, dále u dilatace levé komory při indexu endsystolického rozměru nad 25 mm/m2 a enddiastolického nad 35 mm/m2 (v doporučeních ČKS se jednoznačně preferuje používání indexovaných rozměrů) [5]. Tato čísla se však v doporučeních jiných států mohou lišit [7]. Pokud je stupeň významnosti AR pouze střední, náhrada chlopně je vždy indikována při nutnosti současného aortokoronárního bypassu nebo přítomnosti jiné vady, která vyžaduje kardiochirurgický zákrok (tab. 4). Zásadním nálezem indikujícím náhradu třeba i u jen středně závažné AR je přítomnost dilatované ascendentní aorty (u trojcípé chlopně > 55 mm, u dvojcípé > 50 mm, u Marfanova syndromu > 45 mm) – zjednodušeně lze spolu s hodnocením ejekční frakce a velikosti endsystolického průměru levé komory použít princip „50“.
![Indikace ke kardiochirurgické léčbě AR (upraveno podle [5]).](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/be8b04be524b4d98e1fcdb18b72df07b.png)
Prognóza operace izolované aortální chlopně je velmi dobrá – mortalita je zhruba v pásmu 2–4 %, při současném aortokoronárním bypassu vzroste na 4–7 % [10,12], zvyšuje se dále podstatně u starých nemocných, kombinovaných výkonů, u nemocných s poruchou funkce levé komory a její dilatací. U pacientů s EF < 30 % a/nebo s dilatací levé komory může perioperační mortalita vzrůst na 10–15 % [7]. Také sledování v delším časovém horizontu od operace vykazuje v těchto případech neuspokojivé výsledky, výraznější pooperační zlepšení funkce levé komory nelze očekávat, zejména pokud jde k tomu ještě o velmi těžce symptomatické nemocné (NYHA IV), kdy se prognóza výkonu dále zhoršuje [3]. Také dlouhodobá prognóza operovaných žen s AR je horší než u mužů [10], což je zřejmě dáno indikačními kritérii velikosti levé komory stejné pro obě pohlaví.
Akutní AR
Dosud jsme pojednávali pouze o chronické AR. Akutní AR (tab. 5) představuje onemocnění, které se od chronické podstatně liší, je poměrně vzácná. Jde o urgentní stav projevující se dušností až obrazem plicního edému, často i známkami nízkého srdečního výdeje až kardiogenním šokem.
V echokardiografickém obraze chybí dilatace levé komory, mohou být známky plicní hypertenze. Bývá patrný i předčasný uzávěr mitrální chlopně (rychlý nárůst tlaku v levé komoře během časné diastoly uzavře dříve mitrální chlopeň). Pokud není jasná etiologie z transtorakální echokardiografie, je na místě provedení jícnového vyšetření, event. CT (zcela suverénní je v diagnóze disekce). Katetrizaci srdeční obvykle neprovádíme (zvláště ne u urgentních stavů s těžkým průběhem), nemocného co nejdříve indikujeme k operaci. Balónková kontrapulzace je kontraindikována (zhoršení regurgitace), do doby operace lze podat u těžkých stavů vazodilatancia (nitráty i.v.), příp. inotropika podle stavu.
Nejčastější příčinou akutní AR je endokarditida s perforací či rupturou cípu, akutní disekce aorty (obr. 4) či akutní dysfunkce chlopenní protézy, ať už na podkladě endokarditidy, trombózy či dehiscence náhrady. AR při endokarditidě vzniká v důsledku destrukce cípů nebo v souvislosti se vznikem paravalvulárního abscesu. AR při akutní disekci aorty vzniká v souvislosti s dilatací aortálního prstence nebo pokračováním disekce na oblast aortálních cípů (obr. 4).
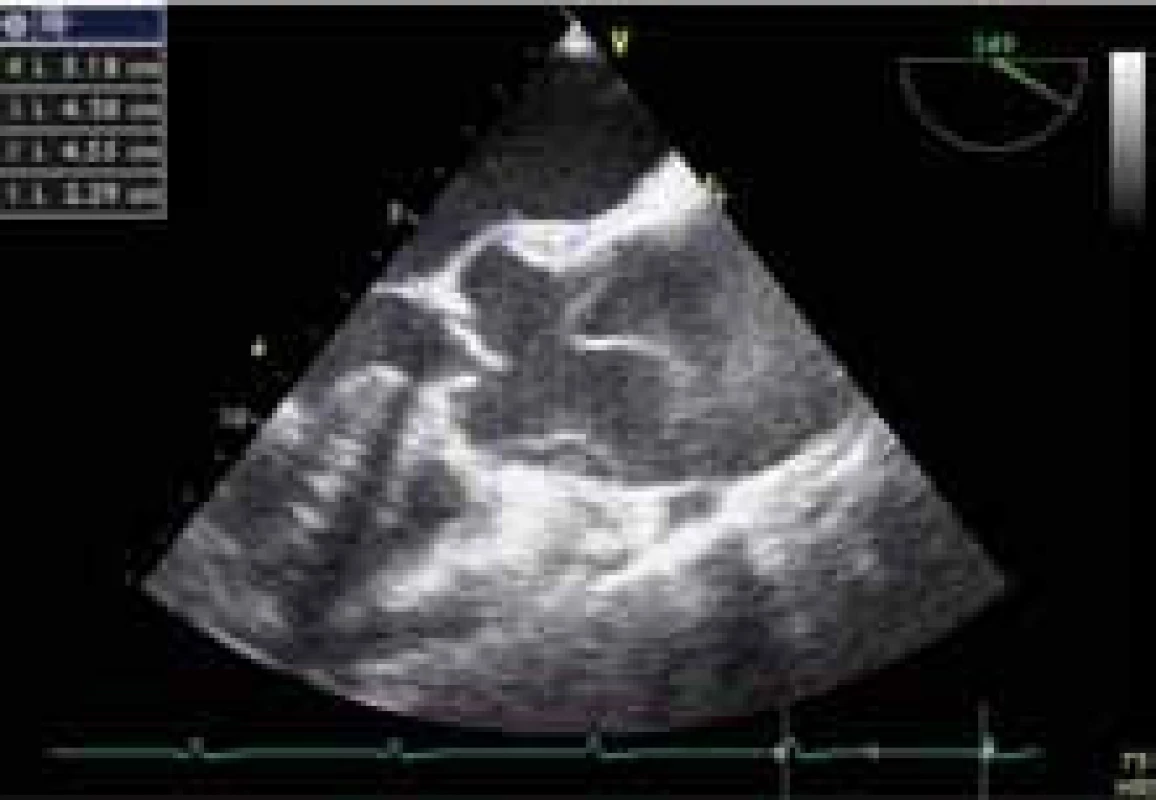
Při akutně vzniklé AR se vrací objem krve v diastole do levé komory nepřipravené na stávající situaci, což vede k akutnímu vzestupu enddiastolického tlaku v levé komoře (LVEDP), jehož důsledkem je vznik plicního edému. Protože k výše uvedenému stavu dochází náhle, levá komora není schopna se stávající situaci přizpůsobit kompenzatorní dilatací, současně v důsledku nízkého dopředného srdečního výdeje může dojít k rozvoji kardiogenního šoku. Srdeční výdej může ještě dále zhoršovat předčasné uzavírání mitrální chlopně, ke kterému dochází v souvislosti s akutními hemodynamickými změnami, a sice v důsledku zřetelně zvýšeného diastolického tlaku v levé komoře. Předčasný uzávěr mitrální chlopně do jisté míry chrání plicní řečiště před vysokým LVEDP, na druhou stranu společně s tachykardií vede k sníženému mitrálnímu přítoku, který se dále podílí na snížení plnění komory. Navíc snížený perfuzní tlak v koronárních tepnách může vést ke vzniku difuzní subendokardiální ischemie, která ještě zhoršuje funkci levé komory. Pokud měl pacient již v předchorobí AR a dilatovanou levou komoru, může být hemodynamický důsledek akutně zhoršené regurgitace méně závažný. U pacientů se zhoršenou diastolickou funkcí levé komory (např. v důsledku hypertenze či u pacientů s aortální stenózou) je naopak hemodynamický důsledek akutně vzniklé AR výrazně dramatičtější [14–16].
Pacienti s akutní AR jsou často v kritickém stavu a mezi symptomy patří rozvoj dušnosti, hemodynamická nestabilita a příznaky šokového stavu, slabost či alterace vědomí. Příznaky jsou dále dány etiologií vady, u pacientů s disekcí aorty krutými bolestmi na hrudi či mezi lopatkami, u pacientů s endokarditidou febrilním stavem. Klinická diagnóza akutní AR je oproti chronické AR značně rozdílná (tab. 5). Pro akutní AR je charakteristický slabý časně diastolický šelest nad aortou (někdy nemusí být vůbec patrný), což může vést při klinickém vyšetření k mylné diagnóze. Pulzový tlak je nízký díky nízkému srdečnímu výdeji a periferní symptomy, které mohou být vidět u chronické regurgitace, nejsou u akutní vyjádřeny.
Rozhodující význam v diagnóze má echokardiografie, která stanoví mechanizmus vzniku a hemodynamické parametry. Přítomnost významné AR a normální velikost levostranných srdečních oddílů by měla vést k podezření na akutní AR, stejně jako normální funkce levé komory. Kvantitativní měření významnosti regurgitace není u akutní AR tak užitečné jako u chronické. Měření efektivního regurgitačního ústí a regurgitačního objemu může být vzhledem k tachykardii nepřesné a závislé na afterloadu a plnění levé komory.
Barevné dopplerovské mapování může významnost vady podhodnotit u excentrických jetů.
Významný přínos v přesném stanovení diagnózy má jícnová echokardiografie, je často nezastupitelná při stanovení významnosti a především mechanizmu vzniku regurgitace, dále při hodnocení dysfunkce chlopenní náhrady a zvláště v případě stanovení diagnózy disekce aorty jako příčiny AR (obr. 4). Katetrizace se standardně neprovádí u pacientů s disekcí aorty, u těchto pacientů je suverénní metodou ke stanovení diagnózy CT hrudní aorty.
Léčba akutní AR je chirurgická. Předoperačně je v případě respirační nedostatečnosti v důsledku srdečního selhávání nutná ventilační podpora a hemodynamické monitorování pacientů. Medikamentózní léčba by měla podle aktuálního stavu zahrnovat diuretika, inotropní podporu a vazodilatační léčbu ke stabilizaci hemodynamického stavu. V případě infekční endokarditidy jako příčiny AR je nutná i.v. antibiotická léčba, a pokud jsou pacienti relativně stabilní, snažíme se alespoň o odložení výkonu o 1–2 týdny za i.v. léčby antibiotiky. Intraaortální balónková kontrapulzace je kontraindikována, protože zvyšuje regurgitující objem přes aortální chlopeň. Také beta-blokátory nejsou v léčbě vhodné, neboť v důsledku prodloužení diastoly dochází ke zvětšení regurgitujícího objemu. U pacientů s akutní AR vzniklou v souvislosti s disekcí aorty je nutné emergentní kardiochirurgické řešení.
Závěr
Chronická aortální regurgitace je onemocnění, které dlouho probíhá asymptomaticky, a proto může dojít ke špatnému načasování chirurgického řešení. Na základě dostupných poznatků a současných doporučení jsou k chirurgickému řešení významné aortální regurgitace indikováni symptomatičtí pacienti nebo asymptomatiční nemocní s progresí velikosti levé komory srdeční nebo poklesu ejekční frakce. Operováni by tedy měli být pacienti, u kterých je systolická velikost levé komory srdeční ≥ 50 mm nebo 25 m/m2 nebo pokud je ejekční frakce levé komory < 50 %. Pečlivé klinické a echokardiografické hodnocení jsou proto nezbytné. Zcela jiná situace je u akutní aortální regurgitace, kde by měla být náhrada aortální chlopně provedena ihned po stabilizaci stavu, v některých situacích emergentně.
prof. MUDr. Pavel Gregor, DrSc.
www.fnkv.cz
e-mail: pavel.gregor@fnkv.cz
Doručeno do redakce: 22. 11. 2012
Přijato po recenzi: 2. 1. 2013
Sources
1. Widimský J. Insuficience aorty. In: Kordač V et al. Vnitřní lékařství I. Praha, Avicenum 1988, 560–563.
2. Čerbák R. Nejčastější chlopenní vady: aortální stenóza a mitrální insuficience. Praha, Galén 2007, 188 s.
3. Veselka J, Honěk T, Špatenka J et al. Získané chlopenní vady srdce. Praha, Medcor 2000, 59–84.
4. Gregor P, Widimský P et al. Kardiologie. Praha, Galén 1999, 595 s.
5. Popelová J, Benešová M, Brtko M et al. Doporučené postupy pro diagnostiku a léčbu chlopenních srdečních vad v dospělosti. Guidelines ČKS. CorVasa 2007; 49: K195–K234.
6. Niederle P et al. Echokardiografie. Praha, Triton 2002, 359 s.
7. Bonow RO, Carabello BA, Chatterjee K et al. ACC/AHA 2006 guidelines for the management of patients with valvular heart disease. J Am Coll Cardiol 2006; 48 : 1–148.
8. Bonow RO, Lakatos E, Maron BJ et al. Serial long-term assessment of the natural history of asymptomatic patients with chronic aortic regurgitation and normal left ventricular systolic function. Circulation 1991; 84 : 1625–1635.
9. Judge DP, Dietz HC. Marfan´s syndrome. Lancet 2005; 366 : 1965–1976.
10. Vahanian A, Alfieri O, Andreotti F et al. Guidelines on the management of valvular heart disease (Version 2012). The Joint Task Force on the Management of Valvular Heart Disease of the European Society of Cardiology and the European Association for Cardio-Thoracic Surgery. Eur Heart J 2012; 33 : 2451–2496.
11. Evangelista A, Roznos P, Symboly A et al. Long-term vasodilator therapy in pacients with severe aortic regurgitation. N Engl J Med 2005; 353 : 1342–1349.
12. Camm AJ, Lüscher TF, Serruys PW. The ESC Textbook of Cardiovascular Medicine. European Society of Cardiology, Blackwell Publishing 2006, 1122 s.
13. Beneš J, Gregor P, Mokráček A Infekční endokarditida: doporučené postupy diagnostiky a léčby, dispenzarizace a profylaxe. Cor Vasa 2007; 49: K157–K171.
14. Kaplan JA, Reich DL, Lake CL et al. Valvular Heart Disease: Replacement and Repair In: Kaplan’s Cardiac Anesthesia. Philadelphia, Saunders Elsevier, 2006, 645–691.
15. Fink MP, Abraham E, Vincent JL et al. Emergent Valvular Disorders In: Textbook of Critical Care. Philadelphia: Saunders Elsevier, 2005, 861–871.
16. Stout KK, Verrier ED. Acute Valvular Regurgitation. Circulation 2009; 119 : 3232–3241.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2013 Issue 2
-
All articles in this issue
- Current trends in treatment and follow-up of patients with differentiated thyroid carcinoma – experience with the use of recombinant human thyrotropin
- Practice guideline and trends for immunosuppressive treatment of glomerulonephritides according to KDIGO (Clinical Practice Guideline for Glomerulonephritis)
- Syncope as first and only sign of left atrial myxoma
- Heart transplantation and the subsequent treatment of AL amyloidosis
- Opinion of the Czech Atherosclerosis Society‘s committee (CSAT) on the ESC/EAS guidlines related to the diagnostics and treatment of dyslipidemias issued in 2011
- Aortic regurgitation
- Ischemic peripheral arterial disease and recurrent iliofemoral venous thrombosis in a 24-year-old man with antiphospholipid syndrome
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Aortic regurgitation
- Practice guideline and trends for immunosuppressive treatment of glomerulonephritides according to KDIGO (Clinical Practice Guideline for Glomerulonephritis)
- Current trends in treatment and follow-up of patients with differentiated thyroid carcinoma – experience with the use of recombinant human thyrotropin
- Heart transplantation and the subsequent treatment of AL amyloidosis

