Manažment hyperlipidémie na Slovensku: observačná štúdia
Hyperlipidemia management in Slovakia: observational study
Aim: A multicountry observational study was conducted to gain insight into the current management of elevated low density lipoprotein cholesterol (LDL-C) in high-risk (HR) and very high-risk (VHR) patients with hyperlipidaemia across central and eastern Europe and Israel. Here we present data from the Slovakian subpopulation.
Methods: We enrolled adult patients who were receiving lipid-lowering therapy (LLT) and attending a specialist (cardiologist/diabetologist/internist) for a routine visit at 9 sites (including academic/specialist centers) across Slovakia. Data were collected retrospectively from patients’ records for the 12 months preceding enrolment.
Results: 150 patients, mean (range) age 62.8 (26–84) years were enrolled, including 24 with familial hypercholesterolemia and 109 secondary prevention patients. Almost all patients (147; 98.0 %) were receiving statins, as monotherapy (114; 76.0 %) or in combination with other LLT (33; 22.0 %): 11 (7.3 %) were classified as having statin intolerance symptoms. Mean LDL-C levels were 3.0 (1.1–7.1) mmol/l at the first, and 2.6 (0.7–7.7) mmol/l at the last, visit of the observation period. Only 2/16 (12.5 %; 95 % CI 1.6–38.4 %) HR patients and 40/134 (29.9 %; 22.3–38.4 %) VHR patients achieved their recommended LDL-C targets of < 2.5 and < 1.8 mmol/l, respectively, during observation. In the FH subset 2/15 (13.3 %; 1.7–40.5 %) HR and 2/9 (22.2 %; 2.8–60.0 %) VHR patients achieved these targets. In patients with definite/probable FH (Dutch Lipid Clinic Network score ≥ 6), these targets were attained by 2/15 (13.3 %; 1.7–40.5) HR patients and 0/6 VHR patients. A total of 41 patients (27.3 %) experienced CV events (≤ 3) during the 12-month observation period.
Conclusion: Our findings provide a picture of patients treated for hyperlipidemia across Slovakia. We found that, despite widespread statin use, a substantial proportion of patients, particularly those with FH, are undertreated and fail to achieve the LDL-C targets recommended in European guidelines. They consequently remain at excess risk of cardiovascular events.
Keywords:
cardiovascular events – dyslipidemias – familial hypercholesterolemia – low-density lipoprotein cholesterol
Authors:
Ľubomíra Fábryová 1,2; Alena Nemcová 3
Authors‘ workplace:
MetabolKLINIK, s. r. o., Ambulancia pre diabetológiu, poruchy látkovej premeny a výživy, Špecializovaná lipidologická ambulancia, MED PED centrum, Bratislava, Slovenská republika
1; Biomedicínske centrum SAV, Bratislava, Slovenská republika
2; Amgen Slovakia, s. r. o., Bratislava, Slovenská republika
3
Published in:
Vnitř Lék 2019; 65(12): 761-769
Category:
Original Contributions
Overview
Cieľ: Medzinárodná observačná štúdia sa uskutočnila s cieľom získať prehľad o súčasnom manažmente zvýšenej hladiny cholesterolu prenášaného lipoproteínmi s nízkou hustotou (LDL-C) u vysoko rizikových (high-risk – HR) a veľmi vysoko rizikových (very high-risk – VHR) pacientov s hyperlipidémiou naprieč strednou, východnou Európou a v Izraeli. V tomto príspevku prezentujeme údaje týkajúce sa slovenskej subpopulácie.
Metódy: Do štúdie sme zaradili dospelých pacientov, ktorí dostávali hypolipidemickú liečbu (lipid-lowering therapy – LLT) a chodili na bežné kontroly k špecialistom (kardiológ/diabetológ/internista) z 9 pracovísk zapojených do štúdie (vrátane univerzitných/špecializovaných centier) na Slovensku. Údaje boli zozbierané retrospektívne zo zdravotných záznamov pacientov a pokrývali obdobie 12 mesiacov pred zaradením do štúdie.
Výsledky: Zaradených bolo 150 pacientov, priemerný (rozmedzie) vek 62,8 (2684) roka, medzi ktorými bolo 24 pacientov s familiárnou hypercholesterolémiou a 109 pacientov liečených v rámci sekundárnej prevencie. Takmer všetci pacienti (147; 98,0 %) dostávali statíny buď v monoterapii (114; 76,0 %), alebo v kombinácii s inou LLT (33; 22,0 %): u 11 (7,3 %) pacientov sa zistila prítomnosť príznakov intolerancie statínov. Priemerná hladina LDL-C bola 3,0 (1,17,1) mmol/l na prvej návšteve a 2,6 (0,77,7) mmol/l na poslednej návšteve zahrnutej do obdobia sledovania. Iba 2 zo 16 HR pacientov (12,5 %; 95% interval spoľahlivosti -IS: 1,638,4 %) a 40 zo 134 VHR pacientov (29,9 %; 95% IS: 22,338,4 %) dosiahli odporúčané cieľové hodnoty LDL-C < 2,5 mmol/l (HR pacienti) a < 1,8 mmol/l (VHR pacienti) počas obdobia sledovania. V podskupine pacientov s FH dosiahli tieto cieľové hodnoty 2 z 15 HR pacientov (13,3 %; 95% IS: 1,740,5 %) a 2 z 9 VHR pacientov (22,2 %; 95% IS: 2,860,0 %). V prípade pacientov s jednoznačnou/pravdepodobnou FH (skóre ≥ 6 podľa Dutch Lipid Clinic Network) dosiahli tieto cieľové hodnoty 2 z 15 HR pacientov (13,3 %; 95% IS: 1,740,5 %) a 0 zo 6 VHR pacientov. Počas 12mesačného obdobia sledovania sa kardiovaskulárne príhody (≤ 3) vyskytli celkovo u 41 pacientov (27,3 %).
Záver: Naše zistenia poskytujú obraz toho, ako sú pacienti liečení na hyperlipidémiu na Slovensku. Zistili sme, že napriek rozšírenému používaniu statínov je značný podiel pacientov „podliečený“ (najmä pacienti s FH) a nedosahuje cieľové hodnoty LDL-C odporúčané v európskych odborných odporúčaniach. V dôsledku toho sú aj naďalej vystavení zvýšenému riziku kardiovaskulárnych príhod.
Klíčová slova:
dyslipidemie – familiárna hypercholesterolémia – cholesterol prenášaný lipoproteínmi s nízkou hustotou – kardiovaskulárne príhody
Úvod
Znižovanie zvýšenej hladiny cholesterolu prenášaného lipoproteínmi s nízkou hustotou (LDL-C) je základným pilierom prevencie vzniku kardiovaskulárnych ochorení podmienených aterosklerózou (ASCVD) [1–3], ktoré sú najčastejšou príčinou smrti a invalidity v rozvinutom svete [4]. Statíny sú liečbou prvej línie v primárnej a sekundárnej prevencii už niekoľko dekád, pričom štandardné statínové režimy (napr. 20–40 mg simvastatínu denne) zvyčajne znižujú hladinu LDL-C približne o tretinu a vysoko intenzívne režimy (napr. 40–80 mg atorvastatínu alebo 10–20 mg rosuvastatínu denne) potenciálne znižujú hladinu LDL-C o 50 % [5]. Dôkazy vysokej kvality potvrdili, že každé zníženie hladiny LDL-C o asi 1 mmol/l znižuje 5-ročné riziko závažných cievnych príhod (úmrtie z koronárnych príčin, nefatálny infarkt myokardu, koronárna revaskularizácia alebo cievna mozgová príhoda) približne o jednu pätinu [6].
V odporúčaniach Európskej kardiologickej spoločnosti/Európskej spoločnosti pre aterosklerózu (European Society of Cardiology/European Atherosclerosis Society, ESC/EAS) [7–9] sú stanovené jasné cieľové hodnoty LDL-C pre pacientov s hyperlipidémiou podľa kategórie kardiovaskulárneho (KV) rizika. V roku 2011 bola cieľová hodnota LDL-C < 2,5 mmol/l odporúčaná pre vysoko rizikových (high-risk – HR) a < 1,8 mmol/l pre veľmi vysoko rizikových (very high-risk – VHR) pacientov [7], pričom v roku 2016 bola cieľová hodnota pre HR pacientov pozmenená na < 2,6 mmol/l [8]. V roku 2019 boli publikované nové odporúčania, ktoré definujú cieľovú hladinu LDL-C < 1,8 mmol/l pre vysoko rizikových pacientov a < 1,4 mmol/l v prípade veľmi vysoko rizikových pacientov [9]. Údaje z početných observačných štúdií a prieskumov však konzistentne preukazujú, že značný podiel pacientov tieto cieľové hodnoty nedosahuje [10–13].
Retrospektívna/prospektívna observačná štúdia sa uskutočnila s cieľom preskúmať manažment hyperlipidémie a dosahovanie cieľových hodnôt LDL-C naprieč krajinami strednej, východnej Európy a v Izraeli [14]. V mnohých krajinách v regióne sú k dispozícii obmedzené údaje o používaní hypolipidemickej liečby (lipid-lowering therapy – LLT) a o kontrole hladín lipidov kvôli nedostatočnému počtu pacientskych registrov a nedostatočnému prístupu k verejným informáciám a k údajom zdravotných poisťovní. V tomto príspevku prezentujeme výsledky štúdie týkajúce sa subpopulácie pacientov zaradených na Slovensku.
Metódy
Regionálna štúdia bola retrospektívna/prospektívna neintervenčná, observačná štúdia, do ktorej boli zaradení pacienti s diagnostikovanou hyperlipidémiou (HR alebo VHR, ako je definované v odporúčaniach ESC/EAS) [7], ktorí dostávali LLT a chodili na bežné kontroly k špecialistovi (kardiológ, diabetológ a/alebo internista) [14]. (Interné ambulancie boli zahrnuté ako centrá iba v Českej republike a Slovenskej republike, nakoľko dispenzarizujú pacientov indikovaných pre LLT liečbu).
Pacienti, ktorí podstupovali liečbu hyperlipidémie v rámci intervenčného klinického skúšania, boli z účasti na štúdii vylúčení. Údaje boli získané zo zdravotných záznamov jednotlivých pacientov a týkali sa obdobia 12 mesiacov pred zaradením do štúdie (retrospektívna fáza: všetky krajiny) a až 6 mesiacov po zaradení do štúdie (prospektívna fáza: iba Rumunsko, Poľsko a Česká republika). Pacienti museli mať zaznamenané aspoň 2 hodnoty LDL-C a riadne zdokumentovanú LLT (typ lieku a dávka). Všetci pacienti poskytli písomný informovaný súhlas.
Ciele
Primárnym cieľom štúdie bolo určiť percento pacientov, ktorí dosiahli hladiny LDL-C < 2,5 mmol/l a < 1,8 mmol/l, čo boli cieľové hodnoty v tom čase definované ESC/EAS pre HR a VHR pacientov v uvedenom poradí [7]. Do našej analýzy bola zahrnutá aj aktualizovaná cieľová hodnota < 2,6 mmol/l pre HR pacientov z roku 2016 [8]. Sekundárne ciele zahŕňali: absolútne hladiny LDL-C; používanie statínov a inej LLT (typ, dávka, frekvencia podávania) v priebehu času; KV príhody, klinické charakteristiky (demografické údaje, zdravotná anamnéza zahŕňajúca diagnózu familiárnej hypercholesterolémie – FH a KV príhody, príznaky intolerancie statínov, hospitalizácie pre KV ochorenia) a parametre klinického manažmentu pacientov. KV príhody zahŕňali ischemickú chorobu srdca (nestabilná angina pectoris/infarkt myokardu/náhle úmrtie z kardiálnych príčin), cerebrovaskulárne ochorenie (tranzitórna ischemická príhoda/cievna mozgová príhoda), ochorenie periférnych artérií (intermitentná klaudikácia/pokojová ischemická bolesť/gangréna), aneuryzmu brušnej aorty, fibriláciu predsiení, srdcové zlyhávanie alebo koronárnu revaskularizáciu. Formálna hypotéza nebola testovaná.
Veľkosť skúmanej vzorky
Plánované bolo zaradiť celkovo 80–150 osôb na každú participujúcu krajinu. Tento počet vychádzal z predpokladu, že 50 % osôb dosiahne primárny cieľový ukazovateľ (dosiahnutie cieľových hodnôt LDL-C podľa ESC/EAS) a umožní odhadnutie percenta s 95% intervalom spoľahlivosti (IS) s polovičnou šírkou medzi 11,0 % (80 pacientov) a 8,0 % (150 pacientov).
Analýza údajov
Prezentovaná je iba sumárna štatistika: pre kategorické premenné (frekvencia a percento v kategórii, s 95% IS) a kontinuálne premenné (počet osôb, priemer, medián, štandardná odchýlka alebo štandardná chyba, interkvartilové rozpätie, minimum a maximum). Imputácia chýbajúcich údajov nebola vykonaná. Hladiny LDL-C boli analyzované v podskupinách pacientov vytvorených podľa nasledovných kategórií: FH, sekundárna prevencia, diabetes mellitus, STEMI (infarkt myokardu s eleváciou segmentu ST) a intolerancia statínov (prítomnosť nežiaducich udalostí prisudzovaných statínovej liečbe).
Výsledky
Skúmaná populácia
Medzi augustom roku 2016 a januárom roku 2017 bolo na 9 slovenských pracoviskách zapojených do štúdie zaradených celkovo 150 pacientov s priemerným (rozmedzie) vekom 62,8 (2684) roka. Charakteristiky pacientov sú zhrnuté v tab. 1 a rizikové faktory životného štýlu sú uvedené v tab. 2. Zaradených bolo 24 (16,0 %) pacientov s FH; 62 (41,3 %) pacientov s diabetes mellitus (DM); 31 (20,7 %) pacientov so STEMI a 109 (72,7 %) pacientov dostávalo LLT v rámci sekundárnej prevencie: 16 (10,7 %) pacientov bolo klasifikovaných ako HR a 134 (89,3 %) ako VHR podľa definície v odporúčaniach ESC/EAS [7]. 94 (62,7 %) pacientov malo dlhotrvajúcu hyperlipidémiu (≥ 5 rokov). Takmer všetci pacienti (21 z 24 pacientov; 87,5 %), u ktorých bola udávaná FH, mali pravdepodobnú/jednoznačnú FH (skóre ≥ 6) podľa kritérií Dutch Lipid Clinic Network (DLCN) [15]. U celkovo 11 (7,3 %) pacientov bola udávaná prítomnosť príznakov intolerancie statínov.
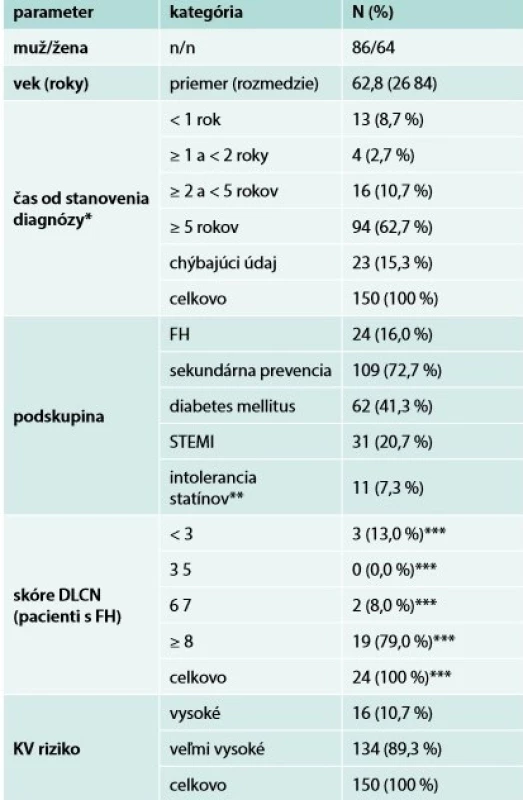
*diagnóza hyperlipidémie
**nežiaduce udalosti prisudzované statínovej liečbe
***percento pacientov s FH
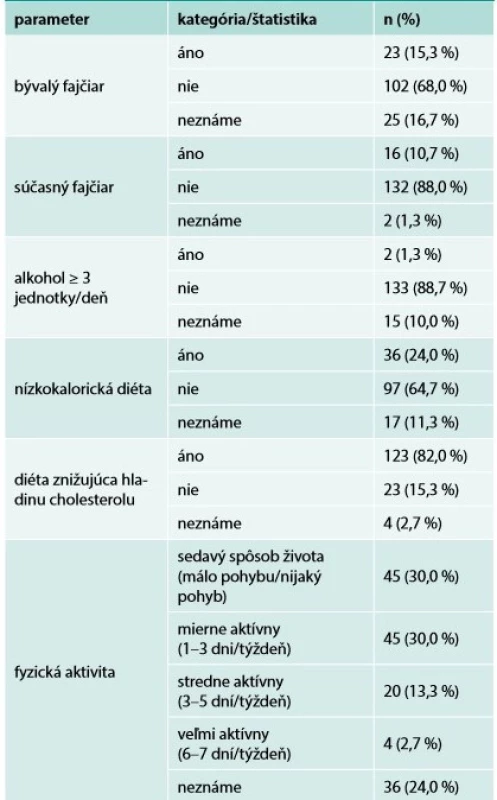
Hypolipidemická liečba
Na prvej návšteve takmer všetci pacienti (147; 98,0 %) dostávali statíny buď v monoterapii (114; 76,0 %), alebo v kombinácii s inou LLT (33; 22,0 %) (tab. 3 a tab. 4). 26 pacientov (17,3 %) dostávalo ezetimib, väčšinou v kombinácii so statínmi (24; 16,0 %). Podrobnosti týkajúce sa statínovej liečby na prvej návšteve sú uvedené v tab. 4; 75,5 % pacientov dostávalo vysoko intenzívnu statínovú liečbu (atorvastatín 4080 alebo rosuvastatín 2040 mg/deň) počas štúdie.
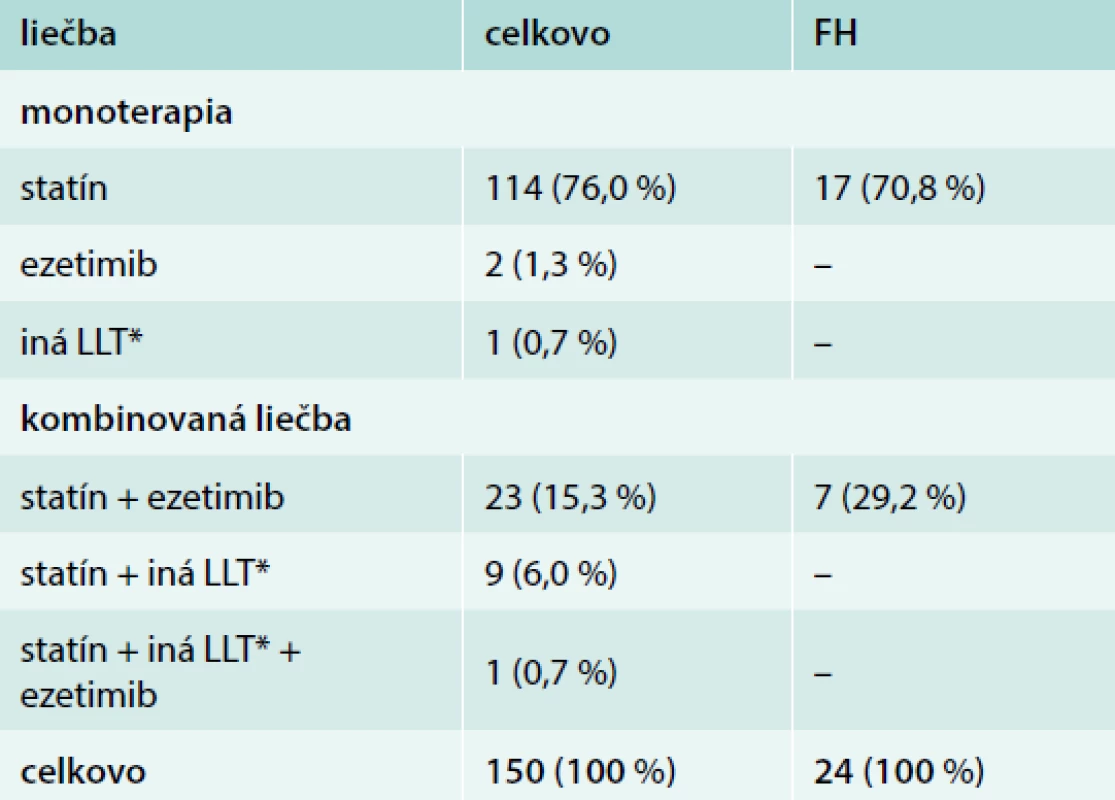
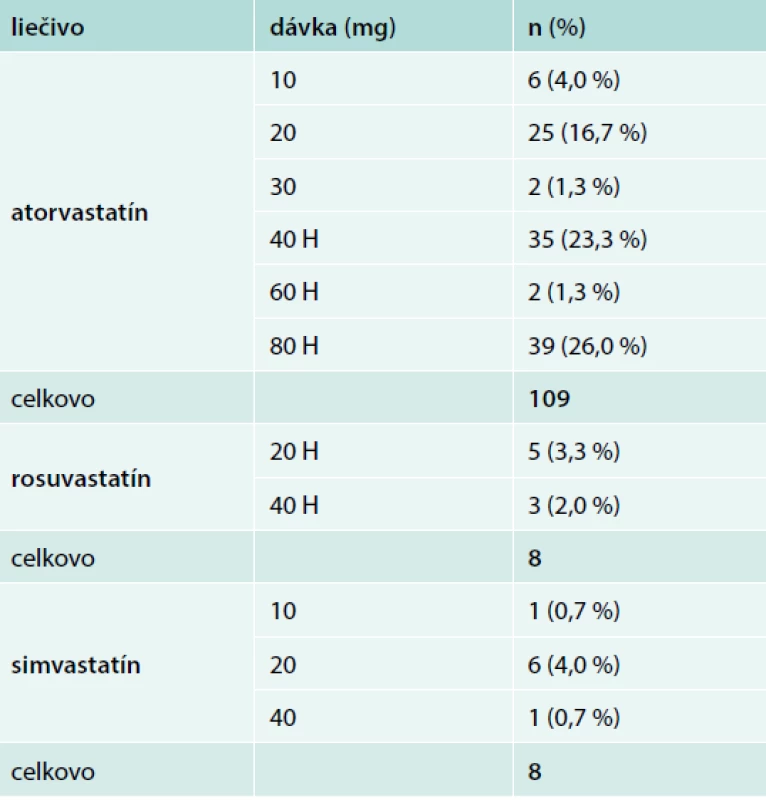
*na prvej návšteve boli dostupné údaje pre 125 pacientov, percentá sú
založené na 150 pacientoch
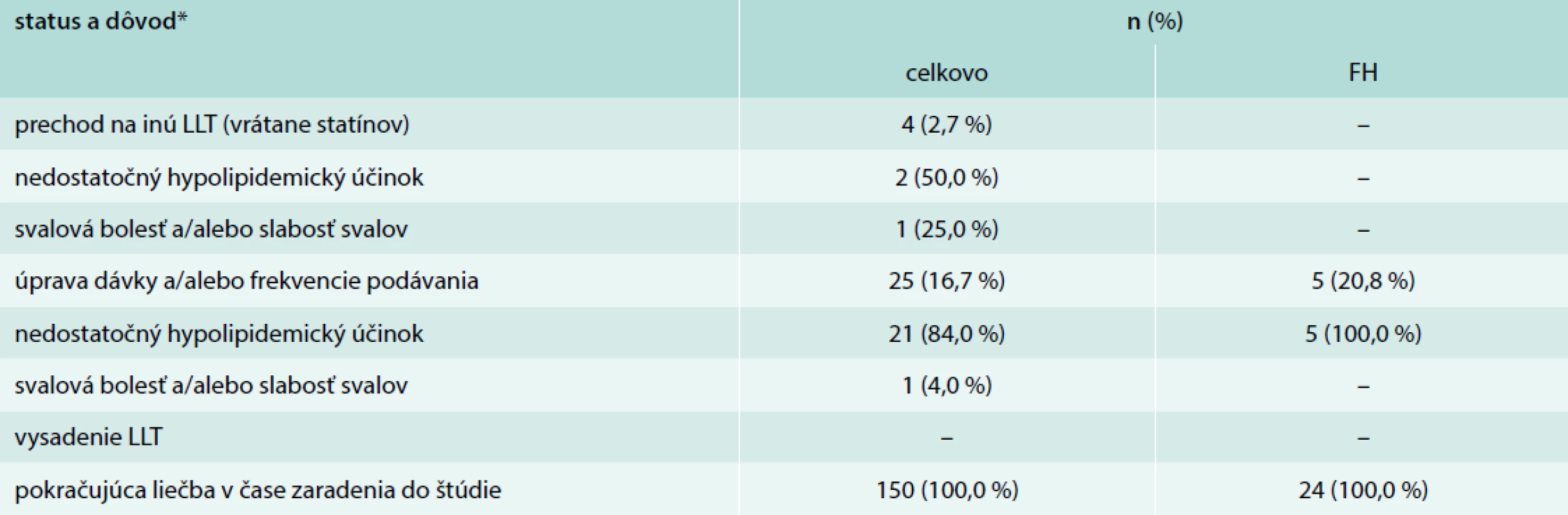
Iba 4 pacienti (2,7 %) prešli na inú LLT počas sledovania a u 25 (16,7 %) pacientov sa vykonali úpravy dávky alebo frekvencie podávania, väčšinou kvôli nedostatočnému hypolipidemickému účinku (n = 23), ako je uvedené v tab. 5. U žiadneho pacienta nedošlo k vysadeniu LLT.
Hladina LDL-cholesterolu a jej cieľové hodnoty
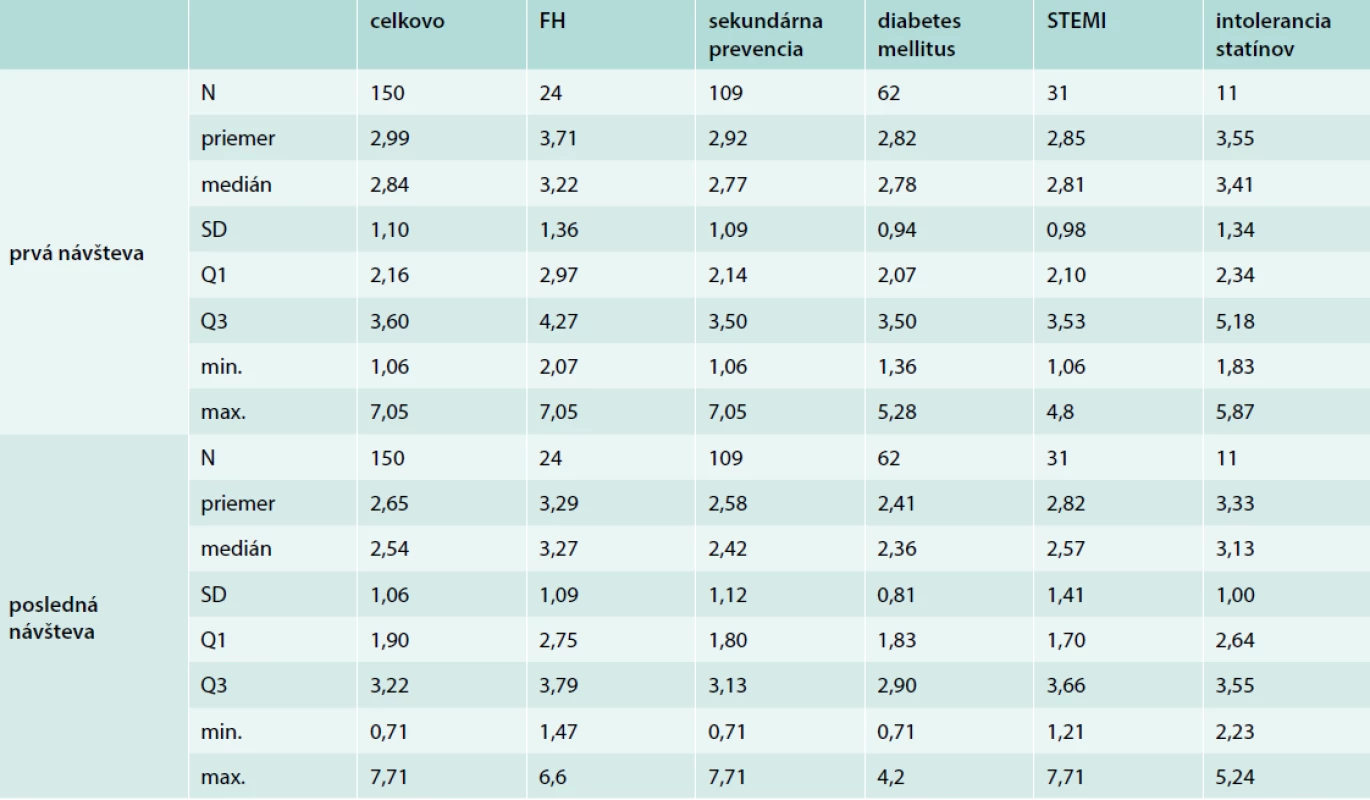
Údaje týkajúce sa LDL-C sú zhrnuté v tab. 6. Graf 1 zobrazuje priemernú hladinu LDL-C na prvej a poslednej návšteve sledovaného obdobia, celkovo a podľa podskupín. Celková priemerná hladina LDL-C bola 3,0 (1,17,1) mmol/l na prvej návšteve a 2,6 (0,77,7) mmol/l na poslednej návšteve. V podskupine pacientov s FH bola priemerná hladina LDL-C vyššia, a to 3,7 (2,17,1) mmol/l (prvá návšteva) a 3,3 (1,56,6) mmol/l (posledná návšteva). Hladina LDL-C bola pri poslednom hodnotení numericky nižšia vo všetkých podskupinách (štatistická významnosť nebola testovaná).

Dosiahnutie cieľových hodnôt LDL-C definovaných ESC/EAS podľa kategórie rizika je zhrnuté v tab. 7. Iba 2 zo 16 HR pacientov (12,5 %; 95% IS: 1,638,4 %) a 40 zo 134 VHR pacientov (29,9 %; 95 % IS: 22,338,4 %) dosiahli odporúčané cieľové hodnoty LDL-C < 2,5 mmol/l (HR pacienti) a < 1,8 mmol/l (VHR pacienti). V podskupine pacientov s FH dosiahli tieto cieľové hodnoty 2 z 15 (13,3 %; 95% IS: 1,740,5 %) HR pacientov a 2 z 9 (22,2 %; 95 % IS: 2,860,0 %) VHR pacientov. V prípade pacientov s jednoznačnou/pravdepodobnou FH (skóre ≥ 6 podľa kritérií DLCN) dosiahli tieto cieľové hodnoty 2 z 15 (13,3 %; 95% IS: 1,740,5 %) HR pacientov a 0 zo 6 VHR pacientov (tab. 7 a graf 2).
![Dosiahnutie cieľových hodnôt LDL-C definovaných ESC/EAS podľa kategórie rizika, celkovo
a u pacientov s FH, kedykoľvek počas sledovaného obdobia [7]. Výsledky sú prezentované ako počet
a percento pacientov v kategórii s obojstranným 95% intervalom spoľahlivosti (IS)](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image_pdf/926629113990be385f65c20b3369999a.png)
![Percento pacientov, ktorí dosiahli cieľové hodnoty LDL-C definované ESC/EAS podľa kategórie rizika
(vysoké riziko < 2,5 mmol/l [7] alebo 2,6 mmol/l [8], veľmi vysoké riziko < 1,8 mmol/l) [7] kedykoľvek
počas sledovaného obdobia](https://pl-master.mdcdn.cz/media/image_pdf/c5db5bc0a29478a0ef1944664a80fb84.png?version=1579715390)
Kardiovaskulárne príhody
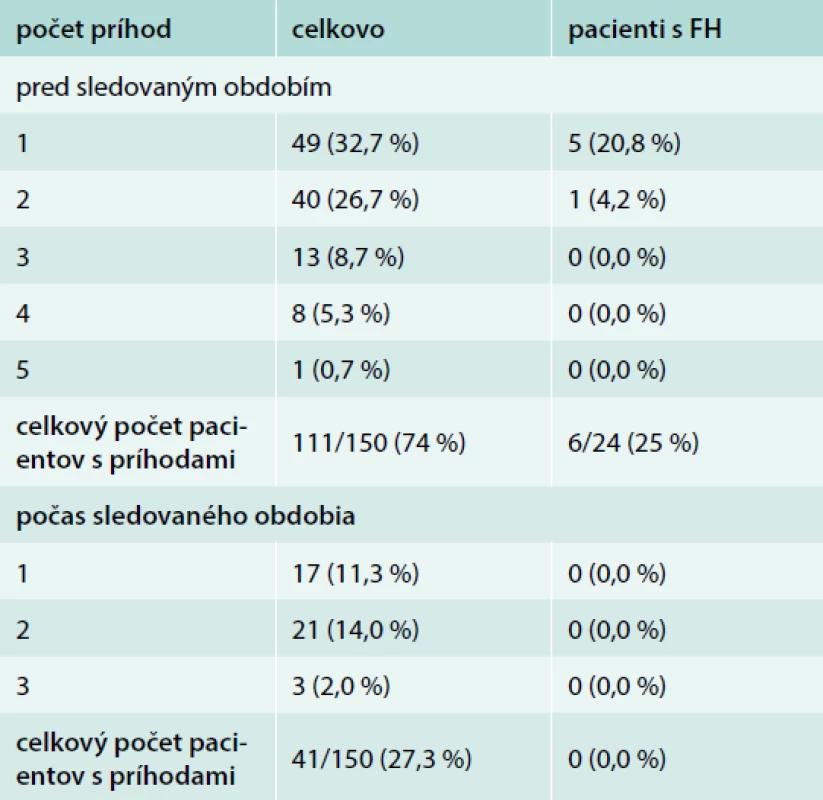
Ako je zhrnuté v tab. 8, predchádzajúce KV príhody (≤ 5) boli zdokumentované u 111 zo 150 (74,0 %) pacientov na začiatku sledovania a u 41 zo 150 (27,3 %) pacientov sa KV príhody (≤ 3) vyskytli počas 12-mesačneho sledovaného obdobia.
Nežiaduce udalosti a hospitalizácie
Ako už bolo spomenuté, u 11 pacientov (7,3 %) bola udávaná prítomnosť príznakov intolerancie statínov. Najčastejšími príznakmi intolerancie statínov boli SAMS (StatinAssociated Muscle Symptoms; svalové symptómy súvisiace s užívaním statínov), ktoré boli hlásené u 3 (2,0 %) pacientov. Počas štúdie bolo hospitalizovaných celkovo 40 (26,7 %) pacientov, najčastejšie z dôvodu koronárnej revaskularizácie (10; 6,7 %), infarktu myokardu s eleváciou segmentu ST (STEMI) (9; 6,0 %) alebo infarktu myokardu bez elevácie segmentu ST / non-STEMI (6; 4,0 %).
Diskusia
Napriek tomu, že Slovenská republika patrí v rámci Organizácie pre hospodársku spoluprácu a rozvoj (Organisation for Economic Cooperation and Development – OECD) medzi 3 krajiny s najvyššou spotrebou liekov znižujúcich hladinu cholesterolu v prepočte na jedného obyvateľa [16], má jednu z najvyšších mier úmrtnosti na KV ochorenia v EÚ. V roku 2014 zomrelo na KV asi 23 000 osôb, čo predstavovalo 50 % všetkých úmrtí u žien a 40 % všetkých úmrtí u mužov [17]. Medzi rokmi 1993 a 2008 klesla úmrtnosť na ischemickú chorobu srdca (ICHS) takmer o tretinu a nedávna analýza naznačila, že sa to dá vo veľkej miere (50 %) pripísať čoraz častejšiemu používaniu liečby založenej na dôkazoch. Nepriaznivé trendy v hlavných KV rizikových faktoroch však podčiarkli potrebu intenzívnejších celopopulačných programov prevencie zameraných na faktory životného štýlu, napr. na fajčenie a stravovacie zvyklosti [18]. Z údajov z CLARIFY, čo je register pacientov so stabilnou ICHS, vyplynulo, že slovenskí pacienti (n = 183), v porovnaní s pacientmi z ostatných európskych krajín, mali vyššiu telesnú hmotnosť, závažnejšiu artériovú hypertenziu, vyšší výskyt ICHS v rodinnej anamnéze, viacej pacientov malo diabetes mellitus či prekonalo infarkt myokardu alebo cievnu mozgovú príhodu a častejšie trpeli srdcovým zlyhávaním alebo anginou pectoris. Takisto mali vyššiu celkovú mortalitu, významne vyšší počet hospitalizácií pre srdcové zlyhávanie a vyšší výskyt tranzitórnej ischemickej príhody [19].
Naša observačná štúdia zaoberajúca sa manažmentom hyperlipidémie a dosahovaním cieľových hodnôt LDL-C u HR a VHR pacientov v Slovenskej republike zistila, že počas sledovaného obdobia sa odporúčané cieľové hodnoty LDL-C dosiahli u menej ako tretiny našich pacientov, pričom hladinu LDL-C < 2,5 mmol/l dosiahlo iba 12,5 % HR pacientov (95% IS: 1,638,4 %) a hladinu LDL-C < 1,8 mmol/l dosiahlo 29,9 % VHR pacientov (95% IS: 22,338,4 %). Uvedené percentá pacientov sú nižšie ako percentá pacientov, ktorí dosiahli cieľové hodnoty v hlavnej regionálnej štúdii HR pacientov (23,8 %; 95% IS: 17,2931,45 %) a 42,0 % VHR pacientov (39,145,0 %) [14]. Zahrnuté centrá a pacienti sa medzi 7 krajinami participujúcimi na regionálnej štúdii značne líšili, a to mohlo prispieť k rozdielom vo výsledkoch. Aj v ďalších štúdiách realizovaných na Slovensku sa zistilo, že cieľové hodnoty LDL-C sa dosahujú u nízkeho percenta pacientov [20,21].
Väčšinu našej skúmanej populácie tvorili pacienti liečení v rámci sekundárnej prevencie/VHR pacienti a takmer polovica z nich (41,3 %) boli diabetici, čo sa odráža v zahrnutí akademických a špecializovaných lipidologických ambulancií. KV príhody boli zaznamenané u 27,3 % pacientov počas 12-mesačného sledovaného obdobia. Je potrebné vziať na vedomie, že tento číselný údaj zahŕňa nezávažné príhody, ako je uvedené v časti s metódami a v tab. 8. Takmer všetci pacienti (98 %) boli liečení statínmi, pričom viac ako dve tretiny pacientov (76 %) dostávali vysoko intenzívnu statínovú liečbu a 16 % pacientov dostávalo kombináciu statín a ezetimib. Najčastejším dôvodom na zmenu LLT bol nedostatočný hypolipidemický účinok. Použitie nízkych začiatočných dávok statínov bez dostatočnej titrácie dávky smerom nahor a vysadenie statínov/slabá adherencia k liečbe sa považujú za kľúčové faktory, ktoré prispievajú k nedostatočnému zníženiu hladiny LDL-C u pacientov s hyperlipidémiou a dávajú sa do súvislosti so slabšími klinickými výsledkami [8,21,22]. Keďže vysadenie statínov a slabá adherencia pacienta k liečbe môžu byť dôsledkom intolerancie statínov, nedávno boli publikované podrobné odborné odporúčania na diagnostikovanie a manažment SAMS [23]. Ďalšiu bariéru pre intenzívnu statínovú liečbu môžu predstavovať problémy súvisiace s úhradou liekov, i keď v našej štúdii nie sú uvedené medzi dôvodmi na vysadenie alebo úpravu LLT [22].
FH je najčastejšou genetickou príčinou predčasného výskytu ischemickej choroby srdca. Takmer všetci naši pacienti s FH (21 z 24) mali jednoznačnú alebo pravdepodobnú FH podľa kritérií DLCN. Ak sa FH nelieči, pacientom hrozí veľmi vysoké riziko vzniku KV príhod (odhaduje sa približne 10násobne vyššie riziko ako vo všeobecnej populácii) [24], preto je dôležitá skorá diagnóza a včasné začatie agresívnej LLT. Hoci z celosvetového hľadiska je FH „poddiagnostikované“ a „podliečené“ ochorenie [25], Slovenská republika a Česká republika patria k najúspešnejším krajinám, pokiaľ ide o odhaľovanie FH, a sú zapojené do medzinárodných programov, akými sú MedPed (Make Early Diagnoses to Prevent Early Deaths in Medical Pedigrees) [26] a ScreenPro FH [27]. Na Slovensku bolo do roku 2016 identifikovaných viac ako 1 900 osôb s FH [26]. Napriek tomu sa v nedávnom prieskume zistilo, že takmer 25 % z 201 pacientov s FH, ktorí navštevujú slovenské lipidologické ambulancie, nie je liečených statínmi a väčšina nedosahuje cieľové hladiny LDL-C [21].
Ak je hladina LDL-C extrémne zvýšená, čo je častým javom u pacientov s FH, dokonca ani maximálne dávky statínov podávané v kombinácii s ezetimibom nemusia znížiť hladinu LDL-C tak, aby dosahovali cieľové hodnoty. Naliehavo potrebujeme alternatívne lieky na liečbu hyperlipidémie. V hlavnej regionálnej štúdii [14] bol malý počet pacientov liečený inhibítormi proproteínkonvertázy subtilizín/kexín typu 9 (PCSK9i), ale žiadny z našich slovenských pacientov nebol liečený týmito sľubnými novými liečivami [28], ktoré neboli uvedené na slovenský trh v období, keď sme uskutočňovali našu štúdiu. PCSK9i zlepšujú recyklovanie LDL receptorov (LDL-R) a zvyšujú dostupnosť LDL-R na povrchu hepatocytov [29], vďaka čomu vedú k dodatočnému poklesu hladiny LDL-C až o 60 %. Keď sa pridajú k existujúcej statínovej liečbe, cieľové hodnoty dosiahneme až u 80 % pacientov [30–33]. Dôležité je spomenúť, že dlhodobé údaje týkajúce sa KV cieľových ukazovateľov zo štúdií FOURIER a ODYSSEY potvrdzujú, že evolokumab [32] a alirokumab [34] významne znižujú výskyt KV príhod. Liečba evolokumabom v štúdii FOURIER významne znížila riziko výskytu primárneho kľúčového kompozitného ukazovateľa a aj klinicky závažnejšieho sekundárneho cieľového ukazovateľa definovaného ako KV úmrtie, infarkt myokardu a cievna mozgová príhoda, v porovnaní s placebom (5,9 % vs 7,4 %; pomer rizík/hazard ratio 0,80; 95% IS: 0,730,88; P < 0,001) [32]. Analýza údajov zo štúdie ODYSSEY Outcomes taktiež preukázala nižší výskyt závažných KV príhod (úmrtie v dôsledku ischemickej choroby srdca, nefatálny infarkt myokardu, fatálna/nefatálna ischemická cievna mozgová príhoda alebo nestabilná angína pectoris vyžadujúca hospitalizáciu) pri alirokumabe v porovnaní s placebom (9,5 % vs 11,1 %; pomer rizík 0,85; 95% IS: 0,78–0,93; P < 0,001) [34]. Zdá sa, že na rozdiel od statínov sa liečba PCSK9i nespája so zvýšením hladiny kreatínkinázy ani s myalgiou/svalovými symptómami a ukončenie liečby kvôli nežiaducim udalostiam je zriedkavé. So záujmom očakávame ďalšie údaje o dlhodobej bezpečnosti a účinnosti [35].
Medzi obmedzenia našej observačnej štúdie patria malá veľkosť niektorých podskupín, napríklad podskupiny pacientov s FH a podskupiny pacientov s intoleranciou statínov, ako aj neistá diagnóza FH u malej časti pacientov. Zmeny hladiny LDL-C v priebehu času by mali byť interpretované s obozretnosťou, a to vzhľadom na heterogénnu populáciu pacientov a rôznu dĺžku trvania ich LLT, ako aj na chýbanie vopred definovaných intervalov vyšetrovania LDL-C. Niektoré nežiaduce udalosti mohli byť nedostatočne hlásené. Napriek tomu naše údaje poskytujú užitočný pohľad na spôsoby manažmentu hyperlipidémie a dosahovanie cieľových hodnôt LDL-C v celej krajine.
Závery
Naše zistenia sa zhodujú s inými publikáciami zo Slovenska, pričom poukazujú na to, že značný podiel pacientov, ktorí sú liečení hypolipidemikami, nedostáva liečbu v súlade s európskymi odporúčaniami založenými na dôkazoch alebo nedosahuje cieľové hodnoty LDL-C. V dôsledku toho sú vystavení reziduálnemu riziku KV príhod, čo potvrdzujú naše výsledky. Naliehavo potrebujeme ďalšie koordinované úsilie na riešenie nenaplnených potrieb u týchto pacientov.
Túto štúdiu financovala spoločnosť Amgen (Europe GmbH).
Konflikt záujmov
Autori deklarovali tieto konflikty záujmov: PharmDr. Alena Nemcová je zamestnankyňa spoločnosti Amgen. MUDr. Ľubomíra Fábryová, PhD. obdržala poplatky za konzultácie od spoločností Abbott, Amgen, Boehringer Ingelheim, Eli Lilly, MSD, Novo Nordisk, Sanofi Aventis, Servier, Valeant a honorár pre prednášajúceho od spoločností Amgen, MSD, Sanofi Aventis a Valeant.
Poďakovanie
Venkatesan Mudaliar z Quartesian, Bangalore, poskytol štatistickú analýzu. Julia Balfour z Northstar Medical Writing and Editing, Dundee, UK, poskytla podporu pri písaní medicínskeho textu (s finančnou podporou od spoločnosti Amgen).
Autori by chceli poďakovať všetkým pacientom a pracovníkom z participujúcich centier.
Doručeno do redakce 9. 5. 2019
Přijato po recenzi 11. 11. 2019
MUDr. Ľubomíra Fábryová, PhD.
MetabolKLINIK, s.r.o., Ambulancia pre diabetológiu, poruchy látkovej premeny a výživy, Špecializovaná lipidologická ambulancia, MED PED centrum, Bratislava, Slovenská republika
Sources
- Kannel WB. The Framingham Study: An epidemiological investigation of cardiovascular disease, Section 30. Some characteristics related to the incidence of cardiovascular disease and death: The Framingham Study. 18-year follow-up. Washington, D.C., Dept. of Health, Education, and Welfare, Publication No. (NIH) 74–599, 1974.
- Kannel WB. Range of serum cholesterol values in the population developing coronary artery disease. Am J Cardiol 1995; 76(9 Suppl): 69C-77C. Dostupné z DOI: <http://dx.doi.org/10.1016/s0002–9149(99)80474–3>.
- Kannel WB, Castelli WP, Gordon T. Cholesterol in the prediction of atherosclerotic disease: New perspectives based on the Framingham study. Ann Intern Med 1979; 90(1): 85–91. Dostupné z DOI: <http://dx.doi.org/10.7326/0003–4819–90–1-85>.
- World Health Organization. Cardiovascular diseases. Fact sheet. Updated May 2017. [cit 09–10–2018]. Dostupné z WWW: <https://www.who.int/en/news-room/fact-sheets/detail/cardiovascular-diseases-(cvds)>.
- National Institute for Health and Care Excellence. Cardiovascular disease: risk assessment and reduction, including lipid modification. Appendix A: Grouping of statins; 2016. [cit 21–11–2018]. Dostupné z WWW: <https://www.nice.org.uk/guidance/cg181>.
- Baigent C, Blackwell L, Emberson J et al. [Cholesterol Treatment Trialists Collaboration]. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet 2010; 376(9753): 1670–1681. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(10)61350–5>.
- Reiner Z, Catapano AL, De Backer G et al. ESC/EAS Guidelines for the management of dyslipidaemias: the Task Force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and the European Atherosclerosis Society (EAS). Eur Heart J 2011; 32(14): 1769–1818. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehr158>.
- Catapano AL, Graham I, De Backer G et al. 2016 ESC/EAS Guidelines for the Management of Dyslipidaemias: The Task Force for the Management of Dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Atherosclerosis 2016; 253 : 281–344. Dostupné z DOI: <http://dx.doi.org/10.1016/j.atherosclerosis.2016.08.018>.
- Mach F, Baigent C, Catapano AL et al. ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk: The Task Force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS). Eur Heart J 2019; pii: ehz455. Dostupné z DOI: <http://doi: 10.1093/eurheartj/ehz455>.
- Marrett E, Zhao C, Zhang NJ et al. Limitations of real-world treatment with atorvastatin monotherapy for lowering LDL-C in high-risk cardiovascular patients in the US. Vasc Health Risk Manag 2014; 10 : 237–246. Dostupné z DOI: <http://dx.doi.org/10.2147/VHRM.S54886>.
- Steinberg BA, Bhatt DL, Mehta S et al. Nine-year trends in achievement of risk factor goals in the US and European outpatients with cardiovascular disease. Am Heart J 2008; 156(4): 719–727. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ahj.2008.05.020>.
- Reiner Ž, De Backer G, Fras Z et al. Lipid lowering drug therapy in patients with coronary heart disease from 24 European countries – Findings from the EUROASPIRE IV survey. Atherosclerosis 2016; 246 : 243–250. Dostupné z DOI: <http://dx.doi.org/10.1016/j.atherosclerosis.2016.01.018>.
- Gitt AK, Lautsch D, Ferrieres J et al. Low-density lipoprotein cholesterol in a global cohort of 57,885 statin-treated patients. Atherosclerosis 2016; 255 : 200–209. Dostupné z DOI: <http://dx.doi.org/10.1016/j.atherosclerosis.2016.09.004>.
- Petrov I, Dumitrescu A, Snejdrlova M et al. Clinical Management of High and Very High Risk Patients with Hyperlipidaemia in Central and Eastern Europe: An Observational Study. Adv Ther 2019; 36(3):608–620. Dostupné z DOI: <http://dx.doi.org/10.1007/s12325–019–0879–1>.
- Hovingh GK, Davidson MH, Kastelein JJ et al. Diagnosis and treatment of familial hypercholesterolaemia. Eur Heart J 2013; 34(13): 962–971. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/eht015>.
- Pharmaceutical consumption. Health at a Glance 2015: OECD Indicators, OECD Publishing, Paris. [cit 9–11–2018]. Dostupné z WWW: <https://read.oecd-ilibrary.org/social-issues-migration-health/health-at-a-glance-2015/pharmaceutical-consumption_health_glance-2015–68-en#page1>.
- OECD and European Observatory on Health Systems and Policies. Slovensko: Zdravotný Profil Krajiny 2017. [cit 20–09–2018]. Dostupné z WWW: <https://read.oecd-ilibrary.org/social-issues-migration-health/slovensko-zdravotny-profil-krajiny-2017_9789264285408-sk#page1>.
- Psota M, Bandosz P, Goncalvesova E et al. Explaining the decline in coronary heart disease mortality rates in the Slovak Republic between 1993–2008. PloS One 2018; 13(1): e0190090. Dostupné z DOI: <http://dx.doi.org/10.1371/journal.pone.0190090>.
- Murín J, Kamenský G et al. Register CLARIFY – pohľad na slovenské údaje po piatich rokoch. Cardiology Lett 2017; 26(4): 236–246.
- Čaprnda M, Hencel J, Farkašovský J et al. Dosiahnutie cieľových hodnôt LDL cholesterolu efektívnejšou dávkou atorvastatínu 30 mg v praxi všeobecného lekára. Via Pract 2015; 12(5): 213–216.
- Vohnout B, Fábryová Ľ, Klabník A et al. Treatment pattern of familial hypercholesterolemia in Slovakia: targets, treatment and obstacles in common practice. Atherosclerosis 2018; 277 : 323–326. Dostupné z DOI: <http://dx.doi.org/10.1016/j.atherosclerosis.2018.06.857>.
- Banach M, Stulc T, Dent R et al. Statin non-adherence and residual cardiovascular risk: There is need for substantial improvement. Int J Cardiol 2016; 225 : 184–196. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ijcard.2016.09.075>.
- Stroes ES, Thompson PD, Corsini A et al. Statin-associated muscle symptoms: impact on statin therapy-European Atherosclerosis Society Consensus Panel Statement on Assessment, Aetiology and Management. Eur Heart J 2015; 36(17): 1012–1022. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehv043>.
- Benn M, Watts GF, Tybjaerg-Hansen A et al. Familial hypercholesterolemia in the danish general population: prevalence, coronary artery disease, and cholesterol-lowering medication. J Clin Endocrinol Metab 2012; 97(11):3956–3964. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2012–1563>.
- Nordestgaard BG, Chapman MJ, Humphries SE et al. Familial hypercholesterolaemia is underdiagnosed and undertreated in the general population: guidance for clinicians to prevent coronary heart disease Consensus Statement of the European Atherosclerosis Society. Eur Heart J 2013; 34(45): 3478–3490. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/eht273>.
- Vrablík M, Rašlová K, Freiberger T et al. Co je nejdůležitější pro pacienty s familiární hypercholesterolemií? Projekt MedPed v České a Slovenské republice. AtheroRev 2016; 1(1): 28–33.
- Ceska R, Freiberger T, Vaclova M et al. ScreenPro FH: from the Czech MedPed to international collaboration. ScreenPro FH is a participating project of the EAS-FHCS. Physiol Res 2017; 66(Suppl 1): S85-S90.
- Fábryová Ľ. Inhibítory PCSK9 v manažmente pacientov s vysokým kardiovaskulárnym rizikom – efektívna liečba na dosah. AtheroRev 2016; 1(1): 42–48.
- Seidah NG, Awan Z, Chrétien M et al. PCSK9: A Key Modulator of Cardiovascular Health. Circ Res 2014; 114(6): 1022–1036. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCRESAHA.114.301621>.
- Lipinski MJ, Benedetto U, Escarcega RO et al. The impact of proprotein convertase subtilisin-kexin type 9 serine protease inhibitors on lipid levels and outcomes in patients with primary hypercholesterolaemia: a network meta-analysis. Eur Heart J 2016; 37(6): 536–545. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehv563>.
- Navarese EP, Kolodziejczak M, Schulze V et al. Effects of Proprotein Convertase Subtilisin/Kexin Type 9 Antibodies in Adults With Hypercholesterolemia: A Systematic Review and Meta-analysis. Ann Intern Med 2015; 163(1): 40–51. Dostupné z DOI: <http://dx.doi.org/10.7326/M14–2957>.
- Sabatine MS, Giugliano RP, Keech AC et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. N Engl J Med 2017; 376(18): 1713–1722. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1615664>.
- Sabatine MS, Giugliano RP, Wiviott SD et al. Efficacy and safety of evolocumab in reducing lipids and cardiovascular events. N Engl J Med 2015; 372(16): 1500–1509. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1500858>.
- Schwartz GG, Steg PG, Szarek M et al. Alirocumab and Cardiovascular Outcomes after Acute Coronary Syndrome. N Engl J Med 2018; 379(22): 2097–2107. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1801174>.
- Fábryová Ľ. Otvorené otázky z kardiovaskulárnych štúdií FOURIER a ODYSSEY Outcomes. AtheroRev 2018; 3(3): 209–212.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2019 Issue 12
-
All articles in this issue
- Poznámky k novému „Doporučení pro léčbu dyslipidemií. Ovlivnění lipidů ke snížení kardiovaskulárního rizika“
- Manažment hyperlipidémie na Slovensku: observačná štúdia
- Vaskulární věk
- Ateroskleróza u pacientů s diabetem 1. typu
- Hypertriglyceridemie a riziko aterosklerózy
- Vyhlazování aterosklerózy nejen v dolních končetinách
- Ateroskleróza a betablokáda: zapomenutá možnost?
- Farmakologicky indukované tyreopatie u pacientů s kardiologickým onemocněním
- Význam fixních kombinací na poli kardiovaskulární prevence aneb možnost léčit dvě diagnózy jednou tabletou
- Úvodník
- Stanovisko výboru České společnosti pro aterosklerózu k doporučením ESC/EAS pro diagnostiku a léčbu dyslipidemií z roku 2019
- Ľubomíra Fábryová, Pavol Holéczy a kolektív. Diabezita. Diabetes a obezita: nerozlučné dvojičky
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Farmakologicky indukované tyreopatie u pacientů s kardiologickým onemocněním
- Vaskulární věk
- Hypertriglyceridemie a riziko aterosklerózy
- Poznámky k novému „Doporučení pro léčbu dyslipidemií. Ovlivnění lipidů ke snížení kardiovaskulárního rizika“
