Raritní koincidence chylothoraxu a hydrothoraxu při adenokarcinomu žaludku – kazuistika
A rare coincidence of a chylothorax and a hydrothorax caused by gastric adenocarcinoma – a case report
We present a case report of a 74-years old patient with a finding of bilateral pleural effusion due to a different fluid composition caused by gastric adenocarcinoma. The finding of a bilateral effusion, where the exudate fluid is of a different chemical composition, is a rare phenomenon. While the right-sided exudate had the characteristics of hydrothorax, the left-sided exudate had those of chylothorax. The initial suspicion of a lung tumor was not confirmed, and further examination surprisingly revealed gastric adenocarcinoma. The patient did not benefit from targeted oncological treatment for a long time and the chemotherapy was terminated after 3 cycles. The cause of right-sided hydrothorax is therefore attributed to hypalbuminemia and secondary pneumonia, left-sided chylothorax was a primo-manifestation of gastric adenocarcinoma. There is only a small number of similar case reports of patients with gastric tumor and chylothorax in the literature. While the recorded cases were mostly Asian ethnic patients, the course of their illness – including survival – was almost strikingly similar (and unfavorable).
Keywords:
gastric adenocarcinoma – chylothorax – bilateral pleural effusion
Authors:
Nela Šťastná 1,2; doc. MUDr. Kristián Brat, Ph.D. 1,2
Authors‘ workplace:
Klinika nemocí plicních a TBC, Fakultní nemocnice Brno
1; Lékařská fakulta Masarykovy Univerzity, Brno
2
Published in:
Vnitř Lék 2020; 66(7): 43-45
Category:
Case Report
Overview
Prezentujeme kazuistiku 74letého pacienta s nálezem bilaterálního pleurálního výpotku stranově odlišného složení tekutiny, zapříčiněného adenokarcinomem žaludku. Nález oboustranného výpotku, kdy tekutina výpotku je jiného chemického složení je vzácným jevem. Zatímco pravostranný výpotek byl charakteru hydrothoraxu, levostranný výpotek byl charakteru chylothoraxu. Prvotní suspekce na tumor plic se neprokázala, dalším vyšetřením byl překvapivě zjištěn adenokarcinom žaludku. Z cílené onkologické léčby pacient dlouho neprofitoval a chemoterapie byla ukončena po 3 cyklech. Příčinu pravostranného hydrothoraxu tedy přisuzujeme hypalbuminemii a sekundární pneumonii, levostranný chylothorax pak znamenal primomanifestaci adenokarcinomu žaludku. V literatuře najdeme pouze malý počet podobných kazuistik pacientů s tumorem žaludku a chylothoraxem. Většinou se jednalo o pacienty asijských etnik; průběh jejich nemoci včetně délky přežití byl až nápadně podobný (nepříznivý).
Klíčová slova:
adenokarcinom žaludku – chylothorax – pleurální výpotek
Popis kazuistiky
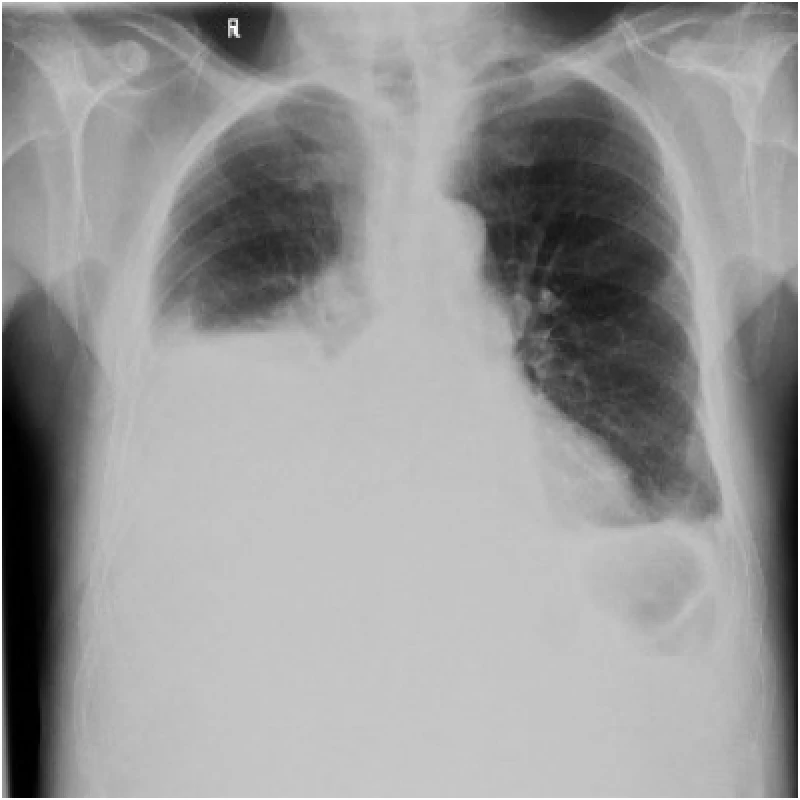
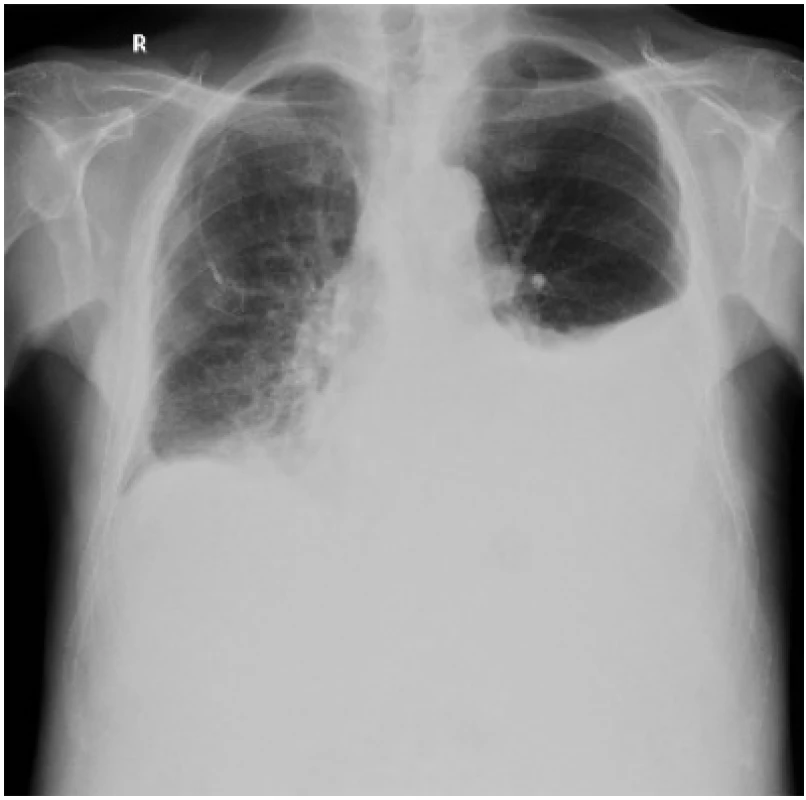
Prezentujeme případ 74letého muže, celoživotního nekuřáka, s pozitivní onkologickou rodinnou anamnézou, bez závažných interních komorbidit v osobní anamnéze. V únoru 2019 absolvoval gastroskopii a kolonoskopii pro mírné bolesti břicha, vyšetření neprokázala žádnou patologii. Na naše pracoviště byl pacient poprvé referován v srpnu 2019. V tom období pacient pro dyspepsii absolvoval CT břicha a byl mu zjištěn ascites a pravostranný fluidothorax, bez lymfadenopatie. Provedli jsme pleurální punkci 200ml žlutého, lehce zkaleného výpotku, kultivačně sterilní tekutiny, bez nálezu onkologicky suspektních buněk, dle Lightových kritérií exsudát. Nemocný byl postupně přeléčen amoxicilin-klavulanátem, moxifloxacinem a ceftriaxonem. Pro časnou progresi pleurálního výpotku bylo pacientovi provedeno CT hrudníku s nálezem atelektázy dolního laloku pravé plíce a progrese fluidothoraxu. Společně s pleurálním výpotkem ale došlo i k progresi ascitu, otoků dolních končetin až ke vzniku anasarky. Kardiogenní příčina obtíží byla nepravděpodobná normálním echokardiografickým nálezem i nízkým NTproBNP (504ng/l). Laboratorně byla u pacienta přítomna hypoproteinemie, hypalbuminemie (celková bílkovina 65g/l, albumin 28g/l). Pro dušnost při progresi pravostranného výpotku byl zaveden hrudní drén, vyšetření punktátu prokázalo stejný charakter výpotku jako jeho předchozí rozbor. Bronchoskopický nález byl v mezích normy, cytologie bronchoalveolární tekutiny byla bez známek malignity. Za hospitalizace se následně manifestoval i levostranný výpotek (de novo), který se rozvinul až do objemu vyžadujícího druhostrannou hrudní drenáž. Levostranný pleurální výpotek byl překvapivě biochemicky a makroskopicky charakteru chylothoraxu, cytologicky maligní buňky nebyly přítomny, dle Lightových kritérií transudát, triacylglycerol (TG) 10,8mmol/l, pH 7,5. Lymfografie nebyla dostupná na našem pracovišti a jednoznačná příčina chylothoraxu v tuto chvíli nebyla vysvětlena. Pacienta jsme převedli na plnou parenterální výživu s nízkou hladinou triglyceridů. Na kontrolním CT hrudníku trvala atelektáza dolního laloku pravé plíce, objevila se reaktivní mediastinální a hilová lymfadenopatie vpravo. Z tumor markerů byly zvýšené CA 72–4 (225 kU/l; 0–6,9 kU/l), CA 19–9 (410 kU/l; 0–27 kU/l). Proto byla provedena kolonoskopie, jenž byla makroskopicky bez pozoruhodností, a gastrofibroskopie, kde byla z drobné vkleslé léze těla žaludku provedena biopsie, která prokázala adenokarcinom žaludku difuzního typu. Hrudní drény byly postupně extrahovány a parenterální výživa ukončena. Pravostranný fluidothorax jsme uzavřeli jako kombinované parapneumonické a hypoalbuminemické etiologie, levostranný chylothorax jako paramaligní. Nemocný byl předán na onkologické pracoviště. Klinický stav byl i nadále velmi dobrý, výkonnostní stav (PS) 1, nebyla prokázána mutace HER2. Počátkem října 2019 mohla být zahájena systémová chemoterapie v kombinaci oxaliplatina v dávce 85mg/m2 , leukovorin v dávce 200mg/m2 a fluorouracil v dávce 400mg/m2 D1, s pokračováním v dávce 1 200mg/m2 na 48 hodin (režim FOLFOX). Po druhém cyklu chemoterapie progredovaly jak otoky dolních končetin, tak ascites a levostranný fluidothorax s nutností thorakocentézy a punkce ascitu. Ascitický punktát byl taktéž chylózního složení. I přes nutriční intervenci hypoproteinemie dosáhla hodnot 19g/l albuminu v séru. Po 3 cyklech chemoterapie (v listopadu 2019) se celkový klinický stav zhoršil na PS 3, objevily se paraneoplastické febrilie, prohlubovala se kachexie. Onkologická léčba byla ukončena a pacient byl předán do péče ambulance paliativní medicíny, kde po dvou měsících umírá na terminální progresi onemocnění.
Diskuze
Chylothorax znamená přítomnost chylózní tekutiny v pohrudniční dutině. Vyskytuje se relativně vzácně. Mízní cévy jsou v těle anatomicky lokalizovány stranově nesouměrně. Zatímco podél abdominální aorty vede silný ductus thoracicus po pravé straně, ve výši 4. hrudního obratle podbíhá aortu a směrem kraniálním již probíhá po její levé straně. Ductus thoracicus ústí do angulus venosus sinister. Pouze z pravé horní poloviny těla nesbírá lymfu zmíněný ductus thoracicus, ale drobnější mízní kmen krční, podklíčkový a bronchomediastinální. Ty společně ústí do angulus venosus dexter (1). Chylothorax je vzhledem k anatomii mízních kmenů pětkrát častěji levostranný než pravostranný. Nejčastější příčiny vzniku chylothoraxu jsou porušení celistvosti ductus thoracicus nádorem (lymfomy) nebo traumatem (úrazy, iatrogenní, zejm. po operacích srdce a jícnu, silným kašlem nebo zvracením). Mezi vzácné příčiny vzniku chylothoraxu patří nemoci lymfatických cév (lymfangioleiomyomatóza, syndrom žlutých nehtů), vrozené anomálie lymfatických cest, stavy se zvýšeným centrálním žilním tlakem (trombóza horní duté žíly), struma nebo sarkoidóza (2). Chylothorax je nápadný již makroskopicky při pleurální punkci typicky mléčně zkalenou barvou. Barvou může chylothorax imitovat zejména empyém. Makroskopicky chylothorax od empyému odlišíme centrifugací – u chylothoraxu zůstává nezměněna, u empyému vzniká sedlina. Empyém taky většinou, na rozdíl od chylothoraxu, putridně páchne. Jiná než mléčná barva však diagnózu chylothoraxu nevylučuje. Diagnózu totiž potvrzujeme laboratorním vyšetřením hladiny TG ve výpotku (TG>1,24mmol/l, event. hladina chylomikronů). Chylothorax může také imitovat velmi vzácný pseudochylothorax, u kterého je při normálních hodnotách TG zvýšen pouze cholesterol nad hodnotu 5,2mmol/l nebo lecitin-globulinové komplexy. V diagnostice může pomoci CT scan, lymfografie, biopsie, flowcytometrie aj.
Terapie chylothoraxu je odvislá od základní příčiny. Dle aktuálního klinického stavu volíme cestu pleurálními punkcemi nebo hrudní drenáží, v určitých případech pomůže video-asistovaná thorakoskopie (VATS) či otevřená thorakotomie s ligací ductus thoracicus. Velice podstatná je však restrikce příjmu tuků ve stravě ve snaze o snížení množství produkce mízy, nižšímu průtoku lymfy v ductus thoracicus a tím i samovolné uzavření defektu v cévní stěně. Proto léčbou první linie je restrikce stravy a parenterální výživa s nízkým obsahem triacylglycerolů.
Zmínky o koincidenci karcinomu žaludku a chylothoraxu jsou v literatuře raritní (3, 4). Přehledová práce kolektivu Wu z roku 2015 vychází z celkového počtu 20 případů, nicméně pouze u 14 z nich byla dostupná podrobnější data. Z těchto pacientů jich 11 mělo výpotek bilaterální. Histologicky se v 9 případech jednalo o karcinom žaludku z prstenčitých buněk, ve 3 případech o nízce diferencovaný adenokarcinom žaludku, u dvou pacientů nebyl tumor histologicky specifikován. V 10 ze 14 případů byl chylothorax doprovázen lymfedémem (3). Je pozoruhodné, jak obdobný průběh měla většina popsaných kazuistik, včetně námi popsaného pacienta. Např. v japonské kazuistice z roku 2019 kolektivu Nagano a spol. (5) autoři popisují případ nemocné ženy v předchorobí léčené pro lymfedém, následně se zjištěným bilaterálním chylothoraxem, PET/CT i CT bez nálezu primárního origa, až biopsií lymfatické uzliny axily prokázaným karcinomem žaludku z prstenčitých buněk. Nemocné byly podány celkem 4 cykly chemoterapie kombinace kapecitabin/oxaliplatina, přičemž progredoval chylózní ascites a pacientka zemřela v době 6 měsíců od zjištění diagnózy. Tato recentní studie popisuje pouze 14 zdokumentovaných současných výskytů chylothoraxu a nádoru žaludku. Zajímavé je, že společné pro všechny popisované pacienty bylo, že trpěli častěji klinickými potížemi respiračního původu, nikoliv gastrointestinálního. Průměrná doba přežití se dle různých autorů příliš neliší a pohybuje se v intervalu 4,3–4,5 měsíce (3, 5).
Patofyziologie vzniku chylothoraxu při karcinomu žaludku není objasněna. Jako možné vysvětlení se nabízí zvětšení lymfatických uzlin, které komprimují ductus thoracicus (4) nebo přítomnost metastatické lymfatické uzliny, která přímo invaduje do mízního kmene (6). Jiní autoři považují za příčinu přímou infiltraci tumorózních buněk do cirkulačního systému lymfy (7).
Závěr
Chylothorax je poměrně vzácná diagnóza jak v pneumologii, tak v interní medicíně. Objasnění jeho příčiny není snadné, obzvláště při koincidenci s adenokarcinomem žaludku, kde je diagnóza stanovena spíše per exclusionem. Druhostranný hydrothorax u námi popisovaného případu byl následkem souběžných příznaků onkologického onemocnění. Z doposud popsaných případů je zřejmé, že objeví-li se u pacienta chylothorax, neměli bychom z diferenciální diagnostiky vylučovat tumor žaludku ani v případě, že pacient netrpí gastrointestinálními potížemi, zejména pokud je přítomen i lymfedém.
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Nela Šťastná,
Klinika nemocí plicních a TBC,
Fakultní nemocnice Brno
Jihlavská 20,
625 00 Brno
Cit. zkr: Vnitř Lék 2020; 66(7): e43–e45
Článek přijat redakcí: 7. 3. 2020
Článek přijat po recenzích k publikaci: 15. 7. 2020
Sources
1. Drake RL, Vogl W, Mitchell AWM, et al. Gray‘s anatomy for students. Philadelphia: Elsevier/Churchill Livingstone 2005. ISBN 9780323611046.
2. Kašák V, Koblížek V, et al. Naléhavé stavy v pneumologii. 2. rozš. vyd. Praha: Maxdorf; 2009. ISBN 9788073451851.
3. Wu J, Lv L, Zhou K, et al. Chylothorax and lymphedema as the initial manifestations of gastric carcinoma: A case report and review of the literature. Oncol Lett 2016; 11(4): 2835–2838.
4. Devaraj U, Ramachandran P, Correa M, et al. Chylothorax in gastric adenocarcinoma: A case report and systemic review of the English literature. Lung India 2014; 31(1): 47–53.
5. Nagano N, Suzuki M, Tamura, et al. Refractory chylothorax and lymphedema caused by advanced gastric cancer. Intern Med 2019; 58 : 3143–3148.
6. Yoshizawa K, Sasaki Y, Abe Y, et al. Chylothorax in a patient with advanced gastric cancer and mediastinal lymph node metastasis causing thoracic duct obstruction. Nihon Shokakibyo Gakkai Zasshi 2013; 110(11): 1943–1949.
7. Majoor CJ, Aliredjo RP, Dekhuijzen PN, et al. A rare cause of chylothorax and lymphedema. J Thorac Oncol 2007; 2 : 247–248.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2020 Issue 7
-
All articles in this issue
- Koagulopatie asociovaná s onemocněním COVID-19
- Současná diagnostika a terapie sarkoidózy
- Obštrukčné spánkové apnoe a arteriálna hypertenzia: úloha črevného mikrobiómu
- CAR T-lymfocyty: horká novinka v léčbě nádorů
- Renální selhání u mnohočetného myelomu a jeho léčba
- Kostní metabolismus u idiopatických střevních zánětů 2
- Metformin -asociovaná laktátová acidóza
- Tangierská nemoc v rodině s fenotypem familiární hypercholesterolemie
- Hypoglykemie u nediabetiků
- Screening a krátká intervence u uživatelů nelegálních drog
- Kostní metabolismus u idiopatických střevních zánětů 1
- Etické konotace léčby onemocnění covid-19
- Biomarkery pro neendoskopické vyšetření sliznice jícnu
- Riziko kardiovaskulárních komplikací v závislosti na hladině glykemie: od diabetes mellitus k prediabetu
- ERCP u pacientů po choledochoduodenoanastomóze
- Přidělovaná ošetřovatelská péče jako jeden z indikátorů výskytu medikačního pochybení
- Raritní koincidence chylothoraxu a hydrothoraxu při adenokarcinomu žaludku – kazuistika
- Muž s dysthymií (převážně negativním hodnocením všeho prožitého) indukoval depresi u senzitivní blízké osoby
- Adenokarcinom tenkého střeva diagnostikovaný pomocí video kapslové endoskopie u pacientky s celiakií: kazuistika a přehled literatury
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Hypoglykemie u nediabetiků
- Metformin -asociovaná laktátová acidóza
- Koagulopatie asociovaná s onemocněním COVID-19
- CAR T-lymfocyty: horká novinka v léčbě nádorů
