Perindopril – dlouholetá jistota v léčbě hypertenze
Perindopril: a long-term certainty in treating hypertension
Blockade of the renin angiotensin aldosterone system (RAAS) is currently considered to be the gold standard of antihypertensive therapy. ACE inhibitors and AT1-blockers are clinically the most relevant groups of RAAS blockers. Even though both drug groups block angiotensin II, ACE inhibitors typically reduce the degradation of bradykinin, which leads to the release of nitric oxide and prostaglandins with subsequent vasodilation. These differences in the mechanism of action can be of clinical relevance for hypertensive patients. Morbidity mortality studies of RAAS blockers have been reported in which ACE inhibitors, particularly perindopril, improved the overall survival in hypertensive patients. In the ONTARGET trial, a direct comparison of both drug groups yielded comparable results. Perindopril, which has been used in the clinical practice for more than 25 years, is a long-acting lipophilic angiotensin-converting enzyme inhibitor with a once-daily dosage schedule and a high affinity to tissue-converting enzyme. Its safety, efficacy, and very good tolerance have been shown in a number of studies. It is part of many fixed combinations which improve patient compliance and increase the effect of treatment of cardiovascular diseases.
Keywords:
hypertension – RAAS system – ACE inhibitors – AT1-blockers – fixed combination
Authors:
Miroslav Souček
Authors‘ workplace:
II. interní klinika Fakultní nemocnice u sv. Anny v Brně a Lékařské fakulty Masarykovy univerzity, Brno
Published in:
Vnitř Lék 2021; 67(2): 119-124
Category:
Overview
Blokáda systému renin‑angiotenzin‑aldosteron (RAAS) je v současné době považována za standard antihyperetenzní léčby. Klinicky nejdůležitější zástupci farmak blokujících RAAS jsou inhibitory ACE (ACEI) a AT1-blokátory. I když obě lékové skupiny blokují angiotenzin II, charakteristickou vlastností ACEI je snížení degradace bradykininu vedoucí k uvolňování oxidu dusnatého a prostagladinů s následnou vazodilatací. Tyto odlišnosti v mechanismu účinku mohou mít pro hypertoniky klinický význam. Uvedeny jsou morbidně‑mortalitní studie s blokátory RAAS, kde ACEI, především perindopril, zlepšily celkové přežití hypertoniků. Ve studii ONTARGET přímé srovnání obou skupin vyšlo srovnatelně. Perindopril, který je v klinické praxi využíván déle než 25 let, je dlouhodobě působící lipofilní inhibitor angiotenzin konvertujícího enzymu s jednodenním dávkováním a vysokou afinitou ke tkáňovému konvertujícímu enzymu. Jeho bezpečnost, účinnost a velmi dobrá tolerance je ověřena v mnoha studiích. Je součástí řady fixních kombinací, které zlepšují compliance nemocného k léčbě a zvyšují účinky léčby kardiovaskulárních (KV) chorob.
Klíčová slova:
hypertenze – systém RAAS – inhibitory ACE – AT1-blokátory – fixní kombinace
Úvod
I přes významné pokroky v léčbě zůstávají KV choroby v moderním světě hlavní příčinou mortality a pracovní neschopnosti. Kvalitnější léčba hypertenze jako významného KV rizikového faktoru zajišťuje prevenci KV chorob nebo zpomaluje rozvoj stávajícího KV onemocnění u široké škály pacientů. Cílem léčby hypertenze je prevence cévních mozkových příhod, ochrana před infarktem myokardu a především snížení mortality. Proto musíme hledat léky, které nejen snižují krevní tlak (TK), ale zmírňují i KV riziko, a to z hlediska morbidity a mortality (1). I když jsou dnes po celém světě široce využívány k léčbě hypertenze inhibitory angiotenzin konvertujícího enzymu (ACEI) a blokátory receptoru AT₁ pro angiotenzin II (AT₁-blokátory, sartany), je důležité nepovažovat tyto dvě třídy léků za zaměnitelné, protože jen u několika málo přípravků byla prokázána účinnost při snižování mortality pacientů s hypertenzí.
Inhibice systému renin ‑ angiotenzin ‑ aldosteron
V současných doporučeních pro diagnostiku a léčbu hypertenze je blokáda RAAS považována za základ antihypertenzní léčby, první volbu v léčbě hypertenze a v léčbě specifických závažných indikací (infarkt myokardu, srdeční selhání, proteinurie), při poškození konkrétních cílových orgánů (hypertrofie levé komory, mikroalbuminurie) nebo v případě přidružených rizikových faktorů (diabetes mellitus) (2). Nadměrná aktivita RAAS vede k excesivní vazokonstrikci, která je spojena s hypertenzí, poškozením ledvin, aterosklerózou a dysfunkcí levé komory. Tyto choroby jsou spojeny s vysokou hladinou tkáňového ACE. Klinicky nejdůležitějšími zástupci farmakologických látek blokujících RAAS jsou v současné době ACEI a AT₁-blokátory.
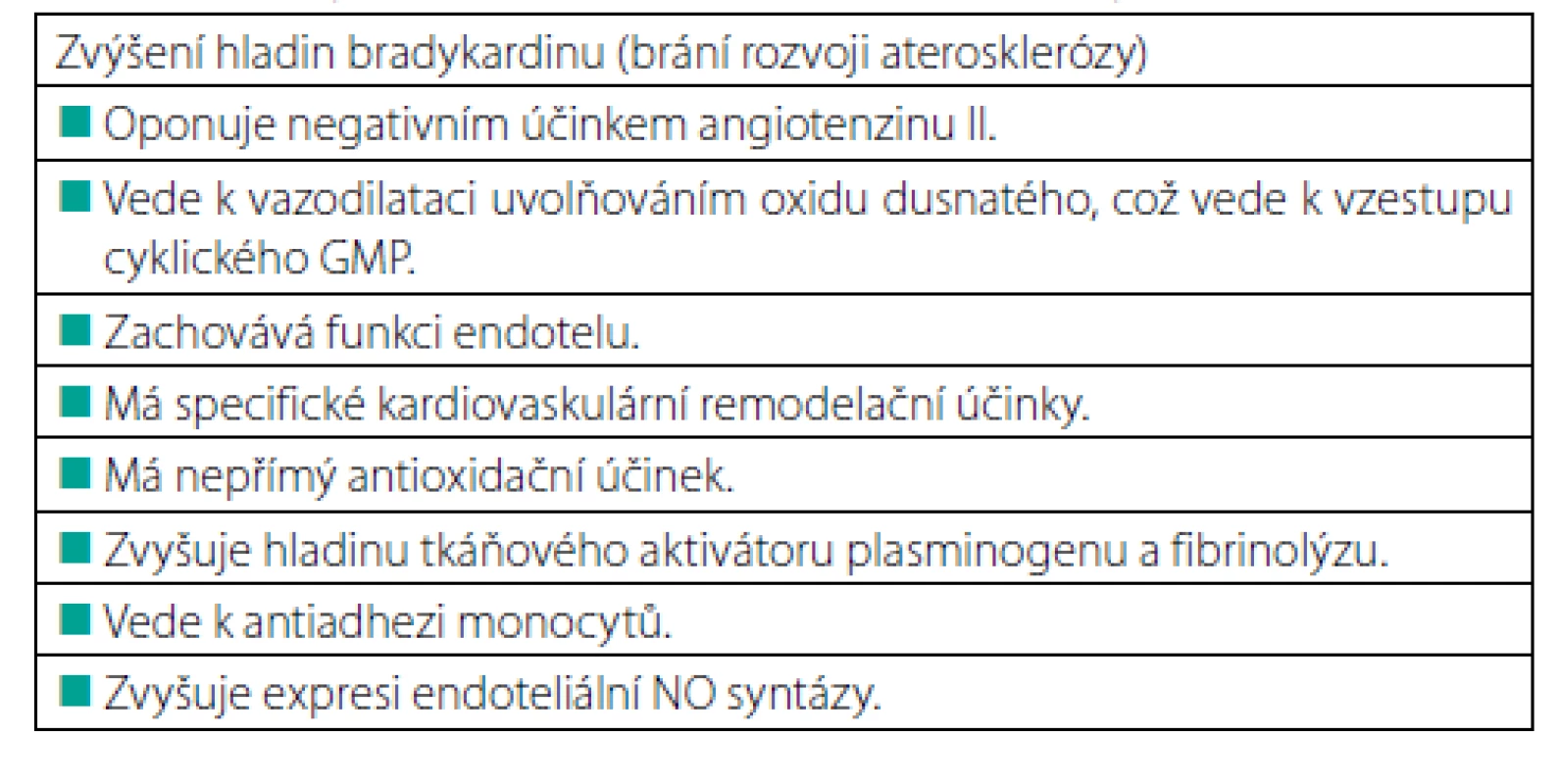
Inhibitory ACE jsou důležitými léky využívanými v léčbě arteriální hypertenze, v terapii a profylaxi dysfunkce levé komory srdeční a v prevenci progrese nefropatie (především diabetické). Inhibují konverzi angiotenzinu I na angiotenzin II (jenž má vazokonstrikční a mitogenní účinky, stimuluje uvolnění aldosteronu a vede též k uvolnění noradrenalinu) a zpomalují odbourávání bradykininu (s vlastní vazodilatační aktivitou, danou stimulací NO syntázy). Výsledkem je pokles periferní cévní rezistence, mírný venodilatační, natriuretický a diuretický účinek a zlepšení endoteliální dysfunkce (Tab. 1).
AT₁-blokátory jsou pak indikovány k léčbě arteriální hypertenze, kardiální insuficience a ke zpomalení progrese dysfunkce levé komory srdeční. Mechanismus jejich působení spočívá v kompetitivním antagonismu angiotenzinu II na AT1-receptorech – jejich účinek se tak projevuje i v případech, kdy dochází ke konverzi angiotenzinu II jinými cestami než prostřednictvím ACE. Nezpomalují tedy degradaci bradykininu (ani dalších vazoaktivních peptidů), což jednak souvisí s jejich lepší snášenlivostí (nižší výskyt kašle a angioedému), zároveň je však tímto oslaben přídatný antihypertenzní (vazodilatační) účinek bradykininu. Je proto velmi pravděpodobné, že AT1-blokátory nejsou plně rovnocenné ACEI.
Důležitá role ACEI byla prokázána celou řadou klinických studií u širokého spektra pacientů.
Inhibitory RAAS a celková mortalita
Je zřejmé, že antihypertenzní léčba vede k poklesu jak KV, tak cerebrovaskulární mortality a že blokáda RAAS (ACEI a AT1-blokátory) hraje v tomto ohledu významnou roli. Otázkou zůstává, jaký vliv mají antihypertenziva na snížení celkové mortality u pacientů s hypertenzí, jako nejtvrdšího parametru léčby hypertenze, a zda ve vlivu na celkovou mortalitu existují rozdíly mezi jednotlivými antihypertenzivy. Odpověď na tuto důležitou otázku přinesla alespoň z části metaanalýza prof. Bertranda a kolektivu holandských autorů (3). Jednalo se o největší metaanalýzu na poli hypertenze, do které bylo zařazeno 20 morbiditně‑mortalitních studií s inhibitory RAAS s 158 998 pacienty (7 studií s ACEI a 13 studií s AT₁-blokátory). Průměrná doba sledování byla 4,3 roky. Zavzaty byly všechny studie s inhibitory RAAS provedené v letech 2000–2011, kde alespoň u 2/3 pacientů byla stanovena diagnóza hypertenze a celková mortalita musela být předem definovaným sledovaným parametrem. Vyřazeny byly studie se srdečním selháním, akutními koronárními syndromy, hemodialýzou, fibrilací síní a studie, v nichž byly inhibitory RAAS podávány současně v obou větvích (důvod vyřazení studií INVEST, ACCOMPLISH a ONTARGET). Cílem metaanalýzy bylo zhodnotit vliv inhibitorů RAAS na další snížení celkové mortality v jejich hlavní indikaci hypertenze. Studie byly vybrány tak, aby zařazení pacienti s hypertenzí byli léčeni moderní terapií včetně statinů a protidestičkových preparátů, a tvořili tak reprezentativní vzorek pacientů, s kterými se setkáváme v běžné praxi.
Základní otázkou studie bylo, zda je snížení celkové mortality závislé na typu léčby a která antihypertenziva blokující RAAS se jeví z tohoto pohledu jako nejvýhodnější. V souhrnné analýze všech 20 studií byla inhibice RAAS spojena s 5% snížením celkové mortality a se 7% snížením KV mortality. I když obě lékové skupiny blokují angiotenzin II, charakteristickou vlastností ACEI je snížení degradace bradykininu vedoucí k uvolňování oxidu dusnatého a prostaglandinů s následnou další vazodilatací. Tyto odlišnosti v mechanismu účinku mohou mít pro hypertoniky klinický význam. Proto byly také ACEI a AT₁-blokátory hodnoceny odděleně (Obr. 1, 2).
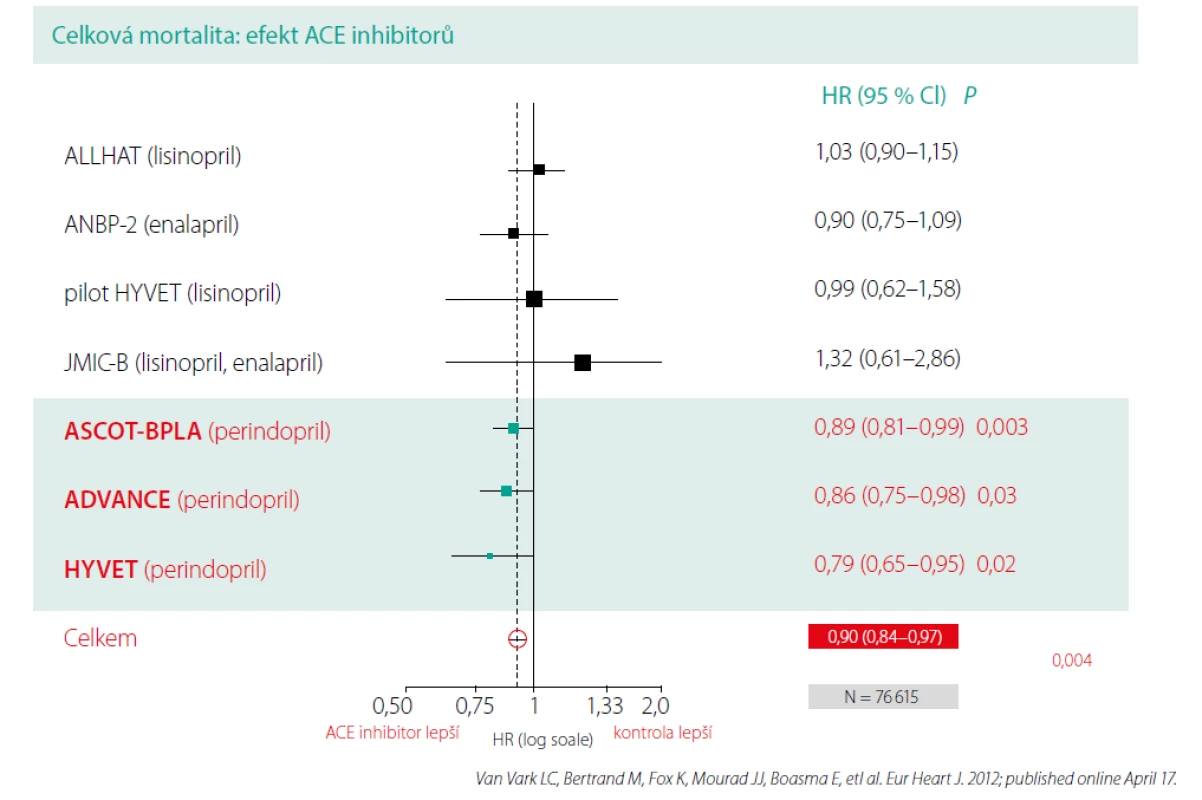
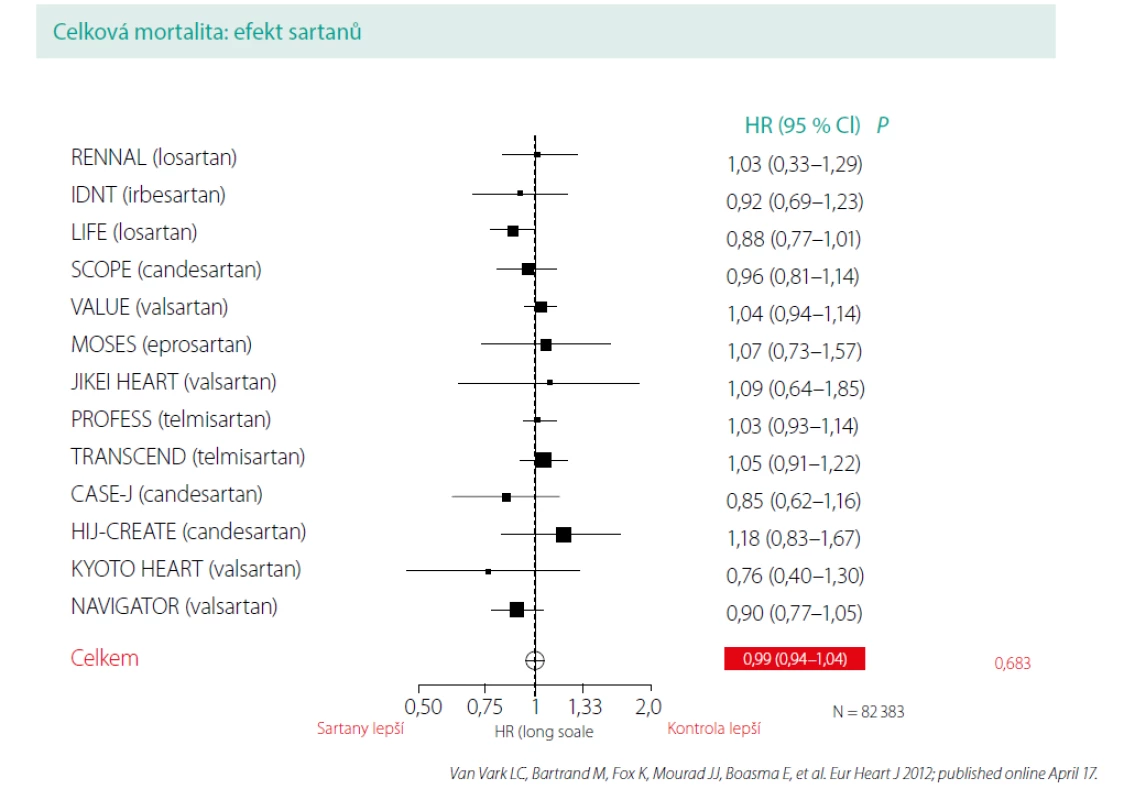
V následné analýze 7 studií z tohoto souboru, ve kterých byl v aktivním ramenu použit inhibitor ACE, ALLHAT, ANBP-2, pilot HYVET, JMIC‑B, ASCOT‑BPLA, ADVACE a HYVET (v pěti ze sedmi z nich tvořili hypertonici 100 % souboru), byl zjištěn rozdílný účinek jednotlivých ACEI na snížení celkové mortality, přičemž pouze léčba obsahující ACEI perindopril byla spojena se statisticky významných poklesem celkové mortality (RRR: 13 %; p < 0,001). Inhibitory ACE souhrnně snížily celkovou mortalitu o 10 %, z čehož je patrné, že benefit celé skupiny ACEI byl dán výsledky studií s perindoprilem. AT₁-blokátory snížení celkové mortality neprokázaly. Rozdíl mezi ACEI a AT₁-blokátory byl statisticky významný. Signifikantní rozdíl mezi léčebnými rameny byl zaznamenán pouze ve třech studiích, a sice ASCOT‑BPLA, HYVET a ADVANCE, v nichž došlo ke snížení celkové mortality o 11–21 % (v průměru o 13 %).
První studie představuje významný mezník v hodnocení různých typů léčby. Zahrnuje více než 19 000 starších pacientů se třemi a více rizikovými faktory. Porovnávala v randomizované studii léčbu, opírající se o dihydropyridinový blokátor kalciových kanálů (BKK) amlodipin, kombinovaný podle potřeby s ACEI perindoprilem, s léčbou opírající se o atenolol, kombinovaný podle potřeby s diuretikem bendroflumethiazidem. Studie byla předčasně ukončena pro významný rozdíl v celkové mortalitě (11 %) ve prospěch novějších léků (amlodipin s perindoprilem) oproti starším lékům atenolol s bendroflumethiazidem. Většina nemocných byla léčena kombinační léčbou. Kombinační léčba amlodipinem s perindoprilem významně snížila rovněž KV mortalitu o 24 %, fatální a nefatální cévní mozkové příhody o 23 %, výskyt nestabilní anginy pectoris o 32 % a onemocnění periferních tepen o 35 %. Kombinace amlodipin s perindoprilem se ukázala vhodnější než kombinace s betablokátorem a diuretikem i v ovlivnění nově vzniklého diabetes mellitus (DM) (4). Studie HYVET představuje první prospektivní, dvojitě zaslepenou studii hodnotící účinnost antihypertenzní léčby ve věkové skupině 80 let a více. Bylo randomizováno 3 845 pacientů v průměrném věku 83,6 let na aktivně léčenou skupinu a na placebovou skupinu. Aktivní léčbu tvořil retardovaný indapamid v dávce 1,5 mg. K aktivní léčbě mohl být přidán perindopril v dávce 2 mg nebo 4 mg, pokud nebylo dosaženo cílových hodnot TK pod 150/80 mm Hg. Po dvou letech trvání studie byl průměrný TK vsedě v aktivně léčené skupině o 15,0/6,1 mm Hg nižší oproti placebové skupině. Cílových hodnot TK bylo dosaženo téměř u 50 % pacientů. Studie byla předčasně ukončena pro významný rozdíl v celkové mortalitě a ve výskytu fatálních cévních mozkových příhod ve prospěch aktivně léčené skupiny. Celková mortalita byla snížena o 21 % (p = 0,02), výskyt fatálních cévních mozkových příhod o 39 % (p = 0,045) a incidence srdečního selhání o 64 % (p < 0,001). Studie HYVET přináší velmi důležité důkazy o tom, že léčba hypertenze u velmi starých osob, která je založena na indapamidu, ke kterému byl u více než 70 % pacientů přidán perindopril, přináší výrazně příznivý účinek těmto nemocným a vede ke snížení rizika úmrtí ze všech příčin, snížení fatálních cévních mozkových příhod a snížení incidence srdečního selhání (5). Studie ADVANCE byla koncipována jako randomizovaná, prospektivní, multicentrická a placebem kontrolovaná. Do studie byli zařazeni pacienti s diabetem 2. typu starší 55 let. Pro zařazení museli mít nejméně jeden rizikový faktor pro rozvoj KV komplikací, nebo u nich musela být přítomna nejméně jedna mikrovaskulární či makrovaskulární komplikace DM. Kombinace indapamidu s perindoprilem snížila KV mortalitu o 18 %, celkovou mortalitu o 14 %, snížila relativní riziko koronárních příhod o 14 % (6). Ve všech těchto studiích, které prokázaly snížení celkové mortality, byl použit perindopril.
Samozřejmě jako všechny klinické práce také tato metaanalýza má své limitace. Především jsou to rozdíly mezi jednotlivými studiemi zařazenými do metaanalýzy – rozdíly v definici hypertenze, dávkování léků, cílových hodnotách TK, době sledování a doprovodné léčbě. Tato analýza byla založena spíše na studijních datech než na údajích o pacientech. Informace o základní terapii a dalších onemocněních nebyly v některých případech dostupné. Na počátku metaanalýza předpokládala „class effect“ mezi ACEI a sartany, ale k tomu, aby se prokázala rozdílnost léků v dané skupině, chybí statistická síla.
Přesto na základě výsledků této metaanalýzy lze konstatovat, že pouze ACEI prokázaly signifikantní snížení o 10 % celkové mortality u pacientů s hypertenzí, zatímco sartany ovlivnění celkové mortality neprokázaly. Z výsledků metaanalýzy lze také vyvodit, že terapie ACEI může zachránit 12 životů na 1 000 pacientů léčených po dobu 4 let, a je potřeba si uvědomit, že i toto relativně mírné ovlivnění celkové mortality má ve skutečnosti dopad na širokou populaci hypertoniků. Z tohoto pohledu se dá říci, že v léčbě hypertoniků je významný nejen samotný pokles TK, ale také skutečnost, jakou látkou jej dosáhneme.
Na základě výsledků této metaanalýzy vznikla otázka, zda tento rozdíl může být i v léčbě hypertenze u pacientů s DM. Pacienti s DM mají 2–4× vyšší výskyt KV onemocnění ve srovnání s pacienty bez DM. Vzhledem k tomu, že nemáme dostatek dat pro přímé srovnání obou skupin, bylo v metaanalýze Chenga a spol. využito srovnání ACEI a AT₁-blokátorů s placebem nebo jinou terapií v ovlivnění celkové mortality, KV mortality a výskytu KV příhod u pacientů s DM (7). Inhibitory ACE vedly ke statisticky významnému poklesu celkové mortality o 13 %. Výsledky byly podobné, jestliže se ACEI srovnávaly s placebem nebo jinou aktivní léčbou. Dále bylo zaznamenáno 17% snížení počtu KV úmrtí ve srovnání s kontrolami. Při léčbě AT₁-blokátory nedošlo k signifikantnímu poklesu celkové mortality ani ve srovnání s placebem, ani ve srovnání s aktivní léčbou. Taktéž v sekundárních ukazatelích vedla léčba inhibitory ke snížení rizika infarktu myokardu o 21 % a srdečního selhání o 19 %. Výskyt cévních mozkových příhod nebyl ovlivněn. Léčba AT₁-blokátory neměla vliv ani na sekundární ukazatele – tj. na výskyt infarktu myokardu a cévních mozkových příhod. Co vyšlo pozitivně, byl výskyt srdečního selhání, kde bylo pozorováno příznivé ovlivnění AT₁-blokátory o 30 %. Lze tedy konstatovat, že ACEI příznivě ovlivňují celkovou mortalitu, KV mortalitu i výskyt KV příhod ve srovnání s AT₁-blokátory i u pacientů s DM.
Rozdíly v ovlivnění celkové mortality při použití různých antihypertenziv, a především jednotlivých inhibitorů RAAS, mohou být dány odlišnostmi v jejich farmakodynamice a farmakokinetice: ACEI mají různý stupeň afinity ke tkáňovému ACE (stupeň vazby ke tkáňovému ACE zřejmě souvisí s organoprotektivním působením ACEI) (8) a k angiotenzinu I, resp. bradykininu (bradykinin je zodpovědný za značnou část kardioprotektivního účinku ACEI (9). V obou těchto případech je afinita perindoprilu oproti dalším srovnávacím ACEI nejvyšší. A právě maximální hladiny cirkulujícího bradykininu při léčbě perindoprilem mohou vést ke snížení celkové mortality hypertoniků, v porovnání se sartany, které hladinu bradykininu neovlivňují a jejich efekt na celkovou mortalitu tak prokázán nebyl. Další rozdíly můžeme hledat v lipofilních vlastnostech sledovaných antihypertenziv. Dále se perindopril vyznačuje velmi dobrou 24hodinovou antihypertenzní účinností s vysokým poměrem trough‑to‑peak.
Další jedinečnou vlastností ACEI je, že na rozdíl od ARB zvyšují množství bradykininu. Bradykinin snižuje jak agregaci trombocytů, tak hladinu cirkulujícího inhibitoru aktivátoru plazminogenu 1 (PAI-1), což je významný inhibitor fibrinolýzy. Bradykinin je také jedním z nejsilnějších stimulátorů aktivátoru tkáňového plazminogenu. Bradykinin má vazodilatační účinky zprostředkované vyplavením prostacyklinu, NO a hyperpolarizačního faktoru odvozeného od endotelinu (EDHF). Bradykinin má i silný antiapoptotický účinek na endotel, což přispívá k zachování jeho celistvosti a funkce (9, 10). Sérum odebrané pacientům s ischemickou chorobou srdeční, jimž byly v sekundární prevenci podávány ACEI, vykazuje snížené koncentrace von Willebrandova faktoru, který je měřítkem dysfunkce endotelu a má bradykininem zprostředkovaný antiapoptotický účinek na izolované lidské endotelové buňky (8). Další důkazy o naprosto zásadním podílu bradykininu na kardioprotekci zajišťované ACEI pocházejí z experimentálních prací, které prokázaly, že kombinace ACEI s antagonisty pro bradykinin B2 vede k vymizení všech kardioprotektivních účinků (11). Přirozený účinek na bradykinin (zesilovaný ACEI, ne však AT₁-blokátory) není jediným důvodem pro rozdíly zjištěné v metaanalýzách. Selektivní působení AT₁-blokátorů na AT₁-receptory ponechává ostatní receptory pro angiotenzin volné pro obsazení angiotenzinu II, jehož tvorba není AT₁-blokátory ovlivněna. Výsledkem je „receptorový posun“ se sníženou aktivitou AT₁ receptorů a zvýšenou aktivitou AT2 receptorů, které vykazují proapoptotické a protirůstové účinky na endotel (12). Zdá se, že toto ovlivňování apoptózy endotelových buněk, které je potlačováno bradykininem a zvyšováno AT2-receptory, je jedním z hlavních rozdílů mezi ACEI a AT₁-blokátory (13).
Inhibitory ACE i AT₁-blokátory tlumí účinky angiotenzinu II, každý svým jedinečným mechanismem. Inhibitory ACE snižují syntézu angiotenzinu II, zatímco ARB se kompetitivně a selektivně vážou na AT1-receptory, čímž brání jejich aktivaci prostřednictvím angiotenzinu II. V důsledku blokády AT1 zvyšují sartany hladinu angiotenzinu II na několikanásobek původní hodnoty. Zvýšená hladina cirkulujícího angiotenzinu II vede k nekontrolované stimulaci receptorů AT2. Předpokládalo se, že AT2-receptory zprostředkovávají vazodilataci a vyplavení oxidu dusnatého.
Bohužel poslední údaje naznačují, že stimulace AT2-receptorů může být méně výhodná, než jsme se původně domnívali, a může být dokonce za určitých okolností nežádoucí. Mezi nepříznivé mechanismy patří podpora růstu, fibrotizace a hypertrofie a proaterogenní a prozánětlivé účinky. Podle posledních výsledků by mohl angiotenzin II přispívat k rupturám plátů zvýšením množství MMP-1 (na leukocytech závislá matrixová metaloproteináza 1) cestou AT2-receptorů, které se nacházejí také v leukocytech. MMP-1 způsobuje snížení zásob kolagenu a další apoptózu buněk v ateromových plátech pokročilejších stadií tím, že brání růstu hladkých svalových buněk cév (14).
Zatím jediná studie, která srovnávala napřímo ACEI a sartan, byla studie ONTARGET, která srovnávala ramipril vs. telmisartan. Cílem bylo zhodnotit, zda je telmisartan podobně účinný jako ramipril v prevenci vaskulárních příhod u pacientů s prokázaným vaskulárním onemocněním či diabetem. Ve studii bylo celkem 25 620 pacientů. Telmisartan zde vyšel srovnatelně s ramiprilem v porovnání celkového cíle studie, což bylo snížení úmrtí z KV příčin, snížení počtu příhod infarktů myokardu, cévních mozkových příhod nebo hospitalizace. Telmisartan byl ve studii účinnější ve snížení TK, ale nebyl zároveň účinnější i ve snížení KV příhod, kde vyšel srovnatelně s ramiprilem (15).
Perindopril, který byl spojen se statisticky významných poklesem celkové mortality, je již více než 25 let účinným a úspěšným lékem řady KV onemocnění. Několik preklinických studií ukázalo, že ACEI mají i antiaterosklerotický efekt (16). Studie PERSPECTIVE (The PERindoril’s Prospective Effect on Coronary aTherosclerosis by IntraVascular ultrasound Evaluation), jako podstudie EUROPY, prokázal příznivý účinek dlouhodobého podávání perindoprilu na velikost koronární plátů, hodnoceno intrakoronárním ultrazvukem (IVUS) (17). Perindopril je tedy využíván nejen v léčbě hypertenze, ale i srdečního selhání, ischemické choroby srdeční, u léčby cerebrovaskulárních příhod a léčby DM.
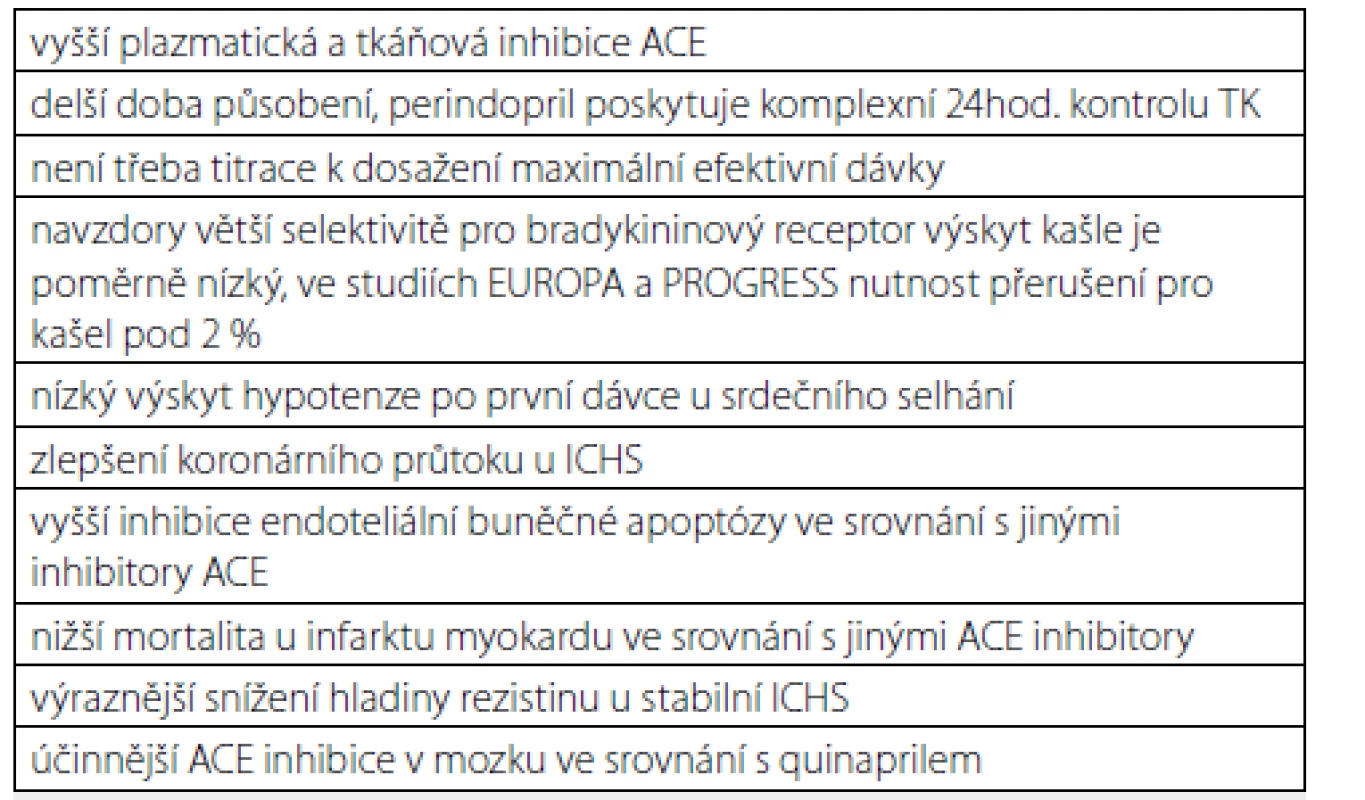
Jaké jsou jeho výhody ve srovnání s ostatními ACEI, uvádí tabulka 2.
Perindopril je ale v klinické praxi využíván především v léčbě hypertenze. Kde jsou jeho hlavní výhody? (18)
Hlavní výhoda perindoprilu v léčbě hypertenze je tam, kde je žádoucí remodelace srdeční a cévní:
při hypertrofii levé komory,
při srdečním selhání a dysfunkci levé komory srdeční,
u stavů po infarktu myokardu (IM),
u stavů po cévní mozkové příhodě (CMP),
při ischemické chorobě dolních končetin,
při diabetické a nediabetické nefropatii,
při proteinurii.
Tam, kde je žádoucí nezhoršit metabolické poměry:
při diabetes mellitus – především 1. typu,
při hyperlipoproteinemii.
S vydáním nových doporučení pro diagnostiku a léčbu hypertenze se klade důraz především na kombinační terapii, a to zvláště fixní, kde má perindopril dominantní postavení.
Kombinovaná léčba antihypertenzivy s odlišným (a vzájemně se doplňujícím) mechanismem působení je považována za nejvýhodnější strategii při nedostatečné kontrole hypertenze.
Nejvíce preferovanou kombinací je současné podávání ACEI s blokátory kalciových kanálů (BKK) nebo diuretiky. Díky aditivnímu antihypertenznímu efektu, který je provázen menším množstvím nežádoucích účinků, tuto strategii upřednostňujeme před podáváním jednoho léčiva ve vysoké dávce. V důkladné metaanalýze 42 studií bylo dokonce prokázáno, že léčba dvojkombinací antihypertenziv základních skupin je přibližně 5× účinnější než zdvojnásobení dávky jednoho léčiva (19). Metaanalýza Bangaloreho et al pak prokázala, že podávání léků ve fixní kombinaci je asi 1,5× účinnější než podávání stejných léků v jednotlivých tabletách (20). Perindopril s řadou dalších přípravků snižujících TK, ochraňujících selhávající myokard či s hypolipidemickým účinkem tak výrazně zlepšuje nejen přístup nemocných k léčbě (compliance), ale také zlepšuje léčebné výsledky KV onemocnění.
Závěr
Ovlivnění systému renin‑angiotenzin je považováno za jeden z nejkomplexnějších způsobů léčby pacientů nejen u pacientů s hypertenzí, ale i dalších KV onemocnění. V porovnání s jinými ACEI je za nejdůležitější výhodu léčby perindoprilem pokládán jeho pomalý nástup a dlouhá doba účinku. Ve srovnání s dalšími představiteli ACEI druhé generace je předností výrazný antihypertenzní potenciál, kterého je dosaženo již dávkou 5 mg. Dosud nashromážděné údaje porovnávají jednotlivě přínos ACEI a AT₁-blokátorů z hlediska účinného snižování TK, snížení KV a celkové mortality, snížení výskytu cévních mozkových příhod a infarktu myokardu, inhibice diabetického postižení ledvin, zmírnění příznaků městnavého srdečního selhání a prevence nově vzniklého diabetu a fibrilace síní.
Metaanalýzy, které porovnávaly účinky ACEI a AT₁-blokátorů, téměř všechny dospěly k závěru, že zatímco ACEI zabraňují vzniku koronárních příhod se současným snížením sledovaných parametrů KV morbidity a mortality, AT₁-blokátory jsou, v nejlepším případě, účinné v prevenci cévních mozkových příhod. Největší význam perindoprilu v současné době tkví ve fixních kombinacích s indapamidem, amlodipinem, bisoprololem a/nebo atorvastatinem. Fixní kombinace je výhodná v podstatě u všech pacientů s KV postižením. Tyto fixní kombinace mají dokumentovaný 24hodinový účinek všech složek a mají teoretické předpoklady i jasné důkazy pro to, že jsou účinné nejen v léčbě hypertenze, ale i dalších KV onemocnění.
KORESPONDENČNÍ ADRESA AUTORA:
prof. MUDr. Miroslav Souček, CSc.
II. interní klinika Fakultní nemocnice u sv. Anny v Brně
Pekařská 664/53
656 91 Brno
Cit. zkr: Vnitř Lék 2021; 67(2): 119–124
Článek přijat redakcí: 18. 11. 2020
Článek přijat po recenzích: 10. 3. 2021
Sources
1. Widimský J jr, Filipovský J, Ceral J et al. Doporučení pro diagnostiku a léčbu arteriální hypertenze ČSH 2017. Hypertenze & kardiovaskulární prevence 2018; 7 (Suppl): 1 – 22.
2. Mancia G, Fagard R, Narkiewicz K, et al. 2013 ESH/ESC Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J Hypertens 2013; 31 : 1281–1357.
3. Van Vark L, Bertrand M et al. Angiotensin ‑ converting enzyme inhibitors reduce mortality in hypertension: a meta‑analysis of randomized clinical trials of RAAS inhibitors involving 158 998 patients.Eur Heart J, 2012; 33 : 2088–2097.
4. Dahlöf B, Sever PS, Poulter NE et al, for the ASCOT Investigators. Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo‑Scandinavian Cardiac Outcomes Trial‑Blood Pressure Lowering Arm (ASCOT‑BPLA). Lancet. 2005; 366 : 895–906.
5. Beckett NS, Peters R, Fletcher AE et al. for the HYVET Study Group. Treatment of hypertension in patients 80 years of age or older. N Engl J Med 2008; 358 : 1887–1898.
6. ADVANCE Collaborative Group. Effects of a fixed combination of perindopril and indapamide on macrovascular and microvascular outcomes in patients with Type 2 dibetes mellitus (the ADVANCE trial): a randomised controlled trial.Lancet 370,829-840(2007).
7. Cheng J, Zhang W, Zhang X et al. Effect of angiotensin‑converting enzyme inhibitors and angiotensin II receptor blockers on all ‑ cause mortality, cardiovascular deaths, and cardiovascular events in patients with diabetes mellitus. JAMA Intern Med 2014; 174 : 773–785.
8. Ferrari R. Angiotensin ‑ converting enzyme inhibition in cardiovascular disease: evidence with perindopril. Expert rev Cardiovasc Ther 2005; 3 : 15–29.
9. Ceconi C, Fox KM, Remme WJ et al. ACE inhibition with perindopril and endothelial dysfunction. Results of a substudy of the EUROPA study; PERTINENT. Cardiovasc Res 2007; 73 : 237–246.
10. Ferrari R, Fox K. Insight into the mode of action of ACE inhibition in coronary artery disease: the ultimate „EUROPA“ story. Drugs 2009; 69 : 265–277.
11. Cargnoni A, Comini L, Bernocchi P et al. Role of bradykinin and eNOS in the anti‑ischaemic effect of trandolapril. Br J Pharmacol 2001; 133 : 145–153.
12. Unger T. Pharmacological properties of angiotensin II antagonists: examining all the therapeutic implications. J Renin Angiotensin Aldosterone Syst 2001; 2(Suppl.2): S4–7.
13. Ferrari R, Rosano GM. Nejen čísla, ale roky vědecké práce: meta‑analýzy porovnání ACE inhibitorů a AT1-blokátorů v kontextu. Int J Cardiology 2013; 166(2): 286–288.
14. Souček M. Účinek inhibitorů ACE a AT1-blokátorů na pokles celkové mortality u pacientů s hypertenzí, diabetes mellitus a bez srdečního selhání. Diabetologie, metabolismus, endokrinologie, výživa 2017 (20) 1 : 7–14.
15. Mann JF, Anderson C, Gao P et al. Dual inhibition of the renin‑angiotensin systém in high‑risk diabetes and risk for stroke and other outcomes: results of the ONTARGET trial. J Hypertens 2013; 31 : 141–421.
16. Hayek T, Hamoud S, Keidar S et al. Omapatrilat decreased macrophage oxidative status and atherosclerosis progression in atherosclerotic apolipoprotein E‑deficient mice. J Cardiovasc Pharmacol 2004; 43 : 140–147.
17. Rodriguez -Granillo GA, Vos J, Bruining N et al. Long term effect of perindopril on coronary atherosclerosis progression (from the PERindopril’s Prospective Effect on Coronary aTherosclerosis by Angiography and IntraVascular Ultrasound Evaluation (PERSPECTIVE Study). Am J Cardiol 2007; 100 : 159–163.
18. Vítovec J, Špinar J, Špinarová L. Perindopril a léčba kardiovaskulárních onemocnění aneb 25 let úspěšného působení perindoprilu v kardiologii. Kardiol Rev Int Med 2018; 20(3): 218–222.
19. Wald DS, Law M, Morris JK et al. Combination therapy versus monotherapy in reducing blood pressure: meta‑analysis on 11,000 participants from 42 trials. Am J Medicine 2009; 122(3): 290 – 300. doi: 10.1016/ j.amjmed.2008. 09. 038.
20. Bangalore S, Kamalakkannan G, Parkar S et al. Fixed‑dose combinations improve medication compliance: a meta‑analysis. Am J Med 2007; 120(8): 713 – 719. doi: 10.1016/ j.amjmed. 2006. 08. 033.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2021 Issue 2
-
All articles in this issue
- Immunoglobulin G4-related disease in gastroenterology
- Diagnostics and therapy of chronic pancreatitis according to UEG guidelines
- Extraintestinal complications of inflammatory bowel diseases
- Current view of diagnosis and treatment of latent autoimmune diabetes in adults
- Glucagon in treatment of hypoglycemia – novelties
- Hemodynamic significant pericardial effusion as a possible rare extraintestinal manifestation of Crohn’s disease
- Massive pulmonary embolism with a large thrombus stuck in patent foramen ovale – an impending paradoxical embolism
- Perindopril: a long-term certainty in treating hypertension
- Hlavní téma: gastroenterologie
-
How to prolong the lives of our patients in health?
And is it possible?
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Diagnostics and therapy of chronic pancreatitis according to UEG guidelines
- Glucagon in treatment of hypoglycemia – novelties
- Perindopril: a long-term certainty in treating hypertension
- Extraintestinal complications of inflammatory bowel diseases
