Můžeme novou léčbou ovlivnit dosavadní terapií neřešený zánět a fibrózu u pacientů s DM2 a CKD?
Authors:
Milan Kvapil
Authors‘ workplace:
Interní klinika 2. LF UK a FN Motol
Published in:
Vnitř Lék 2022; 68(7): 475-478
Category:
Advertorial
Úvod
Diabetické onemocnění ledvin (Diabetic Kidney Disease, DKD) je chronické onemocnění ledvin (Chronic Kidney Disease, CKD) vznikající na podkladě specifických morfologických a funkčních změn ledvin u nemocných s diabetem 1. i 2. typu, případně s ostatními typy diabetu při nepřítomnosti známek přítomnosti jiné choroby, která by mohla být příčinou poškození funkce ledvin.
DKD se manifestuje dvěma základními příznaky (v čase progredující patologicky zvýšená albuminurie a snižující se glomerulární filtrace). Ty se ve své intenzitě kombinují podle základní příčiny vzniku DKD.
DKD zahrnuje řadu klinických podjednotek, mezi nimiž nejvýznamnější místo zaujímá přímý důsledek hyperglykemie – starším názvoslovím diabetická nefropatie (DN).
DKD patří mezi časté komplikace DM 1. i 2. typu a je nejčastější příčinou chronického renálního selhání (CHRI) ve většině států světa včetně České republiky. Prevalence DKD u diabetiků 1. typu je asi 30 % po 20 letech trvání choroby a asi u 50 % z nich dochází k terminálnímu selhání ledvin do deseti let od nástupu onemocnění.
Etiopatogeneticky (klasická diabetické nefropatie) jde o glomerulopatii vznikající na podkladě mikroangiopatie a obecně změn vaskulárních, resp. makroangiopatie. Důsledkem hyperglykemie jsou oxidační stres a glykace proteinů. K rozvoji přispívá i hypertenze (typicky se vyskytující u diabetu 2. typu), dyslipidemie. Rizikové faktory způsobují ztluštění glomerulární bazální membrány, expanzi mesangia, fibrotické změny vas afferens a vas efferens. Funkčním důsledkem jsou porucha hemodynamiky glomerulu, zvýšená propustnost glomerulární membrány a hyperfiltrace. Změny mohou být difuzní i pouze fokální.
Typickým klinickým nálezem u DN je perzistentní albuminurie (> 300 mg/24 hod. nebo > 200 mg/min) s postupným zhoršováním renální funkce (glomerulární filtrace). Při proteinurii nad 500 mg za 24 hodin je téměř u všech diabetiků přítomna hypertenze a většinou i proliferativní retinopatie. Postupně může docházet k rozvoji nefrotického syndromu, přičemž rychlost progrese do stadia nevratného renálního selhání je závislá na kvalitě léčby.
Význam stanovení stadia chronického onemocnění ledvin (CKD) u diabetiků se zvyšuje úměrně skutečnosti, jak se rozšiřují možnosti účinné terapeutické intervence, která prokazatelně snižuje rychlost progrese úbytku glomerulární filtrace. Normalizace kompenzace diabetu má významný pozitivní vliv pouze v počátečním stadiu DN. Zásadní význam má léčba hypertenze, přičemž zařazení ACEi do terapie vedlo dokonce k dvojnásobnému prodloužení doby od první manifestace proteinurie do selhání. Zásadním pokrokem pro zlepšení prognózy nemocných s DKD byl průkaz efektu gliflozinů (inhibitorů SGLT2), jejichž potenciál je stále předmětem intenzivního studia.
Komplexní intervence tedy prokazatelně oddaluje přechod do „terminálního stadia“, ve kterém je indikováno použití eliminačních metod jako intervence nezbytné k udržení života. Zabránění přechodu do ESRD (terminální stadium renálního onemocnění, nověji užívaná zkratka korelující nové názvosloví ESKD – terminální stadium onemocnění ledvin) má zásadní dopad nejen na kvalitu života pacienta (udržení života je možné pouze s využitím eliminačních metod), ale také na životní prognózu. Ještě v nedávných dobách pouze 20 % pacientů s diabetem v chronickém hemodialyzačním programu přežívalo přes 5 let. S progredujícím snižováním glomerulární filtrace (GFR) a souběžně se zvyšující albuminurií se také zvyšuje pravděpodobnost závažné kardiovaskulární příhody, resp. úmrtí (1).
Finerenon
Finerenon (ATC kód: C03DA05) je perorální přípravek nové generace, nesteroidní antagonista mineralokortikoidního receptoru (MR), s vysokou selektivitou vůči MR. Klinický efekt je zprostředkován blokádou účinku aldosteronu s pozitivním ovliněním glomerulární a tubulární sklerózy. Tento účinek je nezávislý na angiotenzinu II. Dalšími přídavnými účinky blokády aldosteronu, které mohou zlepšit funkci ledvin, jsou efekty protizánětlivé a antioxidační. Finerenon dále inhibuje nadměrnou expresi transformujícího růstového faktoru‑β1 a inhibitor-1 aktivátoru plazminogenu, snižuje infiltraci makrofágy v glomerulech a tubulointersticiu (2). Blokováním účinku aldosteronu dojde k obnovení aktivity glukózo-6-fosfátdehydrogenázy, čehož důsledkem je zvýšení produkce glutathionu a nikotinamidadeninu dinukleotid fosfátu, což jsou primární intracelulární redukční činidla (3).
Mechanismus antagonismu mineralokortikoidních receptorů (MR)
Jaderné receptory, jako jsou receptory mineralokortikoidní, obsahují diskrétní domény pro specifické funkce včetně vazby ligandu, aktivace a rozpoznávání DNA. Existuje nejméně 22 známých kofaktorů, které se spojují s MR, které určují plnou transkripční odpověď zprostředkovanou MR buněčně specifickým způsobem. Studie molekulárního modelování komplex finerenon–MR naznačuje, že finerenon blokuje MR jako pasivní antagonista. Tento mechanismus se liší od steroidních MRA, které by mohly ovlivnit jeho rozdílnou klinickou odpověď (4).
Porovnáním komplexního efektu finerenonu se známými etiopatogenetickými mechanismy DN (CKD u pacientů s diabetem) je zřejmé, že pozitivního klinického efektu může být touto molekulou dosaženo právě u pacientů s diabetem.
Nejdůležitější experimentální a klinické studie s finerenonem
ARTS‑DN. Ve studii fáze IIb finerenon prokázal na dávce závislé snížení poměru albumin/kreatinin (UACR) ve srovnání s placebem. Průměrné placebem korigované poměry UACR v den 90 vs. výchozí hodnota ve skupinách s finerenonem 7,5, 10, 15 a 20 mg/den byly 0,79 (90% CI, 0,68–0,91; p = 0,004), 0,76 (90% CI, 0,65–0,88; p = 0,001), 0,67 (90% CI, 0,58–0,77; p < 0,001) a 0,62 (90% CI, 0,54–0,72; p < 0,001) (5).
FIDELIO‑DKD. V randomizované, dvojitě zaslepené, placebem kontrolované studii fáze III FIDELIO‑DKD (n = 5 674) u pacientů s diabetem 2. typu a CKD (poměr albuminu ke kreatininu v moči (UACR) 30 až < 300 mg/g, odhadovaná rychlost glomerulární filtrace (eGFR) 25 až < 60 ml/min a diabetická retinopatie, nebo UACR 300 až 5 000 mg/g a eGFR 25 až < 75 ml/min) snížil finerenon incidenci renálního složeného parametru, který zahrnoval dobu do prvního výskytu selhání ledvin, přetrvávajícího poklesu eGFR o 40 % nebo více ve srovnání s výchozí hodnotou po dobu nejméně 4 týdnů, nebo úmrtí z renálních příčin, který se vyskytl u 17,8 % pacientů s finerenonem a u 21,1 % pacientů s placebem (poměr rizik (HR) 0,82 (95% CI 0,73; 0,93), p = 0,001).
Ve stejné studii byl zároveň hodnocen složený KV parametr, který zahrnoval úmrtí z KV příčin, nefatální infarkt myokardu, nefatální cévní mozkovou příhodu nebo hospitalizaci pro srdeční selhání, a u pacientů lečených finerenonem byl ve srovnání s placebem pozorován relativní pokles rizika o 14 % (p = 0,034), a to bez ohledu na přítomnost KV onemocnění při vstupu do studie (6). Analýza podskupin v této studii dále ukázala, že finerenon vykazoval ve srovnání s placebem příznivé účinky na renální i KV parametry a snížil poměr albumin/kreatinin v moči nezávisle na současném podávání GLP-1 agonistů, nebo SGLT2 inhibitorů (7, 8).
V předem specifikované subanalýze studie FIDELIO‑DKD finerenon snížil výskyt kompozitního kardiovaskulárního endpointu u pacientů s chronickým onemocněním ledvin a diabetem 2. typu bez rozdílů v účinku léčby na základě již existující ischemické choroby srdeční (9).
Klinický přínos výsledků studií s finerenonem
Experimentální práce prokázaly, že finerenon může ovlivnit pozitivně řadu rizikových faktorů, které se podílejí na vzniku a progresi diabetického onemocnění ledvin/diabetické nefropatie. Antagonismus aldosteronu prostřednictvím finerenonu má nejen experimentální, ale, a to zejména, klinické pozitivní dopady. Efekt byl studován na populaci diabetiků 2. typu s přítomným diabetickým onemocněním ledvin a vysokým kardiovaskulárním rizikem. Analýzy přesvědčivě prokázaly příznivé ovlivnění kardiovaskulárních i renálních příhod. Finerenon se tak zařazuje mezi nové postupy, které mohou pozitivně ovlivnit vysoké riziko závažných komplikací přítomné u pacientů s diabetem 2. typu.
Poznámky pro praxi (10)
Finerenon (přípravek Kerendia®) je indikován k léčbě chronického onemocnění ledvin (stadia 3 a 4 s albuminurií) spojeného s diabetem 2. typu u dospělých pacientů. Ke zjištění, zda lze zahájit léčbu finerenonem, a k určení počáteční dávky je třeba stanovit hladinu draslíku v séru a odhadovanou glomerulární filtraci (eGFR). Pokud je hladina draslíku v séru ≤ 4,8 mmol/l, lze zahájit léčbu finerenonem. Pokud je hladina draslíku v séru > 4,8 až 5,0 mmol/l, lze zvážit zahájení léčby finerenonem při dalším sledování hladiny draslíku v séru během prvních 4 týdnů založeném na charakteristikách pacienta a hladinách draslíku v séru. Pokud je hladina draslíku v séru > 5,0 mmol/l, léčba finerenonem nemá být zahájena. Hladina draslíku v séru a eGFR musí být znovu stanovena za 4 týdny po zahájení nebo opětovném zahájení léčby finerenonem. Poté je třeba kontrolovat sérovou hladinu draslíku v pravidelných intervalech a dále také v případě potřeby na základě charakteristik pacienta a hladin draslíku v séru.
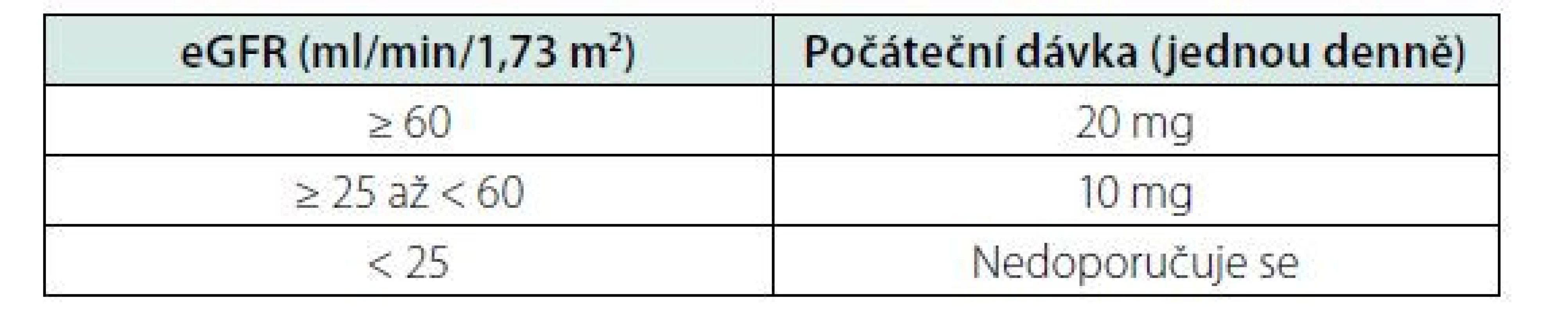
Závěr
Finerenon je nesteroidní antagonista mineralokortikoidního receptoru. V experimentálních studiích prokázal pozitivní ovlivnění rizikových faktorů diabetického onemocnění ledvin/diabetické nefropatie, z nichž má dominantní význam přetrvávající zánět, oxidační stres a postupně se rozvíjející skleróza. V klinických studiích byl u pacientů s diabetem 2. typu a vysokým kardiovaskulárními rizikem s přítomným CKD prokázán jeho významný efekt ve smyslu snížení kardiovaskulárního rizika (sdružený endpoint kardiovaskulární úmrtí, nefatální infarkt myokardu, nefatální cévní mozková příhoda, hospitalizace kvůli srdečnímu selhání) a snížení rizika závažných renálních příhod. Finerenon se tak zařadil mezi základní terapeutické intervence u pacientů s diabetem 2. typu a diabetickým onemocněním ledvin/ diabetickou nefropatií.
Podpořeno společností BAYER, s. r. o. 10/2022 PP-KER-CZ-0048-1
Zkrácené informace o léčivém přípravku Kerendia® naleznete na stránce 477.
KORESPONDENČNÍ ADRESA AUTORA:
prof. MUDr. Milan Kvapil, CSc., MBA
Interní klinika 2. LF UK a FN Motol
V Úvalu 84, 150 00 Praha 5
Cit. zkr: Vnitř Lék. 2022;68(7):475-478
Článek přijat redakcí: 20. 9. 2022
Sources
1. Ryšavá R. Viklický O et al. Doporučené postupy v nefrologii. Maxdorf: Praha; 2022.
2. Fujisawa G, Okada K, Muto S et al. Spironolactone prevents early renal injury in streptozotocin‑induced diabetic rats. Kidney Int. 2004;66(4):1493-502.
3. Han S‑Y, Kim CH, Kim H‑S et al. Spironolactone prevents diabetic nephropathy through an anti‑inflammatory mechanism in type 2 diabetic rats. J Am Soc Nephrol. 2006;17(5):1362-72.
4. Agarwal R, Kolkhof P, Bakris G, Bauersachs J, Haller H, Wada T, Zannad F. Steroidal and non‑steroidal mineralocorticoid receptor antagonists in cardiorenal medicine. Eur Heart J. 2021;42(2):152-161.
5. Bakris GL, Agarwal R, Chan JC et al. Mineralocorticoid Receptor Antagonist Tolerability Study–Diabetic Nephropathy (ARTS‑DN) Study Group. Eff ect of Finerenone on Albuminuria in Patients With Diabetic Nephropathy: A Randomized Clinical Trial. JAMA. 2015;314(9):884-94.
6. Bakris GL, Agarwal R, Anker SD et al. FIDELIO‑DKD Investigators. Effect of Finerenone on Chronic Kidney Disease Outcomes in Type 2 Diabetes. N Engl J Med. 2020; 383(23):2219-2229.
7. Rossing P, Agarwal R, Anker SD et al. FIDELIO‑DKD Investigators. Efficacy and safety of finerenone in patients with chronic kidney dinase and type 2 diabetes by GLP-1RA treatment: A subgroup analysis from the FIDELIO‑DKD trial. Diabetes Obes Metab. 2022;24(1):125-134.
8. Rossing P, Filippatos G, Agarwal R et al. FIDELIO‑DKD Investigators. Finerenone in Predominantly Advanced CKD and Type 2 Diabetes With or Without Sodium‑Glucose Cotransporter - 2 Inhibitor Therapy. Kidney Int Rep. 2021;7(1):36-45.
9. Filippatos G, Anker SD, Agarwal R, Pitt B, Ruilope LM, Rossing P, Kolkhof P, Schloemer P, Tornus I, Joseph A, Bakris GL; FIDELIO‑DKD Investigators. Finerenone and Cardiovascular Outcomes in Patients With Chronic Kidney Disease and Type 2 Diabetes. Circulation. 2021 Feb 9;143(6):540-552.
10. Souhrn údajů o přípravku Kerendia®. Available from: https://www.bayer.com/sites/default/ files/Kerendia_SPC.pdf. Nahlíženo 07. 10. 2022
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2022 Issue 7
-
All articles in this issue
- Hlavní téma – Nefrologie
- Current options for slowing the progression of chronic kidney disease
- Expert opinion on the cooperation of diabetologists and internists with nephrologists in the care of patients with chronic kidney diseases
- Glomerulonephritides associated with infections
- New developments in anaemia treatment – erythropoietin versus prolyl hydroxylase inhibitors?
- Covid-19 in kidney transplant recipients
- Reactive, infectious, or post‑infectious arthritis?
- Effect of SGLT2 inhibitor empagliflozin on the stabilization of heart failure progress with the possibility of further interventions in a patient with HFrEF – a case report
- New technology in the hypolipidemic drugs development. Inclisiran (LEQVIO)
- Therapy of hypertension in elderly population and its potential risks
- Thyroid incidentalomas
- Můžeme novou léčbou ovlivnit dosavadní terapií neřešený zánět a fibrózu u pacientů s DM2 a CKD?
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Reactive, infectious, or post‑infectious arthritis?
- Thyroid incidentalomas
- New developments in anaemia treatment – erythropoietin versus prolyl hydroxylase inhibitors?
- Current options for slowing the progression of chronic kidney disease
