Venózní tromboembolismus u antifosfolipidového syndromu
Venous thromboembolism in antiphosholipid syndrome
Antiphosholipid syndrome (APS) is defined by the presence of clinical and laboratory criteria, it means by presence of antiphospholipid antibodies. Venous thromboembolism belongs to the most frequent clinical manifestation of this syndrome. Here we summarised basic pathophysiological mechanisms of venous thrombosis and lung embolism development, epidemiology of APS, and also the situations when this syndrome should be considered. The possible difficulties of laboratory diagnosis and their therapy involvement are mentioned.
Keywords:
treatment – antiphospholipid syndrome – diagnose
Authors:
Alena Buliková; Miroslav Penka
Authors‘ workplace:
Oddělení klinické hematologie Fakultní nemocnice Brno
; Interní hematologická a onkologická klinika Masarykovy univerzity v Brně
; Alena Buliková, Miroslav Penka
Published in:
Vnitř Lék 2022; 68(8): 493-497
Category:
Main Topic
doi:
https://doi.org/10.36290/vnl.2022.106
Overview
Antifosfolipidový syndrom (APS) je definován přítomností klinických a laboratorních kritérií, tj. přítomností antifosfolipidových protilátek. Venózní tromboembolismus patří k nejčastějším klinickým manifestacím tohoto syndromu. Jsou shrnuty základní patofyziologické mechanizmy vzniku žilní trombózy a plicní embolie, epidemiologie APS, resp. i situace, kdy má být tento syndrom zvažován. Jsou zmíněna možná úskalí laboratorní diagnostiky a dopad na léčbu.
Klíčová slova:
diagnostika – léčba – antifosfolipidový syndrom
Úvod
Antifosfolipidový syndrom (APS) je klinicko‑patologickou jednotkou, která je charakterizována přesně definovanými klinickými nálezy v přítomnosti antifosfolipidových protilátek. Byl popsán Hughesem v roce 1983, proto je taktéž nazýván jako Hughesův syndrom. Kritéria pro definici tohoto syndromu od svého prvního popisu doznala řadu změn. V současné době však stále platí mezinárodní konsenzus kritérií definitivní diagnózy APS, který byl ustanoven pracovní skupinou na workshopu, který předcházel 11. kongresu o antifosfolipidových protilátkách v Sydney v roce 2005. Tento konsenzus byl publikován krátce na to, na začátku roku 2006 (1) a jeho hlavní principy shrnuje tabulka 1. Nicméně nárůst poznatků o problematice v patofyziologii, klinické manifestaci a zejména v laboratorní diagnostice se vynutil mezioborovou a mezinárodní spolupráci nad tvorbou nových kritérií, přičemž toho úsilí probíhá koordinovaně již od roku 2013. Nová diagnostická a klasifikační kritéria měla původně být sumarizována v letošním roce. Nicméně proběhlá pandemie covidu-19 zamíchala se záměry odborníků pro hemostázu nevídanou silou, včetně nevyjasněného vztahu této infekce k antifosfofolipidovým protilátkám, které se zdály být v jisté fází vývoje poznatků jednou z příčin neobvykle vysoké manifestace žilního tromboembolismu. Proto se zdá, že i předpokládaná doba ukončení práce na nových kritériích APS v organizaci Evropské ligy proti revmatismu (EULAR) by mohla být zpožděna. To nás nutí vycházet z aktuálních informací dle literatury a nedržet se striktně řadu let starých diagnostických schémat (2).

LA – lupus antikoagulant, ACLA – antikardiolipinové protilátky, antiβ2-GP I – protilátky proti iβ2-glykoproteinu I, GPL‑
fosfolipidové jednotky ve třídě IgG, MPL – fosfolipidové
jednotky ve třídě IgM
Patofyziologie trombotických komplikací v přítomnosti antifosfolipidových protilátek
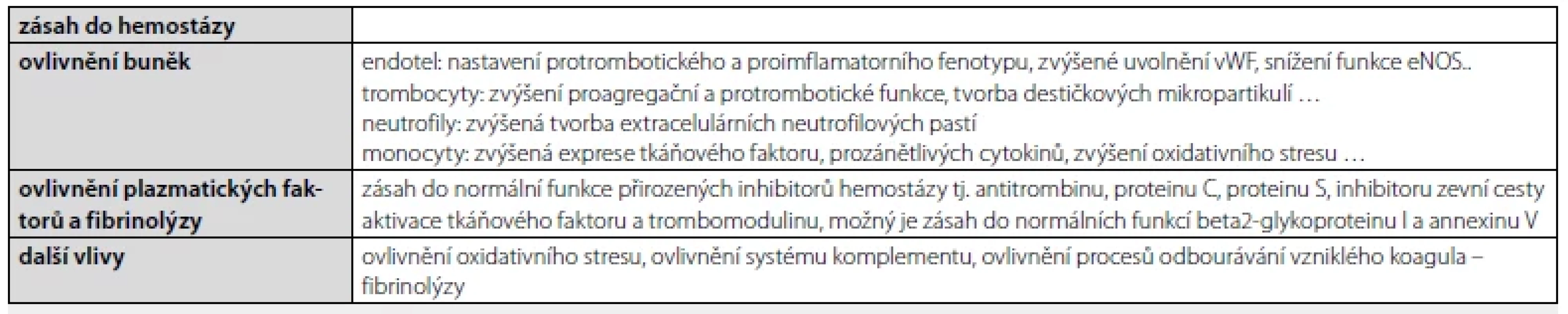
V první řadě je nutno připomenout známou skutečnost, že klinická manifestace venózního tromboembolismu je multifaktoriální geneze a že průkaz antifosfolipidových protilátek (APA) u klinické manifestace žilní trombózy a/nebo plicní embolie je jen jedním z kamínků složité mozaiky ovlivnění klasické Wirchovovy triády. Jak mohou APA ovlivňovat hemostázu ve smyslu zvýšení trombotické tendence, je shrnuto velmi rámcově v tabulce 2. Kromě zvýšené protrombotické tendence mohou APA působit na buněčné úrovni na celou řadu tkání (mimo jiné přímá aktivace neuronu, přímé ovlivnění syncicio‑trofoblastu, ovlivnění destičkových glykoproteinů a další), což se může podílet na pestré klinické manifestaci nemocných s nálezem APA, resp. s diagnózou APS. Nutné informace v péči nemocné s venózním tromboembolismem (VTE) se dále jiné opírají o zjištění, zda jde o neprovokovanou či provokovanou příhodu, případně zda jsou přítomny další choroby, které mohou samy o sobě, nebo jejich léčba, zvyšovat riziko tromboembolismu.
Asi v polovině případů je důvod ke tvorbě antifosfolipidových protilátek nejasný. Mohou se však vyskytovat i u zdravých osob běžné populace a jejich nárůst, resp. procento výskytu je závislé na rase a zejména věku jejich nositele; tak jako u jiných autoprotilátek jejich výskyt ve stáří narůstá, ale častý je jejich transientní, a v tomto případě většinou neškodný, výskyt i v dětském věku (3). Nicméně v řadě případů lze identifikovat, proč tyto protilátky, a v některých případech s malou klinickou významností a/nebo s přechodným působením, vznikly.
Kromě systémových a revmatických procesů, kdy tito nemocní APA mohou exprimovat ve 30–40 % případů, je tento typ autoprotilátek popisován u nádorových onemocnění, ať již solidních či hemo - či lymfopoetických.
APA mohou být indukovány řadou infekčních agens, kdy tyto nálezy většinou jsou, ale ne výlučně, transientní a nesymptomatické, nicméně jsou popisovány i situace spojené s tromboembolickými komplikacemi (popisy případů u HIV, lepra, ricketsióza a Q horečka), nebo mohou asociovány se spuštěním katastrofické varianty APS (CAPS – bezmála polovina těchto komplikací je takto indukována). Přehled přináší tabulka 3 (4). Hodně diskuzí o detekci APA u virových onemocnění rozvířila pandemie covidu-19, kdy u akutně nemocných hospitalizovaných případů byla tato pozitivita, zejména LA, popisována u poloviny nemocných. Nicméně meta‑analýza těchto případů neprokázala vyšší incidenci venózního tromboembolismu u hospitalizovaných pacientů s covidem-19 při porovnání APA pozitivních a negativních nemocných (5).

tučně uvedená agens jsou zmiňována s asociací s venózním
tromboembolismem a/nebo s indukcí katastrofického antifosfoslipidového syndromu
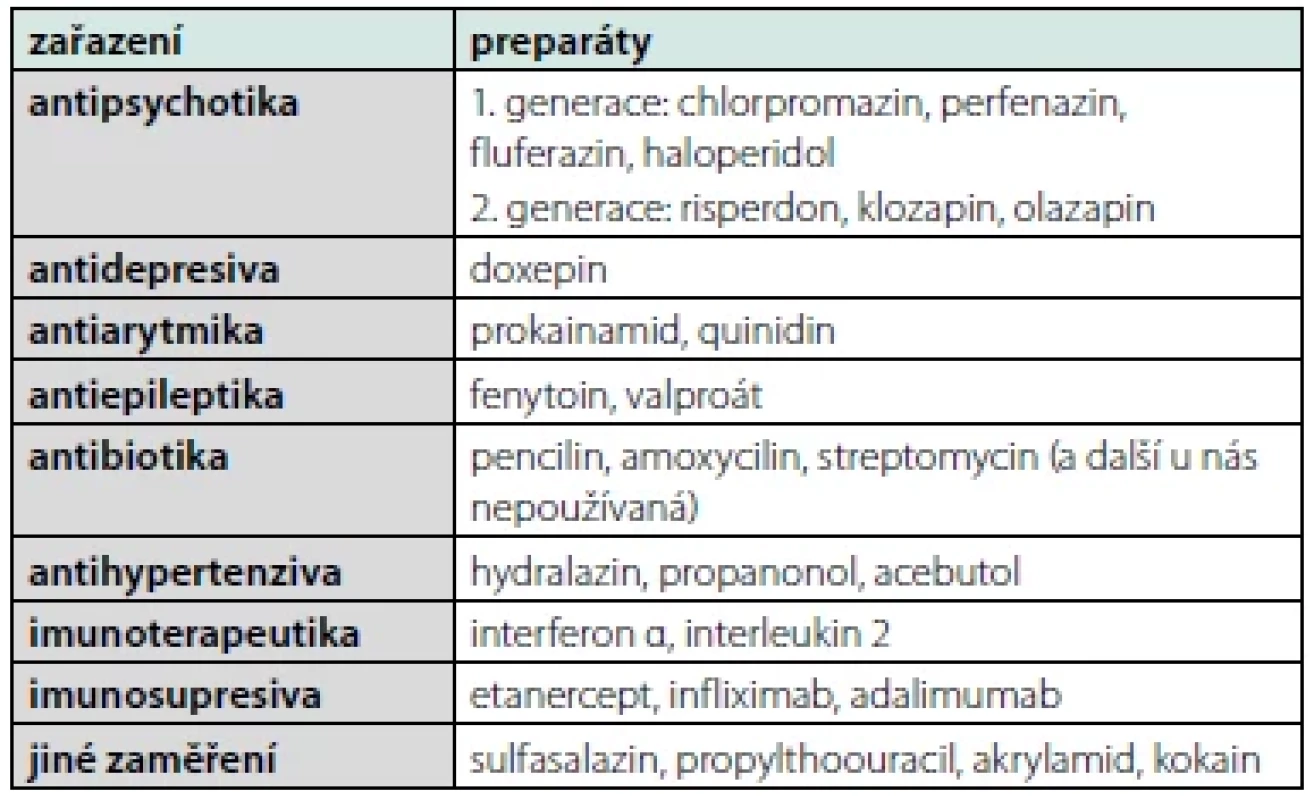
APA mohou být taktéž spojeny s celou řadou léků. Přehled přináší tabulka 4. Role takto indukovaných protilátek je sporná. V řadě případů je poléková indukce APA přechodná, tudíž z klinického pohledu málo zajímavá (6). Více trombotických komplikací je spojeno s medikací antipsychotik (7) či inhibitorů TNFα. Nicméně v těchto případech může být trombotická tendence způsobena více základním onemocnění, pro něž je léčba zaváděna, než vlastní medikací.
Klinická manifestace APA
APA mohou být u svých nositelů klinicky zcela němé u 1–10% případů, kdy tato prevalence byla obvykle stanovena na relativně zdravé populaci, většinou u dárců krve či těhotných ženách s normálním průběhem gravidity. Pozitivita záleží na věku (vyšší u starších jedinců), rase (vyšší u černošské populace) a typu detekované autoprotilátky (vyšší u sérologických nálezů zejména třídy IgM v porovnání s detekcí lupus antikoagulant). Incidence klinicky zjevného APS je odhadována na 2,1 na 100 000 ročně, prevalence 50 na 100 000 obyvatel (8).
Trvalá pozitivita antifosfolipidových protilátek v případě venózního tromboembolismu se nezdá být dramaticky vyšší než v běžné populaci a i u relativně mladých lidí a neprovokované příhodě je udávána v 9,0 % (9). Nicméně z pohledu diagnostiky a sledování nemocných s antifosfolipidovým syndromem, je žilní tromboembolismus nejčastější klinickou manifestací. Ve studii „Euro‑phosholipid project“, na níž participuje 13 evropských zemích, je sledováno dlouhodobě 1000 pacientů s jasně naplněnou diagnózou antifosfolipidového syndromu (10). V tomto projektu mělo při vstupu do sledování hlubokou žilní trombózu (DVT) 38,9% nemocných a plicní embolii (PE)14,1 %. Pro srovnání – cévní mozkovou příhodu mělo 19,8 % a transitorní ischemickou ataku 11,1 % zařazených jedinců. Nutno připomenout, že jde o klinická kritéria pro stanovení vlastní diagnózy APS, proto jde o čísla vyšší, než jsou očekávána v běžné populaci, resp. i u nemocných s VTE. V desetiletém sledování došlo k další klinické manifestaci DVT u 4,3 %, resp. i EP u 3,5 %, nemocných. Tato čísla jasně dokladují skutečnost, že přestože není vyšetření APA indikováno ve všech případech VTE, může mít toto vyšetření zásadní dopad v přesně vymezených klinických situacích. Navíc rozhodně hraje roli i skutečnost, zda byla některá z antifosfolipidových protilátek detekována jako izolovaný laboratorní nález, či zda jde o vícenásobný průkaz různých APA. U nemocných, kde byla prokázána trojnásobná pozitivita těchto autoprotilátek, tzv. „triple pozitivita“, což značí současný výskyt inhibitoru lupus antikoagulant (LA), vysoké titry protilátek proti kardiolipinu a protilátek proti beta-2glykoproteinu I ve stejné třídě imunoglobulinu (tedy buď IgG nebo IgM), je zřetelně vyšší riziko rekurence tromboembolismu; kumulativně 12,2 % po roce sledování, 26,1 % po 5 letech a 44,2 % po 10 letech (11).
Kromě žilního tromboembolismu se mohou APA projevovat celou řadou symptomů, jejichž přehled přináší tabulka 5. Z ní jednoznačně vyplývá, že APS je systémové onemocnění.

Limitace standardní akutní léčby VTE u APS/ APA
U pacientů se známou „triple“ pozitivitou antifosfolipidových protilátek a s první neprovokovanou příhodou VTE by neměla být léčba zahajována přímými orálními antrombotiky (DOAC), byť v jiných případech vzniku DVT či PE je tato léčba po vyhodnocení klinické závažnosti stavu upřednostňována. DOAC nejsou lékem první volby ani u nemocných s APA, kteří mají v anamnéze trombózu tepennou, postižení malých cév, s APA asociovanou chorobou srdečních chlopní (1, podrobně viz tabulka 5), ale ani u nemocných, kterým selhala léčba kumariny, případně u těch, kteří nejsou adherentní k léčbě Warfarinem (12, 13).
V případech, kdy je nutné při těžším průběhu léčby plicní embolie použít přechodně nefrakcionovaný heparin, musíme počítat s tím, že nelze využít aktivovaný parciální tromboplastinový čas (aPTT) k monitorování této léčby u nemocných, kteří mají LA. Aktuální hodnota testu je tímto inhibitorem ovlivněna, a to nepředvídatelným způsobem, takže neodráží vlastní vliv heparinu. V těchto případech je nezbytná kontrola stanovením anti‑Xa aktivity, která je kalibrována na nefrakcionovaný heparin s cílovou terapeutickou hodnotou 0,3–0,7 U/ml.
Jinou limitací akutní léčby VTE u APS může být trombocytopenie. Tato je u nemocných s APS relativně častá, provází 20–25 % případů v případě primárního APS, resp. až 30–40 % sekundárního APS, tedy tam, kde nález APA provází systémová onemocnění. V „Euro‑phosholipid‑project“ byl pokles trombocytů vstupně zjištěn 29,6 % zařazených jedinců a u dalších 8,7 % nemocných tento nález vznikl v desetiletém sledování (10). Trombocytopenie však naštěstí bývá nejčastěji lehká nebo středně významná (obvykle vyšší než 50 × 109/l), takže antitrombotickou medikaci je obvykle možné zavést, nicméně část nemocných vyžaduje přechodnou nebo trvalou imunosupresi, případně jinou léčbu k udržení náležitého počtu destiček.
Krvácivé komplikace u APS mohou vznikat i z jiných důvodů, jako jsou sekundární hypoprotrombinemie navozená lupus antikoagulant, trombocytopatie navozená vazbou APA na destičkové glykoproteiny, resp. i velmi obávaná difusní alveolární hemoragie. Řešení trombo‑hemorhagické klinické manifestace těchto stavů si již obvykle vyžaduje multioborovou spolupráci.
Sekundární profylaxe VTE u APS
V případě neprovokované příhody VTE u APS jsou lékem volby antagonisté vitamínu K, kumariny, s cílovým INR 2–3 (12), a to podávané doživotně. U trombózy či plicní embolie provokované je příhoda řešena stejně dlouho, jak to určují běžná národní či mezinárodní doporučení s tím, že před jejím ukončením musí být uváženo, zda byly odstraněny vyvolávající rizikové faktory, resp. zda byl či nebyl zjištěn vysoce rizikový profil APA. Toto posouzení může vyústit v protrahovaní antitrombotické medikace (12).
O použití DOAC u nemocných s APS jsou stále vedeny diskuze. Ty otevřela zejména studie TRAPS (14), která srovnávala léčbu trombotických projevů APS rivaroxabanem a warfarinem u nemocných s vysoce rizikovým profilem APA, tedy s „triple“ pozitivitou a byla předčasně ukončena pro nesrovnatelně vyšší výskyt trombóz zejména v arteriálním řečišti u pacientů na standardních dávkách Xarelta. Taktéž studie ASTRO‑APS, která srovnávala použití apixabanu v porovnání s warfarinem při trombotických projevech APS, a přes různé změny dávkování, limitace zařazených pacientů atd. byla taktéž předčasně ukončena pro vyšší výskyt ischemických cévních mozkových příhod ve skupině nemocných s Eliquisem. Bylo provedeno několik meta‑analýz publikovaných případů a žádná z nich nevyzněla ve prospěch DOAC. Proto taktéž Evropská kardiologická společnost (European Society of Cardiology – ESC) a Americká hematologická společnost (American Society of Hematology – ASH) vydaly doporučení, že DOAC nemají být používány u všech nemocných s APS (16). Jisté zvážení těchto léků připouští EULAR (12), mezinárodní společnost pro trombózu a hemostázu (International Society of Thrombosis and Haemostasis – ISTH) (13), resp. i Britská hematologická společnosti (BSH). Obvykle jde o nemocné, kteří nemají vysoký rizikový profil APA zejména přítomnost LA, jsou dlouhodobě stabilní na zavedené léčbě DOAC pro žilní trombózu a byli náležitě informováni o možných rizicích tepenné trombózy přes zavedenou medikaci (13).
Existuje řada teoreticky zvažovaných možných dalších léčebných postupů, které jsou brány v úvahu v případech, kdy běžná antitrombotická medikace pacientům nepomáhá. Kromě vyššího dávkování kumarinů s cílovým INR 2,5–3,5 jsou jako přídatná medikace k antitrombotickým postupům nejčastěji používány hydroxychloroquin, statiny, vitamin D, je taktéž používána léčba biologická, zde nejčastěji rituximab, belimumab či blokace TNFα. Blokace komplementu – eculizumab – byla rovněž použita, a to jak na trombotické, porodnické, ale i na mikrovaskulární klinické projevy. Je zmiňovány i koenzym Q10, resp. po té, co byla zjištěna role extracelulárních neutrofilových pastí, tedy základního mechanismu působení periferních neutrofilů k zachycení různých patogenů, i v patofyziologii APS, uvažuje se i posílení role adenosinu či použití agonistů adenozinových receptorů, což protrombotické nastavení u pacientů s APA může ovlivňovat (17).
Vyšetřování antifosfolipidových protilátek u nemocných s žilním tromboembolismem
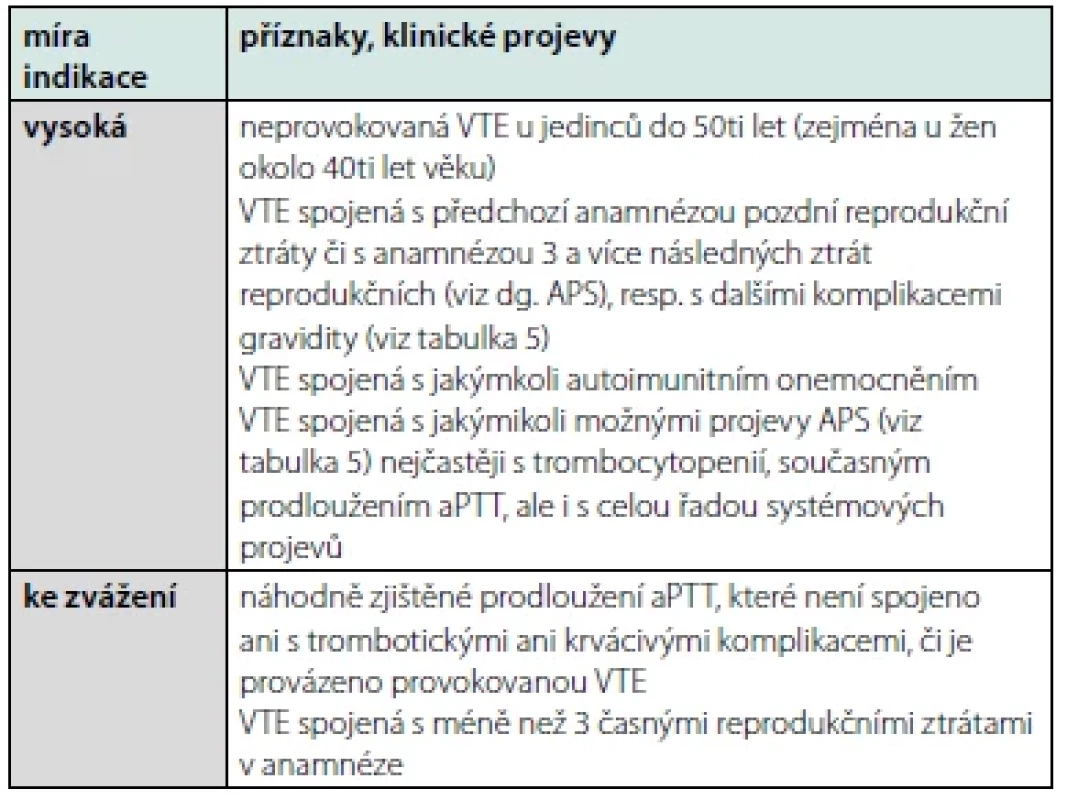
Plošná screeningová vyšetření výskytu APA u každé DVT či EP jsou vysoce nedoporučována (18). Zejména u starších jedinců, u nichž je častý nález nepatogenních APA, resp. u nemocných v akutním stavu, kdy může být pozitivita APA tranzientní nebo „falešně pozitivní“, může být aktuální stanovení APA zavádějící a vést k nesprávnému léčebnému rozhodnutí. Souhrn indikací k vyšetření APA u DVT či EP se pokouší shrnout tabulka 6. Výše uvedené však neupozorňuje na limitace a nutné procesy. Jedním se základů diagnostického schématu je podmínka, že pro diagnózu APS je nezbytně nutné opakované stanovení APA v časovém úseku 12 a více týdnů. Toto je „sine qua non“ diagnostiky APS a tím respektování výše uvedených léčebných doporučení.
Nicméně diagnostika zejména lupus antikoagulant (LA) není jednoduchá a v případě akutní manifestace VTE není vůbec doporučena, neboť celá řada vlivů, jako je vyšší CRP, použití katecholaminů, antitrombotická medikace, zánětlivé procesy a jiné situace, mohou být provázeny falešnou pozitivitou i negativitou testování (19). Průkaz APA může být problematický zejména v graviditě, kdy vysoká hladina faktoru VIII navozená těhotenstvím může limitovat průkaz LA, ale i vazba jiných APA na cílové struktury může titry APA snižovat, což se projeví ve falešné negativitě jejich průkazu.
I testování LA na jakékoli antitrombotické léčbě (ať již se jedná o testování na nefrakcionovaném heparinu, nízkomolekulárním heparinu, při léčbě pentasacharidem, na kumarinech či DOAC) může být potencionálně ovlivněno. Proto je nutná úzká spolupráce kliniků s hemostazeologickou laboratoří, která by měla mít nastaven systém limitních nálezů (cut off) pro určení pozitivních a negativních výsledků v jednotlivých situacích včetně limitací terapeutickým ovlivněním. Je doporučena řada postupů, jak eliminovat vliv DOAC na stanovení přítomnosti LA, žádná z nich nefunguje na 100 %.
Závěr
Antifosfolipidové protilátky mohou být kauzální příčinou vzniku žilní tromboembolismu a jejich průkaz je v tom případě součástí diagnózy APS, která u nemocného může být důvodem ke změně léčebné strategie. Nicméně průkaz APA je u těchto nemocných relativně řídký a vyloučení APS u nemocných s klinickou manifestací žilní trombózy/ a nebo plicní embolizace je nutno uvážit dle řady dalších klinických a laboratorních nálezů.
Podpořeno MZ ČR – RVO (FNBr, 65269705)
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Alena Buliková, Ph.D.
Oddělení klinické hematologie, Fakultní nemocnice Brno
Jihlavská 20, 625 00 Brno
Cit. zkr: Vnitř Lék. 2022;68(8):493-497
Článek přijat redakcí: 22. 9. 2022
Článek přijat po recenzích: 10. 11. 2022
Sources
1. Miyakis S, Lockshin D, Atsumi T et al. International consensus statement on an update of the classification criteria for definite antiphospholipid syndrome (APS). J Thromb Haemost. 2006;4 : 295-306.
2. Garcia D, Erkan D. Diagnosis and management of the antiphosholipid syndrome. NEJM. 2018;378 : 2010-2021.
3. Rumsey DG, Myones B, Massicotte P. Diagnosis and treatment of antiphosholipid syndrome in childhood: A review. Blood Cells Mol, DiS. 2017;67 : 34-40.
4. Rauch et al. Origin of antiphoshopilid antibodies. In Ercan G, Loschin MD. Antiphosholipid syndrome. Current research highlights and clinical insights. Springer international publishing 2017; pp 29-52. DOI: 1007/978-319-55442-6.
5. Taha M, Samavati L. Antiphosholipid antibodies in COVID-19: a meta‑analysis and systematic review. RMD Open 2021;7:e001580.
6. Risse J, Viera M, Beuret F et al. Reversible drug ‑ induced antiphosholipid syndrome. Lupus. 2018;27 : 333-33.
7. Malý R, Masopust J, Hosák L, Konupčíková K. Assessment of a risk of a venous thromboembolism and its possible prevention in psychiatric patients. Psychiatry Clin Neurosci. 2008;62 : 3-8
8. Duarte‑Garcia A, Pham MM, Crowson CS et al. The epidemiology of antipshopholipid syndrome: A population‑based study. Arthrit Rheumatol. 2019; 71 : 1545-1552
9. Miranda S, Park J, Le Gal G et al. Prevalence of confirmed antiphosholipid syndrome in 18-50 years unselected patients with first unprovoked venous thromboembolism. J Thromb Haemost. 2020;18 : 916-930.
10. Cervera R, Serrano R, Pons‑Estel GI et al. Morbidity and mortality in the antiphosholipid syndrome during a 10-year period: a multicentre prospective study of 1000 patients. Ann Rheumat, DiS. 2015;74 : 1011-1018.
11. Pengo V, Ruffatti A, Lenani C et al. Clinical course of high‑risk patients diagnosed with antiphosholipid syndrome. J Thromb Haemost. 2009;8 : 237-242.
12. Tektonidou MG, Andreoli L, Limper M et a. EULAR recommendations for the management of antiphosholipid syndrome in adults. Ann Rheum, DiS. 2019;78 : 1296-1304.
13. Zuily S, Cohen H, Isenbergr D et al. Use of direct oral anticoagulants in patients with thrombotic antiphosholipid syndrome: Guidance from the Scientific and Standardization Committee of the International Society on Thrombosis and Haemostasis. J Thromb Haemost. 2020;18 : 2126-2137.
14. Pengo V, Denas D, Zopplellaro G et al. Rivaroxaban vs warfarin in high risk patients with antiphospholipid syndrome. Blood 2018. doi: 10.1182/Blood-2018-04-848333.
15. ASTRO‑APS investigators. Apixaban compared with warfarin to prevent thrombosis in thrombotic antiphospholipid syndrome: a randomized trial. Blood Advances 2021. doi: 10.1182/bloodadvances.2021005808/1829277
16. Pastori D, Menichelli D, Cammisotto V, Pignatelli P. Use of direct oral anticoagulants in patients with antiphosholipid syndrome: A systematic review and comparison of the international Guidelines. Front Cardiovasc Med. 2021; doi: 10.3389/fcvm.2021. 715878.
17. Cohen H, Cuadrado MJ, Erkan D et al. 16th International congress on antiphosholipid antibodies task force report on antiphosholipid antibodies treatment trends. Lupus. 2020;29 : 1571-1593.
18. Keeling D, Mackie I, Moore GW et al. Guidelines on the investigation and management of antiphospholipid syndrome. BJH 2012;157 : 47-58.
19. Pengo V, Tripodi A, Reber G et al. Up‑date of the guidelines for lupus anticoagulant detection. J |Thromb Haemost. 2009;7 : 1737-1740.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2022 Issue 8
-
All articles in this issue
- Hlavní téma – Hematologie
- Dnešní pohled na dědičné trombofilie
- Venózní tromboembolismus u antifosfolipidového syndromu
- Vybrané závažné „hematologické“ syndromy u dospělých pacientů v intenzivní péči
- Vývoj léčby žilní trombózy od pijavic k mechanické trombektomii
- Tradiční a nové biomarkery kongesce u srdečního selhání
- Alergenová imunoterapie v léčbě alergického eozinofilního astmatu
- Plicní střádání
- Porucha kognitivních funkcí a hrozba pandemie demence aneb cesta hypertoniků k nesoběstačnosti
- Antitrombotická léčba a digestivní endoskopie
- Jak dobře jsme léčili hypertenzi v posledních 25 letech?
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Vybrané závažné „hematologické“ syndromy u dospělých pacientů v intenzivní péči
- Dnešní pohled na dědičné trombofilie
- Alergenová imunoterapie v léčbě alergického eozinofilního astmatu
- Antitrombotická léčba a digestivní endoskopie
