Kyselina bempedoová v kontextu současných možností hypolipidemické léčby a výsledků studie CLEAR OUTCOMES
Bempedoic acid in the context of current hypolipidemic treatment options and the results of the CLEAR OUTCOMES trial
Despite huge global efforts to reduce the incidence of cardiovascular disease (CVD), it is still the dominant cause of morbidity and mortality in the developed world. In recent years, there has been a significant reduction in the prevalence of CVDs due to the impact of major risk factors on primary and secondary prevention, especially the consistent treatment of arterial hypertension and dyslipidemia. However, despite the remarkable effect of statins, we are still not able to achieve the recommended target serum lipid levels in up to two-thirds of patients, which is why efforts to intensify hypolipidemic treatment are ongoing. Bempedoic acid, an ATP-citrate lyase inhibitor, represents a novelty among hypolipidemics. By limiting endogenous cholesterol synthesis, it reduces LDL-cholesterol levels and consequently the incidence of cardiovascular events. This new treatment is promising both as monotherapy in statin-intolerant patients (in whom it can achieve up to 40% reduction in LDL-cholesterol concentration) and as part of combination regimens. The following text summarises the current knowledge on the effects and safety of bempedoic acid and, in the light of the new findings and expert guidelines, provides practical recommendations on when the therapy should be indicated.
Keywords:
ATP-citrate lyase inhibitor – atherosclerosis – cardiovascular disease – bempedoic acid
Autori:
Eva Tůmová; Michal Vrablík
Pôsobisko autorov:
III. interni klinika – endokrinologie a metabolismu, 1. LF UK a VFN v Praze
Vyšlo v časopise:
AtheroRev 2023; 8(2): 85-94
Kategória:
Přehledové práce
Súhrn
I přes obrovské celosvětové úsilí snížit výskyt kardiovaskulárních onemocnění (KVO) jsou stále dominantní příčinou nemocnosti a úmrtnosti ve vyspělém světě. V posledních letech došlo k významné redukci prevalence KVO dané ovlivněním hlavních rizikových faktorů v rámci primární a sekundární prevence, především důslednou léčbou arteriální hypertenze a dyslipidemie. Navzdory pozoruhodnému léčebnému efektu statinů ovšem stále nejsme schopni dosáhnout doporučovaných cílových hodnot sérových lipidů až u dvou třetin pacientů, a proto trvá snaha o intenzifikaci hypolipidemické léčby. Kyselina bempedoová, inhibitor ATP-citrát lyázy, představuje novinku mezi hypolipidemiky. Omezením endogenní syntézy cholesterolu snižuje hladinu LDL-cholesterolu a následně také incidenci kardiovaskulárních příhod. Perspektivní je tato nová léčba jak v monoterapii u statin-intolerantních pacientů (u nichž umožňuje dosáhnout až 40% poklesu koncentrace LDL-cholesterolu), tak jako součást kombinačních režimů. Následující text shrnuje současné znalosti o účincích a bezpečnosti kyseliny bempedoové a ve světle nových zjištění a odborných guidelines uvádí praktická doporučení, v jakých případech terapii indikovat.
Klíčová slova:
ateroskleróza – inhibitor ATP-citrát lyázy – kardiovaskulární onemocnění – kyselina bempedoová
Úvod
Celosvětově patří kardiovaskulární onemocnění (KVO) stále mezi nejčastější příčiny úmrtí. V roce 2019 zemřelo v souvislosti s KVO 19 milionů osob, do roku 2030 je očekávaný vzestup až na 22,2 milionu [1], přičemž KVO na podkladě aterosklerózy (ASKVO) jsou zodpovědná až za dvě třetiny těchto úmrtí. Teoreticky by tedy valná většina KVO a úmrtí z jejich příčin měla být preventabilní [1]. Navzdory bezútěšné populační statistice lze zásadního snížení individuálního kardiovaskulárního (KV) rizika docílit ovlivněním jednotlivých rizikových faktorů (RF) KVO, mezi které patří arteriální hypertenze, a především koncentrace LDL-cholesterolu (LDL-C) [2]. Mnohé studie (randomizované kontrolované studie, observační studie, mendelovské randomizační studie) konzistentně poukazují na silnou asociaci celoživotně vyšších koncentrací LDL-C se narůstajícím KV-rizikem. Současně je jasný efekt intervence a následného poklesu hladiny LDL-C s poklesem tohoto rizika až o polovinu [3] faktem, který podložil zásadní pravidlo hypolipidemické léčby s ohledem na LDL-C „čím níže a déle, tím lépe“ [4].
Statiny inhibují enzym HMG-CoA-reduktázu v kaskádě endogenní produkce cholesterolu v hepatocytu, což vede ke zvýšené expresi LDL-receptorů jaterní buňkou a intenzivnějšímu vychytávání LDL-C. Spolu s poklesem koncentrace LDL-C v krevním oběhu klesá také intenzita ukládání LDL-C ve stěně cév a rychlost progrese aterosklerózy. Prokázaný efekt a bezpečnost statinů v prevenci KVO [5,6] vedly k jejich zásadnímu postavení v terapii. Postupně sílí důkazy, že velice nízké koncentrace LDL-C vedou k dalším poklesu KV-rizika a monoterapie statiny (jakkoli často poddávkovaná) se zhusta stává nedostatečnou k dosažení cílových hladin LDL-C, což potvrdila studie DA VINCI z roku 2021 [7] – u vysoce KV-rizikových pacientů bylo koncentrací LDL-C doporučených guidelines z roku 2019 [8] docíleno pouze u 17 % osob v primární prevenci a u 22 % jedinců v prevenci sekundární. Výsledky jsou ještě horší ve střední a východní Evropě, kde se koncentraci LDL-C < 1,4 mmol/l podařilo dosáhnout jen u 13 % pacientů. Dalším důležitým, ale pozitivním poznatkem je, že byl zaznamenán jen nízký výskyt nežádoucích účinků, které by limitovaly dávku statinu – statinová intolerance byla referována v < 7 % případů [9]. Vzhledem k těmto výsledkům je zřejmé, že k redukci rizika KVO potřebujeme další účinné hypolipidemikum vhodné jak ke kombinační terapii, tak k monoterapii [10]. V praxi již několik let využíváme ezetimib (v posledních několika letech i velice výhodné fixní kombinace se statiny), nově také inhibitory PCSK9 (proprotein konvertázy subtilizin/kexin typu 9) alirokumab a evolokumab [11] a také inklisiran (siRNA, malá interferující RNA) [12]. Nejen v našich podmínkách jsou úhradová kritéria podávání těchto nových injekčně aplikovaných léků poměrně úzká, a jsou tak omezena na menší skupinu pacientů. Stále trvá snaha o nalezení další vhodné molekuly, která by byla dostupná pro širší spektrum rizikových jedinců, u nichž dosavadní hypolipidemická léčba nedostačuje.
Kyselina bempedoová
Kyselina bempedoová je nový lék snižující hladinu cholesterolu inhibicí enzymu adenozin trifosfát-citrát lyázy (ATC) [13], což ústí ve snížení endogenní syntézy cholesterolu stejně jako při léčbě statiny (tyto účinkují v totožné kaskádě, jen dva kroky dále). Kyselina bempedoová je podávána ve formě proléčiva, které je aktivováno po navázání na koenzym A katalyzovaný jaterní acyl-CoA syntetázou 1 (ASCV1L), čímž vzniká účinná forma bempedoyl-CoA [13]. Aktivace léčiva v játrech a jeho extenzivní first-pass metabolizmus má za následek limitovanou expozici aktivní látce v systémové cirkulaci [14], což vysvětluje výbornou toleranci léčby a minimum nežádoucích účinků [15,16].
Metaanalýza 10 randomizovaných kontrolovaných studií s celkovým počtem 3 788 pacientů poskytla důležitá data z hlediska ovlivnění různých RF KVO podáváním kyseliny bempedoové [17]. Tato nová léčba byla spojena se signifikantním poklesem nově diagnostikovaného diabetes mellitus (DM) či se zhoršením jeho kompenzace (OR 0,59; 95% CI 0,39– 0,9; p = 0,01), tab. 1. Podobné výsledky přinesla souhrnná analýza dat z další studie s kyselinou bempedoovou [18].
![Shrnutí vlivu kyseliny bempedoové (180 mg denně) vs placebo na biomarkery kardiovaskulárního rizika.
Upraveno podle [17]](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image_pdf/b74e5afe1cb401dd3e3363b1be0f2b18.png)
Údaje 2 884 pacientů ze 4 randomizovaných, placebem kontrolovaných třífázových studií s kyselinou bempedoovou byly použity ve validovaném predikčním modelu s cílem odhadnout výchozí 10leté riziko MACE u pacientů s prokázaným KVO na základě poklesu hladiny LDL-C [19]. Následný odhad změny 10letého KV-rizika při terapii kyselinou bempedoovou byl stanoven pro každého pacienta na základě CTT (Cholesterol Treatment Trialist‘s) modelu. U pacientů léčených vysoce intenzivní léčbou statiny byl předpokládaný absolutní pokles MACE -3,3 % (-3,7 % až -2,9 %), u pacientů s léčbou nízké intenzity pak -6,0 % (-7,7 % až 4,3 %) [19]. Modelováním nelze nahradit dobře navrženou randomizovanou studii, ale tato data vypadají velmi slibně a novou hypolipidemickou léčbu kyselinou bempedoovou jasně podporují.
Další metaanalýza 6 randomizovaných kontrolovaných studií s 3 956 zařazenými pacienty a dobou sledování 52 týdnů ukázala pokles MACE při léčbě kyselinou bempedoovou o 16 % ve srovnání s placebem [20], jakkoli nebyl tento pokles statisticky signifikantní (OR 0,84; 95% CI 0,61–1,15). Autoři také nezaznamenali žádný vliv kyseliny bempedoové na celkovou mortalitu (OR 2,37; 95% CI 0,80–6,99) a mortalitu z KV- -příčin (OR 1,66; 95% CI 0,45–6,04). Na druhou stranu byl pozorován pozitivní trend vzhledem k riziku nefatálního infarktu myokardu (OR 0,57; 95% CI 0,32–1,00) a podávání kyseliny bempedoové bylo spojené s poklesem rizika nově diagnostikovaného DM či zhoršení již probíhající nemoci (OR 0,68; 95% CI 0,49–0,94).
Studie CLEAR Outcomes
Studie CLEAR Outcomes je třífázová, dvojitě zaslepená, multicentrická randomizovaná kontrolovaná studie srovnávající efekt 180 mg kyseliny bempedoové a placeba na incidenci KV- -příhod u pacientů se statinovou intolerancí ve vysokém KV- -riziku s elevací LDL-C [21]. Do studie bylo zařazeno celkem 13 970 pacientů [22,23], 6 992 bylo randomizováno k léčbě kyselinou bempedoovou a 6 978 k placebu. Průměrný věk osob byl 65,5 let, 48,1 % z léčebné větve a 48,4 % z placebové větve tvořily ženy. Průzkumu se zúčastnilo více než 1 200 center ve 32 zemích. Studie měla pokračovat do naplnění primárního endpointu u 1 620 účastníků, z nichž minimálně 810 mělo splňovat kritéria ischemické příhody (úmrtí z KV-příčin, nefatální infarkt myokardu, nefatální cévní mozková příhoda). Minimální doba léčby byla stanovena na 36 měsíců, medián léčby na 42 měsíců [21].
Již v prosinci 2022 sponzor studie oznámil dosažení primárního endpointu, tedy statisticky signifikantního poklesu rizika 4bodového MACE u léčebné větve [22]. Konečné výsledky studie CLEAR Outcomes byly prezentovány na kongresu Americké kardiologické společnosti (ACC Congress) 2023 v New Orleans. Medián sledování účastníků studie byl 40,6 měsíců. Průměrná počáteční koncentrace LDL-C u všech zařazených pacientů byla 3,6 mmol/l. Po 6 měsících podávání studiové léčby/placeba bylo v terapeutické větvi dosaženo většího absolutního poklesu LDL-C o 0,756 mmol/l, což je redukce koncentrace LDL-C o 21,1 % ve srovnání s placebovou větví [23]. Incidence primárního cíle byla signifikantně nižší u jedinců užívajících kyselinu bempedoovou, a to o 13 % ve srovnání s pacienty užívajícími placebo: 819 příhod (11,7 %) vs 927 příhod (13,3 %); HR 0,87; 95 % CI 0,79–0,96; p = 0,004. Absolutní rozdíl mezi větvemi v incidenci MACE byl 1,6 %, number needed to treat (NNT) = 62. Incidence složeného cíle (úmrtí z KV-příčin, nefatální infarkt myokardu, nefatální cévní mozková příhoda) byla také významně nižší při podávání kyseliny bempedoové, a to o 15 %: 575 (8,2 %) vs 663 (9,5 %); HR 0,85; 95% CI, 0,76–0,96; p = 0,006. Výskyt infarktu myokardu, ať smrtícího, či nikoli, byl redukován o 23 %: 261 (3,7 %) vs 334 (4,8 %); HR 0,77; 95% CI 0,6–0,91; p = 0,002. Nutnost ošetření koronární revaskularizací klesla o 19 %: 435 (6,2 %) vs 529 (7,6 %); HR 0,81; 95% CI 0,72–0,92; p = 0,001 (graf 1). V terapeutické větvi nebyl pozorován žádný efekt na incidenci fatální či nefatální cévní mozkové příhody (HR 0,85; 0,67–1,07), úmrtí z KV-příčin (HR 1,04; 0,88–1,24) a úmrtí z jakýchkoli příčin (HR 1,03; 0,90–1,18). Za zmínku též stojí skutečnost, že podávání kyseliny bempedoové vedlo k poklesu sekundárního endpointu, což byla hospitalizace pro nestabilní anginu pectoris, a to o celých 34 % (HR 0,66; 0,50– 0,86) [23].
V každém grafu znázorňuje vložený obrázek stejná data na zvětšené ose y. Hodnoty p byly vypočteny pomocí
log-rank testu. Upraveno podle [23]
Graf 1.1 | Kumulativní incidence primárního cíle – 4bodový MACE (úmrtí z KV-příčin, nefatální infarkt
myokardu, nefatální cévní mozková příhoda a koronární revaskularizace) Graf 1.2 | Kumulativní incidence
primárního cíle – 3bodový MACE (úmrtí z KV-příčin, nefatální infarkt myokardu a nefatální cévní mozková
příhoda)
![Kumulativní riziko kardiovaskulárních příhod ve studii CLEAR Outcomes s kyselinou bempedoovou. <br>
V každém grafu znázorňuje vložený obrázek stejná data na zvětšené ose y. Hodnoty p byly vypočteny pomocí
log-rank testu. Upraveno podle [23] <br>
Graf 1.1 | Kumulativní incidence primárního cíle – 4bodový MACE (úmrtí z KV-příčin, nefatální infarkt
myokardu, nefatální cévní mozková příhoda a koronární revaskularizace) Graf 1.2 | Kumulativní incidence
primárního cíle – 3bodový MACE (úmrtí z KV-příčin, nefatální infarkt myokardu a nefatální cévní mozková
příhoda)](https://pl-master.mdcdn.cz/media/image_pdf/705ca6f095a5ba9d0a22d9d6dd9baad4.png?version=1691849614)
V každém grafu znázorňuje vložený obrázek stejná data na zvětšené ose y. Hodnoty p byly vypočteny pomocí
log-rank testu. Upraveno podle [23]
Graf 1.3 | Kumulativní incidence fatálního nebo nefatálního infarktu myokardu
Graf 1.4 | Kumulativní incidence koronární revaskularizace
![Kumulativní riziko kardiovaskulárních příhod ve studii CLEAR Outcomes s kyselinou bempedoovou. <br>
V každém grafu znázorňuje vložený obrázek stejná data na zvětšené ose y. Hodnoty p byly vypočteny pomocí
log-rank testu. Upraveno podle [23] <br>
Graf 1.3 | Kumulativní incidence fatálního nebo nefatálního infarktu myokardu <br>
Graf 1.4 | Kumulativní incidence koronární revaskularizace](https://pl-master.mdcdn.cz/media/image_pdf/b0dab04472c30d52000166d4d6f2385d.png?version=1691850147)
Bezpečnost léčby
Bezpečnost kyseliny bempedoové byla komplexně vyhodnocena souhrnnou analýzou 3 621 pacientů ze 4 třífázových randomizovaných studií, v nichž byly stanovovány jak vedlejší účinky udávané pacienty, tak biochemické parametry [24]. Pacienti v průměrném věku 65,2 ± 9,3 let, (66 % mužů) užívali kyselinu bempedoovou nebo placebo v kombinaci s maximální tolerovanou dávkou statinu, medián léčby byl 363 dní. Počet nežádoucích účinků způsobených léčbou (TEAEs – Treatment-Emergent Adverse Events) adjustovaných na expozici činil 87,1/100 osobo-roků pro kyselinu bempedoovou a 82,9/100 osobo-roků pro placebo [23]. Zajímavým zjištěním je fakt, že referované svalové obtíže, které vídáme v souvislosti s léčbou statiny, byly podobné v obou větvích (léčebná 1,5/100 paciento-roků vs placebová 2,0/100 paciento- roků) [24].
Podávání kyseliny bempedoové je zřejmě spojené s mírným poklesem hladiny hemoglobinu a mírnou elevací urey, kreatininu a kyseliny močové, což pravděpodobně nemá žádný klinický dopad. Ve shodě s observačními studiemi je vyšší výskyt dny u osob, které užívají kyselinu bempedoovou (1,6/100 paciento-roků) ve srovnání s placebem (0,5/100 paciento- -roků) [24]. Vyšší incidence dnavých záchvatů v souvislosti s touto terapií se většinou objevuje u osob s anamnézou dny a jak příznaky, tak zvýšené koncentrace kyseliny močové jsou po ukončení léčby reverzibilní [24]. Tento nežádoucí účinek je s největší pravděpodobností způsobem inhibicí transportéru OATC2 v ledvinách a jedná se o plně reverzibilní efekt, nejde tedy o toxický vliv léčby [24].
Dále byla v souvislosti s terapií kyselinou bempedoovou zjištěna mírná elevace aminotransferáz (maximální do 3násobku horní hranice normy) – 0,8/100 paciento-roků při podávání kyseliny bempedoové vs 0,3/100 paciento-roků při podávání placeba. Tento efekt byl ovšem pouze přechodný a reverzibilní po ukončení léčby [24].
Byla také zmíněna souvislost mezi léčbou kyselinou bempedoovou a zvýšeným rizikem šlachových ruptur. Je třeba zdůraznit, že tento nežádoucí účinek byl pozorován pouze ve 2 studiích (CLEAR Harmony a CLEAR Wisdom), do nichž byl zařazen velice malý počet pacientů (pouze 10) a všichni měli další rizikový faktor pro vznik šlachových ruptur (krom jiného také léčbu statiny) [24]. Jistě je nezbytné další zkoumání větších skupin léčených pacientů, aby byla odhalena případná kauzální souvislost těchto pozorování.
Celková incidence vedlejších účinků, závažných vedlejších účinků a vedlejších účinků vedoucích k ukončení léčby se ve studii CLEAR Outcomes mezi terapeutickou a placebovou větví významně nelišila. Účast ve studii předčasně ukončilo 2 035 osob (29,1 %), které užívaly účinnou látku, a 2 212 osob (31,7 %) užívajících placebo. Incidence předem daných nežádoucích účinků zvláštního zájmu byla také u obou větví srovnatelná, kromě elevace jaterních transamináz (4,5 % ve skupině léčené kyselinou bempedoovou vs 3,0 % v placebové větvi) a renálních parametrů (11,5 % ve větvi léčené kyselinou bempedoovou vs 8,6 % v placebové větvi) – šlo ovšem o klinicky irelevantní vzestup hladin, v případě kreatininu průměrně o 4,42 ± 17,68 μmol/l. Myalgie byly hlášené častěji v placebové větvi (6,8 % vs 5,6 % při léčbě kyselinou bempedoovou). Incidence hyperurikemie byla vyšší při podávání kyseliny bempedoové ve srovnání s placebem (10,9 % vs 5,6 %), ovšem vzestup koncentrace byl klinicky zcela irelevantní (průměrně o 45,2 ± 71,38 μmol/l za 6 měsíců terapie). Incidence dny (3,1 % vs 2,1 %) a cholelitiázy (2,2 % vs 1,2 %) byla také při podávání kyseliny bempedoové nepatrně zvýšená [23].
Pokud zvážíme veškerá dostupná data zohledňující výskyt nežádoucích účinků při léčbě kyselinou bempedoovou, jeví se jako terapie bezpečná a velmi dobře tolerovaná. Pozorované vedlejší účinky jsou mírné a reverzibilní.
Léková forma a dávka kyseliny bempedoové
Kyselina bempedoová je dostupná v potahovaných tabletách o síle 180 mg a také ve fixní kombinaci s ezetimibem (180 mg kyseliny bempedoové + 10 mg ezetimibu), obě lékové formy se užívají 1krát denně. Terapie je indikovaná k léčbě dospělých osob s familiární hypercholesterolemií nebo smíšenou dyslipidemií v kombinaci se statinem či dalšími hypolipidemiky u osob, které nedosahují cílových koncentrací LDL-C i přes užívání maximální tolerované dávky statinu. Kyselinu bempedoovou lze indikovat do kombinace s jiným hypolipidemikem nebo jako monoterapii u jedinců, kteří léčbu statinem netolerují, nebo je u nich statin kontraindikován [25].
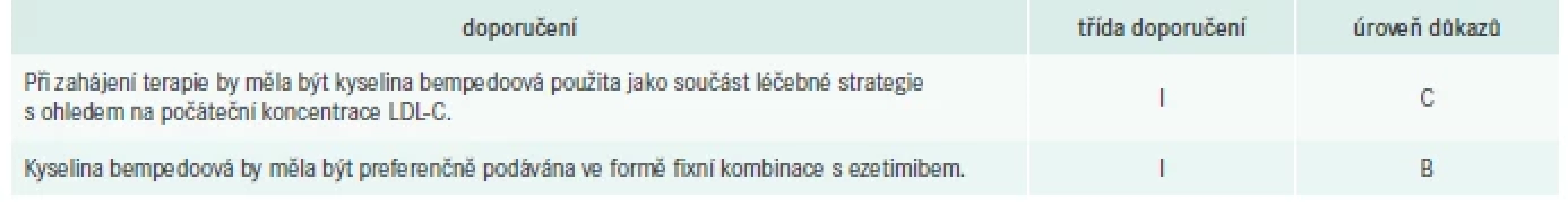
Léčba kyselinou bempedoovou má významný potenciál, kterým může přispět k dosažení cílových hladin sérových lipidů, především v rámci kombinační terapie [10]. Ve formě fixní kombinace s ezetimibem nejenže přispívá ke zlepšení adherence k léčbě, ale je schopna dodatečně snížit hladinu LDL-C až o dalších 40 % (tab. 2).
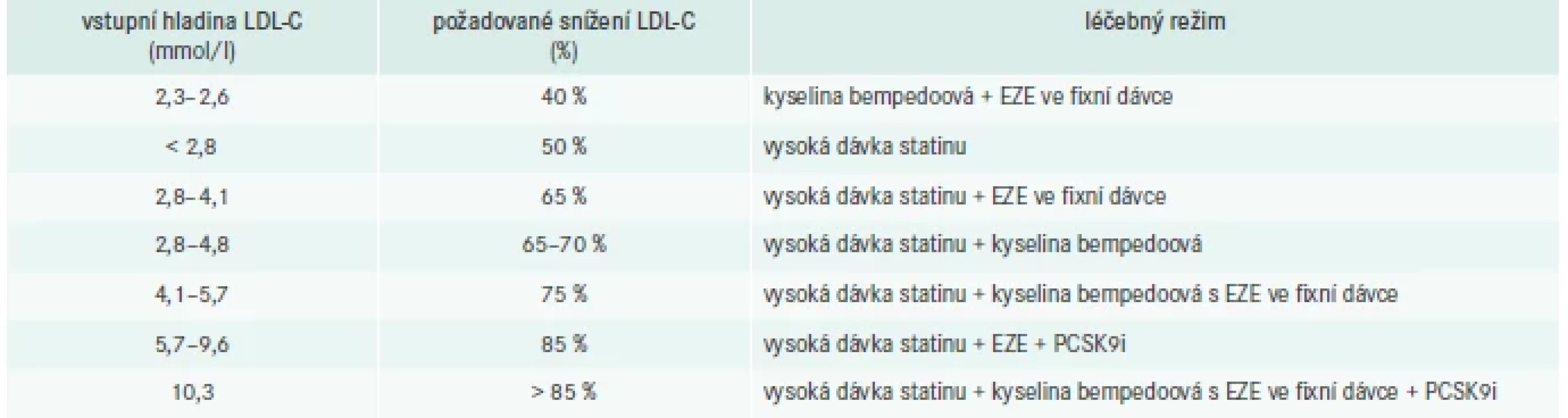
Vzhledem k množství důkazů z klinických studií je dosažitelný účinek konkrétních kombinací hypolipidemik do značné míry předvídatelný (tab. 3). V souladu s doporučeným přístupem „čím níže, tím lépe“, ale také „čím dříve, tím lépe“ je zpravidla upřednostňováno zahájit léčbu jedním lékem a další přidávat v případě nedosažení terapeutického cíle. Rizikem takového přístupu ale může být pozdější docílení doporučených hladin LDL-C, případně ponechání stávající nedostatečné léčby jen kvůli jakési setrvačnosti. Dle vstupních koncentrací LDL-C lze poměrně dobře odhadnout efekt indikované léčby, který již od prvopočátku můžeme cílit dle individuálního KV-rizika našich pacientů (tab. 4).
![Předpokládané percentuální snížení hladiny LDL-C při léčbě kyselinou bempedoovou jak v monoterapii,
tak především v kombinacích s jinými hypolipidemiky (v některých případech se jedná o odhad provedený
na základě dostupných dat). Upraveno podle [8]](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image_pdf/7f3d07b38bd4f3165885f4aae49e2690.png)
Pokud se jedná o kombinaci kyseliny bempedoové se statinem, je třeba opatrnosti při podávání starších molekul, jako je pravastatin, ale také simvastatin. Společné podávání těchto léčiv může vést až k 2násobnému vzestupu koncentrace statinu, což zvyšuje riziko vzniku myopatie spojené s podáváním pravastatinu a simvastatinu, proto bychom se měli vyhnout dávce > 20 mg v případě simvastatinu a dávce > 40 mg v případě pravastatinu [22]. V současné době je kontraindikováno podávání kyseliny bempedoové v kombinaci s 80 mg simvastatinu [25].
Léčba pacientů s ASKVO
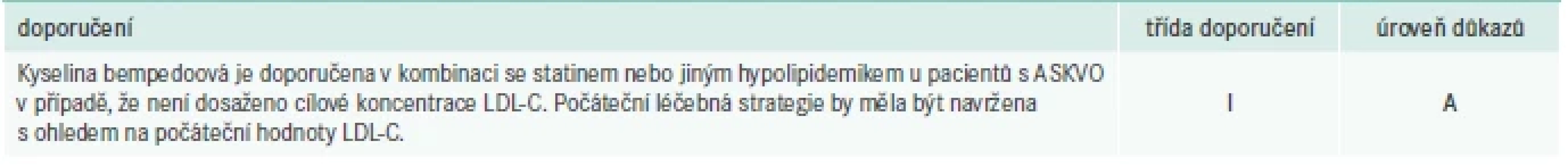
Pacienty s ASKVO je nezbytné léčit intenzivně a terapií optimalizovat rizikové faktory tak, abychom zabránili další KV-příhodě. Bohužel, terapeutických cílů je v současnosti dosahováno zřídkakdy, ať už je to dáno poddávkováním, špatnou adherencí pacientů nebo setrvačností ošetřujících lékařů, kteří netitrují léčbu dostatečně [7,8], tab. 5.
Léčba pacientů s heterozygotní formou FH
Dlouhodobá a výrazná redukce hladiny LDL-C s cílem snížit celoživotní KV-riziko je nezbytná i v této skupině pacientů [26–29]. Efekt kyseliny bempedoové [18,30] je u tohoto typu pacientů prokázán dostupnými studiemi, a to i v dlouhodobém horizontu sledování (až 130 týdnů) [31], tab. 6.

Intolerance statinů
Kyselina bempedoová má potencionální roli při léčbě pacientů netolerujících hypolipidemickou léčbu statiny, a to v rámci doporučeného algoritmu „SLAP“ (Switch statins, Lower dose, Alternate day dosing, Polypharmacy), konkrétně v kroku „Polypharmacy“ [32,33]. Studie CLEAR Outcomes [23] potvrdila benefit i bezpečnost kyseliny bempedoové u statin- -intolerantních osob – prokázala výraznější pokles hladiny LDL-C ve srovnání s nemocnými léčenými redukovanou, maximální tolerovanou dávkou statinu [34–36], tab. 7.

Pokud pacient nesnese ani minimální dávku statinu, je doporučena monoterapie kyselinou bempedoovou nebo její fixní kombinace s ezetimibem (případně volná kombinace s jiným hypolipidemikem). Pokud není ani tímto způsobem dosaženo cílových hodnot LDL-C, je třeba zvážit přidání inhibitoru PCSK9. Ve studii CLEAR Outcomes byla četně za stoupena skupina osob s intolerancí statinů (z nich 22,9 % osob snášejících alespoň malou dávku statinu), u nichž byla potvrzena vysoká účinnost a bezpečnost kyseliny bempedoové [23], tab. 8.

Centrová léčba a primární prevence KVO
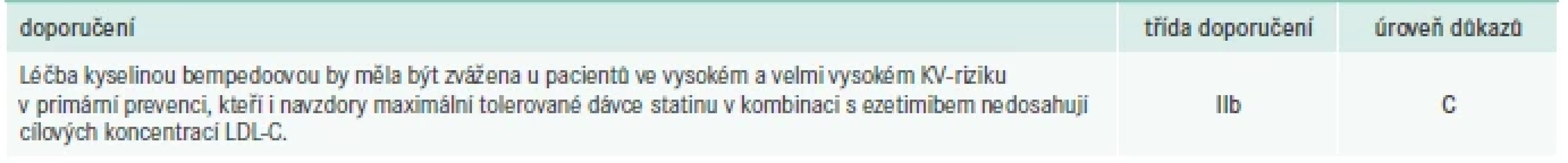
V rámci primární prevence KVO by léčba založená na vysoce dostupných a levných lécích, jako jsou statiny a ezetimib, měla vést až u 80 % pacientů k dosažení cílových hladin LDL-C. Vzhledem ke chronickému extrémnímu poddávkovávání statinů, nedostatečnému využití kombinační léčby statinu a ezetimibu a v neposlední řadě chabé komplianci pacientů je to pouze hypotetický předpoklad [7]. Proto bychom se měli zaměřit také v rámci primární prevence i na jiná hypolipidemika, jakými jsou kyselina bempedoová, inhibitory PCSK9 a inklisiran [8], tab. 9.
Prozánětlivý stav u KVO
Jakkoli je již dlouho uznávaným faktem, že podkladem ASKVO je zánětlivý proces [37], teprve nedávno byl prokázán pozitivní vliv protizánětlivých působků na prevenci KVO [38]. Studie CANTOS prokázala příznivý efekt kanakinumabu (lidská monoklonální protilátka anti-ILβ), jehož podáváním došlo k signifikantnímu poklesu KV-příhod zcela bez ovlivnění hladin plazmatických lipidů [39], bohužel ovšem také k výraznému vzestupu život ohrožujících vedlejších účinků. Podobný vliv na incidenci KV-příhod a pokles koncentrace prozánětlivých markerů byl následně demonstrován při léčbě kolchicinem u pacientů v sekundární KV-prevenci [40]. Dostupné výsledky klinických studií prokazují, že také kyselina bempedoová je schopna snížit hladinu CRP až o 42 %, především u osob se vstupně zvýšenou hladinou C-reaktivního proteinu (CRP) ≥ 2 mg/l [51]. V 6. měsíci studie CLEAR Outcomes byl zaznamenán pokles koncentrace CRP o 21,6 % (95% CI -23,7 až -19,6) ve větvi léčené kyselinou bempedoovou [23]. Navzdory těmto příznivým výsledkům v současné době stále neexistují žádné přímé důkazy o klinickém přínosu snížení koncentrace plazmatického CRP, které bylo navozeno léčbou kyselinou bempedoovou. Ve studiích na zvířatech kyselina bempedoová zprostředkovávala aktivaci hepatální AMP-aktivované protein-kinázy (AMPK), která je zapojena do prozánětlivé signální dráhy, což mělo za následek pokles zánětu [41,42]. Aktivace AMPK pravděpodobně přispívá k signifikantnímu poklesu hs-CRP během podávání kyseliny bempedoové [41]. Proto lze předpokládat, že si kyselina bempedoová najde své místo v terapii osob se zvýšenou plazmatickou koncentrací CRP nebo jiných prozánětlivých parametrů [43], tab. 10.

Diabetes 2. typu a metabolický syndrom
Jak je známo, statiny, především ve vysokých dávkách, mohou zvyšovat riziko vzniku diabetes mellitus 2. typu (DM2T). Tento efekt statinu je ovšem malý (50–100 nových případů na 10 000 pacientů léčených statiny za 5 let) a terapie statiny je i u těchto osob významně prospěšná (3,5- až 5krát vyšší benefit v redukci KV-příhod) [5,8]. Na druhou stranu, kyselina bempedoová má pozitivní vliv na hladinu glykemie, jak již bylo výše zmíněno. Metaanalýza zahrnující 2 419 pacientů léčených kyselinou bempedoovou prokázala významný pokles případů nově diagnostikovaného DM2T, případně snížení počtu případů zhoršení již probíhajícího onemocnění (OR 0,66; 95% CI 0,48–0,90) [44]. Tyto výsledky byly potvrzeny v následující analýze, v níž roční počet případů nově diagnostikovaného DM2T při podávání kyseliny bempedoové činil ve srovnání s placebem u pacientů se vstupní normoglykemií 0,3 % vs 0,8 % a u osob s prediabetem v době zahájení studie pak 4,7 % vs 5,9 % [45]. U pacientů s diabetem nebo prediabetem kyselina bempedoová signifikantně snížila koncentraci HbA1c o 0,12 %, resp. 0,06 %, a nezhoršila glykemii na lačno ve srovnání s podáváním placeba [45]. I studie CLEAR Outcomes přinesla podobný závěr, protože celkový počet nově diagnostikovaného DM2T byl v léčebné větvi nižší (o 0,8–1 %), jakkoli ve skupině léčené kyselinou bempedoovou nebyl zaznamenaný pokles případů nově vzniklého onemocnění (HR 0,95; 0,83–1,09) [23]. Indikaci kyseliny bempedoové bychom jistě měli zvažovat u pacientů, kteří mají riziko rozvoje DM2T nebo mají kolísavé hladiny glykemie. Již v minulosti bylo doporučováno přidání kyseliny bempedoové a ezetimibu k léčbě statiny u pacientů s DM2T, u nichž je třeba dosáhnout snížení koncentrace LDL-C o 65–80 % oproti výchozí hodnotě [46], tab. 11.

Závěr
Kyselina bempedoová je bezpečná, dobře tolerovaná molekula významně snižující koncentraci LDL-C, pozitivně ovlivňující glykemii a prozánětlivé parametry. Ve světle těchto účinků by mohla brzy hrát důležitou roli v kombinační hypolipidemické léčbě a usnadňovat dosahování stanovených terapeutických cílů. Obecně uznávaný přístup k terapii KV- -rizikových jedinců „čím níže a déle, tím lépe“, je uznávaný napříč mezinárodními doporučeními. Uvedli jsme praktická doporučení založená na důkazech týkajících se použití kyseliny bempedoové u nemocných s ASKVO, FH a statinovou intolerancí. Prozatím nemáme k dispozici data hodnotící vliv kyseliny bempedoové v primární KV-prevenci, ale vzhledem k pozitivnímu vlivu na glykemii a prozánětlivé markery by zřejmě i v tomto využití byla více než vhodná. Největší výzvou samozřejmě bude zajistit celosvětovou dostupnost lékové formy s vhodnými úhradovými podmínkami, umožňující její široké užití. Očekávané zkušenosti z klinické praxe dále pomůže potvrdit anebo rozšířit roli kyseliny bempedoové v léčbě dyslipidemií či KV-rizikových pacientů.
Podpořeno MZ ČR – RVO-VFN64165.
Doručeno do redakce 28. 3. 2023
Přijato po recenzi 21. 4. 2023
MUDr. Eva Tůmová, Ph.D.
AtheroRev 2023; 8(2): 85–94
Zdroje
1. Roth GA, Mensah GA, Johnson CO et al. [GBD-NHLBI-JACC Global Burden of Cardiovascular Diseases Writing Group]. Global Burden of Cardiovascular Diseases and Risk Factors, 1990–2019: Update From the GBD 2019 Study. J Am Coll Cardiol 2020; 76(25): 2982–3021. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2020.11.010>.
2. Ference BA, Ginsberg HN, Graham I et al. Low-density lipoproteins cause atherosclerotic cardiovascular disease. 1. Evidence from genetic, epidemiologic, and clinical studies. A consensus statement from the European Atherosclerosis Society Consensus Panel. Eur Heart J 2017; 38(32): 2459–2472. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ ehx144>.
3. Jóźwiak JJ, Studziński K, Tomasik T et al. [LIPIDOGRAM2015 Investigators]. The prevalence of cardiovascular risk factors and cardiovascular disease among primary care patients in Poland: results from the LIPIDOGRAM2015 study. Atheroscler Suppl 2020; 42:e15-e24. Dostupné z DOI: <http://dx.doi.org/10.1016/j.atherosclerosissup.2021.01.004>.
4. Penson PE, Pirro M, Banach M. LDL-C: lower is better for longer-even at low risk. BMC Med 2020; 18(1): 320. Dostupné z DOI: <http://dx.doi. org/10.1186/s12916–020–01792–7>.
5. Collins R, Reith C, Emberson J et al. Interpretation of the evidence for the efficacy and safety of statin therapy. Lancet 2016; 388(10059): 2532–2561. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(16)31357–5>.
6. Hobbs FD, Banach M, Mikhailidis DP et al. Is statin-modified reduction in lipids the most important preventive therapy for cardiovascular disease? A pro/con debate. BMC Med. 2016; 14: 4.10. Dostupné z DOI: <http:// dx.doi.org/1186/s12916–016–0550–5>.
7. Ray KK, Molemans B, Schoonen WM et al. [DA VINCI study]. EU-Wide Cross-Sectional Observational Study of Lipid-Modifying Therapy Use in Secondary and Primary Care: the DA VINCI study. Eur J Prev Cardiol 2021; 28(11): 1279–1289. Dostupné z DOI: <http://dx.doi.org/10.1093/eurjpc/ zwaa047>.
8. Mach F, Baigent C, Catapano AL et al. [ESC Scientific Document Group]. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J 2020; 41(1): 111–188. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehz455>.
9. Bytyci I, Penson PE, Mikhailidis DP et al. Prevalence of statin intolerance: a meta-analysis. Eur Heart J 2022; 43(34): 3213–3223. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehac015.>.
10. Banach M, Penson PE. Lipid-lowering therapies: Better together. Atherosclerosis 2021; 320: 86–88. Dostupné z DOI: <http://dx.doi.org/ 10.1016/j.atherosclerosis.2021.01.009>.
11. Banach M, Penson PE. What have we learned about lipids and cardiovascular risk from PCSK9 inhibitor outcome trials: ODYSSEY and FOURIER? Cardiovasc Res 2019; 115(3): e26-e31. Dostupné z DOI: <http://dx.doi. org/10.1093/cvr/cvy301>.
12. Henney NC, Banach M, Penson PE. RNA Silencing in the Management of Dyslipidemias. Curr Atheroscler Rep 2021; 23(11): 69. Dostupné z DOI: <http://dx.doi.org/10.1007/s11883–021–00968–7>.
13. Penson P, McGowan M, Banach M. Evaluating bempedoic acid for the treatment of hyperlipidaemia. Expert Opin Investig Drugs 2017; 26(2): 251– 259. Dostupné z DOI: <http://dx.doi.org/10.1080/13543784.2017.128045 8>.
14. Pinkosky SL, Newton RS, Day EA et al. Liver-specific ATP-citrate lyase inhibition by bempedoic acid decreases LDL-C and attenuates atherosclerosis. Nat Commun 2016; 7: 13457. Dostupné z DOI: <http://dx.doi. org/10.1038/ncomms13457>.
15. Ballantyne CM, Davidson MH, Macdougall DE et al. Efficacy and safety of a novel dual modulator of adenosine triphosphate-citrate lyase and adenosine monophosphate-activated protein kinase in patients with hypercholesterolemia: results of a multicenter, randomized, double-blind, placebo-controlled, parallel-group trial. J Am Coll Cardiol 2013; 62(13): 1154–62. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2013.05.050>.
16. Thompson PD, Rubino J, Janik MJ et al. Use of ETC-1002 to treat hypercholesterolemia in patients with statin intolerance. J Clin Lipidol 2015; 9(3): 295–304. Dostupné z DOI: <http://dx.doi.org/10.1016/j. jacl.2015.03.003>.
17. Cicero AFG, Fogacci F, Hernandez AV et al. Lipid, Blood Pressure Meta- Analysis Collaboration G, the International Lipid Expert P. Efficacy and safety of bempedoic acid for the treatment of hypercholesterolemia: A systematic review and meta-analysis. PLoS Med 2020;17(7): e1003121. Dostupné z DOI: <http://dx.doi.org/10.1371/journal.pmed.1003121>.
18. Banach M, Duell PB, Gotto AM Jr et al. Association of Bempedoic Acid Administration With Atherogenic Lipid Levels in Phase 3 Randomized Clinical Trials of Patients With Hypercholesterolemia. JAMA Cardiol 2020; 5(10): 1124–1135. Dostupné z DOI: <http://doi 10.1001/jamacardio.2020.2314>.
19. Gunn LH, McKay AJ, Feng et al. Estimated cardiovascular benefits of bempedoic acid in patients with established cardiovascular disease. Atheroscler Plus 2022; 49: 20–27. Dostupné z DOI: <http://dx.doi.org/ 10.1016/j.athplu.2022.05.003>.
20. Lin Y, Parco C, Karathanos A et al. Clinical efficacy and safety outcomes of bempedoic acid for LDL-C lowering therapy in patients at high cardiovascular risk: a systematic review and meta-analysis. BMJ Open 2022; 12(2): e048893. Dostupné z DOI: <http://dx.doi.org/10.1136/ bmjopen-2021–048893>.
21. Nicholls S, Lincoff AM, Bays HE et al. Rationale and design of the CLEAR-outcomes trial: Evaluating the effect of bempedoic acid on cardiovascular events in patients with statin intolerance. Am Heart J 2021; 235: 104–112. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ahj.2020.10.060>.
22. Esperion Therapeutics Inc. Esperion Announces CLEAR Cardiovascular Outcomes Trial of NEXLETOL® (bempedoic acid) Meets Primary Endpoint. Dostupné z WWW: <https://www.aspconline.org/uncategorized/esperion- -announces-clear-cardiovascular-outcomes-trial-of-nexletol-bempedoic- -acid-meets-primary-endpoint/>.
23. Nissen SE, Lincoff AM, Brennan D et al. Bempedoic acid and cardiovascular outcomes in statin-intolerant patients. N Engl J Med 2023; 388(15): 1353–1364. Dostupné z DOI: <http://dx.doi.org/10.1056/ NEJMoa2215024>.
24. Bays HE, Banach M, Catapano AL et al. Bempedoic acid safety analysis: Pooled data from four phase 3 clinical trials. J Clin Lipidol 2020; 14(5): 649– 659 e6. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacl.2020.08.009>.
25. Nilemdo 180 mg film-coated tablets. SPC. Dostupné z WWW: <https://www.ema.europa.eu/en/documents/product-information/ nilemdo-epar-product-information_en.pdf>.
26. Banach M, Penson PE. Cellular senescence, telomeres, and cardiovascular risk in familial hypercholesterolaemia. Eur J Prev Cardiol 2022; 29(5): 718–720. Dostupné z DOI: <http://dx.doi.org/10.1093/eurjpc/zwaa145>.
27. Lewek J, Konopka A, Starostecka E et al. Clinical Features of Familial Hypercholesterolemia in Children and Adults in EAS-FHSC Regional Center for Rare Diseases in Poland. J Clin Med 2021; 10(19): 4302. Dostupné z DOI: <http://dx.doi.org/10.3390/jcm10194302>.
28. Banach M, Penson PE. Genetic testing in familial hypercholesterolaemia: What does it add? Eur J Prev Cardiol 2020; 27(1): 105–106. Dostupné z DOI: <http://dx.doi.org/10.1177/2047487319870342>.
29. Banach M, Penson PE. Homozygous familial hypercholesterolaemia: shedding new light on a rare but deadly condition. Eur J Prev Cardiol 2022; 29(5): 815–816. Dostupné z DOI: . <http://dx.doi.org/10.1093/eurjpc/ zwac032>.
30. Ray KK, Bays HE, Catapano AL et al. CLEAR Harmony Trial. Safety and Efficacy of Bempedoic Acid to Reduce LDL Cholesterol. N Engl J Med 2019; 380(11): 1022–1032. Dostupné z DOI: <http://dx.doi.org/10.1056/ NEJMoa1803917>.
31. Ballantyne CM, Banach M, Bays HE et al. Long-Term Safety and Efficacy of Bempedoic Acid in Patients With Atherosclerotic Cardiovascular Disease and/or Heterozygous Familial Hypercholesterolemia (from the CLEAR Harmony Open-Label Extension Study). Am J Cardiol 2022; 174: 1–11. Dostupné z DOI: <http://dx.doi.org/10.1016/j.amjcard.2022.03.020>.
32. Penson PE, Bruckert E, Marais D et al. [International Lipid Expert Panel]. Step-by-step diagnosis and management of the nocebo/drucebo effect in statin-associated muscle symptoms patients: a position paper from the International Lipid Expert Panel (ILEP). J Cachexia Sarcopenia Muscle 2022; 13(3): 1596–1622. Dostupné z DOI: <http://dx.doi.org/10.1002/ jcsm.12960>.
33. Penson PE, Banach M. Nocebo/drucebo effect in statin-intolerant patients: an attempt at recommendations. Eur Heart J 2021; 42(47): 4787– 4788. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehab358.
34. Laufs U, Ballantyne CM, Banach M et al. Efficacy and safety of bempedoic acid in patients not receiving statins in phase 3 clinical trials. J Clin Lipidol 2022; 16(3): 286–297. Dostupné z DOI: <http://dx.doi.org/10.1016/j. jacl.2022.03.001>.
35. Laufs U, Banach M, Mancini GBJ et al. Efficacy and Safety of Bempedoic Acid in Patients With Hypercholesterolemia and Statin Intolerance. J Am Heart Assoc 2019; 8(7): e011662. Dostupné z DOI: <http://dx.doi. org/10.1161/JAHA.118.011662>.
36. Ballantyne CM, Banach M, Mancini GB et al. Efficacy and safety of bempedoic acid added to ezetimibe in statin-intolerant patients with hypercholesterolemia: A randomized, placebo-controlled study. Atherosclerosis 2018; 277: 195–203. Dostupné z DOI: <http://dx.doi.org/10.1016/j. atherosclerosis.2018.06.002>.
37. Ross R. Atherosclerosis – an inflammatory disease. N Engl J Med 1999; 340(2): 115–126. Dostupné z DOI: <http://dx.doi.org/10.1056/ NEJM199901143400207>.
38. Penson PE, Long DL, Howard G et al. Associations between very low concentrations of low density lipoprotein cholesterol, high sensitivity C-reactive protein, and health outcomes in the Reasons for Geographical and Racial Differences in Stroke (REGARDS) study. Eur Heart J 2018; 39(40): 3641–3653. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ ehy533>.
39. Ridker PM, Everett BM, Thuren T et al. CANTOS Trial Group. Antiinflammatory Therapy with Canakinumab for Atherosclerotic Disease. N Engl J Med 2017; 377(12): 1119–1131. Dostupné z DOI: <http://dx.doi. org/10.1056/NEJMoa1707914>.
40. Bytyci I, Bajraktari G, Penson PE et al. [Lipid and Blood Pressure Meta- Analysis Collaboration (LBPMC) Group; International Lipid Expert Panel (ILEP)]. Efficacy and safety of colchicine in patients with coronary artery disease: A systematic review and meta-analysis of randomized controlled trials. Br J Clin Pharmacol 2022; 88(4): 1520–1528. Dostupné z DOI: <http://dx.doi.org/10.1111/bcp.15041>.
41. Stroes ESG, Bays HE, Banach M et al. Bempedoic acid lowers high- -sensitivity C-reactive protein and low-density lipoprotein cholesterol: Analysis of pooled data from four phase 3 clinical trials. Atherosclerosis 2023; 373: 1–9. Dostupné z DOI: <http://dx.doi.org/10.1016/j. atherosclerosis.2023.03.020>.
42. Pinkosky SL, Newton RS, Day EA et al. Liver-specific ATP-citrate lyase inhibition by bempedoic acid decreases LDL-C and attenuates atherosclerosis. Nat Commun 2016; 7: 13457. Dostupné z DOI: <http://dx.doi. org/10.1038/ncomms13457>.
43. Maierean S, Webb R, Banach M et al. The role of inflammation and the possibilities of inflammation reduction to prevent cardiovascular events. Eur Heart J Open 2022; 2(4): oeac039. Dostupné z DOI: <http://dx.doi. org/10.1093/ehjopen/oeac039>.
44. Masson W, Lobo M, Lavalle-Cobo A et al. Effect of bempedoic acid on new onset or worsening diabetes: A meta-analysis. Diabetes Res Clin Pract 2020; 168: 108369. Dostupné z DOI: <http://dx.doi.oeg/10.1016/j. diabres.2020.108369>.
45. Leiter LA, Banach M, Catapano AL et al. Bempedoic acid in patients with type 2 diabetes mellitus, prediabetes, and normoglycaemia: A post hoc analysis of efficacy and glycaemic control using pooled data from phase 3 clinical trials. Diabetes Obes Metab 2022; 24(5): 868–880. Dostupné z DOI: <http://dx.doi.org/10.1111/dom.14645>.
46. Banach M, Surma S, Reiner Z et al. Personalized management of dyslipidemias in patients with diabetes-it is time for a new approach (2022). Cardiovasc Diabetol 2022; 21(1): Dostupné z DOI: <http://dx.doi. org/263.10.1186/s12933–022–01684–5>.
Štítky
Angiológia Diabetológia Interné lekárstvo Kardiológia Praktické lekárstvo pre dospelýchČlánok vyšiel v časopise
Athero Review

2023 Číslo 2
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Fixní kombinace paracetamol/kodein nabízí synergické analgetické účinky
- Antidepresivní efekt kombinovaného analgetika tramadolu s paracetamolem
- Kombinace metamizol/paracetamol v léčbě pooperační bolesti u zákroků v rámci jednodenní chirurgie
- 100 let s metamizolem: jaké je jeho současné postavení v léčbě bolesti
Najčítanejšie v tomto čísle
- Kyselina bempedoová v kontextu současných možností hypolipidemické léčby a výsledků studie CLEAR OUTCOMES
- Stanovisko ČSAT ke Konsenzu Evropské společnosti pro aterosklerózu: Lipoprotein(a) při aterosklerotických kardiovaskulárních onemocněních a aortální stenóze
- Význam nestatínových liekov pre znižovanie LDL-cholesterolu v manažmente veľmi vysokého a vysokého aterosklerotického kardiovaskulárneho rizika
- Hyperlipidemická krize jako rizikový faktor pro vznik akutní pankreatitidy
