-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Vplyv teploty a koncentrácie tenzidu na farmaceutickú dostupnosť liečiva
Influence of temperature and concentration of a surfactant on pharmaceutical availability
This study aimed to analyze the influence of surfactant concentration and temperature on drug liberation from hydrogels and their flow properties. The surfactant benzethonium chloride (BZCl) was used in concentrations of 0.01, 0.1 and 0.5 % (w/w), while the drug chlorhexidine dihydrochloride (CHX) was used in a concentration of 0.1 % (w/w). Chitosan (CHIT) in 2.5 % (w/w) concentration was used as a gel-creating substance. The drug and surfactant liberation were evaluated within the temperature range of 25–40 °C. The largest amounts of both of them were liberated at the temperature of 40 °C. Through the concentration changes it was possible to obtain statistically significant differences (P < 0.05) between the liberation of CHX and BZCl. An analysis of the flow properties revealed that the character of the plastic system was not influenced by the changing concentration of the surfactant. The experimental results led to the conclusion that the optimum composition of the gel was as follows: 2.5 % (w/w) CHIT + 0.1 % (w/w) CHX + 0.01 % (w/w) BZCl.
Keywords:
chlorhexidine dihydrochloride •benzethonium chloride • chitosan • liberation • critical micelle concentration
Autori: Petra Herdová; Zuzana Vitková; Jarmila Oremusová; Alexandra Kodadová
Pôsobisko autorov: Univerzita Komenského v Bratislave ; Farmaceutická fakulta, Katedra galenickej farmácie ; PharmDr. Petra Herdová, PhD. (∗) • Zuzana Vitková • Alexandra Kodadová
Vyšlo v časopise: Čes. slov. Farm., 2013; 62, 223-226
Kategória: Původní práce
Súhrn
Predmetom tejto štúdie bolo sledovanie vplyvu zmeny koncentrácie tenzidu a teploty na liberáciu liečiva z hydrogélov a ich tokové vlastnosti. Použitým tenzidom bol benzetóniumchlorid (BZCl), v koncentrácii – 0,01; 0,1 a 0,5 % (m/m). Liečivo chlórhexidíniumdichlorid (CHX) bolo použité v 0,1 % (m/m) koncentrácii. Vo funkcii gélotvornej látky bol použitý chitosan (CHIT) v 2,5 % (m/m) koncentrácii. V práci sa hodnotila liberácia liečiva a tenzidu v teplotnom intervale 25–40 °C. Najviac liečiva sa uvoľnilo pri teplote 40 °C, rovnako to bolo aj v prípade tenzidu. Zmenou koncentrácie tenzidu v géloch sa získali štatisticky významné rozdiely (P < 0,05) v uvoľňovaní CHX a BZCl. Na základe štúdie tokových vlastností gélov sa zistilo, že zmena koncentrácie tenzidu neovplyvnila charakter plastickej sústavy. Na základe dosiahnutých výsledkov sa stanovil gél optimálneho zloženia: 2,5 % (m/m) CHIT + 0,1 % (m/m) CHX + 0,01 % (m/m) BZCl.
Kľúčové slová:
chlórhexidíniumdichlorid • benzetóniumchlorid • chitosan • liberácia • kritická micelová koncentráciaÚvod
Tenzidy (povrchovoaktívne látky) majú dôležitú úlohu v základných aj aplikovaných vedách. Jednou z významných vlastností týchto látok je schopnosť vytvárať asociáty, napr. micely. Vďaka tomu majú veľký význam vo farmácii pri zvyšovaní rozpustnosti ťažko rozpustných liečiv. Využitie miciel ako nosičov liečiv má viacero výhod oproti iným systémom1). Povrchovoaktívne látky sa v súčasnej farmaceutickej biotechnológii využívajú v rôznych dávkovacích schémach na úpravu biologickej dostupnosti liečiv. Vo farmaceutickej technológii sa vo veľkej miere uplatňujú ako emulgátory, na stabilizovanie disperzných systémov – emulzií a suspenzií. Vo funkcii enhancerov urýchľujú penetráciu a zvyšujú prestup liečiv cez membrány.
Pre využitie a aplikáciu tenzidov je dôležité poznať ich správanie v rôznych sústavách. Asociáty vznikajú po prekročení určitej koncentrácie – kritická micelová koncentrácia (CMC). Táto koncentrácia je pre tenzidy významnou charakteristikou. Čím nižšia je hodnota CMC daného tenzidu, tým sú micely stabilnejšie.
Proces tvorby miciel je výsledkom rovnováhy molekulových síl – hydrofóbnych, sférických, hydrostatických, vodíkových, van der Walsových väzieb a síl vzájomného ovplyvňovania. Či k micelizácii dôjde alebo nie, závisí od koncentrácie tenzidu a od rovnováhy síl podporujúcich a zabraňujúcich micelizácii a agregácii. Tvar a veľkosť miciel môže byť ovplyvnená zmenou chemickej štruktúry tenzidu, ako aj zmenou podmienok v roztoku, ako je teplota, celková koncentrácia tenzidu, pH a iónová sila2).
Kritická micelová koncentrácia sa môže s rastúcou teplotou zvyšovať, pozorované u iónových tenzidov, alebo znižovať, pozorované u neiónových tenzidov. Na jednej strane spôsobí zvýšenie teploty zníženie hydratácie hydrofilnej skupiny, čo podporuje micelizáciu, na druhej strane zvýšenie teploty zapríčiní narušenie štruktúry vody obklopujúcej hydrofóbne skupiny, čo znižuje micelizáciu. Veľkosť týchto protichodných účinkov rozhoduje o zvýšení, resp. znížení CMC v závislosti od teploty3). Minimum v závislosti CMC od teploty sa pri iónových tenzidoch nachádza pri teplote okolo 25 °C4).
Kvartérne amóniové zlúčeniny sú najdôležitejšou skupinou povrchovoaktívnych látok. Význam katiónových tenzidov spočíva hlavne v dezinfekčných a antiseptických účinkoch. Katiónové tenzidy vytvárajú adsorpčnú vrstvu na mikroorganizmoch, a tým narušia ich respiračné a metabolické funkcie, čo vedie postupne k zániku mikrobiálnych látok. Je známe, že katiónové tenzidy nepoškodzujú pokožku a majú veľmi malú toxicitu, preto sa používajú ako antiseptiká, sú súčasťou kúpeľových pien a kozmetických výrobkov5).
Medzi katiónové tenzidy patrí aj benzetóniumchlorid (N-benzyl-N,N-dimetyl-2-{2-[4-(2,4,4-trimetylpentan-2-yl)-fenoxy]etoxy}-etanamínium-chlorid). Táto syntetická soľ je biela až bezfarebná tuhá kryštalická látka bez zápachu, veľmi horkej chuti, rozpustná vo vode, alkohole, glykole, benzéne, acetóne a iných organických rozpúšťadlách. Teplota topenia je 164–166 °C. Je inkompatibilný s aniónovými povrchovoaktívnymi látkami a silnými oxidačnými činidlami. Môže reagovať s nitrátmi. Je citlivý na svetlo. Má povrchovoaktívne, antiseptické a antiinfekčné vlastnosti. Používa sa v kozmetike a hygienických potrebách, ako sú ústne vody, masti proti svrbeniu a antibakteriálne vlhčené obrúsky6–7). Vykazuje široké spektrum aktivity ako baktericídna látka. Jeho baktericídna aktivita spočíva v rozrušení permeability bunkovej membrány. Koncentrácia pri ktorej vykazuje baktericídnu aktivitu sa pohybuje od 0,005 do 0,01 %. Bolo preukázané, že inhibuje aj množstvo proteolytických enzýmov a má malú inhibičnú aktivitu aj na acetylcholínesterázu. Ústne vody obsahujúce benzetóniumchlorid v koncentrácii od 0,075 do 0,01 % vykazujú zníženie akumulácie zubného plaku. Takisto bol začlenený aj do polymerizovaného metylmetakrylátu, ktorý sa používa v kontaktných šošovkách. V koncentrácii 0,2 % má spermicídne účinky. Vodné roztoky nie sú absorbované kožou8). Zlúčenina je po perorálnom podaní toxická, spôsobuje neuromuskulárnu blokádu6).
Cieľom tejto práce bolo sledovať vplyv teploty a zmeny koncentrácie benzetóniumchloridu na liberáciu liečiva chlórhexidín z chitosanových gélov a ich tokové vlastnosti.
Pokusná časť
Použité chemikálie
Chlórhexidíniumdichlorid (CHX) – Chlorhexidini dichloridum SL1 – Imperial chemical industries, Geshire, GB;
Chitosan – stredná molekulová hmotnosť – stupeň deacetylácie 75–85 % (CHIT) – Sigma – Aldrich, USA;
benzetóniumchlorid (BZCl) – Benzethonii chloridum SL1 – Sigma – Aldrich, USA;
kyselina mliečna – Interpharm, SR; permeačná celofánová membrána – EKOZ s.r.o., SR;
čistená voda – FaF UK, Bratislava, SR.
Použité prístroje a materiál
Permeačná aparatúra vyrobená na KGF, FaF, UK, Bratislava, SR;
permeačná membrána (celofán) – EKOZ s. r. o, SR;
spektrofotometer – Philips Pyll Unicam 8625 Ltd., Cambridge, GB;
termostat U 10-Prüfgeräte – Werk Medingen, D;
viskotester VT 500 Haake Mess-Technik GmbH, Karlsruhe, D.
Zloženie a príprava hydrogélov
Boli pripravené gély na báze 2,5 % (m/m) CHIT. Nakoľko CHIT sa rozpúšťa a tvorí gély len v kyslom prostredí, použila sa kyselina mliečna v 1 % (m/m) koncentrácii. Pridávalo sa liečivo chlórhexidíniumdichlorid použité v 0,1 % (m/m) koncentrácii a vo funkcii tenzidu sa použil benzetóniumchlorid v koncentrácii 0,01 %; 0,1 % a 0,5 % (m/m). Pre porovnanie výsledkov boli pripravené blanky.
vzorka č. 1: 2,5 % (m/m) CHIT + 0,1 % (m/m) CHX + 0,01 % (m/m) BZCl
vzorka č. 2: 2,5 % (m/m) CHIT + 0,1 % (m/m) CHX + 0,1 % (m/m) BZCl
vzorka č. 3: 2,5 % (m/m) CHIT + 0,1 % (m/m) CHX + 0,5 % (m/m) BZCl
Liberácia liečiv z hydrogélov a stanovenie obsahu liečiv
Liberácia liečiv sa sledovala použitím permeačnej aparatúry v 6 komôrkach, kde do donorovej časti sa dali 3 g gélu a do akceptorovej časti 20 ml aqua purificata. Aparatúra sa temperovala na 25; 30; 35 a 40 ± 0,2 °C. Odbery sa robili v časovom rozsahu 3 hodín, t.j. po 15, 30, 45, 60, 90, 120 a 180 minúte. Ako semipermeabilná membrána bol použitý celofán. Vykonalo sa 6 paralelných stanovení. Uvoľnené množstvo CHX a BZCl sa stanovilo spektrofotometricky pri príslušnej vlnovej dĺžke: λCHX = 254 nm, λBZCl = 274 nm.
Stanovenie reologických parametrov
Reologické vlastnosti hydrogélov sa hodnotili 48 h po príprave hydrogélov pomocou rotačného viskozimetra VISCOTESTER VT 500 pri teplote 20 ± 0,2 °C.
Výsledky
V predchádzajúcich štúdiách bola zistená kritická micelová koncentrácia tenzidu – BZCl9). Na základe uvedených poznatkov (tab. 1) bola pre experimenty zvolená koncentrácia pod CMC 0,01 % a 0,1 % (m/m) a nad CMC 0,5 % (m/m). Cieľom štúdie bolo zhodnotiť vplyv zmeny koncentrácie tenzidu a teploty na liberáciu liečiva z hydrogélov a ich tokové vlastnosti. Merania boli vykonané pri teplotách v rozmedzí 25–40 °C.
Tab. 1. CMC pre BZCl pri teplote 25–40 °C 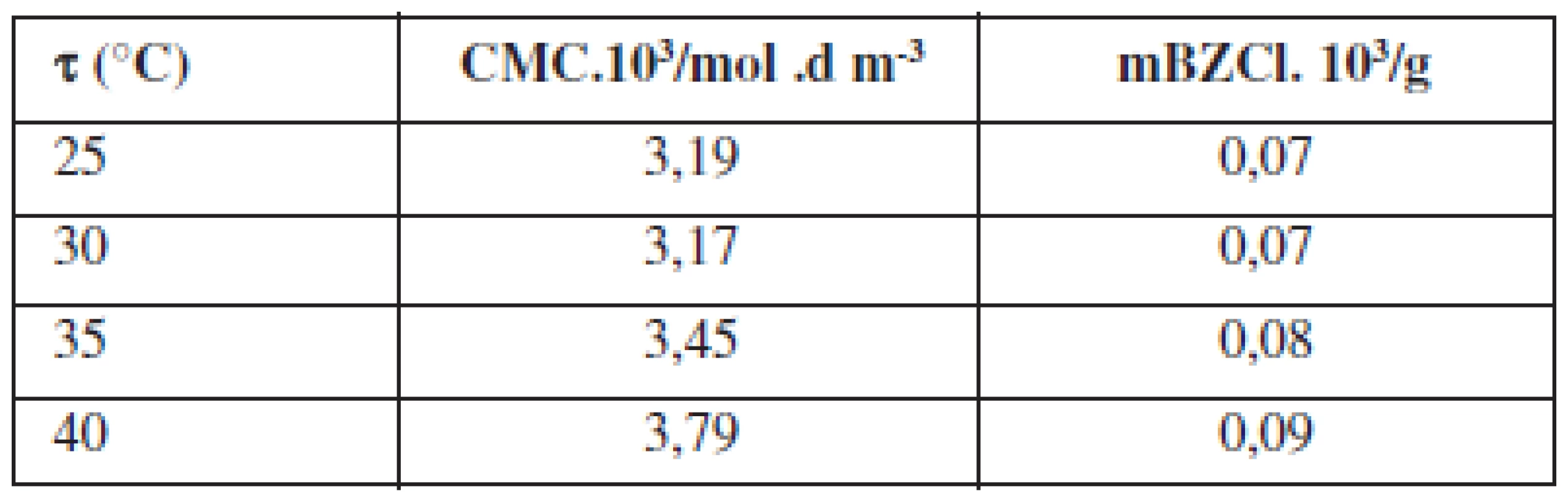
Výsledky liberácie BZCl a CHX sú zhrnuté v tabuľke 2. Vo vzorke č. 1 sa zvolila koncentrácia tenzidu 0,01 % (m/m), čo zodpovedá hodnote pod CMC. Pri tejto hodnote sa najlepšie uvoľňoval CHX ako aj BZCl. Ako je z obr. 1A vidieť, najviac liečiva CHX sa uvoľnilo po 180 min pri teplote 40 °C a to 96,28 % (m/m). S rastúcou teplotou medzi 25–35 °C sa štatisticky významne nemenili (P > 0,05) množstvá uvoľneného CHX (tab. 2). Štatisticky významné rozdiely (P < 0,05) v množstve uvoľneného CHX sa zistili v intervale 35–40 °C. Podobný priebeh uvoľňovania mal aj BZCl (obr. 1B), kedy sa pri 40 °C uvoľnilo najvyššie percento BZCl 98,49 % (m/m). Z hľadiska štatistickej významnosti sa nezistili štatisticky významné (P > 0,05) rozdiely v množstve uvoľneného BZCl medzi 30 °C a 35 °C, pri ostatných teplotách boli naopak zistené štatisticky významné rozdiely (P < 0,05).
Obr. 1. Liberácia CHX (A) a BZCl (B) zo vzorky č. 1 pri rôznej teplote (25–40 °C) 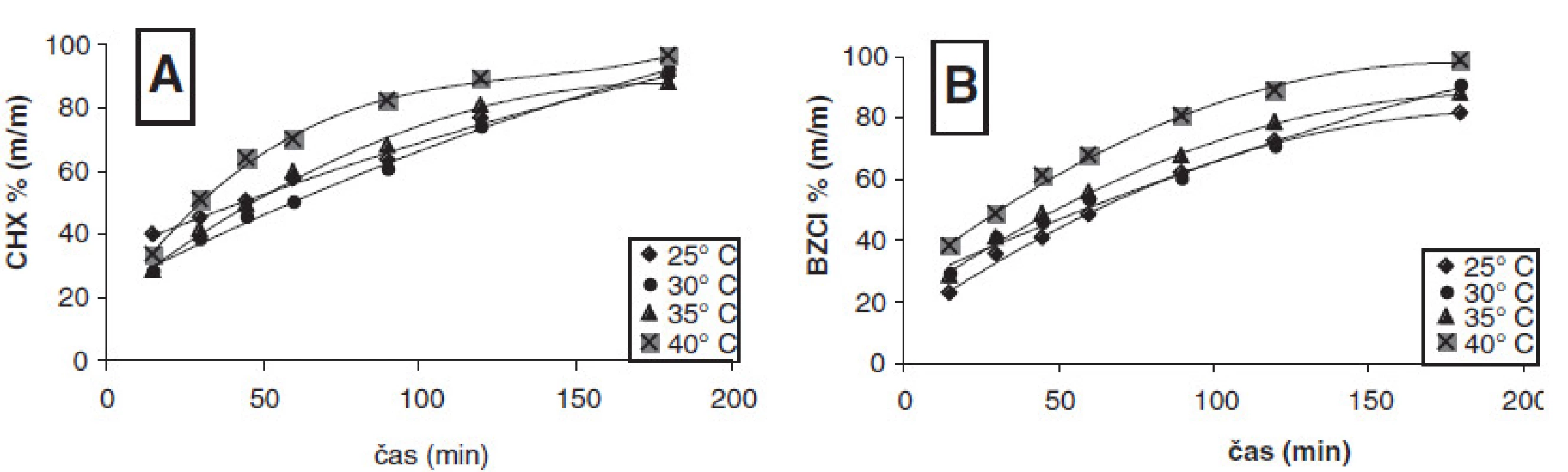
Tab. 2. Uvoľnené množstvo CHX a BZCl (% m/m) po 180 min 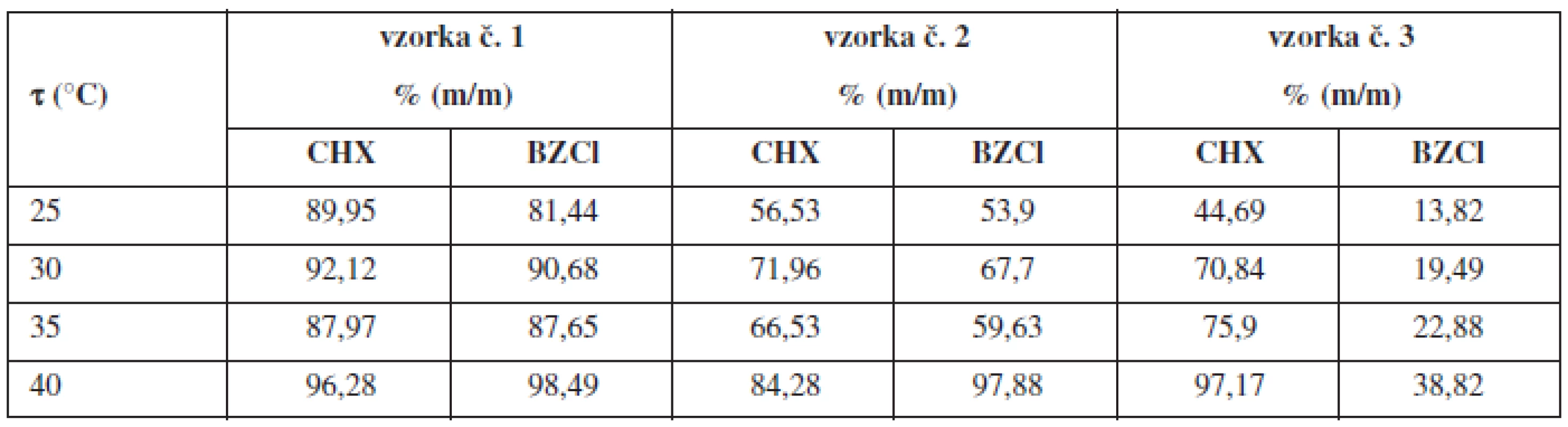
V ďalšej časti výskumu sa pripravil gél s vyšším obsahom tenzidu – v koncentrácii 0,1 % (m/m), tesne pod CMC. Na obrázku 2A vidieť, že najviac liečiva CHX sa uvoľnilo pri 40 °C 84,28 % (m/m). Vplyv teploty sa prejavil aj na množstve uvoľneného liečiva, zistili sa štatisticky významné rozdiely (P < 0,05) v množstve uvoľneného CHX v celom teplotnom intervale 25–40 °C. V prípade uvoľňovania BZCl (obr. 2B) sa dosiahlo najvyššie percento uvoľnenia BZCl pri 40 °C 97,88 % (m/m). Rovnako ako pri CHX boli zistené štatisticky významné rozdiely (P < 0,05) v množstve uvoľneného BZCl medzi jednotlivými teplotami v intervale 25–40 °C (tab. 2).
Obr. 2. Liberácia CHX (A) a BZCl (B) zo vzorky č. 2 pri rôznej teplote (25–40 °C) 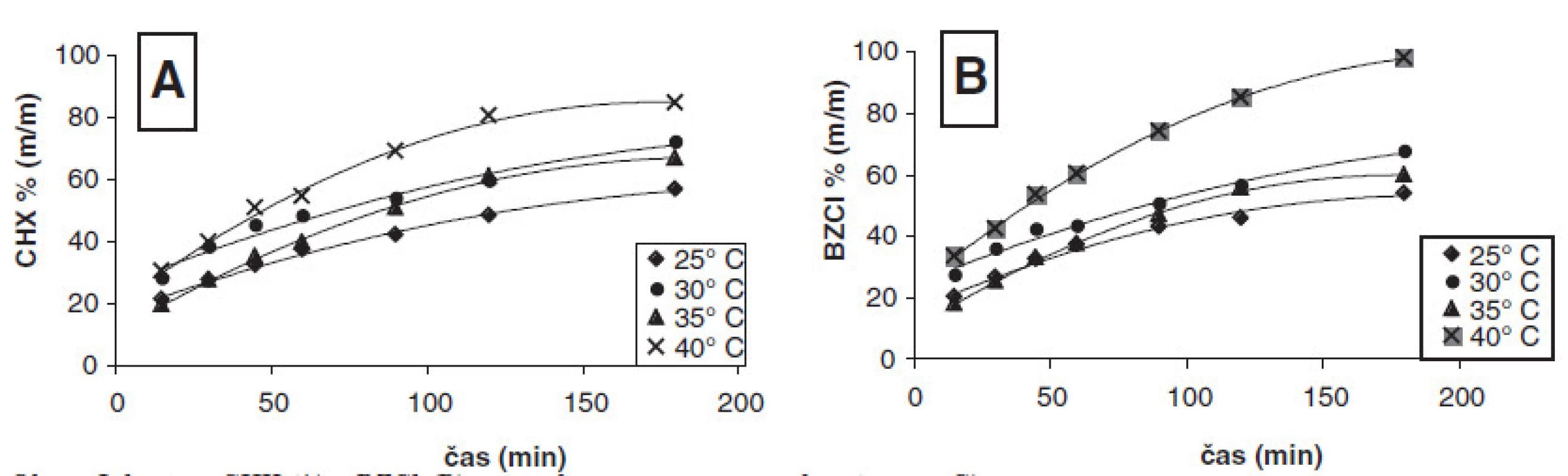
Experimentálne najvyššia zvolená koncentrácia tenzidu bola 0,5 % (m/m), čo je už nad hodnotou CMC tenzidu. Všeobecne možno konštatovať, že s rastúcou teplotou stúpalo množstvo uvoľneného CHX (obr. 3A) ako aj BZCl (obr. 3B). V oboch prípadoch boli zistené štatisticky významné rozdiely (P < 0,05) v množstve uvoľňovania CHX a BZCl v sledovanom teplotnom intervale (tab. 2). Najvyššie množstvá uvoľneného CHX (97,17 % (m/m)) ako aj BZCl (38,82 % (m/m)) sa dosiahli pri 40 °C. Pri porovnaní výsledkov vzorky č. 3 so vzorkami č. 1 a 2 je vidieť, že prekročenie CMC (vzorka č. 3) sa prejavilo aj na výraznom poklese uvoľňovania BZCl oproti CHX.
Obr. 3. Liberácia CHX (A), BZCl (B) zo vzorky č. 3 pri rôznej teplote (25–40 °C) 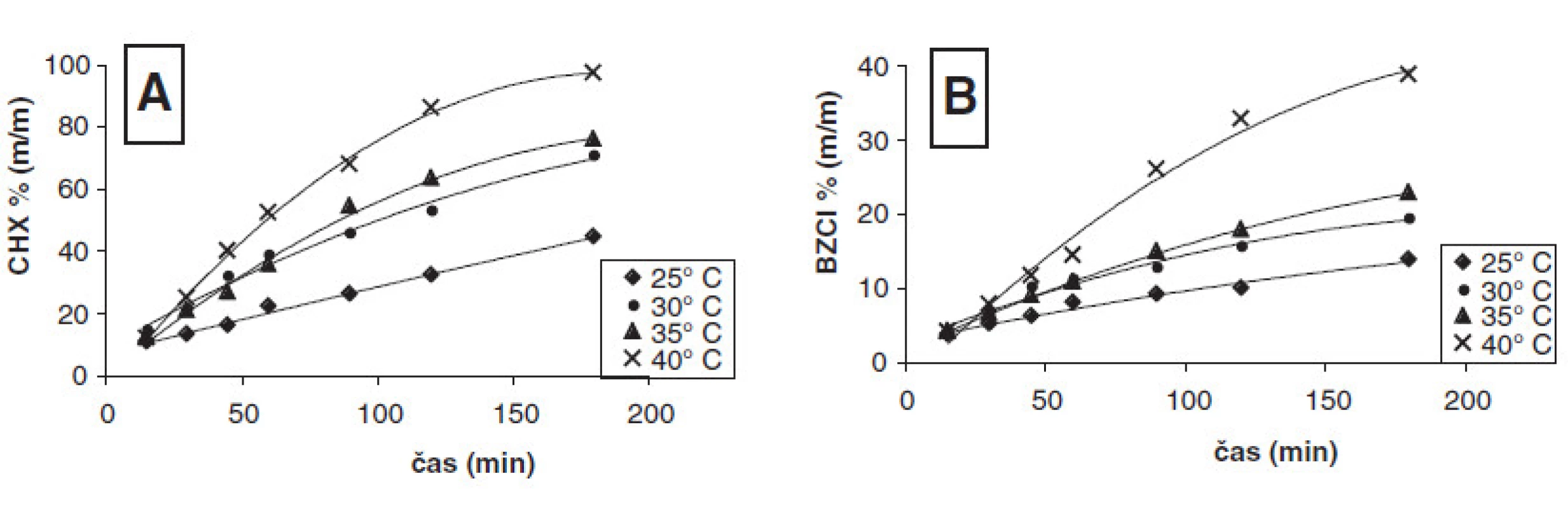
V poslednej etape výskumu sa hodnotili tokové vlastnosti hydrogélov. Pripravené gély mali charakter plastických sústav s časovo nezávislým tokom (obr. 4). Koncentrácia tenzidu nemala vplyv na zmenu tokových vlastností sústav.
Obr. 4. Tokové krivky vzorky č. 1–3 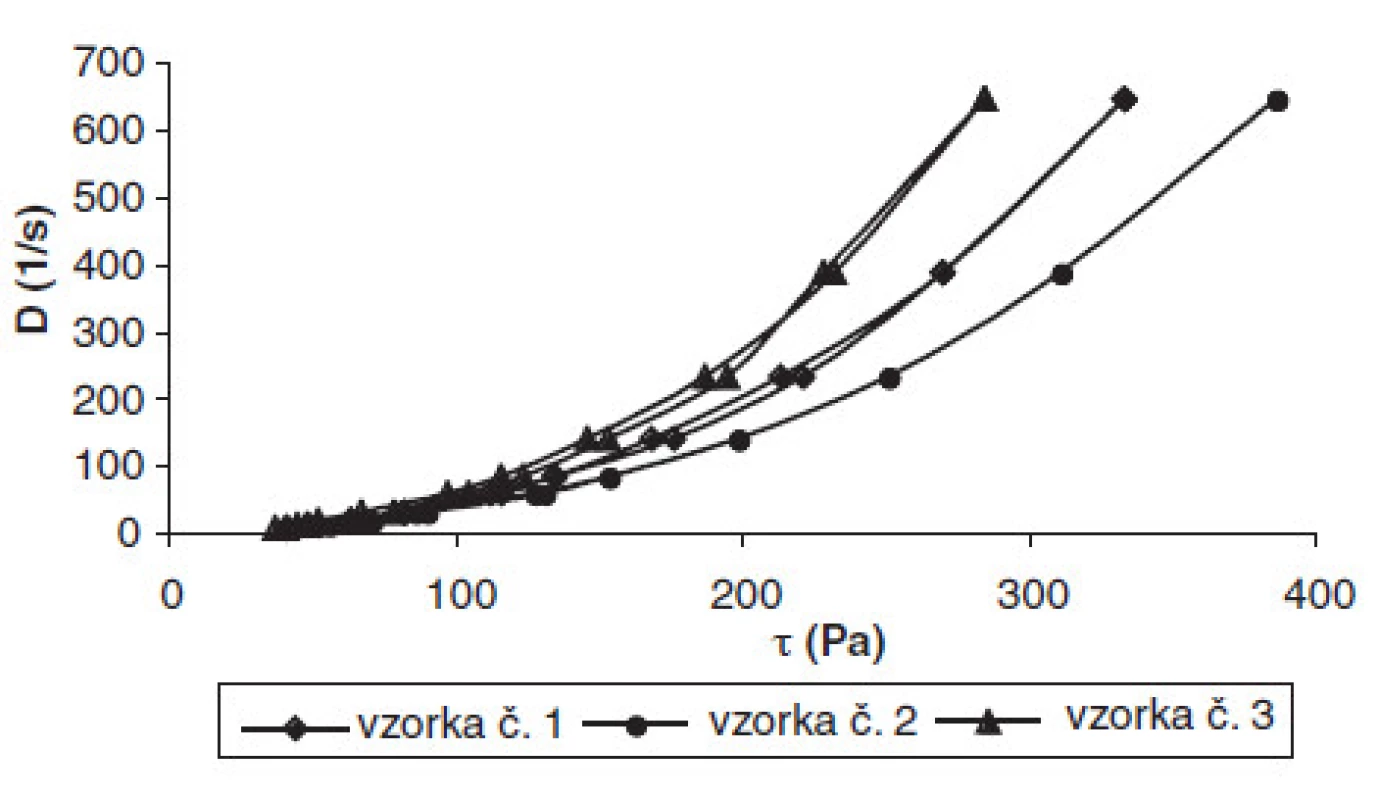
Na liberáciu CHX a BZCl výrazne vplývala aj teplota, najlepšie sa uvoľňoval CHX ako aj BZCl pri teplote 40 °C. Porovnaním dosiahnutých výsledkov liberácie CHX pri 40 °C v závislosti od hodnoty CMC tenzidu sa zistili štatisticky významné rozdiely (P < 0,05) v množstve uvoľneného liečiva medzi vzorkou č. 1 a 2; 2 a 3. V prípade uvoľňovania BZCl boli zistené štatisticky významné rozdiely medzi vzorkami č. 1 a 3; 2 a 3.
Na základe dosiahnutých výsledkov sa zistilo, že prekročenie kritickej micelovej koncentrácie BZCl v géloch môže významne ovplyvniť uvoľňovanie liečiva CHX. So zvyšovaním koncentrácie BZCl v závislosti od teploty sa pozorovali štatisticky významné (väčšie) rozdiely v uvoľňovaní CHX a BZCl. Zvýšenie koncentrácie BZCl sa prejavilo na znížení v množstve uvoľnenom CHX a BZCl. Optimálne zloženie gélu bolo nasledovné:
2,5 % (m/m) CHIT + 0,1 % (m/m) CHX + 0,01 % (m/m) BZCl (vzorka č. 1).
Výskum bol podporený grantami FAF UK/3/2013, UK/101/2013, VEGA 1/0024/11.
Stret záujmov: žiadny.
Došlo 9. září 2013
Přijato 19. září 2013
PharmDr. Petra Herdová, PhD. (∗) • Zuzana Vitková • Alexandra Kodadová
Univerzita Komenského v Bratislave
Farmaceutická fakulta, Katedra galenickej farmácie
Odbojárov 10, 832 32 Bratislava, Slovenská republika
e-mail: herdova@fpharm.uniba.sk
Jarmila Oremusová
Univerzita Komenského v Bratislave
Farmaceutická fakulta, Katedra fyzikálnej chémie liečiv
Zdroje
1. Rangel-Yagui C. O., Pessoa A., Tavares L. C. Micellar Solubilization of Drugs. J Pharm Pharmaceut Sci 2005; 8(2), 147–165.
2. Bartovská L. Fyzikální chemie povrchových a koloidných soustav. 5 vyd. Praha: VŠCHT 2005; 244, 186–191.
3. Kim H-U., Lim K-H. A model on the temperature dependence of critical micelle concentration. Colloids and Surfaces A: Phys. Chem. Engin. Aspects, 2004; 235(1–3), 121–128.
4. Chen L-J., Lin S-Y., Huang C.C., Chen E. M. Temperature dependence of critical micelle concentration of polyoxyethylenated non - ionic surfactants. Colloids and Surfaces A: Phys. Chem. Engin. Aspects,1998; 135(1–3), 175–181.
5. Schramm L. L., Stasiuk E. N., Marangoni D. G. Surfactants and their applications. Annu. Rep. Prog. Chem., Sect. C, 2003; 99, 3–48.
6 http://pubchem.ncbi.nlm.nih.gov/summary/summary.cgi?sid= 162180433&loc=es_rss#x395[cit. 3.9.2013]
7. http://cameochemicals.noaa.gov/chemical/19856 [cit. 26.8.2013]
8. NTP Toxicology and Carcinogenesis Studies of Benzethonium Chloride (CAS No. 121-54-0) in F344/N Rats and B6C3F1 Mice (Dermal Studies). Natl Toxicol Program Tech Rep Ser. 1995; 438, 1–220.
http://www.ncbi.nlm.nih.gov/pubmed/12595925 [cit. 20.8.2013]
9. Kiselovičová M. Štúdium interakcií katiónového tenzidu s vybranými liečivami (lokálne anestetiká). Diplomová práca. Bratislava: Univerzita Komenského, Farmaceutická fakulta, 2012; 62.
Štítky
Farmácia Farmakológia
Článok vyšiel v časopiseČeská a slovenská farmacie

2013 Číslo 5-
Všetky články tohto čísla
-
Standardní receptura pro přípravu léčivých přípravků v lékárnách
VI. Sbírka Neues Rezeptur-Formularium* - Kombinace extraktu z grapefruitových semínek a koncentrované šťávy z klikvy velkoplodé jako potenciální protimikrobní konservans ke zvýšení mikrobiologické stability hypromelosového gelu
- Hodnotenie liberácie kofeínu z dermálnych polotuhých liekov
- Vplyv teploty a koncentrácie tenzidu na farmaceutickú dostupnosť liečiva
- Vnímání tělesné hmotnosti lékárníky a farmaceutickými laboranty na Slovensku I
- Vnímání tělesné hmotnosti lékárníky a farmaceutickými laboranty na Slovensku II
- Pracovní den u příležitosti životního jubilea prof. Jana Solicha a doc. Václava Ruska
- Prof. Ing. Milan Remko, DrSc. CChem FRSC – 65 ročný
-
Standardní receptura pro přípravu léčivých přípravků v lékárnách
- Česká a slovenská farmacie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle-
Standardní receptura pro přípravu léčivých přípravků v lékárnách
VI. Sbírka Neues Rezeptur-Formularium* - Kombinace extraktu z grapefruitových semínek a koncentrované šťávy z klikvy velkoplodé jako potenciální protimikrobní konservans ke zvýšení mikrobiologické stability hypromelosového gelu
- Vplyv teploty a koncentrácie tenzidu na farmaceutickú dostupnosť liečiva
- Prof. Ing. Milan Remko, DrSc. CChem FRSC – 65 ročný
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



