-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Dvouleté zkušenosti s intravitreální léčbou makulárního edému ranibizumabem u pacientů s okluzí retinální vény
Autori: Z. Hladíková; E. Klofáčová; B. Kalvodová
Pôsobisko autorov: Oční klinika, 1. lékařská fakulta, Univerzita Karlova a Všeobecná fakultní nemocnice v Praze, přednostka doc. MUDr. Jarmila Heissigerová, Ph. D., MBA
Vyšlo v časopise: Čes. a slov. Oftal., 73, 2017, No. 2, p. 43-51
Kategória: Původní práce
Výsledky byly prezentovány na 18. Vejdovského olomouckém vědeckém dnu 1. 4. 2017
Súhrn
Cíl:
Cílem této práce je prezentovat dvouleté zkušenosti s intravitreální léčbou makulárního edému (ME) ranibizumabem (anti VEGF A) v dávce 0,5 mg u pacientů s centrální (CRVO) a větvovou (BRVO) retinální venózní okluzí na Oční klinice Všeobecné fakultní nemocnice v Praze a 1. lékařské fakulty Univerzity Karlovy.Metodika:
Retrospektivní studie.Výsledky:
Dvouleté sledování ukončilo 18 pacientů s ME při CRVO a 16 pacientů s ME při BRVO. Průměrný věk při stanovení diagnózy byl u pacientů s ME při CRVO 63 let, průměrný interval mezi vznikem ME a zahájením léčby byl 3,6 měsíce. V průběhu prvního roku léčby dosáhli pacienti průměrného zisku 17,4 písmen Early Treatment of Diabetic Retinopathy Study (ETDRS) optotypu, tento výsledek se ve druhém roce léčby ještě mírně zlepšil (+2,4 písmene). Průměrný počet aplikací byl v prvním roce léčby 6,8 (medián 7, rozpětí 3–12), ve druhém roce léčby 3,6 (medián 2,5, rozpětí 0–10), celkem 10,2 injekcí (medián 10, rozpětí 3–20). U pacientů s ME při BRVO byl průměrný věk při stanovení diagnózy 68 let, průměrné trvání ME před zahájením léčby 6 měsíců, zisk písmen v prvním roce léčby 19,7 a zisk písmen ve druhém roce léčby 1 písmeno ETDRS optotypu. Průměrný počet aplikací byl v prvním roce léčby 7 (medián 7, rozpětí 3–12), ve druhém roce 3,2 (medián 2, rozpětí 0–10), celkem 9,6 (medián 8,5, rozpětí 3–22).Závěr:
Intravitreální léčbou ranibizumabem jsme u našich pacientů v prvním roce léčby dosáhli výrazného zlepšení nejlépe korigované zrakové ostrosti. Toto zlepšení se udrželo i během druhého roku léčby. V porovnání s výsledky klinických studií jsou naše výsledky ve skupině pacientů s ME při CRVO mírně lepší (ve studii CRUISE +13,9 písmen ETDRS optotypu, ve studii HORIZON -4,1 písmene), ve skupině pacientů s ME při BRVO jsou srovnatelné (ve studii BRAVO +18,3 písmen, ve studii HORIZON -0,7 písmene). V průběhu léčby jsme nezaznamenali žádné vážné oční ani celkové nežádoucí účinky.Klíčová slova:
Retinální venózní okluze, centrální retinální venózní okluze, větvová retinální venózní okluze, makulární edém, ranibizumab, dvouleté sledováníÚvod
1.1 Základní pojmy a dělení retinální venózní okluze
Retinální venózní okluze (RVO) je po diabetické retinopatii druhým nejčastějším cévním onemocněním sítnice (12). Z anatomického hlediska se dělí na větvovou retinální venózní okluzi (BRVO, z anglického Branch Retinal Vein Occlusion), centrální retinální venózní okluzi (CRVO) a hemiokluzi, při níž dochází k postižení jen horní či dolní poloviny sítnice. Hemiokluze je považována za variantu CRVO (hemi CRVO) (1).
1.2 Etiopatogeneze a klinické projevy
K obstrukci krevního toku vény dochází tvorbou trombu v jejím lumen, nejčastěji v místě útlaku ateroskleroticky změněnou arterií (20). U pacientů s CRVO k tomuto dochází v oblasti lamina cribrosa, u pacientů s BRVO pak v místě křížení vény s arterií, kde mají obě cévy společnou adventícii (19). Dalšími možnými příčinami mohou být zevní komprese jiné etiologie nebo onemocnění cévní stěny (např. u vaskulitid) (20).
1.3 Prevalence
V roce 2010 byla publikována rozsáhlá práce shrnující výsledky populačních studií z USA, Evropy, Asie a Austrálie. Jednalo o data celkem 68751 osob z 15 studií. Prevalence RVO v tomto souboru byla 5,2/1000, CRVO 0,8/1000 a BRVO 4,42/1000 (17).
1.4 Rizikové faktory
Při vzniku RVO mají velmi důležitou úlohu systémové rizikové faktory. Nejčastěji uváděným je vyšší věk (11, 13, 16, 17) a dále systémová onemocnění jako jsou arteriální hypertenze (11, 26), diabetes mellitus (DM), (11, 26), hyperlipidémie a hypercholesterolémie (6), stavy spojené s hyperviskozitou krve a poruchy koagulační kaskády, mezi které patří deficit proteinu C a S, antitrombinu, hyperprotrombenémie nebo Leidenská mutace (19). Z očních rizikových faktorů je pak nejčastěji uváděný glaukom s otevřeným úhlem (13, 26).
1.5 Prognóza
Významnými prognostickými faktory jsou vstupní zraková ostrost (22, 23) a stupeň prokrvení sítnice. U pacientů s ischemickou formou CRVO je prognóza výrazně horší než u pacientů s neischemickou formou.
1.6. Komplikace
Nejdůležitějšími komplikacemi RVO jsou vznik makulárního edému (ME) a ischemie sítnice vedoucí ke vzniku neovaskularizací (NV) předního (duhovky a komorového úhlu) a zadního (neovaskularizace terče zrakového nervu a sítnice) segmentu oka (20). Klíčovou úlohu při vzniku ME má zejména vysoký intrakapilární tlak a dále uvolňování řady angiogenních a zánětlivých faktorů, jako jsou vaskulární endotelový růstový faktor (VEGF) a interleukin 6 (IL6) (14, 18).
1.7. Léčba
1.7.1 Laserová koagulace sítnice
Zlatým standardem v léčbě byla dlouhá léta laserová koagulace sítnice. Central Vein Occluson Study Group (CVOS) neprokázala zlepšení nejlépe korigované zrakové ostrosti (NKZO) u pacientů s ME při CRVO ošetřených mřížkovou laserovou koagulací makuly a její provedení u těchto pacientů nedoporučuje (24). Tato skupina dále zkoumala vliv preventivního provedení panretinální fotokoagulace (PRF) sítnice na rozvoj NV předního segmentu oka a dospěla k závěru, že profylaktická PRF nezabrání u všech pacientů rozvoji NV duhovky a komorového úhlu. Provedení PRF tedy doporučuje až po objevení těchto NV (25).
Účinnost mřížkové laserové koagulace makuly u pacientů s ME při BRVO zkoumala Branch Vein Occlusion Study Group (BVOS). V roce 1984 publikovala tato skupina data, která ukázala, že v průběhu tří let získalo 65 % (28 ze 43) pacientů ošetřených mřížkovou laserovou koagulací makuly 2 a více řádků NKZO v porovnání s pouze 37 % (13 z 35) pacientů ve skupině, která byla pouze sledována (22).
1.8. Medikamentózní léčba – intravitreální preparáty
Zavedení intravitreálních preparátů do léčby ME při RVO výrazně zlepšilo prognózu tohoto onemocnění.
1.8.1. Kortikosteroidy
Ze skupiny kortikosteroidů je v současné době používán biodegradabilní implantát s dexamethasonem v dávce 0,7 mg (Ozurdex, Allergan). Účinnost a bezpečnost použití tohoto implantátu u pacientů s ME při CRVO a BRVO zkoumala studie GENEVA (7). Hlavními nežádoucími účinky jsou vzestup nitroočního tlaku (NOT) a progrese katarakty (u 29,8 % fakických očí po dvou aplikacích biodegradabilního implantátu s dexamethasonem v dávce 0,7 mg).
Použití tohoto preparátu v České republice limituje omezení úhrady na pouze 2 biodegradabilní implantáty s dexamethasonem 0,7 mg do každého oka na jednu epizodu ME při RVO (10). Toto množství není pro řadu pacienty dostačující (21).
1.8.2 Ranibizumab
Ranibizumab (Lucentis, Novartis) je fragment humanizované monoklonální protilátky, který selektivně váže a neutralizuje všechny isoformy VEGF-A. Používá se v dávkování 0,5mg/0,05ml v jedné intravitreální injekci, interval mezi jednotlivými aplikacemi by neměl být kratší než 4 týdny. Účinnost a bezpečnost ranibizumabu v prvním roce léčby ME u CRVO sledovala studie CRUISE (3), u BRVO studie BRAVO (2). Na tyto studie dále navázaly studie HORIZON (2. rok léčby) (8) a RETAIN s průměrnou sledovací dobou 49 měsíců (4). Pro praxi nepříznivým zjištěním studie RETAIN bylo, že pouze u 44 % (14 z 32) pacientů s ME při CRVO (z toho u 71 % v průběhu dvou let léčby) a u 50 % pacientů (17 ze 34) s ME u BRVO (z toho u 76 % v průběhu dvou let léčby) se ME v průběhu sledování trvale resorboval. Perzistence ME byla v obou skupinách spojena s horší výslednou zrakovou ostrostí.
1.8.3 Aflibercept
Aflibercept (Eylea, Bayer) je fúzní protein skládající se z fragmentů extracelulárních domén humánního VEGF receptoru 1 a 2 fúzovaných na Fc fragment humánního IgG1. Aflibercept váže VEGF A, VEGF B a placentární růstový faktor. V léčbě ME při CRVO se používá intravitreálně v dávce 2 mg/0,05 ml, interval mezi dvěma dávkami nemá být kratší než jeden měsíc.
Účinnost a bezpečnost intravitreálně podávaného afliberceptu v léčbě ME při CRVO hodnotily dvě studie – COPERNICUS (v USA, Kanadě, Kolumbii, Indii a Izraeli) a GALILEO (v Evropě a jihovýchodní Asii) (9, 15). Účinnost intravitreálně podávaného afliberceptu v porovnání s mřížkovou laserovou koagulací makuly u pacientů s ME při BRVO zkoumala studie VIBRANT (5).
Cílem této práce je retrospektivní zhodnocení výsledků dvouleté intravitreální léčby ranibizumabem v dávce 0,5 mg u pacientů s ME při CRVO a BRVO na Oční klinice Všeobecné fakultní nemocnice v Praze a 1. lékařské fakulty Univerzity Karlovy.
Metodika
Data pacientů byla získána z lékařské dokumentace naší kliniky. U pacientů jsme sledovali věk při stanovení diagnózy ME při RVO, pohlaví, přítomnost rizikových faktorů, interval mezi vznikem ME a zahájením léčby, typ RVO, stav prokrvení sítnice podle fluorescenční angiografie (FAG), přítomnost NV předního a zadního segmentu oka při zahájení a v průběhu léčby, vstupní NKZO a centrální tloušťku sítnice (CRT) a jejich vývoj v průběhu léčby a počet aplikací ranibizumabu. NKZO byla vyšetřována na ETDRS optotypech.
Léčba byla zahájena u pacientů splňujících omezení úhrady přípravku. Tedy těch, u kterých se NKZO zhoršila vlivem ME při RVO, změny v makule nebyly ireverzibilního charakteru a byly refrakterní na laserovou léčbu, NKZO se pohybovala mezi 6/120 a 6/12, CRT byla > 250 µm a doba trvání ME byla ≤ 12 měsíců. U všech pacientů jsme před zahájením léčby vyžadovali kompenzaci celkového stavu (zejména DM, arteriální hypertenze, dyslipidémie a dále) praktickým lékařem či internistou. Vylučujícím kritériem byl infarkt myokardu (IM), či cévní mozková příhoda (CMP) v posledních 3 měsících. Podmínkou zahájení léčby byl dále kompenzovaný NOT. U každého pacienta bylo léčeno vždy jen jedno oko.
Léčba byla zahájena aplikacemi ranibizumabu intravitreálně každé 4 týdny do dosažení stabilizace, tj. stabilní NKZO a CRT při třech po sobě jdoucích návštěvách. Poté byli pacienti v intervalu 4 týdnů pouze sledováni. U pacientů, u kterých bylo dosaženo dlouhodobě stabilních výsledků, se dále intervaly kontrol individuálně prodlužovaly. Pro účely zhodnocení výsledků byly v těchto případech použity hodnoty z předchozí kontroly. Aplikace byly znovu zahájeny, pokud se zhoršila NZKO a/nebo jsme zaznamenali nárůst CRT, tedy při relapsu ME. V těchto případech jsme opět aplikovali v intervalu 4 týdnů do dosažení stabilizace. Při každé kontrole nezávisle na tom, zda byla či nebyla indikována aplikace, bylo provedeno měření NOT bezkontaktním tonometrem, vyšetření NKZO, biomikroskopické vyšetření předního segmentu, vyšetření zadního segmentu v arteficiální mydriáze a optická koherenční tomografie (OCT) přístrojem Spectralis firmy Heidelberg Engineering. U všech pacientů byla v průběhu prvních tří měsíců léčby provedena FAG. Toho vyšetření jsme po roce opakovali. Podle FAG jsme provedli laserové ošetření oblastí neperfuze a prosakování, u pacientů s ME při BRVO jsme provedli fokální nebo mřížkovou laserovou koagulaci makuly.
Výsledky
4.1 CRVO
Dvouleté sledování dokončilo celkem 18 pacientů (11 mužů a 7 žen) léčených ranibizumabem. Průměrný věk pacientů při stanovaní diagnózy ME byl 63 let (23–81). Nejčastěji se vyskytujícím systémovým rizikovým faktorem byla arteriální hypertenze přítomná u 13 z 18 (72 %) pacientů, následovala dyslipidémie (u 7 z 18, 39 %) a DM (u 6 z 18, 33 %). Jeden pacient trpěl chronickou fibrilací síní, u žádného pacienta nebyla diagnostikována trombofilní mutace. Poměrně vysoký byl mezi našimi pacienty výskyt glaukomu s otevřeným úhlem a to u 9 z 18 (50 %) pacientů. Průměrný interval mezi vznikem ME a zahájením léčby byl 3,6 měsíce (medián 2,5 měsíce, rozpětí 1–11). Na základě FAG provedené v průběhu prvních tří měsíců jsme CRVO u třech pacientů hodnotili jako ischemickou. U dvou z nich jsme pro přítomnost NV provedli PRF, u zbývajícího pacienta bylo provedeno pouze cílené ošetření oblastí neperfuze dle FAG. U jednoho pacienta došlo ke konverzi z neischemické na ischemickou formu CRVO během prvního roku léčby, pro rozvoj NV sítnice jsme provedli PRF. U zbylých 14 pacientů jsme CRVO hodnotili jako neischemickou. Průměrná vstupní NKZO byla 49,9 písmen ETDRS optotypu, průměrná vstupní CRT byla 690 µm. Po prvním roce léčby stoupla průměrná NKZO na 67,3 písmen ETDRS optotypu (+17,4 písmen) a CRT poklesla na 340 µm (-350 µm). Po druhém roce léčby se průměrná NKZO zlepšila na 69,7 písmen ETDRS optotypu (+19,8 písmen od vstupní hodnoty, +2,4 za druhý rok léčby) a průměrná CRT byla 354 µm (-336 µm od začátku léčby, +14 µm za druhý rok). Dvanáct pacientů z 18 (67 %) získalo ≥ 15 písmen ETRDS optotypu, žádný z našich pacientů neztratil ≥ 15 písmen ETDRS optotypu – nejhorší výsledek byl -10 písmen. U 9 pacientů (50 %) došlo během léčby k úplné regresi ME, tzn. tito pacienti byli bez známek ME na OCT snímcích 6 a více měsíců před ukončením dvouletého sledování.
Během dvou let jsme pacientům průměrně aplikovali 10,2 injekcí (medián 10, celkem 3-20), z toho průměrně 6,8 v prvním roce léčby (medián 7, celkem 3-12) a 3,6 (medián 2,5, celkem 0-10) ve druhém roce. NV předního a zadního segmentu byly na začátku léčby přítomny u dvou pacientů, u jednoho pacienta se v průběhu léčby objevily NV sítnice. U všech tří pacientů NV regredovaly po provedení PRF a intravitreální terapii ME ranibizumabem. V průběhu léčby jsme nezaznamenali žádné závažné oční či celkové nežádoucí účinky.
Obr. 1. Pacient – muž, r. 1965, vstupní NKZO byla 60 písmen ETDRS optotypu, CRT 699 μm. 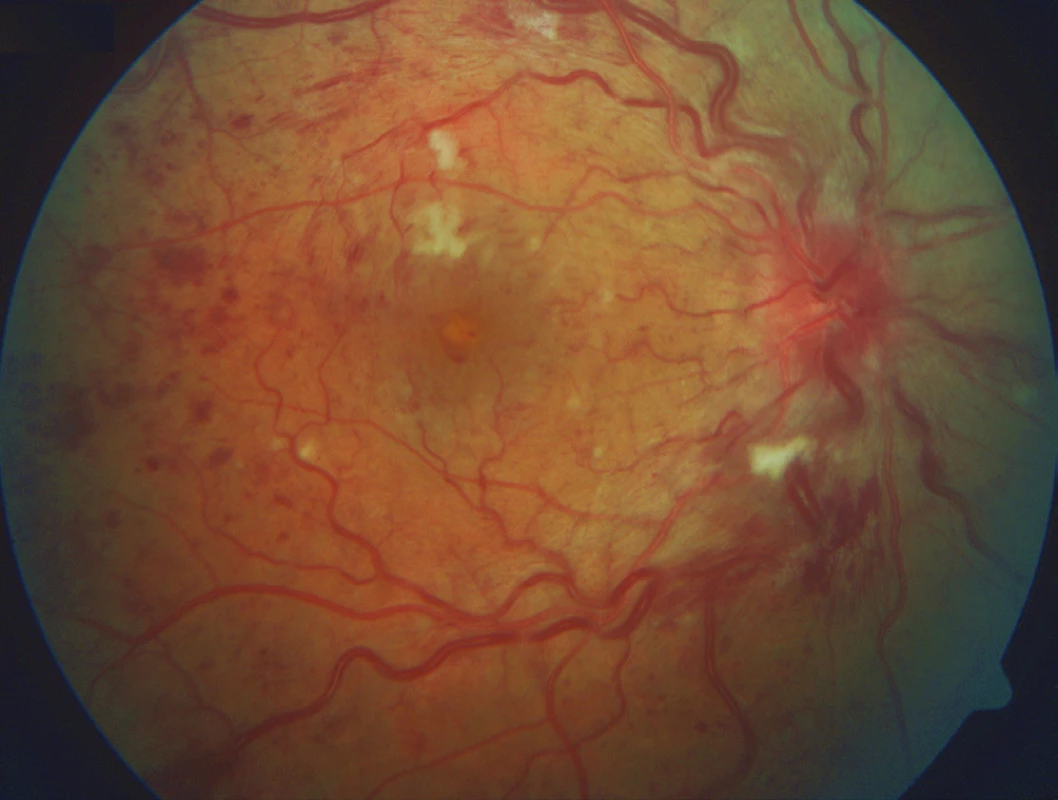
Stav před zahájením léčby – CRVO s edémem a překrvením terče zrakového nervu, dilatací a tortuozitou sítnicových vén, přítomností plaménkových a kaňkovitých retinálních hemorhagií, měkkých exsudátů a makulárním edémem Obr. 2. OCT snímek před zahájením léčby – přítomnost cystoidního makulárního edému 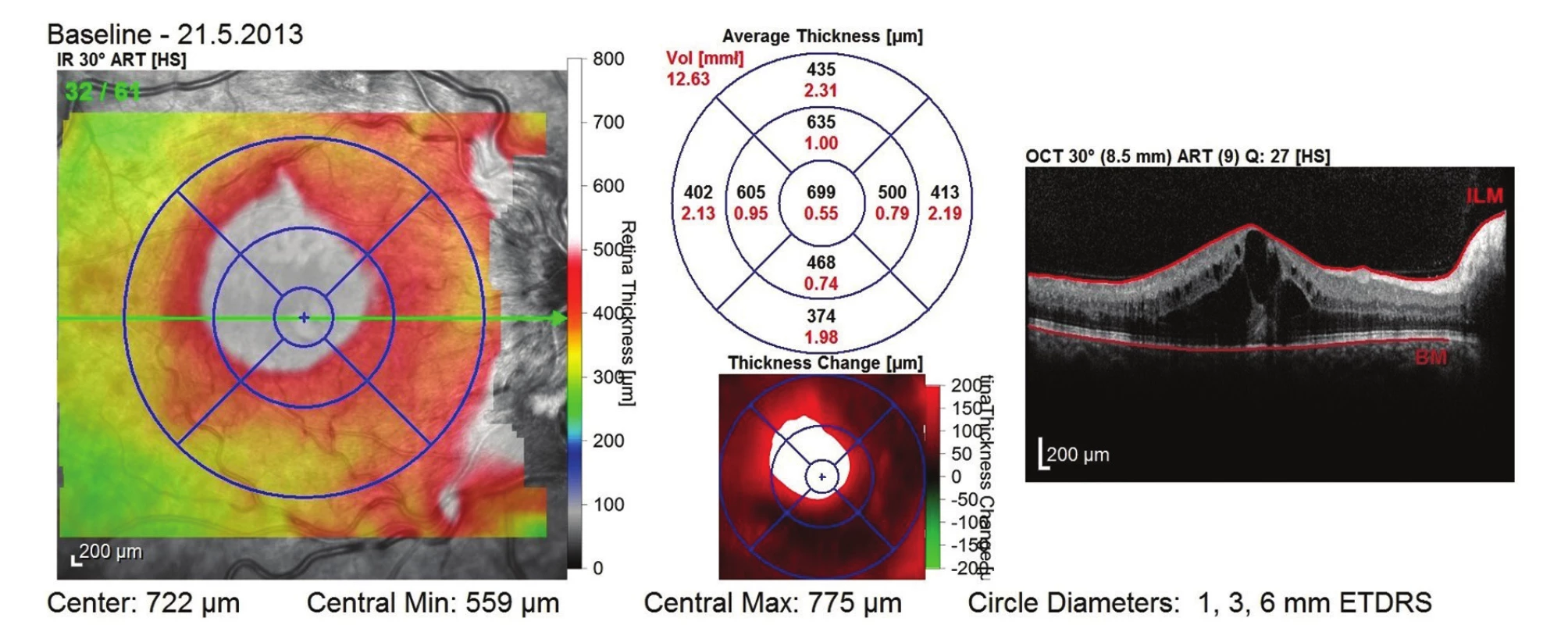
Obr. 3. Stav po 1. roce léčby – přetrvává mírné překrvení terče zrakového nervu a dilatované, tortuózní vény, došlo k významnému ústupu retinálních hemorhagií, měkkých exsudátů i ME 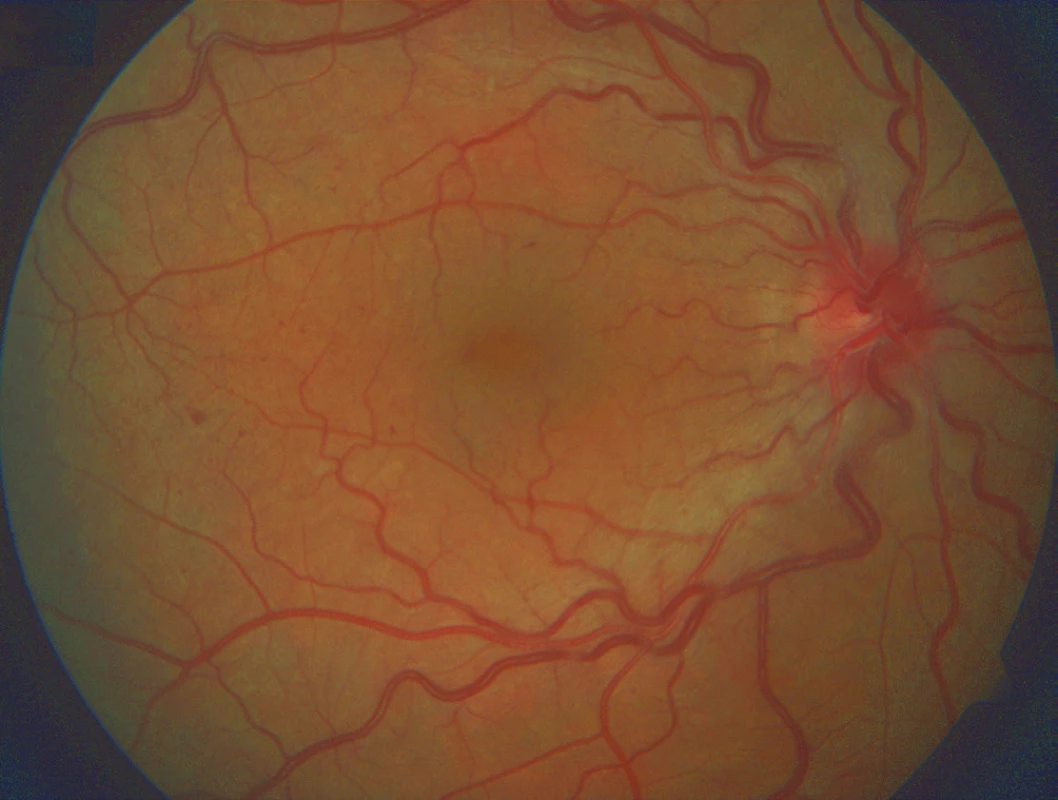
Obr. 4. FAG po 1. roce léčby prokazuje prosakování barviva z dilatovaných kapilár zejména v horním temporálním kvadrantu v oblasti zadního pólu 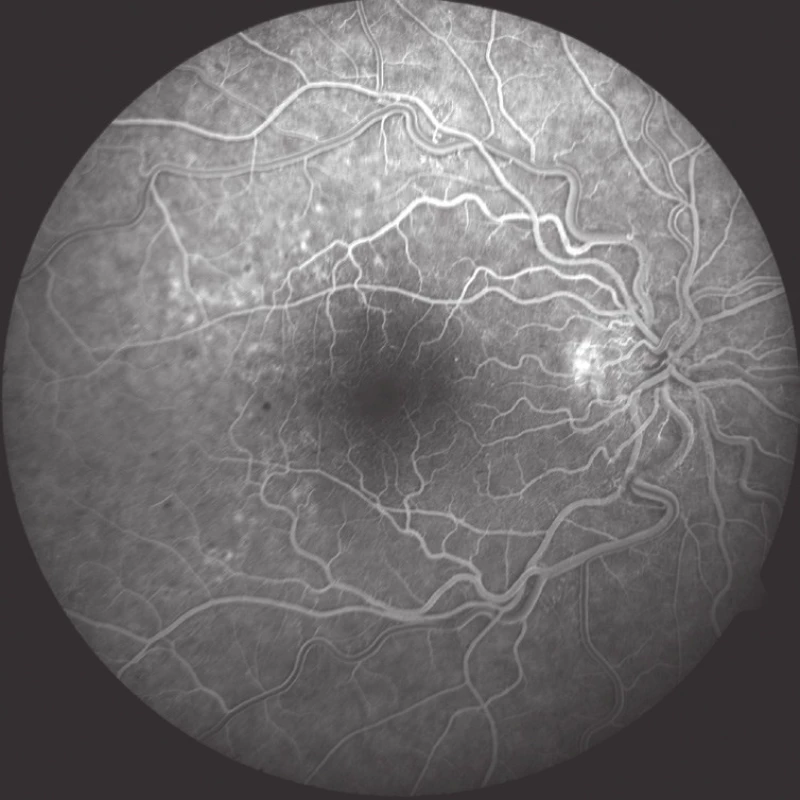
Obr. 5. OCT snímek po 1. roce léčby (celkem 5 aplikací) – regrese ME, dobrá morfologie zevních vrstev neuroretiny, CRT 302 μm a NKZO 81 písmen ETDRS optotypu 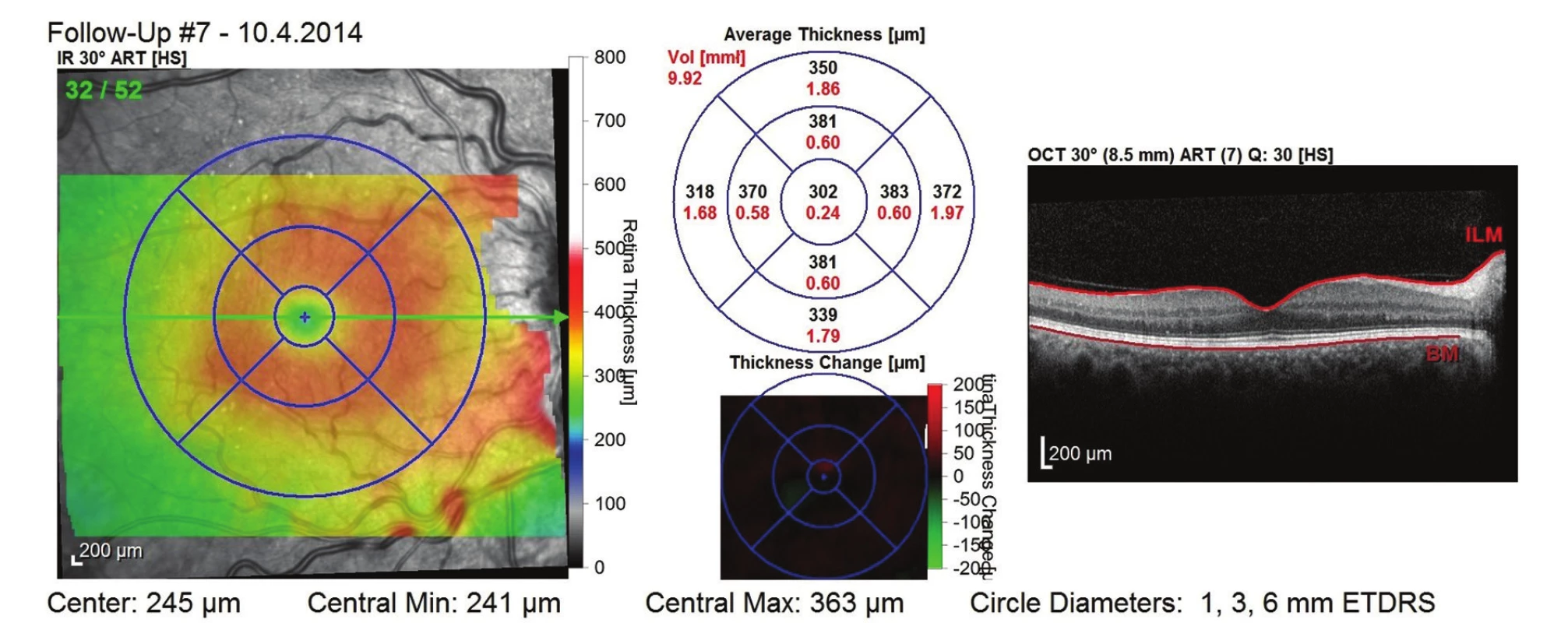
Obr. 6. OCT snímek po dvou letech – i bez aplikací během 2. roku léčby přetrvává stabilní nález bez známek ME s dobrou morfologií zevních vrstev neuroretiny, CRT 288 μm a NKZO 85 písmen ETDRS optotypu 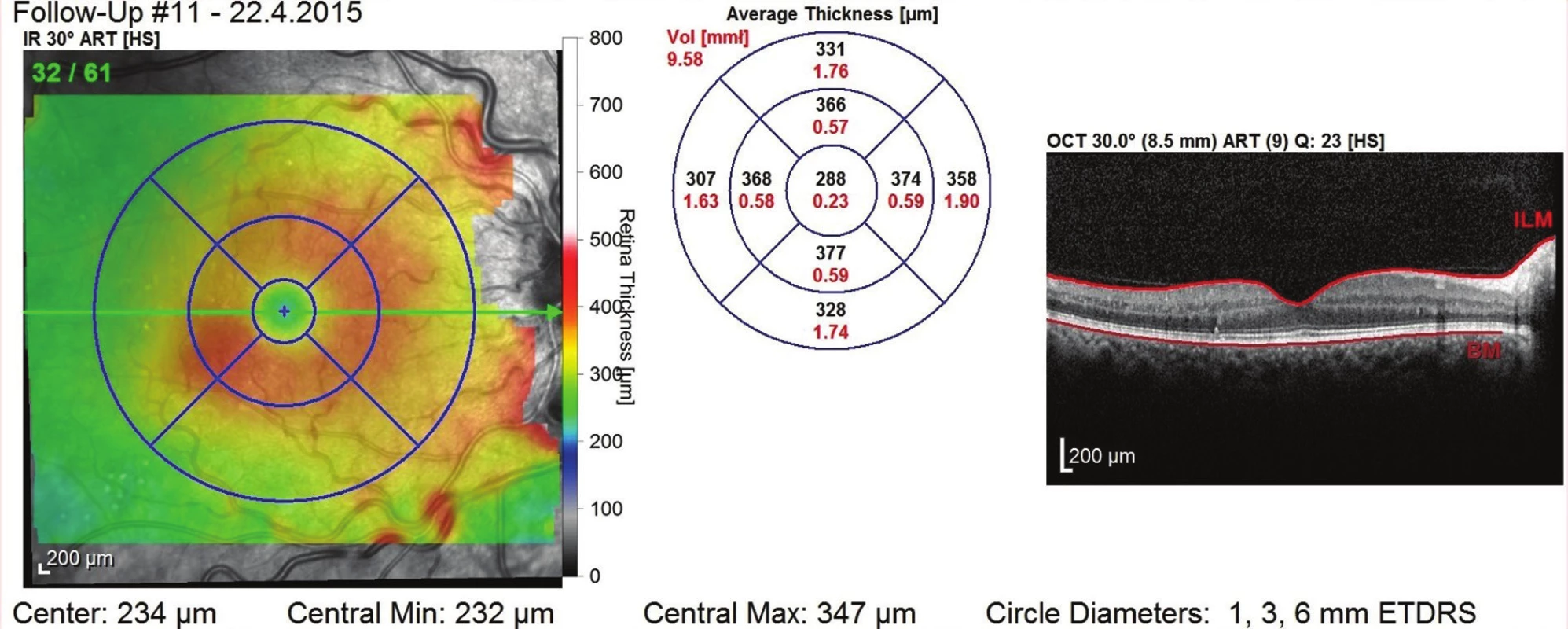
4.2 BRVO
Dvouleté sledování dokončilo celkem 16 pacientů – 11 mužů a 5 žen. Průměrný věk pacientů při stanovaní diagnózy ME byl 68 let (43–85). Nejčastěji se vyskytujícím systémovým rizikovým faktorem byla arteriální hypertenze přítomná u 14 ze 16 (88 %) pacientů, následovala dyslipidémie (u 7 ze 16, 44 %) a DM (u 4 ze 16, 25 %). Dva pacienti prodělali před lety CMP, jeden IM. U jedné pacientky byla během interního vyšetření před zahájením léčby ranibizumabem diagnostikována trombofilní mutace, a to mutace faktoru II (protrombin) v heterozygotní formě. Výskyt glaukomu s otevřeným úhlem byl nižší než u pacientů s CRVO – pouze u 3 ze 16 (19 %) pacientů. Průměr i medián intervalu mezi vznikem ME a zahájením léčby byl 6 měsíců (2 týdny až 11 měsíců). Průměrná vstupní NKZO byla 51,4 písmen ETDRS optotypu a průměrná vstupní CRT 588 µm. Po prvním roce léčby stoupla průměrná NKZO na 70,1 písmen ETDRS optotypu (+18,7 písmen) a CRT klesla na 331 µm (-257 µm). Po druhém roce léčby byla průměrná NKZO 71,1 písmen ETDRS optotypu (+19,7 oproti vstupní hodnotě, + 1 za druhý rok léčby) a průměrná CRT 296 µm (-292 µm oproti začátku léčby, -35 µm za druhý rok). Deset pacientů ze 16 (63 %) získalo ≥ 15 písmen ETRDS optotypu, žádný z našich pacientů neztratil ≥ 15 písmen ETDRS optotypu – nejhorší výsledek byl 0 písmen. U 7 pacientů (44 %) došlo během léčby k úplné regresi ME, tzn. tito pacienti byli bez známek ME na OCT snímcích 6 a více měsíců před ukončením dvouletého sledování. V případě jedné pacientky z této skupiny se nicméně jednalo o atrofii makuly (CRT 119 um, již po 3 úvodních aplikacích) s neuspokojivou zrakovou ostrostí.
Obr. 7. Pacient – muž, r. 1950, vstupní NKZO 62 písmen ETDRS optotypu a CRT 603 μm 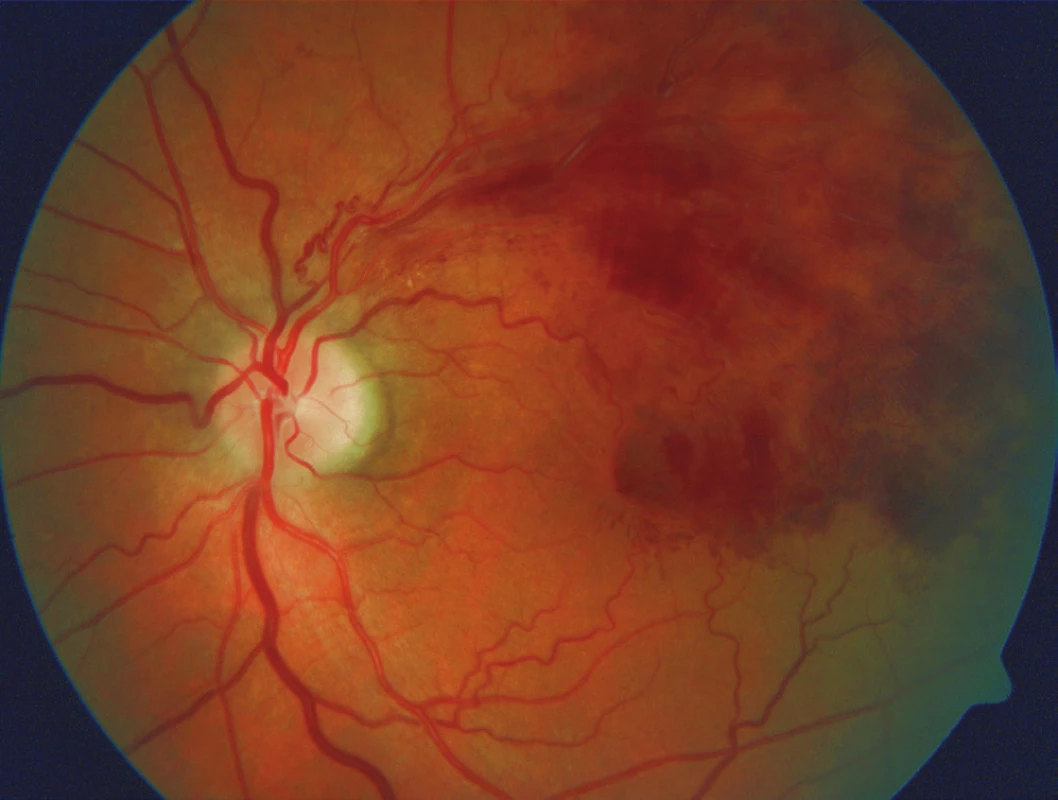
Obr. 8. OCT snímek před zahájením léčby – přítomnost cystoidního makulárního edému 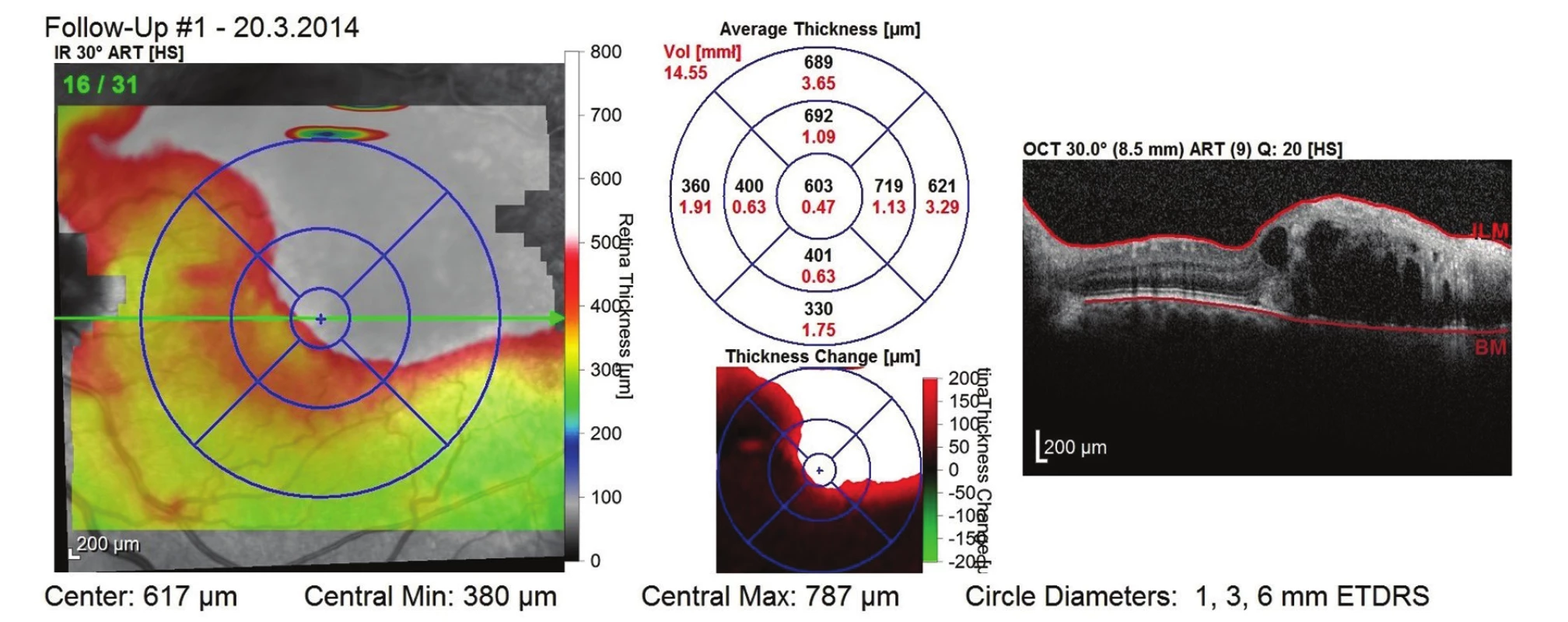
Obr. 9. Stav po 1. roce léčby, došlo k významnému ústupu hemorhagií a ME, je patrná přítomnost kolaterál v postižené oblasti 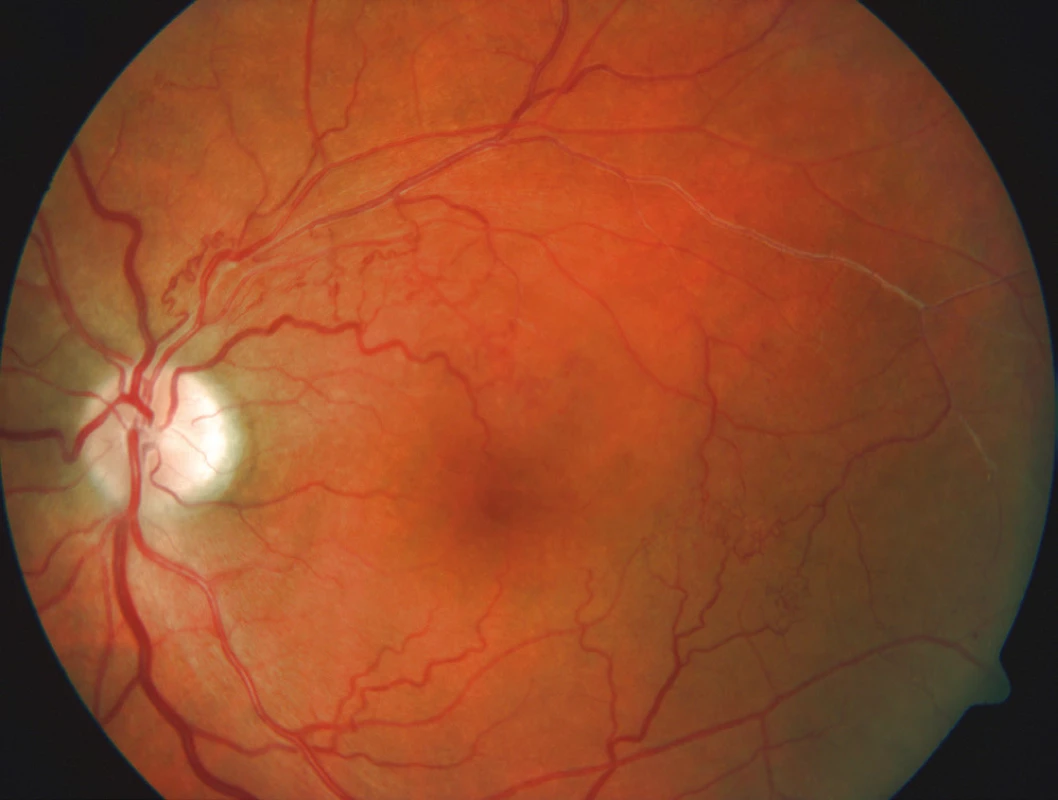
Obr. 10. FAG po 1. roce léčby – v arteriovenózní fázi je patrné opožděné plnění vény periferně od uzávěru a přítomnost kolaterál 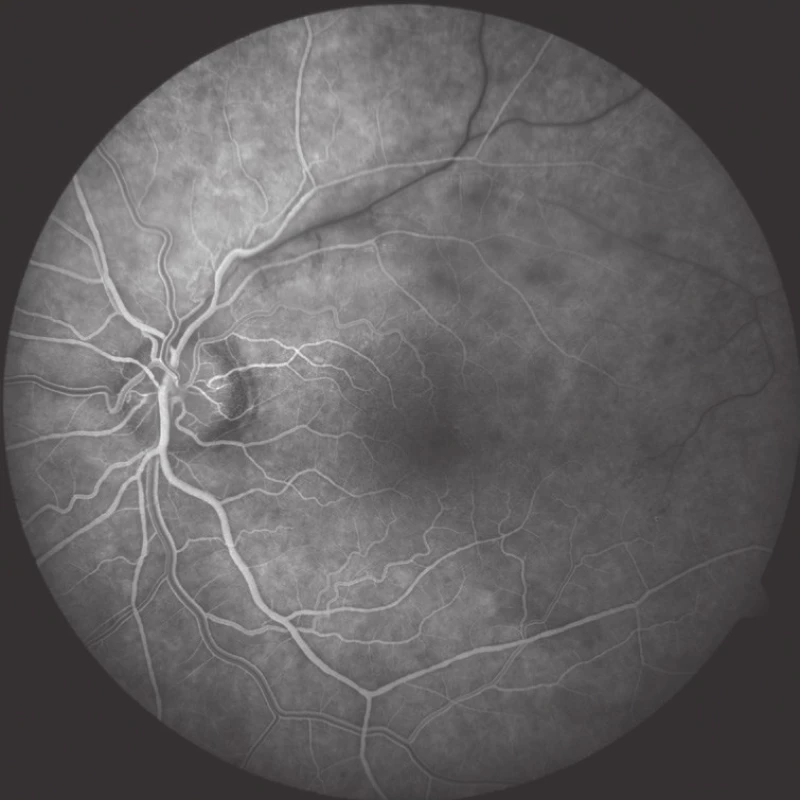
Obr. 11. OCT snímek po 1. roce léčby (9 aplikací) – bez známek ME, mírná desorganizace zevních vrstev neuroretiny, CRT 281 μm a NKZO 85 písmen ETDRS optotypu 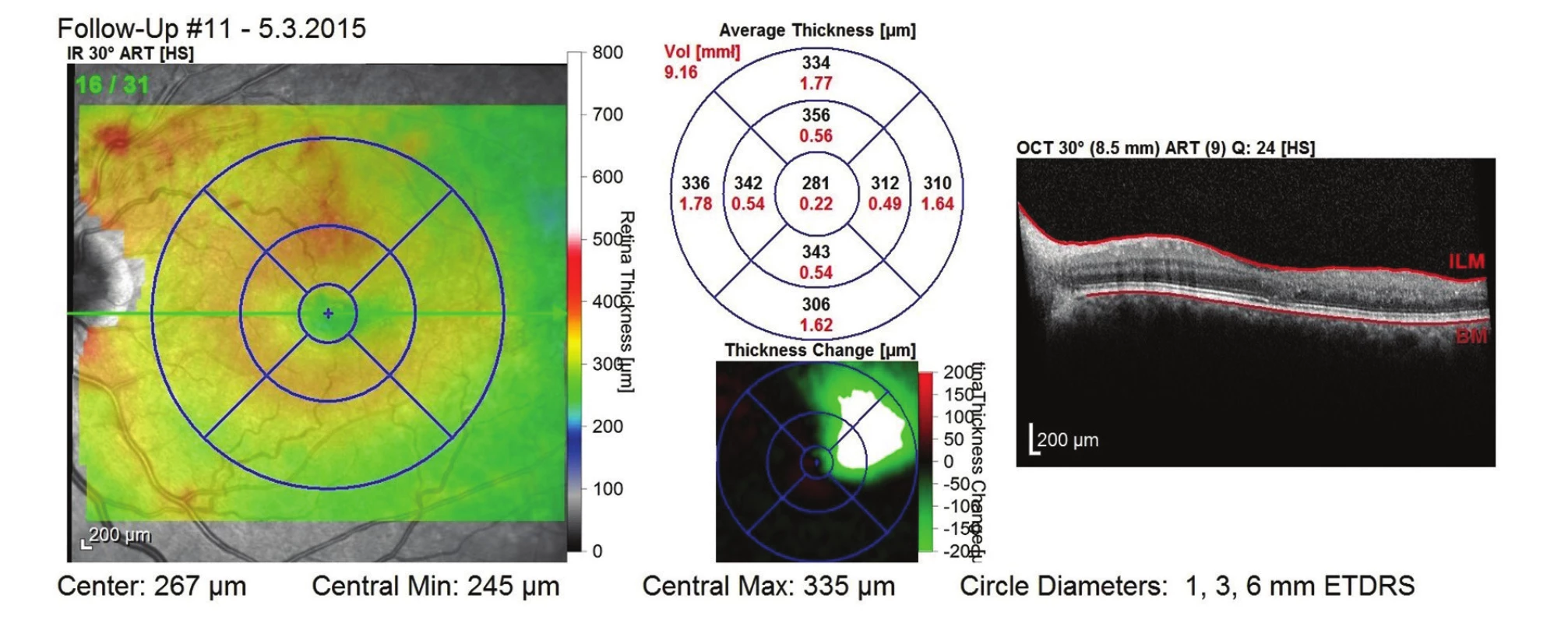
Obr. 12. OCT snímek po dvou letech léčby (během 2. roku léčby bylo podáno 6 aplikací) – bez známek ME, mírná desorganizace zevních vrstev neuroretiny, CTR 255 μm a NKZO 80 písmen ETDRS optotypu 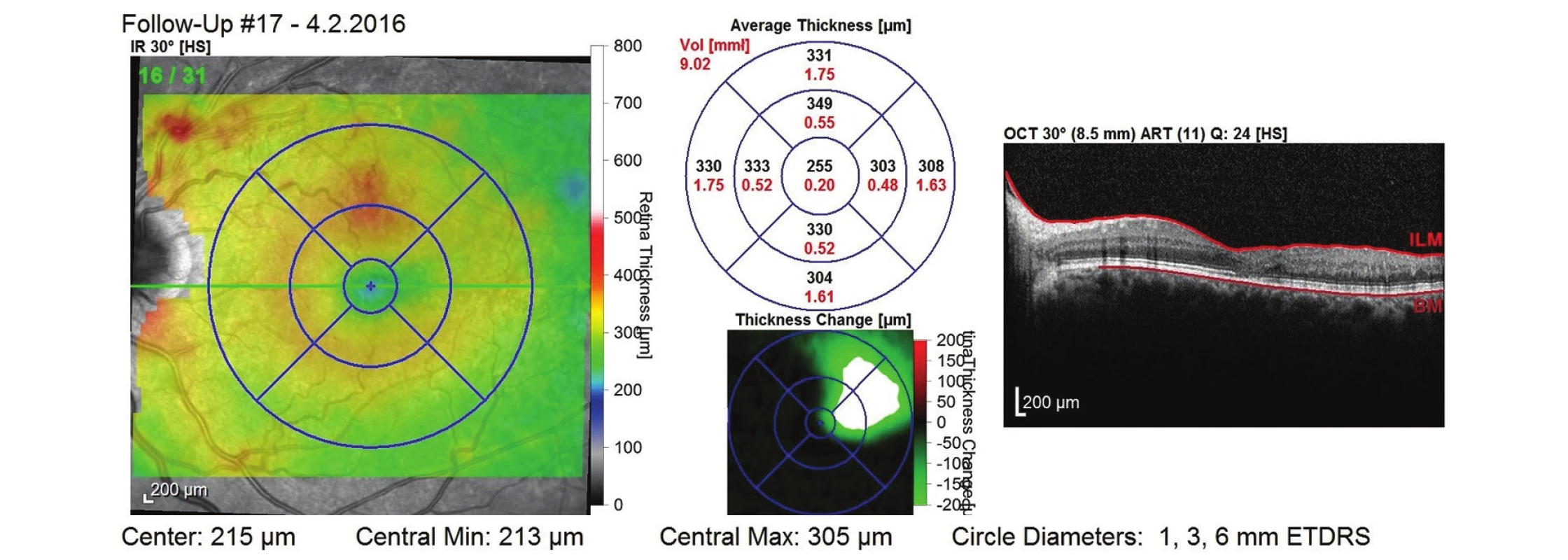
Za dva roky léčby bylo průměrně podáno 9,6 injekcí (medián 8,5, celkem 3–22), z toho v průběhu prvního roku průměrně 7 (medián 7, celkem 3–12) a v průběhu druhého roku průměrně 3,2 (medián 2, celkem 0–10). V průběhu léčby jsme, obdobně jako u pacientů s ME při CRVO, nezaznamenali žádné závažné oční či systémové nežádoucí účinky. U žádného pacienta se v průběhu léčby neobjevily NV.
Diskuse
AntiVEGF terapie je v současné době metodou první volby u pacientů s ME při RVO. Její zavedení do klinické praxe vedlo k výraznému zlepšení prognózy tohoto onemocnění. V našem souboru pacientů s ME při RVO jsme měli v úmyslu ověřit bezpečnost a účinnost intravitreální léčby ranibizumabem a porovnat naše výsledky s výsledky mezinárodních klinických studií.
Ačkoliv je náš soubor poměrně malý, svým složením odpovídá souborům uvedených studií. Shodně s těmito studiemi byl průměrný věk našich pacientů více než 60 let – ve skupině CRVO 63 let (rozptyl 23–81) ve srovnání s 68 lety ve studii CRUISE (20–91 let) (3), ve skupině BRVO pak 68 let (43–85) ve srovnání s 66 lety ve studii BRAVO (26–91) (2).
I v našem souboru se potvrdila mírná převaha postižení mužů – 61 % (11 z 18) ve skupině CRVO ve srovnání 57 % ve studii CRUISE (3) a 69 % (11 ze 16) ve skupině BRVO ve srovnání s 53 % ve studii BRAVO (2).
Ve spolupráci s ambulantními oftalmology a diagnostickými centry se ve skupině CRVO podařilo dosáhnout stejně včasného zahájení léčby, jakého bylo dosaženo ve studii CRUISE – průměrný interval mezi vznikem ME a zahájením léčby byl u našich pacientů 3,6 měsíce, medián 2,5 měsíce, ve studii 3,3 měsíce, medián 2 měsíce (3). Ve skupině pacientů s ME při BRVO byla léčba v našem souboru zahájena o něco později – průměr i medián intervalu mezi vznikem ME a zahájením léčby byl 6 měsíců oproti průměru 3,5 a mediánu 2 měsíce ve studii BRAVO (2). Pozdější zahájení léčby u pacientů s ME při BRVO si vysvětlujeme tím, že pokles NKZO v této skupině může být pozvolnější, a tudíž si ho pacienti při binokulárním vidění mohou uvědomit později.
Vstupní funkční a anatomické parametry našich pacientů byly rovněž velmi podobné těm v porovnávaných studiích – průměrná vstupní NKZO byla v našem souboru ve skupině pacientů s CRVO 49,9 písmen ETRDS optotypu a průměrná vstupní CRT byla 690 µm, ve studii CRUISE 48,3 písmen a 685 µm (3). Ve skupině pacientů s ME při BRVO byla průměrná vstupní NKZO 51,4 písmen ETRDS optotypu a průměrná vstupní CRT 588 µm, ve studii BRAVO 54,6 písmen a 521 µm (2).
Ve skupině pacientů s ME při BRVO jsme dosáhli obdobných funkčních výsledků, jakých bylo dosaženo v porovnávaných klinických studiích (2, 8). Ve skupině pacientů s ME při CRVO jsou naše výsledky mírně lepší (3). Na konci prvního roku léčby byl ve skupině pacientů s ME při CRVO průměrný zisk 17,4 písmen ETDRS optotypu a CRT poklesla o 350 µm při průměrně 6,8 injekcích na pacienta. Ve studii CRUISE dosáhli pacienti zlepšení 13,9 písmen ETDRS optotypu a poklesu 462 µm při 8,8 injekcích (3). Lepší anatomický efekt dosažený ve studii CRUISE připisujeme vyššímu počtu injekcí podaných v prvním roce léčby a zejména měsíčnímu dávkování v prvních 6 měsících. Výsledky za druhý rok léčby byly v našem souboru zisk 2,4 písmen ETDRS optotypu a vzrůst CRT o 14 µm při průměrně 3,6 injekcích, v porovnání se studií HORIZON, kde se na konci druhého roku léčby NKZO zhoršila o 4,1 písmen ETDRS optotypu a CRT vzrostla o 68,4 µm při 3,5 injekcích (8). Předpokládáme, že lepší výsledky našich pacientů v průběhu druhého roku léčby mohou být způsobeny jak malou velikostí souboru, tak také tím, že část pacientů jsme pro nedostatečnou odpověď na léčbu či tachyfylaxi ještě před dokončením dvou let sledování převedli na jinou léčbu a nejsou tedy v tomto souboru zahrnuti.
Výsledky ve skupině pacientů s ME při BRVO byly za první rok léčby +18,7 písmen a -257 µm při průměrně 7 injekcích na pacienta ve srovnání s +18,3 písmeny a -347 µm při průměrně 8,4 injekcích ve studii BRAVO (2), ve 2. roce léčby pak +1 písmeno a -35 µm při 3,2 injekcích ve srovnání s -0,7 písmene a +35,3 µm při 2,1 injekcích ve studii HORIZON (8). Horší anatomický výsledek našich pacientů v prvním roce, a naopak mírně lepší v roce druhém opět připisujeme rozdílu v počtu podaných injekcí.
Shodně s výsledky klinických studií i v našem souboru se ukázalo, že počáteční výrazné zlepšení NKZO a pokles CRT dosažené při častých aplikacích v průběhu prvního roku, lze u většiny pacientů udržet i při snížení počtu aplikací při přechodu do režimu PRN nebo Treat and Extend v dalším sledování. Na druhou stranu je ale zřejmé, že časté aplikace ranibizumabu sice eliminují vliv VEGF-A a způsobí pokles ME, ale nevedou k potlačení jeho produkce a někteří pacienti tedy k udržení dobrých funkčních výsledků vyžadují krátký interval mezi aplikacemi – shodně v obou skupinách pacientů byl nejvyšší počet aplikací v prvním roce 12 (rozptyl 3–12) a ve druhém 10 (rozptyl 0–10).
Výsledný funkční výsledek není závislý jen na míře ústupu ME, zásadní význam má i stupeň ischemie makuly a změny morfologie zevních vrstev neuroretiny. I v našem souboru tedy byli pacienti, u kterých byla i přes vymizení ME výsledná NZKO pro výše popsané změny neuspokojivá.
V klinických studiích s anti-VEGF preparáty, ať již se jedná o studie s ranibizumabem, či afliberceptem, bývá na porovnání výsledků skupin léčených a skupin dostávajících zpočátku pouze placebo zdůrazňována nutnost včasného zahájení léčby anti-VEGF pro dosažení maximálního funkčního efektu. V našem souboru, vzhledem k jeho velikosti, nebylo bohužel srovnání pacientů, u nichž byla léčba zahájená časně, s pacienty, u nichž byla léčba zahájená později, možné provést. Klinická praxe nás však vede ke stejnému názoru.
Závěr
Výsledky našeho souboru potvrzují účinnost a bezpečnost intravitreální léčby ranibizumabem u pacientů s ME při RVO. Více než 15 písmen ETRDS optotypu získalo 12 z celkem 18 (67 %) pacientů s ME při CRVO a 10 ze 16 (63 %) pacientů s ME při BRVO. Žádný z našich pacientů neztratil za 2 roky sledování ≥ 15 písmen ETDRS optotypu. Tyto výsledky odpovídají výsledkům publikovaných klinických studií (2, 3, 8) a ukazují jejich použitelnost v běžné praxi.
Terapie anti-VEGF preparáty je pro pacienty s ME při RVO nesporným přínosem. K jejím nevýhodám však patří nutnost častých kontrol, nejlépe v měsíčních intervalech, které jsou zatěžující jak pro pacienty, tak také pro aplikační centra a dále fakt, že dle výsledků studie RETAIN (4) vyžaduje prakticky polovina pacientů dlouhodobou léčbu.
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmu a není podpořeno žádnou farmaceutickou firmou.
Do redakce doručeno dne 23. 3. 2017
Do tisku přijato dne 6. 6. 2017
MUDr. Zuzana Hladíková
Oční klinika, 1. LF UK a VFN v Praze
U Nemocnice 2
128 08 Praha 2
e-mail: zuzana.hladikova@vfn.cz
Zdroje
1. Bowling, B.: Kanski´s Clinical Ophthalmology: A Systemic Approach, Eighth edition, Edinburgh, Elsevier, 2016, p. 539–44.
2. Brown, D.M., Campochiaro, P.A., Bhisitkul, R.B. et al.: Sustained Benefits from Ranibizumab for Macular Edema Following Branch Retinal Vein Occlusion: 12-Month Outcomes of a Phase III Study. Ophthalmology, 118, 2011 : 1594–1602.
3. Campochiaro, P.A., Brown, D.M., Awh C.C. et al.: Sustained Benefits from Ranibizumab for Macular Edema following Central Retinal Vein Occlusion: Twelve-Month Outcomes of a Phase III Study. Ophthalmology, 118, 2011 : 2041–49.
4. Campochiaro, P.A, Sophie, R., Pearlman, J. et al.: Long-term Outcomes in Patients with Retinal Vein Occlusion Treated with Ranibizumab The RETAIN Study. Ophthalmology, 121, 2014 : 209–19.
5. Clark, W.L., Boyer, D.S., Heier, J.S. et al.: Intravitreal Aflibercept for Macular Edema Following Branch Retinal Vein Occlusion 52-Week Results of the VIBRANT Study. Ophthalmology, 123, 2016 : 330–36.
6. Dodson, P.M., Galton, D.J., Hamilton, A.M. et al.: Retinal vein occlusion and the prevalence of lipoprotein abnormalities. Br J Ophthalmol, 66, 1982 : 161–64.
7. Haller, J.A., Bandello, F., Belfort, R. Jr. et al.: Dexamethasone Intravitreal Implant in Patients with Macular Edema Related to Branch or Central Retinal Vein Occlusion Twelve-Month Study Results. Ophthalmology, 118, 2011 : 2453–2460.
8. Heier, J.S., Campochiaro, P.A., Yau, L. et al.: Ranibizumab for Macular Edema Due to Retinal Vein Occlusions Long-term Follow-up in the HORIZON Trial. Ophthalmology, 119, 2012 : 802–809.
9. Heier, J.S., Clark, W.L., Boyer, D.S. et al.: Intravitreal Aflibercept Injection for Macular Edema Due to Central Retinal Vein Occlusion: Two-Year Results from the COPERNICUS Study. Ophthalmology, 121, 2014 : 1414–1420.
10. http://www.sukl.cz/modules/medication/detail.php?code=0167756&tab=prices
11. Klein, R., Klein, B.E.K., Moss, S.E. et al: The Epidemiology of Retinal Vein Occlusion: The Beaver Dam Eye Study. Tr. Am. Ophth. Soc., 98, 2000 : 133–143.
12. Kuchynka, P.: Oční lékařství, Praha, Grada Publishing, 2007, 291 s.
13. Mitchell, P., Smith, W., Chang, A.: Prevalence and associations of retinal vein occlusion in Australia. The Blue Mountains Eye Study. Arch Ophthalmol, 114, 1996 : 1243–1247
14. Noma, H., Funatsu, H., Mimura, T. et al.: Aqueous humor levels of vasoactive molecules correlate with vitreous levels and macular edema in central retinal vein occlusion. Eur J Ophthalmol, 20, 2010 : 402–409.
15. Ogura, Y., Roider, J., Korobelnik, J. F. et al.: Intravitreal Aflibercept for Macular Edema Secondary to Central Retinal Vein occlusion: 18-Month Results of the Phase 3 GALILEO Study. See comment in PubMed Commons below Am J Ophthalmol, 158, 2014 : 1032–1038.
16. Ponto, K.A., Elbaz, H., Peto, T. et al.: Prevalence and risk factors of retinal vein occlusion: the Gutenberg Health Study. J Thromb Haemost, 13, 2015 : 1254–1263.
17. Rogers, S., McIntosh, R. L., Cheung, N. et al.: The Prevalence of Retinal Vein Occlusion: Pooled Data from Population Studies from the United States, Europe, Asia, and Australia. Ophthalmology, 117, 2010 : 313–319.
18. Řehák, J.: Makulární edém u okluze sítnicové vény. In Ernest, J. et al.: Makulární edémy, Praha, Mladá fronta, 2014, s. 176–199.
19. Řehák J., Rehák, M.: Venózní okluze sítnice, Praha, Grada Publishing, Praha, 2011, s. 51, s. 58.
20. Sivaprasad, S., Amoaku, W. M., Hykin, P. et al.: The Royal College of Ophthalmologists Guidelines on retinal vein occlusions: executive summary. Eye, 29, 2015 : 1633–1638.
21. Studnička J., Dusová, J., Skoupá, J. et al.: Léčba makulárního edému při okluzi centrální sítnicové žíly Ozurdexem. Čes. a Slov. Oftal, 71, 2015 : 199–203.
22. The Branch Vein Occlusion Study Group: Argon Laser Photocoagulation for Macular Edema in Branch Vein Occlusion. Am J Ophthalmol, 98, 1984 : 271–282.
23. The Central Vein Occlusion Study Group: Natural History and Clinical Management of Central Retinal Vein Occlusion, Arch Ophthalmol, 115, 1997 : 486–491.
24. The Central Vein Occlusion Study Group M report: Evaluation of grid pattern photocoagulation for macular edema in central vein occlusion. Ophthalmology, 102, 1995 : 1425–1433.
25. The Central Vein Occlusion Study Group N report: A randomized clinical trial of early panretinal photocoagulation for ischemic central vein occlusion. Ophthalmology, 102, 1995 : 1434–1444.
26. The Eye Disease Case-Control Study Group: Risk Factors for Central Retinal Vein Occlusion. Arch Ophthalmol. 114, 1996 : 545–554.
Štítky
Chirurgia maxilofaciálna Oftalmológia
Článok vyšiel v časopiseČeská a slovenská oftalmologie
Najčítanejšie tento týždeň
2017 Číslo 2- Cyklosporin A v léčbě suchého oka − systematický přehled a metaanalýza
- Dlouhodobé výsledky lokální léčby cyklosporinem A u těžkého syndromu suchého oka s 10letou dobou sledování
- Účinnost a bezpečnost 0,1% kationtové emulze cyklosporinu A v léčbě těžkého syndromu suchého oka − multicentrická randomizovaná studie
- Pomocné látky v roztoku latanoprostu bez konzervačních látek vyvolávají zánětlivou odpověď a cytotoxicitu u imortalizovaných lidských HCE-2 epitelových buněk rohovky
- Konzervační látka polyquaternium-1 zvyšuje cytotoxicitu a zánět spojený s NF-kappaB u epitelových buněk lidské rohovky
-
Všetky články tohto čísla
- Dvouleté zkušenosti s intravitreální léčbou makulárního edému ranibizumabem u pacientů s okluzí retinální vény
- Translaminárny gradient a glaukóm
- Hodnotenie intrakraniálneho tlaku oftalmológom
- Selektivní laserová trabekuloplastika – význam pro přerušení medikamentózní léčby glaukomu u těhotných a kojících žen
- Steroidní glaukom jako komplikace lokální léčby atopického ekzému
- Přínos a kontraproduktivita terapie kortikosteroidy u afekcí rohovky
- ŽIVOTNÍ JUBILEUM PROF. MUDr. ANTONA GERINCE, CSc.
-
Klinický konsensus pro refrakční chirurgii
Vypracovala Česká společnost refrakční a kataraktové chirurgie
- Česká a slovenská oftalmologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Přínos a kontraproduktivita terapie kortikosteroidy u afekcí rohovky
- Steroidní glaukom jako komplikace lokální léčby atopického ekzému
- Hodnotenie intrakraniálneho tlaku oftalmológom
- Dvouleté zkušenosti s intravitreální léčbou makulárního edému ranibizumabem u pacientů s okluzí retinální vény
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy






