-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Dysfunkce mikce u pacientů s posttraumatickou míšní lézí - úloha urologa
Voiding dysfunction in patients with post-traumatic spinal cord lesion: the urologist’s role
Urological care of patients with a spinal cord lesion begins immediately after the injury. Approaches to treatment and to bladder evacuation are different in various phases of the spinal cord shock. It is important to diagnose the definitive type of lower urinary tract dysfunction and thus establish appropriate treatment. This helps to prevent complications and maintain a high quality of life.
KEY WORDS:
Spinal cord lesion, lower urinary tract dysfunction, overactive bladder, urinary tract infection, autonomic dysreflexia.
Autori: Klára Havlová
Pôsobisko autorov: Urologická klinika FN Motol, Praha
Vyšlo v časopise: Ces Urol 2017; 21(2): 129-138
Kategória: Přehledový článek
Súhrn
Urologická péče o pacienty s míšní lézí začíná bezprostředně po úrazu. Přístupy k léčbě a k evakuaci močového měchýře jsou odlišné v různých fázích míšního šoku. Je důležité diagnostikovat definitivní typ dysfunkce dolních močových cest a nastavit tak vhodnou léčbu. Tím předcházíme komplikacím a pomáháme udržovat vysokou kvalitu života.
Klíčová slova:
Míšní léze, dysfunkce dolních močových cest, hyperaktivní močový měchýř, infekce močových cest, autonomní dysreflexie.ÚVOD
Míšní léze je způsobena poraněním míchy, které vede k dočasnému, nebo trvalému porušení motorické, senzorické nebo autonomní funkce. Poranění míchy jakékoliv etiologie znamená zásah do kvality života pacienta a způsobuje těžké trvalé tělesné i psychické následky. Takovýto nemocný vždy vyžaduje komplexní, multidisciplinární péči zaměřenou na celého člověka (5). Patologické změny mohou ovlivnit funkci většiny orgánových systémů včetně funkce dolních močových cest. Dysfunkce močových cest výrazně zvyšují morbiditu pacienta tím, že zvyšují riziko vzniku infekce močových cest, urolitiázy a poruchy renálních funkcí (1). V minulosti byly urologické komplikace nejčastější příčinou předčasného úmrtí. Klinický obraz je anatomicky určen transverzálním rozsahem míšního poranění a jeho výškovou lokalizací.
Podle transverzálního míšního poranění jde buď o kompletní, nebo inkompletní lézi. Obrazem kompletní transverzální léze je úplná ztráta funkce míchy pod úrovní poranění. Inkompletní léze vede k různě rozsáhlé ztrátě motorických, senzorických a autonomních funkcí. Pro klinické hodnocení stavu je nejrozšířenější hodnocení podle American Spinal Injury Association (ASIA) Impairment Scale (AIS). Postižení můžeme rozdělit do pěti stupňů (4) (tabulka 1).
Tab. 1. ASIA Impairment Scale Tab. 1 ASIA Impairment Scale 
EPIDEMIOLOGIE
Ve většině případů se jedná o míšní léze způsobené úrazem. Na prvním místě jsou to pády, dále pak dopravní nehody a sportovní úrazy (cyklistika, skoky do vody, motokros, lyžování). Menší procento představují neúrazové míšní léze – jde o akutně vzniklé míšní léze na podkladě cévního, zánětlivého, degenerativního, nádorového, nebo demyelinizačního onemocnění (2). Od roku 2005 – 2013 bylo více jak 50 % míšních poranění v České republice úrazové etiologie (43 % pád, 30 % autonehoda, 10 % úrazy ve vodě). Neúrazové míšní léze byly z 26 % způsobeny zánětem a z 23 % tumorem. V roce 2013 bylo na rehabilitačních spinálních jednotkách ošetřeno 266 pacientů – 184 mužů, 82 žen (tabulka 2). Průměrný věk byl 53,9 let. 113 pacientů mělo poraněnou krční, 113 pacientů hrudní a 40 pacientů bederní páteř. Podle mezinárodní klasifikace AIS byli pacienti postižení nekompletní míšní lézí typu D (42 %). Etiologie byla především úrazová – 55 % (3).
Tab. 2. Statistika počtu pacientů na Spinálních rehabilitačních jednotkách za rok 2013 Tab. 2 Statistics on the number of patients at Spinal Rehabilitation Units in 2013 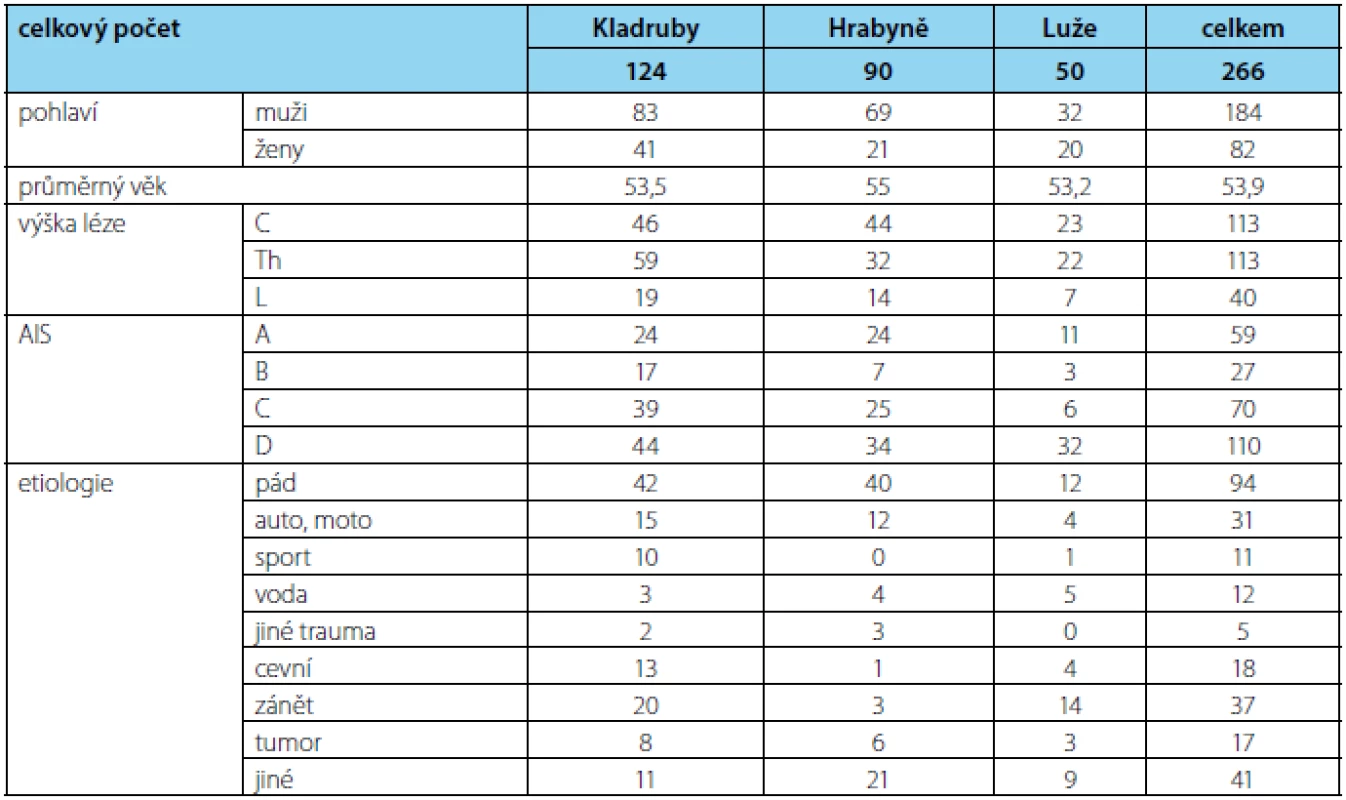
INERVACE DOLNÍCH MOČOVÝCH CEST
Jímání a vyprazdňování močového měchýře je pod kontrolou periferních parasympatických, sympatických a somatických nervů, které jsou ovlivňovány centrálním nervovým systémem.
Parasympatické eferentní (motorické) nervové dráhy vycházejí ze sakrální míchy (segmenty S2–S4) a ovlivňují kontrakci močového měchýře. Sympatická nervová vlákna vycházejí z hrudní a lumbální míchy, ze segmentů Th11–L2, inervují především oblast trigona, hrdla močového měchýře a proximální uretry. Jejích stimulací dochází ke kontrakci svaloviny v této oblasti a tím ke kontrakci svěrače. Aktivací sympatiku je schopen močový měchýř plnění. Somatické nervové dráhy odstupují ze sakrálních segmentů S3–S4 z tzv. Onufova jádra a cestou pudendálních nervů inervují svaly pánevního dna a zevní svěrač. Samotný proces mikce je pod kontrolou tří důležitých center – korové mikční centrum, pontinní mikční centrum a sakrální mikční centrum. Sakrální mikční centrum (S2–S4) je reflexní centrum mikce. Eferentní nervové dráhy cestou parasympatiku způsobují kontrakci svaloviny močového měchýře, aferentní dráhy nás informují o plnosti močového měchýře. Pontinní mikční centrum je zodpovědné za koordinaci mikce – relaxaci sfinkteru během kontrakce svaloviny močového měchýře. Korové mikční centrum inhibuje sakrální mikční centrum. Odpovídá za možnost oddálit samotný proces mikce (11, 18).
DYSFUNKCE DOLNÍCH MOČOVÝCH CEST U PACIENTŮ S MÍŠNÍM PORANĚNÍM
Dysfunkce dolních močových cest můžeme podle lokalizace místa postižení rozdělit na léze suprapontinní, suprasakrální a subsakrální. Další dělení využívá Madersbacherovy klasifikace, která vychází z urodynamicko‑klinického nálezu (obrázek 1).
Obr. 1. Madersbacherova klasifikace Fig. 1 Madersbacher classification system 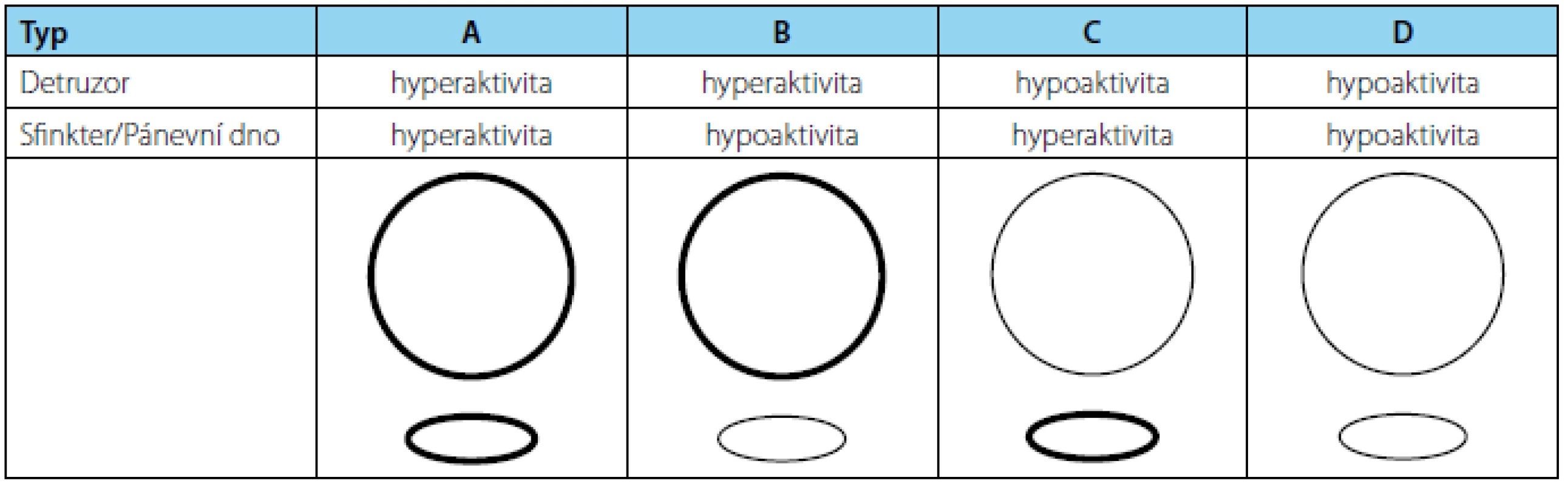
Suprasakrální léze (infrapontinní) bývá nejčastěji přítomná u pacientů s traumatickou míšní lézí nad míšní segment S2. U takovýchto pacientů je přítomná hyperaktivita detruzoru často spojená s detruzoro‑sfinkterickou dyssynergií. Tato kombinace patří mezi nejrizikovější pro ohrožení horních močových cest.
Příčinou sakrální a subsakrální léze mohou být traumatická poranění páteře, diskopatie, lumbální stenóza, periferní neuropatie nebo tumory v míšních segmentech S2–S4 a v oblasti caudy equiny. Je přerušen mikční reflex, dochází k denervaci detruzoru, což se projevuje jeho hypokontraktilitou. Činnost sfinkteru může být zachována. Většinou ale dochází k jeho dysfunkci, svěrač je bez volní kontroly a ztrácí schopnost relaxace. Pacienti mohou být inkontinentí z tzv. přetékání. Typická je ztráta citlivosti v oblasti perinea typu jezdeckého sedla a ztráta citlivosti na laterální straně nohy. Bulbokavernózní a anorektální reflex je snížený, nebo nevýbavný (12).
UROLOGICKÁ PÉČE V JEDNOTLIVÝCH FÁZÍCH MÍŠNÍHO ŠOKU
Fáze míšního šoku
I. fáze
I. fáze, někdy také nazývaná jako fáze míšního šoku, se dělí na akutní (1A) a postakutní stadium (1B). Akutní fáze vzniká bezprostředně po úrazu, její délka je variabilní, 1–2 týdny. Je charakterizovaná absencí reflexní aktivity pod úrovní míšní léze, projevují se plegií kosterního svalstva a retencí moči. Pacient je nejčastěji hospitalizován na anesteziologicko‑resuscitačním oddělení, nebo na jednotce intenzivní péče neurochirurgického nebo spondylochirurgického oddělení. V tomto období je důležité zajištění vitálních funkcí pacienta, dekomprese míchy, stabilizace páteře a chirurgické řešení sdružených poranění. V postakutním stadiu (2.–12. týden po vzniku onemocnění) je pacient většinou umístěn na Spinální rehabilitační jednotce. Cílem léčby, která probíhá za účasti specialistů z jednotlivých oborů (neurologie, ortopedie, chirurgie, urologie, psychiatrie, spondylochirurgie, rehabilitace, sociální péče), je minimalizovat důsledky míšního traumatu. V této době dochází k postupné obnově reflexů.
V akutní fázi míšního šoku je rolí urologa zajistit adekvátní evakuaci dolních močových cest. Nezávisle na úrovni míšní léze je detruzor akontraktilní a areflexní, což vede k retenci moči. Derivace moči je v této době zajištěna nejčastěji permanentním močovým katétrem (PMK). V ideálním případě je PMK použit pouze v rámci neodkladné péče po úrazu. Snaha je v co nejkratší době změnit PMK na epicystostomii, nebo zahájit čistou intermitentní katetrizaci (9). V tomto případě je důležité zhodnotit časovou perspektivu pacienta. Zásadním faktorem je úroveň míšního poranění. Epicystostomie a autokatetrizace snižují riziko vzniku symptomatické uroinfekce a vzniku striktury, nebo dekubitu močové trubice. Pokud nemůže dojít ke změně způsobu evakuace, ať už na epicystostomii nebo intermitentní katetrizaci, je vhodné používat silikonové močové katétry 14 nebo 16 Ch, které u mužů fixujeme náplastí na podbřišek. U žen je katétr fixován proximálně ke stehnu.
U pacientů s transverzální míšní lézí (TLM) v úrovni C4–C5 dochází k významné poruše hybnosti horních končetin a jemné motoriky. Soběstačnost pacienta je výrazně omezena. Pacient je neschopen autokatetrizace, proto je důležité založení punkční epicystostomie. U TLM v rozsahu C6–C7 je pacient schopen tzv. náhradního funkčního úchopu pomocí dorzální flexe zápěstí a zvládá běžné denní činnosti. Nácvik autokatetrizace je možný po zlepšení motoriky horních končetin. Přechodně lze pacienta ponechat na epicystostomii, či provádět asistovanou intermitentní katetrizaci. Pacient je v rozmezí 2–3 měsíců při dobré rehabilitaci a nácviku na trenažéru schopen autokaterizaci zvládnout, někdy s dopomocí různých kompenzačních pomůcek. Transverzální míšní léze C8 a níže jsou bez postižení motoriky horních končetin.
Vstupně by měl každý pacient absolvovat minimálně ultrazvuk močových cest k vyloučení případných sdružených poranění. Je důležité dbát na dostatečnou hydrataci pacienta (příjem vyšší než 1 500 ml/den) a tím zajistit prevenci uroinfekce a urolitiázy. Riziko vzniku urolitiázy je v období akutní fáze vyšší jako následek zvýšeného vyplavování kalcia ze skeletu při imobilizaci. Na lůžkách intenzivní péče je pacient vystaven četným nosokomiálním patogenům, ale je důležité se k léčbě postavit racionálně a léčit pouze symptomatické uroinfekce.
II. fáze
V zotavovací fázi se začínají obnovovat reflexní aktivity, ať už normální, nebo patologické. Během této doby je důležité zvládnout časné komplikace a nastavení dlouhodobého terapeutického plánu. Pacienti procházejí rehabilitací a jsou připravováni na návrat do normálního života (6).
Úlohou urologa je klasifikovat dysfunkci dolních močových cest a zavedení individuálního režimu evakuace moči. Dochází k postupnému obnovování míšních reflexů, somatické reflexy se obnovují dříve než vegetativní. Cíle urologické péče v tomto stadiu je detailní vyšetření dysfunkce dolních močových cest a nastavení individuálního režimu jímání a evakuace moči (10). Důležité je informovat pacienta o možných postupech a řešeních. Je nezbytné pacienta vstupně urologicky vyšetřit, zhodnotit neurourologický stav a naplánovat urodynamické vyšetření. Je třeba zmínit, že nález při vyšetření nemusí korelovat s výškou míšní léze. Ke změně v nálezu může dojít i po delší době od úrazu, proto je důležité pacienta pravidelně kontrolovat a některá vyšetření v určitém intervalu opakovat. Fyzikální vyšetření u spinálních pacientů zahrnuje mimo jiné neurourologické vyšetření perianogenitální oblasti, při kterém hodnotíme čití v segmentech S2–S5, hodnotíme anální reflex, bulbokavernózní reflex a volní kontrakci sfinkteru. U mužů bychom neměli opomenout vyšetření prostaty. Pokud je to možné, mělo by být součástí diagnostiky vyplnění mikčního deníku. Nutná jsou kultivační vyšetření moči a ultrasonografie močových cest. Uroflowmetrie a hodnocení postmikčního rezidua patří mezi neinvazivní diagnostické metody. U pacientů především s transverzální míšní lézí má omezené využití. Vedoucí úlohu má plnící cystometrie. Jedná se o metodu, která dokáže kvantifikovat jímací funkci močového měchýře. U neurogenních dysfunkcí je podle Mezinárodní společnosti pro kontinenci nutné plnění rychlostí 20–50 ml/min irigačním roztokem o pokojové nebo tělesné teplotě (13). Při začátku plnění by měl být močový měchýř prázdný. Během plnící cystometrie můžeme diagnostikovat detruzorovou hyperaktivitu, nebo hypoaktivitu, patologickou senzitivitu močového měchýře, abnormální compliance nebo inkontinenci. Detrusor leak point pressure je charakterizovaný jako nejnižší detruzorový tlak, při kterém dochází k úniku irigační tekutiny, bez elevace tlaku abdominálního. Za kritickou hodnotu je považován tlak nad 40 cm H2O, který je asociován s vysokým rizikem poškození horních močových cest. Mikční fázi hodnotíme pomocí mikční cystometrie, která je součástí tlakově průtokové studie (P/Q studie). Možné patologické nálezy jsou hypokontraktilita, nebo akontraktilita detruzorou, detruzoro‑sfinkterická dyssynergie. P/Q studie má omezené použití u neurourologických onemocnění. Tato vyšetření lze doplnit o elektromyografické vyšetření análního sfinkteru, který koreluje s funkcí zevního uretrálního svěrače. Tímto způsobem můžeme diagnostikovat detruzoro-sfinkterickou dyssynergii. Za zlatý standard je v současné době považováno videourodynamické vyšetření, při kterém se využívá irigace rentgen kontrastní látky. Toto vyšetření je schopné kombinovat běžné součásti urodynamického vyšetření spolu s vizualizací morfologie dolních a horních močových cest. Je možné zhodnotit funkci hrdla močového měchýře, diferencovat přítomnost vezikouretrálního reflexu, nebo divertiklů močového měchýře.
TERAPIE
Principem terapie je nastavení optimálního režimu evakuace močového měchýře s cílem ochrany horních močových cest a dosažení sociálně přijatelné míry kontinence. Je třeba zajistit důslednou prevenci urologických komplikací spojených s neurogenním močovým měchýřem.
Podle Madersbacherovy klasifikace patří mezi nejrizikovější dysfunkce typu A. U takovýchto pacientů je hyperaktivita močového měchýře nejčastěji spojena s hyperaktivitou sfinkteru. Tato kombinace patří potenciálně mezi nejrizikovější pro horní močové cesty a sekundárně též pro močový měchýř. Cílem terapie je ovlivnit hyperaktivitu močového měchýře, změnou dysfunkce na typ C (hypoaktivní, normoaktivní detruzor), a tím ochránit horní močové cesty s využitím hyperaktivního sfinkteru k zajištění kontinence. Typ B (hyperaktivní detruzor, hyoaktivní sfinkter) je pro postiženého touto dysfunkcí obtěžující především pro inkontinenci. Po zvládnutí hyperaktivity je možné přemýšlet nad eventuálním ovlivněním uzávěrového mechanizmu. Typ C (hypoakitvní detruzor, hyperaktivní sfinkter) není třeba terapeuticky měnit. U takovýchto pacientů je riziko deteriorace horních močových cest při dobré evakuaci močového měchýře minimální. Typ D, spojený s inkontinencí, se zaměřuje též na léčbu hypoaktivity sfinkteru.
U pacientů se suprasakrální míšní lézí, kteří nejčastěji trpí postižením typu A a B, je možný nácvik reflexního vyprazdňování pomocí tzv. triggerování, které spočívá ve vyvolání reflexní kontrakce detruzoru. Používá se poklepávání na podbřišek, nebo anorektální manipulce. Tato metoda se může používat u limitovaného počtu pacientů, za pravidelné urodynamické kontroly, u kterých nedochází při triggerování k rozvoji autonomní dysreflexie. Je důležité věnovat pozornost možnému vzniku hyperaktivity detruzoru a infekčním komplikacím. U více jak 90 % pacientů je přítomna detruzoro‑sfinkterická dyssynergie, proto se jako standard preferuje čistá intermitentní katetrizace. Frekvence je individuální, ale obvykle se pacienti katetrizují 4–6 krát denně a nejčastěji používaný katétr má velikost 12–16 F. Ideální objem by neměl překročit 400–500 ml během jednorázové katetrizace (14). U pacientů se suprasakrální míšní lézí je přítomna detruzorová hyperaktivita a je ji tedy třeba terapeuticky ovlivnit. Za první linii léčby je považována léčba anticholinergiky. Tato léková skupina ovlivňuje parasympatickou dráhu svým antagonistickým účinkem na muskarinové receptory urotelu, pomáhá zvyšovat kapacitu močového měchýře, snižuje detruzorovou hyperaktivitu, a tím redukuje počet epizod urgentní inkontinence. Limitujícím faktorem léčby anticholinergiky jsou jejich možné nežádoucí účinky. Mezi nejčastější patří xerostomie, obstipace, poruchy akomodace, nebo kardiální obtíže. Kontraindikací léčby je glaukom s uzavřeným úhlem, obstrukce trávicího traktu, myastenia gravis a těhotenství. Mezi I. generaci anticholinergik patří oxybitinin, trospium chlorid, propiverin, jejichž výhodou je vysoká efektivita. Bohužel díky své neselektivitě vykazují vyšší výskyt nežádoucích účinků. II. generace anticholinergik (tolterodin, solifenacin, fesoterodin, darifenacin) je pacientem lépe tolerována, neboť působí selektivně na muskarinové receptory vyskytující se v močovém měchýři. Při selhání medikamentózní terapie lze využít intravezikální terapie botulinum toxinem. Ten blokuje neuromuskulární přenos acetylcholinu na úrovni periferních nervových zakončení. Injekční aplikace se provádí v rozsahu 30 vpichů difuzně do detruzoru, alternativou je subslizniční aplikace. Odpověď na léčbu je zřejmá již po 48 hodinách, maximum efektu nastupuje mezi 6.–8. týdnem. Účinnost léčby lze objektivně dokumentovat snížením počtu mikcí (katetrizací), urgencí či urgentních inkontinencí, dále výrazným zlepšením kvality života dokumentováno použitím standardizovaných dotazníků, signifikantním zlepšením sledovaných urodynamických parametrů, jako je zvětšení cystometrické kapacity, snížení maximálního detruzorového tlaku (15). Účinek toxinu je reverzibilní, efekt léčby trvá po dobu 6–12 měsíců. Aplikaci je možné opakovat ale ne dříve než za tři měsíce, kvůli možnému vzniku protilátek proti botulinum toxinu (21). Kontraindikací aplikace botulinumtoxinu je uroinfekce, myastenia gravis, alergie na botulinumtoxin, současné podávání aminoglykosidových antibiotik, kojení, těhotenství, hemofile (16). Velmi vzácně se u pacientů může po aplikaci objevit svalová slabost, sucho v ústech, obstipace. Všechny tyto nežádoucí účinky jsou pouze přechodné (17). Sfinkterotomie – transuretrální incize zevního uretrálního svěrače patří mezi endoskopické chirurgické metody. Využívá se nejčastěji u mužů s vysokou míšní lézí, u kterých je zachovaná reflexní mikce, mají prokázanou detruzoro‑sfinkterickou dyssynergii a kteří nejsou schopni intermitentní katetrizace a mají vysoké riziko deteriorace močových cest působením vysokého intravezikálního tlaku, který není jinak možné ovlivnit. Snížením infravezikální obstrukce pomáhá sfinkterotomie stabilizovat nebo zlepšit renální funkce, snižuje riziko uroinkfekce, poškození horních močových cest a příznivě ovlivňuje symptomy autonomní dysreflexie (18, 19, 20). Je možné využít různé techniky, v současné době se zdá být nejefektivnější použití laseru. Následnou inkontinenci nejčastěji řešíme kondomovým urinálem.
Po vyčerpání méně invazivních technik je možné pacienta indikovat k trvalé neurostimulaci, nebo neuromodulaci. Pacientům s inkompletní míšní lézí můžeme nabídnout sakrální neuromodulaci, při této technice dochází ke stimulaci plexus pelvicus. Jedná se o stimulaci aferentních drah pomocí perkutánně zavedené elektrody k sakrálním kořenům (22). Mechanizmus účinku zahrnuje inhibici aktivity detruzoru přímým působením na sakrální centrum a útlum detruzorového reflexu na supraspinální úrovni. Další metodou je sakrální deaferentace (sakrální rhizotomie). Metoda se nejčastěji používá u pacientů s kompletní transverzální míšní lézí nad úroveň Th6. Přetnutím zadních kořenů míšních v rozsahu S2–S5 dojde k přerušení sakrálního reflexního oblouku, a tím dojde ke vzniku akontraktilního detruzoru. Použitím sakrální deaferentace u pacientů s inkompletní míšní lézí dojde k porušení senzorických funkcí, čímž vymizí zbylé senzorické funkce tj. reflexní erekce a defekace. Proto se tato metoda indikuje zcela výjimečně. Evakuace močového měchýře je poté řešena intermitentní katetrizací, nebo stimulací předních kořenů sakrální míchy. Stimulátor, který je implantován do podkoží na břiše, ovlivňuje elektrody na předních kořenech S3 a S4 a stimuluje mikci a dokáže u pacientů stimulovat defekaci a erekci (27).
Jednou z posledních možností řešení hyperaktivity jsou operační techniky. Za zmínku stojí autoaugmentace nebo augmentace močového měchýře s následnou autokatetrizací, tuto techniku lze kombinovat s vezikostomií podle Mitrofanoffa (28).
U sakrální léze (typ dysfunkce C, D) dochází k hypoaktivitě až k areflexii detruzoru v důsledku poškození sakrálního mikčního centra. Důležité je říct, že vnější svěrač není inervován stejnými nervovými drahami jako detruzor. To znamená, že velmi často dochází ke vzniku areflexie detruzoru s intaktním svěračem. Typickým příznakem je retence nebo slabý proud moči. Pacienti mohou močit přerušovaně se zapojením břišního lisu.
Dalším příznakem může být inkontinence – buď z přetékání, nebo postižením pánevního dna a dysfunkcí svěrače (18). Kvalita života je též ovlivněna ztrátou citlivosti zevního genitálu a neschopností normální defekace. Nejvhodnější terapií je zvládnutí intermitentní katetrizace, která zajistí adekvátní evakuaci močového měchýře. Při zachované mikci u pacientů s inkompletní míšní lézí je možné zkusit využít konzervativního postupu – užívání alfalytické terapie s pravidelnou ultrazvukovou kontrolou rezidua, nebo kombinace alfalytik a intermitentní katetrizace. U pacientů s hypoaktivním svěračem, u kterých je největším problémem inkontinence, je po pečlivé diskuzi možnost pacienta indikovat ke slingové operaci nebo k implantaci artificiálního sfinkteru. Pacient musí zvládnout intermitentní katetrizaci a je třeba vyloučit hyperaktivitu močového měchýře.
Ve III. fázi dochází ke stabilizaci onemocnění. Je důležité průběžně udržovat fyzickou kondici pacienta a předejít možným komplikacím v průběhu celého života. Pacienti jsou dispenzarizováni v urologických ambulancích. Cílem je udržet co nejvyšší kvalitu života a předejít komplikacím spojeným s dysfunkcí dolních močových cest. Každé 2–3 měsíce se provádí pravidelné vyšetření moči buď cestou praktického lékaře, nebo urologa. Ultrazvukové vyšetření ledvin a močového měchýře plánujeme každých šest měsíců. Každý rok by měl pacient absolvovat klinickou kontrolu a laboratorní vyšetření včetně vyšetření funkce ledvin. Specializované vyšetření, jako je urodynamika, je indikovaná individuálně.
AUTONOMNÍ DYSREFLEXIE
Autonomní dysreflexie (AD) je závažná komplikace, která se projeví u více než poloviny pacientů s míšním poraněním nad šestým hrudním segmentem. Závažnost AD ovlivňuje výška léze, čím výše je poranění, tím může být projev AD významnější. Kompletní míšní léze má těžší projevy AD než léze inkompletní (8). Při poruše autonomního nervového systému je podráždění pod úrovní míšní léze zdrojem těžké vazokonstrikce, která způsobí paroxyzmální hypertenzi. Obecně se považuje za projev AD zvýšení krevního tlaku o více než 20 – 30 mmHg. Doprovází ji bradykardie, prudká cefalea, nauzea, anxiozita, zastřené vidění, pocení a zarudnutí nad úrovní léze, někdy se však může vyskytovat bez subjektivních příznaků. Pod úrovní léze se může objevit piloerekce a zblednutí kůže. Nejčastější příčinou je distenze močového měchýře, distenze rekta, operační zákroky na dolních močových cestách, ale i popáleniny, dekubity nebo fraktury. I jiné vnější příčiny mohou způsobit autonomní dysreflexii. Je to například těsné oblečení nebo obuv, excesivní příjem alkoholu nebo abúzus omamných látek. Nekontrolovaná hypertenze může vyústit v krvácení do mozku, krvácení do sítnice, v infarkt myokardu a může vést i ke smrti. Léčba spočívá ve vertikalizaci, která pomůže ortostaticky snížit krevní tlak, především je ale třeba neodkladně vyřešit příčinu podráždění. To vede zpravidla k normalizaci krevního tlaku. Při přetrvávající hypertenzi je nutné použít antihypertenziva s rychlým nástupem účinku. Na autonomní dysreflexii je důležité myslet při endoskopickém a urodynamickém vyšetření u pacientů s touto anamnézou.
INFEKCE MOČOVÝCH CEST
Nejčastějšími infekcemi u pacientů po poranění míchy jsou infekce močových cest, infekce krevního oběhu, měkkých tkání a rané infekce. Navíc mají tito pacienti významně vyšší riziko rozvoje nozokomiálních infekcí (23). V současné době neexistují kritéria pro kvantifikaci bakteriurie, nebo pro spektrum příznaků, které určují symptomatickou uroinfekci. Obecně je přijímán názor, že za signifikantní bakteriurii se považuje ≥102 b/ml u pacientů na režimu intermitentní katetrizace, ≥104 b/ ml při ostatních způsobech mikce, či derivace (24). Přítomnost permanentního močového katétru zvyšuje riziko symptomatické uroinfekce, proto je žádoucí, co nejdříve změnit způsob derivace dolních močových cest. Pokud v ideálním případě nedojde k obnovení spontánní mikce, je nejpreferovanější metodou čistá intermitentní katetrizace. Jestliže není pacient schopen autokatetrizace, nebo není možnost asistence druhé osoby, je považováno za metodu volby založení epicystostomie. Mezi další rizikové faktory vzniku symptomatické infekce patří detruzoro‑sfinkterická dyssynergie, hyperaktivní močový měchýř, velká postmikční rezidua, přítomnost konkrementů v močovém traktu a vezikoureterální reflux (25). Asymptomatická bakteriurie není indikací k antibiotické terapii z důvodu rizika selekce polyrezistentních kmenů. Při symptomatické uroinfekci zahajujeme antibiotickou léčbu podle citlivosti z poslední kultivace. V případě, že nemáme k dispozici aktuální kultivaci, zahajujeme léčbu empiricky širokospektrými antibiotiky, abychom pokryli co největší spektrum bakterií. Po dvou dnech máme již první výsledky nové kultivace a léčbu eventuelně upravujeme po konzultaci s antibiotickým střediskem. Mezi symptomy patří pyurie, horečka, diskomfort nebo citlivost ledvin nebo močového měchýře, dysurie, močová inkontinence, zvýšená spasticita, autonomní dysreflexie, netečnost, stísněný pocit (26). Jako prevenci uroinfekce nebo v případě recidivujících uroinfekcí lze doporučit i preventivní užívání fytopreparátů, jako jsou extrakty z brusinek a lichořeřišnice větší, nebo podávání probiotik s mléčnými bakteriemi vaginálně nebo perorálně ke zlepšení stavu mikroflóry. Brusinkové extrakty snižují fragilitu kapilár a zabraňují přilnutí patogenní E. coli na sliznici. E. coli mají fimbrie, které jim umožňují adherenci na urotel. Na vrcholu fimbrie je glykoprotein, který se váže s monosacharidem D‑manózou.
Podáme‑li ji v nadbytku, mikroby ztrácí schopnost adherence a jsou vyloučeny močí. Další terapeutickou možností je využití imunomodulace. Jedná se o systémovou perorální imunoterapii preparáty obsahujícími imunostimulující frakce extrahované z buněk E. coli. Máme k dispozici preparát Uro‑Vaxom, který se užívá jednou denně ráno nalačno po dobu tří až šesti měsíců s následným podáváním posilujících dávek v časovém odstupu. Cílem profylaxe je posílení slizniční imunity dolních močových cest. Další alternativou dlouhodobé profylaxe je užívání antibiotik v subinhibičních dávkách. Nejvhodnější k takové léčbě je nitrofurantoin 50–100 mg, trimetoprim 100 mg, trimetoprim/sulfametoxazol 240 mg po dobu 3–12 měsíců. Vznikne‑li během profylaxe symptomatický zánět močových cest, po jeho vyléčení se v profylaktickém podávání antimikrobiálního léku může pokračovat.
ZÁVĚR
Urologická péče o pacienty s míšní lézí je součástí komplexního multidisciplinárího přístupu. Začíná bezprostředně po traumatu a pokračuje v průběhu celého života, Kromě vyřešení akutního stavu, je potřeba neustále pečovat o močové cesty, abychom snížili morbiditu pacienta a zlepšili dlouhodobě jeho kvalitu života. Důležitá je správná diagnostika dysfunkce dolních cest močových a nastavení adekvátní terapie k typu dysfunkce, abychom předešli možným komplikacím.
Došlo: 6. 5. 2016
Přijato: 11. 6. 2017
Střet zájmů: žádný
Prohlášení o podpoře: Autorka prohlašuje, že zpracování článku nebylo podpořeno farmaceutickou firmou.
Kontaktní adresa: MUDr. Klára Havlová
Urologická klinika FN Motol, Praha
V Úvalu 84, 150 06 Praha
e-mail: klara.havlova@fnmotol.cz
Zdroje
1. Hansen RB, Biering‑Sørensen F, Kristensen JK. Bladder emptying over a period of 10–45 years after a traumatic spinal cord injury. Spinal Cord 2004; 42(11): 631–637.
2. Wendesche P, Kříž J. Doporučené postupy péče v akutní fázi po poškození míchy [online]. 2005 [cit. 2016 - 02-25]. Dostupné z: http://www.spinalcord.cz/_userfiles/dokumenty/doporucene‑postupy/ akutni_pece.pdf.
3. Statistiky. Česká společnost pro míšní léze ČLS JEP. [online]. [2016] [cit. 2016-02-25]. Dostupné z: http:// www.spinalcord.cz/cz/statistiky/
4. Ambler Z. Základy neurologie. 6. vyd. Praha: Galén, 2006.
5. Jirků H, Kyriánová A. Doporučené postupy pro ošetřovatelskou péči o pacienty po poškození míchy [online]. 2006 [cit. 2016-02-25]. Dostupné z: http://www.spinalcord.cz/_userfiles/dokumenty/doporucene-postupy/osetrovani.pdf.
6. Kirshblum C, Priebe MM, Ho CH, Scelza VM, Chiodo AE, Wuermser LA. Spinal cord injury medicine. 3. Rehabilitation phase after acute spinal cord injury. Archives of physical medicine and rehabilitation 2007; 88(3): S62–S70.
7. Kříž J, Rejchrt M. Autonomní dysreflexie – závažná komplikace u pacientů po poranění míchy. Cesk Slov Neurol N 2014; 77/110(2): 168–173.
8. Šámal V, Mečl J. Autonomní dysreflexie u pacientů po spinálním poranění. Ces Urol 2014; 18(4): 279–287.
9. Doležel J. Traumatické léze míšní. Urol. praxi 2004; 5(4): 146–155.
10. Krhut J, Doležel J, Zachoval R. Doporučené postupy pro urologickou péči o pacienty po poškození míchy. Praha: Svaz paraplegiků s podporou MZČR, 2006.
11. Yoshimura N, Chancellor MB. Neurophysiology of lower urinary tract function and dysfunction. Reviews in urology 2003; 5: S3.
12. Lukáš K. Chorobné znaky a příznaky. Grada Publishing a.s., 2010.
13. Krhut J, Doležel J, Doležil D, Zachoval R, Ženíšek J. Neurourologie. 1. vyd. Praha: Galén, 2005 : 141.
14. Blok B, Pannek J, Castro Diaz D, et al. Guidelines on neuro‑urology. 2015.
15. Šámal V. Botulinumtoxin a jeho aktuální použití v urologii. Ces Urol 2009; 13(3): 199–206.16. Cone EB, Ellsworth P. Neurogenic detrusor overactivity: an update on management options. RI Med J 2013; 96(4): 38–40.
17. Ghei M, Marai BH, Miller R, et al. Effects of botulinum toxin BoNT/A on refraktory detrusor overactivity: a randomised, double blind, placebo‑controlled, crossover trial. J Urol 2005; 174 : 1873–1878.
18. Consortium for Spinal Cord Medicine. Bladder management for adults with spinal cord injury: a clinical practice guideline for health‑care providers. J Spinal Cord Med. 2006; 29(5): 527–573.
19. Perkash I. Transurethral sphincterotomy provides significant relief in autonomic dysreflexia in spinal cord injured male patients: long‑term followup results. J Urol. 2007 Mar; 177(3): 1026–1029.
20. Vapnek JM, Couillard DR, Stone AR. Is sphincterotomy the best management of the spinal cord injured bladder? J Urol. 1994; 151(4): 961–964.
21. Krhut J. Botulotoxin – struktura, mechanizmus účinku a klinické použití. Urol. praxi 2006; 5 : 278–282.
22. Mackerle Z, Brichtová E, Zerhau P, et al. Neurostimulace, neuromodulace a neurotizace v terapii neurogenního močového měchýře. Cesk Slov Neurol N 2015; 78/111(1): 83–87.
23. Evans CT, Lavela SL, Weaver FM, et al. Epidemiology of hospital-acquired infections in veterans with spinal cord injury and disorder. Infect Control Hosp Epidemiol. 2008; 29 : 234–242.
24. National Institute on Disability and Rehabilitation Research (NIDRR) consensus statement, January 27–29, 1992: the prevention and management of urinary tract infection among people with spinal cord injuries. J Am Paraplegia Soc. 1992; 15 : 194–204.
25. García Leoni ME, Esclarín de Ruz A. Management of urinary tract infection in patients with spinal cord injuries. Clin Microbiol Infect. 2003; 9 : 780–785.
26. Massa LM, Hoffman JM, Cardenas DD. Validity, accuracy, and predictive value of urinary tract infection signs and symptoms in individuals with spinal cord injury on intermittent catheterization. J Spinal Cord Med. 2009; 32 : 568–573.
27. Brindley GS, Polkey CE, Rushton DN. Sacral anterior root stimulator for bladder control in paraplegia. Paraplegia 1982; 20 : 365–381.
28. Doležel J. Traumatická míšní léze. Urol. praxi 2004; 5(4): 146–155.
Štítky
Detská urológia Nefrológia Urológia
Článok vyšiel v časopiseČeská urologie
Najčítanejšie tento týždeň
2017 Číslo 2- Aktuálne európske odporúčania pre liečbu renálnej koliky v dôsledku urolitiázy
- MUDr. Šimon Kozák: V algeziológii nič nefunguje zázračne cez noc! Je dôležité nechať si poradiť od špecialistov
- Vyšetření T2:EGR a PCA3 v moči při záchytu agresivního karcinomu prostaty
- Lék v boji proti benigní hyperplazii prostaty nyní pod novým názvem Adafin
-
Všetky články tohto čísla
- Editorial
- Využití flexibilní nefroskopie k extrakci urolitiázy při laparoskopické a roboticky asistované pyeloplastice
- Intravezikální chemoterapie s využitím tepelné energie u pacientů s uroteliálním karcinomem močového měchýře bez invaze svaloviny
- Dysfunkce mikce u pacientů s posttraumatickou míšní lézí - úloha urologa
- Sledování a léčba pacientů po radikální prostatektomii s pozitivními okraji preparátu
- Funkční výsledky pyeloplastiky provedené v kojeneckém věku
- Nefrometrická skóre první a druhé generace pro predikci peri- a pooperačních výsledků resekcí ledvin
- Efficacy and safety of extracorporeal shock wave lithotripsy in the 21th century – controversy and clinical practice.
- Spontánní ruptura renálního angiomyolipomu
- Trombóza povrchové dorzální žíly penisu (Penilní Mondorova choroba)
- Zpráva o proběhlém 5. ročníku Video‑semináře Tipy a triky v Urologické operativně
- Zpráva z workshopu Sekce urodynamiky, neurourologie a urogynekologie ČUS ČLS JEP: Funkční urologie - Novinky 2017
- 2. ročník konference KNOU, pohled mladého lékaře
- ASSOC. PROF. ROMAN ZACHOVAL, M.D., PH.D., MBA, CELEBRATED HIS 50TH BIRTHDAY
- Česká urologie
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Trombóza povrchové dorzální žíly penisu (Penilní Mondorova choroba)
- Dysfunkce mikce u pacientů s posttraumatickou míšní lézí - úloha urologa
- Sledování a léčba pacientů po radikální prostatektomii s pozitivními okraji preparátu
- ASSOC. PROF. ROMAN ZACHOVAL, M.D., PH.D., MBA, CELEBRATED HIS 50TH BIRTHDAY
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



