-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Porovnanie účinnosti ranibizumabu a pegaptanibu sodného v liečbe diabetického edému makuly
Comparison of the effectiveness of ranibizumab and pegaptanib sodium in the treatment of diabetic macular edema
Objective:
To review the effectiveness of ranibizumab and pegaptanib sodium in the treatment of diffuse diabetic macular edema in a loading dose (3 injections).Materials and Methods:
Patients with diffuse diabetic macular edema, central macular thickness (CMT) ≥ 250 μm and best-corrected visual acuity (BCVA) between 39 and 73 letters were prospectively divided into 2 groups according to the applied drug – ranibizumab (ranibizumab 0.5 mg) and pegaptanib (pegaptanib sodium 0.3 mg). According on the application schema for monitored drugs eyes treated with ranibizumab were evaluated at 4, 8 and 12 weeks and eyes treated with pegaptanib sodium after 6, 12 and 18 weeks. Best-corrected visual acuity, CMT and macular volume werere followed – up.Results:
Prospective study enrolled 20 patients/21 eyes with diffuse DEM group ranibizumab 11 eyes and group pegaptanib 10 eyes. The value of HbA1c were 7.55, 7.95 respectively. The ranibizumab group, the baseline BCVA was 51.9 letters CMT 553.45 μm and macular volume 10.68 mm3. After 12 weeks BCVA increased +11.2 letters, mean change CMT -135.9 μm and macular volume -1.62 mm3. In the group pegaptanib baseline BCVA was 54.1 letters CMT 499,6μm and macular volume 10.4 mm3. After 18 weeks BCVA increased +3.25 letteres, mean change CMT +4.38 μm, and macular volume -0.56 mm3. In ranibizumab group, 29 injections were administered. In 4 eyes after the initial two applications treatment was discontinued in accordance with criteria to discontinue treatment (CMT ≤ 250 μm or BCVA ≥ 84 letters). In pegaptanib group 28 injections were administered, 1 patient died of cardiac failure after 10 weeks of treatment initiation.Conclusion:
Intravitreal antivascular endothelial growth factors in the treatment of diabetic macular edema improves visual acuity and reduces central thickness and macular volume on OCT. In this study ranibizumab 0.5 mg demonstrated superior efficacy to pegaptanib sodium 0.3 mg after the initial three doses.Key words:
diabetic macular edema, ranibizumab, pegaptanibReceived:
30. 12. 2016Accepted:
17. 2. 2017
Autori: Jana Štefaničková; Jaroslav Hasa
Pôsobisko autorov: Klinika oftalmológie LF UK a UNB, Nemocnica Ružinov, Bratislava
Vyšlo v časopise: Forum Diab 2017; 6(1): 20-26
Kategória: Hlavná téma
Súhrn
Cieľ:
Sledovať účinnosť ranibizumabu a pegaptanibu sodného v liečbe difúzneho diabetického edému makuly v úvodnej nasycovacej dávke (3 aplikácie).Materiál a metódy:
Pacienti s difúznym diabetickým edémom makuly, centrálnou hrúbkou makuly (CMT) ≥ 250 µm a najlepšie korigovanou centrálnou ostrosťou zraku (NKCOZ) medzi 39 a 73 písmen boli prospektívne rozdelení do 2 skupín podľa aplikovaného liečiva – ranibizumab (ranibizumab 0,5 mg) a pegaptanib (pegaptanib sodný 0,3 mg). Na základe doporučenej aplikačnej schémy pre sledované liečivá, oči liečené ranibizumabom sme hodnotili po 4, 8 a 12 týždňoch a oči liečené pegaptanibom sodným po 6, 12 a 18 týždňoch. Sledovali sme najlepšie korigovanú centrálnu ostrosť zraku (NKCOZ) – počet písmen, centrálnu hrúbku makuly (CMT) a objem makuly.Výsledky:
Do prospektívneho sledovania bolo zaradených 20 pacientov/21 očí s difúznym diabetickým edémom makuly, skupina s ranibizumabom 11 očí a skupina s pegaptanibom 10 očí. Priemerná hodnota HbA1c bola 7,55, respektíve 7,95. V skupine s ranibizumabom bola priemerná vstupná NKCOZ 51,9 písmena, CMT 553,45 µm a objem makuly 10,68 mm3. Po 12 týždňoch bol priemerný zisk písmen +11,2 písmena, CMT -135,9 µm, a objem makuly -1,62 mm3. V skupine s pegaptanibom bola priemerná vstupná NKCOZ 54,1 písmena, CMT 499,6 µm a objem makuly 10,4 mm3. Po 18 týždňoch bol priemerný zisk +3,25 písmena, priemerná CMT zmena +4,38 µm, a objem makuly zmena -0,56 mm3. V skupine s ranibizumabom bolo aplikovaných 29 injekcií, u 4 očí po úvodných 2 aplikáciách bola liečba prerušená podľa kritérií na prerušenie liečby (CMT ≤ 250 µm alebo NKCOZ ≥ 84 písmen). V skupine s pegaptanibom 28 injekcií 1 pacient zomrel na kardiálne zlyhanie po 10 týždňoch od začatia liečby.Záver:
Intravitreálne podávané blokátory cievneho endotelového rastového faktoru v liečbe diabetického edému makuly zlepšujú centrálnu ostrosť zraku a zmenšuje centrálnu hrúbku aj objem makuly na OCT. V tomto sledovaní ranibizumab 0,5 mg preukázal vyššiu účinnosť ako pegaptanib sodný 0,3 mg už po úvodných 3 dávkach.Kľúčové slová:
diabetický edém makuly, pegaptanib, ranibizumabÚvod
Diabetický edém makuly (DEM) je najčastejšou príčinou zhoršenia najlepšie korigovanej centrálnej ostrosti zraku (NKCOZ) u ľudí s ochorením diabetes mellitus. Môže sa objaviť v každom štádiu neproliferatívnej aj proliferatívnej diabetickej retinopatie. Veľmi často postihuje populáciu v produktívnom veku, a ak je ponechaný bez liečby, viac ako 50 % pacientov stratí > 2 riadky NKCOZ v rozmedzí 2 rokov [1]. V doteraz jedinej európskej štúdii bol zaznamenaný pokles zhoršenia NKCOZ pri DEM približne 5,4% [2]. Pri očakávanom raste prevalencie diabetu v budúcnosti bude rásť aj počet pacientov s DEM a s tým spojené zhoršovanie NKCOZ.
Hoci patogenéza diabetickej retinopatie a DEM nie je stále úplne známa, hyperglykémia je pravdepodobne najdôležitejší impulz pri jej vzniku. Zlá glykemická kontrola vedie k zhoršeniu diabetickej retinopatie. Zvýšená hladina glykémie poškodzuje cievy sietnice so vznikom krvácaní, mikroaneuryziem a uzáverom kapilár. Uzáver kapilár spôsobuje hypoxiu, a ako už bolo známe v minulosti, neovaskularizácie na sietnici. V ischemickej sietnici sa tvoria vysoké hladiny cievneho endotelového rastového faktoru (VEGF), ktorý nielen spôsobuje vznik neovaskularizácií na sietnici, ale zároveň je aj najsilnejším mediátorom zvýšenej cievnej permeablility, a tým aj opuchu makuly. V experimente injekcia VEGF do očí myší spôsobila zrútenie vnútornej hematookulárnej bariéry a následne opuch makuly [3].
V liečbe diabetickej retinopatie a DEM má nezastupiteľné miesto laserkoagulácia sietnice. Štandardná liečba DEM fokálnou alebo mriežkovou laserkoaguláciou v mnohých prípadoch dokáže NKCOZ len stabilizovať [1,4]. V Early Treatment Diabetic Retinopathy Study (EDTRS) u pacientov s DEM liečba laserkoaguláciou znížila riziko zhoršenia NKCOZ o 50 % [1]. Vedľajším nežiadúcim účinkom laserkoagulácie môže byť vznik skotómov, často veľmi negatívne vnímaných pacientami [5]. V štúdii DRCR.net [6] pacienti liečení laserkoaguláciou po 2 rokoch získali len 2 písmená. Snaha o zlepšenie liečby DEM spolu s novými údajmi o poruche regulácie VEGF v sietnici u diabetikov priniesla do liečby nové látky – blokátory VEGF, ktoré dokážu NKCOZ nielen stabilizovať, ale aj zlepšiť [6–11].
Cieľom tejto práce je sledovať účinnosť 2 blokátorov VEGF, ranibizumabu a pegaptanibu sodného, v liečbe DEM v úvodnej nasycovacej dávke (3 aplikácie).
Materiál a metódy
Do prospektívneho sledovania boli zaradené oči s difúznym DEM po splnení nasledujúcich kritérií:
- centrálna hrúbka makuly (CMT) ≥ 250 µm
- NKCOZ 20–73 písmen
- hodnota glykovaného hemoglobínu (HbA1c) za posledné 3 mesiace
Exklúzne kritéria:
- laserkoagulácia makuly < 3 mesiace a panretinálna laserkoagulácia < 4 mesiace pred začiatkom liečby
- intravitreálna aplikácia kortikosteroidov alebo inhibítorov VEGF < 3 mesiace pred iniciáciou liečby
Pacienti boli zaraďovaní do sledovania od decembra 2010 do januára 2011. Oči boli rozdelení do 2 súborov. V súbore „Ranibizumab“ bol pacientom intravitreálne aplikovaný ranibizumab 0,5 mg a v súbore „Pegaptanib“ liek pegaptanib sodný v dávke 0,3 mg. Na základe rôzne dlhých polčasov rozpadu a všeobecne známych aplikačných schém ranibizumabu a pegaptanibu sodného sme oči liečené ranibizumabom hodnotili po 4, 8 a 12 týždňoch a oči liečené pegaptanibom sodným po 6, 12 a 18 týždňoch od prvej aplikácie. Sledovali sme NKCOZ – počet písmen, CMT a objem makuly a nežiadúce účinky. V súbore „Ranibizumab“ bol podávaný ranibizumab v dávke 0,5 mg každé 4 týždne, spolu 3-krát. Liečba bola pozastavená, ak bola dosiahnutá CMT ≤ 250 µm alebo NKCOZ ≥ 84 písmen. Pacientom v súbore „Pegaptanib“ boli aplikované 3 intravitreálne injekcie pegaptanibu sodného 0,3 mg každých 6 týždňov. V tejto skupine neboli stanovené kritéria na prerušenie liečby vzhľadom na výsledky publikovaných štúdií s pegaptanibom sodným v liečbe DEM. U jedného pacienta liečeného ranibizumabom boli liečené 2 oči. Pri každej návšteve boli realizované tieto vyšetrenia: centrálna ostrosť zraku na EDTRS tabulách certifikovaným lekárom na toto vyšetrenie, meranie vnútroočného tlaku, vyšetrenie štrbinovou lampou predného segmentu, biomikroskopické vyšetrenie zadného segmentu v mydriáze, farebná fotografia fundu, fluoresceínová angiografia pred zaradením a na konci sledovania. Pri vyšetrení OCT na prístroji Stratus (Carl Zeiss, Meditec, Dublin, USA) sme použili fast macular scan 6 mm, Cross hair 6 mm a na zhodnotenie vitreomakulárneho rozhrania line scan 8 mm.
Na štatistické zhodnotenie parametrov pred a po aplikácii sme použili Wilcoxonov neparametrický test (ten sme si vybrali z dôvodu malého počtu pacientov v sledovaných skupinách).
Výsledky
Do skupiny „Ranibizumab“ bolo zaradených 10 pacientov/11 očí a do skupiny „Pegaptanib“ 10 pacientov/10 očí. Priemerný vek 59,7 a 60,3 roka. Priemerná hodnota HbA1c bola 7,55 %, resp. 7,95 %. Dĺžka zhoršovania NKCOZ bola v obidvoch súboroch približne rovnaká 21,7 a 18,9 mesiaca. Dve oči z prvého súboru a 6 očí z druhého súboru mali v minulosti podaný triamcinolon acetonid (TRIAM). U všetkých očí bol zistený DEM bez prítomnosti trakcie na OCT (8 mm scan). Doba sledovania bola 12 týždňov v súbore „Ranibizumab“ a 18 týždňov v súbore „Pegaptanib“ (tab. 1 a tab. 2).
Tab. 1. Charakteristika súborov podľa pohlavia, typu DM, výskytu hypertenzie, štádia DR a predchádzajúcej oftalmologickej liečby 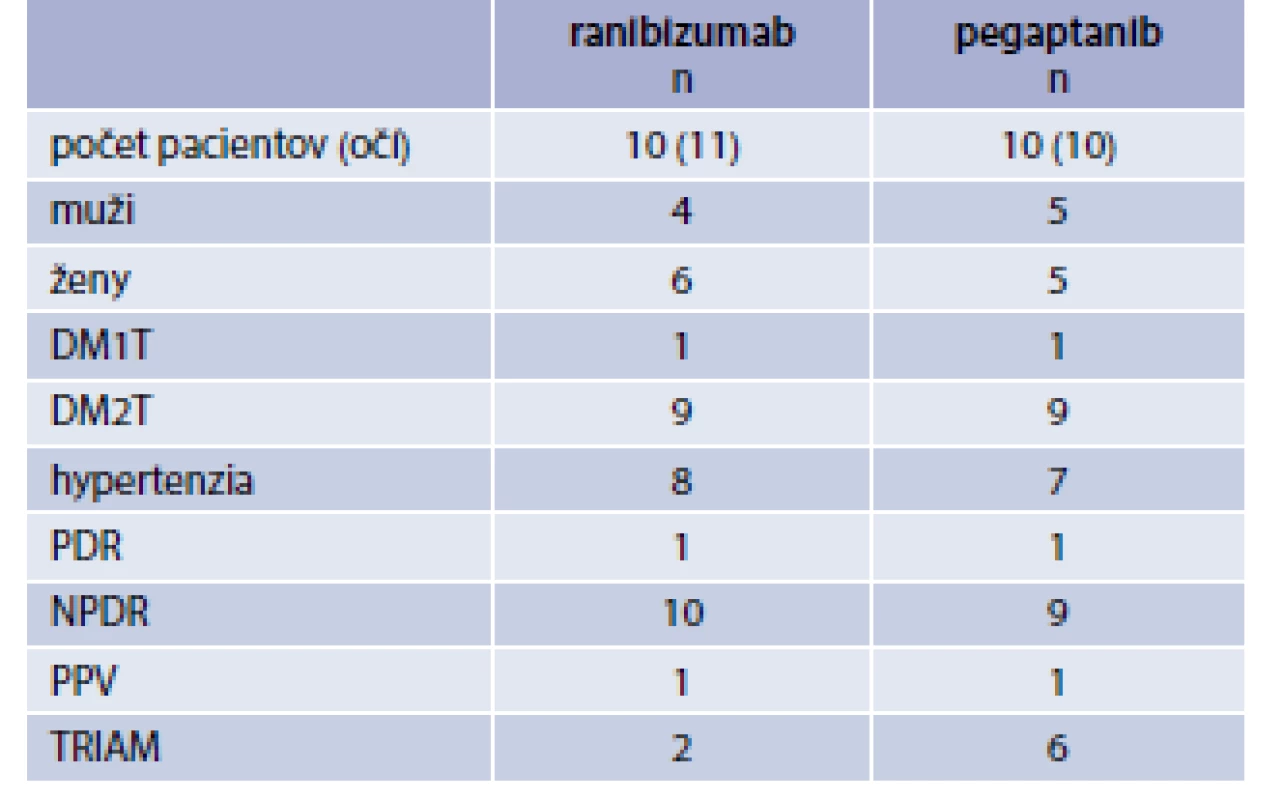
DM1T/DM2T – diabetes 1./2. typu NPDR – neproliferatívna diabetická retinopatia PDR – proliferatívna diabetická retinopatia PPV – pars plana vitrectomia TRIAM – triamcinolon acetonid Tab. 2. Charakteristika súborov podľa veku, trvania DM, HbA<sub>1c</sub>, dĺžky sledovania a zhoršovania NKCOZ 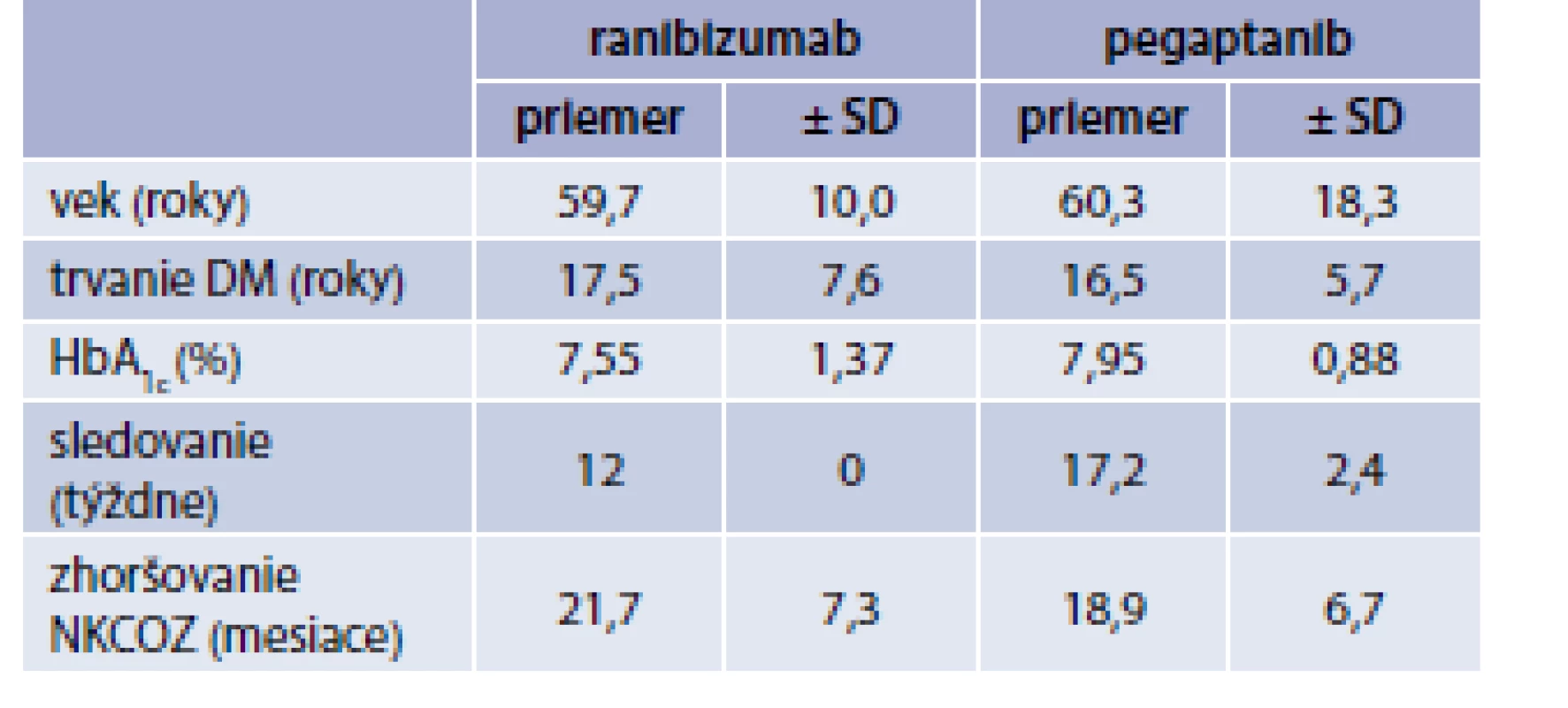
V skupine „Ranibizumab“ bola priemerná vstupná NKCOZ 51,9 písmena, CMT 553,5 µm a objem makuly 10,7 mm3. Po 4 týždňoch bola priemerná zmena NKCOZ +11,1 písmena, pokles CMT o -174,9 µm a objemu o -1,8 mm3.Po 8 týždňoch tento trend pokračoval a NKCOZ sa zlepšila priemerne o +12,4 písmena, CMT poklesla o -208,4 µm a objem makuly o -2,4 mm3. Po 12 týždňoch bola priemerná výsledná NKCOZ 63 písmena, priemerná zmena vs vstupná NKCOZ +11,1 písmena. Zisk 15 a viac písmen bol u 27,3 %, 10 a viac písmen u 54,5 %, Priemerná CMT bola 424,4 µm, priemerná zmena -129,1 µm, a objem makuly 9,3 mm3, priemerná zmena -1,4 mm3. Aplikovaných bolo 29 injekcií, u 4 očí po úvodných 2 aplikáciách bola liečba prerušená podľa vyššie uvedených kritérií na prerušenie liečby (CMT ≤ 250 µm alebo NKCOZ ≥ 84 písmen). Zlepšenie všetkých sledovaných parametrov vo všetkých sledovaných týždňoch bolo na hladine štatistickej významnosti p < 0,05 (tab. 3).
Tab. 3. Výsledné hodnoty NKCOZ, CMT a objemu makuly v skupine „Ranibizumab“ 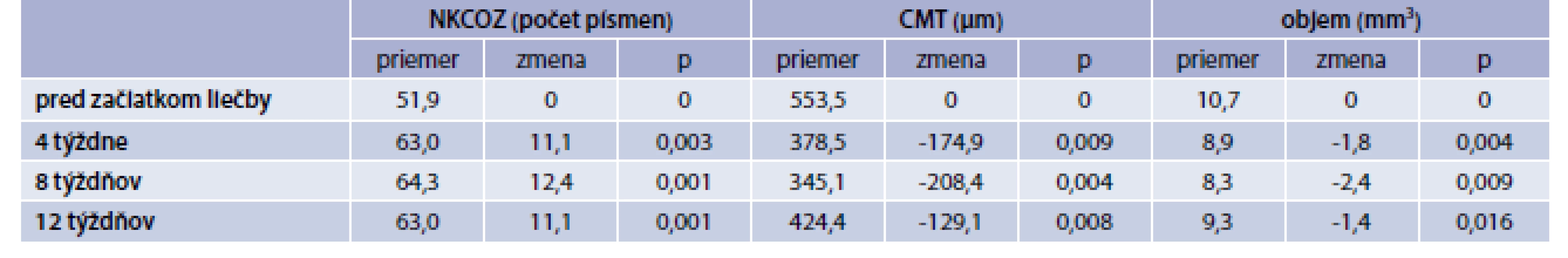
V súbore „Pegaptanib“ bola priemerná vstupná NKCOZ 54,1 písmena, CMT 499,6 µm a objem makuly 10,4 mm3. V 6. týždni sme zaznamenali len mierne zlepšenie NKCOZ o 0,2 písmena, V 12. týždni NKCOZ poklesla o -1,4 písmena a výsledná COZ v 18. týždni bola +2,8 písmena. V 18 týždňoch bola priemerná CMT 486,0 µm, priemerná zmena -13,6 µm, a objem makuly 9,8 mm3, priemerná zmena -0,6 mm3. V súbore „Pegaptanib“ bolo aplikovaných 29 injekcií. V tejto skupine jeden pacient zomrel na kardiálne zlyhanie po 10 týždňoch od zaradenia do sledovania. V 18. týždni bolo hodnotených 9 očí. V danom súbore sme ani v jednom parametre nezaznamenali štatisticky významnú zmenu p < 0,05 (tab. 4).
Tab. 4. Výsledné hodnoty NKCOZ, CMT a objemu makuly v skupine „Pegaptanib“ 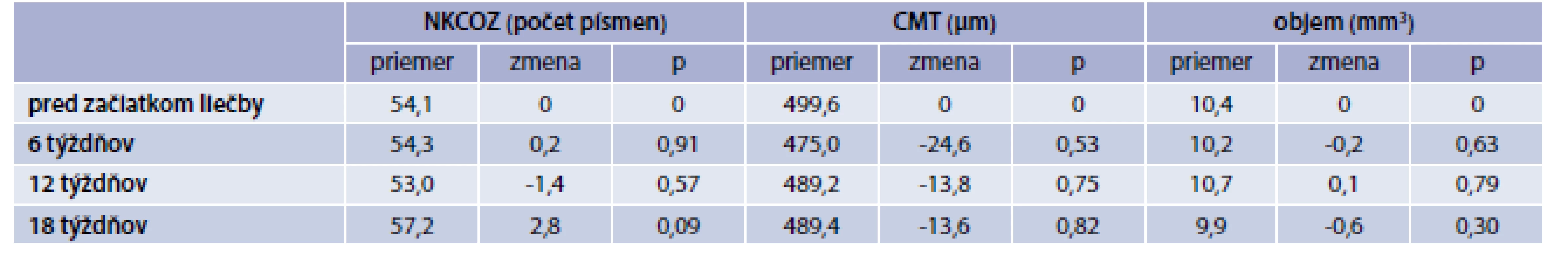
Priemerný zisk ≥ 15 písmen v súbore „Ranibizumab“ bola 27,3 %, v súbore „Pegaptanib“ 0 %, zisk ≥ 10 písmen 54,5 %, resp. 10 % a zisk ≥ 1 písmeno 100 %, resp. 60 % (tab. 5).
Tab. 5. Porovnanie skupín a výsledná NKCOZ 
Nepozorovali sme žiadnu závažnú očnú komplikáciu (endoftalmitídu alebo odlúčenie sietnice). Jeden pacient v súbore „Pegaptanib“ zomrel 10 týždňov od začatia liečby na kardiálne zlyhanie.
Porovnanie zmeny NKCOZ, CMT a objemu makuly k vstupným hodnotám uvádzajú grafy 1, 2 a 3.
Graf 1. Zmena najlepšej korigovanej centrálnej ostrosti zraku (počet písmen) 
Graf 2. Zmena centrálnej hrúbky makuly (μm) 
Graf 3. Zmena objemu makuly (mm<sup>3</sup>) 
Diskusia
Cievny endotelový rastový faktor je najdôležitejší stimulus pre vznik DEM [10]. Vzniká následkom zrútenia hematookulárnej bariéry a spôsobuje zhrubnutie sietnice v makule v dôsledku hromadenia tekutiny v sietnici. Primárnym endogénnym mediátorom DEM je VEGF, glykoproteín, ktorý sa tvorí v endotelových bunkách sietnice (REC), pericytoch a pigmentovom epiteli sietnice. Cievny endotelový rastový faktor kontroluje permeabilitu endotelových buniek v sietnici naväzovaním na receptor VEGF2. Prvým krokom pri vzniku DEM je pravdepodobne dysfunkcia REC. Hyperglykémia a následná hypoxia pri diabetickej retinopatii zvyšujú hladiny VEGF [2].
V preklinických štúdiách Deissler a Lang [12,13] realizovali in vitro štúdie na bovinných endotelových bunkách sietnice (bREC), skúmali VEGF – stimulovaný proces v REC a chceli zistiť, či môže byť tento proces zmenený účinkom ranibizumabu. V bielkovinových zlúčeninách REC zistili vysoké hodnoty VEGF165 – najdôležitejšej substancie zúčastňujúcej sa na vzniku opuchu makuly a proliferatívnej retinopatie. Pevné spojenia REC reprezentujú vnútornú hematookulárnu bariéru, ktorá sa skladá z rôznych proteínov, napríklad okludín, zonula occludens proteín (ZO-1) a klaudínov. Autori sledovali, že v prítomnosti VEGF165 klaudín-1 a okludín vymizli, pričom koncentrácia ostatných proteínov pevného spojenia REC, ako napr. ZO-1 klaudínu 5 sa menila len nevýrazne. Molekuly klaudínu 1 a okludínu sa presúvali z plazmatickej membrány do cytoplazmy REC. Po pridaní ranibizumabu do média s bunkami REC sa tento transfer zastavil a na základe týchto výsledkov predpokladajú, že klaudín 1 je jedným z najdôležitejších proteínov vnútornej hematookulárnej bariéry. Tieto výsledky podporujú používanie ranibizumabu v liečbe DEM.
My sme sa v našom sledovaní rozhodli porovnať účinok dvoch blokátorov VEGF – ranibizumabu a pegaptanibu sodného, ktoré v čase realizácie tohto sledovania boli jediné antiVEGF látky dostupné na trhu a používané v liečbe vlhkej formy vekom podmienenej degenrácie makuly.
Pegaptanib sodný je aptamér RNA, ktorý sa selektívne viaže na VEGF165 [14]. Do dvojito zaslepenej multicentrickej randomizovanej placebom kontrolovanej štúdie fáza 2/3 pri DEM bolo zaradených 260 a 207 očí, ktorí boli rozdelené do 4 liečebných skupín: pegaptanib sodný 0,3 mg, 1 mg, 3 mg alebo placebo. Pegaptanib sodný alebo placebo injekcia boli aplikované každých 6 týždňov. Od 18. týždňa bola povolená fokálna/mriežková laserkoagulácia, ak bola nutná podľa rozhodnutia investigátora. V 2. roku sledovania bolo možné prerušiť liečbu, ak boli CMT ≤ 175 µm a NKCOZ ≥ 20/25. Tieto údaje sme my pri zaraďovaní pacientov do sledovania nemali k dispozícii. Spolu 49 očí (36,8 %) liečených pegaptanibom sodným a 25 očí (19,7 %) liečených placebom získalo ≥ 10 písmen v prvom roku sledovania, v druhom roku sledovania 38,3 % a 30,0 %. Zmena NKCOZ od začiatku liečby do 2. roka bola vyššia pri liečbe pegaptanibom sodným ako placebom (p < 0,05). Priemerný zisk písmen v 54. týždni bol +5,2 a v 102. týždni +6,1 písmena vs +1,2 a +1,3 písmena skupine liečených placebom. Pokles CMT ≥ 50 % bol u 19,2 % liečených pegaptanibom sodným a 26,1 % liečených placebom. Signifikantne menej očí pri liečbe pegaptanibom sodným potrebovalo doplňujúcu fokálnu alebo mriežkovú laserkoaguláciu. Pegaptanib sodný bol dobre tolerovaný a výskyt nežiadúcich účinkov bol porovnateľný v obidvoch súboroch [7].
Ranibizumab je rekombinantná humánna monoklonová protilátka, fragment, ktorá inhibuje všetky formy VEGF-A. Bolo zrealizovaných viacero veľkých štúdií, v ktorých bol sledovaný pozitívny vplyv ranibizumabu na DEM [8–11].
V štúdii Restore [11] boli pacienti rozdelení do 3 skupín: ranibizumab 0,5 mg, ranibizumab 0,5 mg + laserkoagulácia a laserkoagulácia. Po úvodných 3 injekciách ranibizumabu v ramene ranibizumab a v kombinácii s laserkoaguláciou boli injekcie aplikované do stabilizácie nálezu. Priemerný zisk písmen v jednotlivých ramenách bol +6,1, +5,9 a +0,8 písmena. Na OCT bol priemerný pokles hrúbky sietnice -128,3 µm, -118,7 µm a -61,3 µm. V skupine ranibizumab v monoterapii bol zisk ≥ 15 písmen v 22,6 %, v kombinovanom ramene 22,9 % oproti 8,2 % liečených laserkoaguláciou [11]. Po troch rokoch sledovania stále pretrvával benefit liečby ranibizumabom [15]. Štúdia Diabetic Retinopathy Clinical Research Network (DRCR.net) [6] mala o niečo komplikovanejší design, nakoľko sa ukázalo, že režim mesačných aplikácií je veľmi ťažko dodržateľný v klinickej praxi. Do sledovania bolo zaradených 854 pacientov, ktorí boli rozdelení do 4 skupín: laserkoagulácia; 0,5 mg ranibizumab plus promptný laser; 0,5 mg ranibizumab plus odložená laserkoagulácia (v 24. týždni a neskôr) a 4 mg triamcinolone plus promptný laser [6]. Na základe výsledkov v 3. roku môžeme predpokladať, že skoré zahájenie laserkoagulácie makuly pri liečbe blokátormi VEGF nevedie k zlepšeniu videnia, naopak, môže v niektorých prípadoch zhoršiť výslednú NKCOZ. V skupine s odloženou laserkoaguláciou bolo zlepšenie o 10 a viac písmen u 47 pacientov a zhoršenie o 10 a viac písmen u 5 %, avšak v skupine s promptnou laserkoaguáciou zlepšenie o 10 a viac písmen len u 42 % a zhoršenie o 10 a viac písmen u 10 % [16].
V našom sledovaní boli oči rozdelené do 2 skupín podľa aplikovanej látky – do skupiny „Ranibizumab“ (ranibizumab 0,5mg) alebo do skupiny „Pegaptanib“ (pegaptanib sodný 0,3mg). Pacienti boli hodnotení po 12 (ranibizumab) alebo 18 týždňoch (pegaptanib sodný) podľa známych vedomostí o farmakokinetike jednotlivých liečiv. V skupine liečených ranibizumabom sme pozorovali rýchlejšie a výraznejšie zlepšenie NKCOZ, CMT a objemu makuly. Pri pegaptanibe sodnom bolo toto zlepšenie oveľa menej výrazne. V skupine ranibizumab už po jednej aplikácii nastalo výrazné zlepšenie NKCOZ o +11,1 písmena (p = 0,003), pokles CMT o -174,9 µm (p = 0,009) a objemu makuly -1,8 mm3 (p = 0,004). V 8. týždni nastalo ďalšie zlepšenie NKCOZ +12,4 písmena (p < 0,001), CMT -208,4 µm (p < 0,001), objem makuly o -2,4 mm3 (p = 0,009). Po 12 týždňoch bola priemerná zmena vs vstupná NKCOZ +11,1 písmena (p = 0,001), priemerná zmena CMT -135,9 µm (p = 0,008), a priemerná zmena objemu makuly -1,62 mm3 (p = 0,016). Pri liečbe pegaptanibom sodným zraková ostrosť sa len pozvoľna menila a táto zmena nebola štatisticky signifikantná, NCOZ +0,4; -1,4; +2,8 v 6., 12. a 18. týždni (p = 0,91; 0,57 a 0,09). Taktiež zmena CMT a objemu makuly bola oveľa pomalšia.
U 4 pacientov v skupine „Ranibizumab“ sme dosiahli už počas úvodnej nasycovacej dávky CMT ≤ 250 µm alebo NKCOZ ≥ 84 písmen a liečba bola prerušená. Aj tento fakt potvrdzuje výraznejší účinok ranibizumabu na zlepšenie NKCOZ a vstrebanie edému oproti pegaptanibu.
Dosiahnuté výsledky v liečbe ochorení sietnice blokátormi VEGF otvárali dvere pre nové preparáty. Aflibercept je ďalší preparát, ktorý v štúdiách preukázal výbornú účinnosť najprv v liečbe vlhkej formy vekom podmienenej degenerácie makuly a následnej sa jeho použitie rozšírilo aj na iné diagnózy [17]. Štúdia VIVID a VISTA [18] u pacientov s DEM potvrdila superioritu afliberceptu 2 mg v skupinách, v ktorých bol podávaný po úvodných 5 mesačných nasycovacích dávkach, buď mesačne 2q4 alebo v dvojmesačných intervaloch 2q8 oproti laserkoagulácii. Po dvoch rokoch v skupine 2q8, ktorá je používaná v liečbe pacientov s DEM afliberceptom, bol zisk písmen vo VIVID +9,4 písmena a VISTA +11,1 písmena [18].
Pacienti s diabetom majú spolu s očnými komplikáciami aj rôzne systémové komplikácie, najmä zvýšené riziko kardiovaskulárnych chorôb. Preto bezpečnosť a znášanlivosť tejto liečby je veľmi dôležitá. V klinických štúdiách zaoberajúcich sa liečbou ranibizumabom a pegaptanibom sodným neboli zistené závažnejšie nežiadúce účinky. Incidencia celkových závažných nežiadúcich účinkov v štúdii RESOLVE bola 13,7% a 12,2% pri liečbe ranibizumabom a placebom a 12,2%, 5,8% a 10% pri monoterapii ranibizumabom, v kombinácii a v monoterapii s laserom v štúdii RESTORE [8,11]. Pegaptanib sodný vykazoval v štúdiách pri vekom podmienenej degenerácii makuly veľmi dobrý bezpečnostný profil a tento trend bol potvrdený aj pri DEM [7,14]. V našom sledovaní bol ranibizumab dobre tolerovaný a neboli zaznamenané žiadne závažné vedľajšie účinky. Jeden pacient, ktorému boli aplikované injekcie pegaptanibu sodného, zomrel na kardiálne zlyhanie po podaní 2 injekcií 10 týždňov od začiatku liečby. Tento pacient už v minulosti prekonal infarkt myokardu.
Výsledky tohto sledovanie potvrdili účinok ranibizumabu pri DEM už po úvodných dávkach. Limitáciou tohto sledovania je malý súbor pacientov. Avšak vzhľadom obmedzenú dostupnosť blokátorov VEGF v liečbe DEM v čase realizovania tohto projektu, nebolo možné zaradiť väčší počet pacientov.
Záver
Diabetický edém makuly je závažnou príčinou poklesu NKCOZ. Laserkoagulácia makuly bola v minulosti štandardom liečby tohto ochorenia. Súčasné štúdie a už aj klinická prax potvrdzujú pozitívny vplyv blokátorov VEGF na NKCOZ a edém makuly ako primárnu liečbu v kombinácii s laserkoaguláciou.
V nami sledovaných malých súboroch u pacientov s DEM ranibizumab 0,5 mg preukázal vyššiu účinnosť v sledovanom období.
Doručené do redakcie 30. 12. 2016
Prijaté po recenzii 17. 2. 2017
MUDr. Jana Štefaničková, PhD.
jstefanicka@gmail.com
www.unb.sk
Zdroje
1. Photocoagulation for diabetic macular edema. Early Treatment Diabetic Retinopathy Study report number 1. Early Treatment Diabetic Retinopathy Study research group. Arch Ophthalmol 1985; 103(12): 1796–1806.
2. Lang GE. Diabetic macular edema. Ophthalmologica 2012; 227(Suppl 1): 21–29. Dostupné z DOI: <http://dx.doi.org/10.1159/000337156>.
3. Joussen AM, Smyth N, Niessen C. Pathophysiology of diabetic macular edema. Dev Ophthalmol 2007; 39 : 1–12.
4. Treatment techniques and clinical guidelines for photocoagulation of diabetic macular edema. Early Treatment Diabetic Retinopathy Study Report Number 2. Early Treatment Diabetic Retinopathy Study Research Group. Ophthalmology 1987; 94(7): 761–774.
5. Sosna T, Bouček P, Fišer I. Diabetická retinopatie, diagnostika, prevence a léčba. Cendelín: Praha 2001.
6. Elman MJ, Aiello LP, Beck RW et al. [Diabetic Retinopathy Clinical Research Network]. Randomized trial evaluating ranibizumab plus prompt or deferred laser or triamcinolon plus prompt laser for diabetic macular edema. Ophthalmology 2010; 117(6): 1064–1077. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ophtha.2010.02.031>.
7. Sultan MB, Zhou D, Loftus J et al. A phase 2/3 multicenter randomized double masked 2 – year trial of pegaptanib sodium for the treatment of diabetic macular edema. Ophthalmology 2011;118(6): 1107–1118. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ophtha.2011.02.045>.
8. Massin P, Bandello F, Garweg JG et al. Safety and efflicacy of ranibizumab in diabetic macular edema (RESOLVE Study): a 12-month, randomized, controlled, double-masked, multicenter phase II study. Diabetes Care 2010; 33(11): 2399–2405. Dostupné z DOI: <http://dx.doi.org/10.2337/dc10–0493>.
9. Nguyen QD, Shah SM, Heier JS et al. Primary end point (six months) results of the ranibizumab for edema of the macula in diabetes (READ-2) Study. Ophthalmology 2009; 116(11): 2175–2181.e1.Dostupné z DOI: <http://dx.doi.org/10.1016/j.ophtha.2009.04.023>.
10. Nguyen QD1, Tatlipinar S, Shah SM et al. Vascular endothelial growth factor is a critical stimulus for diabetic macular edema. Am J Ophthalmol 2006;142(6): 961–969.
11. Mitchell P, Bandello F, Schmidt-Erfurth U et al. The RESTORE study: ranibizumab monotherapy or combined with laser versus laser monotherapy for diabetic macular edema. Ophthalmology 2011; 118(4): 615–625. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ophtha.2011.01.031>.
12. Deissler HL, Lang GE. In vitro studies on the mechanism of action of VEGF and its inhibitors. Klin Monatsbl Augenheilkd 2008; 225(7): 623–628. Dostupné z DOI: <http://dx.doi.org/10.1055/s-2008–1027513>.
13. Deissler H, Deissler H, Lang S et al. VEGF – induced effects on proliferation, migration and tight junctions are restored by ranibizumab (Lucentis) in microvascular retinal endothelial cells. Br J Ophthalmol 2008; 92(6): 839–843. Dostupné z DOI: <http://dx.doi.org/10.1136/bjo.2007.135640>.
14. Gragoudas ES, Adamis AP, Cunningham ET Jr et al. Pegaptanib for neovascular age-related macular degeneration. N Engl J Med 2004; 351(27): 2805–2816.
15. Schmidt-Erfurth U, Lang GE, Holz FG et al. Three – year outcomes of individualized ranibizumab treatment in patients with diabetic macular edema: the RESTORE extension study. Ophthalmology 2014; 121(5): 1045–1053. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ophtha.2013.11.041>.
16. Elman MJ, Qin H, Aiello LP et al. [Diabetic Retinopathy Clinical Research Network]. Intravitreal Ranibizumab for diabetic macular edema with prompt versus deferred laser treatment: 3 – year randomized trial results. Ophthalmology 2012; 119(11): 2312–2318. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ophtha.2012.08.022>.
17. Heier JS, Brown DM, Chong V et al. Intravitreal Aflibercept (Trap –Eye) inwet age – related macular degeneration. Ophthalmology 2012; 119(12): 2537–2548. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ophtha.2012.09.006>. Erratum in Ophthalmology 2013;120(1): 209–2010.
18. Korobelnik JF, Do DV, Schmidt-Erfurth U et al. Intravitreal aflibercept for diabetic macular edema. Ophthalmology 2014;121(11): 2247–2254. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ophtha.2014.05.006>.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článek EditorialČlánek Z odbornej literatúry
Článok vyšiel v časopiseForum Diabetologicum
Najčítanejšie tento týždeň
2017 Číslo 1- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Statinová intolerance
- Genetický podklad a screening familiární hypercholesterolémie
- Metabolit živočišné stravy produkovaný střevní mikroflórou zvyšuje riziko závažných kardiovaskulárních příhod
-
Všetky články tohto čísla
- Angio OCT – nová neinvazívna zobrazovacia vyšetrovacia metóda diagnostiky a monitoringu diabetickej retinopatie
- Porovnanie účinnosti ranibizumabu a pegaptanibu sodného v liečbe diabetického edému makuly
- Autoimunita a diabetes mellitus
- Editorial
- Diabetes mellitus a dermatologické ochorenia
- Nastal čas pre redukciu ischemickej choroby srdca pomocou ovplyvnenia sérového Lp(a)?
- Ako monitorovať detského pacienta a adolescenta s diabetickou retinopatiou: kazuistika 20-ročnej pacientky a angio OCT
- Katarakta u pacienta s vrodeným deficitom galaktokinázy: kazuistika
- Z histórie diabetológie – humanizmus a renesancia (pokračovanie)
- Z odbornej literatúry
- Metabolické choroby a oko v detskom veku
- Forum Diabetologicum
- Archív čísel
- Aktuálne číslo
- Informácie o časopise
Najčítanejšie v tomto čísle- Angio OCT – nová neinvazívna zobrazovacia vyšetrovacia metóda diagnostiky a monitoringu diabetickej retinopatie
- Autoimunita a diabetes mellitus
- Metabolické choroby a oko v detskom veku
- Diabetes mellitus a dermatologické ochorenia
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



