-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Senzibilizace polytransfundovaných hematologických pacientů alogenními erytrocytovými a HLA antigeny
Prevalence of red blood cell and HLA antibodies in multi-transfused haematological patients
Blood transfusions represent an integral part of the treatment of haematological patients. One of the side effects of this therapy is the possible alloimmunisation of recipients to donor blood cell antigens, which may complicate subsequent transfusion therapy. A retrospective analysis of 100 multiply transfused haematological patients was performed. The aim of this study was to establish the prevalence of anti-red-blood cell and anti-HLA antibodies in these patients. Column agglutination methods in NAT and the enzyme test were used for screening and identification of red blood cell antibodies. The standard complement-dependent lymphocytotoxicity test (CDC-NIH) and ELISA techniques were used for screening of HLA antibodies: QuikScreen [GTI] for HLA class I antibodies detection (IgG and IgM), B-Screen [GTI] for HLA class II antibodies detection (IgG). Kit Quik-ID Class I GTI for HLA class I (IgG) antibodies. The prevalence of HLA and/or red-blood-cell alloimmunisation in our studied group was 29%. 11% of patients developed antibodies against red-blood-cell antigens, 23% of patients developed anti-HLA antibodies. The degree of immunisation differed according to gender: the prevalence of antibodies against red-blood-cell was 6.5% in women and 14.8% in men (this difference was not statistically significant). The prevalence of anti-HLA antibodies was significantly higher in women compared to men (32.6% versus 14.8%; p=0.035).
Key words:
alloimmunisation to red blood cell antigens, alloimmunisation to HLA antigens, platelet refractoriness, post transfusion reactions
Autori: H. T. Bolcková; E. Matějková; M. Písačka; Z. Gašová; M. Böhmová; Z. Bhuiyanová; J. Žlabová; J. Čermák; A. Vítek
Pôsobisko autorov: Ústav hematologie a krevní transfuze, Praha
Vyšlo v časopise: Transfuze Hematol. dnes,18, 2012, No. 1, p. 25-30.
Kategória: Souhrnné práce, původní práce, kazuistiky
Súhrn
Podávání transfuzních přípravků je nedílnou součástí léčby hematologických pacientů. Přítomnost protilátek proti alogenním antigenům krevních buněk u příjemce může transfuzní terapii komplikovat. Byla provedena retrospektivní analýza 100 polytransfundovaných hematologických pacientů ÚHKT s cílem zjistit u nich míru senzibilizace alogenními erytrocytovými a HLA antigeny. Pro screening a identifikaci erytrocytových protilátek byl použit NAT test a enzymový test v systému sloupcové aglutinace. Pro detekci HLA protilátek byl použit lymfocytotoxický test (LCT-NIH) a ELISA kity: QuikScreen [GTI] pro detekci HLA protilátek I. třídy (IgG a IgM) a B-Screen [GTI] pro detekci HLA protilátek II. třídy (IgG), pro identifikaci a určení % PRA (panel reactive antibody) HLA I. třídy (IgG) byl použit kit Quik-ID Class I [GTI]. Celkem bylo imunizováno alogenními erytrocytovými a/nebo HLA antigeny 29 % pacientů. Alogenními antigeny erytrocytů bylo imunizováno 11 % pacientů, HLA antigeny bylo imunizováno 23 % pacientů. Míra imunizace se lišila podle pohlaví: HLA antigeny se statisticky významně více imunizovaly ženy než muži (32,6 % versus 14,8 %; p = 0,035), erytrocytovými antigeny se imunizovalo více mužů než žen (14,8 % versus 6,5 %), tento rozdíl nebyl statisticky významný.
Klíčová slova:
aloimunizace erytrocytovými antigeny, aloimunizace HLA antigeny, refrakternost na podání trombocytů, potransfuzní reakceÚvod
Transfuzní terapie je nedílnou součástí léčby hematologických pacientů. Imunizace příjemce antigeny krevních buněk, jako jeden z vedlejších účinků transfuzí nebo u žen během těhotenství, může tuto terapii komplikovat.
Přítomnost aloprotilátky proti erytrocytům u příjemce vyžaduje podání erytrocytového přípravku bez příslušného antigenu. Výběr takového přípravku může být v závislosti na specifitě a četnosti protilátek časově náročný proces zahrnující typování dostupných přípravků a hledání kompatibilního dárce v národních případně i mezinárodních registrech dárců krve.
Anti-HLA protilátky u příjemce mohou způsobit refrakternost na podání trombocytů (1), febrilní nehemolytickou potransfuzní reakci (2), akutní a pozdní hemolytické reakce (3) a ve vzácných případech také TRALI (4). Screening HLA protilátek není běžnou součástí předtransfuzního vyšetření, na přítomnost těchto protilátek často upozorní až výskyt potransfuzních reakcí, mohou na ně také ukazovat nespecifické reakce při vyšetřování protilátek proti erytrocytům.
Cílem této studie bylo zjistit míru senzibilizace alogenními erytrocytovými a HLA antigeny u polytransfundovaných hematologických pacientů ÚHKT.
Materiál a metodika
Charakteristika souboru
Byla provedena retrospektivní analýza 100členné skupiny hematologických pacientů ÚHKT, kteří byli v období mezi lednem 2009 a květnem 2010 hospitalizováni na lůžkových odděleních ÚHKT a dostali alespoň 9 transfuzních jednotek (T.U.) nebo terapeutických dávek erytrocytů a/nebo trombocytů.
Ve vyšetřovaném souboru bylo 54 mužů a 46 žen, z těchto žen mělo 44 v anamnéze graviditu. 26 pacientů podstoupilo alogenní transplantaci kostní dřeně nebo krvetvorných buněk (14 mužů, 12 žen), doba mezi transplantací a odběrem vzorku byla 4 dny až 46 měsíců s mediánem 2 měsíce.
Tito pacienti dostali v ÚHKT od 9 do 278 transfuzních jednotek nebo terapeutických dávek deleukotizovaných erytrocytových a trombocytových koncentrátů s mediánem počtu podaných jednotek/ terapeutických dávek 67, délka jejich transfuzní terapie v ÚHKT se pohybovala od 11 dnů do 62 měsíců s mediánem 26,5 měsíce. Počet podaných erytrocytových přípravků byl 0 až 131 s mediánem 22.
V ÚHKT se deleukotizují všechny vyrobené erytrocytové a trombocytové koncentráty. Deleukotizace erytrocytových koncentrátů z plné krve a deleukotizace trombocytových koncentrátů připravených technikou hemaferézy se provádí v den výroby buď filtračními technikami, nebo centrifugací. Trombocytové koncentráty připravené z buffy-coatu se deleukotizují v průběhu pětidenní doby uchovávání těchto transfuzních přípravků. Deleukotizace se provádí filtračními postupy.
Sledovaní pacienti byli v ÚHKT transfundováni výhradně deleukotizovanými koncentráty erytrocytů a trombocytů.
Počty leukocytů ve všech deleukotizovaných typech transfuzních přípravků byly nižší než 1x106. Transfuzní přípravky vyhověly tomuto požadavku ve 100% testovaných přípravků. Obsah přimísených leukocytů a parametry účinných krevních složek v jednotlivých přípravcích splňovaly požadavky Doporučení Rady Evropy a vyhlášky 143/2008 Sb. (5).
Transfuzní anamnéza těchto pacientů před přijetím do ÚHKT není známa.
Metody
Pro detekci anti-HLA protilátek byl použit lymfocytotoxický test (LCT-NIH) se 40 HLA otypovanými dárci (6) a ELISA kity: QuikScreen [od firmy GTI] pro detekci anti-HLA protilátek I. třídy (IgG a IgM) a B-Screen [od firmy GTI] pro detekci anti-HLA protilátek II. třídy (IgG), pro identifikaci anti-HLA protilátek I. třídy (IgG) a určení % panel reactive antibody (PRA) byl použit kit Quik-ID Class I [od firmy GTI].
Pro screening a identifikaci erytrocytových protilátek byl použit nepřímý antiglobulinový test (NAT) a enzymový test v systému sloupcové aglutinace.
Metody statistického zpracování
Pro statistickou analýzu kategoriálních (alternativních) veličin byly použity kontingenční tabulky – chí-kvadrát test nezávislosti a v případě malých počtů Fisherův přesný test. Pro porovnání kvantitativních veličin v různých skupinách byl použit Wilcoxonův test. Pro odhad procent byly vypočteny exaktní binomické intervaly spolehlivosti. Pro výpočty byl použit statistický program SPSS v 19. Všechny testy byly prováděny na 5% hladině významnosti. Hodnoty p vyšší než 10 % nejsou v textu uvedeny.
Výsledky
Celkem bylo ve skupině vyšetřovaných hematologických polytransfundovaných pacientů senzibilizováno alogenními erytrocytovými a/nebo HLA antigeny 29 pacientů. Z těchto imunizovaných pacientů 17 % (5 pacientů) vytvořilo aloprotilátky proti erytrocytovým i HLA antigenům, 21 % (6 pacientů) vytvořilo aloprotilátky pouze proti erytrocytům, 62 % (18 pacientů) vytvořilo aloprotilátky pouze proti HLA antigenům (graf 1).
Graf 1. Podíl pacientů imunizovaných erytrocytovými a/nebo HLA antigeny v souboru imunizovaných pacientů. 
Imunizace alogenními antigeny erytrocytů
Alogenními antigeny erytrocytů bylo imunizováno 11 % (11/100) pacientů, těmito antigeny se imunizovalo 6,5 % žen a 14,8 % mužů (graf 2).
Graf 2. Imunizace erytrocytovými a HLA antigeny. 
11 imunizovaných pacientů vytvořilo 14 specifických antierytrocytových aloprotilátek (8 pacientů vytvořilo jednu specifickou aloprotilátku, 3 pacienti vytvořili po 2 specifických aloprotilátkách). Detekovali jsme následující specifity aloprotilátek: anti-D (2x), anti-E (4x), anti-C (1x), anti-Cw (1x), anti-K (1x), anti-Fya (2x), anti-Wra (1x), anti-Leb (1x), anti-A1 (1x) (graf 3). Všechny čtyři detekované anti-E aloprotilátky reagovaly pouze v enzymových testech.
Graf 3. Specificita a četnost detekovaných erytrocytových aloprotilátek. 
Imunizace HLA antigeny
HLA antigeny bylo imunizováno 23 % (23/100) pacientů. Protilátky proti HLA antigenům vytvořilo 32,6 % žen a 14,8 % mužů (graf 2).
Ze 23 pacientů s anti-HLA protilátkami 9 % (2 pacienti) bylo pozitivních pouze v LCT testu, 43 % (10 pacientů) bylo pozitivních v LCT i v ELISA testech, 48% (11 pacientů) bylo pozitivních pouze v ELISA testech (graf 4).
Graf 4. Detekované anti-HLA protilátky dle reaktivity v metodách. 
Ze 21 ELISA pozitivních pacientů byly u 38 % (8 pacientů) detekovány IgM anti-HLA protilátky I. třídy, u 24 % (5 pacientů) byly detekovány současně IgM a IgG protilátky anti-HLA I. třídy, u 19 % (4 pacienti) byly detekovány pouze IgG protilátky anti-HLA I. třídy, u 5 % (1 pacient) byly spolu s IgG protilátkami anti-HLA I. třídy detekovány také protilátky anti-HLA II. třídy (IgG), u 14 % (3 pacienti) byly spolu s IgM a IgG protilátkami anti-HLA I. třídy přítomny také protilátky anti-HLA II. třídy (IgG), (graf 5). Protilátky anti-HLA II. třídy byly detekovány pouze u žen.
Graf 5. Detekované ELISA pozitivní anti-HLA protilátky dle třídy. 
U 12 ze 13 pacientů s IgG protilátkami anti-HLA I. třídy reagujících v ELISA testu bylo stanoveno % PRA, to se pohybovalo od 12,5 % do 97,5 % s mediánem 52,5 %, u 10 z nich bylo možno určit specifitu protilátek, v 6 případech byly protilátky namířeny proti HLA antigenům A i B lokusu, ve třech případech pouze proti antigenům A lokusu, v jednom případě pouze proti antigenům B lokusu.
Refrakternost na podání trombocytů u HLA imunizovaných pacientů
U pacientů s anti-HLA protilátkami byla hodnocena odpověď na substituci trombocytů. Vzhledem k retrospektivnímu charakteru studie bylo možno kvantifikovat odpověď na podání trombocytových přípravků pouze pomocí hodnoty PI (platelet increment), což je rozdíl mezi počtem trombocytů před transfuzí a po ní (7). PI byl stanoven z rozdílu krevních obrazů (KO) (nejbližší KO následující po transfuzi – nejbližší KO předcházející transfuzi), potransfuzní KO byl stanoven v době 1 hodina až 22,5 hodin po substituci trombocytů (medián 5,5 hodin), minimální počet hodnocených podání byl 4 (4–13, medián 7), jako refrakterní byla považována podání jejichž PI ≤ 5 (7).
Účinnost substituce trombocytů mohla být hodnocena u 21 z 23 pacientů imunizovaných HLA antigeny (1 pacient byl bez substituce, 1 byl substituován ambulantně a nebyl u něj vyšetřen krevní obraz po substituci). 4 pacienti (19%) nebyli refrakterní, 4 pacienti (19 %) byli refrakterní na 1–25 % podaných přípravků, 4 (19 %) pacienti byli refrakterní na 26–50 % podaných přípravků, 3 pacienti (14 %) byli refrakterní na 51–75 % podaných přípravků, 4 pacienti (19 %) byli refrakterní na 76–99 % podaných přípravků, 2 pacienti (10 %) byli refrakterní na všechna sledovaná podání trombocytů.
Přehled všech imunizovaných pacientů v souboru je uveden v tabulce 1.
Tab. 1. Přehled imunizovaných pacientů. 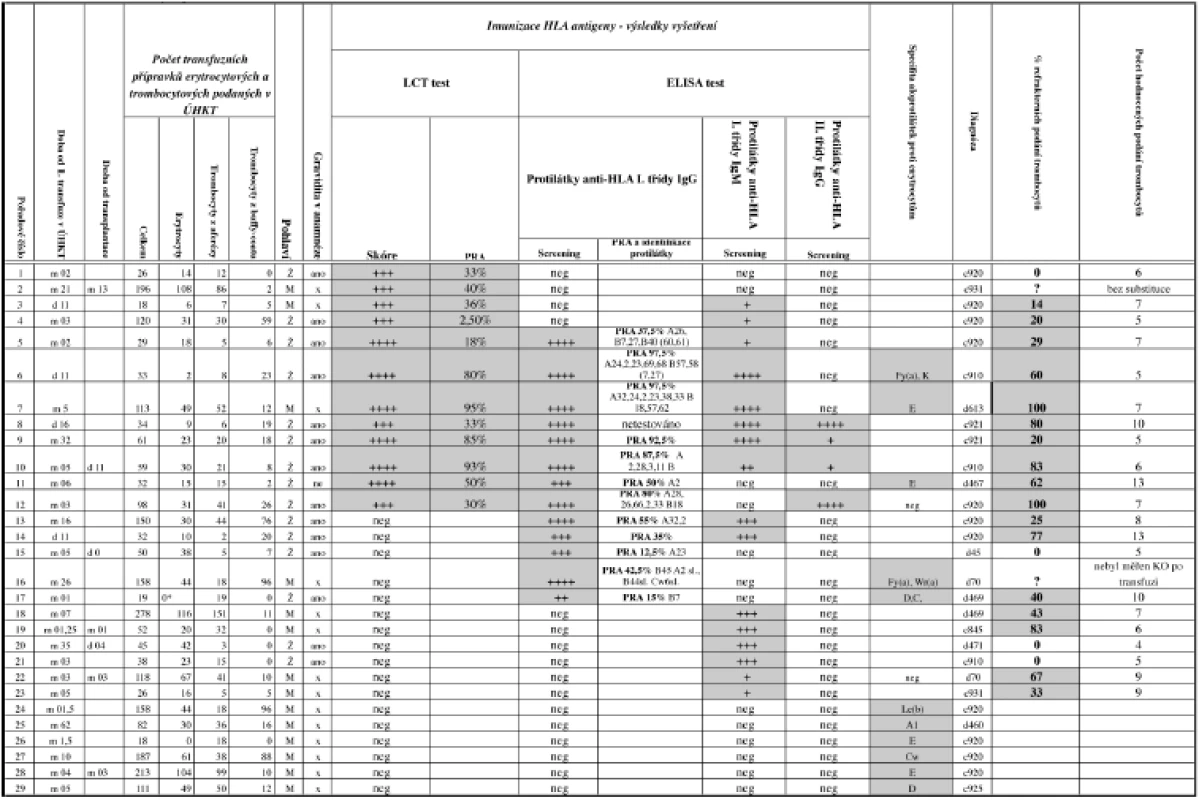
d = den, m = měsíc, Ž = žena, M = muž, KO = krevní obraz * tato pacientka byla již dříve transfundována v jiném zdravotnickém zařízení Diskuse
Ve sledovaném souboru bylo imunizováno antigeny erytrocytů a/nebo HLA antigeny 29 % pacientů, celková míra imunizace se signifikantně nelišila mezi pohlavími (33 % žen versus 26 % mužů). V celém souboru se statisticky významně více pacientů imunizovalo HLA antigeny než erytrocytovými antigeny (23 % versus 11 %; p = 0,0024), rovněž mezi ženami bylo statisticky významně více imunizovaných HLA antigeny než erytrocytovými antigeny (32,6 % versus 6,5 %; p = 0,0016), u mužů v našem souboru nebyl žádný rozdíl v imunizaci HLA nebo erytrocytovými antigeny (14,8% versus 14,8 %).
Zkoumali jsme, zda je rozdíl v imunizaci u různých diagnóz. Mezi nejčetněji zastoupenými diagnózami (akutní myeloidní leukemie: 43 pacientů, akutní lymfoblastická leukemie: 16 pacientů, myelodysplastický syndrom: 12 pacientů) nebyl nalezen statisticky významný rozdíl, ostatní diagnózy nebylo možno hodnotit pro malé četnosti pacientů (tab. 2).
Tab. 2. Zastoupení diagnóz v souboru. 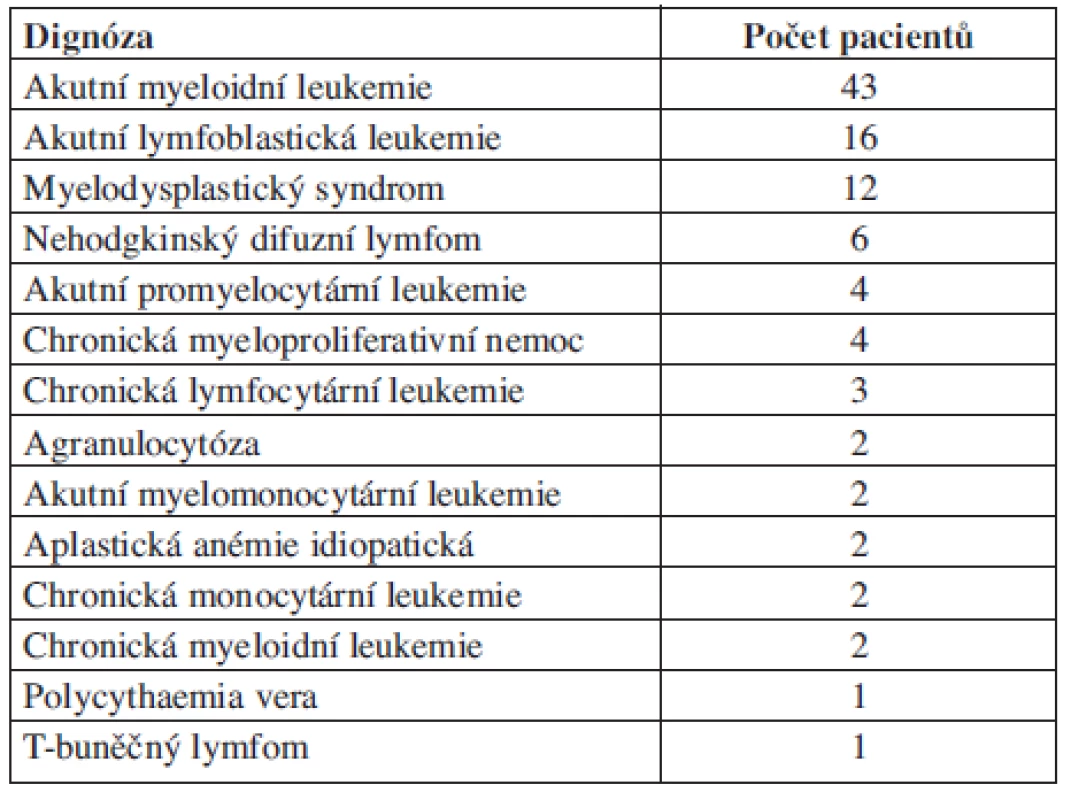
Míra senzibilizace alogenními erytrocytovými antigeny v našem souboru – 11% odpovídá údajům Fluita a spol. (8). V literatuře uváděná míra senzibilizace alogenními erytrocytovými antigeny závisí na délce a intenzitě transfuzní terapie (9), u jednorázových podání při chirurgických výkonech se pohybuje kolem 5,2–5,3 % (10, 11), u polytransfundovaných hematologických pacientů 11,8 % (8), u pacientů na intenzivních a dlouhodobých terapiích erytrocyty 18,9 % (pacienti se srpkovitou anémií a terapií výměnnou erytrocytaferézou) (12). K imunizaci alogenními antigeny erytrocytů mohou přispět i erytrocyty kontaminované trombocytové přípravky (12). Míru imunizace je možno snížit podáváním přípravků shodných v Rh a Kell fenotypu (13). V literatuře není prokazován vliv pohlaví na míru imunizace erytrocytovými antigeny (8), i když se v našem souboru imunizovalo erytrocytovými antigeny více mužů než žen (14,8 % versus 6,5 %) nebyl tento rozdíl statisticky významný.
Míra imunizace HLA antigeny v našem souboru byla 23 %. Ženy se HLA antigeny imunizovaly častěji než muži (32,6 % versus 14,8 %) a tento rozdíl byl statisticky významný (p = 0,035). Ze 13 žen imunizovaných HLA antigeny pouze jediná neměla v graviditě anamnézu. I když výsledek LCT testu byl negativní u všech pacientů na začátku transfuzní terapie v ÚHKT, je možné že u některých z těchto žen mohla být přítomna pouze ELISA pozitivní anti-HLA protilátka indukovaná během gravidity.
V literatuře se míra imunizace HLA antigeny uvádí od 3,1 % do 34 % v závislosti na použité screeningové metodě, na obsahu leukocytů v transfuzních přípravcích a intenzitě transfuzní terapie (10, 11, 14, 15, 16). Je také popsána vyšší míra imunizace HLA antigeny u pacientů s protilátkami proti erytrocytům (10, 11, 14). V našem souboru byla vazba imunizace alogenními antigeny erytrocytů s imunizací HLA antigeny na hranici statistické významnosti (p = 0,061), u žen tato vazba statisticky významná byla (p = 0,030), u mužů nikoliv.
V námi vyšetřovaném souboru pacientů se vyskytovali pacienti pozitivní pouze v jednom z použitých screeningových testů (LCT, ELISA IgG, ELISA IgM). U více než třetiny (38 %) ELISA pozitivních pacientů byly detekovány anti-HLA protilátky třídy IgM. Dostupné ELISA testy detekci IgM protilátek běžně neumožňují, není ani možno tyto protilátky identifikovat.
V našem souboru jsme detekovali protilátky anti-HLA II. třídy pouze u žen, v literatuře byla popsána přítomnost protilátek anti-HLA II. třídy také u mužů (2).
LCT-NIH byl původní sérologickou metodou pro stanovení HLA protilátek, v poslední době se zavádějí další testy (ELISA testy, Luminex, Flow cytometry, MAIPA), tyto testy jsou citlivější, detekují i protilátky, které nejsou schopny vázat a aktivovat komplement.
Z 21 HLA imunizovaných pacientů, u kterých bylo možno hodnotit refrakternost, jich bylo refrakterních 17 (81 %). Zjišťovali jsme zda refrakternost souvisí s pozitivitou v některé z použitých screeningových metod (LCT, ELISA IgG, ELISA IgM). Refrakternost nejvíce predikoval výsledek ELISA IgG testu (p = 0,095). Protilátky detekovatelné ELISA IgG testy mohou mít tedy klinický význam, nicméně refrakterní (i když statisticky nevýznamně) byli i někteří pacienti s pouze IgM protilátkami. IgM protilátky se mohou u polytransfundovaných pacientů vyskytovat ve formě auto - ale i aloprotilátek (17, 18). U sledovaných pacientů nemohly být zcela vyloučeny neimunologické příčiny refrakternosti.
Detekce (resp. identifikace) anti-HLA protilátek u polytransfundovaných pacientů je významnou součástí prevence event. terapie potransfuzních reakcí, zejména refrakternosti na podání trombocytů. Na rozdíl od antierytrocytových protilátek, které se vyšetřují před každým podáním přípravku s obsahem erytrocytů, se anti-HLA protilátky před transfuzemi běžně nevyšetřují. Naše výsledky podporují názor, že doplnění screeningu anti-HLA protilátek u polytransfundovaných pacientů o citlivější ELISA metodu, jak je doporučováno Německou transfuzní společností (19), umožní optimalizovat léčbu u těchto nemocných. Ze stejného důvodu jsou před podáním trombocytů u refrakterních pacientů imunizovaných HLA antigeny zaváděny také trombocytové cross-match testy metodou pevné fáze (ELISA, MAIPA, Capture) (19). Rozšíření registrů HLA otypovaných dárců by umožnilo získat HLA kompatibilní transfuzní přípravky pro větší počet pacientů imunizovaných HLA antigeny.
Závěr
Ve sledovaném souboru se statisticky významně více pacientů imunizovalo HLA antigeny než erytrocytovými antigeny (23 % versus 11 %; p = 0,0024). Také mezi ženami bylo statisticky významně více imunizovaných HLA antigeny než erytrocytovými antigeny (32,6 % versus 6,5 %; p = 0,0016), zatímco u mužů nebyl zjištěn rozdíl v imunizaci HLA nebo erytrocytovými antigeny (14,8% versus 14,8 %).
Ženy byly častěji imunizovány HLA antigeny než muži (32,6 % versus 14,8 %; p = 0,035), u žen byla také statisticky významná vazba mezi imunizací HLA antigeny a imunizací antigeny erytrocytů (ženy s aloprotilátkami proti erytrocytům se častěji imunizovaly HLA antigeny, než ženy bez aloprotilátek proti erytrocytům; p = 0,030).
V našem souboru se vyskytovali i pacienti pozitivní pouze v jednom z použitých screeningových testů (LCT, ELISA IgG, ELISA IgM). Pro sledování HLA imunizace těchto pacientů považujeme za optimální kombinaci obou metod - LCT i ELISA.
Podrobnější zhodnocení klinického významu anti-HLA protilátek detekovaných v různých screeningových testech vyžaduje cílenou prospektivní studii.
Poděkování: RNDr. Bohumíru Procházkovi, CSc. za statistické zpracování dat.
Tato práce vznikla za podpory grantu CEZ 237360001 UHKT
Mgr. Hana Tereza Bolcková
oddělení imunohematologie
Ústav hematologie a krevní transfuze
U nemocnice 1
128 20 Praha 2
e-mail: hana.bolckova@uhkt.cz
Doručeno do redakce: 14. 7. 2011
Přijato po recenzi: 12. 12. 2011
Zdroje
1. Rebulla P. A mini-review on platelet refractoriness. Haematologica 2005; 90 (2): 247–253.
2. Imoto S, Kawamura K, Tokumine Y. Acute non-hemolytic transfusion reactions and HLA class I antibody: advantages of solid phase assay compared with conventional complement-dependent assay. Transfusion Medicine 2010; 20 : 95–103.
3. Benson K, Agosti SJ, Latoni-Benedetti GE, Leparc GF. Acute and delayed hemolytic transfusion reactions secondary to HLA alloimunization. Transfusion 2003; 43(6): 753–7.
4. Ozier Y, Muller JY, Mertes PM, et al. Transfusion-related acute lung injury: reports to the French Hemovigilance Network 2007 through 2008. Transfusion 2011; 51(10): 2102–2110.
5. Guide to the preparation, use and quality assurance of Blood components 15th edition, CE, Strasbourg, Index, 189–242.
6. Terasaki PI, McClelland JD. Microdroplet assay of human serum cytotoxins. Nature 1964; 204 : 998.
7. Bishop JF, Matthews JP, Yuen K, McGrath K, Wolf MM, Szer J. The definition of refractoriness to platelet transfusions. Transfusion Medicine 1992; 2 : 35–41.
8. Fluit CR, Kunst VA, Drenthe-Schonk AM. Incidence of red cell antibodies after multiple blood transfusion. Transfusion 1990; 30(6): 532–535.
9. Zalpuri S, Zwaginga JJ, Cessie S, Elshuis J, Schonewille H, Bom JG: Red-blood-cell alloimmunization and number of red-blood-cell transfusions. Vox Sang 2011 Jul 6. doi: 10.1111/j.1423-0410.2011.01517.
10. Sanz C, Ghita G, Franquet C, Martinez I, Pereira A. Red-blood cell alloimunization and female sex predict the presence of HLA antibodies in patients undergoing liver transplant. Vox Sang 2010; 99(3): 261–6.
11. Van de Watering L, Hermans J, Witvliet M, Versteegh M, Brand A. HLA a RBC immunization after filtered and buffy-coat-depleted blood transfusion in cardiac surgery: a randomized controlled trial. Transfusion 2003; 43(6): 765–71.
12. Kitazawa J, Nollet K, Morioka H, Tanaka K, Inomata M, Kubuki Y, Ohto H. Non-D Rh antibodies appearing after apheresis platelet transfusion: stimulation by red cells or microparticles? Vox Sang 2011; 100(4): 395–400.
13. Godfrey G J, Lockwood W, Kong M, Bertolone S, Raj A. Antibody development in pediatric sickle cell patients undergoing erythrocytapheresis. Pediatr Blood Cancer 2010; 55(6): 1134–7.
14. McPherson ME, Anderson AR, Castillejo MI. HLA alloimmunization is associated with RBC antibodies in multiply transfused patients with sickle cell disease. Pediatr Blood Cancer 2010; 54 (4): 552–558.
15. McKenna D H Jr, Eastlund T, Segall M, Noreen HJ, Park S. HLA alloimmunization in patients requiring ventricular assist device support. J Heart Lung Transplant 2002; 21(11): 1218–24.
16. Ohto H, Nomizu T, Kuroda F, Hoshi T, Rokkaku Y. HLA alloimmunization of surgical patients by transfusion with bedside leukoreduced blood components. Fukushima J Med Sci 2003; 49 (1): 45–54.
17. Laundy GJ, Bradley BA, Rees BM, Younie M, Hows JM. Incidence and specificity of HLA antibodies in multitransfused patients with acquired aplastic anemia. Transfusion 2004; 44 : 814–825.
18. Barocci S, Valente U, Gusmano R, et al. Autoreactive lymphocytotoxic IgM antibodies in highly sensitized dialysis patients waiting for a kidney transplant: identification and clinical relevance. Clin Nephrol 1991; 36(1): 12–20.
19. Cross-Sectional Guidelines for Therapy with Blood Components and Plasma Derivatives. Platelet concentrates. Transf Med Hemother 2009; 36 : 379.
Štítky
Hematológia Interné lekárstvo Onkológia
Článok vyšiel v časopiseTransfuze a hematologie dnes
Najčítanejšie tento týždeň
2012 Číslo 1- Nejasný stín na plicích – kazuistika
- Těžké menstruační krvácení může značit poruchu krevní srážlivosti. Jaký management vyšetření a léčby je v takovém případě vhodný?
- Když se ve střevech děje něco nepatřičného...
- Statinová intolerance
- Význam missense mutací pro tvorbu inhibitoru proti faktoru VIII
-
Všetky články tohto čísla
- Genetické polymorfismy destičkových receptorů u mladých pacientů s akutním infarktem myokardu (AIM) a rezistencí k protidestičkové léčbě
- Žilní trombózy u dětských pacientů s akutní lymfoblastickou leukemií
- Senzibilizace polytransfundovaných hematologických pacientů alogenními erytrocytovými a HLA antigeny
- Význam fyzické aktivity u pacientů s hematoonkologickými malignitami
- Asymptomatický makroadenom hypofýzy komprimující optické chiasma – „incidentalom“ – identifikovaný při diagnostickém stážování nemocného s primárně extranodálním difúzním B-velkobuněčným lymfomem očnice a paranasálních dutin – popis případu
- Vyhlášení ceny firmy Janssen
- Anti-Escherichia coli asparaginase antibody levels determine the activity of second-line treatment with pegylated E. coli asparaginase: a retrospective analysis within the ALL-BFM trials
- Warfarin and acetaminophen interaction: a summary of the evidence and biologic plausibility (Evidence-based focused review)
- Úvodní slova
- VKORC1 and CYP2C9 genotype and patient characteristics explain a large proportion of the variability in warfarin dose requirement among children
- XXVI. Olomoucké hematologické dny
- Pražské hematologické dny
- Mobilizace krvetvorných buněk pomocí plerixaforu - zkušenosti transplantačních center v České republice
- Transfuze a hematologie dnes
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Asymptomatický makroadenom hypofýzy komprimující optické chiasma – „incidentalom“ – identifikovaný při diagnostickém stážování nemocného s primárně extranodálním difúzním B-velkobuněčným lymfomem očnice a paranasálních dutin – popis případu
- Význam fyzické aktivity u pacientů s hematoonkologickými malignitami
- Senzibilizace polytransfundovaných hematologických pacientů alogenními erytrocytovými a HLA antigeny
- Mobilizace krvetvorných buněk pomocí plerixaforu - zkušenosti transplantačních center v České republice
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



