Ultrazvukové mapování žilního systému dolních končetin s ohledem na výskyt a anatomii přední přídatné velké safény
Ultrasound mapping of lower-limb vascular system with regard to occurrence and anatomy of additional front great saphenous vein
A primary survey study involving a set of 113 lower limbs of 66 patients was focused on the prevalence of additional front great saphenous vein (AFGSV) and the measurement of the distance between its start in the great saphenous vein (GSV) and the saphenofemoral junction (SFJ), the measurement of the distance between the passage of AFGSV through the saphenous fascia and its start in GSV, and compared the width of AFGSV anechogenous lumen with the calibre of GSV. The prevalence of AFGSV in the observed set was 42.5%. Reflux was proved in 6 AFGSVs (12.5%). The width of the AFGSV anechogenous lumen was on an average 0.29 cm (M 0.26 cm, SD ± 0.15 cm), and the width of GSV anechogenous lumen measured on lower limbs with simultaneous occurence of AFGSV was 0.38 cm (M 0.38 cm, SD ± 0.11 cm) on an average. Comparison of the anechogenous lumen width of the two veins showed a statistically significant difference (p < 0,001). AFGSV in the observed set of lower limbs started in VS at an average distance of 0.8 cm from the saphenofemoral junction (M 0.8 cm, SD ± 0.46 cm). The minimum start point distance was 0.1 cm, the maximum was 1.84 cm. In 3 cases (6.3%), AFGSV started directly in the common femoral vein (v. femoralis communis), which was the place where also the saphenous vein begins. The distance between the passage of AFGSV through saphenous fascia to upper subcutaneous layers and the start of the vein in GSV was on an average 13.2 cm (M 14.5 cm, SD ± 6.5 cm). The maximum distance between the pasage of AFGSV through saphenous fascia and the start of the vein in GSV was 4 cm, the maximum distance being 30 cm.
Key words:
frontal additional great saphenous vein – great saphenous vein – saphenous compartment – duplex sonography - ultrasound mapping of lower-limb vascular system
Autori:
D. Musil 1,2; J. Herman 3
Pôsobisko autorov:
Nestátní interní a cévní ambulance, II. poliklinika, Olomouc
1; Ústav patofyziologie Lékařské fakulty UP Olomouc, přednosta prof. MUDr. Jaroslav Veselý, CSc.
2; II. chirurgická klinika Lékařské fakulty UP a FN Olomouc, přednosta prof. MUDr. Miloslav Duda, DrSc.
3
Vyšlo v časopise:
Vnitř Lék 2006; 52(12): 1150-1155
Kategória:
Původní práce
Súhrn
Primární průzkumná studie na souboru 113 dolních končetin u 66 pacientů zjišťovala prevalenci přední přídatné velké safény (PPVS), měřila vzdálenost jejího odstupu z velké safény (VS) od safénofemorální junkce (SFJ), měřila vzdálenost místa průniku PPVS safénovou fascií od odstupu žíly z VS a srovnávala šíři anechogenního lumen PPVS s kalibrem VS. Prevalence PPVS v našem souboru byla 42,5 %. Reflux jsme prokázali u 6 PPVS (12,5 %). Šíře anechogenního lumen PPVS byla průměrně 0,29 cm (M 0,26 cm, SD ± 0,15 cm) a šíře anechogenního lumen VS měřená na dolních končetinách se současným výskytem PPVS byla průměrně 0,38 cm (M 0,38 cm, SD ± 0,11 cm). Srovnáním šíře anechogenního lumen obou žil byl zjištěn statisticky významný rozdíl (p < 0,001). PPVS v našem souboru dolních končetin odstupovala z VS v průměrné vzdálenosti 0,8 cm od safénofemorální junkce (M 0,8 cm, SD ± 0,46 cm). Minimální vzdálenost odstupu byla 0,1 cm, maximální vzdálenost 1,84 cm. Ve 3 případech (6,3 %) PPVS odstupovala přímo ze společné stehenní žíly (v. femoralis communis) v místě současného odstupu VS. Průnik PPVS safénovou fascií do vyšších vrstev podkoží jsme pozorovali v průměrné vzdálenosti 13,2 cm (M 14,5 cm, SD ± 6,5 cm) od místa odstupu žíly z VS. Minimální vzdálenost průniku PPVS safénovou fascií od odstupu žíly z VS byla 4 cm, maximální vzdálenost 30 cm.
Klíčová slova:
přední přídatná velká saféna - velká saféna - safénový kompartment - duplexní sonografie - ultrazvukové mapování žil dolních končetin
Úvod
Při předoperačním ultrazvukovém mapování žil dolních končetin je důležité u povrchového žilního systému prokázat nejenom insuficienci velké a malé safény, ale také reflux v nepravidelně se vyskytujících přídatných (variabilních) safénách.
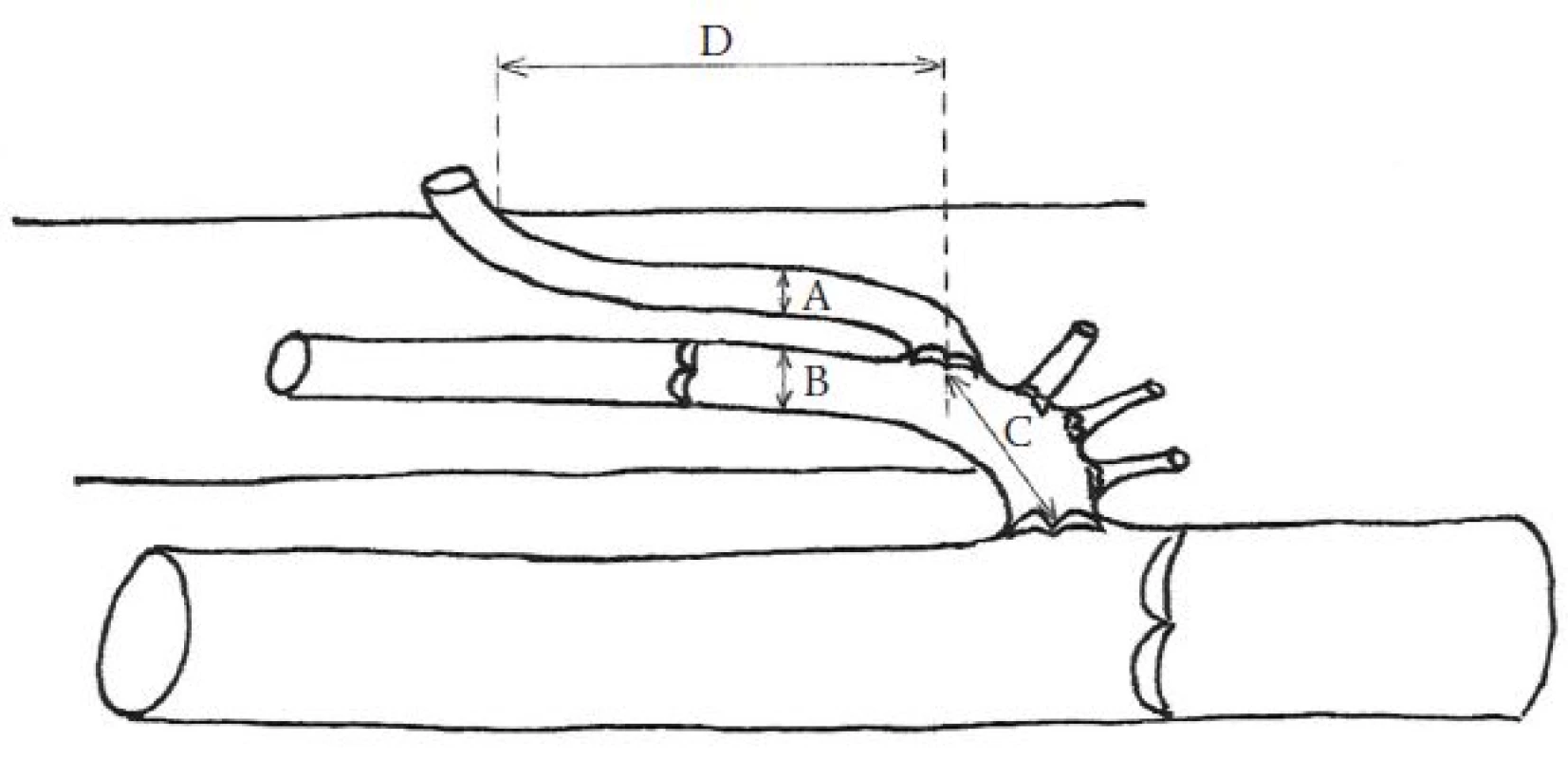
Přídatné safény jsou podkožní žíly, které odstupují ze safén těsně za safénofemorální nebo safénopopliteální junkcí a probíhají paralelně s velkou nebo malou safénou. Jde o kolaterální žíly, paralelní cestu alternativního krevního toku. V případě velké safény (VS) se jedná o přední, zadní a povrchovou přídatnou velkou safénu (vena saphena magna accessoria anterior, posterior et superficialis). Tyto názvy přídatných velkých safén, v rámci nové terminologie žilního systému dolních končetin, byly doporučeny Mezinárodní interdisciplinární komisí zasedající v roce 2001 v Římě u příležitosti 14. světového kongresu IUP (International Union of Phlebology) a posléze oponovány, doplněny a upraveny během 21. světového kongresu IUA (International Union of Angiology) v roce 2004 v Římě [2,3]. Mají nahrazovat a upřesňovat původní termín vena saphena accessoria [1,5], popisující povrchové variabilní žíly na přední, vnitřní a zadní straně stehna probíhající paralelně s velkou safénou a někdy také označované jako vena saphena accessoria medialis et lateralis. Průběh podkožních žil na dolní končetině, pojmenované již podle nové terminologie, ukazuje obr. 1.
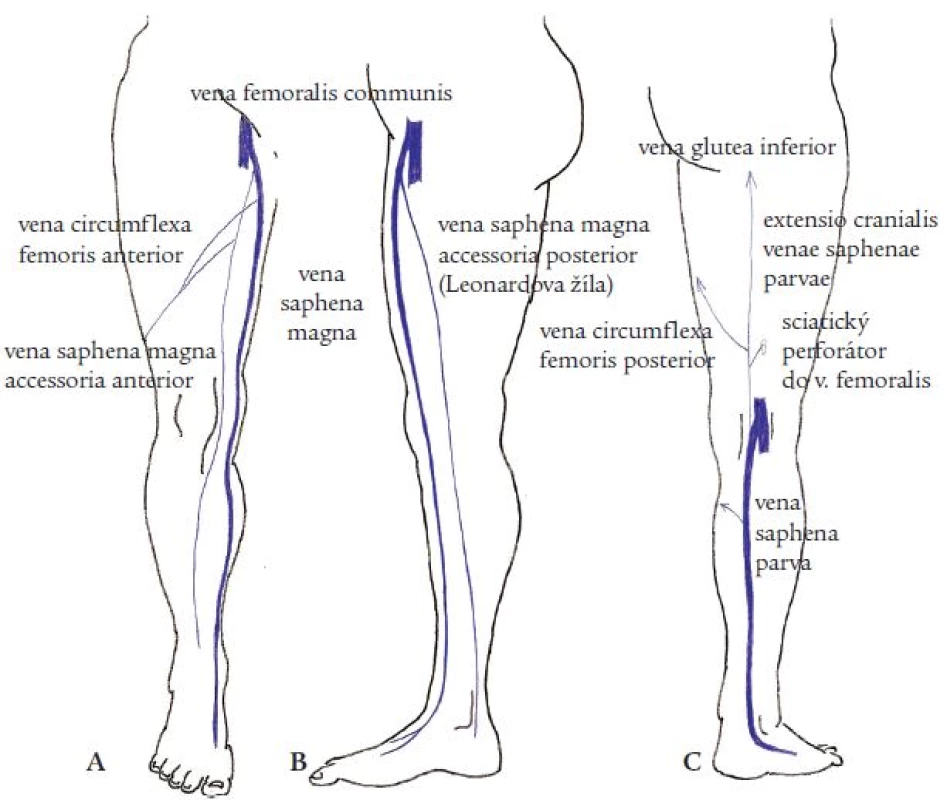
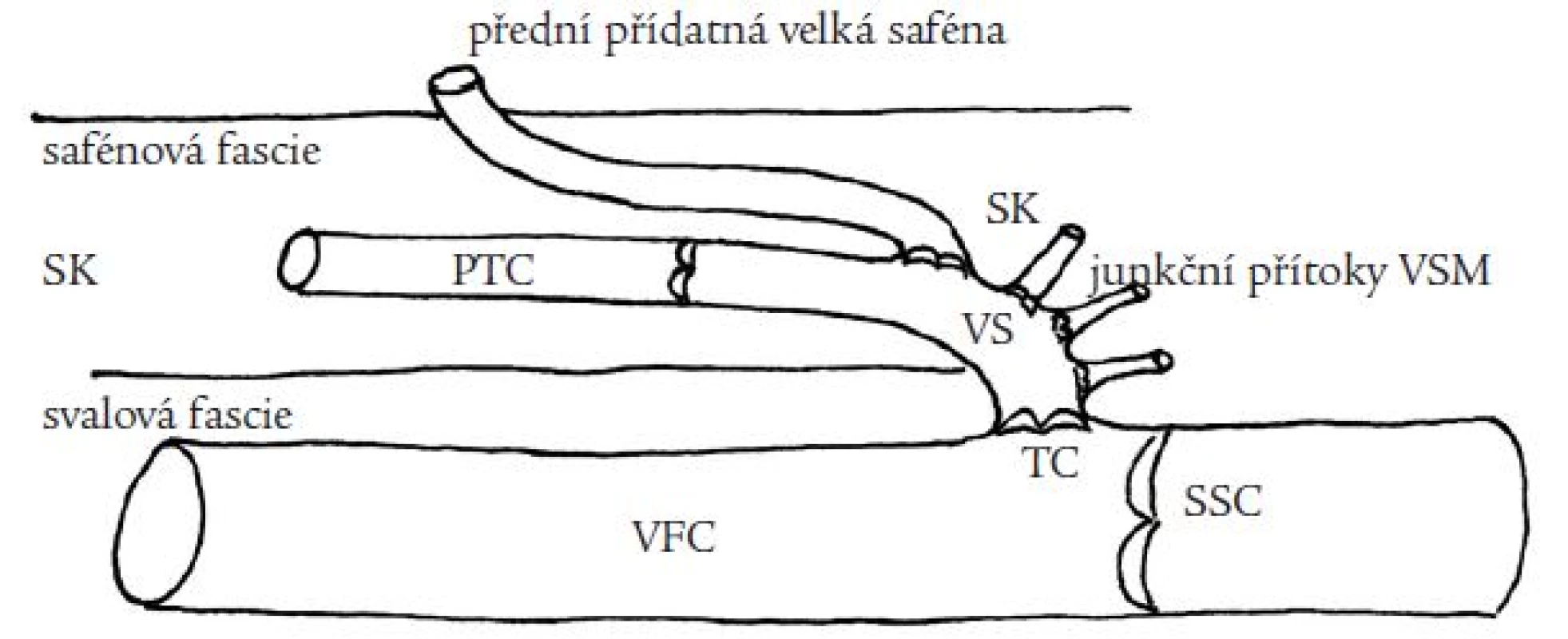
Stejně jako velká saféna, tak také přídatné velké safény nejdříve probíhají v safénovém kompartmentu (část podkoží ležící mezi svalovou a safénovou fascií, obr. 6), který v různé vzdálenosti od svého odstupu opouštějí do povrchnějších vrstev podkoží (obr. 2). V třísle a na stehně se podle naší klinické zkušenosti často setkáváme s přední přídatnou velkou safénou (PPVS). Při ultrazvukovém vyšetření tak může dojít k záměně PPVS za VS. Nejčastěji dochází k případům, kdy je insuficietní a dilatovaná PPVS omylem považována za VS. Zatímco se kmenové varixy VS většinou objevují na mediální až dorzomediální části stehna, varixy kmene PPVS nacházíme spíše pod tříslem a na ventrální či ventromediální straně stehna. Někdy mohou zasahovat až na laterální stranu stehna a ke kolenu. Oblasti výskytu kmenových varixů obou safén se často překrývají, klinickým vyšetřením tedy nejsme schopni postižení obou podkožních žil odlišit. Proto jsme se ve své práci soustředili na tuto variabilní žílu a pokusili se odpovědět na několik otázek s ní spojených.
Cíle práce
Při ultrazvukovém mapování povrchového žilního systému dolních končetin před operací varixů je potřebné počítat s výskytem přední přídatné velké safény (PPVS). Abychom ji mohli popsat, musíme znát její odstup z velké safény, jak daleko PPVS v safénovém kompartmentu probíhá a v jaké vzdálenosti od svého odstupu ho nejčastěji opouští. Všeobecné tvrzení „v horní části stehna“ je velmi nepřesné. Měli bychom spolehlivě odlišit PPVS od VS a vědět, jak často se u našich pacientů může PPVS vyskytnout. Proto si naše práce kladla za cíl objasnit tyto skutečnosti:
- zjistit výskyt PPVS na dolních končetinách u vyšetřené skupiny pacientů
- zjistit, v jaké vzdálenosti od safénofemorální junkce (SFJ) odstupuje PPVS z VS, případně jak často PPVS odstupuje přímo ze společné stehenní žíly (v. femoralis communis)
- zjistit, v jaké vzdálenosti od vyústění do VS prostupuje PPVS safénovou fascií (fascie v podkoží, pod kterou leží VS a po svém odstupu z VS zpočátku také přídatné safény)
- srovnat šíři anechogenního lumen PPVS s kalibrem VS
Soubor nemocných a metodika
Do naší primární průzkumné studie bylo zařazeno 113 dolních končetin u 66 po sobě jdoucích pacientů, vyšetřeno bylo 46 žen (průměrný věk 55,8 let ± 12 let) a 20 mužů (průměrný věk 59 let ± 15 let). Tito pacienti byli odesláni do cévní ambulance k ultrasonografickému vyšetření z různých důvodů: 17 pacientů pro podezření na flebotrombózu (diagnóza potvrzena u 6 nemocných), 44 pacientů pro podezření na žilní insuficienci (u 35 nemocných byla prokázána insuficience hlubokých a/nebo povrchových žil) a 1 pacient odeslán k vyšetření pro tromboflebitidu. Do studie byly zařazeny všechny dolní končetiny pacientů v tom sledu, jak tito pacienti postupně přicházeli k ultrasonografickému vyšetření. Jediným vyřazovacím kritériem byl stav po operaci nebo skleroterapii varixů na stehně.
Pomocí duplexní ultrasonografie jsme obvyklým způsobem lineární sondou 7,5 a 10 MHz v B-modu a barevným mapováním krevního toku (color flow mapping - CFM) v poloze vleže na zádech, v třísle a na ventromediální straně stehna, pátrali po výskytu přední přídatné velké safény (PPVS).
Hodnotili jsme přítomnost (prevalenci) PPVS, její vybrané anatomické parametry (viz níže) a výskyt refluxu v této žíle. Za PPVS jsme pokládali každou žílu odstupující z VS v oblasti safénofemorální junkce, probíhající zpočátku v safénovém kompartmentu ventrolaterálně od VS a v různé vzdálenosti od svého odstupu prorážející na stehně safénovou fascii směrem do podkoží. Na dolních končetinách s nálezem PPVS jsme měřili také šíři lumen velké safény. Všechny měřené vzdálenosti byly měřeny v centimetrech. Termín safénofemorální junkce (SFJ) zde vyjadřuje anatomické místo vyústění VS do společné stehenní žíly (VFC).
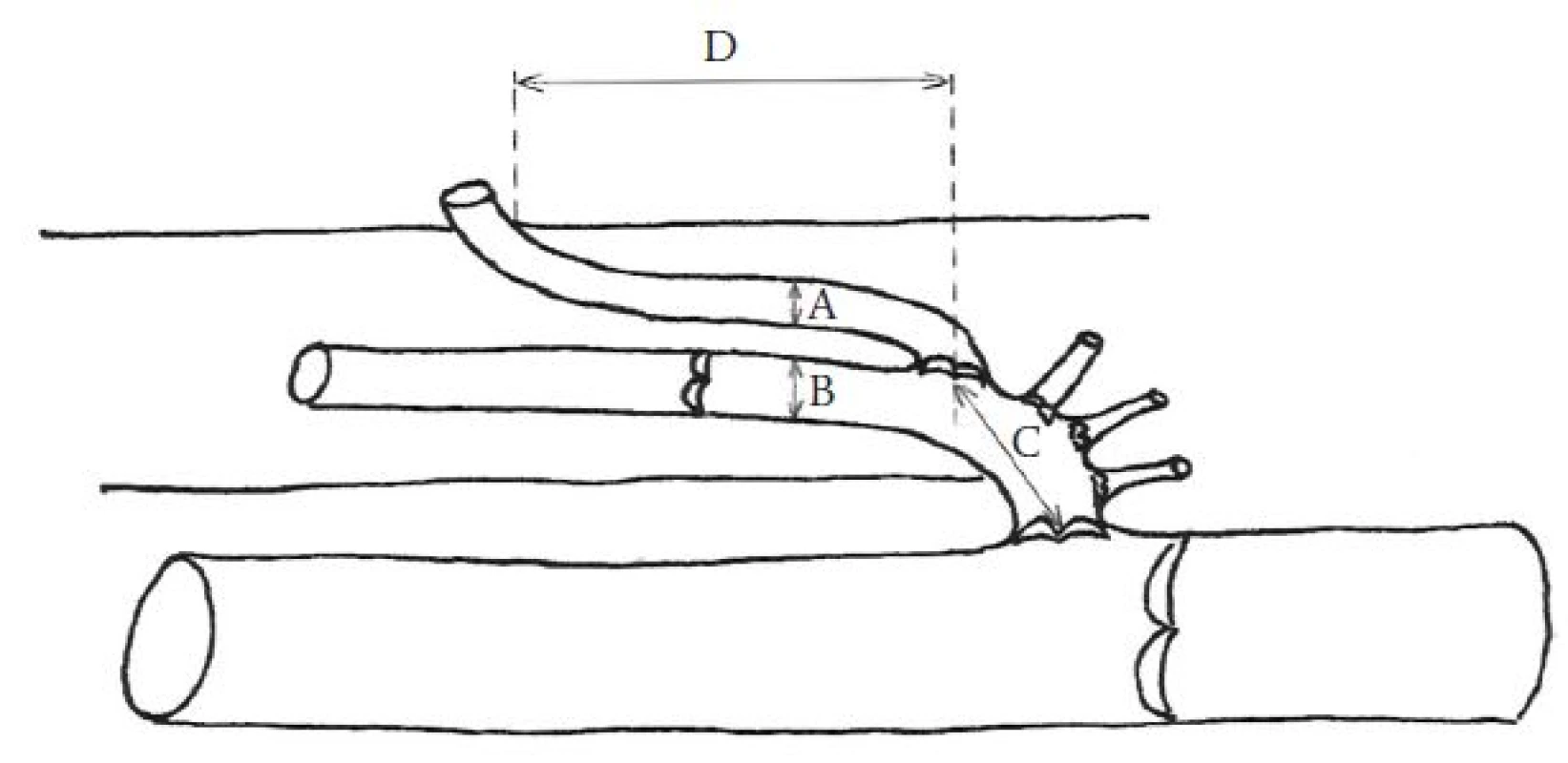
Na dolních končetinách s nálezem PPVS jsme v B-módu a CFM ultrazvukového zobrazení měřili tyto anatomické parametry PPVS (obr. 3):
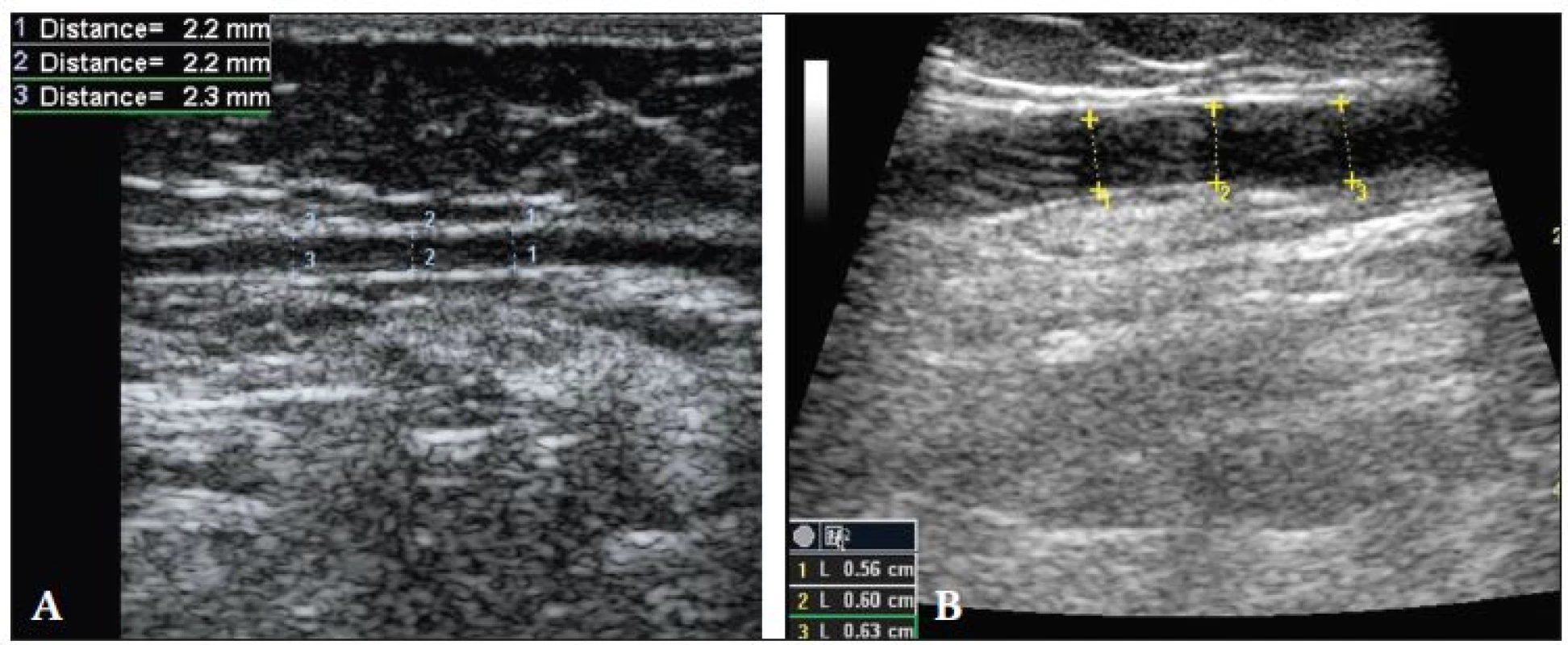
- šíře anechogenního lumen VS a PPVS - měřena v podélném zobrazení (B-mód) vždy na 3 pravidelně od sebe vzdálených místech v úseku dlouhém 3 cm, ve vzdálenosti do 5 cm od safénofemorální junkce (obr. 4),
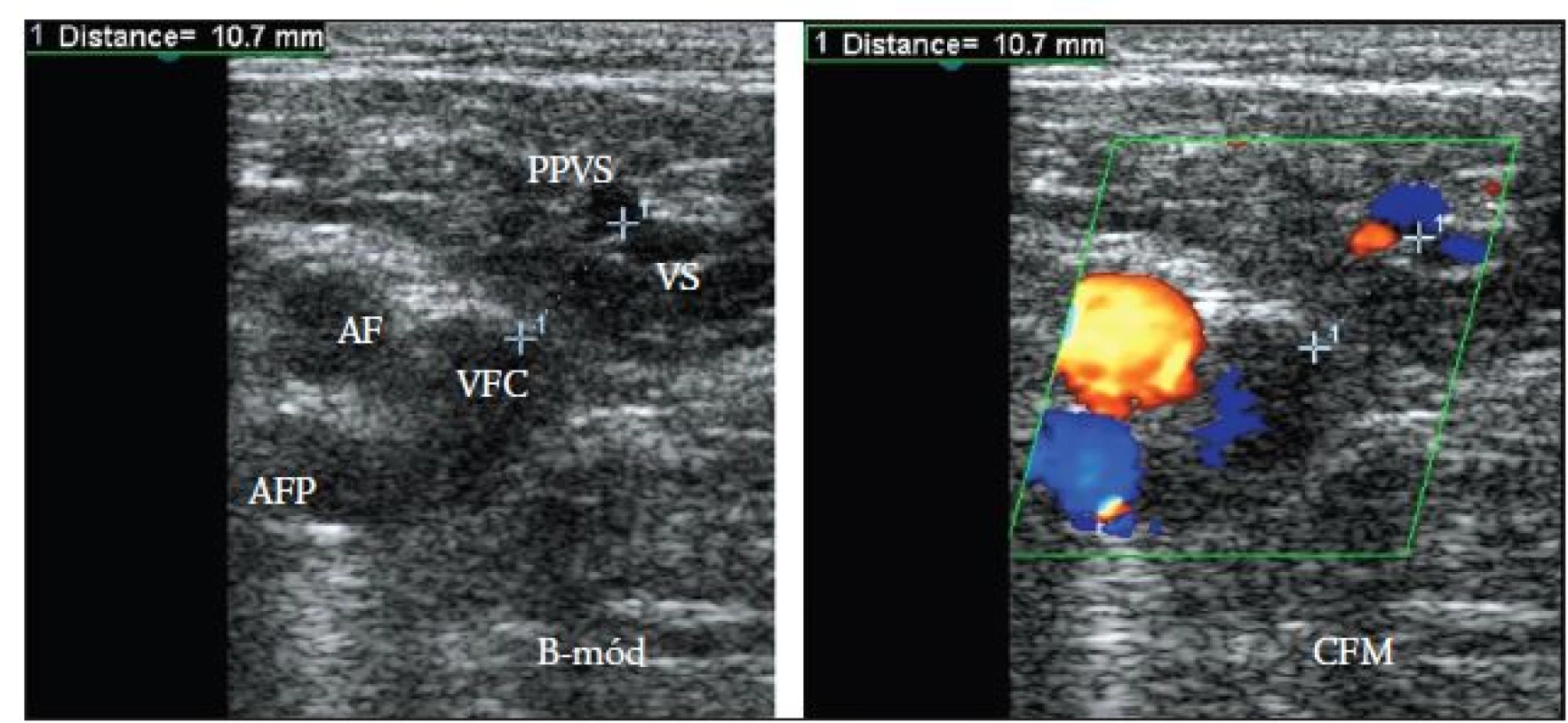
- vzdálenost odstupu PPVS z VS od SFJ - měřena v příčném zobrazení (B-mód a CFM) od okraje anechogenního lumen společné stehenní žíly (v. femoralis communis) k místu, kde se od sebe oddělovala anechogenní lumen PPVS a VS (obr. 5),
- vzdálenost místa prostupu PPVS safénovou fascií od jejího odstupu z VS - měřena v podélném zobrazení PPVS (B-mód), obr. 6.
U každé zjištěné PPVS jsme také hodnotili přítomnost refluxu při Valsalvově manévru prováděného pacientem. Reflux byl potvrzen, pokud zpětný tok krve při Valsalvově manévru trval 1 s a déle.
Statistické zpracování výsledků měření bylo provedeno popisnými statistickými metodami (výpočet průměru - A, mediánu - M, standardní odchylky - SD). Šířku anechogenního lumen VS a PPVS, vždy na jedné dolní končetině, jsme srovnali pomocí párového t-testu.
Výsledky
PPVS byla nalezena u 48 z celkového počtu 113 vyšetřených dolních končetin s prevalencí 42,5 %. Ze 48 předních přídatných safén jsme reflux prokázali u 6 (12,5 %). Obě dolní končetiny byly vyšetřeny 48 pacientům (72,7 % všech vyšetřených osob). Z tohoto počtu jsme u 18 osob (37,5 %) nezjistili PPVS ani na jedné dolní končetině, u 17 osob (35,4 %) pouze na jedné dolní končetině a u 13 osob (27,1 %) byla PPVS prokázána na obou dolních končetinách.
Šíře anechogenního lumen PPVS měřená ve vzdálenosti do 5 cm od safénofemorální junkce byla průměrně 0,29 cm (medián 0,26 cm, SD ± 0,15 cm) a šíře anechogenního lumen VS měřená na dolních končetinách se současným výskytem PPVS byla průměrně 0,38 cm (medián 0,38 cm, SD ± 0,11 cm). Srovnáním šíře anechogenního lumen obou žil byl zjištěn statisticky velmi významný (p < 0,001), graf 1 a obr. 7.

PPVS v našem souboru dolních končetin odstupovala z VS v průměrné vzdálenosti 0,8 cm od safénofemorální junkce (medián 0,8 cm, SD ± 0,46 cm). Minimální vzdálenost odstupu byla 0,1 cm, maximální vzdálenost 1,84 cm. Pouze ve 3 případech (6,3 %) PPVS odstupovala přímo ze společné stehenní žíly (v. femoralis communis) v místě současného odstupu VS (obr. 7).
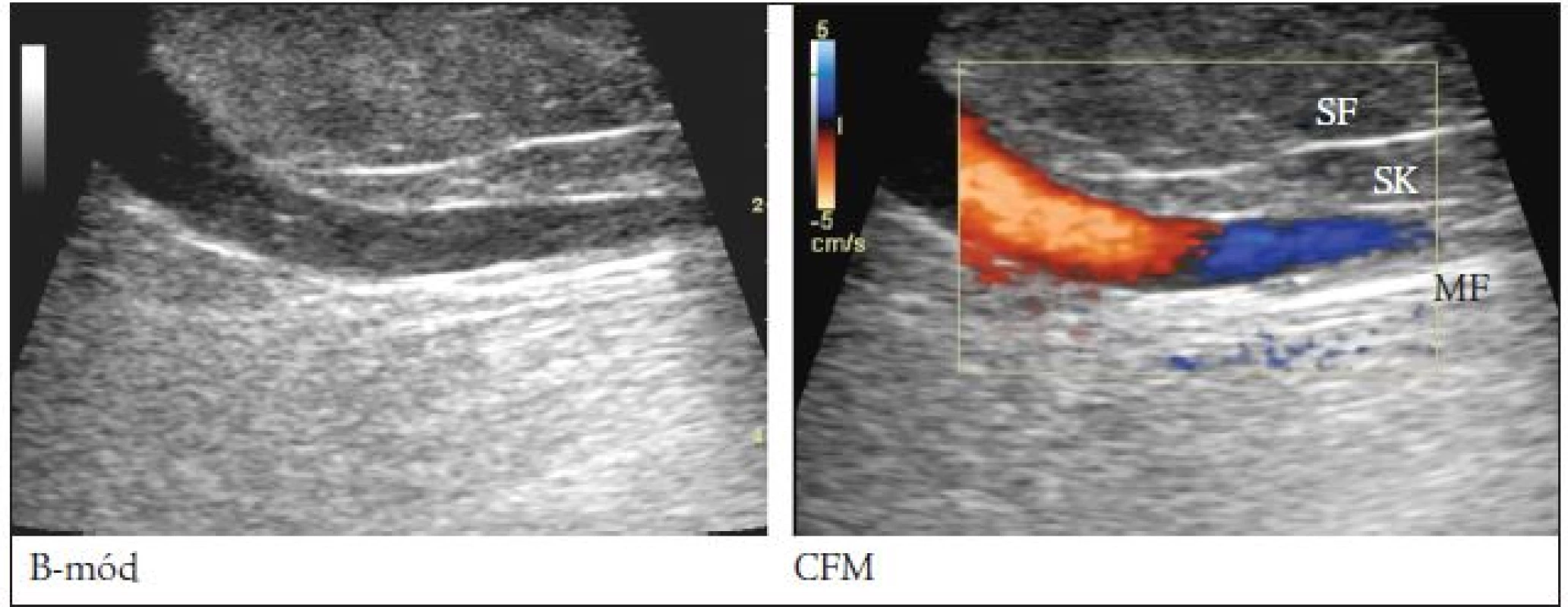
Průnik PPVS safénovou fascií do vyšších vrstev podkoží jsme pozorovali v průměrné vzdálenosti 13,2 cm (medián 14,5 cm, SD ± 6,5 cm) od místa odstupu žíly z VS. Minimální vzdálenost průniku PPVS safénovou fascií od odstupu žíly z VS byla 4 cm, maximální vzdálenost 30 cm (obr. 6 a 7).
Diskuse
Výsledky této práce potvrzují naši klinickou zkušenost, že PPVS je velmi často se vyskytující variabilní žílou na stehně dolních končetin (42,5 %), takže je s ní nutno při ultrazvukovém vyšetření počítat. Studie potvrzuje také naše předchozí zjištění, při němž jsme v souboru 309 dolních končetin s klinickými projevy žilní nedostatečnosti nalezli přídatnou velkou safénu (v. saphena accessoria) jako nejčastější variabilní žílu (54,8 %) [8], i když jsme zde ještě nerozlišovali mezi její přední, zadní a povrchovou variantou (vena saphena magna accessoria anterior, posterior et superficialis) [2]. Pokud jsme si všímali přítomnost PPVS na obou dolních končetinách u jedné osoby, byl výskyt PPVS pouze na jedné DK srovnatelný s oboustranným chyběním PPVS (37,5 % vs. 35,4 %). Osob s PPVS prokázanou na obou dolních končetinách bylo signifikantně nejméně (27,1 %).
Do souboru jsme zařadili všechny dolní končetiny odeslané k ultrasonografickému vyšetření, včetně těch s prokázanou flebotrombózou (6 dolních končetin). I když v případě flebotrombózy lze předpokládat určitou dilataci podkožních žil, domníváme se, že s výjimkou rozsáhlé ileofemorální flebotrombózy, která se v našem souboru nevyskytla, probíhá žilní tok kolaterálami v hlubokém svalovém kompartmentu v okolí uzavřené žíly a rozšíření podkožních žil je nevýznamné. Navíc jsme párovým t-testem srovnávali šířku lumen VS a PPVS vždy na jedné dolní končetině. Proto nebyl důvod tyto končetiny do studie nezařadit.
Ultrasonografista by měl být schopen PPVS najít a spolehlivě odlišit od VS, případně od zadní přídatné VS. Zjistit její průběh a popsat reflux ve VS a/nebo PPVS. Operace bez předchozího ultrasonografického vyšetření často ponechávají PPVS, funkční nebo insuficietní, in situ při odstranění VS [8,9]. Nebo naopak, příčinou recidivy může být, když chirurg odstraní pouze přídatnou safénu a hlavní kmen VS zůstane in situ [10].
Vyhledávání PPVS by mělo začít pátráním po jejím odstupu z VS. Jak jsme v této práci ukázali, odstup PPVS musíme hledat těsně pod tříselným vazem v příčném ultrazvukovém zobrazení vzhledem k předpokládanému průběhu žíly. Podle našeho pozorování PPVS odstupuje v průměrné vzdálenosti 0,8 cm od SFJ, maximálně však asi 2 cm daleko. Pokud předpokládáme, že se preterminální chlopeň VS nachází ve vzdálenosti 3-5 cm od terminální chlopně, tedy od vyústění velké safény do společné stehenní žíly [3,6], odstupuje PPVS vždy proximálně od preterminální chlopně (obr. 2).
Ultrasonografista by měl být schopen PPVS spolehlivě odlišit od VS, případně od zadní přídatné velké safény. Jednoduchým kritériem pro odlišení obou žil je signifikantně větší šíře anechogenního lumen VS ve srovnání s PPVS (p < 0,001), graf 1. Dále bychom si měli všímat průběh VS a PPVS vzhledem k podkožní safénové fascii. Průchod safénovou fascií do povrchnějších vrstev podkoží na stehně je jedním z hlavních anatomických znaků, podle kterého PPVS při ultrazvukovém vyšetření rozpoznáváme.
Velká saféna byla definována jako intrafasciální žíla probíhající v podkoží, uzavřená mezi svalovou a safénovou fascií v tzv. safénovém kompartmentu (obr. 2), od vnitřního kotníku nahoru k tříslu [4]. Podle původního mezinárodního interdisciplinárního konsenzu z roku 2002, týkajícího se nomenklatury žil dolní končetiny [2], všechny přídatné safény záhy po svém odstupu z velké safény opouštějí safénový kompartment a vzhledem k hlavnímu kmeni velké safény běží povrchněji. Toto všeobecné tvrzení ale bylo novým konsensem z roku 2005 revidováno [3]. V citovaném sdělení se uvádí, že PPVS navzdory všeobecnému pravidlu, týkajícího se průběhu přídatných safén, probíhá v horní části stehna hlouběji, nad svalovou fascií v safénovém kompartmentu, podobně jako VS, ale na rozdíl od kmene velké safény leží více vepředu a její průběh koresponduje s průběhem v hloubce ležící stehenní žíly a tepny [3].
V našem souboru bylo místo prostupu safénovou fascií nejvíce variabilní anatomickou vlastností PPVS. K průniku PPVS většinou docházelo 13,2 cm pod odstupem z VS, ale žíla v našem souboru procházela fascií v rozmezí od 4 cm až do 30 cm pod svým odstupem, tedy buď v třísle nebo až v distální třetině stehna. Vyhledání místa průniku fascií na stehně, a tedy definitivní potvrzení, že se jedná o přídatnou VS, nikoliv o vlastní VS, je jedním z důležitých úkolů při mapování PPVS.
Závěr
Přední přídatná velká saféna je běžnou variabilní žílou přední a ventromediální strany stehna dolní končetiny. Respektováním její anatomie (šíře anechogenního lumen, místo odstupu z VS a průnik safénovou fascií) ji při pozorném předoperačním ultrazvukovém mapování žil dolní končetiny lze dobře identifikovat a přesně popsat její průběh. Průkaz a popis PPVS patří k faktorům, které mohou významně ovlivnit procento pooperačních recidiv varixů dolních končetin, protože izolovaný reflux v safénofemorální junkci je nejčastěji zjišťovanou příčinou recidivy [7,9,11].
MUDr. Dalibor Musil, Ph.D.
www.upol.cz
e-mail: musil.dalibor@quick.cz
Doručeno do redakce: 18. 4. 2006
Přijato po recenzi: 7. 8. 2006
Zdroje
1. Federative International Committee for Anatomical Terminology. Terminologia Anatomica. Stuttgart: George Thieme Verlag 1998.
2. Caggiati A et al. Nomenclature of the veins of the lower limbs: An international interdisciplinary consensus statement. J Vasc Surg 2002; 36: 416-422.
3. Caggiati A et al. Nomenclature of the veins of the lower limb: Extensions, refinements, and clinical application. J Vasc Surg 2005; 41: 719-724.
4. Caggiati A, Ricci S. Long saphenous vein compartment. Phlebology 1997; 12: 107-111.
5. Feneis H. Anatomický obrazový slovník. 1. ed. Praha: Avicenum 1981.
6. Haeger K. The surgical anatomy of the sapheno-femoral and the sapheno-popliteal junctions. J Cardiovasc Surg 1962; 3: 420-427.
7. Jutley RR, Cadle I, Gross KS. Perioperative examination of the primary varicose veins: study of the venous insufficiency by the duplex ultrasound. Eur J Vasc Endovasc Surg 2001; 21: 370-373.
8. Musil D, Herman J. Anatomické a hemodynamické změny na žilním řečišti dolních končetin postižených chronickou žilní insuficiencí. Vnitř Lék 2003; 49: 610-617.
9. Musil D, Herman J, Duda M. Recidiva varixů dolních končetin. Vnitř Lék 2004; 50: 587-590.
10. Rutgers PH, Kitslaar PJ. Randomized trial of stripping versus high ligation combined with sclerotherapy in the treatment of the incompetent great saphenous vein. Am J Surg 1994; 168: 311-315.
11. Wong JKF, Duncan JL, Nichols DM. Whole-leg duplex mapping for varicose veins: observations on patterns of reflux in recurrent and primary varicose veins, with clinical correlation. Eur J Vasc Endovasc Surg 2003; 25: 267-275.
Štítky
Diabetológia Endokrinológia Interné lekárstvoČlánok vyšiel v časopise
Vnitřní lékařství

2006 Číslo 12
- Statinová intolerance
- Hydroresponzivní krytí v epitelizační fázi hojení rány
- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Metamizol v liečbe pooperačnej bolesti u detí do 6 rokov veku
Najčítanejšie v tomto čísle
- Aktuální přístupy k diagnostice a terapii hemoptýzy: editorial
- Postavení embolizace bronchiální tepny v terapii klinicky významné hemoptýzy
- Ultrazvukové mapování žilního systému dolních končetin s ohledem na výskyt a anatomii přední přídatné velké safény
- Statiny a osteoporóza
