-
Články
- Časopisy
- Kurzy
- Témy
- Kongresy
- Videa
- Podcasty
Covid-19 u nemocných po transplantaci ledviny
Covid-19 in kidney transplant recipients
Kidney transplant recipients are a very vulnerable population at risk of severe course and death from Covid-19. Several antiviral drugs are now available for the treatment of nonhospitalized individuals with mild to moderate Covid-19 and hospitalized patients with severe disease. The combination of monoclonal antibodies is also available to be used as pre-exposure prophylaxis in elderly patients.
Previously used monoclonal antibodies for post-exposure prophylaxis are no longer effective because of the new mutations and are no longer recommended. Although the immune response to Covid-19 vaccines is impaired in kidney transplant recipients, the effectiveness of the Covid-19 vaccines was described even in this immunocompromised group. Therefore vaccination, together with anti-epidemic measures, remains the most important tool to prevent Covid-19.
Keywords:
vaccination – Monoclonal antibodies – kidney transplantation – COVID-19 – antiviral drugs – vaccine effectiveness – mRNA vaccine – pre‑exposure prophylaxis – SARS‑CoV- 2 – vector vaccine
Autori: Mária Magicová; Ondřej Viklický
Pôsobisko autorov: Klinika nefrologie, Transplantační centrum, Institut klinické a experimentální medicíny, Praha
Vyšlo v časopise: Vnitř Lék 2022; 68(7): 444-448
Kategória:
doi: https://doi.org/10.36290/vnl.2022.093Súhrn
Pacienti po transplantaci ledviny jsou velmi zranitelnou skupinou ohroženou závažným průběhem a úmrtím na onemocnění covid-19. V současnosti je dostupných několik antivirotik určených k ambulantní léčbě mírného až středně závažného průběhu onemocnění a nemocniční léčbě závažného onemocnění. K dispozici je také preparát směsi monoklonálních protilátek k pre‑expoziční profylaxi (pasivní imunizace). Problémem jsou však nové mutace viru, proti kterým dříve užívané monoklonální protilátky k post‑expoziční profylaxi již nejsou účinné. Nové mutace mohou navíc snižovat schopnost vakcín indukovat tvorbu neutralizačních protilátek a efektivitu vakcín. Ačkoliv mají pacienti po transplantaci ledviny porušenou odpověď na vakcinaci proti covidu-19, je i u této imunokompromitované skupiny prokázán klinický efekt covidových vakcín. Očkování a pasivní imunizace tak zůstávají spolu s protiepidemickými opatřeními nejdůležitější prevencí onemocnění covid-19.
Klíčová slova:
monoklonální protilátky – transplantace ledvin – očkování – preexpoziční profylaxe – COVID-19 – antivirotika – efektivita vakcín – mRNA vakcína – SARS‑CoV- 2 – vektorová vakcína
ÚVOD
Covid-19 (coronavirus disease 2019) je onemocnění způsobené RNA virem SARS‑CoV - 2 (severe acute respiratory syndrome coronavirus 2). První prokázaný případ se objevil v lednu 2020 v Číně a od té doby se nákaza rychle rozšířila do celého světa. Zvláště rizikovou skupinou jsou pacienti po transplantaci ledviny, kteří jsou z důvodu užívaní imunosuprese vnímavější k infekcím a ve srovnání s běžnou populací jsou více ohroženi závažným průběhem a úmrtím na onemocnění covid-19. Tito pacienti by měli být prioritně léčeni antivirotiky, jejichž cena si ale vyžaduje určitou selekci pacientů, kterým budou podány. Nejdůležitější farmakologické preventivní opatření je očkování, které ale má v této populaci své limity. Další možností jak tyto pacienty chránit je forma pasivní imunizace. Následující text má za cíl seznámit čtenáře se základními principy terapie a problematikou očkování proti covidu-19 u pacientů po transplantaci ledviny.
Terapie
Onemocnění covid-19 může probíhat variabilně, od asymptomatické infekce až po kritické onemocnění s respiračním selháním. V léčbě covidu-19 u pacientů po transplantaci ledviny uplatňujeme doporučované postupy platné pro obecnou populaci (1), protože chybí studie analyzující efektivitu jednotlivých preparátů přímo u transplantované populace. V textu uvádíme doporučení pro ambulantní i nemocniční léčbu covidu-19.
Ambulantní léčba pacientů s mírným až středním průběhem onemocnění
V současnosti je k dispozici několik terapeutických možností ambulantní léčby covidu-19 přímo působícími antivirotiky. Týká se pacientů s mírným až středně závažným průběhem onemocnění, který nevyžaduje hospitalizaci ani léčbu kyslíkem (1). V případě omezené dostupnosti těchto preparátů by podle doporučení měli být rizikoví pacienti, jako jsou ti po orgánových transplantacích, upřednostňováni. Volbu preparátu vhodného pro ambulantní léčbu neovlivňuje jen klinická účinnost, ale i způsob podání. Například remdesivir je v případě ambulantní léčby nutno podávat v infuzi celkem tři dny, což může být organizační problém nejen pro pacienty, ale i nemocnice a jejich prostorové i personální kapacity. Dalším specifikem léčby transplantovaných pacientů je omezená možnost podání některých preparátů u pacientů s renální dysfunkcí a lékové interakce antivirotik, které obsahují ritonavir (viz níže). Z doporučovaných antivirotik jsou u nás v současnosti dostupné dva: přípravek Veklury (remdesivir) a Lagevrio (molnupiravir). Preferovanou volbou je vzhledem k vyšší účinnosti remdesivir. Ve studii PINETREE u pacientů bez nutnosti hospitalizace s alespoň jedním rizikovým faktorem progrese onemocnění (věk ≥ 60 let, obezita, koexistující onemocnění) s trváním symptomů do 7 dnů snížil remdesivir (200 mg 1. den, 100 mg 2. a 3. den) riziko hospitalizace či úmrtí o 87 % v porovnání s placebem (2). Přípravek Veklury obsahuje renálně eliminovanou pomocnou látku sodnou sůl sulfobutoxybetadexu, proto se jeho podání nedoporučuje pacientům s eGFR < 30 ml/min a tito pacienti ani nebyli do intervenčních studií zařazováni. Avšak na základě observačních studií, které nezaznamenaly vyšší výskyt nežádoucích účinků u pacientů s pokročilou renální insuficiencí, může být jeho podání prospěšné (3). V případě nedostupnosti remdesiviru či kontraindikace podání je alternativou přípravek Lagevrio (molnupiravir). Vzhledem k nižší účinnosti je lékem druhé volby. V randomizované placebem kontrolované studii MOV‑e OUT snížil molnupiravir riziko hospitalizace nebo úmrtí o 30 % (4). Výhodou oproti remdesiviru je však možnost perorálního podání a v případě renální insuficience není potřebná úprava dávkování. Ačkoliv farmakokinetika molnupiraviru a jeho metabolitu NHC (N‑hydroxycytidinu) u pacientů s eGFR < 30 ml/min nebyla hodnocena, renální clearance nepředstavuje významnou cestu eliminace. Jak remdesivir, tak molnupiravir vykazují aktivitu proti variantě Omicron (5). V neposlední řadě je potřeba zmínit třetí velmi účinný preparát indikovaný k ambulantní léčbě mírných až středně závažných onemocnění – přípravek Paxlovid (kombinace antivirotik nirmatrelviru a ritonaviru). Podle aktuálních amerických doporučení je první volbou, zatím (srpen 2022) však není v České republice dostupný. Ve studii EPIC‑HR snížil Paxlovid riziko hospitalizace nebo úmrtí neočkovaných nemocných o 88 % ve srovnání s placebem (6). Vykazuje aktivitu proti Omicronu a jeho subvariantám. Pro transplantované pacienty mohou být limitací jeho podání lékové interakce. Ritonavir je silný inhibitor cytochromu P450 (CYP) 3A4 a vede ke zvýšení hladin kalcineurinových a mTOR inhibitorů. To by však vzhledem k jeho vysoké účinnosti nemělo být absolutní kontraindikací podání. Možností je vysazení kalcineurinových inhibitorů po dobu léčby Paxlovidem (5 dní) a po ukončení léčby kontrola jejich hladin. U pacientů s chronickým onemocněním ledvin ve stadiu CKD G3 je nutná redukce dávky, pacientům s eGFR < 30 ml/ min není doporučován (1). Je potřeba uvést, že všechny 3 studie na dané preparáty zahrnovaly pouze neočkované pacienty.
Monoklonální protilátky jako bamlanivimab, bamlanivimab + etesivimab nebo casirivimab + imdevimab, dříve používané pro pacienty v riziku progrese onemocnění a bez nutnosti oxygenoterapie, již v současnosti nejsou doporučovány (1), vzhledem k neúčinnosti proti aktuálně dominující variantě omikron (5). U nehospitalizovaných pacientů s mírným průběhem není doporučována ani rutinní aplikace LMWH v prevenci tromboembolické nemoci, pokud k tomu není jiná indikace (1).
Léčba hospitalizovaných pacientů se středně závažnou až těžkou formou onemocnění
Doporučení pro léčbu hospitalizovaných pacientů se odvíjí od závažnosti stavu a případné potřeby oxygenoterapie (1). U pacientů, kteří nevyžadují léčbu kyslíkem na základě dostupných dat, není doporučována léčba dexamethasonem ani jinými kortikosteroidy. Pro transplantované pacienty, vzhledem k riziku progrese, lze ale zvážit léčbu remdesivirem. V případě nutnosti oxygenoterapie je doporučován remdesivir (pouze v případě minimální kyslikové podpory), dexamethason nebo kombinace. U pacientů s high‑flow oxygenoterapií či na neinvazivní ventilaci je doporučována kombinace remdesiviru s dexamethasonem nebo dexamethason samotný. Remdesivir ve studii ACTT-1 zkrátil u nemocných s nutností kyslíkové podpory (bez potřeby high‑flow oxygenoterapie či ventilace) dobu do zotavení a v post‑hoc analýze snížil riziko úmrtí v prvních 28 dnech o 70 % v porovnání s placebem (7). Méně pacientů dospělo k high‑flow oxygenoterapii, mechanické ventilaci, či nutnosti zahájení ECMO. Ve studii RECOVERY vedla terapie dexamethasonem u hospitalizovaných pacientů léčených kyslíkem k signifikantnímu snížení 28denní mortality ve srovnání se standardní léčbou (8). Naopak u hospitalizovaných pacientů bez nutnosti oxygenoterapie podání dexamethasonu nepřineslo benefit. Kombinovaná léčba dexamethasonem a remdesivirem nebyla v kontrolovaných studiích zkoumána. Specifika terapie na jednotkách intenzivní péče přesahují rámec tohto příspěvku a odkazujeme čtenáře na recentní doporučení.
Úpravy imunosupresivní terapie
Podobně jako u jiných infekčních onemocnění se v případě covidu - 19 u imunosuprimovaných pacientů nabízí upravit či dokonce dočasně vysadit imunosupresi. Tyto zásahy by měly být provedeny po zhodnocení klinického průběhu infekce a rizika progrese, rizika rejekce štěpu a měly by být přísně individuální. Změny imunosuprese by měl vést lékař se zkušenostmi s imunosupresí a optimálně po dohodě s dispenzarizujícím transplantačním centrem. Pokud je redukce imunosuprese indikovaná, obecně je v prvním kroku přistupováno k redukci/ vysazení antimetabolitu (mykofenolátu nebo azathioprinu) v případě, kdy pacient užívá současně kalcineurinový inhibitor a kortikoidy. V případě těžkého průběhu onemocnění je možno vysadit imunosupresi celou a podávat stresové dávky kortikoidů. Naopak u mírných forem infekce by imunosuprese být vysazována neměla. V tomto případě je hlavním problémem identifikovat pacienty, kteří se sice zprvu prezentují mírným průběhem, ale jsou ve vysokém riziku progrese do závažnějších forem.
Imunitní odpověď pacientů po transplantaci ledviny na infekci virem SARS‑CoV-2
Pacienti po transplantaci ledviny mají z důvodu užívání imunosuprese porušenou imunitní odpověď na infekci virem SARS‑CoV-2. Míra sérokonverze udávaná v různých studiích se liší v závislosti od použité laboratorní metody a typu detekovaných protilátek. Metody detekující protilátky proti tzv. receptor vázající doméně (RBD, receptor binding domain) S‑proteinu jsou senzitivnější a lépe korelují s titrem neutralizačních protilátek (9). Během druhé vlny pandemie covidu-19 jsme v IKEM analyzovali protilátkovou odpověď u pacientů po transplantaci ledviny a zdravotníků (10). Detekovali jsme protilátky proti S1 a S2 podjednotce S‑proteinu. Sérokonverze dosáhlo 82,6 % pacientů po transplantaci ledviny a 95,2 % zdravotníků se symptomatickým průběhem covidu-19. Pacienti po transplantaci ledviny tvořili překvapivě vyšší hladiny protilátek než imunokompetentní skupina zdravotníků. V multivariantní analýze bylo zjištěno, že tíže symptomů signifikantně ovlivňuje hladinu SARS‑CoV - 2 protilátek. Nejvyšší hladiny protilátek byly detekované u pacientů se závažnými respiračními příznaky, naopak nejnižší hladiny protilátek tvořili pacienti s asymptomatickou infekcí.
Pro virovou clearance je ale důležitá nejen humorální, ale i buněčná imunitní odpověď, která u pacientů navíc přetrvává i po vymizení protilátek a pravděpodobně je chrání před reinfekcí (11). Studie francouzské kohorty pacientů po transplantaci ledviny prokázala buněčnou imunitní odpověď u všech pacientů, kteří prodělali covid-19 (11). Zdá se tedy, že navzdory užívání imunosuprese není adaptivní imunitní odpověď na infekci virem SARS‑CoV - 2 u transplantovaných nemocných oslabená tak výrazně, jak se původně očekávalo.
Tab. 1. Prevence a ambulantní léčba covidu-19 po translantaci ledviny v ČR 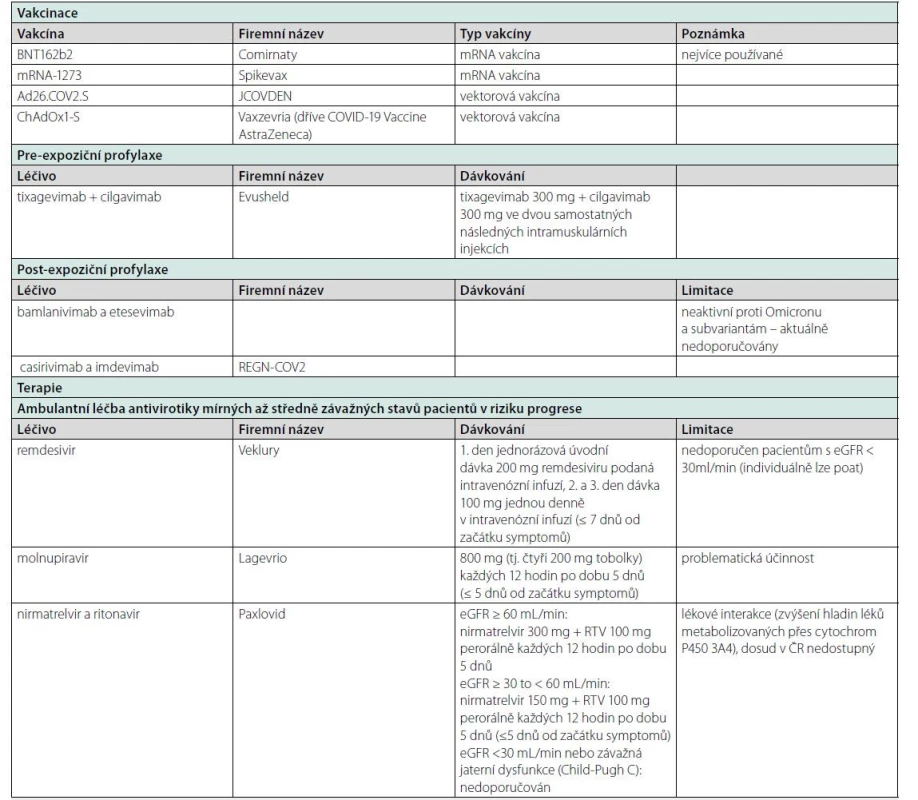
Zdroj: https://www.covid19treatmentguidelines.nih.gov/ Očkování
Imunitní odpověď po očkování
Nedostatečná odpověď je v transplantované populaci dobře známá i u jiných vakcín, proto byly od počátku přítomny také obavy ze snížené odpovědi pacientů po transplantaci ledviny na vakcíny proti covidu-19. Tento předpoklad potvrdily sérologické studie, které prokázaly výrazně sníženou protilátkovou odpověď u transplantovaných pacientů po plném očkování (tj. 2 dávkami) mRNA vakcínami (12, 13). V naší studii na 736 pacientech jsme prokázali sérokonverzi po dvou dávkách mRNA vakcíny pouze u 45,8 % pacientů po transplantaci ledviny (13). Většina studií vylučovala pacienty s předchozí infekcí, a tak vliv infekce na tvorbu postvakcinačních protilátek u transplantovaných nemocných nebyl jasný. Ukázalo se, že předchozí nákaza virem významně zlepšuje imunitní odpověď na očkování u pacientů po transplantaci ledviny. Z naší kohorty dosáhlo sérokonverzi až 97,1 % pacientů s hybridní imunitou (tj. po prodělaném onemocnění covid-19 a plném očkování). Naproti tomu pacienti, kteří se dosud nesetkali s nákazou, dosáhli sérokonverzi jen v 40,1 % případů. Pacienti s hybridní imunitou tvořili také nejvyšší hladiny SARS‑CoV - 2 protilátek. U většiny pacientů s hybridní imunitou byla pozorována i buněčná odpověď.
Hlavním důvodem snížené schopnosti vakcín indukovat tvorbu protilátek je imunosuprese, především mykofenolát mofetil, který je součástí standardní trojkombinace imunosupresiv užívaných po transplantaci ledviny. Negativní vliv na protilátkovou odpověď po vakcinaci proti SARS‑CoV - 2 má také recentní depleční léčba před očkováním (13) a léčba belataceptem (14). Naproti tomu postvakcinační protilátková odpověď u pacientů očkovaných na čekací listině včetně dialyzovaných pacientů je srovnatelná s obecnou populací (13) a tato skutečnost jen potvrzuje zásadní roli imunosupresivní terapie ve snížené humorální odpovědi po očkování. V naší kohortě dosáhli sérokonverze všichni pacienti očkovaní na čekací listině a protilátky byly detekovány i v časném potransplantačním období. Dalšími faktory, které negativně ovlivňují humorální imunitu po očkování, jsou starší věk, ženské pohlaví, nižší glomerulární filtrace a kratší doba od transplantace, což opět ukazuje na vliv imunosupresivní terapie, která je silnější v časném období po transplantaci (13).
Efektivita vakcín
Zatím není jasný klinický význam testování adaptivní imunity po očkování proti SARS‑CoV-2. Nebyla stanovena jednoznačná hranice titru protilátek, který by měl ochranný vliv před onemocněním a není také jasné, do jaké míry jsou detekované postvakcinační protilátky zároveň neutralizační. Navíc neutralizační aktivita protilátek proti variantě Omicron ve srovnání s přechozími variantami klesá (15) a jejich testování není součastí rutinní praxe. V klinické praxi nás zejména zajímá míra ochrany poskytovaná covidovými vakcínami před infekcí, závažným průběhem onemocnění a úmrtím. Existuje jen málo dat týkajících se klinické efektivity vakcín a dosud chybí randomizované kontrolované studie. Z observačních studií jsou metodologicky nejrelevantnější tři práce. Jak ukázala práce amerických autorů, očkování 2 dávkami mRNA vakcíny nebo jednou dávkou vektorové vakcíny redukovalo výskyt symptomatického covidu-19 u pacientů po orgánových transplantacích o 80 % (16). V naší studii byla zjištěna redukce rizika nákazy o 46 % (17). Výhodou naší studie je velmi spolehlivý zdroj dat spočívající ve využití národního registru ISIN (Informační systém infekčních nemocí zřizovaný Ústavem zdravotnických informací a statistiky). Přesto ve srovnání s obecnou populací byla efektivita u pacientů po transplantaci ledviny o řád nižší. V období těchto obou studií dominovala varianta alfa (B.1. 1. 7). V rozporu s těmito výsledky je studie z Británie, která neprokázala efekt na redukci rizika nákazy po očkování 2 dávkami BNT162b2 mRNA nebo ChAdOx-1-S vektorové vakcíny (18). U mRNA BNT162b2 nebyla pozorována žádná redukce rizika úmrtí, očkování vektorovou vakcínou bylo asociováno s 20% redukcí rizika úmrtí. Medián intervalu mezi první a druhou dávkou byl 77 dní. V té době se totiž vláda ve Spojeném království rozhodla ve snaze proočkovat co největší část populace prodloužit interval mezi 2 dávkami z doporučovaných 3 týdnů na 12 týdnů. Toto rozhodnutí mohlo negativně ovlivnit efektivitu očkování v transplantované populaci a tyto výsledky proto nelze generalizovat na státy, které dodržely doporučovaný interval. Navíc dominantní variantou v období této studie byla již varianta delta (B.1.617), proti které je pozorována nižší efektivita vakcín i mezi obecnou populací (19). Zhoršenou efektivitu lze očekávat i proti variantě Omicron (20), ale studie zatím chybí.
Komplexní opatření chránící pacienty po transplantaci ledviny
Přesto, že očkování zůstává nejdůležitější a nejdostupnější možností prevence covidu-19 s prokázanou efektivitou i u pacientů po transplantaci ledviny, je zásadní implementovat všechna opatření snižující riziko infekce. Ačkoliv hlavním faktorem snížené imunitní odpovědi na vakcinaci je užívání imunosuprese, zejména mykofenolát mofetilu a pro jeho vysazení v perivakcinačním období sice recentně existují data, tento postup by mohl zvýšit riziko rejekce.
Další možností je podání posilujících dávek. Očkování čtvrtou (tzv. druhý booster) dávkou je v současnosti doporučováno pacientům po transplantaci ledviny v mnoha centrech. V současnosti je pro rizikové pacienty doporučována pasivní imunizace. K dispozici je preparát dlouhodobě působících monoklonálních protilátek tixagevimab + cilgavimab (pod firemním názvem Evusheld) poskytující dlouhodobou ochranu před infekcí virem SARS‑CoV - 2 včetně varianty Omikron (1). Táto látka se v některých zemích podává u všech nemocných po transplantaci, většinou ale jenom u více rizikových nemocných. V České republice může být přípravek Evusheld podán všem transplantovaným starším 12 let bez účinné postvakcinační ochrany.
Covid-19 nadále představuje vysoké riziko pro pacienty po transplantaci ledviny. Proto je nezbytné chránit je všemi možnými farmakologickými i nefarmakologickými prostředky: očkovat pacienty na čekací listině k transplantaci, ještě před tím, než jsou vystaveni vlivu imunosuprese, očkovat jejich blízké okolí a ošetřovatelský personál a dodržovat základní protiepidemická opatření. Nadále platí, že nemocný po transplantaci musí dodržovat sociální distanc, dbát na hygienu rukou, ale především nosit ochranu dýchacích cest všude tam, kde dochází ke koncentraci lidí, jako je hromadná doprava a obchody.
KORESPONDENČNÍ ADRESA AUTORA:
prof. MUDr. Ondřej Viklický, CSc.
Klinika nefrologie, Transplantační centrum, Institut klinické a experimentální medicíny, Praha
Vídeňská 1958, 140 21 Praha 4
Cit. zkr: Vnitř Lék. 2022;68(7):444-448
Článek přijat redakcí: 1. 7. 2022
Článek přijat po recenzích: 12. 9. 2022
Zdroje
1. Information on COVID-19 Treatment, Prevention and Research. COVID-19 Treatment Guidelines. [cited June 2022]. Avalible from: https://www.covid19treatmentguidelines.nih.gov/
2. Gottlieb RL, Vaca CE, Paredes R et al. Early Remdesivir to Prevent Progression to Severe Covid-19 in Outpatients. N Engl J Med. 2022;386(4):305-315.
3. Ackley TW, McManus D, Topal JE, Cicali B, Shah S. A Valid Warning or Clinical Lore: an Evaluation of Safety Outcomes of Remdesivir in Patients with Impaired Renal Function from a Multicenter Matched Cohort. Antimicrob Agents Chemother. 2021;65(2):e02290-20.
4. Jayk Bernal A, Gomes da Silva MM, Musungaie DB et al. Molnupiravir for Oral Treatment of Covid-19 in Nonhospitalized Patients. N Engl J Med. 2022;386(6):509-520.
5. Takashita E, Kinoshita N, Yamayoshi S, et al. Efficacy of Antibodies and Antiviral Drugs against Covid-19 Omicron Variant. N Engl J Med. 2022;386(10):995-998.
6. Hammond J, Leister‑Tebbe H, Gardner A et al. Oral Nirmatrelvir for High‑Risk, Nonhospitalized Adults with Covid-19. N Engl J Med. 2022;386(15):1397-1408. doi:10.1056/NEJMoa2118542.
7. Beigel JH, Tomashek KM, Dodd LE et al. Remdesivir for the Treatment of Covid-19 - Final Report. N Engl J Med. 2020;383(19):1813-1826.
8. RECOVERY Collaborative Group, Horby P, Lim WS et al. Dexamethasone in Hospitalized Patients with Covid-19. N Engl J Med. 2021;384(8):693-704.
9. Prendecki M, Clarke C, Gleeson S et al. Detection of SARS‑CoV - 2 Antibodies in Kidney Transplant Recipients. J Am Soc Nephrol. 2020;31(12):2753-2756.
10. Magicova M, Fialova M, Zahradka I et al. Humoral response to SARS‑CoV - 2 is well preserved and symptom dependent in kidney transplant recipients. Am J Transplant. 2021;21(12):3926-3935.
11. Bertrand D, Hamzaoui M, Drouot L et al. SARS‑CoV - 2-specific Humoral and Cellular Immunities in Kidney Transplant Recipients and Dialyzed Patients Recovered From Severe and Nonsevere COVID-19. Transplant Direct. 2021;7(12):e792.
12. Boyarsky BJ, Werbel WA, Avery RK, et al. Antibody Response to 2-Dose SARS‑CoV - 2 mRNA Vaccine Series in Solid Organ Transplant Recipients. JAMA. 2021;325(21):2204-2206.
13. Magicova M, Zahradka I, Fialova M et al. Determinants of Immune Response to Anti‑SARS‑CoV - 2 mRNA Vaccines in Kidney Transplant Recipients: A Prospective Cohort Study. Transplantation. 2022;106(4):842-852.
14. Chavarot N, Ouedrani A, Marion O et al. Poor Anti‑SARS‑CoV - 2 Humoral and T‑cell Responses After 2 Injections of mRNA Vaccine in Kidney Transplant Recipients Treated With Belatacept. Transplantation. 2021;105(9):e94-e95.
15. Li P, Wang Y, Lavrijsen M et al. SARS‑CoV - 2 Omicron variant is highly sensitive to molnupiravir, nirmatrelvir, and the combination. Cell Res. 2022;32(3):322-324.
16. Aslam S, Adler E, Mekeel K, Little SJ. Clinical effectiveness of COVID-19 vaccination in solid organ transplant recipients. Transpl Infect, DiS. 2021;23(5):e13705.
17. Zahradka I, Petr V, Modos I, Magicova M, Dusek L, Viklicky O. Association Between SARS‑CoV - 2 Messenger RNA Vaccines and Lower Infection Rates in Kidney Transplant Recipients : A Registry‑Based Report [published online ahead of print, 2022 May 3]. Ann Intern Med. 2022;M21-2973.
18. Callaghan CJ, Mumford L, Curtis RMK et al. Real‑world Effectiveness of the Pfizer‑BioNTech BNT162b2 and Oxford‑AstraZeneca ChAdOx1-S Vaccines Against SARS‑CoV - 2 in Solid Organ and Islet Transplant Recipients. Transplantation. 2022;106(3):436-446.
19. Bruxvoort KJ, Sy LS, Qian L et al. Effectiveness of mRNA-1273 against delta, mu, and other emerging variants of SARS‑CoV - 2: test negative case‑control study. BMJ. 2021;375:e068848. Published 2021 Dec 15.
20. Andrews N, Stowe J, Kirsebom F et al. Covid-19 Vaccine Effectiveness against the Omicron (B.1. 1. 529) Variant. N Engl J Med. 2022;386(16):1532-1546.
Štítky
Diabetológia Endokrinológia Interné lekárstvo
Článek Hlavní téma – NefrologieČlánek Incidentalomy štítné žlázy
Článok vyšiel v časopiseVnitřní lékařství
Najčítanejšie tento týždeň
2022 Číslo 7- Parazitičtí červi v terapii Crohnovy choroby a dalších zánětlivých autoimunitních onemocnění
- Intermitentní hladovění v prevenci a léčbě chorob
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Statinová intolerance
- Monoklonální protilátky v léčbě hyperlipidemií
-
Všetky články tohto čísla
- Hlavní téma – Nefrologie
- Současné možnosti zpomalení progrese chronického onemocnění ledvin
- Expertní stanovisko ke spolupráci diabetologů a internistů s nefrology v péči o nemocné s chronickým onemocněním ledvin
- Glomerulonefritidy asociované s infekcemi
- Novinky v léčbě renální anémie – erytropoetin vs. inhibitory prolylhydroxylázy?
- Covid-19 u nemocných po transplantaci ledviny
- Reaktivní, infekční nebo postinfekční artritida?
- Účinek inhibitoru SGLT2 empagliflozinu na stabilizaci průběhu srdečního selhání s možností dalších intervencí u pacienta s HFrEF
- Nové technologie ve vývoji hypolipidemik. Inclisiran (LEQVIO®)
- Léčba hypertenze starších osob a její úskalí
- Incidentalomy štítné žlázy
- Můžeme novou léčbou ovlivnit dosavadní terapií neřešený zánět a fibrózu u pacientů s DM2 a CKD?
- Vnitřní lékařství
- Archív čísel
- Aktuálne číslo
- Iba online
- Informácie o časopise
Najčítanejšie v tomto čísle- Reaktivní, infekční nebo postinfekční artritida?
- Incidentalomy štítné žlázy
- Novinky v léčbě renální anémie – erytropoetin vs. inhibitory prolylhydroxylázy?
- Současné možnosti zpomalení progrese chronického onemocnění ledvin
Prihlásenie#ADS_BOTTOM_SCRIPTS#Zabudnuté hesloZadajte e-mailovú adresu, s ktorou ste vytvárali účet. Budú Vám na ňu zasielané informácie k nastaveniu nového hesla.
- Časopisy



