Úspěšné použití methylenové modři u pacienta v refrakterním šoku na veno-arteriální extrakorporální membránové oxygenaci
Succesful use of methylene blue in a patient with refractory shock on veno-arterial extracorporeal membrane oxygenation
Refractory circulatory shock is associated with excessive mortality in critically ill patients. Non-adrenergic vasopressors, including methylene blue, are often considered as an adjuvant therapy to the ordinary vasopressor treatment. In this case report we present a case of successful use of methylene blue reversing refractory septic shock in a patient on veno-arterial extracorporeal membrane oxygenation due to septic cardiomyopathy.
Keywords:
methylene blue – distributive shock – refractory vasoplegia – cardiomyopathy – extracorporeal membrane oxygenation
Authors:
M. Pořízka 1; J. Kunstýř 1; P. Kopecký 1; M. Balík 1
Authors‘ workplace:
Klinika anesteziologie, resuscitace a intenzivní medicíny, Všeobecná fakultní nemocnice v Praze, 1. lékařská fakulta, Univerzita Karlova
1
Published in:
Anest. intenziv. Med., 28, 2017, č. 5, s. 305-308
Category:
Intesive Care Medicine - Case Report
Overview
Refrakterní cirkulační šok představuje u kriticky nemocných stav s vysokou mortalitou. Non-adrenergní vazopresory, mezi něž patří i methylenová modř, získávají stále na významu jako tzv. záchranná léčba u vazoparalytických stavů. V této kazuistice popisujeme případ úspěšného zvládnutí refrakterního šoku u pacienta se septickou kardiomyopatií na veno-arteriální extrakorporální membránové oxygenaci, u něhož maximální krevní průtoky této podpory nestačily k udržení adekvátního perfuzního tlaku.
Klíčová slova:
methylenová modř – distributivní šok – refrakterní vazoplegie – kardiomyopatie – extrakorporální membránová oxygenace
ÚVOD
Cirkulační šok s hypotenzí a nutností podávání vysoké vazopresorické podpory nadále představuje u kriticky nemocných stav s vysokou nemocniční mortalitou přesahující 50 % [1]. Nezávisle na etiologii oběhového selhání je jeho progrese do tzv. refrakterního šoku, který je v literatuře nejčastěji definován jako šok s noradrenergní podporou vyšší než 0,5 µg/kg/min [2], spojena s dalším významným navýšením mortality [3]. Mechanismem je vždy různě závažná distributivní forma šoku spouštěná systémovou hypoperfuzí tkání vedoucí k rozvoji systémové zánětlivé odpovědi a generalizované vazodilataci. Patofyziologicky se nejvíce uplatňuje cytokiny indukovaná hyperprodukce oxidu dusnatého, aktivace ATP-senzitivních draselných kanálů v cévním endotelu, deficience endogenního vazopresinu či relativní kortikosteroidová insuficience [2].
V poslední době se při refrakterním šoku nezvladatelném běžnými vazopresory začaly používat nové postupy jako záchranná léčba (tzv. „rescue“ terapie). Vedle substituce kortikosteroidů je to použití tzv. non-adrenergních vazopresorů, jako jsou methylenová modř, vazopresin či terlipresin [4]. Výsledky klinických studií provedené s těmito prostředky potvrzují příznivé ovlivnění refrakterního šoku ve smyslu poklesu dávek vazopresivně působících katecholaminů a rychlejšího zvládnutí šoku. Nicméně efekt na mortalitu je prozatím nejasný [5].
Methylenová modř je tradičně používána jako redukční činidlo při léčbě methemoglobinemie, stále častěji se však stává součástí záchranných postupů při léčbě refrakterního distributivního šoku. Úspěšné použití bylo dokumentováno u pacientů s vazoplegickým syndromem po použití mimotělního oběhu, u pacientů v septickém šoku či u letálních otrav dihydropyridiny [5]. Prezentujeme zde případ úspěšného použití methylenové modři u pacienta v refrakterním septickém šoku napojeného na veno-arteriální extrakorporální membránovou oxygenaci (VA-ECMO) pro extrémní systolickou dysfunkci při kombinované septické a alkoholové kardiomyopatii.
Popis případu
Třicetiletý alkoholik a bezdomovec byl nalezen v silném mrazu venku v bezvědomí. Při příjezdu rychlé záchranné služby byl částečně v kontaktu, ale delirantní a halucinující. Spontánně ventilující bez nutnosti intubace byl transportován na naše pracoviště, kde byl při příjmu diagnostikován těžký minerálový rozvrat (hyponatremie 115 mmol/l, hypochloremie 76 mmol/l) s hypoglykemií (1,8 mmol/l) a hypotermie (33,6 °C). Po zahřátí k normotermii a korekci hypoglykemie a mineralogramu přetrvávalo u pacienta těžké hyperaktivní delirium s nutností intravenózní aplikace neuroleptik (Haloperidol) i fyzického omezení. Druhý den po příjmu došlo u pacienta k rozvoji těžké bilaterální pneumonie (agens Staphylococcus aureus) s progresí do respirační insuficience a nutností orotracheální intubace s napojením na umělou plicní ventilaci. Oběhově stav progredoval do obrazu septického šoku s noradrenergní podporou 0,1 µg/kg/min. Bylo provedeno kontrolní transtorakální echokardiografické vyšetření (TTE) s nálezem středně těžké systolické dysfunkce levé komory (LK) s ejekční frakcí (EF) 40 % při difuzní hypokinezi stěn myokardu, s dobrou funkcí pravé komory a bez nálezu významných chlopenních vad. Vzhledem k nepřítomnosti ischemických elektrokardiografických změn, negativitě kardioenzymů, věku a anamnéze pacienta byla tato dysfunkce LK hodnocena jako alkoholická kardiomyopatie.
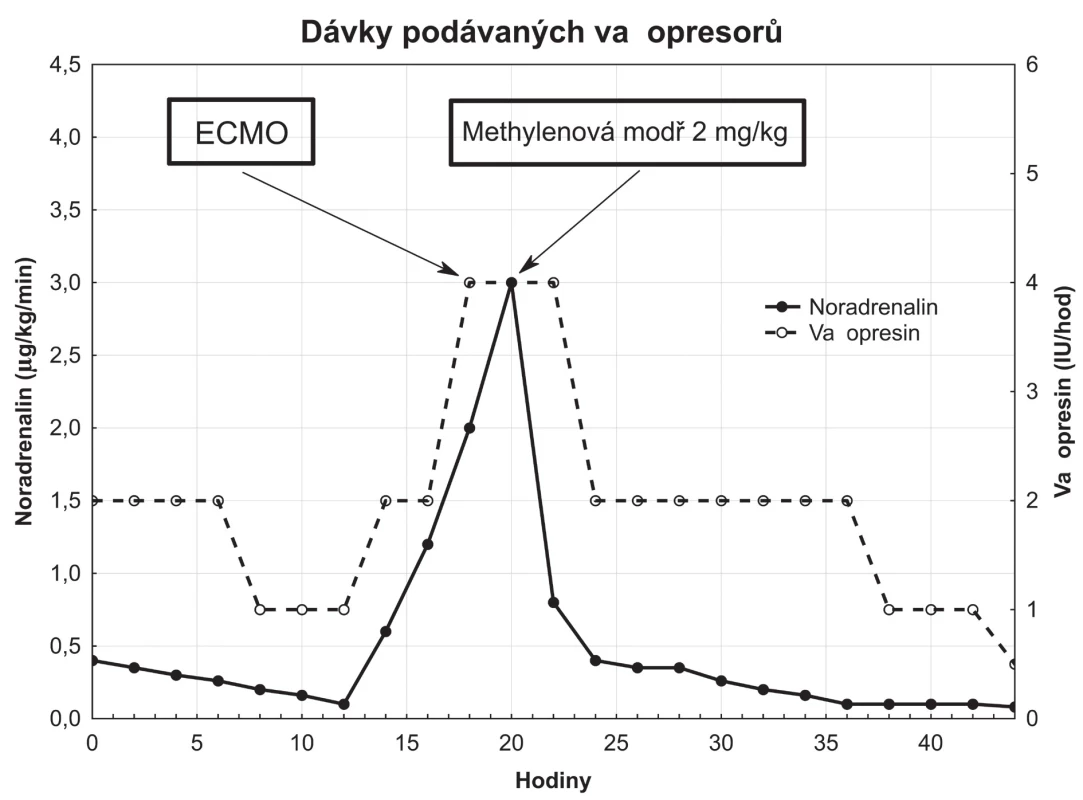
Čtvrtý den hospitalizace došlo ke krvácení z duodenálního vředu s těžkou oběhovou nestabilitou a nutností masivní volumoterapie. Krvácení bylo nakonec úspěšně ošetřeno endoskopicky adrenalinovým opichem a aplikací čtyř klipů. Po přechodné hemodynamické stabilizaci dochází následující den k nové atace sepse při recidivě pneumonie. I přes eskalaci antibiotické léčby a volumoterapii došlo k progresi šokového stavu. Ani maximální vazopresorickou podporou (noradrenalin 2 µg/kg/min a vazopresin 4 jednotky/hod) a bolusem kortikoidů (hydrokortizon 100 mg i. v.) se nedařilo udržet adekvátní perfuzní tlak. Na kontrolním TTE bylo patrné zhoršení nálezu s těžkou systolickou dysfunkcí obou komor (EF LK 10 %). Tento další pokles systolické funkce LK byl hodnocen jako rozvoj septické kardiomyopatie v terénu alkoholového postižení myokardu. Eskalace dobutaminu až na 15 µg/kg/min byla bez efektu na kontraktilitu myokardu. Stav velmi rychle vyústil v zástavu oběhu při srdeční elektromechanické disociaci. Byla zahájena kardiopulmonální resuscitace automatickým systémem LUCAS a rozhodnuto o zavedení VA-ECMO periferním přístupem. Po úspěšném zavedení ECMO kanyl cestou arteria femoralis (21F) a vena femoralis (29F, obě Duraflo Edwards Lifesciences, Irviene, CA, USA) byla mechanická podpora úspěšně spuštěna s maximálními krevními průtoky 6 l/min (Maquet Rotaflow RF 32, Maquet Cardiopulmonary AG, Hirrlingen, Německo), a to za 20 minut od oběhového kolapsu. Po přechodné stabilizaci na VA-ECMO dochází k další progresi refrakterního šoku a i přes korekci preload a navýšení noradrenergní podpory na 3 µg/kg/min byl pacient nadále těžce hypotenzní se středním arteriálním tlakem 40 mmHg. Jako „ultimum refugium“ byla aplikována methylenová modř (methylthioninium chlorid) v dávce 2 mg/kg jako kontinuální infuze během 30 minut. Již během podávání dochází k postupné hemodynamické stabilizaci a poklesu podpory noradrenalinem na 0,8 µg/kg/min (viz graf).
V následujících dnech se klinický stav postupně zlepšil s dalším poklesem oběhové podpory a regresí pneumonie. Echokardiograficky došlo ke zlepšení funkce LK na EF 15‒20 % a normalizaci funkce pravé komory. S předpokladem odpojování od srdeční podpory byla pacientovi po sedmi dnech na VA-ECMO podána infuze levosimendanu v dávce 12,5 mg formou kontinuální infuze 0,1 µg/kg/min, nicméně echokardiograficky bez známek dalšího zlepšení funkce myokardu. I přes těžkou systolickou dysfunkci LK (EF 25 %) byl pacient následující 8. den podpory úspěšně od VA-ECMO odpojen.
Po vysazení sedace byl pacient 14. den hospitalizace při plném vědomí bez neurologického deficitu extubován. Pro relabující plicní zánět byl opět reintubován, tentokrát již hemodynamicky stabilní.
V dalším klinickém průběhu dominovalo velmi pomalé odvykání pacienta od umělé plicní ventilace s nutností provedení punkční dilatační tracheostomie 19. den hospitalizace a postantibiotický průjem, bez průkazu klostridiové infekce. 26. den od příjmu byl pacient úspěšně odpojen od umělé plicní ventilace a následně 27. den byla odstraněna tracheostomická kanyla. Ventilačně suficientní a bez katecholaminové podpory byl 30. den hospitalizace přeložen na spádovou koronární jednotku v místě původního bydliště.
Diskuse
Tato kazuistika popisuje úspěšné zvládnutí refrakterního septického šoku bolusem methylenové modři u pacienta na VA-ECMO. Septický šok s přechodem do refrakterity zůstává navzdory medicínskému pokroku stále stavem s vysokou mortalitou [7]. Součástí klinického obrazu bývá často rozvoj septické kardiomyopatie s poklesem systolické funkce LK a snížením srdečního výdeje [8]. VA-ECMO představuje postup, jak mnohdy toto katastrofické, nicméně většinou přechodné snížení srdečního výdeje úspěšně překlenout [9]. Problém může nastat, když u pacienta připojeného na VA-ECMO dochází k další progresi vazoparalýzy a cirkulačního šoku. Krevní průtoky na VA-ECMO podléhají technickému omezení při specifické velikosti perfuzních kanyl s maximem 6‒6,5 l/min. Při progredující vazoparalýze a vzrůstajících požadavcích na efektivní cirkulující krevní objem nemusí být i přes dodatečnou volumoterapii a běžnou vazopresorickou léčbu maximální dosažitelné krevní průtoky na VA-ECMO dostatečné a v tom případě může pacient zemřít v pokračujícím refrakterním šoku s nezvladatelnou hypotenzí.
Methylenová modř představuje jeden z tzv. non-adrenergních vazopresorů, které jsou v případě refrakterního šoku stále častěji užívány jako tzv. „rescue“ léčba. Mechanismus jejího účinku spočívá v interferenci se signální cestou oxidu dusnatého v periferních cévách, specificky v inhibici tvorby cyklického guanosin-fosfát mononukleotidu a ve svém důsledku pak v periferní cévní vazokonstrikci [6]. Methylenová modř byla úspěšně použita u pacientů s distributivní formou šoku, nicméně se vždy jednalo o případové studie či klinické studie s malým počtem pacientů [4, 6]. Efekt na mortalitu proto není spolehlivě znám, jak dokazuje recentní metaanalýza [4, 5]. Dávkování methylenové modři v této indikaci bývá v literatuře uváděno jako bolusové 1‒2 mg/kg, s eventuálně krátkou kontinuální infuzí 0,25 mg/kg/hod [5]. V našem případě byl již efektivní bolus 2 mg/kg, který u pacienta na VA-ECMO, těžce hypotenzního i přes maximální noradrenergní i non-adrenergní podporu (vazopresin, kortikoidy), vedl k dosažení adekvátních perfuzních tlaků (střední arteriální tlak 70 mmHg). Navzdory tomu může mít podání methylenové modři i nežádoucí účinky. Ve vyšších dávkách je v literatuře popisován rozvoj dušnosti, křečí či serotoninového syndromu. Překročení toxické dávky 7 mg/kg pak může indukovat paradoxní methemoglobinemii nebo akutní hemolytickou anemii [5]. Ani jednu z těchto komplikací jsme při jednorázovém bolusovém podání u našeho pacienta nezaznamenali.
Závěrem lze konstatovat, že methylenová modř může úspěšně zvrátit progredující vazoparalýzu při refrakterním šoku na VA-ECMO, kdy technické limitace oběhové podpory již nedovolují další navyšování krevního průtoku.
Práce je původní, nebyla publikována ani není zaslána k recenznímu řízení do jiného média.
Autoři prohlašují, že v souvislosti s tématem práce nemají střet zájmů.
Všichni autoři rukopis četli, souhlasí s jeho zněním a zasláním do redakce časopisu Anesteziologie a intenzivní medicína.
Echokardiografická monitorace byla podporována z projektu reg.no. CZ.2.16/3.1.00/21565 z OP Prague Competitiveness.
Do redakce došlo dne 20. 3. 2017.
Do tisku přijato dne 15. 6. 2017.
Adresa pro korespondenci:
MUDr. Michal Pořízka, Ph.D., E.D.I.C.
michal.porizka@vfn.cz
Sources
1. De Backer D, Biston P, Devriendt J, Madl C, Chochrad D, Aldecoa C, Brasseur A, Defrance P, Gottignies P, Vincent JL. SOAP II Investigators. Comparison of dopamine and norepinephrine in the treatment of shock. N Engl J Med. 2010;362 : 779–789. doi: 10.1056/NEJMoa0907118.
2. Bassi E, Park M, Azevedo LC. Therapeutic strategies for high-dose vasopressor-dependent shock. Crit Care Res Pract. 2013;2013 : 654–708. doi: 10.1155/2013/654708.
3. Jenkins CR, Gomersall CD, Leung P, Joynt GM. Outcome of patients receiving high dose vasopressor therapy: a retrospective cohort study. Anaesth Intensive Care. 2009;37 : 286–9.
4. Belletti A, Musu M, Silvetti S, Saleh O, Pasin L, Monaco F, Hajjar LA, Fominskiy E, Finco G, Zangrillo A, Landoni G. Non-Adrenergic Vasopressors in Patients with or at Risk for Vasodilatory Shock. A Systematic Review and Meta-Analysis of Randomized Trials. PLoS One. 2015;10:e0142605. doi: 10.1371/journal.pone.0142605.
5. Avni T, Lador A, Lev S, Leibovici L, Paul M, Grossman A. Vasopressors for the Treatment of Septic Shock: Systematic Review and Meta-Analysis. PLoS One.;108:e0129305. doi: 10.1371/journal.pone.0129305.
6. Jang DH, Nelson LS, Hoffman RS. Methylene blue for distributive shock: a potential new use of an old antidote. J Med Toxicol. 2013;9 : 242–9. doi: 10.1007/s13181-013-0298-7.
7. Vincent JL, Sakr Y, Sprung CL, Ranieri VM, Reinhart K, Gerlach H, Moreno R, Carlet J, Le Gall JR, Payen D. Sepsis Occurrence in Acutely Ill Patients Investigators. Sepsis in European intensive care units: results of the SOAP study. Crit Care Med. 2006;34 : 344–53.
8. Price S, Anning PB, Mitchell JA, Evans TW. Myocardial dysfunction in sepsis: mechanisms and therapeutic implications. Eur Heart J. 1999;20 : 715–24.
9. Huang CT, Tsai YJ, Tsai PR, Ko WJ. Extracorporeal membrane oxygenation resuscitation in adult patients with refractory septic shock. J Thorac Cardiovasc Surg. 2013;146 : 1041–1046.
Labels
Anaesthesiology, Resuscitation and Inten Intensive Care MedicineArticle was published in
Anaesthesiology and Intensive Care Medicine

2017 Issue 5
-
All articles in this issue
-
Anestezie v Rakousko-Uhersku během I. světové války a po vzniku samostatného československého státu
Část II – Metody místní anestezie - Anestezie a analgezie plodu při intervencích in utero
- Neurotoxicita anestetik a dozrávající dětský mozek
- Endoteliální glykokalyx a tekutinová terapie v intenzivní a perioperační medicíně
- Kognitivní poruchy v perioperační a intenzivní péči
- Úspěšné použití methylenové modři u pacienta v refrakterním šoku na veno-arteriální extrakorporální membránové oxygenaci
- Echokardiografické vyšetření u akutního aortálního syndromu
-
Anestezie v Rakousko-Uhersku během I. světové války a po vzniku samostatného československého státu
- Anaesthesiology and Intensive Care Medicine
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Úspěšné použití methylenové modři u pacienta v refrakterním šoku na veno-arteriální extrakorporální membránové oxygenaci
- Neurotoxicita anestetik a dozrávající dětský mozek
- Kognitivní poruchy v perioperační a intenzivní péči
- Endoteliální glykokalyx a tekutinová terapie v intenzivní a perioperační medicíně
