Editorial
Published in:
Klin Onkol 2021; 34(Supplementum 1): 4-5
Category:
Editorial
Léčba především nemalobuněčných plicních karcinomů (non-small cell lung cancer – NSCLC) zaznamenala snad největší pokrok mezi všemi solidními nádory. Preklinické a klinické novinky se objevují téměř „každý den“. Každá přehledná publikace se tak může jevit při svém vydání jako zastaralá. Opak je pravdou. Shrnutí a zejména názory nové generace odborníků jsou klíčem k budoucnosti. Je zásluhou Klinické onkologie jako vůdčího odborného časopisu v české onkologii, že umožnila v celé šíři prezentovat odborné názory na aktuální problematiku plicních karcinomů.
Kapitola Karcinom plic – diagnostika a včasný záchyt je klíčem k posunu léčby do časných stadií, která jsou stále v menšině. Záchyt preklinických stadií pomocí molekulární detekce i při propracované metodice tekutých biopsií je stále klinickou iluzí a je třeba zabránit předčasnému zneužití někdy falešně proklamované diagnostiky „z kapky krve“. Klíčem k časné diagnostice je i přes řadu kontroverzí adresný screening. Záchyt časných stadií přispěje k nárůstu chirurgických intervencí a v kombinaci s adjuvantní léčbou významně zvýší šanci na dlouhodobé přežití. Při předpokládaném nárůstu indikací adjuvantní léčby nemusí dojít k proklamovanému razantnímu ušetření nákladů na inovativní léčbu. Cílená terčová léčba a imunoterapie se posunou do časnějších stadií. Příkladem nových indikací adjuvantního podání jsou výsledky klinické studie ADAURA [1]. Výsledky randomizované studie fáze II NEOSTAR [2] jsou předpovědí neoadjuvantní a adjuvantní indikace check point inhibitorů.
Při rozvoji precizní genomické medicíny zasáhl klinickou onkologii exponenciální nárůst medicínských informací. Důsledky trvalého nárůstu vědeckých informací odhadl v 80. letech 20. století profesor Vladimír Vondráček: „Věda se rozrostla katastrofálně, tragicky. Nelze zvládnout všechny informace oboru, ani jejich poměrně malou část. Z toho rezultují pro některé osoby těžké výčitky. Je obtížné stanovit ideální typ moderního vědeckého pracovníka, jeho rozložení vědomostí. Svůj obor samozřejmě má znát, některé jeho části intenzivně, ale má mít i určité všeobecné vzdělání a doplňovat si je, aby mohl pochopit někdy neočekávané souvislosti a vztahy [3].“ Nárůst nových medicínských informací přináší nárůst individuálních řešení klinických situací, které vyžadují mezioborový přístup. Klíčem rozhodovacího procesu při indikaci chirurgické intervence a časové sekvence multimodalitní léčby časného a lokálně pokročilého NSCLC je proto rozhodnutí multidisciplinárního týmu (MTD), viz kapitola Role multidisciplinárního týmu a molekulárního tumor boardu v léčbě pacienta s karcinomem plic. Kapitoly Chirurgická léčba karcinomu plic a Nové možnosti léčby časného a lokálně pokročilého NSCLC jsou zpracovány ve sborníku odděleně, ale z pohledu multidisciplinarity spolu úzce souvisejí. Pokud MTD stanoví kurativní (radikální) léčebný cíl, je adekvátní využití všech léčebných modalit v předem plánované návaznosti klinickou povinností. Jedinou zárukou ukončení „necíleného podávání cílené léčby“ je klinická utilizace personalizované a precizní onkologie. Precizní onkologie se neobejde bez komprehenzivního molekulárního vyšetření zahrnujícího sekvenování nové generace (new generation sequencing – NGS), transkriptomiku a analýzu proteinů a další omické metody. Bez dostupné, adekvátně prováděné molekulární diagnostiky není možné rozhodovat o výběru cílené léčby. Výběr a zahájení léčby bez určení prediktivních biomarkerů nebudou v brzké budoucnosti možné. Neprovedení molekulárního vyšetření může nemocného poškodit. Příkladem jsou nemalobuněčné plicní karcinomy, kde se výběr správné léčby neobejde bez molekulární subklasifikace (mutace EGFR, ALK, ROS a další). Neznalost přítomné aberace může nemocnému významně snížit šanci na dlouhodobé přežití. Pro kliniky je proto kapitola Prediktivní testování u nemalobuněčného karcinomu plic povinnou četbou. Výskyt některých aberací je relativně prevalenčně omezený (např. ALK fúze < 5 %), ale efekt terčové léčby je vzhledem k její precizní definici dramaticky lepší ve srovnání s nádory, u kterých nebyla molekulární aberace detekována. Dobrou zprávou je, že paralelně s identifikací nových řídících molekulárních aberací přibývají cílené terčové léky. Postupná implementace všech inovativních terčových léků (tab. 1) do terapeutického armamentaria nemalobuněčných karcinomů plic je cestou prodlužující přežití nemocných. Tab. 1 zahrnuje léky povolené FDA a nevyjadřuje současný stav registrace a indikačních doporučení jednotlivých léků v ČR [4].
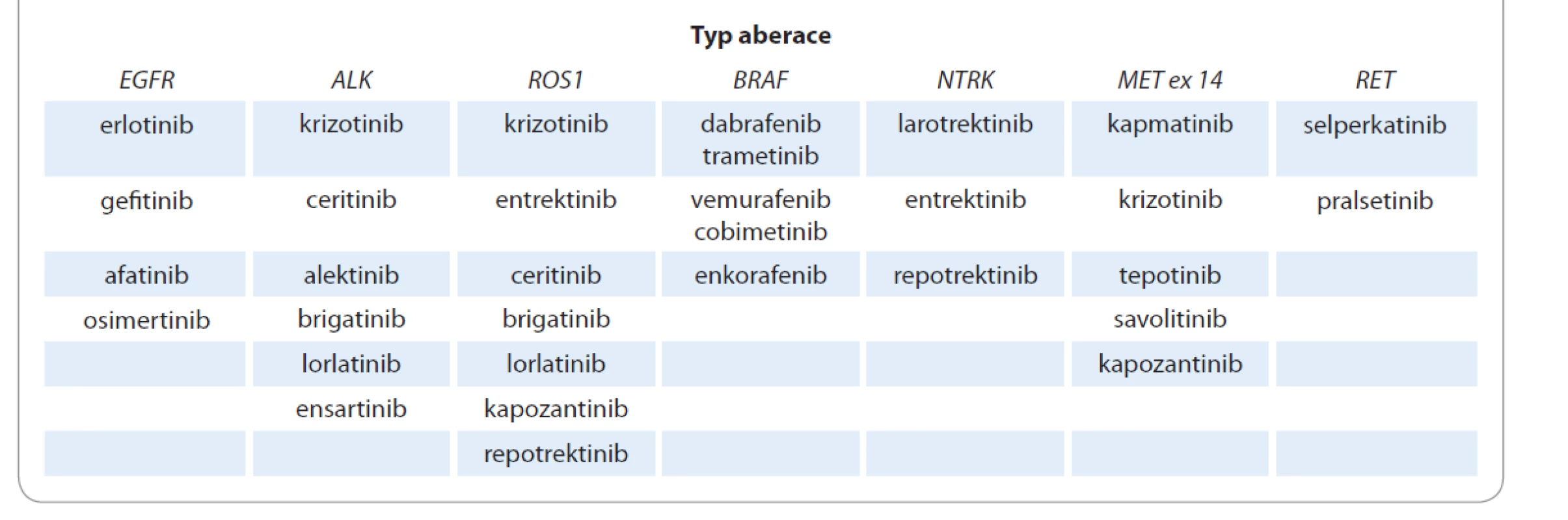
Problematice terčové léčby NSCLC je ve sborníku věnována samostatná kapitola Cílená léčba nemalobuněčného karcinomu plic.
„Znovuobrození“ imunoterapie patří mezi zásadní události poslední doby, a proto jí byla věnována samostatná kapitola, a sice Imunoterapie v léčbě nemalobuněčného karcinomu plic. Inhibitory kontrolních bodů imunitní reakce, „check point inhibitory“, se staly nepostradatelnou modalitou onkologické léčby. Jedná se o terapeutickou modalitu s odlišnými mechanizmy účinku oproti chemoterapii a cílené terčové léčbě, která má odlišný profil nežádoucích účinků a vyžaduje odlišný management. Přesná (precizní) imunoterapie je zatím iluzorní. Imunoterapie je sice účinná napříč solidními nádory, ale hrdlo účinnosti je poměrně úzké a léčebné odpovědi lze zatím dosáhnout jen u 20–35 % léčených pacientů. Širší hrdlo účinnosti je u nejvíce imunogenních nádorů, jako jsou maligní melanomy, renální a plicní karcinomy. Limitací této inovované terapeutické modality je absence širší palety prediktivních biomarkerů a imunomarkerů. Roztříštěná metodika stanovení exprese PD-L1 je příkladem nevhodným k následování. Pravděpodobnost léčebné odpovědi se zvyšuje s narůstající expresí PD-L1, ale u některých PD-L1 negativních nádorů lze navodit léčebnou odpověď. Řešením není prohlásit expresi PD-L1 za zbytečný a nepotřebný biomarker. Do doby, než budou definovány a klinicky validovány inovativní imunoprediktory, zůstane exprese PD-L1 klinickým klíčem imunopredikce pro PD-L1 inhibitory. Identifikace a validace dalších prediktorů je proto klinickou urgencí. Budoucnost imunopredikce není v izolovaném, ale naopak v kombinovaném využití prediktorů při utilizaci informací z nádoru a nádorového mikroprostředí, ale i periferního imunomu a imunologické charakteristiky hostitele nemoci, vč. jeho mikrobiomu. Úvahy o aplikaci kombinované imunochemoterapie v 1. linii bez potřeby znalosti exprese PD-L1 je cestou, jak zahubit precizní imunoterapii. Odborná lékařská veřejnost zastoupená odbornými společnostmi bude vždy nezávisle formulovat své názory a doporučení. Cílem je zúžení indikačního hrdla, zvýšení účinnosti a eliminace rizik nežádoucích projevů. Imunoterapie check point inhibitory působí bez ohledu na lokalizaci a typ tkáně. V některých indikacích je možné imunoterapii považovat za nádorově, lokalizačně a histologicky agnostickou léčbu. Aktuální kontroverzní otázky imunoterapie (primární, sekundární rezistence, hyperprogrese, hypertoxicita, doba podávání, reindukce) musejí být též urgentně řešeny. Aplikace precizní medicíny vyžaduje změnu klinického myšlení – nejedná se o výběr nejlepší léčebné modality, ale o výběr (optimální) léčby pro každého nemocného.
Většina odborných textů se zabývá problematikou NSCLC. Léčba malobuněčných karcinomů plic nezaznamenala v posledních téměř 20 letech žádné zásadní změny. Chemoterapie se prakticky nezměnila, ale stále zůstává klíčovou systémovou modalitou. Pro uplatnění cílené terčové léčby chybí targetabilní genové aberace. Výsledky kombinace chemoterapie s check point inhibitory [5,6] jsou po dlouhém čekání konečně pozitivní. Modulovaná imunoterapie, imunokonjugáty, PARP inhibice, identifikace targetabilních epigenetických struktur v kontextu NGS vyžadují větší výzkumné nasazení. Zařazení kapitoly Pokroky v léčbě malobuněčného karcinomu plic je proto víc než nutné.
Závěrem uvádím vlastní nezávislou předpověď budoucího využití chemoterapie, imunoterapie a terčové léčby v léčbě nemalobuněčných plicních karcinomů po roce 2025:
více než 70 % nemocných bude v průběhu onemocnění léčeno imunoterapií;
více než 40 % nemocných bude léčeno cílenou terčovou léčbou v 1. linii;
dojde k útlumu indikací samostatné chemoterapie v 1. linii léčby.
Vlastní predikce budoucího využití chemoterapie, imunoterapie a terčové léčby u malobuněčných plicních karcinomů po roce 2025:
více než 50 % nemocných se solidními nádory bude léčeno imunoterapií v průběhu onemocnění;
chemoterapie zůstane klíčovou modalitou léčby;
novou klinickou systémovou modalitou se stanou imunokonjugáty.
Léčba především nemalobuněčných plicních karcinomů (non-small cell lung cancer – NSCLC) zaznamenala snad největší pokrok mezi všemi solidními nádory. Preklinické a klinické novinky se objevují téměř „každý den“. Každá přehledná publikace se tak může jevit při svém vydání jako zastaralá. Opak je pravdou. Shrnutí a zejména názory nové generace odborníků jsou klíčem k budoucnosti. Je zásluhou Klinické onkologie jako vůdčího odborného časopisu v české onkologii, že umožnila v celé šíři prezentovat odborné názory na aktuální problematiku plicních karcinomů.
Kapitola Karcinom plic – diagnostika a včasný záchyt je klíčem k posunu léčby do časných stadií, která jsou stále v menšině. Záchyt preklinických stadií pomocí molekulární detekce i při propracované metodice tekutých biopsií je stále klinickou iluzí a je třeba zabránit předčasnému zneužití někdy falešně proklamované diagnostiky „z kapky krve“. Klíčem k časné diagnostice je i přes řadu kontroverzí adresný screening. Záchyt časných stadií přispěje k nárůstu chirurgických intervencí a v kombinaci s adjuvantní léčbou významně zvýší šanci na dlouhodobé přežití. Při předpokládaném nárůstu indikací adjuvantní léčby nemusí dojít k proklamovanému razantnímu ušetření nákladů na inovativní léčbu. Cílená terčová léčba a imunoterapie se posunou do časnějších stadií. Příkladem nových indikací adjuvantního podání jsou výsledky klinické studie ADAURA [1]. Výsledky randomizované studie fáze II NEOSTAR [2] jsou předpovědí neoadjuvantní a adjuvantní indikace check point inhibitorů.
Při rozvoji precizní genomické medicíny zasáhl klinickou onkologii exponenciální nárůst medicínských informací. Důsledky trvalého nárůstu vědeckých informací odhadl v 80. letech 20. století profesor Vladimír Vondráček: „Věda se rozrostla katastrofálně, tragicky. Nelze zvládnout všechny informace oboru, ani jejich poměrně malou část. Z toho rezultují pro některé osoby těžké výčitky. Je obtížné stanovit ideální typ moderního vědeckého pracovníka, jeho rozložení vědomostí. Svůj obor samozřejmě má znát, některé jeho části intenzivně, ale má mít i určité všeobecné vzdělání a doplňovat si je, aby mohl pochopit někdy neočekávané souvislosti a vztahy [3].“ Nárůst nových medicínských informací přináší nárůst individuálních řešení klinických situací, které vyžadují mezioborový přístup. Klíčem rozhodovacího procesu při indikaci chirurgické intervence a časové sekvence multimodalitní léčby časného a lokálně pokročilého NSCLC je proto rozhodnutí multidisciplinárního týmu (MTD), viz kapitola Role multidisciplinárního týmu a molekulárního tumor boardu v léčbě pacienta s karcinomem plic. Kapitoly Chirurgická léčba karcinomu plic a Nové možnosti léčby časného a lokálně pokročilého NSCLC jsou zpracovány ve sborníku odděleně, ale z pohledu multidisciplinarity spolu úzce souvisejí. Pokud MTD stanoví kurativní (radikální) léčebný cíl, je adekvátní využití všech léčebných modalit v předem plánované návaznosti klinickou povinností. Jedinou zárukou ukončení „necíleného podávání cílené léčby“ je klinická utilizace personalizované a precizní onkologie. Precizní onkologie se neobejde bez komprehenzivního molekulárního vyšetření zahrnujícího sekvenování nové generace (new generation sequencing – NGS), transkriptomiku a analýzu proteinů a další omické metody. Bez dostupné, adekvátně prováděné molekulární diagnostiky není možné rozhodovat o výběru cílené léčby. Výběr a zahájení léčby bez určení prediktivních biomarkerů nebudou v brzké budoucnosti možné. Neprovedení molekulárního vyšetření může nemocného poškodit. Příkladem jsou nemalobuněčné plicní karcinomy, kde se výběr správné léčby neobejde bez molekulární subklasifikace (mutace EGFR, ALK, ROS a další). Neznalost přítomné aberace může nemocnému významně snížit šanci na dlouhodobé přežití. Pro kliniky je proto kapitola Prediktivní testování u nemalobuněčného karcinomu plic povinnou četbou. Výskyt některých aberací je relativně prevalenčně omezený (např. ALK fúze < 5 %), ale efekt terčové léčby je vzhledem k její precizní definici dramaticky lepší ve srovnání s nádory, u kterých nebyla molekulární aberace detekována. Dobrou zprávou je, že paralelně s identifikací nových řídících molekulárních aberací přibývají cílené terčové léky. Postupná implementace všech inovativních terčových léků (tab. 1) do terapeutického armamentaria nemalobuněčných karcinomů plic je cestou prodlužující přežití nemocných. Tab. 1 zahrnuje léky povolené FDA a nevyjadřuje současný stav registrace a indikačních doporučení jednotlivých léků v ČR [4].
Problematice terčové léčby NSCLC je ve sborníku věnována samostatná kapitola Cílená léčba nemalobuněčného karcinomu plic.
„Znovuobrození“ imunoterapie patří mezi zásadní události poslední doby, a proto jí byla věnována samostatná kapitola, a sice Imunoterapie v léčbě nemalobuněčného karcinomu plic. Inhibitory kontrolních bodů imunitní reakce, „check point inhibitory“, se staly nepostradatelnou modalitou onkologické léčby. Jedná se o terapeutickou modalitu s odlišnými mechanizmy účinku oproti chemoterapii a cílené terčové léčbě, která má odlišný profil nežádoucích účinků a vyžaduje odlišný management. Přesná (precizní) imunoterapie je zatím iluzorní. Imunoterapie je sice účinná napříč solidními nádory, ale hrdlo účinnosti je poměrně úzké a léčebné odpovědi lze zatím dosáhnout jen u 20–35 % léčených pacientů. Širší hrdlo účinnosti je u nejvíce imunogenních nádorů, jako jsou maligní melanomy, renální a plicní karcinomy. Limitací této inovované terapeutické modality je absence širší palety prediktivních biomarkerů a imunomarkerů. Roztříštěná metodika stanovení exprese PD-L1 je příkladem nevhodným k následování. Pravděpodobnost léčebné odpovědi se zvyšuje s narůstající expresí PD-L1, ale u některých PD-L1 negativních nádorů lze navodit léčebnou odpověď. Řešením není prohlásit expresi PD-L1 za zbytečný a nepotřebný biomarker. Do doby, než budou definovány a klinicky validovány inovativní imunoprediktory, zůstane exprese PD-L1 klinickým klíčem imunopredikce pro PD-L1 inhibitory. Identifikace a validace dalších prediktorů je proto klinickou urgencí. Budoucnost imunopredikce není v izolovaném, ale naopak v kombinovaném využití prediktorů při utilizaci informací z nádoru a nádorového mikroprostředí, ale i periferního imunomu a imunologické charakteristiky hostitele nemoci, vč. jeho mikrobiomu. Úvahy o aplikaci kombinované imunochemoterapie v 1. linii bez potřeby znalosti exprese PD-L1 je cestou, jak zahubit precizní imunoterapii. Odborná lékařská veřejnost zastoupená odbornými společnostmi bude vždy nezávisle formulovat své názory a doporučení. Cílem je zúžení indikačního hrdla, zvýšení účinnosti a eliminace rizik nežádoucích projevů. Imunoterapie check point inhibitory působí bez ohledu na lokalizaci a typ tkáně. V některých indikacích je možné imunoterapii považovat za nádorově, lokalizačně a histologicky agnostickou léčbu. Aktuální kontroverzní otázky imunoterapie (primární, sekundární rezistence, hyperprogrese, hypertoxicita, doba podávání, reindukce) musejí být též urgentně řešeny. Aplikace precizní medicíny vyžaduje změnu klinického myšlení – nejedná se o výběr nejlepší léčebné modality, ale o výběr (optimální) léčby pro každého nemocného.
Většina odborných textů se zabývá problematikou NSCLC. Léčba malobuněčných karcinomů plic nezaznamenala v posledních téměř 20 letech žádné zásadní změny. Chemoterapie se prakticky nezměnila, ale stále zůstává klíčovou systémovou modalitou. Pro uplatnění cílené terčové léčby chybí targetabilní genové aberace. Výsledky kombinace chemoterapie s check point inhibitory [5,6] jsou po dlouhém čekání konečně pozitivní. Modulovaná imunoterapie, imunokonjugáty, PARP inhibice, identifikace targetabilních epigenetických struktur v kontextu NGS vyžadují větší výzkumné nasazení. Zařazení kapitoly Pokroky v léčbě malobuněčného karcinomu plic je proto víc než nutné.
Závěrem uvádím vlastní nezávislou předpověď budoucího využití chemoterapie, imunoterapie a terčové léčby v léčbě nemalobuněčných plicních karcinomů po roce 2025:
více než 70 % nemocných bude v průběhu onemocnění léčeno imunoterapií;
více než 40 % nemocných bude léčeno cílenou terčovou léčbou v 1. linii;
dojde k útlumu indikací samostatné chemoterapie v 1. linii léčby.
Vlastní predikce budoucího využití chemoterapie, imunoterapie a terčové léčby u malobuněčných plicních karcinomů po roce 2025:
více než 50 % nemocných se solidními nádory bude léčeno imunoterapií v průběhu onemocnění;
chemoterapie zůstane klíčovou modalitou léčby;
novou klinickou systémovou modalitou se stanou imunokonjugáty.
prof. MUDr. Luboš Petruželka, CSc.
Onkologická klinika 1. LF UK, VFN a ÚVN v Praze
Sources
1. Ramalingam SS, Vansteenkiste J, Planchard D et al. Overall survival with osimertinib in untreated, EGFR-mutated advanced NSCLC. N Engl J Med 2020; 382 : 41–50. doi: 10.1056/NEJMoa1913662.
2. Cascone T, William WN, Weissferdt A et al. Neoadjuvant nivolumab or nivolumab plus ipilimumab in operable non-small cell lung cancer: the phase 2 randomized NEOSTAR trial. Nat Med 2021; 27 (3): 504–514. doi: 10.1038/s41591-020-01224-2.
3. Vondráček V. Úvahy psychologicko-psychiatrické. Praha: Avicenum 1981.
4. NCCN clinical practise guidelines in oncology. [online]. Available from: https: //www.nccn.org/professionals/physician_gls/default.aspx.
5. Horn L, Mansfield AS, Szczęsna A et al. IMpower133 Study Group. First-line atezolizumab plus chemotherapy in extensive-stage small-cell lung cancer. N Engl J Med 2018; 379 (23): 2220–2229. doi: 10.1056/ NEJMoa1809064.
6. Paz-Ares L, Dvorkin M, Chen Y et al. Durvalumab plus platinum-etoposide versus platinum-etoposide in first-line treatment of extensive-stage small-cell lung cancer (CASPIAN): a randomised, controlled, open-label, phase 3 trial. Lancet 2019; 394 (10212): 1929–1939. doi: 10.1016/S0140-6736 (19) 32222-6.
Labels
Paediatric clinical oncology Surgery Clinical oncologyArticle was published in
Clinical Oncology

2021 Issue Supplementum 1
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Metamizole vs. Tramadol in Postoperative Analgesia
- Spasmolytic Effect of Metamizole
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
- Safety and Tolerance of Metamizole in Postoperative Analgesia in Children
-
All articles in this issue
- Lung cancer – dia nosis and early detection
- The role of multidisciplinary team and molecular tumor board in the treatment of a patient with lung cancer
- Predictive testing in non-small cell lung carcinoma
- Surgical treatment of lung cancer
- New treatment modalities in the early stage and locally advanced non-small cell lung cancer
- Targeted therapy of non-small cell lung cancer
- Immunotherapy in the treatment of non-small cell lung cancer
- Pokroky v léčbě malobuněčného karcinomu plic
- Editorial
- Future of lung cancer treatment
- Clinical Oncology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Lung cancer – dia nosis and early detection
- Surgical treatment of lung cancer
- Pokroky v léčbě malobuněčného karcinomu plic
- Future of lung cancer treatment
