Endoskopická laváž intraventrikulárního krvácení nezralých novorozenců
Authors:
T. Radovnický 1; P. Hitka 2; M. Sameš
Authors‘ workplace:
Neurochirurgická klinika Fakulty zdravotnických studií UJEP a Masarykovy nemocnice v Ústí nad Labem, o. z
1; Neonatologická klinika Fakulty zdravotnických studií UJEP a Masarykovy nemocnice v Ústí nad Labem, o. z.
2
Published in:
Cesk Slov Neurol N 2020; 83/116(6): 655-658
Category:
Letter to Editor
doi:
https://doi.org/10.48095/cccsnn2020655
Vážená redakce,
předčasně narození jsou skupinou s vysokým rizikem postižení CNS. Nejčastějším takovým postižením je intraventrikulární krvácení (intraventricular haemorrhage; IVH), které způsobuje závažné následky ovlivňující další vývoj dítěte [1]. Zásadně negativním faktorem je možný rozvoj posthemoragického hydrocefalu (post-haemorrhagic hydrocephalus; PHH). Ten je spojen s velmi vysokou morbiditou a mortalitou [2]. Víme, že IVH se diagnostikuje u 15–20 % novorozenců s porodní váhou nižší než 1 500 g a u 50 % novorozenců s váhou nižší než 750 g [3]. U pacientů s IVH stupně III a IV se PHH s nutností intervence vyvine u 29–49 % pacientů, z toho pak 38–92 % vyžaduje zavedení trvalé drenáže likvoru [5]. Ta je sama o sobě zatížena vysokým rizikem komplikací. Jedná se zejména o následnou infekci (u 11–28 % operací [6]) a velmi častou pozdní malfunkci shuntu. Udává se téměř 80% riziko malfunkce shuntu v prvních 5 letech po zavedení [7]. Léčba IVH s rozvinutým PHH zůstává široce diskutovaným tématem. Je zřejmé, že snaha by měla být zaměřená na zlepšení výsledného neurologického stavu a redukci rizika rozvoje shunt‑dependentního PHH. Jelikož se PHH vyvíjí díky intraventrikulárnímu koagulu, mělo by být prioritní jeho časné odstranění. Tímto směrem byla zaměřená studie založená na intraventrikulárním podávání rekombinantního aktivátoru tkáňového plazminogenu ve snaze rozpustit intraventrikulární koagula. Studie však byla předčasně ukončena, protože se neprokázala redukce permanentního PHH, navíc bylo vysoké riziko recidivy krvácení (34 %). Při hodnocení výsledků po 2 letech byl ale prokázán lepší neurologický stav takto léčených pacientů [8]. Endoskopickou laváž IVH uvedli Schulz et al jakožto metodu, která taktéž slibuje časné odstranění koagul, navíc s lepšími možnostmi kontroly krvácení. Svá data prezentují v pilotním souboru 10 pacientů léčených konvenčně a 19 pacientů léčených laváží. U pacientů po endoskopické laváži komplikaci spojenou s výkonem nezaznamenali. Především se ale nevyskytl ani jeden případ recidivy krvácení a riziko perzistujícího PHH bylo 58 % oproti 100 % v konvenčně léčené skupině [9]. Data na větším souboru a srovnání s ostatními metodami léčby slibuje probíhající studie TROPHY registry study vedená stejným pracovištěm [10].
Před vlastním operačním výkonem jsou podána profylaktická antibiotika (augmentované peniciliny [amoxicillin/klavulanát] nebo cefalosporiny II. generace [cefuroxim]). Pacient je v poloze na zádech s podloženou hlavou v lehkém předklonu a fixovanou náplastí tak, aby byla přístupná oblast velké fontanely. Po sterilní přípravě operačního pole je pomocí peroperační sonografie zaveden endoskop (systém Minop®, Aesculap, Center Valley, PA, USA) do frontálního rohu té postranní komory, která je vyplněna koaguly, při oboustranném postižení do komory, ve které je koagul více. Právě sonografické zaměření je důležité, protože vlastní vizuální kontrola zavedení je limitovaná špatnými optickými vlastnostmi likvoru. Pomocí UZ tedy vyměříme jak trajektorii, tak i potřebnou hloubku zavedení endoskopu. Po inzerci endoskopu do postranní komory je nutný proplach alespoň k částečnému vyčeření likvoru. Jako proplachovací medium využíváme Ringerův roztok zahřátý průtokovým ohřívačem na tělesnou teplotu. Zahřívání roztoku je nutné, protože je třeba značného objemu roztoku (asi 1,5–3 l) a snadno by pak mohlo dojít k podchlazení dítěte. Zpočátku proplachování vidíme zpravidla charakteristický obraz „sněhové bouře“, tedy vír bělavých částeček na tmavém pozadí. Postupně se při proplachu optické vlastnosti likvoru zlepšují, můžeme tedy provést základní ventrikuloskopii. Identifikujeme intraventrikulární koagulum, které je nutné odstranit. Jako nejefektivnější metoda odstranění se ukázala aspirace koagula. Prakticky ji provádíme tak, že napojíme injekční stříkačku přes spojovací hadičku na výplachový kanál endoskopu. Po přiblížení optiky ke koagulu jej pak můžeme aktivně aspirovat, adherence k ependymu komor nebývá výrazná. Tím, jak koagula postupně odstraňujeme, opět zhoršujeme zakalení likvoru, proto musí být proplach kontinuální. Po odstranění dosažitelných koagul z ipsilaterální postranní komory provádíme stomii septum pellucidum k získání přístupu k odstranění koagul z kontralaterální postranní komory. Případná koagula v temporálních rozích musíme ponechat, neboť rigidním endoskopem nejsou dosažitelná. Poté, co odstraníme koagula z obou postranních komor, pokračujeme v proplachu Ringerovým roztokem až do uspokojivého vyčeření likvoru. Po extrakci endoskopu zavedeme punkčním kanálem katetr, který napojíme na podkožní port pro možnost následných odlehčovacích punkcí.
Další průběh léčby se neliší od zavedených postupů. Na základě sonografických parametrů, měření obvodu hlavy a klinického stavu je rozhodnuto o nutnosti odlehčovací punkce portu. Jejich četnost závisí na stupni poruchy cirkulace likvoru. Pokud přetrvává dependence na punkcích, dítě dosáhne hmotnosti 2 000 g a biochemické parametry likvoru se relativně normalizují, je indikovaná MR mozku. Při průkazu obstrukce v likvorových cestách zvažujeme endoskopický zákrok, v opačném případě indikujeme implantaci ventrikulo-peritoneálního shuntu. Uvedenou metodou jsme léčili zatím 2 pacienty.
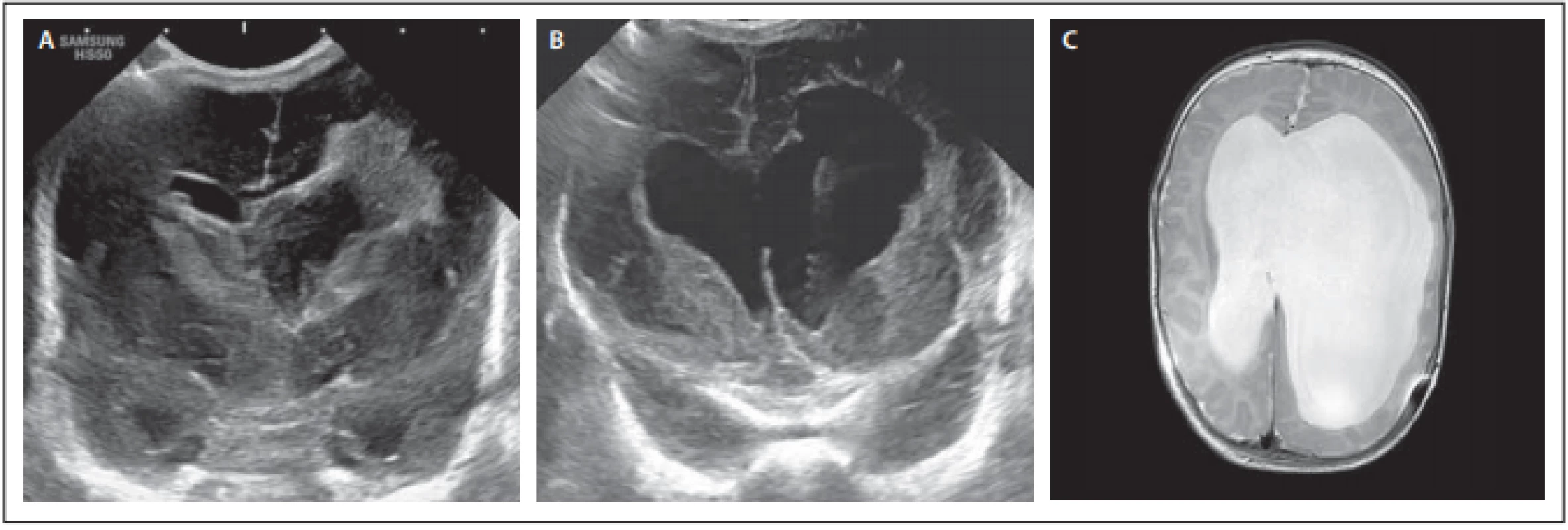
Pacientka 1 byla narozená císařským řezem matce narkomance ve stáří 26 týdnů a 3 dnů s porodní váhou 850 g. Den po porodu bylo sonograficky diagnostikováno IVH stupeň IV vlevo s výrazným periventrikulárním prokrvácením a III. stupněm vpravo. Sedmý poporodní den progredovaly obstrukčního hydrocefalu (OH), šíře komor a RI, pacientka měla zvýšenou dráždivost. Týž den byla provedena endoskopická laváž zleva s implantací portu (obr. 1). Deset dnů nebyla punkce portu nutná, 11. den se ale objevily napjatá velká fontanela a spontánní likvorea z jizvy. Další den byla pacientka febrilní, proto byla provedena punkce portu s laboratorním nálezem meningitidy (Staphylococcus capitis). Při punkci byl tlak pod 10 cm H2O. Byla nasazena terapie antibiotiky (cefotaxim, vancomycin). Za další 4 dny byly pro rozvoj příznaků hydrocefalu opakovaně prováděny odlehčovací punkce portu (celkem 12× během 42 dnů). Po zaléčení meningitidy byl pro perzistující hydrocefalus implantován ventrikulo-peritoneální shunt (Miethke proGAV® 2.0, SHUNTASSISTANT® 20 cm H2O, Christoph Miethke GmbH & Co. KG, Potsdam, DE). V současnosti je doba sledování 6 měsíců, neurologický stav je navzdory vstupně těžkému IVH IV. stupně překvapivě dobrý.
Fig. 1. Female patient 1 – (A) preoperative sonography with visible blood clots in both lateral ventricles with periventricular extension
to the left; (B) postoperative sonography with visible subcutaneous port catheter; (C) MRI of the brain before shunt implantation.
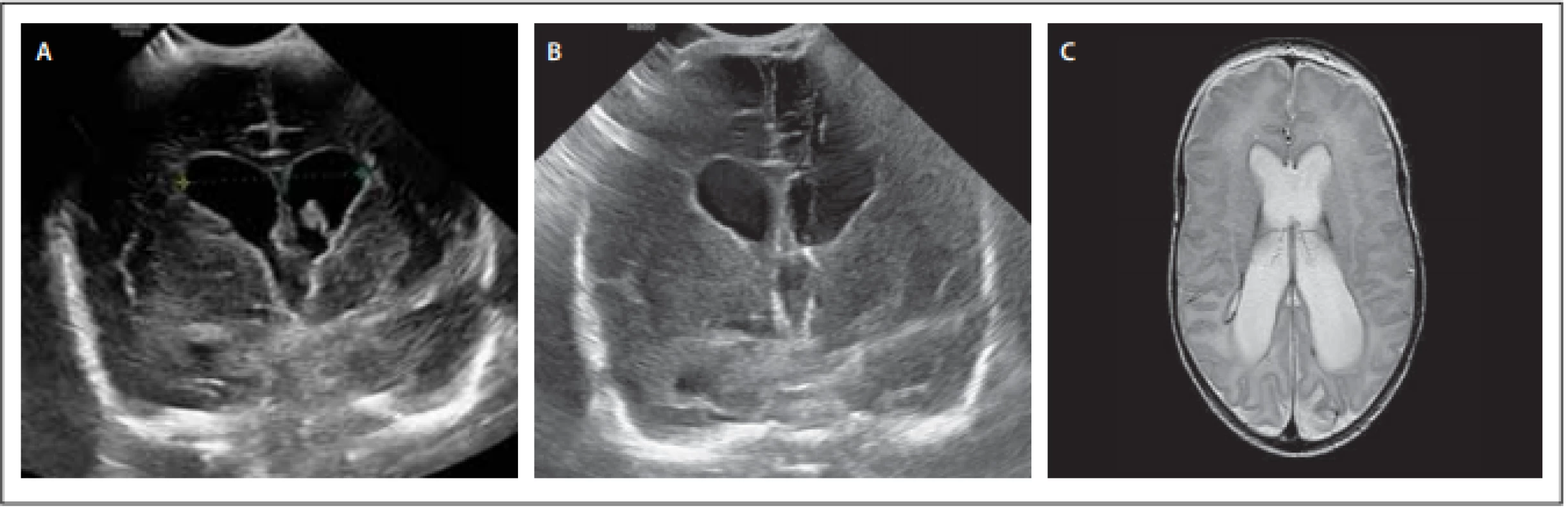
Pacient 2 byl narozen ve 30. týdnu a 3. dnu císařským řezem pro bradykardii. Porodní váha byla 1 600 g. Den po porodu sonograficky diagnostikováno IVH II. stupně oboustranně. Za 4 dny progrese OH, desaturace, sonografický obraz IVH III. stupně oboustranně, sice s regresí hematomu, ale progresí šíře komor. Týž den provedena endoskopická laváž s implantací portu (obr. 2). Dvanáct dnů po operaci progrese OH, pacient dráždivý, proto provedena odlehčovací punkce portu se vstupním tlakem 17 cm H2O. V dalším průběhu již bez klinických a grafických známek hydrocefalu, proto implantace shuntu indikovaná nebyla. V současné době je pacient sledován 6 měsíců, neurologický stav je i nadále dobrý a bez projevů hydrocefalu.
Fig. 2. Male patient 2 – (A) preoperative sonography in the phase of partial reduction of clot volume, but progression of ventricular width; (B) postoperative sonography with visible catheter; (C) MRI of the brain 3 months later with an image of non-tension dilatation of
the ventricular system.
Finanční podpora
Financováno Interní grantovou podporou vědecké, výzkumné a inovační činnosti zaměstnanců Krajské zdravotní, a. s. Registrační číslo IGA6 – 217111023.
MUDr. Tomáš Radovnický, Ph.D.
Neurochirurgická klinika Fakulty zdravotnických studií UJEP Masarykovy nemocnice v Ústí nad Labem, o.z
Sociální péče 3316/12 A
401 13 Ústí nad Labem
e-mail: tomas.radovnicky@kzcr.eu
Přijato k recenzi: 6. 5. 2020
Přijato do tisku: 9. 12. 2020
Sources
1. Whitelaw A. Intraventricular haemorrhage and posthaemorrhagic hydrocephalus: pathogenesis, prevention and future interventions. Semin Neonatol SN 2001; 6 (2): 135–146. doi: 10.1053/siny.2001.0047.
2. Vassilyadi M, Tataryn Z, Shamji MF et al. Functional outcomes among premature infants with intraventricular hemorrhage. Pediatr Neurosurg 2009; 45 (4): 247–255. doi: 10.1159/000228982.
3. du Plessis AJ. The role of systemic hemodynamic disturbances in prematurity-related brain injury. J Child Neurol 2009; 24 (9): 1127–1140. doi: 10.1177/0883073809339361.
4. Limbrick DD, Mathur A, Johnston JM et al. Neurosurgical treatment of progressive posthemorrhagic ventricular dilation in preterm infants: a 10-year single-institution study. J Neurosurg Pediatr 2010; 6 (3): 224–230. doi: 10.3171/2010.5.PEDS1010.
5. Wellons JC, Shannon CN, Kulkarni AV et al. A multicenter retrospective comparison of conversion from temporary to permanent cerebrospinal fluid diversion in very low birth weight infants with posthemorrhagic hydrocephalus. J Neurosurg Pediatr 2009; 4 (1): 50–55. doi: 10.3171/2009.2.PEDS08400.
6. Simon TD, Hall M, Riva-Cambrin J et al. Infection rates following initial cerebrospinal fluid shunt placement across pediatric hospitals in the United States. Clinical article. J Neurosurg Pediatr 2009; 4 (2): 156–165. doi: 10.3171/2009.3.PEDS08215.
7. Notarianni C, Vannemreddy P, Caldito G et al. Congenital hydrocephalus and ventriculoperitoneal shunts: influence of etiology and programmable shunts on revisions. J Neurosurg Pediatr 2009; 4 (6): 547–552. doi: 10.3171/2009.7.PEDS08371.
8. Whitelaw A, Evans D, Carter M et al. Randomized clinical trial of prevention of hydrocephalus after intraventricular hemorrhage in preterm infants: brain-washing versus tapping fluid. Pediatrics 2007; 119 (5): e1071–e1078. doi: 10.1542/peds.2006-2841.
9. Schulz M, Bührer C, Pohl-Schickinger A et al. Neuroendoscopic lavage for the treatment of intraventricular hemorrhage and hydrocephalus in neonates. J Neurosurg Pediatr 2014; 13 (6): 626–635. doi: 10.3171/2014.2.PEDS13397.
10. Thomale UW, Cinalli G, Kulkarni AV et al. TROPHY registry study design: a prospective, international multicenter study for the surgical treatment of posthemorrhagic hydrocephalus in neonates. Childs Nerv Syst ChNS Off J Int Soc Pediatr Neurosurg 2019; 35 (4): 613–619. doi: 10.1007/s00381-019-04077-4.
Labels
Paediatric neurology Neurosurgery NeurologyArticle was published in
Czech and Slovak Neurology and Neurosurgery

2020 Issue 6
- Memantine Eases Daily Life for Patients and Caregivers
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Memantine in Dementia Therapy – Current Findings and Possible Future Applications
- Advances in the Treatment of Myasthenia Gravis on the Horizon
-
All articles in this issue
- Progresivní supranukleární obrna
- Mezinárodní klasifikace orofaciální bolesti (ICOP) – oficiální český překlad prvního vydání
- Supraskapulární neuropatie
- Endoskopické vs. skríninkové vyšetření polykání a jejich vliv na výsledný stav u pacientů po akutní cévní mozkové příhodě
- Srovnání měření průtokových parametrů v oblastikarotické stenózy in vivo a in vitro – pilotní výsledky testování hemodynamického fantomu
- Encefalopatie při infekci COVID-19 s odezvou na léčbu intravenózními imunoglobuliny
- Nemocný s pomalu progredující symptomatikou cervikokraniálního přechodu
- Syndrom neadekvátní sekrece antidiuretického hormonu jako první příznak estezioneuroblastomu
- Koincidence roztroušené sklerózy a myasthenia gravis
- Časná revaskularizace po kombinovaném výkonu u nemoci moyamoya
- Endoskopická laváž intraventrikulárního krvácení nezralých novorozenců
- Stanovisko České neurologické společnosti ČLS JEP k organizaci péče o pacienty s akutní bolestí zad v bederní úrovni u dospělých
- Doporučené postupy pro nutriční podporu u cévních mozkových příhod
- Odešel doc. MUDr. Roman Schröder, CSc.
- Zemřel doc. MUDr. Edgar Lukáš, DrSc. (1932–2020)
- MUDr. Michal Králik, CSc. Spomienka na vzácneho človeka.
- Prof. MUDr. Ľubomír Lisý, DrSc.
- Rozloučení s prof. MUDr. Valentinou Stýblovou, DrSc. (1922–2020)
- MUDr. Hanuš Baš, CSc., devadesátiletý
- Prof. MUDr. Peter Kukumberg, PhD. – 75-ročný
- Léčba aktivní sekundárně progresivní roztroušené sklerózy selektivním modulátorem receptoru pro sfingosin-1-fosfát
- Hemodynamické změny ve čtyřech aneurysmatech vedoucí k jejich ruptuře v průběhu sledování
- Klinická charakteristika nově diagnostikovaných pacientů s Parkinsonovou nemocí zařazených do longitudinální studie BIO-PD
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Progresivní supranukleární obrna
- Supraskapulární neuropatie
- Endoskopické vs. skríninkové vyšetření polykání a jejich vliv na výsledný stav u pacientů po akutní cévní mozkové příhodě
- Encefalopatie při infekci COVID-19 s odezvou na léčbu intravenózními imunoglobuliny
