Přínos alergenové imunoterapie Phostalem v léčbě sezonní alergické rýmy (dva roky aplikace)
Contribution of allergen immunotherapy using Phostal in the treatment of seasonal allergic rhinitis (two years of use)
Allergen immunotherapy consists in the administration of the appropriate allergen to which the patient is hypersensitive. The objective is to induce immunological tolerance of the organism. In the present study, the effect of the administration of Phostal on the occurrence of seasonal symptoms of pollinosis in a group of 35 outpatients was observed during two years. The substance was administered according to the regular dosage schedule, all year round. The results of the study have demonstrated a significant effect of the product on the decrease in the occurrence of observed objective symptoms of the disease, starting already from the first year of treatment. This is in correlation with changes in the spirometric functions, selected laboratory parameters and results of the prick tests in the treated group in comparison to the control group.
Key words:
allergen immunotherapy – pollinosis – Phostal
Authors:
L. Bartošíková 1; J. Nečas 1; T. Bartošík 2; M. Pavlík 2; J. Fráňová 3
Authors‘ workplace:
Univerzita Palackého v Olomouci, Lékařská fakulta, Ústav fyziologie
1; Fakultní nemocnice U sv. Anny v Brně, Anesteziologicko-resuscitační klinika
2; Fakultní nemocnice Brno, Dětská nemocnice, II. dětská klinika
3
Published in:
Čes. slov. Farm., 2008; 57, 99-102
Category:
Original Articles
Overview
Alergenová imunoterapie spočívá v aplikaci příslušného alergenu, na který je pacient přecitlivělý. Cílem je navození imunologické tolerance organismu. Ve studii byl sledován vliv aplikace Phostalu na výskyt sezonních příznaků polinózy u skupiny 35 ambulantně léčených pacientů v průběhu dvou let. Phostal byl aplikován dle běžného dávkovacího schématu, a to celoročně. Výsledky studie ukazují významný efekt preparátu na snížení výskytu sledovaných objektivních příznaků onemocnění, a to již od prvního roku léčby. Tyto jsou v korelaci se změnami v hodnotách spirometrických funkcí, vybraných laboratorních parametrů a výsledků kožních testů u skupiny léčené ve srovnání se skupinou kontrolní.
Klíčová slova:
alergenová imunoterapie – polinóza – Phostal
Úvod
Alergenová imunoterapie (AIT) je léčebná metoda, jejímž cílem je změnit odpověď imunitního systému alergika na určitý alergen. Tento léčebný princip je starý téměř 100 let 1, 2). Dříve se také užívaly názvy „SIT – Specifická imunoterapie“ nebo „Hypo-/Desenzibilizace“.
Vlastní AIT spočívá v podávání postupně se zvyšujících dávek alergenové vakcíny až k dávce udržovací, která je aplikována opakovaně v určitém časovém intervalu. Tímto způsobem je zajištěno podání dostatečné kumulativní dávky alergenu, které by mělo vyústit do klinického zmírnění nebo vymizení potíží při opakované expozici daného alergenu.
AIT je definována jako opakované aplikování specifických alergenových vakcín pacientům s IgE zprostředkovanou alergií za účelem získání ochrany proti alergickým symptomům a zánětlivým reakcím spojených s přirozenou expozicí těchto alergenů 3).
Cílem alergenové imunoterapie je snížit závažnost onemocnění, zlepšit kvalitu života nemocného a omezit farmakoterapii, která může být často spojena s určitými riziky, nežádoucími účinku léků a vyššími náklady.
Nepřetržitý výzkum v oblasti teoretické imunologie spolu s rychle zaváděnými moderními postupy při výrobě vakcín přispívají k určitému zpoždění v přenosu informací do klinické praxe. Zavedené postupy se prolínají s návody výrobců, které jsou u každé firmy a často u každého nového alergenu poněkud odlišné 4).
Mechanismus účinku AIT není dosud zcela objasněn. Cílem imunologického ovlivnění je normalizovat patologickou převahu cytokinové produkce Th2 lymfocytů směrem ke zvýšení tvorby cytokinů produkovaných Th1 lymfocyty a stimulace IgG-protilátek. IgG protilátky indukované AIT mohou působit jako alergen blokující protilátky. U pylové AIT by se tak měl potlačit sezonní nárůst specifických IgE-protilátek. Přes počáteční zvýšení IgE-protilátek snižuje se postupně uvolňování histaminu basofily a žírnými buňkami po expozici alergenu 5, 6).
Podmínkou pro používání AIT je dostupnost standardizovaných alergenových vakcín. V současnosti je doporučována standardizace vakcín na celkovou alergenní potenci, biologickou aktivitu a vyjádření množství hlavního alergenu v hmotnostních jednotkách (μg/ml). V minulosti vyjadřovaná koncentrace alergenu pouze pomocí obsahu bílkovinného dusíku není již v současnosti považována za dostačující. Kvantifikace obsahu všech hlavních alergenů podle doporučení WHO (WHO Position Paper) zaručuje bezpečný lék, na druhé straně podstatně zvyšuje jeho cenu 7, 8).
Je zapotřebí velmi pečlivě zvážit poměr očekávaného přínosu AIT s nároky a rizikem této léčby. AIT není doporučena tam, kde stačí pouze eliminace alergenů. Nejvýhodnější je zahájení AIT v časné fázi alergického onemocnění, neboť AIT působí preventivně na vznik alergického zánětu, a tím i na prevenci dalšího zhoršování nemoci. Je tedy zejména vhodná u pacientů s alergií na aeroalergeny, které nemohou být dostatečně eliminovány. Uplatňuje se tedy u alergických rhinokonjuktivitid, nebo u astmatu, které již vyžadují pravidelnou farmakoterapii.
Délka aplikace AIT je většinou 3–5 let. Obecně je dnes doporučována celoroční aplikace AIT i u sezonních alergií z důvodu snížení rizik nežádoucích účinků, neboť udržovací fáze je méně riziková než fáze iniciální. Ukončení AIT se doporučuje v situaci, kdy jsou symptomy alergie výrazně redukovány a tato redukce trvá již 1–2 roky. V případě relapsu je možno AIT znovu zahájit 9).
Cílem studie bylo sledovat a hodnotit změny symptomů a laboratorních nálezů polinózního onemocnění v rámci dvouleté léčby Phostalem. Dále bylo sledováno, zda aplikace AIT ovlivňuje současnou ko-medikaci příznaků alergické rýmy.
Pokusná část
Soubor pacientů a metodika
Soubor tvořilo 35 pacientů, z toho 23 mužů s průměrným věkem 31,33 let a 12 žen s průměrným věkem 33,57 let. U pacientů byla stanovena diagnóza sezonní alergické rýmy a byli léčeni ambulantně. Všem pacientům byl subkutánně aplikován v rámci specifické AIT Phostal®. Aplikoval se podle doporučení výrobce; při iniciální léčbě jedenkrát týdně, při udržovací léčbě byla maximální tolerovaná dávka podávána pravidelně ve čtrnáctidenních intervalech po dobu prvních 3 až 6 měsíců, dále jedenkrát měsíčně. Interval mezi dvěma injekcemi nepřesahoval 6 týdnů. V léčbě se pokračuje i nadále.
Všichni pacienti byli alergičtí podle prick testu na trávy z čeledi lipnicovitých (bojínek, jílek, lipnice, srha, tomka). U všech pacientů bylo kromě prick testu provedeno spirometrické vyšetření a odebrána krev na stanovení celkového IgE, IgG a specifických IgE. U pacientů jsme sledovali příznaky onemocnění (byly pouze sezonního charakteru) a jejich změny jsme statisticky zhodnotili.
Statistická hodnocení byla prováděna pomocí programu SPSS verze 12.0. U všech měření se stanovoval průměr a směrodatná odchylka. Friedman test a Kendal’s W test byl použit při třech hodnotách, Wilcoxonův test znaménkových pořadí byl použitý při dvou hodnotách. Hodnotu p ≤ 0,05 jsme považovali za signifikantní.
Výsledky
U všech sledovaných symptomů došlo již po prvním roce léčby k signifikantním změnám v porovnání se vstupní hodnotou, po druhém roce léčby hodnoty sledovaného skóre jednotlivých symptomů poklesly ještě markantněji. Výjimkou bylo kýchání, kde se po prvním roce léčby skóre nezměnilo. Teprve po druhém roce léčby poklesla jeho hodnota signifikantně (tab. 1).
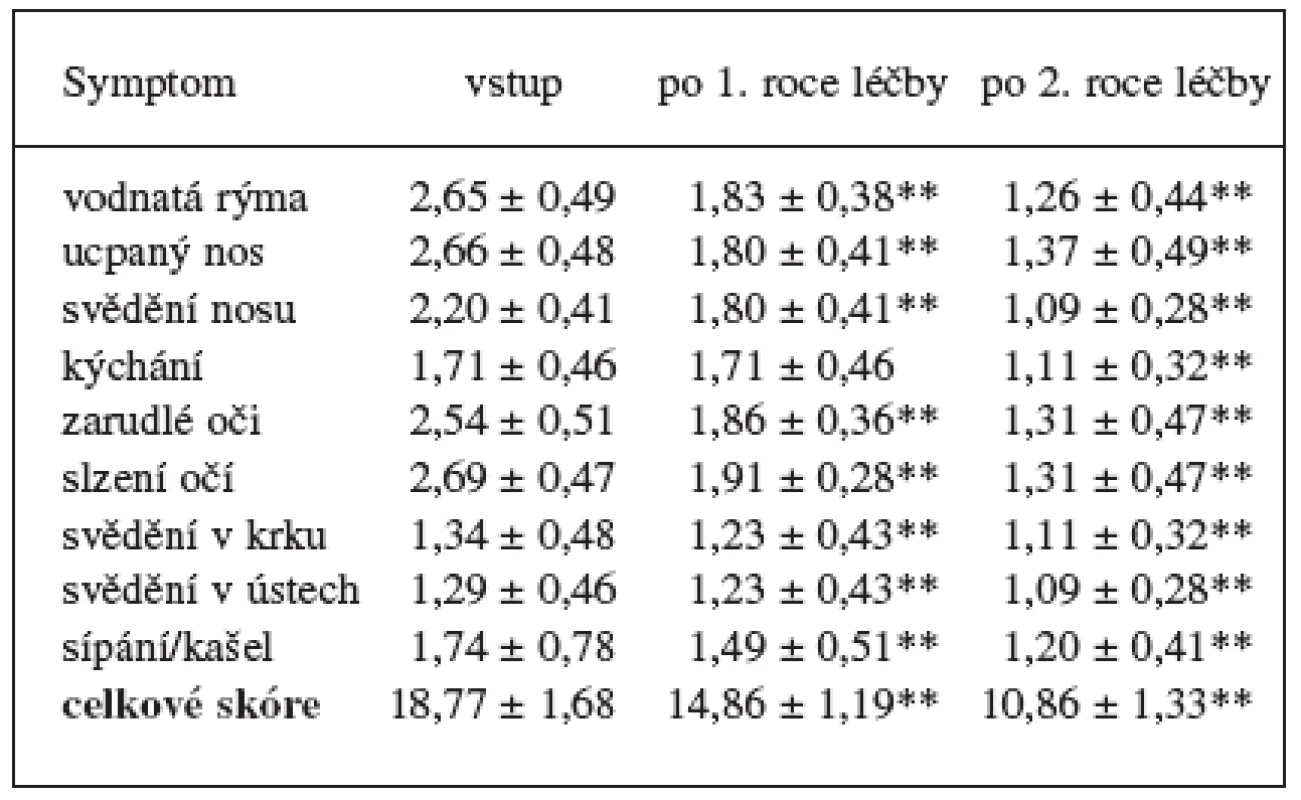
Všechny sledované parametry spirometrických funkcí se výrazně zlepšily (tab. 2).
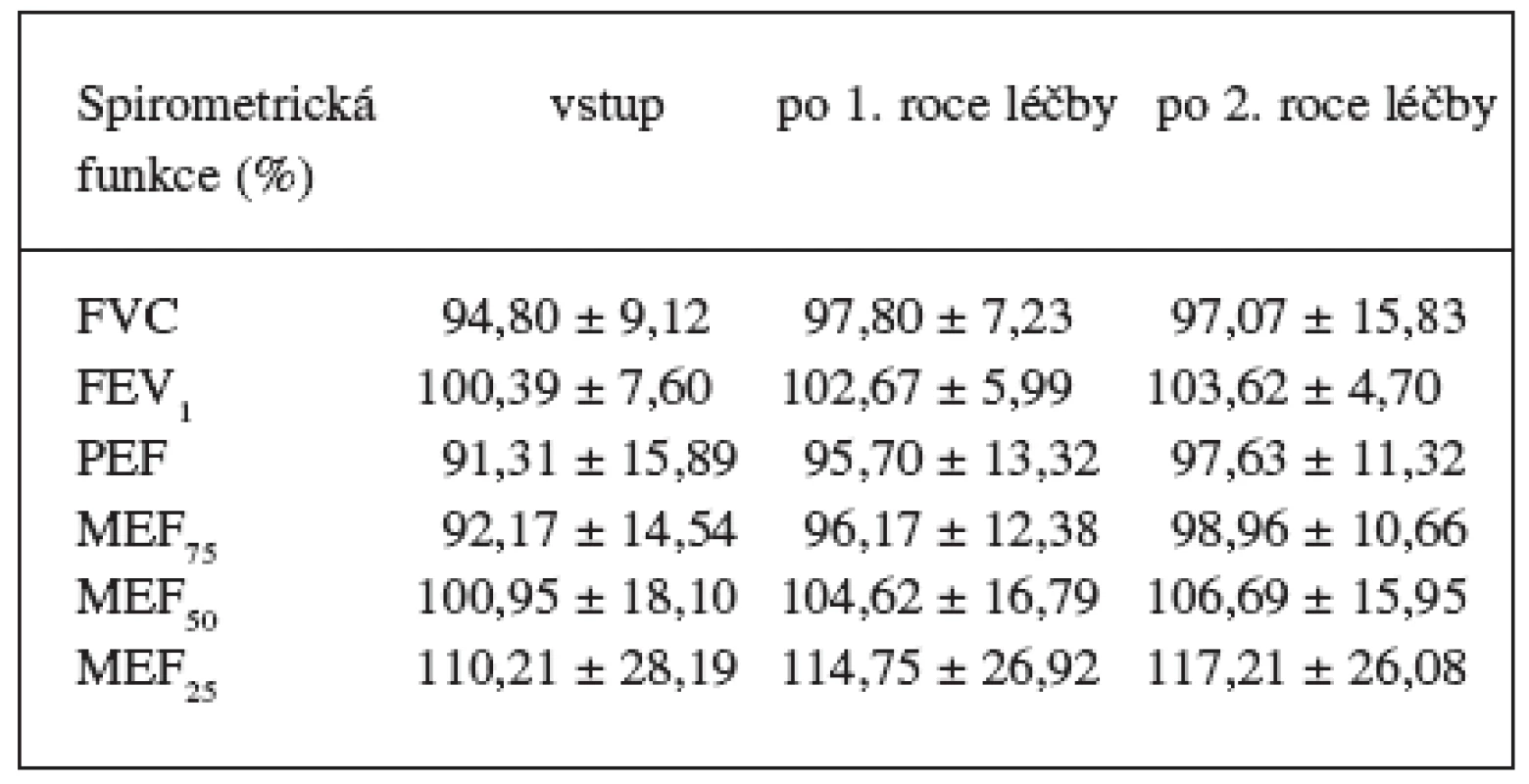
V rámci sledování spotřeby přídatné medikace došlo ke snížení spotřeby u inhalačních kortikosteroidů (aplikovány Pulmicort nebo Becodisks), bronchodilatancií (aplikovány Ventolin, Berotec nebo Foradil), topických nosních přípravků (aplikovány Rhinocort nasal nebo Flixonase) a rovněž topických očních přípravků (aplikovány Spersalerg, Livostin nebo Naaxia)
Hodnocení velikosti pupenů u prováděných prick testů nedosáhlo ani u jedné ze sledovaných trav signifikantních změn, přesto se po dvou letech terapie Phostalem v porovnání se vstupní hodnotou jejich velikost snížila.
Rovněž porovnání vstupních hodnot u specifických IgE s hodnotami po dvou letech terapie Phostalem nedosáhlo signifikantních změn, i když ve všech případech došlo k jejich mírnému snížení. Hodnoty IgG nedosáhly signifikantních změn.
Diskuze
Studie prokázala pozitivní vliv aplikace Phostalu v rámci AIT při terapii alergické sezonní rýmy. Ve sledovaném souboru došlo k signifikantním změnám manifestujících se symptomů alergické rýmy. Současně se zlepšily i hodnoty spirometrických funkcí a snížila se spotřeba přídatné medikace. Dle subjektivního hodnocení pacientů je možno léčbu považovat za přínosnou za daného patologického stavu.
Hodnocené laboratorní ukazatele a výsledky prick testů se statisticky výrazně nezměnily. Hlavní příčinou může být nedostatečně dlouhá doba aplikace (podle výrobce se doporučuje minimálně 3 roky). U prick testu může být příčinou i chybný odpočet provedený lékařem při stanovování velikosti poměru pupen/zarudnutí. Konečně i nestejně provedený vpich při vlastním prick testu může zkreslit výslednou kožní reakci. Rovněž užívání antihistaminika a jeho případné pozdní vysazení před prováděným prick testem může změnit výsledné hodnoty. Další z možností je skutečnost, že alergen vyvolávající symptomy alergické rýmy je nedominantní formou, která není obsažena v aplikovaném Phostalu, protože AIT se v současné době provádí jenom s dominantními formami alergenů.
Santilli a Nathan 10) ve své studii prováděné na 175 pacientech s alergickou rýmou, léčených pomocí AIT, porovnávali symptomy onemocnění před a v průběhu léčby. Hodnoty symptomů se pohybovaly ve škále 0–5. Kromě změn příznaků onemocnění byla hodnocena rovněž vlastní kvalita života pacientů. V průběhu léčby se výrazně snížila závažnost příznaků, ale i zlepšila kvalita života (pokles návštěv u lékaře, snížení nutné hospitalizace, snížení absence v práci či ve škole).
Studie PAT 11) z roku 2002 sledovala možnost prevence astmatu u dětí se sezonní rýmou při včasné terapii AIT. Dvě stě pět dětí ve věku od 6 do 14 let s alergií na pyly trav dostávalo 3 roky AIT, nebo bylo zařazeno do kontrolního souboru. Žádné z dětí nemělo astma vyžadující denní léčbu a 20 % dětí mělo lehké příznaky astmatu během pylové sezony. Skupina aktivně léčených dětí vykazovala po 3 letech léčby signifikantně nižší výskyt příznaků astmatu ve srovnání s kontrolní skupinou.
Feliziani 12) v roce 1995 ve své studii léčby pylových alergií pomocí Pangramin-SLITu (perorální forma AIT) sledoval 34 pacientů alergických na pyl trav a trpících alergickou rýmou. Studie byla dvojitě slepá, placebem kontrolovaná. Studie prokázala výrazné snížení ve spotřebě léků mezi léčenou a placebo skupinou. Rovněž příznaky rýmy byly v aktivně léčené skupině výrazně nižší.
Velmi rozsáhlou studii provedli v roce 2002 Gonzales a Floriso 13). Studie porovnávala toleranci, bezpečnost a účinnost AIT proti kontrolní skupině bez AIT u pacientů, kteří byli alergičtí jenom na jeden druh alergenu (čeleď olivovité). Po roce léčby se snížila kožní (p < 0,001) a bronchiální reaktivita (p ≤ 0,001) v léčené skupině oproti kontrolní. Taktéž došlo ke snížení specifického IgE a vzrůstu podtříd IgG1 a IgG4. Dále se statisticky významně snížily nosní (p ≤ 0,05) a dechové (p ≤ 0,05) symptomy, za současného snížení i příslušné medikace antihistaminiky (p ≤ 0,05) a beta 2-agonisty (p ≤ 0,01).
V České republice se v současné době spíše posuzuje kvalita života nemocných léčených AIT. Studie u nemocných s alergickou rinokonjunktivitidou byla provedena na 5 alergologických pracovištích v České republice. Sto čtyřicet čtyři pacientů vyplnilo dotazník RQLQ v sezoně a mimo sezonu. Symptomatickými léky užívanými pacienty byly nejčastěji antihistaminika, pravidelně je užívalo 60 pacientů ze sledovaného souboru nemocných. Inhalační kortikosteroidy (IKS) dostávalo 35 % nemocných. Alergenová imunoterapie proběhla u 59 % sledovaných pacientů. Studie potvrdila, že příznaky alergické rýmy závažným způsobem zhoršují kvalitu života nemocných. Průměrné skóre v jednotlivých oblastech bylo u nemocných se sezonní rýmou v sezoně dvojnásobně až trojnásobně vyšší v porovnání s dobou mimo sezonu 14).
O pozitivních klinických a laboratorních změnách po aplikaci AIT hovoří studie Parka et al. 15). Patnáct pacientů podstoupilo AIT terapii. Hodnotily se parametry před terapií, po ukončení iniciální fáze a jeden rok po skončení léčby. U symptomového skóre se výrazně snížily příznaky (p ≤ 0,05), hodnoty specifických IgE a celkového IgE se statisticky nezměnily, významně ovšem stouply hladiny podtřídy IgG4 (p ≤ 0,05). Klesla také kožní reaktivita, ne však signifikantně.
Dle Tonnela a Scherperela 16) má použití AIT vliv jak na snížení symptomů rýmy u alergiků, tak i vliv na snížení další spotřeby léků a snížení kožní reaktivity. Sto dvacet pacientů v randomizované studii užívalo sublinguální formu AIT po dobu 2 let. Po skončení léčby došlo ke snížení celkového skóre příznaků (p ≤ 0,05), snížení nosních potíží (p ≤ 0,01) a ke snížení kožní reaktivity (p ≤ 0,01).
Hansen a Normann 17) se ve své studii zaměřili na opomíjenou stránku AIT, a to na bezpečnost při vlastním podávání AIT. Aplikovali podkožně depotní formu alergenového extraktu 64 pacientům. U některých pacientů se vyskytly nežádoucí účinky patřící do skupiny 1 či 2 závažnosti, nešlo o signifikantní rozdíly ve srovnání s jinými aplikačními formami (p ≤ 0,05). Nežádoucí účinek patřící do skupiny 3 nebo 4 se nevyskytl u sledovaného souboru vůbec.
Na změny bronchiální hyperreaktivity (BHR) při aplikaci SIT se v roce 2003 zaměřil Polosa et al.18). V randomizované, dvojitě zaslepené, placebem kontrolované skupině porovnávali sezonní změny BHR při aplikaci AIT po dobu 36 měsíců. Výsledek potvrdil zlepšení BHR (p ≤ 0,05) u léčených pacientů, oproti placebem kontrolované skupině.
Wilson et al. provedli v roce 2005 metaanalýzu 19) u pacientů s alergickou rýmou léčených pomocí AIT. Celkem porovnali 22 studií, ve kterých bylo zařazeno 979 pacientů. Všechny studie byly dvojitě slepé a placebem kontrolované. V 8 studiích probíhala léčba pomocí AIT méně než 6 měsíců, v 10 studiích mezi 6 a 12 měsíci a ve 4 studiích bylo AIT podáváno více než 12 měsíců. I když rozdíl mezi studiemi byl velmi výrazný, ve většině studií se symptomové skóre zlepšilo (p ≤ 0,05), a to jak ve studiích s dětskými, tak i s dospělými pacienty. Při porovnání sledovaných hodnot imunoglobulinů nedošlo ke statistickým změnám pro specifické IgE, výrazně se však zvýšily hodnoty IgG4. Kožní reaktivita nebyla porovnána.
Z hlediska aplikace AIT je také důležité dlouhodobé přetrvání účinku po skončení podávání udržovacích dávek. Ariano et al. 20) ve své dvojitě slepé, placebem kontrolované studii, porovnávali nejen změny v průběhu aplikace AIT, ale také případné změny po 4 letech od ukončení aplikace. Po této době příznaky při respiračních potížích byly méně závažné než před vstupem do studie (p ≤ 0,05), taktéž došlo k poklesu specifického IgE a ke zvýšení IgG4 (p ≤ 0,05) u sledovaného souboru pacientů.
K podobným výsledkům ohledně přetrvávajícího klinického účinku této léčby ještě několik let po podání poslední udržovací dávky, k omezení, či úplnému přerušení preskripce symptomatických léků došla i studie Di Rienzo et al.21).
Závěr
Studie prokázala v souladu se závěry studií dalších autorů jednoznačně pozitivní vliv alergenové imunoterapie na snížení závažnosti symptomů provázejících sezonní alergickou rýmu a jejich výskyt v následných sezonách. Tento stav pozitivně ovlivňuje i vlastní kvalitu života pacienta. Taktéž snížení počtu současně aplikovaných léků lze považovat za přínosný výsledek. Změny některých laboratorních výsledků a výsledků prováděného prick testu nebyly signifikantní, v průběhu let však došlo k jejich pozitivním změnám. V souladu se zkušenostmi s aplikací AIT je vhodné doporučit pokračování zavedeného léčebného postupu minimálně 3 roky.
Došlo: 24. ledna 2008 / Přijato: 28. února 2008
Adresa pro korespondenci:
MUDr. PharmDr. Lenka Bartošíková, Ph.D.
Ústav fyziologie LF UP
Hněvotínská 3, 775 15 Olomouc
e-mail: bartosil@tunw.upol.cz
Sources
1. Noon, L.: Lancet, 1911; 1, 1572–1573.
2. Freeman, J.: Lancet, 1914; 1, 1178.
3. Rybníček, O., Seberová, E.: Průvodce alergenovou imunoterapií. 1. vyd. Praha, ČIPA, 2004.
4. Pereira, C., Botelho, F., Tavarez, B.: Allerg. Immunol., 2004; 36, 375–386.
5. Schmidt-Weber, C. B., Laser, K.: Curr. Opin. Aller. Clin. Immunol., 2005; 5, 525–530.
6. Akdis, C. A., Barlan, I. B., Bahceciler, N., Akdis, M.: Allergy, 2006; 61 (Suppl 81), 11–14.
7. Batard, T.: Alergie, 1999; 3, 12–14.
8. Bouquet, J., Jockey, H. J.: Allergy, 1998; 53 (Suppl. 44), 4–42.
9. Bartošíková, L., Fráňa, L., Nečas, J., Fráňa, P.: Klin. Imunol. Alergol., 2000; 1, 5–10.
10. Santilli, J., Nathan, R.: Ann. Allergy Asthma Immunol., 2001; 86, 219–225.
11. Miller, C., Dreborg, S., Ferdousi, H. A. et al.: J. Allergy Clin. Immunol., 2002; 109, 251–256.
12. Feliziani, V.: Allergol. Immunopathol., 1995; 23, 224–230.
13. Gonzales, P., Florido, F.: J. Invest. Allerg. Clin Immunol., 2002; 12, 263–271.
14. Vondra, V., Malý, M., Rybníček, O. et al.: Alergie, 2004; 1, www.tigis.cz.
15. Park, H. S., Hahm, D. H., Kim, H. Y. et al.: Ann. Allergy. Asthma Immunol., 2001; 86, 444–448.
16. Tonnel, A. B., Scherpereel, A.: Allergy, 2004; 59, 491–497.
17. Hansen, I., Normann, K.: Laryngo Rhin. Otol., 2003; 82, 558–563.
18. Polosa, R., Gotti M., Li, F., Mangano, G.: J. Brit. Soc. Allergy, 2003; 33, 873–881.
19. Wilson, D. R., Lima, L., Torres, M., Durham, S. R.: Allergy, 2005; 1, 4–12.
20. Ariano, R., Orion, A. M., Augeri, G. et al.: Allergy, 1999; 54(4), 313–319.
21. Di Rienzo, V., Marcucci, F., Puccinelli, P. et al.: Clin. Exp. Allergy, 2003; 33, 206–210.
Labels
Pharmacy Clinical pharmacologyArticle was published in
Czech and Slovak Pharmacy

2008 Issue 2
-
All articles in this issue
- Standardní receptura pro přípravu léčivých přípravků v lékárnách I. Suspenze k aplikaci na kůži
- Interakcia 1,4-dihydropyridínov s iónovými kanálmi
- Polosyntetické deriváty celulosy jako základ hydrofilních gelových systémů
- Radioaktivně značené peptidy v diagnostice a terapii nádorů
- Léčivé rostliny a diabetes mellitus
- Moderní instrumentální metody studia isoflavonů
- Laktobacily a ich probiotické vlastnosti
- Přínos alergenové imunoterapie Phostalem v léčbě sezonní alergické rýmy (dva roky aplikace)
- Czech and Slovak Pharmacy
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Polosyntetické deriváty celulosy jako základ hydrofilních gelových systémů
- Laktobacily a ich probiotické vlastnosti
- Standardní receptura pro přípravu léčivých přípravků v lékárnách I. Suspenze k aplikaci na kůži
- Léčivé rostliny a diabetes mellitus
