Přehled stomatologické péče o pacienty s kongenitálními krvácivými chorobami
Review Dental Treatment of Patients with Congenital Bleeding Disorders
Objectives:
The commonest congenital bleeding disorders in childhood are hemophilia, von Willebrand disease and deficiency of factor XI. Disease is characterized by a deficient of coagulability. It is a gonosomal recessive condition. There are two main types of hemophilia: Hemophilia A is characterized by a deficiency of factor VIII (FVIII) and hemophilia B is characterized by a deficiency of factor IX (FIX). Hemophilia is an X-linked hereditary disorder and affects predominantly males because of their hemizygous (karyotyp 46, XY). Females – heterozygot (karyotyp 46, XX) are transmitter of gene for hemophilia and they are rarely affected unless there is an unequal lyonisation of the X – chromosome. There are two other common diseases which are needed to mention: von Willebrand disease and factor XI deficiency. Von Willebrand disease is the commonest congenital bleeding disorder on the other hand deficiency of factor XI is not so common. Both of them have similar clinical manifestation a treatment such as hemophilia. The provision of dental treatment in patients with congenital bleeding disorders has often been neglected. In past most treatments were carried out under general anesthesia and usually the only one treatment plan was extraction followed by provision of dentures. Since the introduction of coagulation factor, use new local hemostatic agents, improvement of operative methods, minimal invasive therapy and an increasing interest in the preventive of dental problems started new era in dental care for patients with congenital bleeding disorders. Nowadays use doctor during the intervention, replacement therapy to increase level of FVIII, FIX, von Willebrand factor and factor XI prophylactic factor with combination fibrin glue, antifibrinolytic agents and other agents which make treatment faster, safe and more comfortable. Point of this article is to provide other dentists general informatics about healing patients with congenital bleeding disorders.
Keywords:
hemophilia A – hemophilia B – von Willebrand disease – factor XI deficiency – orthodontic treatment – anesthesia – periodontal disease – oral surgical procedures – dental extraction – fibrin glue
:
J. Papež; K. Chleborád; T. Dostálová
:
Stomatologická klinika dětí a dospělých 2. LF UK a FNM, Praha
:
Česká stomatologie / Praktické zubní lékařství, ročník 114, 2014, 6, s. 109-115
:
Review Article
Předmět sdělení:
Nejčastějšími vrozenými koagulopatiemi u dětských pacientů jsou hemofilie, von Willebrandova choroba a méně častý je pak deficit faktoru XI. Jde o onemocnění charakterizované poruchou srážlivosti krve. Hemofilie je onemocnění s gonozomálně recesivní dědičností. Rozlišujeme dva hlavní typy hemofilie: hemofilie A, která je charakterizována nedostatkem faktoru VIII (FVIII) a hemofilie B, která je charakterizována nedostatkem faktoru IX (FIX). Geny zodpovědné za správnou funkci faktorů VIII a IX jsou vázány na pohlavním chromozomu X. Porucha se vyskytuje převážně u mužské části populace, protože muži jsou hemizygoti (karyotyp 46, XY). Ženy-heterozygotky (karyotyp 46, XX) jsou nosičkami; onemocnění se u nich projeví jen velmi zřídka, a to v případě inaktivace chromozomu X, tzv. lyonizace. V rámci kongenitálních krvácivých chorob je nutné zmínit i von Willebrandovu chorobu a deficit faktoru XI. Von Willebrandova choroba je vůbec nejčastější vrozenou koagulopatií, naopak deficit FXI je v populaci zastoupen nejméně. Klinicky mají průběh podobný hemofilii A i B a jejich léčba je obdobná. Poskytování odborné stomatologické péče pacientům s krvácivými chorobami bývá často zanedbáno. V minulosti probíhala ošetření těchto jedinců pouze v celkové anestezii a zpravidla jediným typem ošetření byla extrakce. Od doby, kdy byly na trhu představeny nové prostředky koagulační léčby, není již takové radikální ošetření indikováno. Nástupem nových materiálů, zlepšením operačních technik, užíváním lokálních hemostatik a zvýšením důrazu na stomatologickou prevenci a minimálně invazivní techniku ošetření započala nová éra péče o pacienty s kongenitálními krvácivými chorobami. V současné době se při stomatologickém ošetření používá substituční léčba za účelem zvýšení hladiny FVIII, FIX, von Willebrandova a FXI faktoru v krvi v kombinaci s tkáňovými lepidly aplikovanými přímo do extrakčních ran, antifibrinolytickou léčbou a dalšími preparáty usnadňujícími léčbu. Cílem článku je představit zubním lékařům problematiku péče o tyto pacienty.
Klíčová slova:
hemofilie A – hemofilie B – von Willebrandova choroba – deficit FXI – ortodoncie – anestezie – onemocnění parodontu – chirurgická léčba – extrakce – tkáňové lepidlo
ÚVOD
Hemofilie
Hemofilie je relativně vzácné onemocnění, přesto jde o nejčastější vrozenou krvácivou chorobu. Existují dva základní typy hemofilie: hemofilie A je nejčastější, tvoří přibližně 85 % všech případů (incidence 1 : 5000 novorozenců) a je charakterizována defektem faktoru VIII (FVIII). Hemofile B je charakterizována defektem faktoru IX – Christmas faktor (FIX) (incidence 1 : 30 000 novorozenců) [20]. Oba typy hemofilie jsou vázány na chromozom X a projevují se stejnými klinickými projevy. Klinicky nelze rozlišit hemofilii A od hemofilie B. Tíže klinického projevu je dána procentním zastoupením zachovaných faktorů VIII či IX.
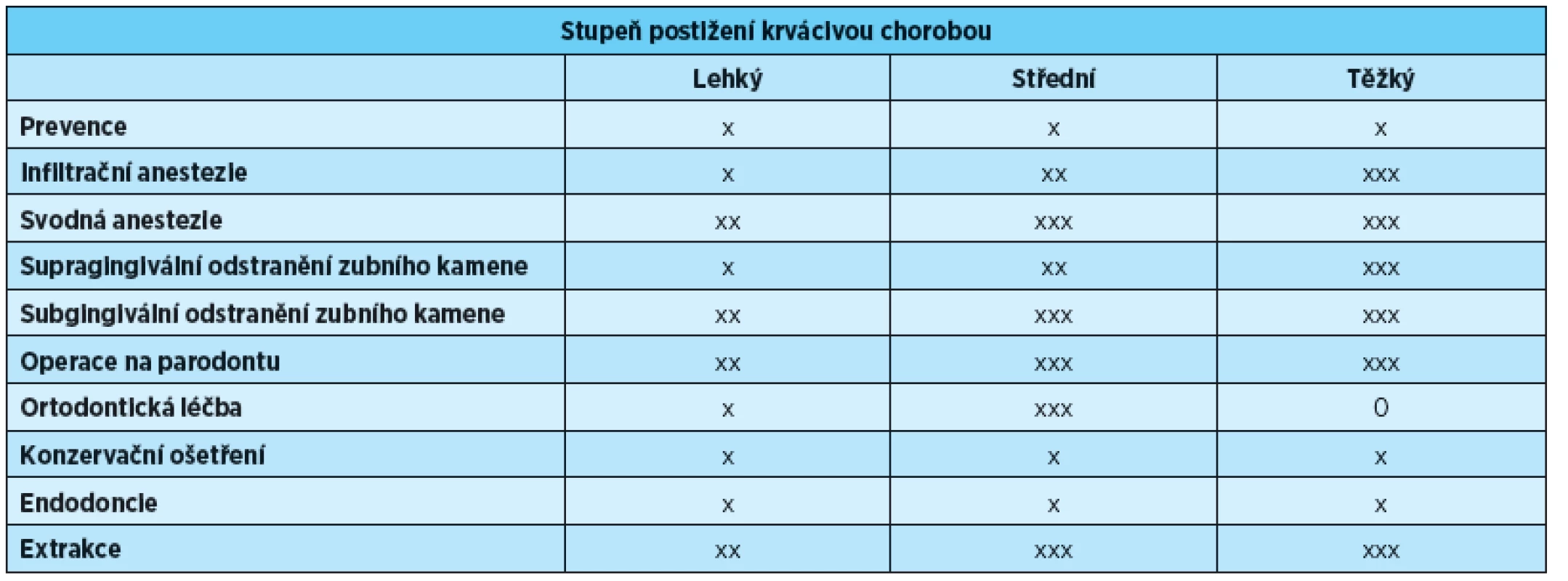
Z tohoto hlediska můžeme rozdělit hemofilii do tří stupňů podle procentuálního zastoupení faktorů (hodnoty udávané jako norma nad 40 %) a jejich množství v plazmě (hodnoty udávané jako norma 50–100 IU/dL) (tab. 1):
- lehká hemofilie: 5–40 % FVIII, FIX (6–40 IU/dL),
- středně těžká hemofilie: 1–5 % FVIII, FIX (2–5 IU/dL),
- těžká hemofilie: do 1 % F VIII, FIX (<1 IU/dL).

Hemofilie může vzniknout řadou různých mutací genů pro faktor VIII (hemofilie A) nebo faktor IX (hemofilie B). Protože geny obou faktorů se nacházejí na chromozomu X, postihuje onemocnění téměř výhradně muže. V případě, že otec bude postižen hemofilií, pak jeho dcery budou jistě přenašečkami genové mutace a všichni synové budou zdrávi. V případě, že hemofilií trpí matka-přenašečka, pak syn i dcera z 50 % zdědí mutovaný gen, takže 50 % synů bude hemofiliků a 50 % dcer bude přenašečkami hemofilie. Stanovením faktoru VIII a jeho srovnáním s množstvím antigenu von Wilebrandova faktoru je často možné určit, zda žena pocházející z rizikového rodu je skutečnou přenašečkou hemofilie A [16]. Podobně stanovením faktoru IX lze často prokázat přenašečství hemofilie B. Na některých specializovaných pracovištích je možno provést analýzu DNA genu faktoru VIII po její amplifikaci z lymfocytů za použití polymerázové řetězové reakce [19].
V České republice existuje centrální registr hemofilických pacientů obsahující necelých 200 hemofiliků do 18 let, s dospělými je jich kolem devíti set a jejich počet neustále vzrůstá. Z celkového počtu hemofiliků je 75 % středně těžkých a těžkých [16].
Von Willebrandova choroba a deficit faktoru XI
Von Willebrandova choroba je charakterizována nedostatečnou tvorbou nebo poruchou proteinu zvaného von Willebrandův faktor (vWF). Von Willebrandova choroba je onemocnění s gonozomálně recesivní dědičností a na rozdíl od hemofilie postihuje stejnou měrou muže i ženy. Von Willebrandův protein stabilizuje FVIII a umožní krevním destičkám interakci s cévní stěnou. Von Willebrandova choroba je velmi často bezpříznaková nebo se projevuje jen nenápadně, silnějším a častějším krvácením z nosu. Některé klinické projevy nedostatku vWF se mohou projevit jako spontánní krvácení do mukózy a krvácení z gingivy [24]. Pouze jeden ze sta lidí trpících von Willebrandovou chorobou má závažné projevy krvácení. Podobně jako hemofilie se i von Willebrandova choroba vyskytuje v různě závažných formách. Existují tři podtypy von Willebrandovy choroby a v každém podtypu se pacienti dělí ještě do tří kategorií podle koncentrace faktoru na lehkou, střední a těžkou formu. Průběh ošetření je ekvivalentní ošetření hemofiliků s lehkou, střední a těžkou formou onemocnění. V případě prvního podtypu se jako substituce při ošetření používá Desmopresin [21]. U druhého a třetího podtypu je nutná substituce von Wilebrandovým faktorem ve spojení i s faktorem VIII, kterou zajistí ošetřující hematolog. Lidé s nejtěžší formou tohoto onemocnění však mohou být ohrožení ještě více než hemofilici, včetně závažných kloubních krvácení s rizikem trvalé invalidity. Nedostatek faktoru XI (FXI) se klinicky projevuje na rozdíl od hemofilie A, B a von Willebrandovy choroby tím, že nedochází ke spontánnímu krvácení do kloubů a svalů. V případě nedostatku faktoru XI dochází k nepředvídatelnému mírnému krvácení, které je zpravidla vyvoláno chirurgickým zákrokem, jako např. tonzilektomií nebo extrakcí zubu. Míra krvácení je dána koncentrací faktoru XI, a protože je krvácení obtížně předvídatelné, je i ošetření značně komplikované [4]. Terapeutické možnosti zahrnují zvýšení hladiny faktoru XI podáním čerstvé mražené plazmy nebo podáním koncentrátu faktoru XI za současného použití antifibrinolytické léčby.
KLINICKÉ PROJEVY
Při poranění pacienta s hemofilií, u kterého dojde k porušení integrity cévního řečiště, dochází k excesivnímu krvácení, kdy nelze klinicky odlišit, zda jde o hemofilii A nebo B. Krvácení není silnější než u pacientů zdravých, ale trvá delší dobu v závislosti na koncentraci faktorů. Spontánně dochází ke krvácení do velkých kloubů (včetně temporomandibulárního kloubu) a svalů u 75 % pacientů. Krvácení do urogenitálního traktu (přítomnost krve v moči – hematurie) se vyskytuje u 60 % pacientů, u těžkých hemofiliků až v 90 %, nejčastěji ve věku 12–21 let. Krvácení do centrálního nervového systému se vyskytuje především u novorozenců. V podkoží se vyskytují mnohočetné hematomy. Hemofilie se může projevit již v novorozeneckém věku jako krvácení z pupečníku a četnými hematomy měkkých tkání kalvy – cefalohematomy. Hemofilie se téměř vždy projeví v předškolním věku [17]. Obtížně stavitelé a profuzní krvácení obvykle nastává i po minimálním traumatu. Charakteristický je výskyt pozdního krvácení třetí až čtvrtý den po otevření krevního řečiště.
PŘEHLED VÝKONŮ A MOŽNOSTI JEJICH PROVEDENÍ
Prevence
Základním pilířem péče o hematologicky kompromitované pacienty je správná instruktáž dentální hygieny. Pokud naučíme pacienty správné orální hygieně, předejdeme tím mnohdy komplikovanému ošetření. V prevenci vzniku zubního kazu a onemocnění dásní využíváme především:
- Zubní kartáček (pacient by si měl čistit chrup minimálně dvakrát denně středně tvrdým kartáčkem). Techniku čištění lékař předvede.
- Doporučuje se použití doplňků s vyšším obsahem fluoru. Fluoridové doplňky je vhodné používat jen v případě, pokud množství fluoru v pitné vodě nepřesahuje 1 ppm. Jako vhodné doplňky lze použít fluoridové tablety, ústní vodu s vyšším obsahem fluoru, pasty a gely s fluorem.
- Výplachy ústní vodou s obsahem chlorhexidinu, který napomáhá redukovat množství plaku.
- Dental floss a mezizubní kartáčky je možné použít pouze u pacientů s lehkou nebo středně těžkou formou hemofilie a pouze po důkladné instruktáži od stomatologa, aby nedocházelo k sebepoškozování.
- Bezpodmínečně je nutné informovat opatrovníky a pacienty o škodlivosti nadměrného příjmu sladkého jídla a pití.
- Důležitá je také pravidelná návštěva stomatologa a pravidelné profesionální odstranění zubního kamene a plaku v rámci preventivních prohlídek.
Často se pacienti s krvácivými chorobami dostaví do ordinace vystrašení, že pozorují krvácení dásní při čištění. Krvácení je ve většině případů způsobeno zánětem dásní, výjimku tvoří spontánní krvácení u deficitu faktoru XI. Pacienti si často ze strachu přestávají čistit zuby, a stav se tím ještě zhoršuje. Je podstatné pacientům vysvětlit problematiku onemocnění zánětu dásní. Dále je nutné pacienty psychicky uklidnit a motivovat v pokračování orální hygieny [5].
Anestezie a kontrola bolesti
Mírnou bolest zubů je možné tlumit malým množstvím běžných analgetik, například paracetamolem (acetaminofen). Zvýšené pozornosti musíme dbát při užívání všech nesteroidních antiflogistik (NSAID), např. preparátů obsahujících kyselinu acetylsalicylovou. Užití všech nesteroidních antiflogistik musí být projednáno s ošetřujícím hematologem vzhledem k jejich inhibičnímu vlivu na srážlivost krevních destiček [5].
Neexistuje žádné omezení týkající se výběru lokálního anestetika, i když vazokontrikční látky obsažené v anestetiku mají dodatečný účinek na lokální hemostázu. Před aplikací anestezie je nutné informovat pacienty a jejich opatrovníky o riziku vzniku lokálního orálního traumatu v podobě hematomu.
Infiltrační anestezii lze podat bez nutnosti substituce faktorů zodpovědných za srážlivost krve. Jsme v ní schopni provádět výkony na všech zubech v horní čelisti a v oblasti frontálního úseku dolní čelisti [5, 6, 9].
Ošetření molárů a premolárů v dolní čelisti je nutné provádět při aplikaci svodné anestezie. Tu lze do oblasti n. alveolaris inferior a n. lingualis aplikovat jen v případě, že pacient je hematologicky kompenzován. Je proto nutné zvýšit hladinu koagulačních faktorů podáním odpovídající náhrady. Hematologickou kompenzaci zajistí ošetřující hematolog po domluvě s ošetřujícím stomatologem. Anestezií do oblasti foramen mandibulae vzniká riziko krvácení do svalových struktur v okolních tkáních s možností rozšíření hematomu do oblasti retromolárového a pterygomandibulárního prostoru. Hematom v těchto lokalizacích může vyvolat dýchací obtíže [8, 9, 14].
Léčba onemocnění parodontu
Zdraví měkkých tkání parodontu je nezbytné pro prevenci krvácení a ztráty zubů. Rutinní vyšetření parodontu, supragingivální scaling a polishing včetně ultrasonického scalingu nezpůsobí prolongované krvácení u pacientů, kteří trpí lehkým typem krvácivé choroby [5, 6]. U pacientů se střední formou krvácivé choroby scaling a další malé zákroky mohou být provedeny pod krytím desmopresinem (DDAVP) [21]. Pro pacienty s těžkou formou krvácivé choroby je nezbytná substituce faktory VIII, IX, XI, vWF před scalingem. V případě, že orální hygiena je nedostačující, gingiva a periodoncium je postiženo zánětem, musí být pacientovi co nejdříve sestaven léčebný plán a je nutností co nejdříve instruovat pacienta o provádění správně orální hygieny. V případě vážného postižení parodontu je nezbytností provést supragingivální scaling v první fázi ošetření souběžně s edukací pacienta. Subgingivální scaling je možno ordinovat až v případě snížené inflamace (zánětu). Léčebný plán musí být naplánován do několika návštěv, ve kterých předejdeme přílišné krevní ztrátě. Je vhodné předepsat výplachový roztok obsahující chlorhexidin diglukonát, který napomáhá snížení zánětlivých projevů. Ztrátu krve během ošetření řešíme buď přímý tlakem na ránu, nebo obvazem obsahujícím antifibrinolytický prostředek. Užití kyseliny tranexamové v podobě výplachové-ho roztoku [19] anebo substituce chybějících faktorů umožní kontrolovat krvácení během ošetřování.
Chirurgické ošetření parodontu je vždy považováno za výkon s vysokým rizikem s možností nadměrné ztráty krve. K této možnosti se uchýlíme jen v případě, že konzervační ošetření selhalo a hygiena pacienta je dobrá. Před samotným zákrokem je nutné konzultovat postup s hematologickým oddělením. Následné užití antibakteriálních výplachů a antibiotik je ve většině případů nutností.
Ortodontická léčba
Fixní a snímatelné ortodontické aparáty lze po-užít jen za předpokladu, že pacient prodělal instruktáž orální hygieny a stupeň jeho postižení je lehký [6, 22]. Speciální péče musí být zavedena u pacientů, kteří trpí středně těžkou formou krvácivé choroby. U těchto pacientů je nezbytností správné nasazení jednotlivých částí aparátu tak, aby nedocházelo k dráždění gingivy a bukální sliznice. V případě, že pacient trpí těžkou formou krvácivé choroby, není ortodontická léčba možná z důvodu zvýšeného krvácení při změně polohy zubů [12]. V případě plánovaných extrakcí z ortodontických důvodů je nezbytná konzultace s ošetřujícím hematologem.
Konzervační ošetření (výplň, korunka, můstek)
Konzervační ošetření je běžně prováděný typ léčby v rámci preventivní péče. V rámci ošetření není nutná specializovaná příprava pacienta. Při ošetření musíme dbát na ochranu okolních měkkých tkání, abychom snížili riziko zvýšeného krvácení při užívání matric a klínků. V těchto případech krvácení stavíme lokálními léčebnými prostředky [5]. O použití lokální anestezie pojednávají předchozí části článku.
Endodoncie
Endodontické ošetření přináší velmi nízké riziko vzniku komplikací. Problémy mohou vyvstat v případě nutnosti podání anestezie, a to především do oblasti n. alveolaris inferior. V případě indikace pulpektomie musí mít zub šanci být kvalitně opracován a zaplněn. Je podstatné, aby ošetření probíhalo co možná nejšetrněji s ohledem na stanovení přesné pracovní délky kořenového kanálku. Dráždění periodoncia při překročení pracovní délky má vliv na opakované krvácení z kanálku a jeho obtížné vysušení [5]. Přetrvávající krvácení z kanálku při dodržení pracovní délky značí nedostatečné opracování a ponechání zbytku měkkých tkání. Po jejich odstranění zpravidla krvácení ustává. K výplachu kořenového kanálku používáme běžně dostupné irigační roztoky (sodium hypochlorid, chlorhexidin diglukonát), k zástavě krvácení pak pastu z hydroxidu vápenatého nanesenou do kořenového kanálku.
Chirurgické ošetření
Chirurgické ošetření, zahrnující i prostou extrakci zubu, musí být pečlivě naplánováno s ohledem na riziko vzniku obtížně stavitelného krvácení nebo hematomu. Všechny plánované chirurgické výkony musí být konzultovány s ošetřujícím hematologem. Ošetření by měl provádět stomatolog, který je s problematikou hemofiliků důkladně seznámen.
Rozvržení léčebného plánu při extrakci:
- zhotovení RTG snímku před zákrokem;
- jak velký výkon budeme provádět (zda jednu, dvě, či více extrakcí);
- vybavení pracoviště, ve kterém bude výkon proveden (je vhodné pacienta uložit na pozorování přes noc) [6];
- spolupráce s ošetřujícím hematologem a stanovení kompenzační léčby během zákroku – nutnost podání chybějících faktorů;
- rozhodnutí o použití tkáňového lepidla;
- podle věku a spolupráce dítěte rozhodujeme o ošetření v lokální nebo celkové anestezii. V minulosti bylo preferováno ošetření v celkové anestezii [1, 13, 18];
- léčbu se snažíme vést maximálně atraumaticky.
Průběh ošetření
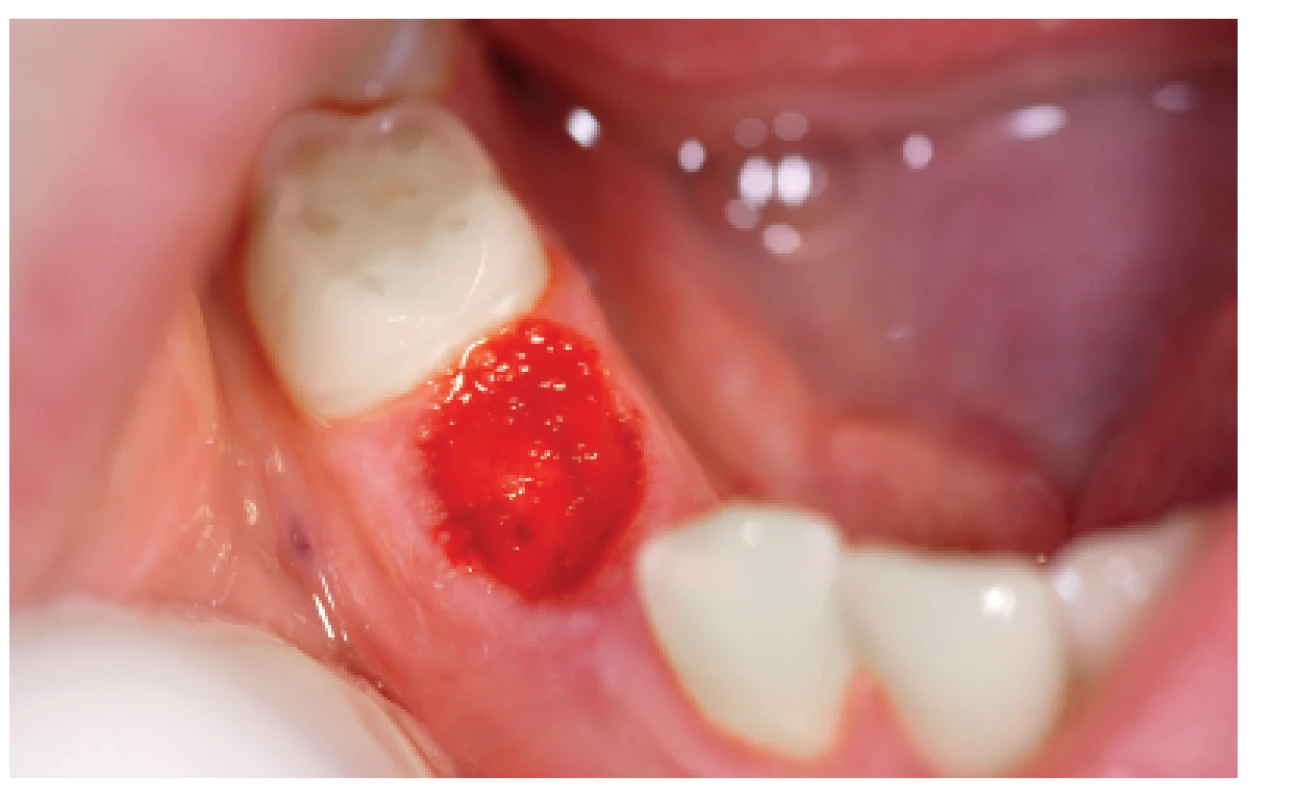
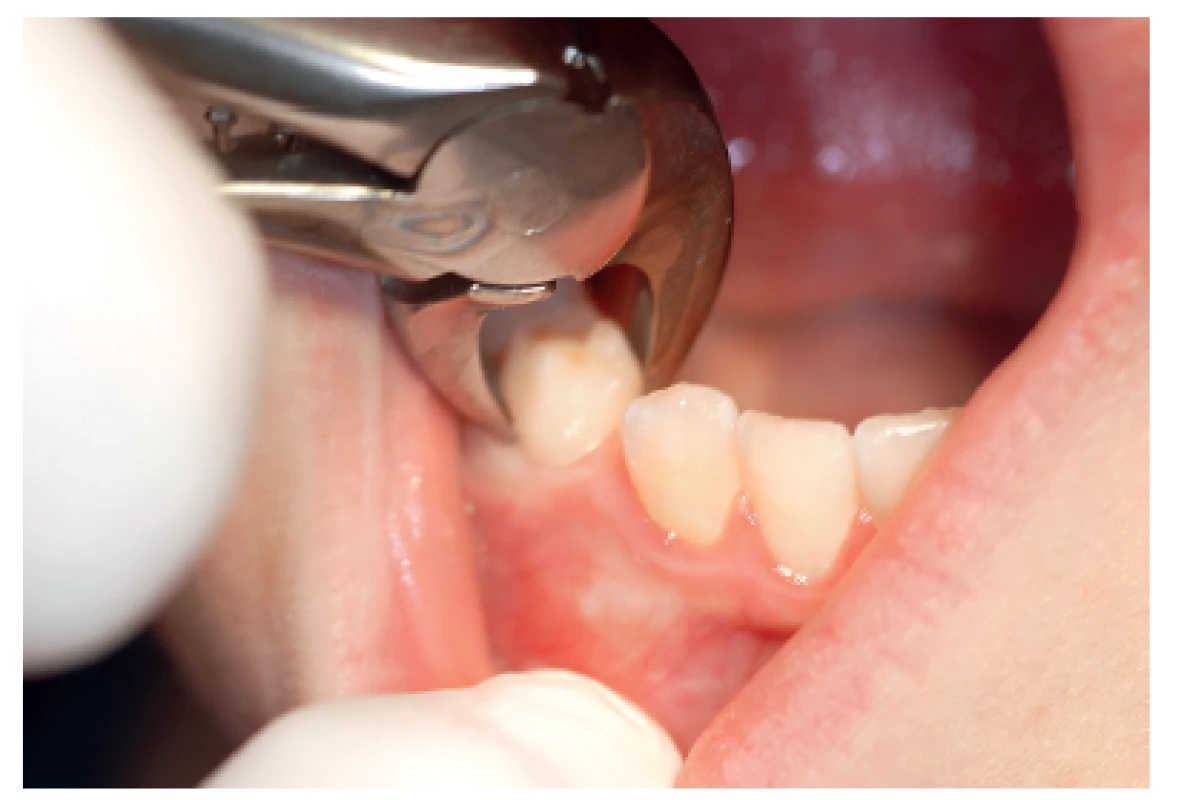
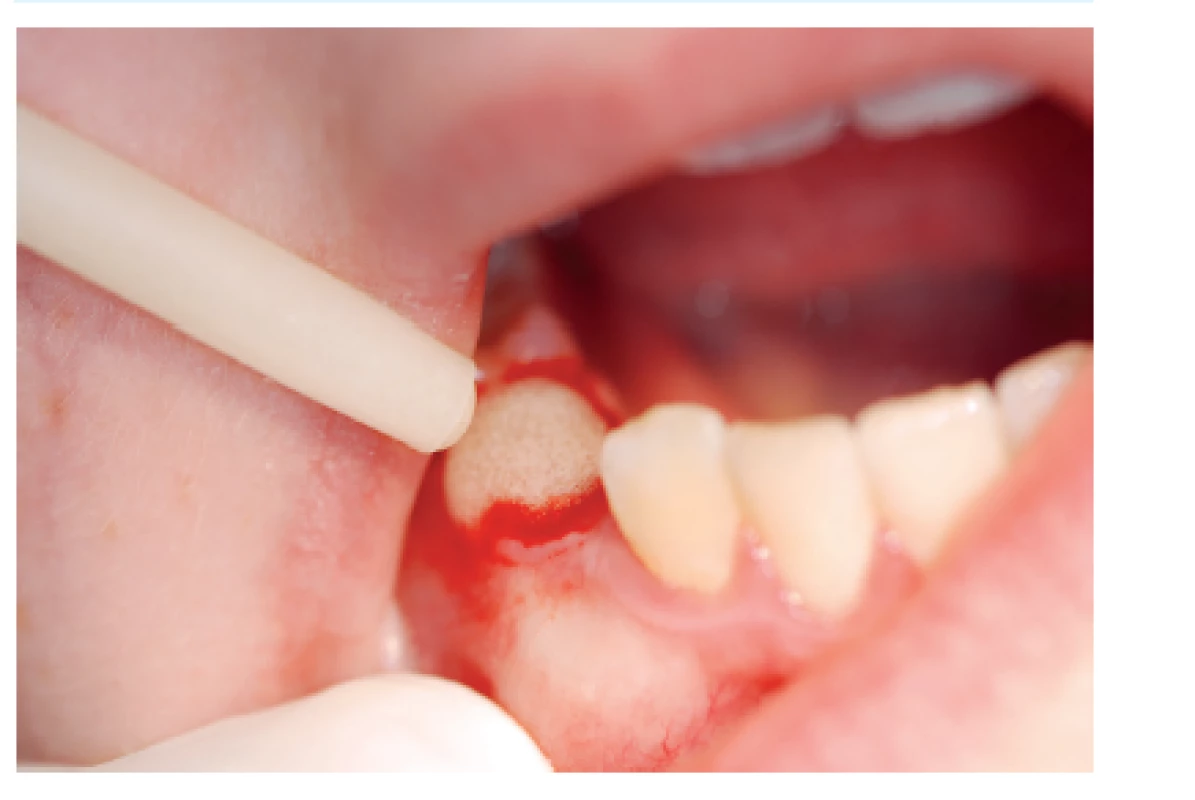
Z důvodu výroby krycí desky zhotovíme před termínem ošetření otisk čelisti, ve které bude probíhat extrakce. Krycí deska může být z měkké fólie, např. Bioplastu. Hematolog ordinuje léčbu [7], která spočívá u středně těžkých a těžkých hemofiliků v substituci koagulačními faktory VIII nebo IX (např. preparát Immunate Stim Plus 1000©, Baxter AG, Rakousko) a eventuálně v antifibrinolytické léčbě preparáty kyseliny tranexamové (preparát Exacyl tbl. 500 mg©, Sanofi-aventis, s.r.o, ČR). U lehkých hemofiliků lze podat pouze antifibrinolytické preparáty. Po této přípravě lze přistoupit k vlastnímu stomatologickému ošetření [6]. V předoperační fázi zkontrolujeme stav ústní dutiny. Je vhodný výplach antibakteriální ústní vodou, např. chlorhexidinem diglukonátem [5]. Následně provedeme extrakce určených zubů (obr. 1) a do extrakčních ran aplikujeme tkáňové lepidlo (např. preparát Tissucol©, Baxter) (obr. 2) [21]. Okraje extrakčních ran sešijeme suturou nejlépe vstřebatelným materiálem (např. Monolac) a poté aplikujeme malé množství tkáňového lepidla na vpichy sutury a následně nasadíme krycí desku na zinkoxid eugenolovou pastu (Repin©, Spofa dental, a.s., ČR) [17]. Celé ošetření se snažíme provádět co nejvíce atraumaticky. Po výkonu musí pacient dodržovat speciální režim určený hematologem i stomatologem.
Na žádost hematologa je pacientovi předepsána po dobu tří až sedmi dnů medikace v podobě antifibrinolytika (např. preparát Exacyl tbl.©). Dávku určí vždy hematolog podle rozsahu výkonu a stupně postižení pacienta.
Stomatolog poučí pacienta, popřípadě opatrovníky o poextrakční péči a informuje o následujících pravidlech: během prvních 24 hodin je zakázáno vyplachovat ústa, platí zákaz kouření, podává se měkká strava po dobu tří dnů, klidový režim po dobu 24 hodin. Dále lékař doporučí analgetika vhodná vzhledem k onemocnění, výplachy antibakteriální ústní vodou se doporučují od druhého dne, maximálně však po dobu sedmi dní [5].
První čtyři dny je každou hodinu nutná kontrola, zda nedochází ke krvácení zpod krycí desky. Čtvrtý den se pacient dostaví na kontrolu k lékaři. Pokud krycí deska neprosakuje a pacient je bez obtíží, přijde na další kontrolu za 10 dní od výkonu. Jestliže ani při druhé kontrole nejsou známky bolesti nebo krvácení, je možné krycí desku sejmout. V případě, že se rána hojí (obr. 3) a pacient je bez obtíží, odesílá se na kontrolu k ošetřujícímu hematologovi [17].
Tkáňové lepidlo
V dnešní době se u pacientů léčených hemofilií ošetřuje extrakční rána tkáňovým lepidlem [2]. Užívá se jako lokální hemostatický prostředek a v kombinaci s antifibrinolityckými prostředky (např. preparát Exacyl©) napomáhá vytvoření koagula v extrakční ráně a snižuje potřebu substituce pacienta faktory VIII a IX. Všechna fibrinová tkáňová lepidla obsahují lidské nebo zvířecí komponenty.
Fibrinové tkáňové lepidlo napodobuje finální část koagulační kaskády v místě, kde fibrinogen je konvertován na fibrin v přítomnosti trombinu, faktoru XIII, fibronektinu a ionizovaného kalcia.
Fibrinových tkáňových lepidel využíváme při ošetření extrakčních ran, při ošetřování v parodontologii a aplikujeme je do míst vpichů při šití rány [10, 15].
ZÁVĚR
Kongenitální krvácivé choroby jsou onemocnění s relativně znatelným zastoupením v populaci. S ohledem na jeho výskyt se každý stomatolog během své dlouholeté praxe s takovým nemocným setká. Stomatologické ošetření je, až na extrakce a „krvavé“ výkony na tvrdých a měkkých tkání (k čemuž náleží i odstranění tvrdého zubního kamene), snadno proveditelné v běžné zubní ordinaci [17]. Chirurgické výkony a extrakce se řadí ke komplikovanějším případům. Před zahájením stomatologického ošetření je vždy nutná konzultace s ošetřujícím hematologem, který řídí adekvátní léčbu [7]. Stomatologické ošetření hemofiliků má svá specifika, která je nutno v zájmu zdárného ošetření dodržet. Obtížnější ošetření typu extrakce by měl provádět stomatolog, který je s problematikou hemofiliků důkladně seznámen [17]. Ošetření probíhá v lokální nebo celkové anestezii – podle spolupráce pacienta. Pokud indikujeme celkovou anestezii, po konzultaci s anesteziologem doporučujeme intubaci flexibilní laryngeální maskou [11]. Stomatologický výkon musí být maximálně šetrný. Při krvácení v dutině ústní využíváme tkáňová lepidla a krycí desku. Díky moderní hematologické léčbě je již možno provádět vícečetné extrakce, ale doporučuje se extrahovat vždy pouze v jedné čelisti. Velice důležitá je také pooperační péče. Hlavně po extrakcích je nutné pacienta v prvních třech až čtyřech dnech po výkonu permanentně sledovat v hodinových intervalech, zda nedochází ke krvácení [17]. I přes velký pokrok v léčbě kongenitálních krvácivých chorob patří ošetřování těchto pacientů stále k obtížným výkonům, zvláště rizikové jsou extrakce. Nezbytné je klást veliký důraz na orální hygienu pacientů s diagnózou kongenitální krvácivé choroby, která usnadní pacientům i lékařům následnou péči [17].
Studie byla podporována projektem IGA MZČR číslo 13351-4.
MDDr. Jakub Papež
Stomatologická klinika dětí a dospělých
2. LF UK a FN Motol
V Úvalu 84
150 06 Praha 5
e-mail: papezjakub@seznam.cz
Sources
1. Anderson, J. A. M., Brewer, A., Creagh, D., Hook, S., Mainwaring, J., McKernan, A., Yee T. T., Yeung C. A.: Guidance on the dental management of patients with haemophilia and congenital bleeding disorders. Brit. Dent. J., roč. 215, 2013, č. 10, s. 497–504.
2. Belozerskaya, G. G., Makarov, V. A., Zhidkov, E. A., Malykhina, L. S.: Local hemostatics (a review). Pharmaceutical Chem. J., roč. 40, 2006, č. 40, s. 353–359.
3. Berkow, R., Fletcher, A. J.: Haemophilia. The Merck manual of diagnosis and therapy, Copyright 1992 by Merk and Co., Inc., Whitehouse Station, New Jersey, U.S.A. 1992, s. 1077.
4. Bolton-Maggs, P. H. B.: Factor XI deficiency and its management, World Federation of Hemophilia, Treatment of Hemophilia, č. 16, 2008, s. 1–18.
5. Brewer, A. K., Correa, M. E.: Guidelines for dental treatment of patients with inherited bleeding disorders, World Federation of Hemophilia Treatment of Hemophilia, č. 40, 2006.
6. Brewer, A. K., Roebuck, E. M., Donachie, M., Hazard, A., Gordon, K., Fung, D., Clarkson, J.: The dental management of adult patients with haemophilia and other congenital bleeding disorders. Haemophilia, roč. 9, 2003, č. 6, s. 673–677.
7. Colvin, B. T., Astermark, J., Fischer, K., Gringeri, A., Lassila, R., Schramm, W., Thomas, A., Ingerslev, J.: European principles of haemophilia care. Haemophilia., roč. 14, 2008, č. 2, s. 361–374.
8. Dougall, A., Fiske, J.: Acces to special care dentistry. Brit. Dent. J., roč. 205, 2008, č. 5, s. 177–190.
9. Freedman, M., Dougall, A., White, B.: An audit of a protocol for the management of patients with hereditary bleeding disorders undergoing dental treatment. J. Disabil. Oral. Health, roč. 10, 2009, č. 4, s. 151–155.
10. Gibble, J. W., Ness, P. M.: Fibrin Glue: the perfect operative sealant. Transfusion, roč. 30, 1990, č. 8, s. 741–747.
11. Ginzelová, K., Hechtová, D.: Laryngeální maska v dětské stomatologii. Quintessenz., roč. 16, 2007, č. 5, s. 77–81.
12. Grossman, R. C.: Orthodontics and dentistry for the hemophilic patient. Am. J. Orthod., roč. 68, 1975, č. 4, s. 391–403.
13. Gupta, A., Epstein, J. B., Cabay, R. J.: Bleeding disorders of importace in dental care and related patient management. J. Can. Dent. Assoc., roč. 73, 2007, s. 77–83.
14. Heiland, M., Weber, M., Schmelzle, R.: Life – threatening bleeding after dental extraction in a haemophilia. A patient with inhibitors to factor VIII: a case report. J. Oral Maxillofac. Surg., roč. 61, 2003, č. 11, s. 1350–1353.
15. Chabbat, J., Tellier, M., Porte, P., et al.: Properties of a new fibrin glue stable in liquid state. Thrombosis Res., roč. 76, 1994, č. 6, s. 525–533.
16. Chleborád, K., Ginzelová, K., Dostálová, T.: Stomatologické ošetření dětského pacienta se středně těžkou formou hemofilie z ortodontických důvodů. LKS., roč. 20, 2010, č. 6, s. 134–137.
17. Chleborád, K., Ginzelová, K., Dostálová, T.: Stomatologické ošetření dětského pacienta s těžkou hemofilií. LKS., roč. 19, 2009, č. 3, s. 85–87.
18. Katz, J. O., Terezhalmy, G. T.: Dental management of the patient with haemophilia. Oral Surg. Oral Med. Oral Pathol., roč. 66, 1988, č. 1, s. 139–144.
19. Lee, A., Boyle, C. A., Savidge, G. F., Fiske, J.: Effectiveness in controlling haemorrhage after dental scaling in people with haemophilia by using tranexamic acid mouthwash. Brit. Dent. J., roč. 198, 2005, č. 1, s. 33–38.
20. Mannucci, P. M., Tuddenham, E. G.: The haemophilias – from royal genes to gene therapy. N. Engl. J. Med., roč. 345, 2001, č. 5, s. 1773–1779.
21. Mannucci, P. M.: Desmopressin (DDAVP) in the treatment of bleeding disorders: the first 20 years. Blood, roč. 90, 1997, č. 7, s. 2515–2521.
22. Scottish Dental Clinical Effectiveness Programme. Oral health assessment and review: guidance in brief. Dundee: Scottish Dental Clinical Effectiveness Programme, 2011.
23. Vinckier, F., Vermylen, J.: Dental extractions in hemophilia: reflections on 10 years´experience. Oral Surg. Oral Med. Oral Pathol., roč. 59, 1985, č. 1, s. 6–9.
24. Wilde, J. T., Cook, R. J.: von Willebrand disease and its management in oral and maxillofacial surgery. Brit. J. Oral Maxillofac. Surg., roč. 36, 1998, č. 2, s. 112–118.
Labels
Gynaecology and obstetrics Maxillofacial surgery Orthodontics Dental medicineArticle was published in
Czech Dental Journal

2014 Issue 6
- The Importance of Limosilactobacillus reuteri in Administration to Diabetics with Gingivitis
- What Effect Can Be Expected from Limosilactobacillus reuteri in Mucositis and Peri-Implantitis?
Most read in this issue
- Review Dental Treatment of Patients with Congenital Bleeding Disorders
- The Assessment of the Biocompatibility of Dental Alloys and Alloys for Dental Amalgam. Part Second
- A Study of Corrosion of Root Parts of Metallic Post and Core Reconstructions after their Extraction