Chronická urinární toxicita 3D-CRT a IMRT karcinomu prostaty
Late urinary toxicity after 3D-CRT and IMRT for prostate cancer
Aim:
The purpose of this research was to retrospectively compare late urinary toxicity of the three-dimensional conformal radiation therapy (3D-CRT) 74 Gy and intensity-modulated radiation therapy (IMRT) 78 Gy for localized prostate cancer.
Material a method:
A total of 203 patients with T1-3 prostate cancer were treated with 3D-CRT (n = 91) and IMRT (n = 112). The median follow-up time was 5.2 years and 3.0 years, respectively. The prescription dose was 74 Gy for 3D-CRT and 78 Gy for IMRT. Late urinary toxicity was graded according to the Fox Chase modification of the Radiation Therapy Oncology Group and Late Effects Normal Tissue Task Force criteria.
Results:
There was no difference between 3D-CRT and IMRT regarding the three-year risk for the development of late urinary toxicity Grade ≥ 2 (14% vs. 11%, p = 0.18). On multivariate analysis, two signifiant toxicity predictors were identified – previous transurethral resection of prostate/open transvesical prostatectomy for benign prostatic hyperplasia TURP/TVPE (relative risk 3.85) and acute urinary toxicity Grade 2 or higher (relative risk 2.35). In the total patient population, there were 22 patients with late urinary toxicity Grade 3. At last follow-up visit, 9 of them (41%) reported no or only minimal symptoms.
Conclusion:
Tolerance of 3D-CRT and IMRT was similar despite the use of high radiation dose 78 Gy with IMRT. Previous TURP/TVPE increased the risk of urinary toxicity.
Key words:
prostate cancer, radiation therapy, urinary toxicity, 3D-CRT, IMRT.
Authors:
Karel Odrážka 1,2,3; Martin Doležel 1,3; Jaroslav Vaňásek 1; Miloslava Vaculíková 4; Milan Zouhar 5; Jana Šefrová 5; Petr Paluska 5; Milan Vošmik 5; Tereza Kohlová 6; Iveta Kolářová 1; Miloš Broďák 7
; Pavel Navrátil 7; Petr Prošvic 8; Petr Hoffmann 9
; Abdulbaset Hafuda 8
Authors‘ workplace:
Oddělení klinické a radiační onkologie
Multiscan s. r. o., Pardubická krajská nemocnice
a. s., Pardubice
1; 1. a 3. lékařská fakulta UK, Praha
2; Katedra radiační onkologie IPVZ, Praha
3; Oddělení klinické onkologie, Oblastní
nemocnice Náchod
4; Klinika onkologie a radioterapie FN
Hradec Králové
5; Oddělení nukleární medicíny FN, Hradec
Králové
6; Urologická klinika FN, Hradec Králové
7; Urologické oddělení, Oblastní nemocnice
Náchod
8; Radiologická klinika FN, Hradec Králové
9
Published in:
Ces Urol 2010; 14(3): 156-163
Category:
Original article
Overview
Cíl:
Retrospektivně porovnat chronickou urinární toxicitu trojrozměrné konformní radioterapie (3D-CRT) 74 Gy a radioterapie s modulovanou intenzitou (IMRT) 78 Gy u lokalizovaného karcinomu prostaty.
Materiál a metoda:
Celkem 203 pacientů s T1-3 karcinomem prostaty bylo léčeno 3D-CRT (n = 91) a IMRT (n = 112). Medián sledování činil 5,2 roků, respektive 3,0 roky. Předepsaná dávka byla 74 Gy u 3D-CRT a 78 Gy u IMRT. Chronická urinární toxicita byla hodnocena podle Fox Chase modifikace Radiation Therapy Oncology Group a Late Effects Normal Tissue Task Force kritérií.
Výsledky:
Tříleté riziko rozvoje chronické urinární toxicity stupeň ≥ 2 po 3D-CRT a IMRT bylo srovnatelné (14 % vs. 11 %, p = 0,18). Multivariační analýza ukázala, že významnými prediktory toxicity jsou předchozí transuretrální resekce prostaty/ otevřená transvezikální prostatektomie pro benigní hyperplazii prostaty TURP/TVPE (relativní riziko 3,85) a přítomnost akutní urinární toxicity 2. a vyššího stupně (relativní riziko 2,35). Chronická urinární toxicita 3. stupně se v celém souboru objevila u 22 pacientů – při poslední kontrole bylo devět z nich (41 %) asymptomatických či s minimálními symptomy.
Závěr:
Eskalace dávky metodou IMRT (78 Gy) nevedla k nárůstu chronické urinární toxicity v porovnání s 3D-CRT. TURP/TVPE před radioterapií zvyšuje riziko urinární toxicity.
Klíčová slova:
karcinom prostaty, radioterapie, urinární toxicita, 3D-CRT, IMRT.
Úvod
Je známým faktem, že schopnost zevní radioterapie (RT) vyléčit karcinom prostaty je závislá na dávce záření. Techniky konvenční RT nemohou bezpečně doručit dávku vyšší než 70 Gy z důvodu nadměrné toxicity (1). S rozvojem technologií se v posledních letech dostaly do klinické praxe nové konformní techniky RT. Trojrozměrná konformní radioterapie (3D-CRT) těží z možnosti tvarování svazku záření podle prostorové projekce tumoru (2). V důsledku toho dochází k podstatnému šetření zdravých tkání a cílovou dávku na tumor je možné zvýšit. Jak retrospektivní, tak prospektivní randomizované studie přinesly důkazy o tom, že vysokodávkovaná 3D-CRT významně zlepšuje přežití bez biochemického relapsu (3–5).
Radioterapie s modulovanou intenzitou (IMRT) kombinuje dva přístupy: inverzní plánování, kdy uživatel nejprve definuje požadavky a limity na dávku, a kontinuální modulaci intenzity napříč svazkem během ozařování. Tak lze dosáhnout dávkové distribuce konkávního tvaru, což umožňuje šetřit kritické orgány nacházející se v těsné blízkosti cílového objemu. Příznivá je skutečnost, že u pacientů léčených vysokodávkovanou IMRT byl zaznamenán poměrně nízký výskyt (15 %) urinární toxicity 2. a vyššího stupně (6).
Máme k dispozici omezené množství informací o přímém porovnání toxicity 3D-CRT a IMRT v léčbě karcinomu prostaty (7–9). Pokud je autorům známo, v tomto kontextu zatím nebylo referováno o úrovni dávky 78 Gy, která byla jako vysoká dávka použita v randomizovaných studiích. Proto bylo naším cílem retrospektivně porovnat chronickou urinární toxicitu 3D-CRT 74 Gy a IMRT s „referenční“ vysokou dávkou 78 Gy.
Materiál a metoda
Charakteristika souboru
V období od prosince 1997 do června 2007 bylo na Klinice onkologie a radioterapie FN Hradec Králové léčeno primární kurativní radioterapií celkem 682 pacientů s lokalizovaným karcinomem prostaty. Pacienti s následujícími parametry byli kandidáty pro radikální radioterapii: lokalizovaný karcinom prostaty, žádné klinické ani chirurgické známky postižení uzlin, žádné klinické známky distančních metastáz – stadium T1-3 N0 (pN0) M0. U všech pacientů byly použity pokročilé techniky radioterapie: 3D-CRT u 458/682 pacientů (67 %) a IMRT u 224/682 pacientů (33 %).
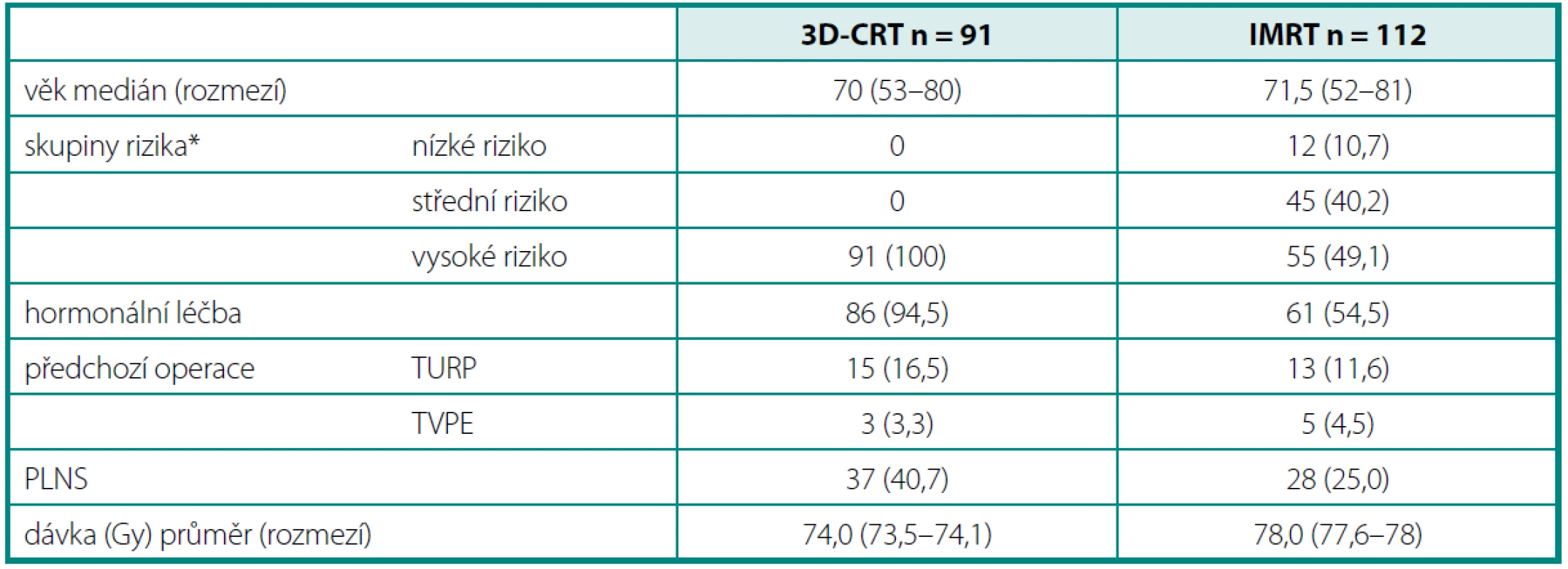
V období 10 let byla dávka záření postupně zvyšována v souladu s informacemi z prospektivních studií (10, 11). Všichni pacienti podepsali před léčbou informovaný souhlas. Pro tuto retrospektivní analýzu byly vybrány dvě skupiny pacientů na základě techniky radioterapie, období léčby a dávky záření. Skupina 3D-CRT zahrnuje 91 pacientů s T3 tumorem, kteří byli léčeni v letech 1998–2003 dávkou 74 Gy, zatímco IMRT skupina má 112 pacientů s T1-3 tumorem, kteří byli léčeni v letech 2003 až 2007 a obdrželi dávku 78 Gy (tab. 1).
3D-CRT
Plánování a provedení 3D-CRT bylo již dříve podrobně popsáno (12). Pacienti byli plánováni a léčeni v poloze na zádech s vakuovou podložkou nebo podložkou pod kolena a nohy (Vac-Lok/Dual Leg Positioner Cushion, MEDTEC) k imobilizaci dolních končetin a pánve. Všechny ozařovací plány byly vyhotoveny v 3D plánovacím systému (CadPlan 2.7.9., Varian). Plánovací cílový objem (PTV) zahrnoval prostatu a bázi semenných váčků/celé semenné váčky (SV) při jejich postižení s lemem 10 mm (ventrálně, dorzálně a laterálně), respektive 15 mm (kraniálně a kaudálně). PTV kompenzuje nepřesnost nastavení a pohyb pánevních orgánů během radioterapie.
Pacienti byli ozařováni technikou čtyř koplanárních polí s klínovými filtry (dvě laterální pole 90°, 270° a dvě přední šikmá pole 30°, 330°). Jednotlivé svazky byly tvarovány vícelistovým kolimátorem (MLC) podle trojrozměrné projekce PTV tak, aby byly šetřeny rizikové orgány (rektum a močový měchýř). Předepsaná dávka byla specifikována do izocentra (přibližně střed prostaty). V PTV jsme akceptovali nehomogenitu dávky v rozmezí 92–107 %, ačkoliv doporučená variace 95–107 % byla dodržena u většiny pacientů. K ozařování byl použit lineární urychlovač s energií fotonů 6 MV (Clinac 600 C, Varian). Předepsaná dávka byla 74 Gy během 7,5 týdne, dávka na frakci 2 Gy, jedna frakce denně.
IMRT
Řada kroků v plánování a provedení 3D-CRT a IMRT je identická. Proto zmiňujeme pouze procesy specifické pro metodu IMRT. Izotropní lem 10 mm byl přidán k prostatě a bázi SV (celým SV při jejich postižení), abychom definovali PTV. IMRT plány byly vytvářeny v plánovacím systému s inverzním plánováním (CadPlan R.6.3.6. s modulem Helios/Eclipse 7.3, Varian). Abychom dosáhli optimální distribuce dávky, použili jsme sadu limitů jak pro PTV, tak pro rizikové orgány. Limitující parametry byly následující: minimálně 95% PTV obdrží 95 % předepsané dávky; maximálně 25 % objemu rekta, respektive 30 % objemu měchýře, obdrží dávku 70 Gy. Pacienti byli ozařováni technikou pěti koplanárních polí (45°, 100°, 180°, 260°, 315°). Modulované svazky byly ozářeny pomocí MLC metodou sliding window. Předepsaná dávka byla 78 Gy během 8 týdnů, dávka na frakci 2 Gy, jedna frakce denně.
Hormonální léčba
Do roku 2002 byla hormonální léčba podávána pacientům s T3 tumorem nebo objemným tumorem. Od roku 2003 se léčebná strategie řídila kategoriemi rizika a hormonální léčba byla podávána u všech pacientů s vysokým rizikem (13). Neoadjuvantní suprese androgenů – LHRH analog a antiandrogen – byla zahájena 3–4 měsíce před 3D-CRT/IMRT a pokračovala v průběhu ozařování. Adjuvantní suprese androgenů – LHRH analog minimálně tři roky nebo oboustranná orchiektomie – byla prováděna u pacientů s nízce diferencovanými tumory (Gleasonovo skóre 8–10).
Hodnocení toxicity
Všichni pacienti byli sledováni v intervalu 3 měsíce během prvních dvou let, v intervalu 6 měsíců mezi třetím a pátým rokem po léčbě, a dále jednou ročně. Známky chronické urinární toxicity byly zaznamenávány při každé návštěvě podle Fox Chase (FC) modifikace Radiation Therapy Oncology Group (RTOG) a Late Effects Normal Tissue Task Force (LENT) kritérií pro chronickou toxicitu (tab. 2) (14, 15). Hlavní výhodou těchto kritérií je lepší popis hematurie a inkontinence.

Statistika
K odhadu kumulativního rizika chronické toxicity v čase byla použita metoda Kaplana a Meiera. Analýza podskupin pomocí log-rank testu byla provedena k určení významných prediktorů chronické toxicity. Proměnné byly analyzovány jako dichotomické parametry: věk (≤ 70 let vs. > 70 let), stadium (T1-2 vs. T3), sampling pánevních lymfatických uzlin (ano vs. ne), hormonální léčba (ano vs. ne), předchozí transuretrální resekce prostaty/otevřená transvezikální prostatektomie pro benigní hyperplazii prostaty TURP/TVPE (ano vs. ne), technika radioterapie (3D-CRT vs. IMRT), akutní toxicita (stupeň 0–1 vs. 2–4). Nakonec byla provedena multivariační analýza metodou Coxovy regrese, abychom identifikovali významné prediktory. Pouze proměnné s možným vztahem k cílovému ukazateli v univariační analýze (p ≤ 0,25) byly zavzaty do Coxovy regrese.
Výsledky
Celý soubor zahrnoval 203 pacientů s mediánem sledování 3,8 roků (0,6–9,3 roků). Ve skupině 3D-CRT (n = 91) byl medián sledování 5,2 roků (1,1–9,3 roků). IMRT skupina zahrnovala 112 pacientů s mediánem sledování 3,0 roků (0,6–5,0 roků). Žijící pacienti ve skupině 3D-CRT a IMRT měli minimální dobu sledování 3,5 roků, resp. 1,5 roků.
V celém souboru 203 pacientů nebylo zaznamenáno úmrtí na radiační toxicitu ani toxicita 4. stupně (graf 1). Kumulativní incidence urinární toxicity 2. a vyššího stupně byla ve skupině 3D-CRT téměř trojnásobná oproti skupině IMRT (26 % vs. 9 %). Rozdíl byl zřetelný především v incidenci toxicity 3. stupně.

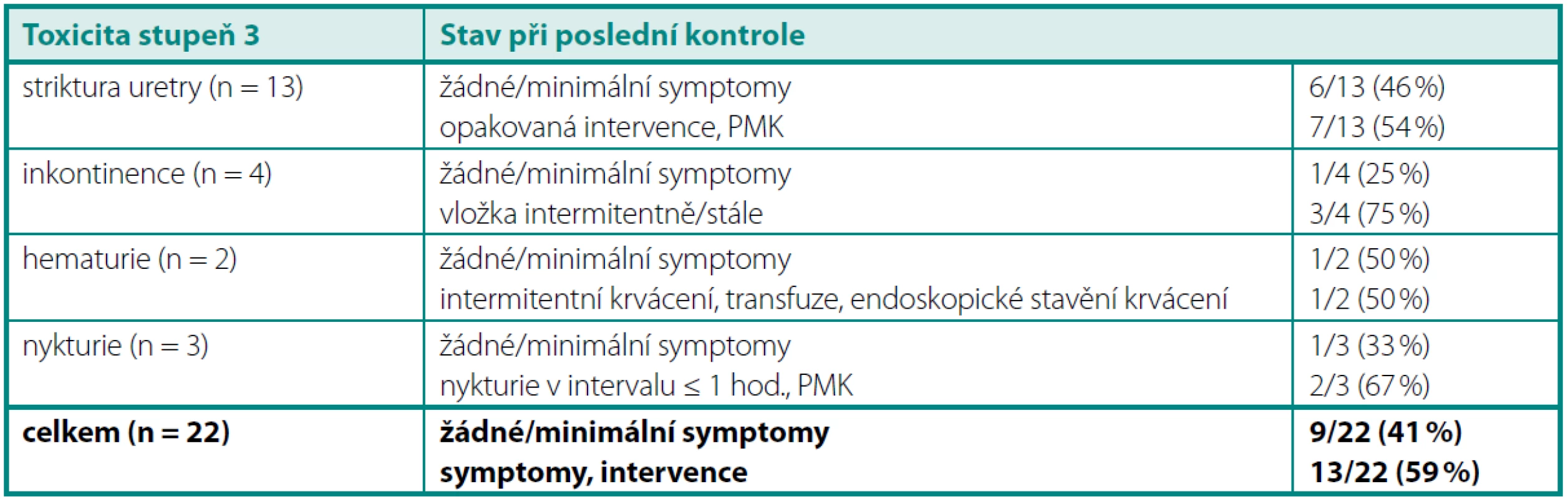
V obou skupinách dohromady (3D-CRT plus IMRT) se urinární toxicita stupeň 3 objevila u 22 pacientů, přičemž devět z nich (41 %) bylo při poslední kontrole bez obtíží nebo měli obtíže minimální (tab. 3).
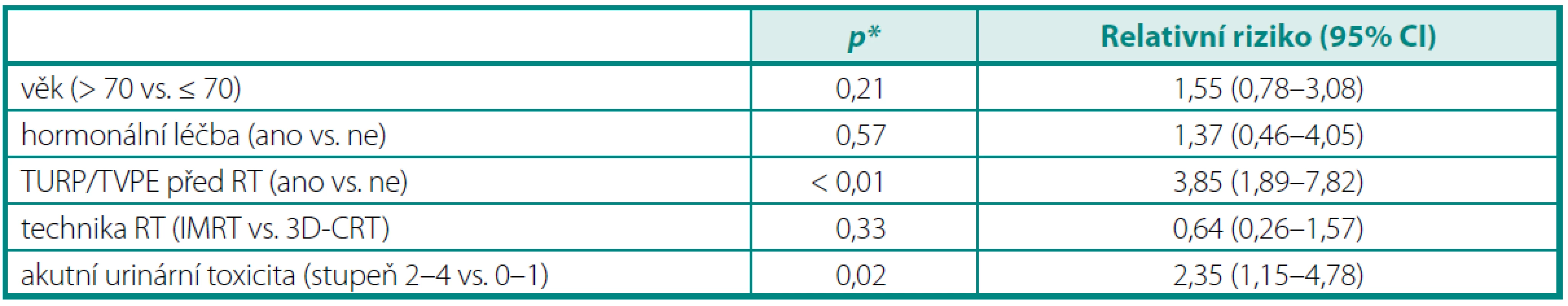
Pacienti léčení 3D-CRT měli tříleté riziko rozvoje chronické urinární toxicity stupeň ≥ 2 vyšší než pacienti léčení IMRT (14 % vs. 11 %), ovšem rozdíl mezi oběma skupinami nebyl statisticky významný (p = 0,18 log-rank) (graf 2). Multivariační analýza ukázala, že předchozí TURP/TVPE a výskyt akutní urinární toxicity 2. a vyššího stupně významně zvyšují riziko chronické urinární toxicity stupeň ≥ 2 (tab. 4).

Diskuse
Lokalizovaný karcinom prostaty je příkladem vysoké účinnosti moderní radioterapie. Lepší lokální kontroly bylo dosaženo pomocí vysokodávkované radioterapie s využitím konformních technik – 3D-CRT a IMRT. S ohledem na tento pokrok v léčbě je nanejvýš důležité detekovat, analyzovat a léčit toxicitu, která léčbu provází. V naší práci jsme demonstrovali, že eskalace dávky záření na 78 Gy je možná bez nárůstu chronické urinární toxicity. Takový příznivý výsledek lze přičítat schopnosti IMRT šetřit více zdravých tkání ve srovnání s 3D-CRT.
Výskyt chronické urinární toxicity byl v našem souboru pacientů nižší než v holandské randomizované studii (68 Gy vs. 78 Gy), kterou publikovali Peeters et al. (16). Autoři uvádějí tříletou incidenci toxicity 2. a vyššího stupně 29 % v rameni s nízkou dávkou, resp. 30 % v rameni s vysokou dávkou. Na rozdíl od našich pacientů s vysokou dávkou byla IMRT metoda použita u menší části pacientů ve finální fázi radioterapie. Data srovnatelná s našimi výsledky pochází z randomizované studie (70 Gy vs. 78 Gy) provedené v M. D. Anderson (4), kde 13 % pacientů s dávkou 78 Gy mělo symptomy urinární toxicity stupeň ≥ 2. Pacienti byli v první fázi radioterapie ozařováni konvenční technikou a ve druhé fázi metodou 3D-CRT.
Povzbudivé výsledky stran chronické urinární toxicity (stupeň ≥ 2 u 4–18 % pacientů) byly v poslední době popsány v souborech léčených vysokou dávkou (74–81 Gy) pomocí metody IMRT (6, 17, 18). Tříletá incidence u našich IMRT pacientů byla srovnatelná (11 %). Nicméně, příznivé výsledky vysokodávkované IMRT – ve smyslu nízkého výskytu urinární toxicity – je třeba posuzovat opatrně. Na rozdíl od rektální toxicity je manifestace urinární toxicity více pozvolná, zato křivka rizika nevykazuje plató. Lékaři z Memorial Sloan-Kettering Cancer Center (8) publikovali dlouhodobá data o chronické toxicitě u pacientů léčených IMRT do dávky 81 Gy. Pravděpodobnost rozvoje chronické urinární toxicity stupeň ≥ 2 byla 10 let po léčbě 20%, což byl takřka dvojnásobek v porovnání s incidencí v 5 letech. V celé populaci našich pacientů byl medián času do manifestace tohoto stupně toxicity 2,2 roků (75 % událostí se objevilo do 3,8 roků). Vezmeme-li v úvahu medián sledování pacientů v IMRT skupině (3,0 roků), definitivní hodnocení urinární toxicity bude možné až po delším časovém období.
Ve shodě s jinými autory (16, 19, 20) jsme prokázali, že transuretrální resekce prostaty (TURP) nebo otevřená transvezikální prostatektomie pro benigní hyperplazii prostaty (TVPE) předcházející RT jsou významným prediktorem rozvoje chronické urinární toxicity. Na pracovišti, kde jsme výzkum prováděli, bylo respektováno pravidlo nezahajovat RT dříve než dva měsíce po TURP/TVPE. Medián intervalu mezi TURP/TVPE a zahájením radioterapie byl 10 měsíců (2–166 měsíců). Mezi symptomy chronické urinární toxicity 3. stupně (n = 22) převládaly striktury uretry (13 pacientů). Rasweiler et al. (21) analyzovali výskyt komplikací po TURP pro benigní hyperplazii prostaty a zaznamenali až 9,8 % pacientů s pozdními strikturami uretry. Údaje z National Cancer Institutes Surveillance, Epidemiology, and End Results a z databáze Medicare (22) ukázaly, že TURP/výkony na hrdle měchýře a dilatace uretry během 5 let po RT byly provedeny u 7 %, resp. 13 % pacientů. Můžeme se domnívat, že radioterapie po TURP/ TVPE pravděpodobně zvyšuje riziko rozvoje striktury uretry. Vzhledem ke kombinaci příčin, které mají za následek tuto komplikaci, pokládáme incidenci uretrálních striktur (13/203, tj. 6,4 %) v našem souboru za přijatelnou.
V současné době očekáváme, že řada postupů může dále snížit radiační morbiditu u pacientů s karcinomem prostaty. Jedním z nich je radioterapie řízená obrazem (IGRT), která je založena na každodenní korekci pozice pacienta bezprostředně před ozářením pomocí registrace implantovaných markerů nebo registrace měkkých tkání (23). IMRT ve spojení s IGRT může profitovat z menšího bezpečnostního lemu kolem prostaty, což vede k redukci zatížení zdravých tkání.
Závěr
Kurativní IMRT karcinomu prostaty s eskalací dávky (78 Gy) vykazuje v porovnání s 3D-CRT (74 Gy) příznivý profil urinární toxicity 2. a vyššího stupně – srovnatelné tříleté riziko a nižší kumulativní incidenci. TURP/TVPE před radioterapií je negativním prediktorem rozvoje urinární toxicity.
Došlo: 3. 3. 2010
Přijato: 8. 3. 2010
Kontaktní adresa
doc. MUDr. Karel Odrážka, Ph.D.
Oddělení klinické a radiační onkologie
Multiscan & Pardubická krajská nemocnice
Kyjevská 44,
532 03 Pardubice
e-mail: odrazka@seznam.cz
Sources
1. Smit WGJM, Helle PA, van Putten WLJ, et al. Late radiation damage in prostate cancer patients treated by high dose external radiotherapy in relation to rectal dose. Int J Radiat Oncol Biol Phys 1990; 18 : 23–29.
2. Hanks GE. Conformal radiotherapy for prostate cancer. Ann Med 2000; 32 : 57–63.
3. Zelefsky MJ, Yamada Y, Kollmeier MA, Shippy AM, Nedelka MA. Long-term outcome following three-dimensional conformal/intensity-modulated external-beam radiotherapy for clinical stage T3 prostate cancer. Eur Urol 2008; 53 : 1172–1179.
4. Kuban DA, Tucker SL, Dong L, et al. Long-term results of the M. D. Anderson randomized dose-escalation trial for prostate cancer. Int J Radiat Oncol Biol Phys 2008; 70 : 67–74.
5. Al-Mamgani A, van Putten WLJ, Heemsbergen WD, et al. Update of Dutch multicenter dose-escalation trial of radiotherapy for localized prostate cancer. Int J Radiat Oncol Biol Phys 2008; 72 : 980–988.
6. Zelefsky MJ, Chan H, Hunt M, et al. Long-term outcome of high dose intensity modulated radiation therapy for patients with clinically localized prostate cancer. J Urol 2006; 176 : 1415–1419.
7. Vora SA, Wong WW, Schild SE, Ezzell GA, Halyard MY. Analysis of biochemical control and prognostic factors in patients treated with either low-dose three-dimensional conformal radiation therapy or high-dose intensity-modulated radiotherapy for localized prostate cancer. Int J Radiat Oncol Biol Phys 2007; 68 : 1053–1058.
8. Zelefsky MJ, Levin EJ, Hunt M, et al. Incidence of late rectal and urinary toxicities after three-dimensional conformal radiotherapy and intensity-modulated radiotherapy for localized prostate cancer. Int J Radiat Oncol Biol Phys 2008; 70 : 1124–1129.
9. Lips I, Dehnad H, Kruger AB, et al. Health-related quality of life in patients with locally advanced prostate cancer after 76 Gy intensity-modulated radiotherapy vs. 70 Gy conformal radiotherapy in a prospective and longitudinal study. Int J Radiat Oncol Biol Phys 2007; 69 : 656–661.
10. Zelefsky MJ, Fuks Z, Hunt M, et al. High dose radiation delivered by intensity modulated conformal radiotherapy improves the outcome of localized prostate cancer. J Urol 2001; 166 : 876–881.
11. Pollack A, Zagars GK, Starkschall G, et al. Prostate cancer radiation dose response: results of the M. D. Anderson phase III randomized trial. Int J Radiat Oncol Biol Phys 2002; 53 : 1097–1105.
12. Odrazka K, Vanasek J, Vaculikova M, et al. Conformal radiotherapy for prostate cancer – longer duration of acute genitourinary toxicity in patients with prior history of invasive urological procedure. Acta Oncol 2001; 40 : 810–815.
13. D’Amico AV, Whittington R, Malkowicz SB, et al. Pretreatment nomogram for prostatespecific antigen recurrence after radical prostatectomy or external-beam radiation therapy for clinically localized prostate cancer. J Clin Oncol 1999; 17 : 168–172.
14. Hanlon AL, Schultheiss TE, Hunt MA, et al. Chronic rectal bleeding after high-dose conformal treatment of prostate cancer warrants modification of existing morbidity scales. Int J Radiat Oncol Biol Phys 1997; 38 : 59–63.
15. Storey MR, Pollack A, Zagars G, et al. Complications from radiotherapy dose escalation in prostate cancer: preliminary results of a randomized trial. Int J Radiat Oncol Biol Phys 2000; 48 : 635–642.
16. Peeters ST, Heemsbergen WD, van Putten WL, et al. Acute and late complications after radiotherapy for prostate cancer: results of a multicenter randomized trial comparing 68 Gy to 78 Gy. Int J Radiat Oncol Biol Phys 2005; 61 : 1019–1034.
17. De Meerleer GO, Fonteyne VH, Vakaet L, et al. Intensity-modulated radiation therapy for prostate cancer: late morbidity and results on biochemical control. Radiother Oncol 2007; 82 : 160–166.
18. Eade TN, Horwitz EM, Ruth K, et al. A comparison of acute and chronic toxicity for men with low-risk prostate cancer treated with intensity-modulated radiation therapy or (125.I permanent implant. Int J Radiat Oncol Biol Phys 2008; 71 : 338–345.
19. Lawton CA, Won M, Pilepich MV, et al. Long-term treatment sequelae following external beam irradiation for adenocarcinoma of the prostate: analysis of RTOG studies 7506 and 7706. Int J Radiat Oncol Biol Phys 1991; 21 : 935–939.
20. Gardner BG, Zietman AL, Shipley WU, Skowronski UE, McManus P. Late normal tissue sequelae in the second decade after high dose radiation therapy with combined photons and conformal protons for locally advanced prostate cancer. J Urol 2002; 167 : 123–126.
21. Rassweiler J, Teber D, Kuntz R, Hofmann R. Complications of transurethral resection of the prostate (TURP. – incidence, management, and prevention. Eur Urol 2006; 50 : 969–979.
22. Berge V, Thompson T, Blackamn D. Additional surgical intervention after radical prostatectomy, radiation therapy, androgen-deprivation therapy, or watchful waiting. Eur Urol 2007; 52 : 1036–1043.
23. Stephans KL, Xia P, Tendulkar RD, Ciezki JP. The current status of image-guided external beam radiotherapy for prostate cancer. Curr Opin Urol 2010 (Epub ahead of print).
Labels
Paediatric urologist Nephrology UrologyArticle was published in
Czech Urology

2010 Issue 3
-
All articles in this issue
- Infekce močových cest po cystektomii s kontinentní ortotopickou derivací – Vesica ileale padovana (V.I.P.)
- Naše zkušenosti s aplikací rázové vlny u pacientů s induratio penis plastica (průměrná doba sledování 13 měsíců)
- Postavení magnetické rezonance a magnetické rezonanční spektroskopie při detekci karcinomu prostaty
- Molekulární vlastnosti klinicky signifikantního karcinomu prostaty
- Genetické riziko karcinomu prostaty
- Mikrochirurgická operace varikokély u dětí a dospívajících – prospektivní srovnání laparoskopické a otevřené subingvinální operace
- Chronická urinární toxicita 3D-CRT a IMRT karcinomu prostaty
- Srovnání akutní toxicity radioterapie technikou IMRT a IMRT + HDR BRT u pacientů s karcinomem prostaty vysokého rizika rekurence
- Czech Urology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Mikrochirurgická operace varikokély u dětí a dospívajících – prospektivní srovnání laparoskopické a otevřené subingvinální operace
- Naše zkušenosti s aplikací rázové vlny u pacientů s induratio penis plastica (průměrná doba sledování 13 měsíců)
- Postavení magnetické rezonance a magnetické rezonanční spektroskopie při detekci karcinomu prostaty
- Molekulární vlastnosti klinicky signifikantního karcinomu prostaty
