Doporučení pro testování PD-L1: metodika testování a reportování výsledků Verze_1 (17. 5. 2021)
Published in:
Čes.-slov. Patol., 57, 2021, No. 3, p. 179-180
Category:
Z pověření výboru SČP ČLS JEP vypracovali:
Pavel Dundr, Radoslav Matěj, Aleš Ryška
Cílem tohoto doporučení je standardizace postupu testování a reportování výsledků exprese PD-L1 u všech aktuálně relevantních indikací. Jedná se tedy dokument zaměřený na laboratorní část testování, jehož cílovou skupinou jsou nejen referenční laboratoře patologie pro prediktivní testování, ale i všichni další odborníci, kterých se testování PD-L1 týká. Nejedná se o doporučení zabývající se indikací a dalšími aspekty testování PD-L1 - v tomto ohledu pouze shrnuje aktuální doporučení definovaná na úrovni jednání odborných společností (ČOS a SČP ČLS JEP) a plátců.
1. Preanalytická fáze charakter materiálu, kvantitativní požadavky
• Materiál by měl být fixován v 10 % pufrovaném formalínu (4% formaldehydu).
• Doba fixace se odvíjí od velikosti vzorku – optimálně je to 6-24 hodin pro malé bioptické vzorky a 24 - 48 hodin pro resekáty.
• Testování PD-L1 se obecně provádí z bioptického materiálu (diagnostické vzorky, resekáty).
• Použití cytologického materiálu není pro účely exprese PDL1 validováno, dostupná data však tuto možnost připouštějí – optimálně však z materiálu zpracovaného v cytobloku. Cytologické vzorky získané z výpotků by neměly být pro účely testování exprese PD-L1 použity.
• Minimální počet nádorových buněk pro hodnocení (v principu vychází z doporučení jednotlivých kitů):
o 22C3, 28-8, SP263: pro hodnocení musí být minimálně 100 vitálních nádorových elementů. Pokud je buněk menší množství, vyšetření je NEVALIDNÍ.
o SP142: pro hodnocení musí být minimálně 50 vitálních nádorových elementů. Pokud je buněk menší množství, vyšetření je NEVALIDNÍ.
2. Používané protilátky
• Spektrum užívaných protilátek pro hodnocení PD-L1 se neustále rozšiřuje. SČP doporučuje užívat protilátky/diagnostické kity asociované s biofarmaky s tím, že je nutné dodržet příslušnou indikaci a na ní vázanou protilátku. Aktuálně lze jako rovnocenné používat klony 22C3, 28-8, SP263 pro stanovení skóre pozitivity nádorových buněk (TPS) u karcinomu plic (NSCLC). U stanovení kombinovaného skóre pozitivity (CPS) (karcinom žaludku a gastroesofageální juknkce, dlaždicobuněčný karcinom hlavy a krku, uroteliální karcinom) se musí použít protilátka/diagnostický kit 22C3. Pro stanovení skóre pozitivity imunitních buněk (IC) u karcinomu prsu a uroteliálního karcinomu se musí použít diagnostický kit SP142.
• S výjimkou SP142, kde je nutné použít diagnostický kit, a SP263, která je dostupná pouze ve formě diagnostického kitu, lze 22C3 a 28-8 použít ve formě diagnostického kitu i LDT („laboratory developed test“). V případě LDT je nutná adekvátní validace metody.
• Vyšetření exprese PD-L1 lze provádět výhradně za použití imunostaineru.
3. Principy hodnocení exprese PD-L1 a indikace typu provedeného testu
• Aktuálně jsou 3 různé principy hodnocení (Obr. 1-3):
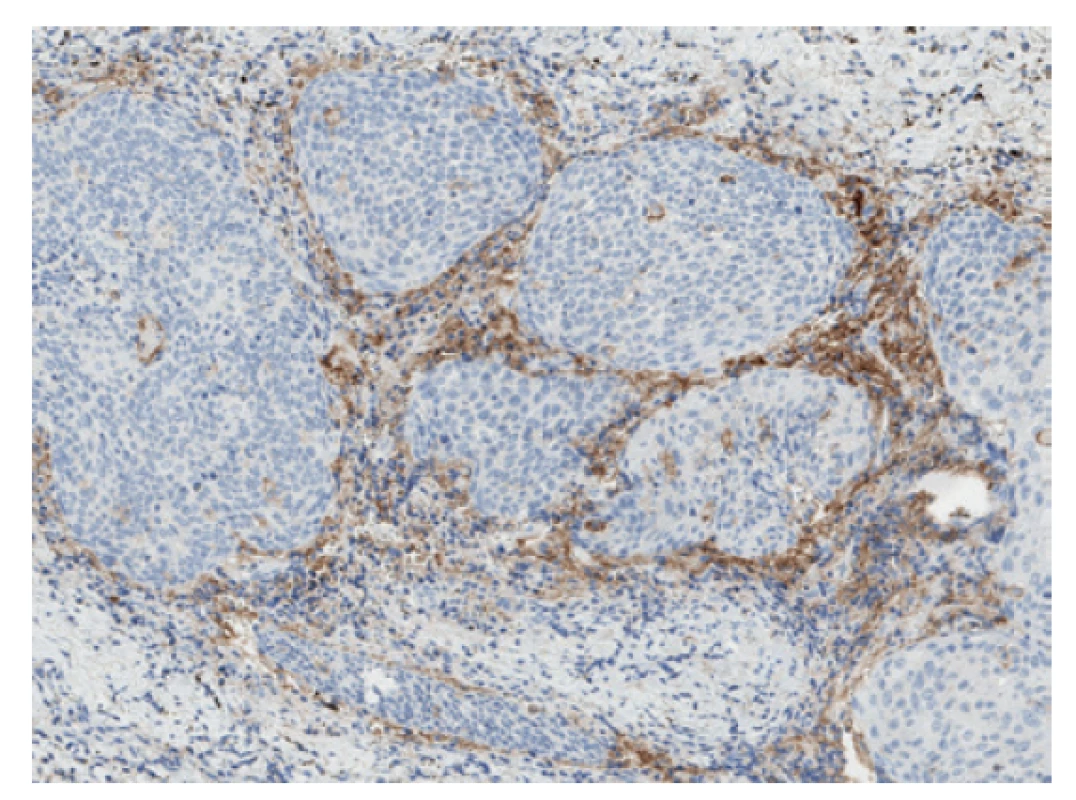
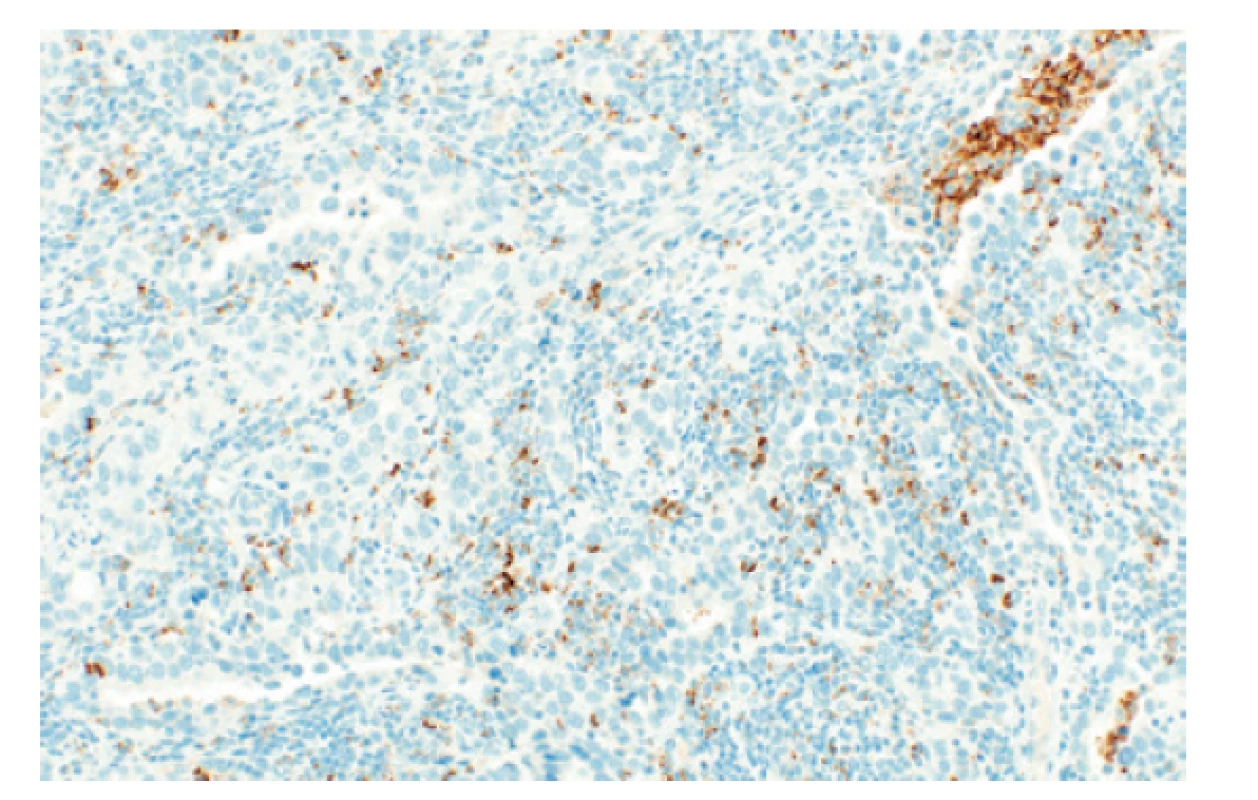
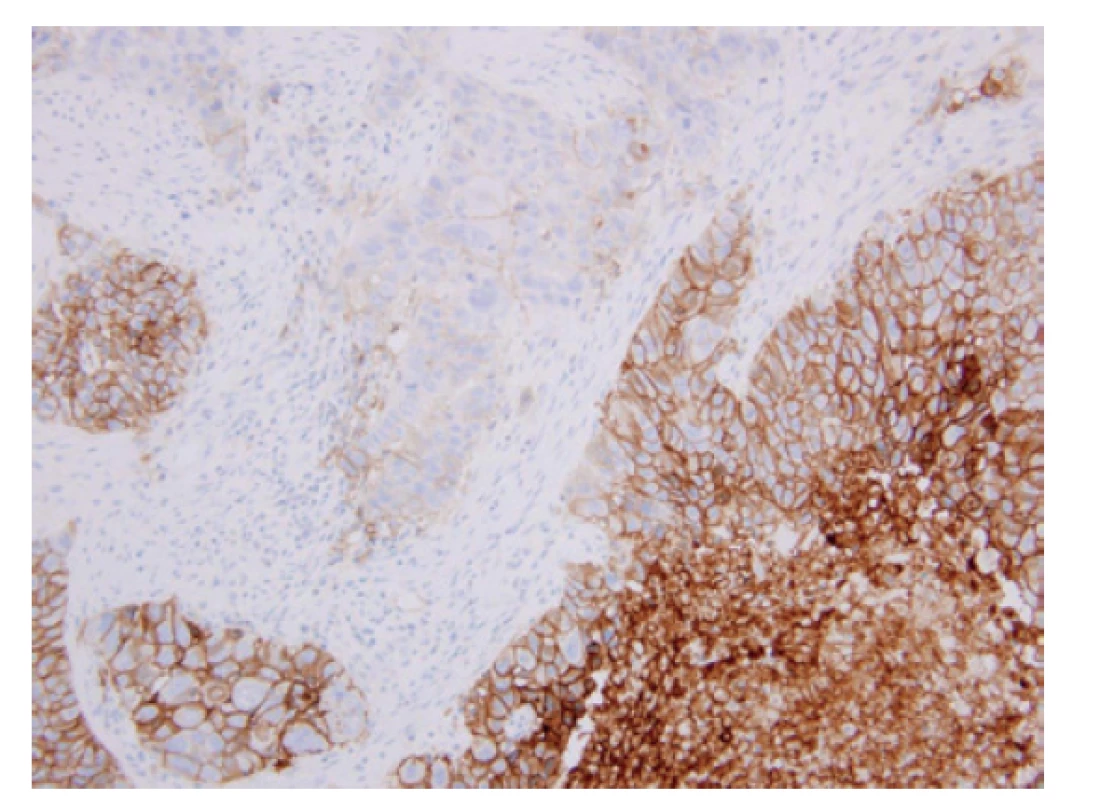
o TPS (tumor proportion score): hodnotí se % pozitivních nádorových elementů
o CPS (combined positive score): způsob výpočtu je daný počtem všech pozitivních buněk (nádorových, lymfocytů, makrofágů) děleným počtem všech vitálních nádorových buněk (PD-L1 pozitivních i negativních) násobený 100. Maximální skóre je definováno jako 100, vyšší CPS se neuvádí.
o IC (immune cells): hodnotí se % plochy nádoru infiltrované PD-L1 pozitivními zánětlivými elementy Přesné postupy / principy hodnocení jsou nad rámec tohoto sdělení, je nutné vycházet z interpretačních manuálů jednotlivých kitů.
• Indikace příslušného testu / protilátky / způsobu hodnocení vychází z nastavených algoritmů testování (např. reflexní testování u NSCLC) a/nebo požadavku indikujícího lékaře, který by měl specifikovat nejen diagnózu, ale případně i pro jakou léčbu žádá prediktivní vyšetření (to je relevantní zejména u diagnóz, u kterých je nebo bude dostupná terapie check-point inhibitory s různým prediktivním testem a způsobem hodnocení - aktuálně např. u uroteliálního karcinomu). Vzhledem k tomu, že problematika se neustále vyvíjí a není stacionární, je v těchto indikacích vždy nutné vycházet z aktuálního stavu.
4. Způsob vyhodnocení exprese PD-L1 a reportování výsledků
Bez ohledu na způsob vyšetření musí být výstupem vyhodnocení informace, jestli je výsledek testu s ohledem na příslušnou indikaci negativní či pozitivní (se zohledněním příslušných cut-offs) a dále absolutní hodnota výsledku testu. Příslušné indikace, u kterých aktuálně může být testování PD-L1 indikováno, a nastavené hraniční hodnoty (cut-offs) jsou uvedeny níže. Jedná se o aktuální stav, jak již bylo uvedeno, problematika se vyvíjí, a to je při hodnocení vždy nutno zohlednit.
Hodnocení TPS, protilátky 22C3, 28-8, SP263), NSCLC
o PD-L1 negativní: exprese PD-L1 zastižena v < 1 % nádorových buněk
o PD-L1 pozitivní: exprese PD-L1 zastižena ve ≥ 1 % NEBO ≥ 50 % nádorových buněk (v závorce uvést absolutní hodnotu TPS v %)
Hodnocení CPS, protilátka 22C3
o PD-L1 negativní: kombinované pozitivní skóre (CPS) negativní: < uvést cut-off pro příslušnou diagnózu
o PD-L1 pozitivní: kombinované pozitivní skóre (CPS) pozitivní: ≥ uvést cut-off pro příslušnou diagnózu (v závorce uvést absolutní hodnotu CPS)
Aktuálně platné hranice pozitivity CPS:
uroteliální karcinom: ≥ 10
karcinom žaludku a gastroesofageální junkce: ≥ 1
dlaždicobuněčný karcinom jícnu: ≥ 10
karcinom děložního hrdla: ≥ 1
dlaždicobuněčný karcinom hlavy a krku: ≥ 1
Hodnocení IC, protilátka SP142
o PD-L1 negativní: imunitní skóre (IC) negativní: < uvést cut-off pro příslušnou diagnózu
o PD-L1 pozitivní: imunitní skóre (IC) pozitivní: ≥ uvést cut-off pro příslušnou diagnózu (v závorce uvést absolutní hodnotu)
Aktuálně platné hranice pozitivity IC:
karcinom prsu: ≥ 1 %
uroteliální karcinom: ≥ 5 %
5. Formální obsah výsledku vyšetření
Každý výsledek MUSÍ obsahovat
• Typ vyšetřeného materiálu
• Typ protilátky (klon, výrobce, případně specifikovat, že jde o diagnostický kit)
• Způsob skórování (TPS, CPS, IC)
• Výsledek vyšetření dle formy hodnocení (viz bod 4)
6. Požadavky na laboratoř provádějící vyšetření exprese PD-L1
• laboratoř ze sítě referenčních laboratoří pro prediktivní patologii, která má příslušné vyšetření nasmlouvané s plátci,
• vyšetření musí být prováděno validovanou a akreditovanou metodou pomocí immunostaineru,
• laboratoř se musí pravidelně účastnit etablovaného programu EHK na expresi PD-L1 na všechny příslušné způsoby hodnocení, které provádí.
7. Další komentáře
• Vyšetření SP142 je aktuálně u karcinomu prsu a uroteliálního karcinomu prováděno pouze v rámci SLP zajišťovaného firmou Roche, a to pouze na několika pracovištích (Bioptická laboratoř Plzeň, VFN Praha, FN Hradec Králové a MOÚ Brno). Dle vyjádření plátců není úhrada testování z prostředků zdravotního pojištění možné, dokud nebude schválena úhrada léčby SÚKL. Po tomto schválení předpokládáme, že bude testování probíhat standardně na těch pracovištích z již zavedené sítě tzv. referenčních laboratoří, která projeví zájem toto vyšetření provádět a budou mít nasmlouvaný příslušný kód s plátci.
• Od 1. 1. 2021 je schválený VZP výkon 87695 „Vyhledání a ověření materiálu pro prediktivní vyšetření, včetně předání na referenční pracoviště“. Tento kód po nasmlouvání mohou vykazovat všechna pracoviště, která materiál do tzv. referenční laboratoře odesílají na kterékoliv prediktivní vyšetření, včetně exprese PD-L1.
Labels
Anatomical pathology Forensic medical examiner ToxicologyArticle was published in
Czecho-Slovak Pathology

2021 Issue 3
-
All articles in this issue
- Next-Generation Pathology
- Cesta k cíli vede přes spolupráci
- 'PATOLOGIE MĚKKÝCH TKÁNÍ
- 'PATOLOGIE ORL OBLASTI
- 'UROPATOLOGIE
- 'GYNEKOPATOLOGIE
- 'NEFROPATOLOGIE
- 'HEPATOPATOLOGIE
- 'KARDIOPATOLOGIE
- 'HEMATOPATOLOGIE
- 'PATOLOGIE MĚKKÝCH TKÁNÍ
- 'PATOLOGIE GIT
- 'CYTODIAGNOSTIKA
- 'LABORATORNÍ METODY
- Next generation sequencing – a science tool or routine pathology?
- 'PULMOPATOLOGIE
- Next generation sequencing and the molecular tumor board from the point of view of oncologists
- The possibilities of molecular testing of somatic aberrations in tumor tissue using NGS in routine practice - current situation in the Czech Republic
- Next generation sequencing and its application in the diagnostics of neuromuscular diseases
- Methylation pattern in the diagnosis and prognosis of brain cancer
- Review of tumor infiltrating lymphocytes assessment in breast cancer in routine diagnostic practice
- Undiagnosed cryptococcal meningoencephalitis with extensive hypoxic-ischemic brain injury mimicking grade 3 diffuse axonal injury
- Doporučení pro testování PD-L1: metodika testování a reportování výsledků Verze_1 (17. 5. 2021)
- Molecular testing in endometrial carcinoma (Joint recommendation of Czech Oncological Society, Oncogynecological Section of the Czech Gynecological and Obstetrical Society, Society of Radiation Oncology, Biology and Physics, and the Society of Czech Pathologists)
- Giant cell myocarditis in young woman diagnosed at the autopsy: a case report
- Czecho-Slovak Pathology
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Doporučení pro testování PD-L1: metodika testování a reportování výsledků Verze_1 (17. 5. 2021)
- Next generation sequencing – a science tool or routine pathology?
- Molecular testing in endometrial carcinoma (Joint recommendation of Czech Oncological Society, Oncogynecological Section of the Czech Gynecological and Obstetrical Society, Society of Radiation Oncology, Biology and Physics, and the Society of Czech Pathologists)
- Methylation pattern in the diagnosis and prognosis of brain cancer
