Antidiabetická liečba v prevencii aterosklerózy: posledné desaťročie
Antidiabetic treatment in prevention of atherosclerosis: last decade
In the last five years, the results of several studies aimed at testing the cardiovascular (CV) safety (so-called “CVOT” studies) of newer antidiabetic drug users have been published, which have attracted special attention and become one of the most important in diabetology. Indeed, they have shown that drugs from the group of SGLT-2 cotransport inhibitors (SGLT2i) and GLP-1 receptor agonists (GLP1-RA) are not only cardiovascular safe, but their addition to treatment is associated with a significant reduction in cardiovascular and renal morbidity and mortality even with previously complexive cardioprotective treatment. In the review article, we analyze the results of the most important randomized controlled trials, as well as a study from real practice, as well as the implementation of these findings into therapeutic recommendations.
Keywords:
antidiabetic treatment – Atherosclerosis – cardiovascular diseases – dipeptidyl peptidase 4 inhibitors – GLP1 receptor agonists – SGLT-2 cotransport inhibitors
Authors:
Emil Martinka 1,2
Authors‘ workplace:
Národný endokrinologický a diabetologický ústav, n. o., Ľubochňa
1; Fakulta zdravotníckych vied Piešťany, Univerzita Sv. Cyrila a Metoda, Trnava
2
Published in:
Forum Diab 2021; 10(Supplementum 1): 16-27
Category:
Overview
V posledných 5 rokoch boli publikované výsledky niekoľkých štúdií zameraných na testovanie kardiovaskulárnej (KV) bezpečnosti (Cardiovascular Outcome Trial – CVOT) novších farmák pre liečbu diabetes mellitus 2. typu (DM2T), ktoré vzbudili mimoriadnu pozornosť a stali sa jednými z najvýznamnejších v diabetológii. Ukázali totiž, že farmaká zo skupiny inhibítorov kotransportu SGLT2 (SGLT2i) a GLP1-receptorových agonistov (GLP1-RA) nielenže sú kardiovaskulárne bezpečné, ale ich pridanie do liečby sa združuje so signifikantnou redukciou ukazovateľov KV - a renálnej morbidity a mortality, a to aj pri predtým vyťaženej kardioprotektívnej liečbe. V prehľadovom článku sa venujeme rozboru výsledkov najvýzamnejších randomizovaných kontrolovaných štúdií, ale aj štúdií z reálnej praxe, ako aj implementácii týchto poznatkov do terapeutických odporúčaní.
Klíčová slova:
antidiabetická liečba – ateroskleróza – GLP1 receptorové agonisty – inhibítory dipeptidylpeptidázy 4 – inhibítory kotransportu SGLT2 – kardiovaskulárne ochorenia
Úvod
V posledných 5 rokoch boli publikované výsledky niekoľkých štúdií zameraných na testovanie kardiovaskulárnej (KV) bezpečnosti (Cardiovascular Outcome Trial – CVOT) novších farmák pre liečbu DM2T, ktoré vzbudili mimoriadnu pozornosť a stali sa jednými z najvýznamnejších v diabetológii. Ukázali totiž, že farmaká zo skupiny inhibítorov kotransportu SGLT2 (SGLT2i) a GLP1-receptorových agonistov (GLP1-RA) nielenže sú kardiovaskulárne (KV) bezpečné, ale ich pridanie do liečby sa združuje so signifikantnou redukciou ukazovateľov KV - a renálnej morbidity a mortality, a to aj pri predtým vyťaženej kardioprotektívnej liečbe. Zjednodušene, pridanie SGLT2i viedlo k redukcii hospitalizácií pre SZ (hSZ), a to aj u pacientov na predtým vyťaženej liečbe pre SZ, ďalej k redukcii ukazovateľov vzniku a progresie chronickej choroby obličiek (Chronic Kidney Disease – CKD) a individuálne aj k redukcii KV - a celkovej mortality, a pridanie GLP1-RA viedlo k redukcii aterosklerotických (ATS) KV-príhod (infarkt myokardu – IM, cievna mozgová príhoda-CMP), ukazovateľov CKD a individuálne aj k redukcii KV - a celkovej mortality. Obe skupiny farmák teda prispievajú k signifikantnej redukcii reziduálneho KV-rizika, pričom každá iným spôsobom, čo význam týchto farmák ešte zvyšuje. Ak vychádzame z predošlých poznaní, že viaceré farmaká z iných skupín (glitazóny, viaceré deriváty sulfonylurey a niektoré inhibítory DPP4 (DPP4i) ako saxagliptín a čiastočne aj alogliptín) sa spájajú so zvýšeným KV-rizikom, potom význam farmák zo skupiny SGLT2i a GLP1-RA zásadným spôsobom vplýva aj na filozofiu antidiabetickej liečby DM2T, obzvlášť keď prinášajú viaceré výhody aj vo všeobecnej rovine, ako sú vysoká efektivita na úpravu glykémie pri nízkom riziku hypoglykémie, priaznivý efekt na telesnú hmotnosť, viscerálnu obezitu, krvný tlak, krvné lipidy, parametre chronického subklinického zápalu, oxidačný stres a ďalšie patofyziologické deje, ktoré sa uplatňujú v procesoch aterotrombogenézy a ovplyvňujú energetický metabolizmus srdca.
GLP1-receptorové agonisty a kardiovaskulárne riziko v medicíne dôkazov
Podstatou svojho účinku sú GLP1-receptorové agonisty (GLP1-RA) najviac príbuzné gliptínom [5,46]. Ich účinok však nezávisí od hladiny a sekrécie vlastných inkretínových hormónov, ale receptory pre GLP1 stimulujú priamo. Účinok na pokles glykémie je výraznejší než pri gliptínoch, riziko hypoglykémie je však nízke. GLP1-RA tiež vedú k významnému poklesu telesnej hmotnosti a výraznejší je aj efekt na pokles krvného tlaku. Zlepšujú profil krvných lipidov, znižujú hladiny markerov chronického subklinického zápalu, prejavy oxidačného stresu, zvyšujú tvorbu oxidu dusnatého (NO), zlepšujú mikrovaskulárny „recruitment“ a mikrovaskulárny prietok krvi, prejavujú priaznivý efekt na endotel ciev, antiproliferatívny účinok na bunky hladkého svalstva ciev a bunky endotelu a iné biomarkery KV-rizika. Tieto účinky môžu mať antiaterotrombotický efekt, môžu spomaľovať progresiu aterosklerózy [1,67] a vysvetľovať tak benefity pozorované v randomizovaných kontrolovaných (Randomized Controlled Trial – RCT) CVOT štúdiách.
Kým v poradí prvá CVOT štúdia ELIXA (6 068 pacientov s DM2T s nedávnou koronárnou príhodou u všetkých účastníkov, s mediánom sledovania 2,1 roka), s GLP1-RA lixisenatidom vs placebo preukázala neutrálny efekt pridania lixisenatidu na mieru rizika KV-morbidity a mortality [59], výsledky v poradí druhej CVOT štúdie – LEADER s liraglutidom preukázali, že pridanie liraglutidu v porovnaní s placebom viedlo k signifikantnej redukcii primárneho kombinovaného ukazovateľa (3P-MACE) zloženého z KV-úmrtia, nefatálneho infarktu myokardu (nfIM) a nefatálnej mozgovej príhody (nfCMP). Spomedzi jednotlivých zložiek dominovala signifikantná redukcia úmrtia z KV-príčin o 22 % a došlo tiež k redukcii výskytu nfIM o 12 % na hranici štatistickej významnosti a štatisticky nevýznamnej redukcii nfCMP o 11 %. Okrem toho, došlo aj k signifikantnej redukcii úmrtia z akejkoľvek príčiny o 15%. Štúdia LEADER bola realizovaná na populácii s viac ako 9 000 pacientmi s DM2T s vysokým KV-rizikom, predošlé KV-ochorenie (KVO) malo 81% účastníkov. Medián sledovania bol 3,8 roka [33].
Štatisticky významný benefit redukcie v rovnakom primárnom kombinovanom ukazovateli 3P-MACE o 26 % preukázala aj ďalšia RCT/CVOT štúdia SUSTAIN-6, v ktorej bol do liečby pridaný semaglutid vs placebo. V rámci jednotlivých komponentov semaglutid síce neviedol k redukcii KV-úmrtia ani k redukcii výskytu nfIM, viedol však k signifikantnej redukcii nfCMP, a to až o 39 %, a k redukcii potreby koronárnej alebo periférnej revaskularizácie o 35 %. Štúdia SUSTAIN-6 bola zrealizovaná na súbore 3 297 pacientov s DM2T, v rámci ktorého malo predošlé KVO 83% účastníkov. Medián sledovania bol 2,1 roka [34]. V poradí ďalšou publikovanou bola RCT/CVOT štúdia EXSCEL s exenatidom QW, v ktorej liečba exenatidom QW síce viedla len k hraničnej redukcii primárneho 3P-MACE, v sekundárnych exploratívnych analýzach sa však spájala so signifikantným poklesom úmrtia z akejkoľvek príčiny o 14 %. Štúdia EXSCEL bola zrealizovaná na súbore 14 752 pacientov s DM2T, z ktorých malo predošlé KVO 73 % a medián sledovania predstavoval 3,2 roka [21]. Ďalšou významnou a vo viacerých otázkach aj kľúčovou bola RCT/CVOT štúdia REWIND s dulaglutidom, ktorá na rozdiel od predošlých zahŕňala nielen účastníkov s už známym predošlým KVO (31 %) ale aj pacientov bez KVO, teda pacientov, ktorí sa výskytom KVO a KV-rizika podobali bežným ambulantným pacientom s DM2T. Štúdia v ramene s pridaním dulaglutidu preukázala v porovnaní s placebom signifikantnú redukciu primárneho kombinovaného ukazovateľa 3P-MACE o 12 %, ako aj signifikantnú redukciu nfCMP o 24 %, a to tak u pacientov s predošlým KVO, ako aj u pacientov bez KVO. Efekt na redukciu nfIM a KV-mortality sa nepreukázal. Došlo tiež k zníženiu celkovej mortality o 10 %, ktorého miera bola len tesne nad hranicou štatistickej významnosti (p = 0,067). Kardiovaskulárny benefit liečby dulaglutidom sa teda v tejto štúdii preukázal nezávisle od prítomnosti, resp. neprítomnosti predošlého KVO. Štúdia REWIND bola zrealizovaná na súbore 9 901 pacientov a bola doteraz najdlhšie trvajúcou CVOT štúdiou s mediánom sledovania až 5,4 roka [15].
Priaznivé sú tiež výsledky štúdie HARMONY s albiglutidom na súbore 9 463 pacientov so 100% prítomnosťou predošlého KVO a mediánom sledovania 1,6 roka, v ktorej liečba albiglutidom v porovnaní s placebom okrem signifikantnej redukcie primárneho kombinovaného ukazovateľa 3P-MACE o 22 %, viedla aj k signifikantnej redukcii samotného nfIM o 25 % [20]. Napokon, priaznivo sa javí aj bezpečnostná RCT/CVOT štúdia PIONEER-6 so semaglutidom prispôsobeným na perorálne použitie. Liečba perorálnym semaglutidom vs placebom preukázala KV-bezpečnosť a naznačila aj redukciu primárneho kombinovaného ukazovateľa 3P-MACE o 21 %, čo však nebolo štatisticky významné. V štúdii bola pozorovaná aj signifikantná redukcia úmrtia z KV-príčin až o 50 %, ako aj úmrtia z akejkoľvek príčiny až o 49 %. Tieto výsledky je však možné považovať len za exploratívne, nakoľko výsledok v primárnom kombinovanom ukazovateli nebol signifikantný. Nepreukázala sa ani redukcia nfIM a nfCMP. Štúdia PIONEER 6 bola zrealizovaná na súbore 3 183 pacientov, v rámci ktorého malo prítomné KVO alebo CKD 85 % účastníkov. Medián sledovania bol iba 15,9 mesiaca [23]. Po potvrdení KV-bezpečnosti aktuálne prebieha s perorálnym semaglutidom RCT/CVOT štúdia SOUL, ktorej cieľom je preukázať KV-benefit. Porovnanie výsledkov jednotlivých CVOT štúdií s GLP1-RA zobrazuje tab. 1. Priaznivý efekt s redukciou miery rizika v primárnom kompozitnom ukazovateli 3P-MACE bol dosiahnutý prakticky vo všetkých štúdiách s výnimkou štúdie ELIXA a EXSCEL a PIONEER-6. Pri štúdii ELIXA s lixisenatidom je však potrebné poukázať na niektoré významné odlišnosti v sledovanej populácii pacientov, výber sa zameral na pacientov s nedávnym akútnym koronárnym syndrómom (AKS), čo je vysokoriziková skupina: počty príhod boli v oboch ramenách 2-krát vyššie než vo väčšine ostatných štúdií, čo mohlo efekt liečby maskovať. Dizajn štúdie by tak mohol do veľkej miery vplývať na konečný výsledok.
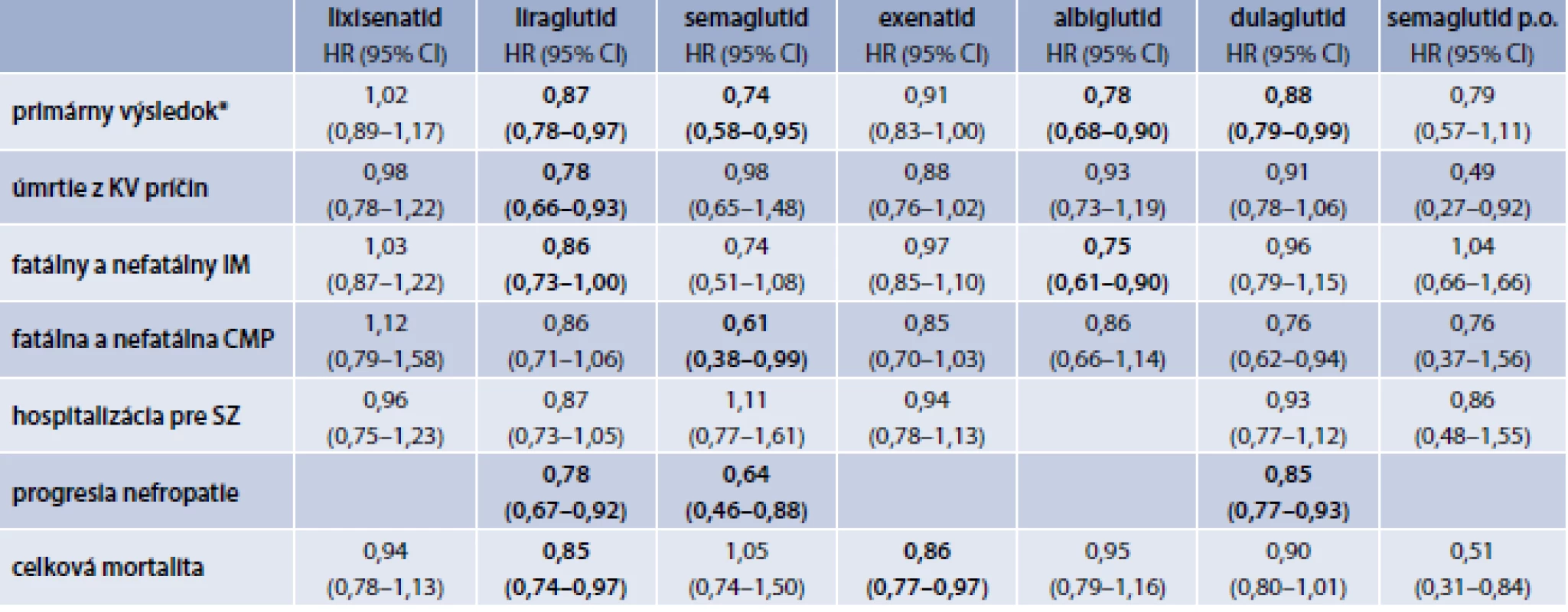
V rámci viacerých RCT/CVOT štúdií s GLP1-RA boli hodnotené aj renálne ukazovatele. Signifikantná redukcia novej alebo zhoršenia jestvujúcej nefropatie bola preukázaná v štúdii LEADER s liraglutidom, SUSTAIN-6 so semaglutidom a v štúdiách REWIND a AWARD 7 s dulaglutidom, a v štúdii ELIXA s lixisenatidom, v rámci kombinovaného ukazovateľa aj jeho jednotlivých zložiek [32,43].
V štúdii LEADER s liraglutidom bol kombinovaný reálny ukazovateľ definovaný ako pretrvávajúca makroalbuminúria, trvalé zdvojnásobenie hladiny kreatinínu v sére alebo trvalá potreba náhradnej liečby dialýzou alebo transplantáciou. Liečba liraglutidom sa v porovnaní s placebom spájala so signifikantnou redukciou kombinovaného ukazovateľa o 22 %, signifikantnou redukciou makroalbuminúrie o 26 %. Rozdiel v dvojnásobnom vzostupe sérového kreatinínu, ani potreba náhradnej liečby dialýzou/transplantáciou nedosiahli štatistický význam [32]. V štúdii SUSTAIN-6 so semaglutidom bol kombinovaný renálny ukazovateľ definovaný ako pretrvávajúca makroalbuminúria, trvalé zdvojnásobernie hladiny kreatinínu v sére alebo eGF < 45 ml/min/1,73 m2 alebo trvalá potreba náhradnej liečby dialýzou alebo transplantáciou. Liečba semaglutidom sa spájala so signifikantnou redukciou kombinovaného ukazovateľa o 36 % [22]. V štúdii REWIND s dulaglutidom bol kombinovaný reálny ukazovateľ definovaný ako nová makroalbuminúria, pretrvávajúci pokles eGF o > 30 %, alebo dialýza/transplantácia). Liečba dulaglutidom sa spájala so signifikantnou redukciou kombinovaného ukazovateľa o 15 %, v rámci čoho dominoval najmä signifikantný efekt na redukciu novej makroalbuminúrie o 23 % [16]. Okrem toho, štúdia AWARD 7 preukázala redukciu poklesu eGF a spomalenie progresie ochorenia u pacientov s DM2T so stredne ťažkou až ťažkou CKD [68]. Napokon, podľa výsledkov post-hoc analýzy výsledkov štúdie ELIXA prejavoval renálny benefit aj lixisenatid, a to redukciou progresie albuminúrie (pomer albuminu a kreatinínu v moči/Urine Albumin-to-Creatinine Ratio – UACR) u pacientov s makroalbuminúriou a nižším rizikom novo vzniknutej makrolabuminúrie, po úprave na východiskovú hodnotu HbA1c a ďalšie tradičné renálne rizikové faktory [43]. V kohortovej registrovej škandinávskej štúdii sa liečba GLP1-RA v porovnaní s DPP4i združovala aj s nižším výskytom závažných renálnych príhod (dialýza, úmrtie, hospitalizácia z renálnych príčin) [53]. Renálny benefit preukázaný v doterajších štúdiách s GLP1-RA sa opiera najmä o pokles albuminúrie, nie však o eGF, konečné štádium renálneho zlyhávania, či úmrtie z renálnej príčiny. To súvisí so skutočnosťou, že doterajšie štúdie boli dizajnované primárne na hodnotenie KV-bezpečnosti a renálne ukazovatele boli sekundárnym ukazovateľom alebo vyplynuli z exploratívnej analýzy, čo mohlo oslabovať silu detekcie renálneho benefitu [76]. Aktuálne prebieha štúdia FOW so semaglutidom s primárnym renálnym ukazovateľom, výsledky ktorej sa očakávajú v roku 2024.
Na základe vyššie uvedených informácií o GLP1-RA, ako je priaznivý efekt na väčšinu KV-rizikových faktorov, telesnú hmotnosť a najmä výsledky CVOT štúdií, v ktorých došlo k redukcii výskytu ATS KVO, sa predpokladá, že GLP1-RA by mohli ovplyvňovať samotný proces aterogenézy. Takéto vysvetlenie KV-benefitu GLP1-RA podporujú aj viaceré experimentálne štúdie s pozorovaním priaznivého účinku na markery chronického subklinického zápalu, oxidačný stres, bunky endotelu, hladké svalstvo ciev či funkcie makrofágov [67].
Súhrn
GLP1-RA sú ideálnou voľbou do včasnej kombinácie s metformínom u všetkých pacientov s DM2T, pokiaľ nie sú kontraindikované alebo netolerované. V porovnaní s inými farmakami prejavujú lepší efekt na kontrolu glykémie nalačno (Fasting Plasma Glucose – FPG) aj postprandiálnej (Postprandial Plasma Glucose – PPG) a úpravu HbA1c, pri nízkom riziku hypoglykémie. Okrem toho prejavujú celý rad fyziologických účinkov, ktoré sa uplatňujú na úrovni viacerých orgánov a poskytujú priaznivý efekt na kontrolu telesnej hmotnosti, krvného tlaku, krvných tukov, markerov chronického subklinického zápalu a ďalších kardiometabolických rizikových faktorov. Prejavujú tiež ochranný efekt na funkcie B-buniek.
U pacientov s už rozvinutým aterosklerotickým KVO alebo vysokým rizikom takéhoto ochorenia, alebo chronickou chorobou obličiek sú GLP1-RA preferovanou a s dôrazom odporúčanou liečbou, a to nezávisle od hladiny HbA1c a na akomkoľvek stupni liečby s cieľom redukcie rizika KV - aj celkovej mortality, redukcie progresie aterosklerózy a aterosklerotických KV-príhod (IM, CMP) a redukcie novej alebo progresie jestvujúcej chronickej choroby obličiek (redukcia albuminúrie). Ak je pacient v čase pridania GLP1-RA už na 2 - alebo viackombinácii iných antidiabetík, alebo ak už dosiahol cieľ pre HbA1c, z hľadiska redukcie rizika hypoglykémie sa odporúča redukcia dávky alebo zastavenie podávania inej účinnej látky. Pri indikácii liečby je podobne ako pri iných liekoch potrebné rešpektovať kontraindikácie a upozornenia uvedené v SPC. Podľa SPC, GLP1-RA sa nemajú podávať pacientom s gastroparézou a so zápalovými ochoreniami čriev a opatrnosť je potrebná u pacientov s ochoreniami štítnej žľazy, rizikom dehydratácie, anamnézou prekonanej pankreatitídy či s rizikom akútnej pankreatitídy. Pacienti majú byť informovaní o typických príznakoch akútnej pankreatitídy. V prípade podozrenia na pankreatitídu sa má liečba vysadiť, a ak sa pankreatitída potvrdí, nemá sa znovu používať. V doteraz ukončených CVOT štúdiách s GLP1-RA sa zvýšené riziko akútnej pankreatitídy ani karcinómu pankreasu nepotvrdilo. V štúdiách LEADER a SUSTAIN-6 bol zaznamenaný vyšší výskyt cholelitiázy a akútnej cholecystitídy v skupine liečených liraglutidom, resp. semaglutidom [33,34].
Inhibítory kotransportu SGLT2 a kardiovaskulárne riziko v medicíne dôkazov
Inhibítory kotransportu SGLT2 – (gliflozíny) sú novou skupinou perorálnych antidiabetík s viacerými špecifickými vlastnosťami a so zásadným prínosom pre medicínsku prax, ako aj pre vývoj vedeckých poznatkov. Pokles glykémie sa dosahuje blokovaním spätnej reabsorpcie glukózy z primárneho moču v proximálnom tubule obličiek inhibíciou kotransportu SGLT2 [70,72]. Dôležitým faktom je, že účinok inhibítorov kotransportu SGLT2 (SGLT2i) na úpravu glykémie je nezávislý od sekrécie inzulínu aj od citlivosti tkanív na inzulín. Gliflozíny tak poskytujú významný a spoľahlivý účinok na kontrolu glykémie nielen pri monoterapii, ale aj aditívny efekt pri všetkých kombináciách vrátane kombinácie s inzulínom. Cennou vlastnosťou je aj skutočnosť, že úprava glykémií sa dosahuje pri minimálnom riziku hypoglykémie a navyše dochádza k redukcii zvýšenej telesnej hmotnosti s redukciou viscerálneho tuku a úpravou rovnováhy adipokínov [68,72]. Okrem toho, gliflozíny vedú k poklesu krvného tlaku s redukciou tzv. after-loadu, bez vzostupu frekvencie srdca. Vedú tiež k poklesu triacylglycerolov, k vzostupu HDL, poklesu kyseliny močovej, tuhosti ciev, plazmatických hladín PAI-1 [6,9]. Prejavujú diuretický účinok, čo vedie k redukcii extracelulárneho objemu a zníženiu tzv. pre-loadu, a priaznivý účinok na remodeláciu srdca. Zvyšujú hladiny provaskulárnych progenitorových buniek, redukujú ischemického-reperfúzne poškodenie myokardu, a vedú k tzv. off-target inhibícii Na+/H+ výmenníka myokardu. Prostredníctvom aktivácie AMP-kinázy spolu so zníženou autofágiou a nižšími hladinami CD36 a kardiotoxických lipidov v srdci chránia srdce pred energetickým vyčerpaním (LPS indukovanou depléciou ATP/ADP), a vedú tiež k redukcii prejavov chronického subklinického zápalu zvýšenou expresiou protizápalových markerových proteínov v makrofágoch s redukciou hladín hsCRP. V kardiomyocytoch a makrofágoch empagliflozín zoslaboval expresiu TNFα a iNOS indukovanú LPS [3,9,17,29,30,71]. Podľa niektorých autorov môžu gliflozíny zlepšovať energetický metabolizmus myokardu aj uprednostňovaním využívania substrátov menej náročných na kyslík, ako sú ketolátky vs voľné mastné kyseliny (VMK) [12]. Energetický metabolizmus srdca je u pacientov s DM2T a inzulínovou rezistenciou zmenený. Metabolizmus glukózy je zredukovaný a zvyšuje sa podiel metabolizmu VMK, ktoré sú náročné na spotrebu kyslíka. Zvýšenie podielu využívania ketolátok – výrazne menej náročných na spotrebu kyslíka, by tak mohlo byť pre myokard výhodné [12,26].
Ako ukázali početné RCT/CVOT štúdie, liečba gliflozínmi prináša viaceré morbiditno-mortalitné benefity zásadného významu. Výsledky prvej publikovanej CVOT štúdie EMPA-REG OUTCOME [77] na populácii viac ako 7 000 pacientov s DM2T s vysokým KV-rizikom a prekonaným KV-ochorením/príhodou preukázali signifikantnú redukciu relatívneho rizika primárneho kompozitného ukazovateľa zloženého z KV-úmrtia, nfIM a nfCMP o 14 %. V rámci jednotlivých zložiek dominovala signifikantná redukcia KV-mortality, a to až o 38 %, ktorá sa ukázala aj ako rozhodujúca zložka, zatiaľ čo efekt na výskyt nfIM a nfCMP zostal neutrálny. Túto diskrepanciu vysvetlila sekundárna analýza výsledkov, ktorá poukázala na výraznú redukciu potreby hospitalizácií pre srdcové zlyhávanie (hSZ) o 35 % a hSZ alebo úmrtia pre srdcové zlyhávanie až o 39 % [77]. K redukcii rizika hSZ a KV-úmrtia viedla liečba empagliflozínom konzistentne nezávisle od predošlej prítomnosti, resp. neprítomnosti SZ pred liečbou [13]. Liečba empagliflozínom tiež viedla k redukcii celkovej mortality o 32 %. Efekt empagliflozínu na mortalitu znamenal, že pri liečbe asi 1 000 pacientov sa zachráni 25 životov, alebo sa predíde jednému z troch KV-úmrtí [77]. Jedna z post-hoc analýz štúdie EMPA-REG OUTCOME zameraná na časové vyhodnotenie priaznivých KV-účinkov v priebehu trvania liečby empagliflozínom ukázala, že redukcia hSZ sa uplatňuje už od 17. dňa liečby, redukcia kombinovaného ukazovateľa zloženého z úmrtia pre KV-príčinu alebo hSZ už od 27. dňa liečby a redukcia samotného úmrtia pre KV-príčinu už od 59. dňa liečby, a tieto pretrvávali počas celého priebehu liečby [73]. Iná analýza ukázala, že liečba empagliflozínom odďaľuje potrebu iniciácie liečby inzulínom u predtým inzulínom neliečených pacientov s DM2T a KVO, a to až o 54 %, a u pacientov s DM2T a KVO, ktorí už boli liečení inzulínom, liečba empagliflozínom viedla k 57% redukcii potreby navýšenia dávky inzulínu o viac ako 20 %. Ďalšia analýza ukázala, že terapeutický benefit empagliflozínu sa ešte prehlbuje, ak sa analyzuje výskyt nielen prvej, ale výskyt všetkých epizód sledovaných KV-ukazovateľov. Analýza ukázala, že liečba empagliflozínom sa združovala so signifikantnou redukciou príhod 3P-MACE o 22 %, 4P-MACE (3P-MACE + hospitalizácia pre nestabilnú anginu pectoris) o 18 %, hlavných koronárnych príhod (nfIM alebo koronárna revaskularizácia) o 20 %, rozšírených koronárnych príhod (nf-IM, koronárna revaskularizácia alebo nestabilná angina pectoris) o 17 %, ako aj signifikantnú redukciu samotných príhod nfIM o 21%. Liečba empagliflozínom súčasne signifikantne znižovala potrebu hSZ o 42 %, hSZ a úmrtie z KV-príčin o 44 %, všetky prípady hospitalizácií o 17 % a tiež samotné úmrtia z KV-príčin o 38 % a úmrtia z akejkoľvek príčiny o 31 %. V porovnaní s redukciou rizika prvej príhody v rámci 3P-MACE o 14 % predstavovala redukcia všetkých príhod 3P-MACE (pri rovnakom počte zaradených pacientov) až 22 %. A podobne, v porovnaní s redukciou počtu prvých príhod nfIM o 13 % (nebol dosiahnutý signifikantný rozdiel), celkový počet príhod nfIM dosiahol pri liečbe empagliflozínom signifikantnú redukciu o 21 % [36]. Podobný efekt bol zistený aj pri porovnaní prvej a celkového počtu hlavných koronárnych príhod. Benefit liečby empagliflozínom sa ešte prehĺbil aj v redukcii hSZ. Zatiaľ čo pri analýze prvej príhody hSZ predstavoval 35 %, pri celkovom počte hSZ predstavoval pokles až o 42 %, a tiež pri analýze prvej a všetkých príhod kompozitného ukazovateľa pozostávajúceho z hSZ a úmrtia z KV-príčin z 34 % na 44 % [37]. Napokon, k zvýrazneniu signifikantného terapeutického benefitu v prospech liečby empagliflozínom došlo aj pri hospitalizáciách z akejkoľvek príčiny a podľa ich počtu. Terapeutický benefit empagliflozínu sa teda z celkovým počtom príhod ešte zvyšoval. Ďalšia post hoc analýza štúdie EMPA-REG OUTCOME ukázala, že pri liečbe empagliflozínom s mediánom trvania 2,6 roka a sledovaní s mediánom 3,4 roka, empagliflozín signifikantne redukoval riziko všetkých príhod/hospitalizácií z akejkoľvek príčiny a úmrtí z akejkoľvek príčiny o 19 %, pričom spomedzi hospitalizácií boli najčastejšou príčinou KVO, infekcie a ochorenia nervového systému [24]. S cieľom prevencie jednej príhody, úmrtia alebo hospitalizácie bolo potrebné liečiť 5,4 pacientov počas 3 rokov [25]. Zásadný význam všetkých týchto zistení podčiarkuje skutočnosť, že uvedené prínosy boli dosiahnuté v teréne už predošlej vyťaženej liečby statínmi a ACE-inhibítormi, ktoré boli donedávna považované za jediné skupiny s dokázaným KV-benefitom. Navyše, efekt empagliflozínu vo vyjadrení na počet pacientov, ktorých treba liečiť, aby sa predišlo jednému úmrtiu, tzv. NNT (počet pacientov, ktorých treba liečiť, aby sa predišlo jednému úmrtiu – Number Needed to Treat – NNT), bol nižší než v prípade simvastatínu či ramiprilu. Empagliflozím sa ukázal ako účinná a bezpečná liečba aj u starších pacientov [41], s vekom však narastá výskyt viacerých rizikových stavov, ako sú napríklad dehydratácia, inkontinencia, hypotenzia, urogenitálne infekcie a pod, prítomnosť ktorých môže znamenať prekážku používania SGLT2i.
Nedávno bola ukončená aj ďalšia RCT-štúdia s empagliflozínom – EMPEROR-Reduced, v ktorej boli zaradení pacienti s DM2T, ale aj bez diabetu, s chronickým srdcovým zlyhávaním a zníženou ejekčnou frakciou (EF ≤ 40 %) [7,47]. Štúdia ukázala, že liečba empagliflozínom sa v porovnaní s placebom združovala so signifikantnou redukciou príhod primárneho kompozitného ukazovateľa zloženého z KV-úmrtia alebo hospitalizácie pre KV-príčinu o 25 %, v rámci ktorého dominovala signifikantná redukcia hSZ o 13,2 %. Signifikantná miera redukcie sa preukázala aj v sekundárnych ukazovateľoch ako celkový počet hospitalizácií, urgentné vyšetrenie pre SZ, hSZ vyžadujúca príjem na JIS, v intenzifikácii liečby diuretikami, ale tiež u novej diagnózy DM2T u pacientov, ktorí predtým DM nemali.
Okrem KV-protektívneho efektu empagliflozín prejavuje aj významný nefroprotektívny efekt. V štúdii EMPA-REG OUTCOME, empagliflozín v porovnaní s placebom po pridaní k štandardnej liečbe pacientov s DM2T s vysokým KV-rizikom signifikantne redukoval vznik novej nefropatie, alebo zhoršenie jestvujúcej nefropatie o 39 %, progresiu do makroalbuminúrie o 38 %, progresiu do zdvojnásobenia hodnoty kreatinínu v sére o 44 % a začiatok potreby dialýzy alebo transplantácie obličiek o 55 %. Renálny benefit bol zhodný u pacientov s už jestvujúcou chronickou chorobou obličiek ako aj bez nej a dostavil sa ako efekt „naviac“ k liečbe inhibítorom renín-angiotenzín-aldosterónového systému (RAAS) [74,77]. Aktuálne prebieha štúdia EMPA-Kidney, pri ktorej je hlavným ukazovateľom primárny renálny kompozitný ukazovateľ, a to u pacientov s chronickou chorobou obličiek a DM2T, ale aj bez diabetu.
Priaznivý KV - a renálny efekt liečby gliflozínmi preukázala aj štúdia CANVAS s kanagliflozínom [58]. Liečba kanagliflozínom viedla k významnej redukcii relatívneho rizika príhod kompozitného ukazovateľa 3P-MACE o 14 %, významnej redukcii potreby hSZ o 33 % a tiež k významnej redukcii progresie nefropatie o 27 % (progresie albuminúrie) až 40 % (redukcia eGF, dialýza, transplantácia alebo úmrtie pre renálnu príčinu). Liečba kanagliflozínom však na rozdiel od empagliflozínu neviedla k redukcii KV - ani celkovej mortality.
Štúdia CREDENCE, ktorej primárnym cieľom boli renálne ukazovatele a v ktorej boli zaradení pacienti s chronickou chorobou obličiek s eGF 30–90 ml/min/1,73 m2 a UACR 300–5 000 mg/g, preukázala signifikantnú redukciu primárneho kompozitného ukazovateľa zloženého z koncového štádia chronickej choroby obličiek (End-Stage Renal Disease – ESRD), zdvojnásobenia kreatinínu v sére alebo úmrtia z renálnej alebo KV-príčiny o 30 % ako aj jeho jednotlivých zložiek s výnimkou renálneho úmrtia a hraničnou signifikantnosťou redukciou KV-úmrtia (p < 0,0502) nezávisle od vstupnej hodnoty eGF. Hranične významná bola aj redukcia potreby dialýzy a transplantácie obličiek. Signifikantnú mieru redukcie nadobudli aj sekundárne KV-ukazovatele ako 3P-MACE o 20 % a KV-úmrtie alebo hospitalizácia hSZ o 31% [57,59].
Výsledky inej RCT/CVOT štúdie DECLARE-TIMI 58 [42,75] s ďalším zástupcom SGLT2i – dapagliflozínom síce nepreukázala signifikantnú redukciu primárneho kombinovaného ukazovateľa 3P-MACE, aj táto štúdia však preukázala signifikantnú redukciu hSZ a redukciu novej alebo progresie jestvujúcej chronickej choroby obličiek (CKD) [42,75]. Okrem toho, v ďalšej štúdii s dapagliflozínom – DAPA-HF, bol efekt liečby dapagliflozínom na srdcové zlyhávanie priamo primárnym ukazovateľom. V súbore boli zahrnutí pacienti s už známym srdcovým zlyhávaním s redukovanou EF (HErEF), avšak nielen s DM2T, ale aj bez diabetu. Štúdia preukázala signifikantnú redukciu v primárnom kompozitnom ukazovateli zloženom z KV-úmrtia, hSZ, urgentného vyšetrenia pre SZ o 25 % u pacientov s DM2T, resp. 27 % u pacientov bez DM, ako aj samotného zhoršenia SZ o 23 %, resp. 38 % a všetkých príčin úmrtia o 22 % (DM2T) [38,39]. Nedávno bola ukončená aj štúdia DAPA-CKD, ktorej primárny kombinovaný ukazovateľ bol zameraný zas priamo na renálne funkcie a do ktorej boli opäť okrem pacientov s DM2T zahrnutí aj pacienti bez diabetu, s chronickou chorobou obličiek s eGF v rozsahu 25–75 ml/min/1,73 m2 a albuminúriou 200–5 000 mg/g. Štúdia ukázala, že liečba dapagliflozínom viedla aj tu, nezávisle od prítomnosti DM2T k signifikantnej redukcii primárneho kombinovaného renálneho ukazovateľa zloženého z poklesu eGF o 50 %, ESRD, alebo úmrtia pre renálnu alebo KV-príčinu o 44 %. Na základe týchto štúdií bolo SPC dapagliflozínu rozšírené aj o indikáciu symptomatického srdcového zlyhávania so zníženou ejekčnou frakciou.
Okrem RCT-štúdií sú k dispozícii aj výsledky RWE-štúdií, ako sú štúdie programu CVD REAL [27,28] či štúdia EMPRISE [49–51,54–56], ktoré potvrdili výsledky RCT-štúdií redukcie mortality, potreby hSZ a progresie poklesu renálnych funkcií. Štúdia CVD-REAL porovnávala hodnotené parametre medzi pacientmi, ktorí v sledovanom období začali liečbu SGLT2i oproti pacientom na iných antidiabetikách. V štúdii boli zahrnuté akékoľvek SGLT2i, pre zrovnanie súborov bola použitá metóda „propensity score matching“ v pomere 1 : 1, a do vyhodnotenia bolo následne zaradených > 300 000 pacientov (> 150 000 v každej skupine). Výsledky štúdie CVD-REAL ukázali, že užívanie SGLT2i v porovnaní s inými antidiabetikami bolo spojené s nižšou mierou hSZ o 39 %; úmrtia o 51 % a hSZ o 46 %. Výsledky CVD-REAL 2 ukázali, že použitie SGLT2i oproti iným antidiabetikám sa združovalo so signifikantne nižším rizikom úmrtia o 49 %, hSZ o 36 %, úmrtia alebo hSZ o 40 %, nfIM o 19 % a nfCMP o 32 %) [27,28]. A napokon, výsledky CVD-REAL 3 ukázali že použitie SGLT2i oproti iným antidiabetikám sa združovalo so signifikantne nižším rizikom progresie poklesu funkcií obličiek o 51 % [18,19]. Štúdia EMPRISE je pokračujúca štúdia s priebežnými analýzami. V jednej kohorte porovnáva hodnotené paramete medzi pacientmi, u ktorých bola v sledovanom období začatá liečba empagliflozínom vs DPP4i, a v druhej kohorte výsledky medzi pacientmi liečenými emagliflozínom vs GLP1-RA. Pre zrovnanie súborov bola použitá metóda „propensity score matching“ s použitím viac ako 140 premenných v pomere 1 : 1 a v každej skupine bolo zaradených viac ako 39 000 pacientov. Výsledky priebežnej analýzy po 3 rokoch ukázali, že porovnaním pacientov liečených empagliflozínom a pacientov liečených DPP4i sa v súlade s výsledkami RCT-štúdií zistila signifikantne nižšia miera mortality pacientov užívajúcich empagliflozín, a to až o 48 %. Riziko incidencie aterosklerotických príhod ako IM, CMP, nestabilná angina pectoris či potreba koronárnej revaskularizácie bolo porovnateľné, signifikantne nižšia však v súlade s RCT-štúdiami bola aj kumulatívna incidencia potreby hSZ, a to až o 49 %. Signifikantne nižšia incidencia hSZ pri rovnakom efekte na mieru incidencie aterosklerotických KV-príhod bola zistená aj pri porovnaní pacientov liečených empagliflozínom a pacientov liečených GLP1-RA [49]. Výsledky štúdie EMPRISE sú zaujímavé aj z hľadiska nákladov hradenej zdravotnej starostlivosti a ekonomickej argumentácie, keď liečba empagliflozínom sa spájala aj s nižšou mierou potreby hospitalizácií z akýchkoľvek príčin o 22 %, s nižšou mierou potreby návštev urgentného príjmu o 20 %, ako aj s kratším trvaním hospitalizácie o 1,4 dňa [10,44,45,54,56]. Podobne v kohortovej registrovej škandinávskej štúdii sa liečba SGLT2i v porovnaní s DPP4i združovala s nižším rizikom srdcového zlyhávania, úmrtia z akejkoľvek príčiny [52] ako aj s nižším výskytom závažných renálnych príhod (dialýza, úmrtie, hospitalizácia z renálnych príčin) [53].
Pokiaľ ide o riziká a nežiaduce účinky, pôvodná obava z výskytu uroinfekcií sa neukázala ako zásadný klinický problém. Je však potrebné na túto komplikáciu myslieť. Výskyt genitálnych infekcií, hlavne kandidovej etiológie, bol však signifikantne zvýšený, a to viac u žien. Opatrnosť pri liečbe gliflozínmi je potrebná aj u pacientov so sklonom k dehydratácii a jej následkom a pravdepodobne tiež u pacientov po CMP, hoci SPC takúto obavu priamo neuvádza. Pokiaľ ide o podávanie gliflozínov u pacientov s poklesom eGF, do hodnoty 60 ml/min/1,73 m2 nie sú potrebné žiadne úpravy dávok pri žiadnej z troch molekúl (empagliflozín, kanagliflozín, dapagliflozín) aktuálne používaných na Slovensku (schéma). Pri poklese eGF medzi 60–45 ml/min/1,73 m2 je možné pokračovať v liečbe empagliflozínom v maximálnej dávke 10 mg, liečba by sa však už nemala začínať. Pri dapagliflozíne je postup rovnaký, dávku však nie je potrebné redukovať. Pri kanagliflozíne je na základe výsledkov štúdie CREDENCE možné začať liečbu aj pokračovať v liečbe až do hodnoty eGF 30 ml/min/1,73 m2, avšak v dávke maximálne 100 mg, pričom pri eGF < 45 ml/min/1,73 m2 je podmienkou indikácie kanagliflozínu aj pomer albuminu a kreatinínu v moči (UACR) > 300 mg/g. V liečbe je možné pokračovať aj pri eGF < 30 ml/min/1,73 m2 s maximálnou dávkou 100 mg, nemala by sa však už začínať. Pri potrebe dialyzačnej liečby je však liečbu kanagliflozínom ukončiť.
U niektorých pacientov bola opísaná tzv. euglykemická diabetická ketoacidóza. Jej výskyt pravdepodobne súvisel s nesprávnou indikáciou SGLT2i pacientom s DM1T, resp. nepoznaným latentným autoimuntným diabetom (LADA), alebo nepoznaným pankreatogénnym diabetom. Za potenciálne spúšťacie mechanizmy sa považuje interkurentné ochorenie, dehydratácia, chirurgický zákrok, stres, znížený príjem potravy a tekutín, redukcia dávok inzulínu, nízka funkčná rezerva B-buniek, zvýšené nároky na inzulín a požitie alkoholu.
Porovnanie výsledkov jednotlivých CVOT štúdií s SGLT2i zobrazuje tab. 2.
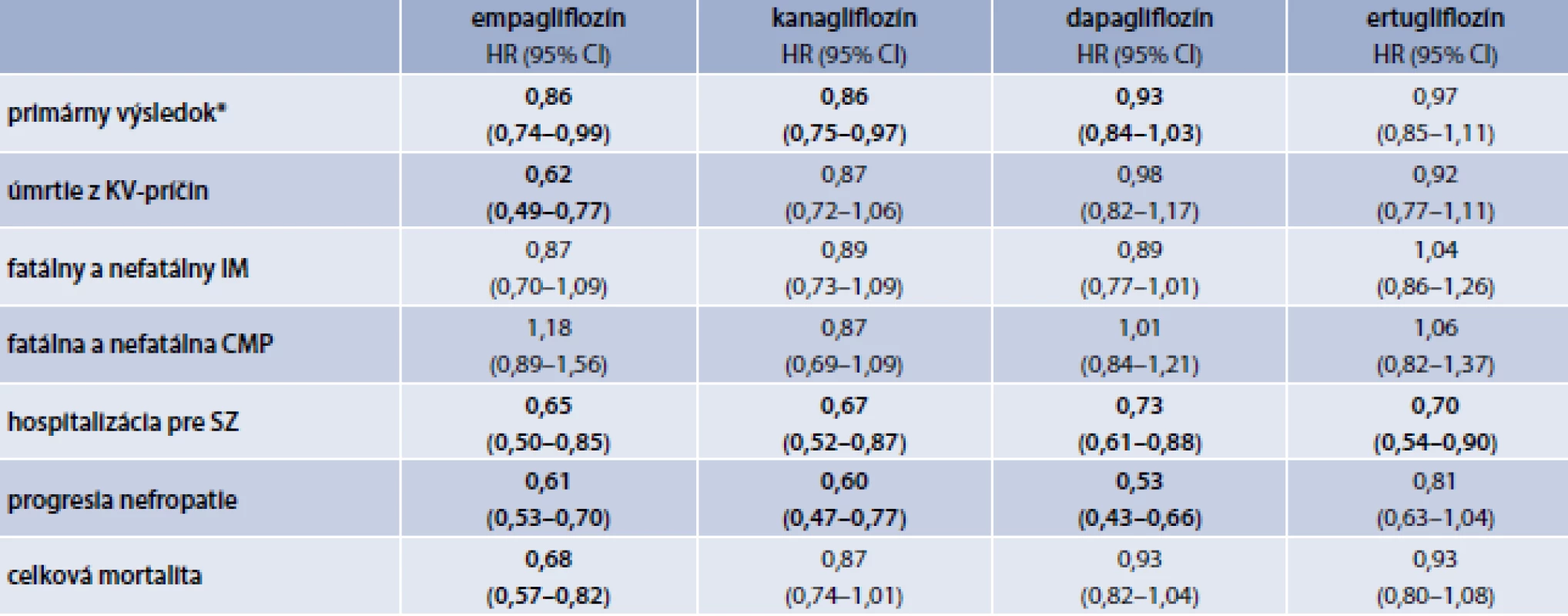
Súhrn
SGLT2i sú ideálnou voľbou do včasnej kombinácie s metformínom u všetkých pacientov s DM2T, pokiaľ nie sú kontraindikované alebo netolerované. V porovnaní s inými perorálnymi antidiabetikami prejavujú lepší efekt na kontrolu glykémie aj úpravu HbA1c pri nízkom riziku hypoglykémie. Naviac, poskytujú priaznivý efekt na kontrolu telesnej hmotnosti, krvného tlaku a väčšinu kardiometabolických rizikových faktorov. U pacientov so srdcovým zlyhávaním, už prítomným KVO s dominanciou rizika rozvoja srdcového zlyhávania alebo vysokým rizikom takéhoto ochorenia alebo chronickou chorobou obličiek sú SGLT2i preferovanou a s dôrazom odporúčanou liečbou, a to nezávisle od hladiny HbA1c, na akomkoľvek stupni liečby, s cieľom redukcie rizika KV - aj celkovej mortality, hospitalizácie pre srdcové zlyhávanie a redukcie novej alebo progresie jestvujúcej CKD (redukcia albuminúrie a progresie poklesu eGF). Ak je pacient v čase pridania SGLT2i už na dvoj - alebo viackombinácii iných antidiabetík, alebo ak už dosiahol cieľ pre HbA1c, z hľadiska eliminácie rizika hypoglykémie sa odporúča redukcia dávky alebo zastavenie podávania inej účinnej látky [2,8,11,63–66].

Inhibítory dipeptidylpeptidázy 4 a kardiovaskulárne riziko v medicíne dôkazov
Inhibítory dipeptidylpeptidázy 4 (gliptíny) sú relatívne široká skupina farmák, ktoré účinkujú prostredníctvom inhibície štiepenia inkretínových hormónov produkovaných črevom, predovšetkým glukagónu podobného peptidu 1 (Glucagon-Like Peptide 1 – GLP1) a od hladiny glukózy závislého inzulínotropného peptidu (Glucose-dependent Insulinotropic Peptide – GIP), čím zvyšujú ich hladiny (tab. 3), ale aj mnohých ďalších substrátov ako mozgový nátriuretický peptid (Brain Natriuretic Peptide – BNP), PYY (peptid YY), GLP2, NPY (neuropeptid Y), SDF1α (Stromal cell-Derived Factor 1α) a iné [4,31,46]. V súčasnosti sem patria molekuly sitagliptín, vildagliptín, alogliptín, linagliptín, saxagliptín, gemigliptín, anagliptín, teneligliptín, evogliptín a ďalšie. Na Slovensku je kategorizovaných prvých päť z nich [40]. Vďaka komplexnému efektu na kontrolu glykémie (stimulácia sekrécie inzulínu, supresia sekrécie glukagónu, spomalenie vyprázdňovania žalúdka) možno pri týchto farmakách očakávať síce mierny, ale spoľahlivý prídavný efekt na úpravu glykémií a HbA1c pri monoterapii, ale aj pri všetkých terapeutických kombináciách vrátane kombinácie s inzulínom. Hlavnou výhodou gliptínov (obzvlášť v porovnaní s prípravkami sulfonylurey) je nízky výskyt hypoglykémie, hmotnostná neutralita a málo nežiaducich účinkov [14,35,62]. Za ďalšie prínosy možno považovať priaznivý efekt na redukciu krvného tlaku, úpravu hladín krvných tukov, redukciu hladín parametrov chronického subklinického zápalu, podporu „recruitmentu“ kmeňových angiogénnych buniek v ischemickom myokarde a ďalšie [4]. V klinických RCT/CVOT štúdiách zameraných na KV-morbiditu a mortalitu sa však prínos týchto farmák neprejavil. Naopak, pri niektorých, ako je saxagliptín [61] a čiastočne aj alogliptín, vznikla obava zo zvýšeného rizika srdcového zlyhávania, ak sa podávali pacientom s vysokým KV-rizikom. Nejde však o „class“ efekt, keďže pri iných prípravkoch (sitagliptín v štúdii TECOS a linagliptín v štúdii CARMELINA) sa takéto riziko nepotvrdilo [48,60,73]. Výhodou linagliptínu je tiež možnosť jeho použitia aj u pacientov v terminálnom štádiu ochorenia obličiek bez potreby redukcie dávky. Zásadnou bezpečnostnou otázkou, ktorá vzišla z klinických štúdií a bola rôzne interpretovaná aj pri viacerých metaanalýzach, je pretrvávajúca obava zo zvýšeného rizika akútnej pankreatitídy, ktoré bolo potvrdené, a rizika karcinómu pankreasu, ktoré nebolo potvrdené [69].
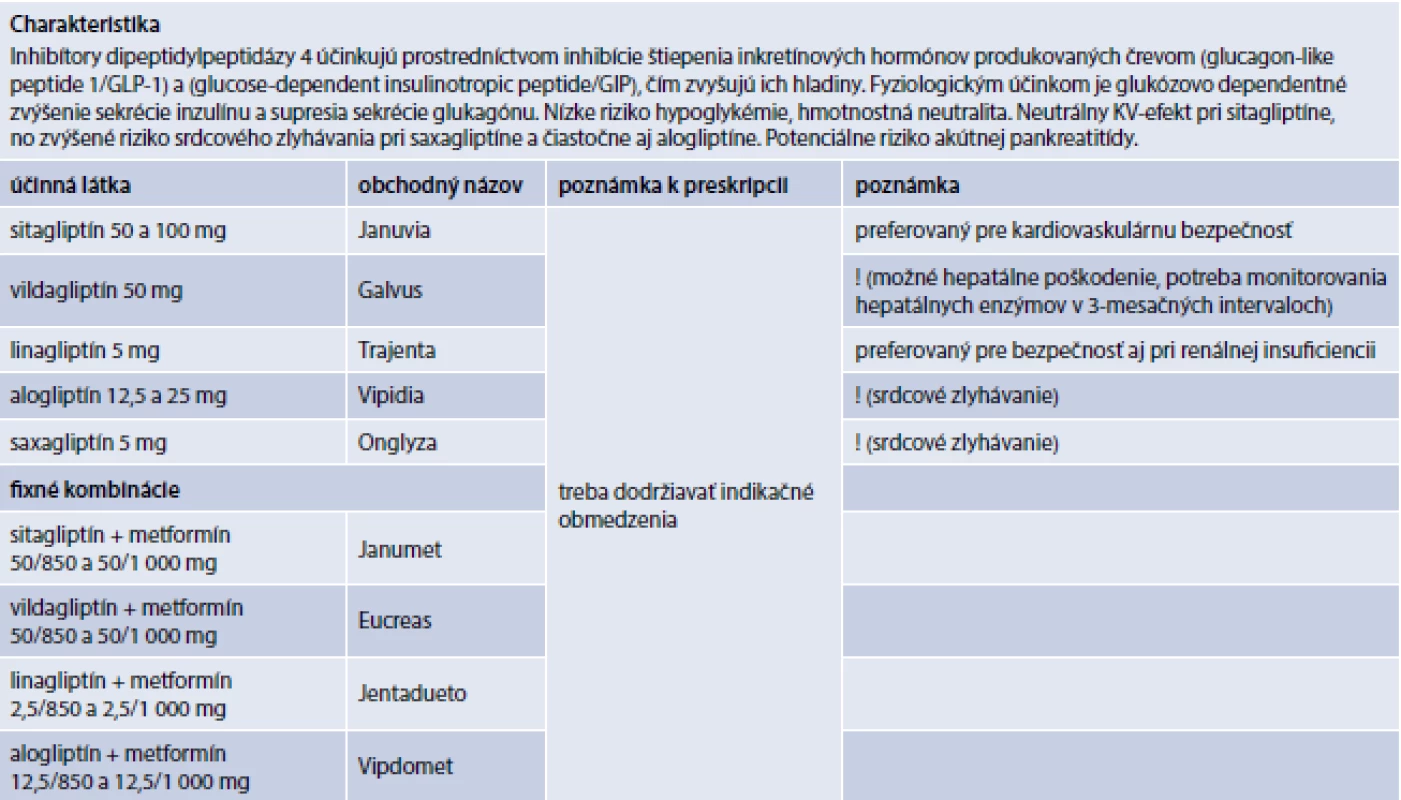
Súhrn
DPP4i sú pomerne širokou skupinou antidiabetických farmák. Kým sitagliptín a linagliptín sú kardiovaskulárne neutrálne, saxagliptín a čiastočne aj alogliptín môžu zvyšovať riziko srdcového zlyhávania. Výhodou DPP4i je v porovnaní s derivátmi sulfonylurey nižšie riziko hypoglykémie a nízke riziko nežiaducich účinkov, ako aj možnosť použitia v celom spektre renálnych funkcií vrátane koncových štádií zlyhania obličiek. Taktiež sú vhodnou voľbou pre starších pacientov s DM2T liečených viacerými farmakami, keďže majú pri zachovanej účinnosti aj veľmi dobrý bezpečnostný profil s nízkym rizikom interakcií, ako bolo potvrdene v subanalýze RCT/CVOT TECOS [48,73]. V odporúčanej hierarchii zastávajú druhú líniu výberu k metformínu, to však platí iba pre sitagliptín a linagliptín, ktoré sú v rámci skupiny preferovaným výberom. Pri indikácii liečby je podobne ako pri iných liekoch potrebné rešpektovať kontraindikácie a upozornenia uvedené v SPC, nepodávať DPP4i pacientom s prekonanou pankreatitídou a uvážiť vhodnosť ich podávania aj u pacientov s prítomnými rizikovými faktormi pre jej vznik. SPC upozorňuje aj na hlásené prípady bulózneho pemfigoidu u pacientov užívajúcich DPP4i. Ak je podozrenie na bulózny pemfigoid, liečba sa má ukončiť.
Záver
Aká je aktuálna filozofia antidiabetickej liečby DM2T? Keďže liečime diabetes, ochorenie, pre ktoré je typický nadmerný vzostup cukru v krvi, určite jeho individualizovaná úprava, pretože bolo dokázané, že redukuje rozvoj mikrovaskulárnych komplikácií, a tiež preto, že v opačnom prípade by sa už nejednalo o antidiabetickú liečbu. Medzi jednotlivými antidiabetikami sú však veľké rozdiely, a to nielen v efektivite a bezpečnosti úpravy glykémií a združených kardiometabolických ukazovateľov, ale najmä v priaznivom vs rizikovom účinku na riziko kardiocerebrovaskulárnej a renálnej morbidity a mortality.
Podľa referenčných odporúčaní [2,8,11,66], ako aj názoru SDiA/SDS, sa za preferovanú iniciálnu farmakologickú liečbu DM2T považuje metformín a za optimálnu kombináciu k metformínu sa považuje GLP1-RA alebo SGLT2i. Tieto farmaká sú preferované nielen z dôvodu výrazného efektu na úpravu glykémií pri nízkom riziku hypoglykémie a priaznivom efekte na telesnú hmotnosť, ale najmä z dôvodu potvrdeného kardiovaskulárneho, cerebrovaskulárneho a renálneho benefitu. Ak GLP1-RA alebo SGLT2i nie je možné použiť, v hierarchii výberu nasleduje DPP4i s potvrdenou KV-bezpečnosťou, a to sitagliptín alebo linagliptín. Na nižšej priečke vhodnosti výberu sú deriváty sulfonylurey (SU – preferenčne glimepirid a gliklazid MR) a inzulín, a za najmenej uprednostňovaný výber, rezervovaný skôr len pre určité typy pacientov (napr. pacienti s nealkoholovou steatohepatitídou) považujeme glitazóny, spomedzi ktorých je preferovaný pioglitazón.
Uvedená hierarchia výberu je vhodná pre všetkých pacientov s DM2T, obzvlášť je však odporúčaná u pacientov s vysokým a veľmi vysokým rizikom KV-príhody, SZ alebo CKD a s dôrazom odporúčaným výberom u pacientov s už prítomným ATS KVO, SZ alebo cerebrovaskulárnym ochorením (CVO) alebo CKD. Ak pacient má prejavy alebo znaky SZ, alebo má CKD, alebo ATS/nonATS kardiovaskulárne ochorenie s dominanciou rizika rozvoja srdcového zlyhávania, alebo má vysoké KV-riziko, je za preferovaný postup považovaná voľba SGLT2i s cieľom redukcie KV - a celkovej mortality, hSZ, ako aj rozvoja a progresie CKD (redukcia albuminúrie a progresie poklesu eGF). Ak pacient má ATS KVO s dominanciou rizika ATS KV-príhody, prekonal ATS KV-príhodu (IM, CMP, ochorenie periférnych artérií ), alebo má vysoké riziko ATS KV-príhody, alebo má CKD, potom je za preferovaný postup považovaná voľba GLP1-RA s cieľom redukcie rizika KV - a celkovej mortality, spomalenia progresie ATS a rizika ATS KV-príhod, ako aj rozvoja a progresie CKD (redukcia albuminúrie) [2,8,11,66]. Všeobecným argumentom preferencie GLP1-RA a SGLT2i do kombinácie s metformínom je v porovnaní s inými skupinami farmák aj výrazný efekt na HbA1c pri nízkom riziku hypoglykémie, redukcia telesnej hmotnosti a priaznivý efekt na viaceré KV-rizikové faktory (krvný tlak, krvné lipidy, chronický subklinický zápal). Iné skupiny farmák v porovnaní s GLP1-RA a SGLT2i neposkytujú žiadne zásadné výhody. Výhodou gliptínov, odporúčaných až na pozícii po SGLT2i a GLP1-RA, je nízke riziko hypoglykémie, hmotnostná neutralita, nízke riziko komplikácií a nežiaducich účinkov. Účinok na úpravu glykémie je však miernejší a nepreukázali ani morbiditno-mortalitný benefit. Ich najväčšou prednosťou je možnosť použitia v celom spektre klesajúcich funkcií obličiek vrátane pacientov s konečným štádiom chronického zlyhávania obličiek. Tieto vlastnosti sú výhodné najmä u starších pacientov [2,8,11,66].
Zaradenie SGLT2i alebo GLP1-RA do liečby u pacientov s KVO, resp. CKD alebo vysokým rizikom KVO sa odporúča nielen pri intenzifikácii glykemickej kontroly, ale aj nezávisle od nej, ako kardioprotektívna, resp. nefroprotektívna liečba, a to pridaním k predošlej liečbe alebo náhradou za iné antidiabetické farmaká. Rovnako pri intenzifikácii glykemickej kontroly farmakom z inej skupiny sa odporúča SGLT2i alebo GLP1-RA ponechať. Uvedené princípy sa objavili už v odporúčaniach SDS z roku 2016 a boli vôbec jednými z prvých, ktoré inkorporovali výsledky nedávnych CVOT štúdií do preferenčného výberu liečby u konkrétneho pacienta s cieľom znížiť konkrétne morbiditno-mortalitné riziko. V súčasnosti je takýto prístup už štandardnou súčasťou všetkých referenčných odporúčaní, ako sú aktuálne odporúčania EASD, ADA, AACE, ESC, CDA, CEEDEG a ďalších [2,8,11,66].
Sources
- Almutairi M, Al Batran R, Ussher JR. Glucagon-like peptide-1 receptor action in the vasculature. Peptides 2019; 111 : 26–32. Dostupné z DOI: <http://dx.doi.org/10.1016/j.peptides.2018.09.002>.
- [American Diabetes Association]. 9. Pharmacologic approaches to glycemic treatment: Standards of medical care in diabetes 2021. Diabetes Care 2021; 44(Suppl 1): S111-S124. Dostupné z DOI: <http://dx.doi.org/10.2337/dc21-S009>.
- Aragón-Herrera A, Feijóo-Bandín S, Otero Santiago M et al. Empagliflozin reduces the levels of CD36 and cardiotoxic lipids while improving autophagy in the hearts of Zucker diabetic fatty rats. Biochem Pharmacol 2019; 170 : 113677. Dostupné z DOI: <http://dx.doi.org/10.1016/j.bcp.2019.113677>.
- Aroor AR, Sowers JR, Jia G et al. Pleiotropic effects of the dipeptidylpeptidase-4 inhibitors on the cardiovascular system. Am J Physiol Heart Circ Physiol 2014; 307(4): H477–492. Dostupné z DOI: <http://dx.doi.org/10.1152/ajpheart.00209.2014>.
- Baggio LL, Drucker DJ. Biology of Incretins: GLP-1 and GIP. Gastroenterol 2007; 132(6): 2131–2157. Dostupné z DOI: Dostupné z DOI: <http://dx.doi.org/10.1053/j.gastro.2007.03.054>.
- Bosch A, Ott C, Jung S et al. How does empagliflozin improve arterial stiffness in patients with type 2 diabetes mellitus? Sub analysis of a clinical trial. Cardiovasc Diabetol 2019; 18(1): 44. Dostupné z DOI: <http://dx.doi.org/10.1186/s12933–019–0839–8>.
- Butler J, Packer M, Anker SD et al. Empagliflozin for the treatment of chronic heart failure and a reduced ejection fraction in patients with and without diabetes: new results of the EMPEROR-Reduced trial. J Am Coll Cardiol 2021; 77(11): 1381–1392. Dostupné z DOI: <https:// doi 10.1016/j.jacc.2021.01.033>.
- Cosentino F, Grant PJ, Aboyans V et al. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. Eur Heart J 2020;41(2): 255–323. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehz486>.
- Covie MR, Fisher M. SGLT2 inhibitors: mechanisms of cardiovascular benefit beyond glycaemic control. Nat Rev Cardiol 2020; 17(12): 761–772. Dostupné z DOI: <http://dx.doi.org/10.1038/s41569–020–0406–8>.
- Daacke I, Kandaswamy P, Tebboth A et al. Impact of Empagliflozin (Jardiance) to the NHS: estimation of budget and event impact based on empa-reg outcome data. Value Health 2016;19(7): PA668. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jval.2016.09.1852>.
- Davies MJ, D’Alessio DA, Fradkin J et al. Management of hyperglycaemia in type 2 diabetes, 2018. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetologia 2018; 2018(61): 2461–2498. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–018–4729–5>.
- Ferrannini E, Mark M, Mayoux E. CV Protection in the EMPA-REG OUTCOME Trial: A „Thrifty Substrate“ Hypothesis. Diabetes Care 2016; 39(7): 1108–1114. Dostupné z DOI: <http://dx.doi.org/10.2337/dc16–0330>.
- Fitchett D, Zinman B, Wanner C, Lachin JM, Hantel S, Salsali A, et al. Heart failure outcomes with empagliflozin in patients with type 2 diabetes at high cardiovascular risk: results of the EMPA-REG OUTCOME® trial. Eur Heart J 2016; 37(19): 1526–1534. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehv728>.
- Galwitz B, Rosenstock J, Rauch T et al. 2-year efficacy and safety of linagliptin compared with glimepiride in patients with type 2 diabetes inadequately controlled on metformin: a randomised, double-blind, non-inferiority trial. Lancet 2012; 380(9840): 475–483. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(12)60691–6>.
- Gerstein HC, Colhoun HM, Dagenais GR et al. Dulaglutide and cardiovascular outcomes in type 2 diabetes (REWIND): a double-blind, randomised placebo-controlled trial. Lancet 2019; 394(10193): 121–130. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(19)31149–3>.
- Gerstein HC, Colhoun HM, Dagenais GR et al. Dulaglutide and renal outcomes in type 2 diabetes: an exploratory analysis of the REWIND randomised, placebo-controlled trial. Lancet 2019; 394(10193): 131–138. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(19)31150-X>.
- Hallow KM, Helmlinger G, Greasley PJ et al. Why do SGLT2 inhibitors reduce heart failure hospitalization? A differential volume regulation hypothesis. Diabetes Obes Metab 2018; 20(3): 479–487. Dostupné z DOI: <http://dx.doi.org/10.1111/dom.13126>.
- Heerspink HJL, Karasik A, Thuresson M et al. Kidney outcomes associated with use of SGLT2 inhibitors in real-world clinical practice (CVD-REAL 3): a multinational observational cohort study. Lancet Diabetes Endocrinol 2020; 8(1): 27–35. Dostupné z DOI: <http://dx.doi.org/10.1016/S2213–8587(19)30384–5>.
- Heerspink HJL, Stefánsson BV, Correa-Rotter R et al. Dapagliflozin in patients with chronic kidney disease. N Engl J Med 2020; 383(15): 1436–1446. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa2024816>.
- Hernandez AF, Green JB, Janmohamed S et al. Albiglutide and cardiovascular outcomes in patients with type 2 diabetes and cardiovascular disease (Harmony Outcomes): a double-blind, randomised placebo-controlled trial. Lancet 2018; 392(10157): 1519–1529. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(18)32261-X>.
- Holman RR, Bethel MA, Mentz RJ et al. Effects of once-weekly exenatide on cardiovascular outcomes in type 2 diabetes. N Engl J Med 2017; 377(13): 1228–1239. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1612917>.
- Hramiak I, Vilsbøll T, Gumprecht J et al. Semaglutide treatment and renal function in the SUSTAIN 6 trial. Can J Diabetes 2018; 42(5 Suppl): S42. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jcjd.2018.08.126>.
- Husain M, Birkenfeld AL, Donsmark M, Dungan K, Eliaschewitz FG, Franco DR, et al. Oral semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med 2019; 381(9):841–851. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1901118>.
- Chiasson JL, Gomis R, Hanefeld M et al. The STOP-NIDDM Trial: an international study on the efficacy of an alpha-glucosidase inhibitor to prevent type 2 diabetes in a population with impaired glucose tolerance: rationale, design, and preliminary screening data. Study to Prevent Non-Insulin-Dependent Diabetes Mellitus. Diabetes Care 1998; 21(10): 1720–1725. Dostupné z DOI: <http://dx.doi.org/10.2337/diacare.21.10.1720>.
- Inzucchi SE, Zinman B, Wanner C et al. Empagliflozin Reduces the Total Burden of All-cause Hospitalizations. American Diabetes Association (ADA) 80th Scientific Sessions 2020, June 12–16. Virtual Meeting. 131-LB. Dostupné z WWW: <https://www.easd.org/virtualmeeting/home.html%20#!resources/43091>.
- Klein LJ, VisserFC. The effect of insulin on the heart. Net Heart J 2010; 18(4): 197–201. Dostupné z DOI: <http://dx.doi.org/10.1007/BF03091761>.
- Kosiborod M, Cavender MA, Fu AZ et al. Lower risk of heart failure and death in patients initiated on sodium-glucose cotransporter-2 inhibitors versus other glucose-lowering drugs: the CVD-REAL study (Comparative Effectiveness of Cardiovascular Outcomes in New Users of Sodium-Glucose Cotransporter-2 Inhibitors) Circulation 2017; 136(3): 249–259. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.117.029190>.
- Kosiborod M, Lam CSP, Kohsaka S et al. Cardiovascular events associated with SGLT-2 inhibitors versus other glucose-lowering drugs: the CVD-REAL 2 study. J Am Coll Cardiol 2018; 71(23): 2628–2639. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2018.03.009>.
- Koyani CN, Plastira I, Sourij H et al. Empagliflozin protects heart from inflammation and energy depletion via AMPK activation. Pharmacol Res 2020; 158 : 104870. Dostupné z DOI: <http://dx.doi.org/10.1016/j.phrs.2020.104870>.
- Lopaschuk GD, Verma S. Mechanisms of cardiovascular benefits of sodium glucose co-transporter 2 (SGLT2) inhibitors: A State-of-the-Art Review. JACC Basic Transl Sci 2020; 5(6): 632–644. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacbts.2020.02.004.
- Makdishi A, Ghanim H, Vora M et al. Sitagliptin exerts an antinflammatory action. J Clin Endocrinol Metab. 2012; 97(9): 3333–3341. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2012–1544>.
- Mann JFE, Ørsted DD, Brown-Frandsen K et al. Liraglutide and renal outcomes in type 2 diabetes. N Engl J Med 2017; 377(9): 839–848. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1616011>.
- Marso SP, Daniels GH, Brown-Frandsen K et al. Liraglutide and cardiovascular outcomes in type 2 diabetes. N Engl J Med 2016; 375(4): 311–322. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1603827>.
- Marso SP, Bain SC, Consoli A et al. Semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med 2016;375(19): 1834–1844. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1607141>.
- Matthews DR Dejager S Ahren B et al. Vildagliptin add-on to metformin produces similar efficacy and reduced hypoglycaemic risk compared with glimepiride, with no weight gain: results from a 2-year study. Diabetes Obes Metab 2010; 12(9): 780–789. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1463–1326.2010.01233.x>.
- Mazzone PJ, Rai H, Beukemann M, Xu M,Jain AK, Sasidhar M. The effect of metformin and thiazolidinedione use on lung cancer in diabetics. BMC Cancer 2012; 12 : 410. Dostupné z DOI: <http://dx.doi.org/10.1186/1471–2407–12–410>.
- McGuire DK, Zinman B, Inzucchi SE et al. Effects of empagliflozin on first and recurrent clinical events in patients with type 2 diabetes and atherosclerotic cardiovascular disease: a secondary analysis of the EMPA-REG OUTCOME trial. Lancet Diabetes Endocrinol 2020; 8(12): 949–959. Dostupné z DOI: <http://dx.doi.org/10.1016/S2213 - 8587(20)30344–2>.
- McMurray JJ, Solomon SD, Inzucchi SE et al. Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction. N Engl J Med 2019; 381(21): 1995–2008. Dostupné z DOI: <http://dx.doi.org/10.1056/ NEJMoa1911303>.
- McMurray JJV, Solomon SD, Inzucchi SE et al. Dapagliflozin in patients with heart failure and reduced ejection fraction. N Engl J Med 2019; 381(21): 1995–2008. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1911303>.
- Monami M, Genovese S, Mannucci E. Cardiovascular Safety Of Sulfonylureas: A Meta-Analysis Of Randomised Clinical Trials. Diabetes Obes Metab 2013; 15(10): 938–953. Dostupné z DOI: <http://doi: 10.1111/dom.12116>.
- Monteiro P, Bergenstal RM, Toural E et al. Efficacy and safety of empagliflozin in older patients in the EMPA-REG OUTCOME® trial. Age Ageing 2019; 48(6): 859–866. Dostupné z DOI: <http://dx.doi.org/10.1093/ageing/afz096>.
- Mosenzon O, Wiviott SD, Cahn A et al. Effects of dapagliflozin on development and progression of kidney disease in patients with type 2 diabetes: an analysis from the DECLARE-TIMI 58 randomised trial. Lancet Diabetes Endocrinol 2019; 7(8): 606–617. Dostupné z DOI: <http://dx.doi.org/10.1016/S2213–8587(19)30180–9>.
- Muskiet MH, Tonneijck L, Huang Y et al. Lixisenatide and renal outcomes in patients with type 2 diabetes and acute coronary syndrome: an exploratory analysis of the ELIXA randomised, placebo-controlled trial. Lancet Diabetes Endocrinol 2018; 6(11): 859–869. Dostupné z DOI: <https://doi.org/10.1016/S2213–8587(18)30268–7>.
- Najafzadeh M, Pawar A, Déruaz-Luyet A et al. PDB128 Reduced healthcare utilization in patients using empagliflozin: an interim analysis from the empagliflozin comparative effectiveness and safety (EMPRISE) study. Value Health 2019; 22(Suppl 2): S161. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jval.2019.04.675>.
- Nagahisa T, Saisho Y. Cardiorenal protection: potential of SGLT2 inhibitors and GLP-1 receptor agonists in the treatment of type 2 diabetes. Diabetes Ther 2019; 10(5): 1733–1752. Dostupné z DOI: <http://dx.doi.org/10.1007/s13300–019–00680–5>.
- Nauck MA, Ouaghlidi AE. The therapeutic actions of DPP-IV inhibition are not mediated by glucagon-like peptide-1 Diabetologia. 2005; 48(4): 608–611. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–005–1704–8>.
- Packer M, Anker SD, Butler J et al. Cardiovascular and renal outcomes with empagliflozin in heart failure. N Engl J Med 2020; 383(15): 1413–1424. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa2022190>.
- Paolisso G, Monami M, Marfella R et al. Dipeptidyl Peptidase-4 Inhibitors in the Elderly: More Benefits or Risks? Adv Ther 2012; 29(3): 218–233. Dostupné z DOI: <http://dx.doi.org/10.1007/s12325–012–0008-x>.
- Patorno E, Pawar A, Bessette LG et al. Cardiovascular outcomes in older adults initiating Empagliflozin vs DPP-4 inhibitors and GLP-1 receptor agonists: a subgroup analysis from the EMPRISE study. American Diabetes Association (ADA) 80th Scientific Sessions 2020, June 12–16. Virtual Meeting. 133-LB. Dostupné z WWW: <https://plan.core-apps.com/tristar_ada20/abstract/ff32b460–6aeb-47be-87a4–99cd64ce1381>.
- Patorno E, Pawar A, Lily G et al. Effectiveness and safety of empagliflozin in routine care patients: interim results from the EMPagliflozin compaRative effectIveness and SafEty (EMPRISE) study. American Diabetes Association (ADA) 80th Scientific Sessions 2020, June 12–16. Virtual Meeting. 134-LB. Dostupné z DOI: <https://doi.org/10.2337/db20–134-LB>.
- Patorno E, Pawar A, Franklin JM et al. Empagliflozin and the Risk of Heart Failure Hospitalization in Routine Clinical Care A First Analysis From the EMPRISE Study. Circulation 2019; 139(25): 2822–2830. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.118.039177>.
- Pasternak B, Ueda P, Eliasson B et al. Use of sodium glucose cotransporter 2 inhibitors and risk of major cardiovascular events and heart failure: Scandinavian register based cohort study. BMJ 2019; 366: l4772. Dostupné z DOI: <http://dx.doi.org/10.1136/bmj.l4772>.
- Pasternak B, Wintzell V, Melbye M et al. Use of sodium-glucose co-transporter 2 inhibitors and risk of serious renal events: Scandinavian cohort study. BMJ. 2020; 369: m1186. Dostupné z DOI: <http://dx.doi.org/10.1136/bmj.m1186>.
- Pawar A, Patorno E, Deruaz-Luyet A et al. Health-care costs and medication burden in routine care initiators of empagliflozin: a first analysis from the Empagliflozin Comparative Effectiveness and Safety (EMPRISE) study. Diabetes 2019; 68(Suppl 1): 1193-P. Dostupné z DOI: <http://dx.doi.org/10.2337/db19–1193-P>.
- Pawar A, Patorno E, Deruaz-Luyet A et al. Reduced healthcare utilization in routine care initiators of empagliflozin with and without heart failure: interim analysis from the EMPagliflozin compaRative effectIveness and SafEty (EMPRISE) study. Eur Heart J 2019; 40(Suppl 1): ehz746.0181. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehz746.0181>.
- Pawar A, Patorno E, Déruaz-Luyet A et al. Comparative healthcare costs and medication burden in real-world patients augmenting metformin monotherapy with empagliflozin from the empagliflozin comparative effectiveness and safety (EMPRISE) study. Value Health 2019; 22(Supp 2): S161. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jval.2019.04.673>.
- Perkovic V, Jardine MJ, Neal B et al. Canagliflozin and renal outcomes in type 2 diabetes and nephropathy. N Engl J Med 2019; 380(24): 2295–2306. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1811744>.
- Perkovic V, de Zeeuw D, Mahaffey KW et al. Canagliflozin and renal outcomes in type 2 diabetes: results from the CANVAS Program randomised clinical trials. Lancet Diabetes Endocrinol 2018; 6(9): 691–704. <http://dx.doi.org/10.1016/S2213–8587(18)30141–4>.
- Pfeffer MA, Claggett B, Diaz R et al. [ELIXA Investigators]. Lixisenatide in Patients with Type 2 Diabetes and Acute Coronary Syndrome. N Engl J Med 2015; 373(23): 2247–2257. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1509225>.
- Rosenstock J, Perkovic V, Johansen OE et al. Effect of Linagliptin vs Placebo on Major Cardiovascular Events in Adults With Type 2 Diabetes and High Cardiovascular and Renal Risk The CARMELINA Randomized Clinical Trial. JAMA 2019; 321(1): 69–79. Dostupné z DOI: <http://dx.doi.org/10.1001/jama.2018.18269>.
- Scirica BM, Bhatt DL, Braunwald E et al. Saxagliptin and Cardiovascular Outcomes in Patients with Type 2 Diabetes Mellitus. N Engl J Med 2013; 369(14): 1317–26. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1307684>.
- Seck T, Nauck M, Sheng D et al. Safety and efficacy of treatment with sitagliptin or glipizide in patients with type 2 diabetes inadequately controlled on metformin: a 2-year study. Int J Clin Pract 2010; 64(5): 562–576. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1742–1241.2010.02353.x>.
- Seferović PM, Fragasso G, Petrie M et al. Sodium glucose co-transporter-2 inhibitors in heart failure: beyond glycaemic control. The Position Paper of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail 2020; 22(9): 1495–1503. <http://dx.doi.org/10.1002/ejhf.1954>.
- Shehadeh N, Raz I, Nakhleh A. Cardiovascular benefit in the limelight: shifting type 2 diabetes treatment paradigm towards early combination therapy in patients with overt cardiovascular disease. Cardiovasc Diabetol 2018; 17(1): 117. Dostupné z DOI: <http://dx.doi.org/10.1186/s12933–018–0760–6>.
- Scheen AJ. SGLT2 inhibitors: benefit/risk balance. Curr Diab Rep 2016; 16(10): 92. Dostupné z DOI: <http://dx.doi.org/10.1007/s11892–016–0789–4>.
- Schernthaner G, Lehmann R, Prázný M et al. Translating recent results from the Cardiovascular Outcomes Trials into clinical practice: recommendations from the Central and Eastern European Diabetes Expert Group (CEEDEG). Cardiovasc Diabetol 2017; 16(1): 137. Dostupné z DOI: <http://dx.doi.org/10.1186/s12933–017–0622–7>.
- Simpson SH, Lee J, Choi S et al. Mortality risk among sulfonylureas: a systematic review and network meta-analysis. Lancet Diabetes Endocrinol 2015; 3(1): 43–51. Dostupné z DOI: <http://dx.doi.org/10.1016/S2213–8587(14)70213-X>.
- Thomas MC, Cherney DZ. The actions of SGLT2 inhibitors on metabolism, renal function and blood pressure. Diabetologia 2018; 61(10): 2098–2107. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–018–4669–0>.
- Tkac I, Raz I. Combined Analysis of Three Large Interventional Trials With Gliptins Indicates Increased Incidence of Acute Pancreatitis in Patients With Type 2 Diabetes. Diabetes Care 2017; 40(2): 284–286. Dostupné z DOI: <http://dx.doi.org/10.2337/dc15–1707>.
- Tsalamandris S, Antonopoulos AS, Oikonomou E et al. The Role of Inflammation in Diabetes: Current Concepts and Future Perspectives. Eur Cardiol 2019; 14(1): 50–59. Dostupné z DOI: <http://dx.doi.org/10.15420/ecr.2018.33.1>.
- Uthman L, Baartscheer A, Bleijlevens B et al. Class effects of SGLT2 inhibitors in mouse cardiomyocytes and hearts: inhibition of Na+/H+ exchanger, lowering of cytosolic Na+ and vasodilation. Diabetologia 2018; 61(3): 722–726. Dostupné z DOI: <http://dx.doi.org/10.1007/s00125–017–4509–7>.
- Vallon V. The mechanisms and therapeutic potential of SGLT2 inhibitors in diabetes mellitus. Annu Rev Med 2015; 66 : 255–270. Dostupné z DOI: <http://dx.doi.org/10.1146/annurev-med-051013–110046>.
- Verma S, Leiter LA, Sharma A et al. How early after treatment initiation are the CV benefits of empagliflozin apparent? A post hoc analysis of EMPA-REG OUTCOME. Diabetes 2020; 69(Suppl 1): 28-OR. Dostupné z DOI: < https://doi.org/10.2337/db20–28-OR>.
- Wanner C, Inzucchi SE, Lachin JM et al. Empagliflozin and progression of kidney disease in type 2 diabetes. N Engl J Med 2016; 375(4): 323–334. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1515920>.
- Wiviott SD, Raz I, Bonaca MP et al. Dapagliflozin and cardiovascular outcomes in type 2 diabetes. N Engl J Med 2019; 380(4): 347–357. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1812389>.
- Yin WL, Bain SC, Min T. The effect of glucagon-like peptide-1 receptor agonists on renal outcomes in type 2 diabetes. Diabetes Ther 2020; 11(4): 835–844. Dostupné z DOI: <http://dx.doi.org/10.1007/s13300–020–00798-x>.
- Zinman B, Wanner C, Lachin JM et al. Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med 2015; 373(22): 2117–2128. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1504720>.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Forum Diabetologicum

-
All articles in this issue
- Súčasné možnosti prevencie aterosklerózy pri diabete
- Antidiabetická liečba v prevencii aterosklerózy: posledné desaťročie
- Hypolipidemická liečba v prevencii aterosklerózy u diabetikov
- Antihypertenzívna liečba v prevencii aterosklerózy u diabetikov
- Antiagregačná liečba v prevencii aterosklerózy u diabetikov
- Efekt antidiabetickej liečby na incidenciu cievnych mozgových príhod u pacientov s diabetom 2. typu
- Limitácie a možná prídavná hodnota štúdií z reálnej klinickej praxe v porovnaní s randomizovanými klinickými štúdiami
- Fakty na zapamätanie: Čo je založené na dôkazoch v prevencii aterosklerózy pri diabete 2. typu?
- Antidiabetická liečba v prevencii aterosklerózy: prvé polstoročie
- Forum Diabetologicum
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Hypolipidemická liečba v prevencii aterosklerózy u diabetikov
- Limitácie a možná prídavná hodnota štúdií z reálnej klinickej praxe v porovnaní s randomizovanými klinickými štúdiami
- Antiagregačná liečba v prevencii aterosklerózy u diabetikov
- Antidiabetická liečba v prevencii aterosklerózy: posledné desaťročie
