Hypoglykemie u diabetes mellitus 2. typu – stručný přehled pro klinickou praxi
Hypoglycaemia in type 2 diabetes mellitus – a brief overview for clinical practice
Hypoglycaemia is a consistent risk of the type 2 diabetes (T2DM) therapy, especially insulin or some older oral hypoglycaemic agents as the insulin secretagogues. It is also associated with various range of health disorders, increased cardiovascular risk or death. Hypoglycaemia can present with diverse symptoms or can be asymptomatic. Almost 10% of patients with T2DM suffer from hypoglycaemia unawareness. The risk of hypoglycaemia is associated with a level of glycaemic control and increases also with age, comorbidities and strength of diabetes therapy. Warning value, in which patients with diabetes should considered initiation of appropriate therapeutic steps, is the level of glycaemia 3.9 mmol/l.
Keywords:
impaired hypoglycaemia awarness
Authors:
J. Brož 1
; J. Urbanová 2
Authors‘ workplace:
Univerzita Karlova v Praze
; 2. lékařská fakulta Interní klinika 2. LF UK a FN Motol Přednosta: prof. MUDr. Milan Kvapil, CSc., MBA
1; 3. lékařská fakulta Centrum pro výzkum diabetu, metabolismu a výživy II. interní klinika 3. LF UK a FNKV Přednosta: prof. MUDr. Michal Kršek, CSc.
2
Published in:
Prakt. Lék. 2019; 99(2): 52-56
Category:
Reviews
Overview
Hypoglykemie je trvalým rizikem léčby diabetes mellitus 2. typu (DM2), především u pacientů léčených inzulinem či některými staršími perorálními antidiabetiky skupiny inzulinových sekretagog, a je asociována s celou řadou zdravotních komplikací, vyšším kardiovaskulárním rizikem i úmrtím. Hypoglykemie může probíhat pod obrazem různých příznaků i zcela asymptomaticky. Poruchu rozpoznávání hypoglykemií trápí odhadem až desetinu všech pacientů s DM2. Riziko hypoglykemie se zvyšuje v souvislosti se stupněm dosažené glykemické kompenzace, věkem, komorbiditami či intenzitou léčby. Varovnou hodnotu nebezpečného poklesu koncentrace krevní glukózy, při které by měly být zahájeny příslušné léčebné kroky, představuje u diabetiků glykemie 3,9 mmol/l.
Klíčová slova:
syndrom porušeného vnímání hypoglykemie
ÚVOD
Hypoglykemie je definována jako stav charakterizovaný abnormálně nízkou hladinou glykemie, který staví organismus do potenciálního nebezpečí. U pacientů s diabetes mellitus je za takovou hladinu považována glykemie, jež by měla upozornit na počínající hypoglykemii nebo její vyšší riziko a zároveň vést k preventivním krokům bránící jejímu dalšímu poklesu, považována hodnota ≤ 3,9 mmol/l. Za klinicky signifikantní hypoglykemii (přinášející riziko poruchy vědomí plynoucí z reálného nedostatku glukózy jako zdroje energie pro mozek) je považována hodnota ≤ 3,0 mmol/l (1). Z hlediska tíže hypoglykemie označujeme ty, které pacient vyřeší sám, za mírné, naopak za hypoglykemie těžké ty, kdy je nutná pomoc další osoby, neboť pacient si hypoglykemii neuvědomuje nebo si není schopen sám pomoci (nemusí nutně být v bezvědomí).
Hypoglykemie jsou spojené především s léčbou inzulinem, deriváty sulfonylurey a glinidy. Ostatní antidiabetické léky samy o sobě (či v kombinaci mezi sebou) podle současných poznatků hypoglykemii pravděpodobně nezpůsobují. Jsou-li však podány v kombinaci s některým preparátem z prvních tří uvedených skupin, mohou její riziko zvyšovat (2).
ETIOPATOGENEZE HYPOGLYKEMIE
Vzhledem k tomu, že glukóza je pro mozek základním zdrojem energie, musí lidský organismus mít a také má akceschopné mechanismy, s jejichž pomocí udrží její koncentraci v krvi v dostatečném množství i za různých nepříznivých okolností. U zdravého jedince se na tomto mechanismu podílí možnost rychlého snížení sekrece inzulinu a navýšení sekrece tzv. kontraregulačních hormonů – tedy glukagonu, katecholaminů, kortizolu a růstového hormonu. Konečným výsledkem působení těchto hormonů je zvýšený přísun glukózy z jater do krve a naopak její snížená utilizace periferními tkáněmi. Tento mechanismus je zodpovědný za to, že u zdravého člověka, s výjimkou extrémních okolností, k hypoglykemii nedojde (3).
U pacienta s diabetes mellitus je však tento systém narušen úplnou absencí či sníženou schopností omezit sekreci inzulinu. Inzulin je mu přímo dodáván zevně nebo je stimulován užívanými léky, takže organismus ztrácí nad hladinou inzulinu kontrolu a jeho koncentraci v případě nutnosti nedokáže snížit. Navíc, především u diabetes mellitus 1. typu (DM1) či sekundárního diabetu způsobeného one-mocněními pankreatu (zejména trvají-li delší dobu), situaci zhoršuje i snížená schopnost navýšit produkci glukagonu.
V momentě, kdy dojde k dysbalanci mezi aktivitou hypoglykemizujících látek a příjmem sacharidů, často ovlivněnou i fyzickou aktivitou, jsou uvedené kontraregulační procesy nedostatečně efektivní a koncentrace glukózy poklesne pod dolní hranici normy.
SYMPTOMY HYPOGLYKEMIE
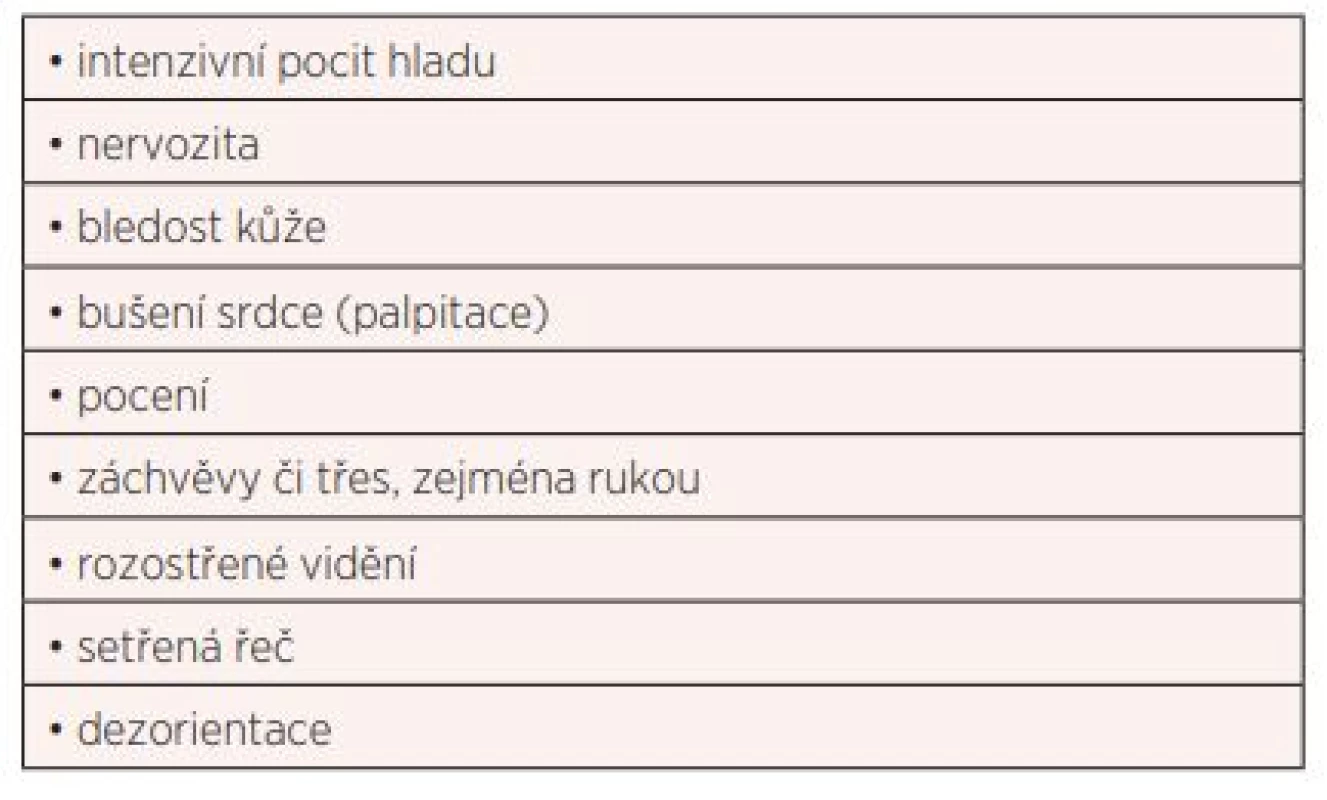
Příznaky, kterými se hypoglykemie projevuje, dělíme na neurogenní a neuroglykopenické. Neurogenní příznaky, způsobené účinkem kontraregulačních hormonů, dále dělíme na adrenergní (třes, palpitace) a cholinergní (pocení, parestezie a pocit hladu). Neuroglykopenické příznaky jsou způsobeny nedostatkem glukózy pro nervový systém (změny chování, zmatenost, slabost, kóma, smrt). Uvedené symptomy (tab. 1) se mohou během hypoglykemie i u stejných jedinců objevovat v různém pořadí a být různě vyjádřené, hypoglykemie však může proběhnout i zcela bez příznaků (4).
SYNDROM PORUŠENÉHO ROZPOZNÁVÁNÍ HYPOGLYKEMIE A JEHO DŮSLEDKY
Pokud se příznaky hypoglykemie neobjeví či jsou méně vyjádřené, takže je pacient může přehlédnout, pak mluvíme o syndromu porušeného rozpoznávání hypoglykemií (SPRH) (5, 6). SPRH postihuje cca 10 % pacientů s diabetes mellitus 2. typu (DM2) léčených inzulinem (11), více pak ty se sníženou sekrecí inzulinu (6), v případě pacientů s DM1 je to přibližně 30 % (7). Častěji je přítomen u pacientů s delší dobou trvání diabetu, anamnézou opakovaných hypoglykemií, intenzivní medikamentózní antidiabetickou léčbou, lepší glykemickou kompenzací a vyšším věkem (8). Přítomnost SPRH zvyšuje riziko významnějšího poklesu koncentrace glukózy v krvi provázenou neuroglykopenií, tedy rozvoj těžké hypoglykemie, a to 6krát u pacientů s DM1 (7) a dokonce 17krát u pacientů s DM2 (9), což lze vzhledem k morbiditě a mortalitě, kterou těžké hypoglykemie významně navyšují (viz dále), považovat za jeho nejzávažnější důsledek. Přítomnost SPRH lze jednoduše zjisti tzv. Goldovým skórem, kdy pacienta požádáme, aby na stupnici od 1 do 7 vybral číslo, které nejlépe odpovídá tomu, jak rozpoznává hypoglykemie
(1 = poznám vždy, 7 = nepoznám nikdy). Skóre od 4 výše již znamená přítomnost určitého stupně SPRH (10).
Základním prvkem v léčbě SPRH je vyhnout se hypoglykemii. Pokud se glykemie stabilizují (přechodně i ve vyšším pásmu) a k hypoglykemiím nedochází, lze u většiny pacientů předpokládat v průběhu několika týdnů zlep-
šení. Důležitá je revize pacientových znalostí o hypoglykemiích a terapeutických návyků a také strukturovaná edukace.
NÁSLEDKY HYPOGLYKEMIÍ (NEBEZPEČÍ ASOCIOVANÉ S HYPOGLYKEMIÍ)
U pacientů s diabetes mellitus je hypoglykemie jedním z důležitých faktorů ovlivňujících metabolickou kontrolu onemocnění. Vyvolává v pacientech nepříjemné pocity, zvyšuje riziko zranění (např. vlivem pádu v souvislosti s poruchou vědomí) a kardiovaskulární riziko, může způsobit i trvalé poškození mozku či smrt (např. vlivem arytmie, cévní mozkové příhody) (11–14). U pacientů s DM2 hypoglykemie zhoršují kvalitu života úměrně
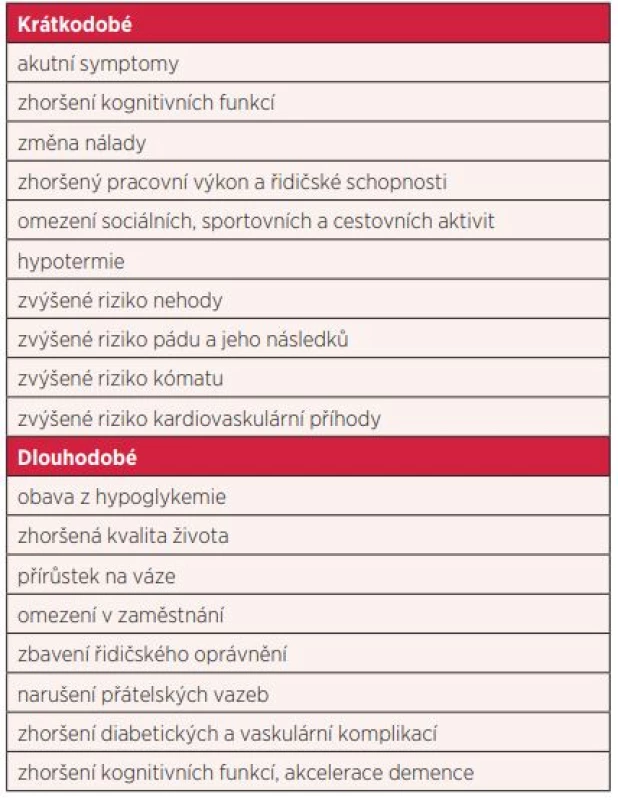
jejich frekvenci a tíži, a mohou proto vést k menší adherenci k léčbě ve snaze se hypoglykemii vyhnout (15, 16). Souhrn možných následků hypoglykemie je shrnut v tabulce 2.
Hypoglykemie a kardiovaskulární riziko
Zhruba před dekádou přinesly tři velké studie – ACCORD (17), ADVANCE (18) a VADT (19) – významné poznatky týkající se účinku těžkých hypoglykemií na organismus. Všechny prokázaly, že ve skupině pacientů s intenzivní léčbou (cílovým HbA1c 42 mmol/mol v ADVANCE a VADT a 48 mmol/mol v ACCORD) došlo k více než dvojnásobnému zvýšení frekvence těžkých hypoglykemií (v porovnání se skupinou pacientů s méně intenzivní léčbou – HbA1c 53–63 mmol/mol) (17–19), které byli navíc prokazatelně spojeny s vyšší kardiovaskulární i celkovou mortalitou, a to bez ohledu na terapeutickou větev, kam byli pacienti zařazeni. Hypoglykemie však nebyly bezprostřední příčinou úmrtí (20, 21).
Četnost hypoglykemií v souvislosti s typem léčby diabetu
Pro určitou, nicméně pouze rámcovou, představu o tom, jaká je frekvence hypoglykemií u pacientů s DM2, uvádíme výsledky několika studií, zaměřených na intenzivní léčbu diabetu.
Jednou z prvních byla studie UKPDS (probíhající v letech 1977–1991), do které byli zařazeni nově diagnostikovaní pacienti s DM2 (bez známek mikrovaskulárních nebo makrovaskulárních komplikací). Polovina z nich byla randomizována do větve s intenzivní léčbou, tj. k nasazení metforminu, derivátu sulfonylurey nebo inzulinu, s cílem dosáhnout glykemie nalačno < 6 mmol/l, druhá polovina pak do větve konvenční léčby, tj. k dodržování diety (v této větvi dále zůstali pouze ti jedinci, jejichž glykemie nalačno se pohybovala do 15 mmol/l a zároveň byli asymptomatičtí) (22, 23). Těžké hypoglykemie se objevily ve skupině léčené dietou v průměru 0,1 na SPR (SPR = sto pacient-roků), ve skupině léčené derivátem sulfonylurey u 0,4–0,6 na SPR a 2,3 na SPR ve skupině léčené inzulinem (23). Alespoň jednu mírnou hypoglykemii hlásilo 0,8/100 pacientů ve skupině s dietou, 1,7/100 ve skupině s metforminem, 7,9/100 pacientů ve skupině se sulfonylureou, 21,2/100 pacientů léčených bazálním inzulinem a 32,6/100 pacientů léčených intenzifikovaným inzulinovým režimem.
Pozdější, tři výše zmíněné studie ADVANCE, VADT a ACCORD, prokázaly frekvenci těžkých hypoglykemií (při srovnání větve s intenzivní léčbou se standardní) 0,7 vs. 0,4 na SPR (ve studii ADVANCE, kde těžké hypoglykemie byly definovány hodnotou < 2,8 mmol/l) (18), 12,0 vs. 4,0 na SPR (ve VADT, definovány jako zhoršení či úplná ztráta vědomí) (19) a 3,1 vs. 1,0 na SPR (v ACCORD, definovány jako nutnost zdravotnického zásahu) (17). Mírných hypoglykemií bylo zachyceno ve studii ADVANCE 120 vs. 90 na SPR (18). Ve VADT činila četnost všech hypoglykemií 1566 vs. 432 na SPR (19).
Riziko hypoglykemie v některých lékových skupinách
Z hlediska hypoglykemií je nejrizikovějším antidiabetickým lékem inzulin, následují deriváty sulfonylurey a glinidy. Riziko těžké hypoglykemie se navíc výrazně navyšuje při léčbě více typy antidiabetik současně (24, 25). Srovnání hypoglykemizujících léků v observačních studiích ukázalo, že riziko těžké hypoglykemie v porovnání s ostatními typy léčby bylo u pacientů léčených deriváty sulfonylurey 2–3krát vyšší a inzulinem 3–4krát vyšší (26–28). Randomizované studie ukázaly, že toto riziko u léčby sulfonylureou bylo 2,5krát vyšší a u inzulinu 4,5krát vyšší (studie ORIGIN) (29). Nicméně toto riziko je variabilní a může se lišit u jednotlivých konkrétních typů inzulinů. Např. bazální inzuliny glargine (U100) a detemir mají ve srovnání s NPH inzulinem nižší riziko hypoglykemií při stejném vlivu na hodnotu HbA1c (30–32). Podle výsledků aktuálních studií jsou dále inzulinová analoga druhé generace – glargine U300 a degludec – ve srovnání s inzulinem glargine U100 spojovány s nižším rizikem hypoglykemií nočních i těžkých, navíc v případě glargine U300 též hypoglykemií po celý den (definovanými hodnotami pod < 3,1 mmol/l ve studiích s inzulinem degludec, a < 3,0 mmol/l s inzulinem glargine U300). U glargine U 300 je pak tento benefit zvláště zřetelný v období titrace optimální dávky (33–37).
Dat o léčbě glinidy není mnoho, výsledky jsou většinou analyzovány v jedné skupině s deriváty sulfonylurey. Stran spojitosti s výskytem těžkých hypoglykemií je jim v porovnání s deriváty sulfonylurey přisuzováno přibližně poloviční riziko (26).
RIZIKOVÉ FAKTORY HYPOGLYKEMIE
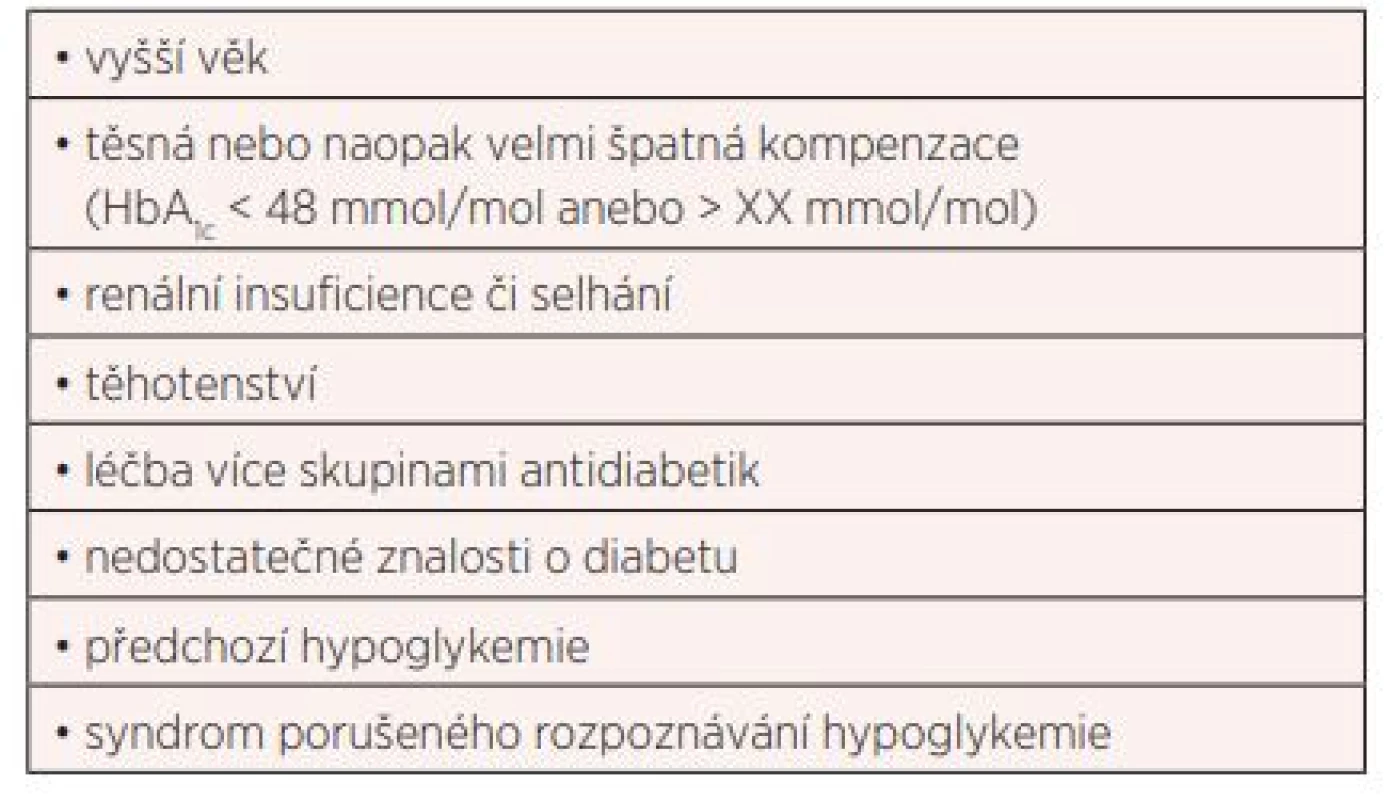
Nejdůležitější rizikové faktory hypoglykemií jsou uvedeny v tabulce 3. Velmi často je zmiňovaný vztah k úrovni kompenzace diabetu, zejména k těsné glykemické kontrole. Křivka rizika hypoglykemie má však ve vztahu k hodnotám HbA1c tvar písmene „U“, tedy stoupá jak směrem k nižším hodnotám, tak i k hodnotám vyšším. U pacientů s vyšším HbA1c (zejména > 9 %, > 75 mmol/mol) toto riziko stoupá zřejmě vlivem vyšší míry nedisciplinovanosti, kterou hodnota HbA1c pravděpodobně symbolizuje (38, 39).
Riziko těžké hypoglykemie se výrazně navyšuje u pacientů starších 75 let (39). Svou roli hraje především častá přítomnost polypragmazie, renální insuficience a kognitivního deficitu. Diabetes mellitus je u některých pacientů spojen se zrychleným úbytkem kognitivních funkcí a těžké hypoglykemie jsou jedním z faktorů, které k tomu přispívají. I z těchto důvodů je u starších pacientů s diabetem důležité riziko hypoglykemií minimalizovat správným výběrem léků a pragmatickým nastavením individuálních cílů kompenzace (40, 41).
Mezi další rizika, která jsou spojena s vyšší frekvencí výskytu hypoglykemie, patří užívání některých léčiv (z běžnějších např. indomethacinu), gastroparéza, malabsorpce, přítomnost diabetických komplikací, celiakie, onemocnění exokrinní části pankreatu, adrenální insuficience, hypopituitarismus, excesivní požívání alkoholu, odmítání nemoci, strach z hyperglykemie i hypoglykemie, deprese a jiná psychiatrická onemocnění či kognitivní dysfunkce (42, 43).
PREVENCE A LÉČBA
Z hlediska ovlivnění frekvence hypoglykemií je klíčová především jejich prevence, jež je vymezena podrobnou edukací pacienta a výběrem vhodného antidiabetika, resp. mírou jeho rizika vyvolat hypoglykemii. Dotaz na přítomnost hypoglykemií by měl padnout při každé návštěvě pacienta v ordinaci a její příčina a způsob léčby by měl být vždy podrobně rozebrán (43).
Každý pacient musí být poučen o tom, že pokud dojde k hypoglykemii (tedy objeví-li se příznaky, poklesne-li glykemie < 3,9 mmol/l, či obojí), je třeba okamžitě navrátit hladinu krevní glukózy zpět nad hodnotu 3,9 mmol/l a zároveň se při tom vyvarovat přílišné hyperglykemii. Za základní terapeutický krok je považováno tzv. pravidlo 15 – požití 15–20 g glukózy a přeměření glykemie glukometrem za 15 minut. Celý postup se opakuje, dokud glykemie nestoupne nad požadovanou hranici 3,9 mmol/l (44). Podrobnému popisu léčby je věnován samostatný článek.
ZÁVĚR
Hypoglykemie zůstává neodmyslitelnou součástí léčby diabetu, především inzulinoterapie, ale též některých antidiabetik, a to navzdory faktu, že řada nových léčiv, včetně nových typů inzulinů, je spojena s menším či dokonce minimálním rizikem hypoglykemie. Jelikož je hypoglykemie asociována s celou řadou zdravotních rizik, včetně smrti, je třeba se jí snažit maximálně předcházet, a to zejména správným výběrem antidiabetické terapie, opakovanou edukací a aktivním dotazováním všech pacientů (v případě nutnosti i rodinných příslušníků) na přítomnost hypoglykemií i jejich rozpoznávání (s ohledem na možný SPRH). Speciální pozornost je třeba věnovat diabetikům s rizikovými faktory pro vznik hypoglykemie (především těch starších 75 let, léčených kombinací antidiabetických léků, s renální insuficiencí apod.).
Konflikt zájmů: žádný.
ADRESA PRO KORESPONDENCI:
MUDr. Jan Brož
Interní klinika 2. LF UK a FN Motol
V Úvalu 84, 150 00 Praha 5
e-mail: zorb@seznam.cz
Sources
1. International Hypoglycaemia Study Group. Glucose concentrations of less than 3.0 mmol/L (54 mg/dL) should be reported in clinical trials: a joint position statement of the American Diabetes Association and the European Association for the Study of Diabetes. Diabetes Care 2017; 40(1): 155–157.
2. International Hypoglycemia Study Group: Minimizing hypoglycemia in diabetes. Diabetes Care 2015; 38 : 1583–1591.
3. Rizza RA, Cryer PE, Gerich JE. Role of glucagon, catecholamines, and growth hormone in human glucose counterregulation. Effects of somatostatin and combined alpha - and beta-adrenergic blockade on plasma glucose recovery and glucose flux rates after insulin-induced hypoglycemia. J Clin Invest 1979; 64 : 62–71.
4. McAulay V, Deary IJ, Frier BM. Symptoms of hypoglycaemia in people with diabetes. Diabet Med 2001; 18 : 690–705.
5. de Galan BE, Schouwenberg BJ, Tack CJ, et al. Pathophysiology and management of recurrent hypoglycaemia and hypoglycaemia unawareness in diabetes. Neth J Med 2006; 64 : 269–279.
6. Moghissi E, Ismail-Beigi F, Devine RC. Hypoglycemia: minimizing its impact in type 2 diabetes. Endocr Pract 2013; 19 : 526–535.
7. Gerstein HC, Miller ME, Byington RP, et al. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med 2008; 358 : 2545–2559.
8. Cryer PE. The barrier of hypoglycemia in diabetes. Diabetes 2008; 57 : 3169–3176.
9. Martín-Timón I, del Cañizo-Gómez FJ. Mechanisms of hypoglycemia unawareness and implications in diabetic patients. World J Diabetes 2015; 6 : 912–926.
10. Gold AE, MacLeod KM, Frier BM. Frequency of severe hypoglycemia in patients with type 1 diabetes and impaired awareness of hypoglycemia. Diabetes Care 1994; 17 : 697–703.
11. McCoy RG, Van Houten HK. Increased mortality of patients with diabetes reporting severe hypoglycemia. Diabetes Care 2012; 35 : 1897–1900.
12. Hemmingsen B, Lund SS, Gluud C, et al. Intensive glycaemic control for patients with type 2 diabetes: systematic review with meta-analysis and trial sequential analysis of randomised clinical trials. BMJ 2011; 343: d6898.
13. Bolek T, Samoš M, Mokáň M, a kol. Akútne príčiny náhlych úmrtí u pacientov so závažnou hypoglykemiou. Vnitř. Lek. 2016; 62 : 462–466.
14. Lee AK, Warren B, Lee CJ, et al. Association of severe hypoglycemia with cardiovascular disease and all-cause mortality in older adults with diabetes: the atherosclerosis risk in communities (ARIC) study. Circulation 2017; 135: A4.
15. Marrett E, Radican L, Davies MJ, Zhang Q. Assessment of severity and frequency of self-reported hypoglycemia on quality of life in patients with type 2 diabetes treated with oral antihyperglycemic agents: a survey study. BMC Res Notes 2011; 4(1): 251.
16. McCoy R, Van Houten H, Ziegenfuss J, et al. Self-report of hypoglycemia and health-related quality of life in patients with type 1 and type 2 diabetes. Endocr Pract 2013; 19(5): 792–799.
17. Action to Control Cardiovascular Risk in Diabetes Study G, Gerstein HC, Miller ME, Byington RP, et al. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med 2008; 358(24): 2545–2559.
18. Aroup AC, Patel A, MacMahon S, et al. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N Engl J Med 2008; 358(24): 2560–2572.
19. Duckworth W, Abraira C, Moritz T, et al. Glucose control and vascular complications in veterans with type 2 diabetes. N Engl J Med 2009; 360(2): 129–139.
20. Zoungas S, Patel A, Chalmers J, et al. Severe hypoglycemia and risks of vascular events and death. N Engl J Med 2010; 363(15): 1410–1418.
21. Bonds DE, Miller ME, Bergenstal RM, et al. The association between symptomatic, severe hypoglycaemia and mortality in type 2 diabetes: retrospective epidemiological analysis of the ACCORD study. BMJ 2010; 340: b4909.
22. UK Prospective Diabetes Study (UKPDS) group. Intensive blood glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet 1998; 352 : 837–843.
23. Wright AD, Cull CA, Macleod KM, et al. Hypoglycemia in type 2 diabetic patients randomized to and maintained on monotherapy with diet, sulfonylurea, metformin, or insulin for 6 years from diagnosis: UKPDS73. J Diabetes Complicat 2006; 20(6): 395–401.
24. Misra-Hebert AD, Pantalone KM, Ji X, et al. Patient characteristics associated with severe hypoglycemia in a type 2 diabetes cohort in a large, integrated health care system from 2006 to 2015. Diabetes Care 2018; 41(6): 1164–1171.
25. Davis TM, Brown SG, Jacobs IG, et al. Determinants of severe hypoglycemia complicating type 2 diabetes: the Fremantle Diabetes Study. J Clin Endocrinol Metab 2010; 95(5): 2240–2247.
26. Quilliam BJ, Simeone JC, Ozbay AB. Risk factors for hypoglycemia-related hospitalization in patients with type 2 diabetes: a nested case-control study. Clin Ther 2011; 33(11): 1781–1791.
27. Misra-Hebert AD, Pantalone KM, Ji X, et al. Patient characteristics associated with severe hypoglycemia in a type 2 diabetes cohort in a large, integrated health care system from 2006 to 2015. Diabetes Care 2018; 41(6): 1164–1171.
28. Davis TM, Brown SG, Jacobs IG, et al. Determinants of severe hypoglycemia complicating type 2 diabetes: the Fremantle Diabetes Study. J Clin Endocrinol Metab 2010; 95(5): 2240–2247.
29. Investigators OT. Predictors of nonsevere and severe hypoglycemia during glucose-lowering treatment with insulin glargine or standard drugs in the ORIGIN trial. Diabetes Care 2015; 38(1): 22–28.
30. Rosenstock J, Dailey G, Massi-Benedetti M, et al. Reduced hypoglycaemia risk with insulin glargine: a meta-analysis comparing insulin glargine with human NPH insulin in type 2 diabetes. Diabetes Care 2005; 28 : 950–955.
31. Horvath K, Jeitler K, Berghold A, et al. Long-acting insulin analogues versus NPH insulin (human isophane insulin) for type 2 diabetes mellitus. Cochrane Database Syst Rev 2007; 2: CD 005613.
32. Monami M, Marchionni N, Mannucci E. Long-acting insulin analogues versus NPH human insulin in type 2 diabetes. A meta-analysis. Diabetes Res Clin Pract 2008; 81 : 184–189.
33. Roussel R, Ritzel R, Boëlle-Le Corfec E, et al. Clinical perspectives from the BEGIN and EDITION programmes: Trial-level meta-analyses outcomes with either degludec or glargine 300 U/ml vs glargine 100 U/ml in T2DM. Diabetes Metab 2018; 44(5): 402–409.
34. Zinman B, Philis-Tsimikas A, Cariou B, et al. Insulin degludec versus insulin glargine in insulin-naive patients with type 2 diabetes: a 1-year, randomized, treat-to-target trial (BEGIN Once Long). Diabetes Care 2012; 35 : 2464–2471.
35. Ritzel R, Roussel R, Giaccari A, et al. Better glycaemic control and less hypoglycaemia with insulin glargine 300 U/mL vs glargine 100 U/mL: 1-year patient-level meta-analysis of the EDITION clinical studies in people with type 2 diabetes. Diabetes Obes Metab 2018; 20 : 541–548.
36. Ritzel R, Roussel R, Bolli GB, et al. Patient-level meta-analysis of the EDITION 1, 2 and 3 studies: glycaemic control and hypoglycaemia with new insulin glargine 300 U/ml versus glargine 100 U/ml in people with type 2 diabetes. Diabetes Obes Metab 2015; 17 : 859–867.
37. Mauricio D, Hramiak I. Second-generation insulin analogues – a review of recent real-world data and forthcoming head-to-head comparisons. Eur Endocrinol 2018; 14(Suppl1): 2–9.
38. Evans Kreider K, Pereira K, Padilla BI. Practical approaches to diagnosing, treating and preventing hypoglycemia in diabetes. Diabetes Ther 2017; 8 : 1427–1435.
39. McCoy RG, Lipska KJ, Yao X, et al. Intensive treatment and severe hypoglycemia among adults with type 2 diabetes mellitus: a population-based study. JAMA Intern Med 2016; 176(7): 969–978.
40. Lipska KJ, Warton EM, Huang ES, et al. HbA1c and risk of severe hypoglycemia in type 2 diabetes: the Diabetes and Aging Study. Diabetes Care 2013; 36(11): 3535–3542.
41. Mathur S, Zammitt NN, Frier BM. Optimal glycaemic control in elderly people with type 2 diabetes: what does the evidence say? Drug Saf 2015; 38(1): 17–32.
42. Frier BM. Hypoglycaemia in diabetes mellitus: epidemiology and clinical implications. Nat Rev Endocrinol 2014; 10 : 711–722.
43. Villani M, de Courten B, Zoungas S. Emergency treatment of hypoglycaemia: a guideline and evidence review. Diabet Med 2017; 34(9): 1205–1211.
Labels
General practitioner for children and adolescents General practitioner for adultsArticle was published in
General Practitioner

2019 Issue 2
- Advances in the Treatment of Myasthenia Gravis on the Horizon
- Hope Awakens with Early Diagnosis of Parkinson's Disease Based on Skin Odor
- Memantine in Dementia Therapy – Current Findings and Possible Future Applications
- Memantine Eases Daily Life for Patients and Caregivers
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
-
All articles in this issue
- Hypoglykemie u diabetes mellitus 2. typu – stručný přehled pro klinickou praxi
- Léčba hypoglykemie v každodenní praxi
- Zneužívání alkoholu a onkologie
- Vaskulární a psychosociální rizikové faktory mírné kognitivní poruchy – pilotní studie
- Trendy v péči v domovech pro seniory v České republice
- Co zůstalo v lékařských sponzích z Hippokratovy přísahy?
- Purple urine bag syndrome
- General Practitioner
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Co zůstalo v lékařských sponzích z Hippokratovy přísahy?
- Léčba hypoglykemie v každodenní praxi
- Trendy v péči v domovech pro seniory v České republice
- Zneužívání alkoholu a onkologie
