Diabetes mellitus a jaterní cirhóza
Diabetes mellitus and the liver cirrhosis
Patients with liver cirrhosis have increased risk of diabetes mellitus development, especially when the underlying disease is hereditary hemochromatosis, autoimune hepatitis, non-alcoholic steatohepatitis or chronic hepatitis C. Patients with associated diabetes according to liver cirrhosis complications have worse prognosis and the therapy is influenced by both diseases. The authors bring short review of particular diseases, diagnosis and treatment strategy.
Key words:
liver cirrhosis – diabetes mellitus
Authors:
T. Fejfar 1; V. Šafka 2; V. Jirkovský 1; J. Štefánková 3; P. Hůlek 1
Authors‘ workplace:
II. interní klinika Lékařské fakulty UK a FN Hradec Králové, přednosta prof. MUDr. Jaroslav Malý, CSc.
1; Ústav fyziologie Lékařské fakulty Hradec Králové, přednostka prof. MUDr. Zuzana Červinková, CSc.
2; Diabetologická ambulance Hradec Králové
3
Published in:
Vnitř Lék 2011; 57(4): 368-371
Category:
12th national Symposium diabetes, "Diabetes and Gastroenterology", Hradec Kralove, 4 to 5 June 2010
Overview
Riziko rozvoje diabetes mellitus u nemocných s jaterní cirhózou výrazně stoupá, zejména u nemocných s jaterním onemocněním na podkladě hereditární hemochromatózy, autoimunitní hepatitidy, nealkoholové steatohepatitidy a chronické infekce virem hepatitidy C. Prognóza nemocných je určována zejména pokročilostí jaterního onemocnění a přidruženými komplikacemi z něho plynoucími. Pokročilé jaterní onemocnění modifikuje terapii jak diabetu, tak i diabetes ovlivňuje léčbu vlastního jaterního onemocnění, zejména asociované portální hypertenze. Autoři přinášejí krátký přehled jednotlivých chorob s vyšším výskytem diabetu a specifika léčby.
Klíčová slova:
jaterní cirhóza – diabetes mellitus
Úvod
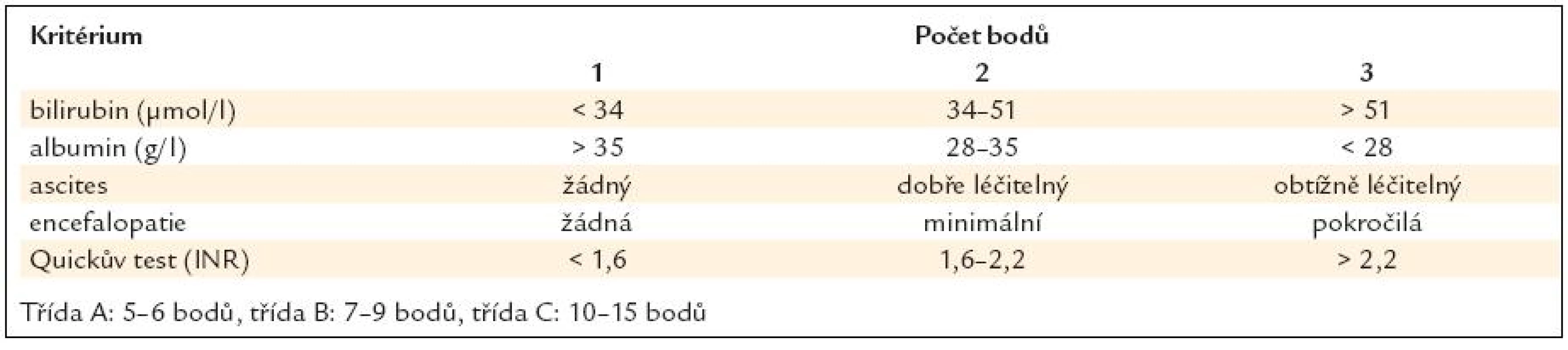
Jaterní cirhóza je konečným stadiem mnoha jaterních onemocnění. Přesná hranice mezi méně závažnou jaterní fibrózou a jaterní cirhózou, která je kromě přítomnosti vazivových sept a nekrózou hepatocytů charakterizována i přítomností uzlovité regenerace, prakticky neexistuje. Zlatým standardem pro diagnózu stále zůstává jaterní biopsie, i když v případě jasného klinického nálezu je pro diagnózu postačující charakteristický nález na zobrazovacích vyšetřeních (UZ, CT) a typický laboratorní obraz s alterací jaterního souboru, koagulopatií a hypoalbuminemií. Vzhledem k poruše portální cirkulace je toto onemocnění spojeno též se syndromem portální hypertenze. Klinická manifestace jaterního onemocnění poté závisí jak na tíži dysfunkce jaterního parenchymu, tak na tíži asociované portální hypertenze a může se pohybovat od zcela bezpříznakového stadia až po stavy ohrožující život nemocného. Pro popis tíže jaterní insuficience je nejčastěji používána Childova-Pughova klasifikace rozdělující nemocné do 3 kategorií (tab. 1).
Závažnost portální hypertenze můžeme posoudit buď přímo invazivním měřením portosystémového gradientu (normální hodnoty tlaku v portální žíle jsou do 5 mm Hg), či nepřímo endoskopickým vyšetřením, popřípadě pomocí zobrazovacích metod (UZ, CT, MRI).
Dysfunkce jater, jako jednoho z hlavních orgánů glycidového metabolizmu, je spojena i s výskytem poruchy metabolizmu glukózy, která je popisována již od začátku minulého století. Poruchu glukózové tolerance nalézáme až u 80 % nemocných, manifestní diabetes mellitus u 15–20 % nemocných. Příčiny tohoto stavu, označovaného někdy jako „hepatogenní diabetes“, nejsou zcela jasné a kromě nutričního stavu, vlivu prostředí nebo hormonálních interakcí se uplatňuje také tíže dysfunkce hepatocytů. Základní charakteristikou je v úvodu přítomná periferní inzulinová rezistence a chronická hyperinzulinemie. Rozvoj manifestního diabetu je pak spojen s progredující dysfunkcí β buněk pankreatu, která je u nemocných s jaterní cirhózou významně modifikována etiologií jaterního onemocnění. U nemocných s jaterní cirhózou a diabetem se většinou nevyskytují klasické rizikové faktory jako věk, BMI a rodinná zátěž. I výskyt pro diabetes typických komplikací ve smyslu mikro - a makroangiopatií je významně nižší v porovnání s nemocnými bez jaterní cirhózy a prognóza nemocného je určována spíše tíží jaterní insuficience a asociované portální hypertenze. Na druhou stranu je však asociace diabetu pro nemocné s jaterní cirhózou významným rizikovým faktorem a je spojena s vyšší úmrtností [1]. Asociovaný diabetes mellitus je i rizikovým faktorem rozvoje další závažné komplikace jaterní cirhózy, kterou je hepatocelulární karcinom [2,3].
Jaterní onemocnění modifikuje i strategii léčby diabetu a v některých případech naopak znesnadňuje léčbu komplikací portální hypertenze.
V praxi diabetologa je vhodné myslet při vyšetření nemocného s diabetem nebo poruchou glukózové tolerance i na možnou asociaci s jaterním onemocněním. Mezi onemocnění, která mohou vést ke vzniku jaterní cirhózy a mají výrazně vyšší riziko rozvoje diabetu, patří zejména nealkoholová steatohepatitida, hereditární hemochromatóza, autoimunitní hepatitida a chronická infekce virem hepatitidy C. Proto by bylo vhodné na tyto choroby v diagnostickém algoritmu myslet i v ordinaci diabetologa.
Hereditární hemochromatóza
Hereditární hemochromatóza je autozomálně recesivně dědičné onemocnění s nízkou fenotypovou penetrancí. Genetický defekt je v úrovni genu pro HFE protein inhibující vstřebávání železa enterocytem (inhibice transferinu). 80 % nemocných s klinicky diagnostikovanou genetickou hemochromatózou má v HFE genu mutaci C2812Y (výměna aminokyseliny cysteinu za tyroxin). V naší populaci je výskyt této mutace poměrně vysoký a je udáván v rozmezí 9–10 %. Výskyt homozygotní formy má prevalenci 1 : 300–800, takže se jedná vůbec o jednu z nejčastěji přenášených genetických chorob. Klinická manifestace je však méně výrazná a podílí se na ní řada dalších faktorů (pohlaví, vrozené vlohy k fibrogenezi). Naopak, 5–15 % homozygotů klinicky manifestní hemochromatózu nevyvine. Akumulace železa probíhá v parenchymatózních orgánech a následně v retikuloendotelovém systému, z čehož plynou i klinické projevy onemocnění. Dominuje postižení jater až s rozvojem jaterní cirhózy, při kterém je fibrogeneze zprostředkována zejména aktivovanými hvězdicovými buňkami. Může dojít k rozvoji kardiomyopatie, atropatie a hypogonadotropického hypogonadizmu. Diabetes mellitus lze prokázat u 53–80 % manifestně nemocných. Naopak, prevalence hemochromatózy se u diabetiků pohybuje kolem 1,3 %, takže hereditární hemochromatóza není jasným etiologickým faktorem [4]. Nadbytek železa snižuje sekreci inzulinu i glukózovou toleranci již v časných fázích onemocnění. V patogenezi vzniku diabetu u těchto nemocných se spolu s rozvojem inzulinové rezistence, která je vlastní i dalším jaterním chorobám, uplatňuje i oxidativní poškozením β buněk pankreatu vlivem katalytické funkce železa.
Diagnostika této choroby je poměrně snadná. Kromě vysoké saturace transferinu (nad 60 % u mužů a nad 50 % u žen) nalézáme typicky vysoké hodnoty ferritinu, obvykle tisícové. Hodnoty jaterních aminotransferáz však bývají většinou zvýšené jen mírně. V současné době je možné provést i genetické vyšetření a stanovit nejčastější mutace (C282Y, H63D a S65C). Jaterní biopsie pak v některých případech není nutná. V případě jejího provedení zjišťujeme vysokou koncentraci železa v jaterní sušině (norma do 35 μmol/ g). Přínosná jsou i zobrazovací vyšetření, zejména magnetická rezonance [5]. Léčba je založena na provádění pravidelných krevních odběrů. Včasné zahájení je prevencí vzniku těžkých orgánových komplikací a v počátečním stadiu choroby vede i ke zlepšení glukózové tolerance. V počátku léčby jsou krevní odběry prováděny týdně a dále dle hodnot ferritinu (hodnoty se udržují pod 50 μg/ l).
Autoimunitní hepatitida
Autoimunitní hepatitida (AIH) je chronické zánětlivé onemocnění jater zatím ne zcela jasné etiologie se zcela typickými projevy autoimunitní choroby. Častěji postihuje mladé ženy (poměr muži : ženy je 1 : 4), ale výjimkou nejsou ani dětští pacienti a nemocní ve věku nad 60 let. Incidence choroby je asi 1–2/100 000. Typická je vazba na HLA B8, DR3 a DR4. K poškození hepatocytů dochází zejména T-lymfocyty zprostředkovanou cytotoxickou reakcí. Velice často bývají s autoimunitní hepatitidou asociovány i další autoimunitně podmíněné choroby, zejména tyreoditida, vitiligo, celiakie, ulcerózní kolitida a diabetes mellitus 1. typu. Na rozdíl od hereditární hemochromatózy bývá zvýšení jaterních aminotransferáz výrazné. Do diagnostické mozaiky patří i typická hypergamaglobulinemie a pozitivita cirkulujících autoprotilátek. Nejčastěji nalézáme protilátky antinukleární (AIH I. typu), protilátky proti hladkému svalu (ASMA), ANCA protilátky a protilátky proti jaterním a ledvinným mikrozomům (LKM1, AIH II. typu). Definitivní diagnóza je v tomto případě ale až histologická. Základem léčby je kombinovaná imunosupresivní terapie (kortikosteroidy, azathioprin, cyklosporin).
U nemocných s AIH a diabetem současně bývá tato léčba problematičtější, a zejména při vyšších dávkách glukokortikoidů bývá spolupráce diabetologa a hepatologa nezbytná.
Chronická infekce virem hepatitidy C
Chronická infekce virem hepatitidy C (RNA virus z čeledi Flaviviridae) je dalším onemocněním z řady jaterních chorob, u kterých je asociace diabetu vyšší než v běžné populaci nemocných se stejně pokročilým jaterním onemocnění. U nemocných s chronickou hepatitidou C je zvýšení rizika sice mírné, ale signifikantní a v porovnání se stejně rizikovými nemocnými téměř dvojnásobné. Příčiny tohoto stavu se stále studují a budou jistě multifaktoriální. Často je citována přímá interakce viru a inzulinové signální cesty [6] i nepřímý virový efekt mediovaný chronickým vzestupem TNFα [7].
Naopak, u nemocných s diabetes mellitus či poruchou glukózové tolerance je pozorována nižší odpověď na protivirovou léčbu (sustaind virological response – SVR) [8]. HOMA index je i jedním z negativních prediktivních faktorů odpovědi na virologickou léčbu. U nemocných, kteří SVR dosáhnou, naopak inzulinová rezistence klesá a snižuje se i incidence diabetu [7].
Hepatocelulární karcinom
Hepatocelulární karcinom (HCC) je celosvětově 5. nejčastější malignitou a 4. nejčastější příčinou úmrtí na maligní onemocnění. V České republice je incidence tohoto onemocnění 0,8/100 000. Až 8krát častěji je postižena mužská populace. 80–90 % případů je asociováno s jaterní cirhózou. Nejrizikovější nemocní jsou přitom pacienti s chronickou infekcí virem hepatitidy C a B, hereditární hemochromatózou, alkoholovým postižením jater a nealkoholovou steatohepatitidou. Mezi rizikovější skupiny nemocných této vážné komplikace konečného stadia jaterního onemocnění patří i pacienti s asociovaným diabetes mellitus (OR 3,12 vs 2,2) [2,3,9]. Za možný patofyziologický faktor je některými autory označován promitogenní efekt hyperinzulinemie a působení insulin like growth faktoru 1 (IGF1) na hepatocyty [9].
Pětileté přežití je v současné době, zejména v důsledku pozdní diagnostiky, jen 5 %. Diagnóza je založena na zobrazovacích vyšetřeních a sérové hladině α-fetoproteinu. Cílená biopsie ložiska bývá nutná většinou jen u lézí pod 2 cm. U nemocných v časném stadiu onemocnění je indikována anatomická či neanatomická resekce ložiska či jaterní transplantace (nemocní s již významnou portální hypertenzí a manifestní jaterní dysfunkcí). V případě lokálně pokročilého onemocnění je metodou volby radiofrekvenční ablace ložiska nebo intraarteriální embolizace. Progresi generalizované choroby u nemocných ve funkční třídě A a B dle Childa a Pugha lze zpomalit podáváním multityrosinkinázového inhibitoru sorafenibu [10].
Specifika léčby
Souběh obou onemocnění komplikuje i léčebnou strategii. Nemocní s jaterní cirhózou mají, v závislosti na pokročilosti jaterní choroby, větší tendenci k rozvoji hypoglykemických stavů. Z tohoto důvodu nebývají dobře tolerovány preparáty sulfonylurey. V pokročilých stadiích je vhodnější léčba inzulinem. Podání biguanidu bývá někdy u nemocných s jaterní cirhózou spojeno s obavou z rozvoje laktátové acidózy, ale u nemocných v kompenzovaném stavu nebylo toto riziko v prospektivních studiích prokázáno [11]. Navíc vede podávání metforminu při současné protivirové léčbě u nemocných s chronickou infekcí virem hepatitidy C podle některých prací k lepší virologické odpovědi na léčbu [12].
Vzhledem ke snížení inzulinové rezistence, jako jednoho z možných promitogenních faktorů, se dle některých prací i podání metforminu jeví, na rozdíl od preparátů sulfonylurey či dlouhodobé inzulinoterapie, jako protektivní faktor rozvoje hepatocelulárního karcinomu [3].
V případě symptomatické portální hypertenze, která bývá spojena s rozvojem významných jícnových, žaludečních či ektopických varixů, je indikována v rámci primární či sekundární prevence varikózního krvácení léčba neselektivním beta-blokátorem. U nemocných s nestabilním diabetem může být tato medikace obtížná či zcela kontraindikována, a je pak třeba volit endoskopické formy léčby.
Závěr
Riziko rozvoje diabetes mellitus u nemocných s jaterní cirhózou výrazně stoupá, zejména u některých jaterních onemocnění. V praxi diabetologa je třeba na tyto choroby myslet a po eventuálním asociovaném jaterním onemocnění pátrat. Pokročilé jaterní onemocnění modifikuje terapii jak diabetu, tak i vlastního jaterního onemocnění, zejména asociované portální hypertenze. Prognóza nemocných je určována zejména pokročilostí jaterního onemocnění a přidruženými komplikacemi z něho plynoucími.
Práce byla podpořena Grantem IGA MZŘ NS 10363-3 a VZ: MZO 00179906.
MUDr. Tomáš Fejfar, Ph.D.
www.lfhk.cuni.cz
e-mail: fejfar@fnhk.cz
Doručeno do redakce: 31. 10. 2010
Sources
1. Bianchi G, Marchesini G, Zoli M et al. Prognostic significance of diabetes in patients with cirrhosis. Hepatology 1994; 20 : 119–125.
2. Lai MS, Hsieh MS, Chiu YH et al. Type 2 diabetes and hepatocellular carcinoma: A cohort study in high prevalence area of hepatitis virus infection. Hepatology 2006; 43 : 1295–1302.
3. Donadon V, Balbi M, Mas MD et al. Metformin and reduced risk of hepatocellular carcinoma in diabetic patients with chronic liver disease. Liver Int 2010; 30 : 750–758.
4. Horák J. Genetická hemochromatóza. In: Ehrmann J, Hůlek P et al (eds). Hepatologie. 1. vyd. Praha: Grada 2010 : 339–345.
5. DuBois S, Kowdley V. Review article: targeted screening for hereditary haemochromatosis in high-risc groups. Aliment Pharmacol Ther 2004; 20 : 1–14.
6. Aytug S, Reich D, Sapiro LE et al. Impaired IRS-1/PI3-kinase signalling in patients with HCV: a mechanism for increase prevalence of type 2 diabetes. Hepatology 2003; 38 : 1384–1392.
7. Alaei M, Negro R. Hepatitis C virus and glucose and lipid metabolism. Diabetes Metab 2008; 34 : 692–700.
8. Romeo-Gómez M, Fernández-Rodriguez CM, Andrare RJ at al. Effect of sustained virological response to treatment on the incidence of abnormal glucose values in chronic hepatitis C. J Hepatol 2008; 48 : 721–727.
9. Donadon V, Balbi M, Ghersetti M et al. Antidiabetic therapy and increased risk of hepatocellular carcinoma in chronic liver disease. World J Gastroenterol 2009; 15 : 2506–2511.
10. Keating GM, Santoro A. Sorafenib: a review of its use in advanced hepatocellular carcinoma. Drugs 2009; 69 : 223–240.
11. Salpeter SR, Greyber E, Pasternak GA et al. Risk of fatal and nonfatal lactic acidosis with metformin use in type 2 diabetes mellitus. Cochrane Database Syst Rev 2010; 20: CD002967.
12. Romero-Gómez M, Diago M, Andrade RJ et al. Spanish Treatment of Resistance to Insulin in Hepatitis C Genotype 1 Group. Treatment of insulin resistance with metformin in naïve genotype 1 chronic hepatitis C patients receiving peginterferon alfa-2a plus ribavirin. Hepatology 2009; 50 : 1702–1708.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2011 Issue 4
-
All articles in this issue
- Diabetes mellitus a dutina ústní
- Xerostomie, hyposialie, sicca syndrom – kvantitativní poruchy salivace
- Gastroduodenální vředová choroba u diabetika
- Poruchy motility a evakuace žaludku u diabetika. Současné možnosti diagnostiky a léčby
- Současné možnosti chirurgické léčby ložiskového postižení jater a pankreatu
- Steatóza a steatohepatitida u diabetika
- Diabetes mellitus a jaterní cirhóza
- Akutní pankreatitida u diabetika
- Celiakie a diabetes
- Kolorektální karcinom a diabetes
- Analoga amylinu, inhibitory α-glukosidáz a trávicí systém v regulaci homeostázy
- Autonomní neuropatie gastrointestinálního traktu
- Dyspeptický syndrom při antidiabetické léčbě
- Metabolická chirurgie – nejúčinnější léčba diabetu
- Metabolická chirurgie – nový směr v léčbě některých onemocnění
- Inkretinové hormony
- Léčba diabetes mellitus 2. typu GLP-1 agonisty
- Inkretinová léčba a metabolický syndrom
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Xerostomie, hyposialie, sicca syndrom – kvantitativní poruchy salivace
- Léčba diabetes mellitus 2. typu GLP-1 agonisty
- Autonomní neuropatie gastrointestinálního traktu
- Diabetes mellitus a jaterní cirhóza
