Péče o tunelizované žilní katétry u nemocných na domácí parenterální výživě podle současných doporučení
Current guidelines on the care of tunelized vascular catheters in patients on home parenteral nutrition
Home parenteral nutrition is the only option to provide nutrition in a number of patients. Care of venous entry, its management and treatment of complications resulting from its use importantly affect patient survival. Appropriate care of the catheter and the use of current knowledge may prolong the lifespan of the catheter, reduce patient morbidity and mortality and thus increase quality of life of patients who are dependent on home parenteral nutrition. The present paper summarizes recommendations for the care of long-term venous catheters.
Key words:
parenteral nutrition – catheter infection – antibiotic lock
:
J. Víšek; J. Maňák; R. Šafránek; M. Kubišová; R. Dlouhá; L. Sobotka; V. Bláha
:
III. interní gerontometabolická klinika Lékařské fakulty UK a FN Hradec Králové, přednosta prof. MUDr. Luboš Sobotka, CSc.
:
Vnitř Lék 2012; 58(12): 955-957
:
Review
Domácí parenterální výživa je nezbytná pro zajištění nutrice u řady pacientů. Péče o žilní vstup, jeho ošetřování a léčba komplikací vyplývající z jeho používání zásadně ovlivňují přežití nemocných. Při správné péči o katétr a aplikaci současných poznatků lze prodloužit životnost katétru, snížit morbiditu a mortalitu nemocných a tím i zvýšit kvalitu života pacientů závislých na domácí parenterální výživě. Tento článek shrnuje aktuální doporučení v péči o dlouhodobé žilní katétry.
Klíčová slova:
parenterální výživa – katétrová infekce – antibiotický zámek
Úvod
Selhání střeva (intestinal failure) můžeme definovat jako situaci, při které střevo není schopno zajistit adekvátní absorpci hlavních nutrientů, elektrolytů a vody nutných k udržení homeostázy vnitřního prostředí. Domácí parenterální výživa pak umožňuje nemocným především se syndromem krátkého střeva jejich dlouhodobé přežití. Podávání parenterální výživy je závislé na cévním přístupu. Jeho ošetřování, případně léčba komplikací vyplývajících z jeho používání, zásadně ovlivňuje přežití nemocných. Významným článkem v péči o katétr je i nemocný, který si parenterální výživu často sám aplikuje. I proto hraje edukace pacienta a jeho okolí významnou roli v péči o katétr. V České republice se odborně domácí parenterální výživou zabývá Pracovní skupina pro domácí parenterální výživu při Společnosti klinické výživy a intenzivní metabolické péče, která na svých stránkách publikuje i své doporučené postupy. Tato publikace shrnuje některá doporučení publikovaná především v zahraniční literatuře.
Cévní přístupy
Již řadu let se k zajištění domácí parenterální výživy využívají tunelizované katétry (např. Hickmanův a Broviacův) a porty. Indikace k jednotlivým typům mohou záležet na preferencích daného pracoviště a pacienta. Podle doporučení Evropské společnosti pro klinickou výživu a metabolismus (ESPEN – European society for parenteral and enteral nutrition) jsou však pro denní aplikaci domácí parenterální výživy doporučovány tunelizované katétry [1]. Obvykle se volí přístupy cestou v. subclavia či v. jugularis interna. Méně často se pak využívají vstupy do v. femoralis či další atypické vstupy. S prodlužující se dobou přežití jsou nemocní často limitováni dostupností cévních přístupů a jejich vyčerpání je jednou z indikací k transplantaci střeva. Kvalita péče o katétry ze strany zdravotníků i nemocných má tedy zásadní význam v přežívání těchto pacientů. Pro implantaci katétru je vhodné volit období, kdy je stav nemocného stabilizovaný a jsou vyřešeny infekční fokusy.
Ošetřování katétrů
U tunelizovaných katétrů se místo výstupu kanyly volí obvykle zhruba v úrovni prsní bradavky. Toto místo (exit site) sterilně kryjeme a krytí měníme jednou za týden, pakliže není důvod dříve. Vhodné je použití průhledných semipermeabilních folií. K lokální dezinfekci je vhodné používat roztok 2% chlorhexidinu v 70% isopropylalkoholu [2]. V dané koncentraci je však v současnosti tento roztok komerčně nedostupný, nicméně ho lze připravit magistraliter. V případě alergie na chlorhexidin lze používat roztok jodovaného povidonu. Na silikonové katétry je však používání jodových přípravků nevhodné. Vhodné je dezinfekční roztoky pravidelně obměňovat. Katétry by měly sloužit pouze k jednosměrnému podávání výživy či jiných léčiv. Neměly se do nich aplikovat krevní deriváty a používat k odběrům krve. Při podezření na katétrovou infekci lze z katétru ev. v indikovaných případech odebrat pouze krevní kultivaci. K minimalizaci vstupu do katétru je vhodné využívat bezjehlové adaptéry. Před jejich použitím je však vždy nezbytná důsledná dezinfekce.
Antikoagulace
Krátce po implantaci katétru dochází na jeho povrchu i v jeho lumen k usazování fibrinu, dalších krevních proteinů a buněčných elementů. Na tomto podkladu se mohou usazovat bakterie, které ho kolonizují a produkují specifické proteiny. Vzniká tak komplikovaná struktura bakterií, jejich produktů a lidských bílkovin – biofilm. Existuje tak úzký vztah mezi případným vznikem trombu a infekcí katétru. Z tohoto pohledu se zdá být logické používání antikoagulace k prevenci vzniku trombů a infekce. Tuto domněnku však vyvracejí některé studie. Multicentrická studie z roku 2002 uskutečněná ESPEN HAN (Home Artificial Nutrition) Group analyzovala 110 896 dnů parenterální výživy u 447 nemocných [3]. V této analýze byl ve skupině používajících heparin prokázán vyšší výskyt infekčních komplikací, nutnost častější výměny katétrů. Navíc se objevovaly komplikace spojené s používáním heparinu jako trombocytopenie, problémy s precipitací tukových emulzí atd. [4]. Dle současných doporučení ESPEN není rutinní použití heparinu doporučováno a zvláště při denním používání (pauza do 8 hod) je možné katétry proplachovat pouze fyziologickým roztokem [5]. Profylaktické podávání nízkomolekulárního heparinu či perorálních antikoagulancií je doporučováno pouze u nemocných s vysokým rizikem trombózy (např. nádorová onemocnění, anamnéza idiopatické trombózy apod.).
Léčba katétrové infekce (CRBSI – catheter related bloodstream infection)
Infekce implantovaného katétru může způsobit lokální infekční komplikace – tunelové infekce, nebo systémové komplikace v podobě katétrové infekce. Katétrovou infekci můžeme diagnostikovat u nemocných s implantovaným katétrem, se zjevnými klinickými známkami infekce, s pozitivní hemokulturou, bez jiného prokázaného zdroje infekce [6]. Diagnózu CRBSI může potvrdit shodná kultivace (včetně antibiotické citlivosti) z periferní hemokultury a konce katétru, či periferní hemokultury a hemokultury odebrané přímo z katétru. Doporučovaný je odběr párových kvantitativních nebo semikvantitativních hemokultur. Počet kolonií v hemokultuře odebrané z katétru má být alespoň 3krát větší než z periferní hemokultury. Eventuálně lze sledovat růst bakterií v hemokultuře v čase. Pozitivita hemokultury odebrané z katétru by pak měla o 2 hod předbíhat periferní hemokulturu (DTP kriterium – differential time to positivity). V případě extrakce infikovaného katétru považujeme za pozitivní nález více než 15 CFU (colony forming unit – počet životaschopných bakterií na 5 cm délky žilního katétru) nebo více než 102 CFU u kvantitativního stanovení.
Při léčbě CRBSI postupujeme podle tíže infekce a infekčního agens. Za nekomplikované CRBSI považujeme infekce, jejichž příznaky při léčbě vymizejí do 72 hod a pakliže není endovaskulárně přítomný cizorodý materiál (např. elektroda kardiostimulátoru). V případě nekomplikované CRBSI lze postupovat konzervativně – implantovaný katétr ponechat a zahájit léčbu systémovými antibiotiky a antibiotickými zámky. V případě infekce Staphylococcus aureus, kandidové a mykobakteriové infekce a ev. infekce gramnegativními mikroorganizmy je však i u nekomplikované CRBSI indikována extrakce katétru. Je však samozřejmě vždy nutno přihlédnou k aktuálnímu stavu nemocného, možnostem nového cévního přístupu apod.
Za komplikované CRBSI považujeme takové, které jsou provázeny lokálními příznaky (tunelová infekce, absces) či těžkým septickým stavem, infekční endokarditidou, tromboflebitidou a tvorbou septických embolizací. Takové případy jsou pak vždy indikací k extrakci katétru a adekvátní antibiotické léčbě. Katétr je dále doporučováno extrahovat, pakliže bakteriemie neodezní ani po 72 hod adekvátní léčby, či při recidivující infekci v krátkém časovém období (6 týdnů), jejichž původcem je stejné agens.
Antibiotickou léčbu zahajujeme ihned po odběru kultivací. Katétr vyřazujeme z činnosti a uzavíráme ho antibiotickým zámkem (ALT – antibiotic lock therapy) s cílem sterilizace katétru. Antibiotické zámky volíme dle zvyklostí a mikrobiálních profilů daného pracoviště. Antibiotické zámky obvykle měníme po 24 hod. Vhodná je obměna používaných antibiotik. Antibiotické zámky se používají v koncentracích převyšujících 1 000krát minimální inhibiční koncentraci u vankomycinu a 100krát pro ostatní antibiotika [7]. Doporučené koncentrace pro různá antibiotika udává tab. 1 [8]. Tyto koncentrace jsou uváděny s ohledem na bezpečnost směsi při smíchání s heparinem. V případě vynechání heparinu se můžeme držet výše uvedeného doporučení týkajícího se překročení minimálních inhibičních koncentrací a tedy používat výrazně vyšší koncentrace antibiotik v zámku.
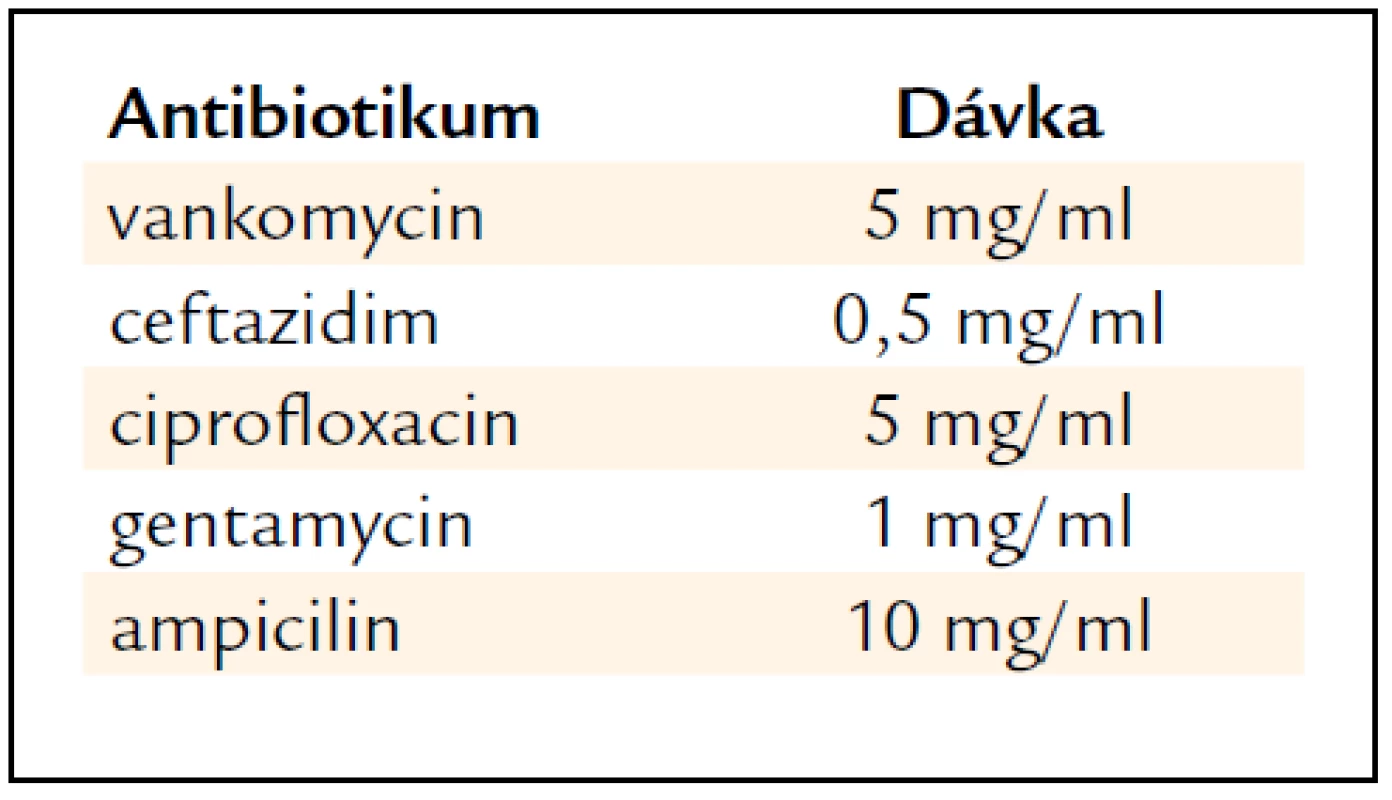
Katétr vyřazujeme z činnosti obvykle na 7–14 dní. Pakliže se ze závažných důvodů rozhodneme katétr i přes infekci Staphylococcus aureus ponechat, aplikujeme ALT po dobu 4 týdnů.
Některá pracoviště používají k uzávěru katétru i 70% roztok etanolu. Etanol působí denaturaci bílkovin bakterií a má široké antibakteriální účinky bez známosti rezistence. Jeho používání však není podle posledních guidelines doporučováno, neboť není dostatečně prokázán jeho efekt v prevenci a léčbě CRBSI (Mermel et al. [8]). Na druhou stranu např. metaanalýza z letošního roku u pediatrických nemocných ukazuje redukci počtu katétrových infekcí na 1 000 katétrodnů o 7,67 události a extrakce katétrů o 5,07 události, tedy snížení počtu CRBSI o 81 % a počtu extrakcí katétru o 72 %. Zároveň ukazuje relativně nízký počet nežádoucích účinků, mezi něž patří především trombotické příhody [9].
Variantou k používaným zámkům je užití taurolidinu. Jedná se o modifikovanou aminokyselinu taurin s širokým účinkem na gramnegativní i grampozitivní mikroorganizmy včetně polyrezistentních bakterií, jako jsou MRSA (meticilin-rezistentní Staphylococcus aureus), VRE (vankomycin-rezistentní Enterococcus spp.) a houby. Mechanizmem jeho účinku je ireverzibilní vazba jeho hydroxymetylové skupiny na buněčnou stěnu a ovlivnění schopnosti adherence bakterií. Taurolidin tak působí preventivně na vznik biofilmu uvnitř katétru. Po podání se v lidském organizmu metabolizuje na taurin, oxid uhličitý a vodu. Zatím nebyla zaznamenána rezistence proti taurolidinu. V řadě studií se jeho preventivní používání osvědčilo a bylo dosaženo snížení počtu katétrových infekcí proti kontrolní skupině. Zatím není dostatek prací, které by se zabývaly srovnáním taurolidinu s ostatními antibiotiky. V jedné in vitro studii však taurolidin vychází lépe ve srovnání s etanolem, vankomycinen, ciprofloxacinem a rifampicinem ve svých účincích při eradikaci Staphylococcus aureus a kandidy [10]. U ostatních mikroorganizmů byly účinky zámků srovnatelné. Nicméně u taurolidinu byla zaznamenána nejrychlejší redukce počtu kolonií mikrobů. Zvláště u pacientů s recidivujícími katétrovými sepsemi lze taurolidin používat i preventivně [11].
Antibiotické zámky však nepodáváme samostatně, ale kombinujeme je se systémovým podáním antibiotik. Léčbu zahajujeme obvykle empiricky dle zvyklosti a mikrobiálního spektra daného pracoviště. Pro empirickou léčbu volíme kombinaci antibiotik pokrývající grampozitivní i gramnegativní floru, tzn. např. vankomycin v kombinaci s 4. generací cefalosporinů nebo karbapenemovým antibiotikem. Případně používáme vankomycin s beta-laktamovým antibiotikem s inhibitorem beta-laktamázy a s aminoglykosidem. Antibiotickou léčbu dále deeskalujeme dle kultivačního nálezu. Dobu podávání antibiotik upravujeme dle kultivačního nálezu, obvykle však aplikujeme 10–14 dnů. Antibiotika však podáváme i 7–14 dnů po extrakci katétru v případě infekce gramnegativními bakteriemi a 4–6 týdnů při infekci Staphylococcus aureus, při nálezu infekční endokarditidy nebo při přetrvávající bakteriemii (více než 72 hod po extrakci katétru).
Závěr
Časná diagnostika a správná léčba katétrových infekcí je nezbytná pro dlouhodobé úspěšné zajištění parenterální výživy. Ve světové literatuře se udává incidence zhruba 0,3 CRBSI na rok s nutností extrakce katétru zhruba 0,5 na rok. Při správné péči o katétry a aplikaci současných poznatků lze prodloužit životnost katétru, snížit morbiditu a mortalitu nemocných a tím i zvýšit kvalitu života pacientů závislých na domácí parenterální výživě.
Tato práce byla podpořena PRVOUK P37/12, IGA MH CR NT/12287-5.
MUDr. Jakub Víšek, Ph.D.
www.fnhk.cz
e-mail: jakub.visek@fnhk.cz
Doručeno do redakce: 12. 6. 2012
Přijato po recenzi: 16. 10. 2012
Sources
1. Pittiruti M, Hamilton H, Biffi R et al. ESPEN Guidelines on Parenteral Nutrition: central venous catheters (access, care, diagnosis and therapy of complications). Clin Nutr 2009; 28 : 365–377.
2. Mimoz O, Pieroni L, Lawrence C et al. Prospective, randomized trial of two antiseptic solutions for prevention of central venous or arterial catheter colonization and infection in intensive care unit patients. Crit Care Med 1996; 24 : 1818–1823.
3. Bozzetti F, Mariani L, Bertinet DB et al. Central venous catheter complications in 447 patients on home parenteral nutrition: an analysis of over 100.000 catheter days. Clin Nutr 2002; 21 : 475–485.
4. Zapletal O, Blatný J, Štarha J. Heparinem indukovaná trombocytopenie při léčbě nízkomolekulárními hepariny u dětí. Je čeho se obávat? Vnitř Lék 2010; 56: (Suppl 1): 55–57.
5. Staun M, Pironi L, Bozzetti F et al. ESPEN Guidelines on Parenteral Nutrition: Home Parenteral Nutrition (HPN) in adult patients. Clin Nutr 2009; 28 : 467–479.
6. Pronovost P, Needham D, Berenholtz S et al. An intervention to decrease catheter-related bloodstream infections in the ICU. N Engl J Med 2006; 355 : 2725–2732.
7. Vanholder R, Canaud B, Fluck R et al. Diagnosis, prevention and treatment of haemodialysis catheter-related blood stream infections (CRBSI): a position statement of European Renal Best Practice (ERBP). NDT Plus 2010; 3 : 234–246.
8. Mermel LA, Allon M, Bouza E et al. Clinical practice guidelines for the diagnosis and management of intravascular catheter-related infection: 2009 update by the Infectious Diseases Society of America. Clin Infect Dis 2009; 49 : 1–45.
9. Oliveira C, Nasr A, Brindle M, Wales PW. Ethanol Locks to Prevent Catheter-Related Bloodstream Infections in Parenteral Nutrition: A Meta-Analysis. Pediatrics 2012; 129 : 318–329.
10. Sherertz RJ, Boger MS, Collins CA, Mason L, Raad II. Comparative in vitro efficacies of various catheter lock solutions. Antimicrob Agents Chemother 2006; 50 : 1865–1868.
11. Touré A, Lauverjat M, Peraldi C et al. Taurolidine lock solution in the secondary prevention of central venous catheter--associated bloodstream infection in home parenteral nutrition patients. Clinical Nutr 2012; 31 : 567–570.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2012 Issue 12
-
All articles in this issue
- Outcomes of AL-amyloidosis treatment with bortezomib, dexamethasone and cyclophosphamide or doxorubicin-containing regimens
- Is antiplatelet therapy always effective?
- Our experience with the treatment of primary lymphomas of the central nervous system
- Arterial hypertension in gravidity – a risk factor for cardiovascular diseases
- Current opinions on gout, its diagnosis and treatment
- Primary cilia of cells of cardiovascular apparatus
- Population-level changes to promote cardiovascular health
- Current guidelines on the care of tunelized vascular catheters in patients on home parenteral nutrition
- Toxic hepatitis induced by Polygonum multiflorum
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Arterial hypertension in gravidity – a risk factor for cardiovascular diseases
- Current opinions on gout, its diagnosis and treatment
- Current guidelines on the care of tunelized vascular catheters in patients on home parenteral nutrition
- Is antiplatelet therapy always effective?
