Subklinické tyreopatie
Subclinical thyroid disease
Importance of subclinical thyroid disease (STh) is now a matter of discussion. Definition of this unit is laboratory: in presence of normal level of thyroxine (T4) TSH value is changed: in lower TSH level the subclinical hyperthyroidism (STx) in increase TSH levels subclinical hypothyroidism (SH) is present. Risk of clinical manifestation is twoo three times highter in comparison with persons with normal TSH level. Clinical importance STh is still not evaluated definitively. SH caused disturbance of lipid metabolism, elasticity of vessels and endothelial function and therefore increases risk of atherosclerosis. STx causes electrical instability of myocardium with increased risk of arythmias, increases risk of osteoporosis and other changes. Most important are effects of STh in cardiology, reproductive medicine and gynecology. Clinical significance of these effects is not definitively evaluated.
Key words:
atherosclerosis – gynecology risks – hyperthyroidism – hypothyroidism – pregnancy risks – subclinical thyroid disease
Authors:
Václav Zamrazil 1,2
Authors‘ workplace:
Endokrinologický ústav Praha, ředitelka doc. RNDr. Běla Bendlová, CSc.
1; Subkatedra endokrinologie IPVZ Praha, vedoucí subkatedry prof. MUDr. Václav Zamrazil, DrSc.
2
Published in:
Vnitř Lék 2015; 61(10): 873-876
Category:
Reviews
Overview
Význam subklinických tyreopatií je v současné době předmětem diskusí. Jde o laboratorně definovanou jednotku, u které je při normální hladině tyroxinu (T4) změněna hodnota tyreotropního hormonu hypofýzy (thyroid-stimulating hormone – TSH). Při jeho snížení jde o subklinickou hypertyreózu/tyreotoxikózu (STx), při zvýšení o subklinickou hypotyreózu (SH). Tyto stavy jsou 2–3krát častější než klinicky manifestní formy. Představují nesporně 2–3krát zvýšené riziko vzniku klinicky manifestních onemocnění. Méně shody je v tom, jak závažná je z klinického hlediska samotná přítomnost subklinických tyreopatií. SH vede k poruchám lipidového metabolizmu, ke změnám elasticity cévní stěny a funkce endotelu. Důsledkem je zvýšené riziko aterosklerózy. STx vyvolává elektrickou instabilitu myokardu s následným rizikem arytmií, poruchy kostního metabolizmu s následnou osteoporózou a další dosud ne zcela jednoznačně hodnocené změny. Největší význam mají subklinické tyreopatie v kardiologii, v reprodukční medicíně a gynekologii a v porodnictví.
Klíčová slova:
ateroskleróza – gynekologická a porodnická rizika – subklinické tyreopatie (hypotyreóza, hypertyreóza)
Úvod
Subklinické tyreopatie (STh) jsou již delší dobu předmětem zájmu a především střetávání různých názorů o jejich významu a o jejich léčbě. V současné době se objevila řada studií, které hodnotí jejich význam v různých oborech medicíny, především v kardiologii, reprodukční medicíně a gynekologii, gerontologii a v řadě dalších oborů. I když zatím nejsou často k dispozici definitivní závěry, stává se zřejmým, že problematika STh přesahuje rámec tyreoidologie a zasahuje do mnoha oborů.
Definice STh
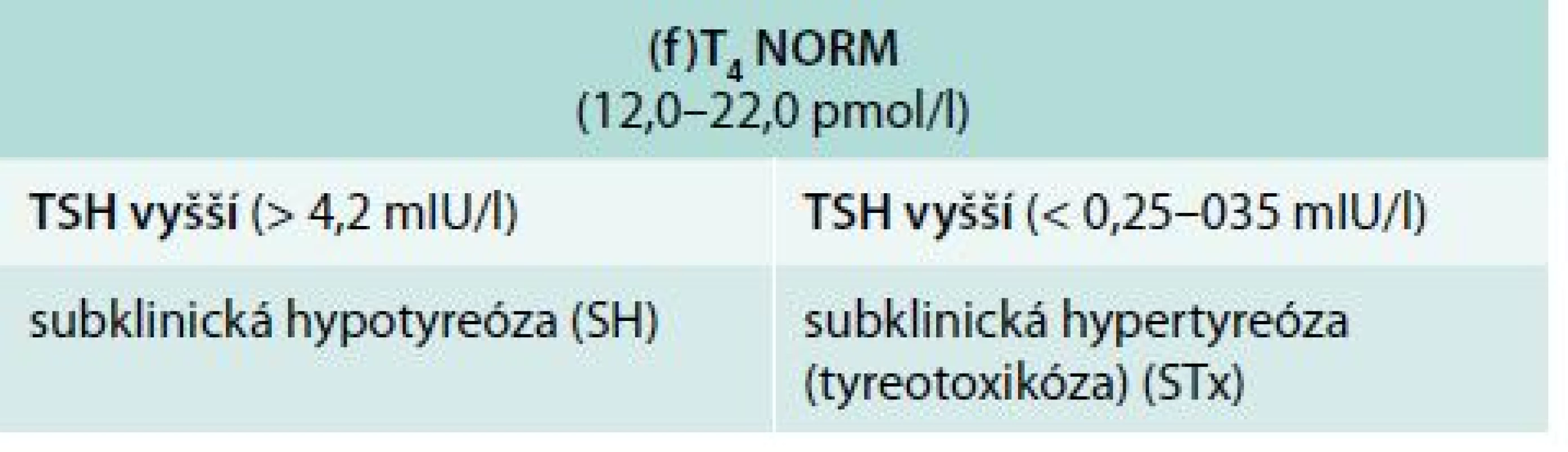
Je nutno zdůraznit, že sama definice je poměrně zmatečná [6,13,29]. Termín „subklinická“ by měl ukazovat na to, že se jedná o stav, který není spojený s výraznou klinickou symptomatologií. Ve skutečnosti je ale termín STh definován čistě laboratorně (tab. 1). Jedná se o stav, při němž hormony štítné žlázy (v klinické praxi hodnotíme především volný tyroxin) jsou v referenčním pásmu, ale hodnota TSH (tyreotropin) je změněná. Při jeho zvýšení nad referenční mez (obvykle se udává 4,2–4,5 mIU/l) mluvíme o subklinické hypotyreóze (SH). Je-li hladina TSH snížena pod udávanou dolní hranici (0,25–0,30 mIU/l), mluvíme o subklinické tyreotoxikóze (STx) nebo hypertyreóze. Je samozřejmě nutno brát v úvahu, že referenční rozmezí se liší podle typu použitých setů a vybavení příslušné laboratoře. Zcela odlišné hodnoty TSH jsou platné v graviditě. V 1. trimestru se jako horní hranice normy uvádí 2,5 mIU/l.
Někteří autoři uvádějí jako subklinické tyreopatie rovněž kategorii mikrokarcinomu štítné žlázy a přítomnost tyreoidálních protilátek (proti tyreoglobulinu a proti tyreoidální peroxidáze) – jako projev subklinické tyreoditidy. Náplní této práce jsou pouze klasické STH, tj. nepoměru mezi normální hladinou tyreoidálních hormonů a změněné hladiny TSH.
Epidemiologie STh
Jedná se o nejčastější choroby štítné žlázy v našich podmínkách [1,2,5,20]. Obecně se udává, že jsou 2–3krát častější než klinicky manifestní formy hypotyreózy a tyreotoxikózy. V průměrné populaci se SH vyskytuje u 5–7 % osob, STx u 0,3–0,5 % osob. Platí zde závislost na pohlaví – jsou 5–7krát častější u žen než u mužů. V případě SH je výrazná věková závislost, výskyt s věkem stoupá. Vyplývá z toho, že u žen po klimakteriu se podle některých dat vyskytují STh až u 15 % této populace. V dětském věku se vyskytují spíše výjimečně.
Etiologie STh
Obecně vyplývá porucha funkce štítné žlázy z vlivu nejrůznějších faktorů [2–4,6,7,22,27,29,30]. Výjimečně může hrát roli parciální defekt enzymatického vybavení štítné žlázy. Tato porucha častěji vede ke klinicky manifestní hypotyreóze. V našich podmínkách prakticky nepřichází v úvahu subklinická hypotyreóza z nedostatku jodu, protože obecně je naše populace v současné době saturována dostatečně (neplatí to obecně, nejdůležitější skupinou ohroženou jodopenií jsou těhotné ženy a novorozenci a kojenci živení mateřským mlékem). Existují však oblasti, v nichž jsou různé stupně poklesu funkce štítné žlázy následkem nedostatku jodu, tedy i subklinická hypotyreóza, časté. Je ale nutno uvést, že za určitých okolností může i nadbytek jodu, působící delší dobu, vyvolat pokles funkce štítné žlázy, který se upraví po snížení přívodu jodu.
Nejčastější příčinou vzniku STh (jak subklinické hypotyreózy, tak tyreotoxikózy) je u nás autoimunitní postižení funkce štítné žlázy. To přispívá i k vysvětlení věkového nárůstu a rozdílu mezi pohlavími. Přesná data chybějí, avšak je možno odhadnout, že 80–90 % STh vzniká na podkladě autoimunitního procesu.
STh stále častěji vznikají vlivem činnosti lékařů. SH často vznikne po subtotální tyreoidektomii, při předávkování tyreostatik, po léčbě radiojodem, nebo po ozáření krajiny krku. STx je poměrně často vyvolána předávkováním tyroxinu podávaného z různé indikace, převážně k substituci hypotyreózy. Suprese TSH, tj. vyvolání subklinické hypertyreózy, je přímo cílem v různých fázích léčby karcinomu štítné žlázy a při různém stadiu choroby.
Problematický, a dosud ne plně vysvětlený, je vliv jodu. Jednorázová zátěž masivní dávkou jodu může vyvolat jak hyperfunkci, tak hypofunkci. Platí to při podání v kardiologii populárního amiodaronu, ale i po RTG vyšetření s jodovou kontrastní dávkou. Dlouhodobé podávání nižších dávek jodu může vyvolat pokles funkce štítné žlázy, tj. SH. Podle většiny literárních dat po vysazení jodu se SH zlepšuje, nebo ustoupí.
Všechny léčebné přípravky, u kterých je popsán výskyt hypotyreózy, jsou i příčinou SH.
Vztah STh a přívodu jodu
Vzhledem k tomu, že nedostatek jodu a výskyt STh jsou časté ve většině lokalit, je nutno jejich vzájemnému vztahu věnovat pozornost [2,18–21]. Je pravděpodobné, že změny zásobení jodem působí převážně tím, že ovlivňují tyreoidální autoimunitu. Většina nálezů svědčí pro zvýšený výskyt tyreoidální autoimunity při zvýšení přívodu jodu. Sami jsme pozorovali na vybraném vzorku naší populace nárůst zvýšeného titru protilátek proti Tg (tyreoglobulin) a TPO (tyreoidální peroxidáza). Jak již bylo uvedeno, dlouhodobě zvýšený přísun jodu může suprimovat funkci štítné žlázy přímým účinkem.
Diagnostika STh
Vyplývá v podstatě ze současného vyšetření TSH a tyroxinu (nejlépe volný T4) a porovnání získaných hodnot (tab. 1).
Jak bylo uvedeno, klinický obraz není rozhodující. U některých osob s STh jsou přítomny příznaky obdobné těm, které pozorujeme u klinicky manifestní hypotyreózy či hypertyreózy. Z hlediska diagnostiky to není rozhodující.
U SH nacházíme často v laboratoři poruchy lipidogramu, u STx na EKG tachykardii, eventuálně sklon k fibrilaci síní (vzácněji i k jiným arytmiím).
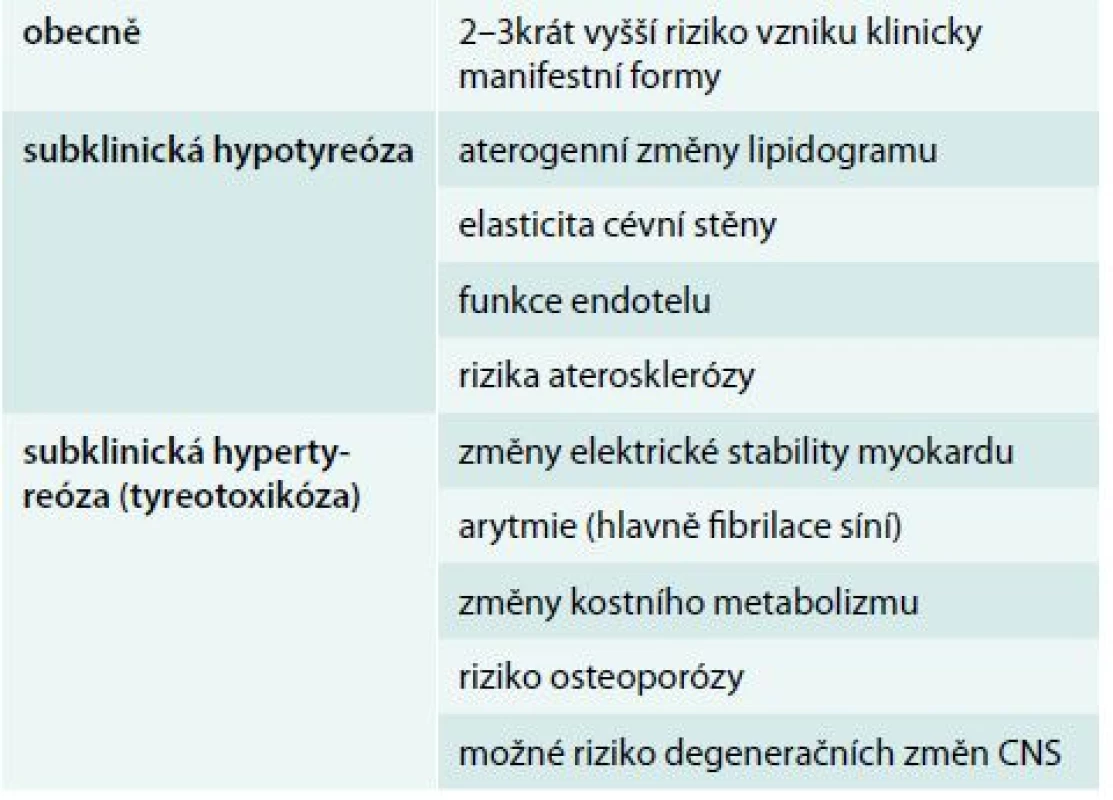
Rizika STh
Rizika STh jsou uvedena v tab. 2. Na tuto problematiku existují různé názory [5,8–11,16,24]. Obecně je přítomnost subklinické tyreopatie spojena se zvýšeným rizikem vzniku klinicky manifestní hypotyreózy či hypertyreózy. Většina nálezů ukazuje, že toto riziko je až 3krát vyšší než u populace s normální hladinou TSH. Zřejmě se riziko zvyšuje u osob s pozitivními tyreoidálními protilátkami, vliv věku je hodnocen různě.
Méně shody je o tom, jak klinicky závažná je samotná přítomnost STh. Jak vyplývá z tab. 2, subklinická hypotyreóza je spojena především se zvýšeným rizikem aterosklerózy. Vyplývá to z vlivu SH na změny lipidogramu, které zvyšují aterogenní index. Kromě toho se zřejmě uplatňuje vliv na funkci endotelu a na elasticitu cévní stěny. Nepříznivý je i vliv SH na činnost myokardu. Častější je sklon k mírné diastolické dysfunkci.
STx působí rovněž výrazně na oběhový systém. U experimentálních zvířat i u lidí zvyšuje elektrickou instabilitu myokardu. Vede to k riziku vzniku arytmií, převážně k fibrilaci síní, ale vzácněji i k poruchám rytmu komor. Většina prací prokazuje, že se tím zvyšuje i riziko náhlé smrti. Kromě vlivu na oběh je STx spojena se zvýšeným rizikem osteoporózy, zejména u žen v periklimakterickém a postklimakterickém věku. Existují názory, že nejen klinicky manifestní tyreotoxikóza, ale i STx zvyšuje riziko degenerativních chorob CNS včetně obávané Alzheimerovy choroby.
Zajímavý, ale málo probádaný je vliv věku na rizika STh. Jak již bylo uvedeno, nepříznivý vliv na skelet je u STx výraznější u žen vyššího věku. Vliv věku na oběh je hodnocen různě. Pravděpodobně v mladším věku je celkem dobře snášena STx, ve vyšším věku je tomu naopak. Existují názory, že SH zvyšuje naději na dlouhověkost.
Terapie SH
Je předmětem největších rozporů [15,18,27,29,30]. Obecně existují 3 zásadní přístupy:
- STH vzhledem k tomu, že málo ovlivňují klinický stav, není nutno léčit, vždy je nutná dispenzarizace s kontrolami klinického stavu TSH a fT4, doporučené intervaly kolísají od 6 měsíců do 2–3 let
- vzhledem k uvedeným rizikům je vhodné léčit všechny osoby s STh, doporučuje se podávání malých dávek tyroxinu podle jeho vlivu na hodnotu TSH, obvykle vystačíme s 25–50 µg/den; je nutno léčbu sledovat (klinický nález, EKG změny, hodnoty TSH a fT4 ve výše uvedených intervalech), hlavním rizikem léčby je předávkování do subklinické hypertyreózy (suprese TSH)
- léčbu tyroxinem indikovat pouze u osob se zvýšeným rizikem STH; zejména u starších osob se SH hrozí riziko oběhových komplikací (fibrilace síní, oběhová dekompenzace), proto se ve stáří indikuje hormonální léčba SH s velkou opatrností a spíše výjimečně
Záleží zřejmě i na původní výši TSH. Řada autorů doporučuje zahájit léčbu tyroxinem, až pokud hladina TSH přesáhne 10 mIU/l. U těchto osob je při přítomnosti pozitivních protilátek proti TPO léčba indikována až u 92 % vyšetřených osob [27]. To samozřejmě neplatí v graviditě, v níž je jednak horní hranice TSH nižší (v 1. trimestru 2,5 mIU/l) a riziko i mírné hypofunkce nepříznivě ovlivňuje průběh těhotenství, vývoj plodu a poporodní komplikace (viz dále).
Před nasazením léčby tyroxinem je nutné stav ověřit opakovaným vyšetřením TSH vzhledem k tomu, že často dochází k jeho spontánní normalizaci. Dispenzarizace je v tomto případě nadále nutná. Často dochází k opakovanému vzniku STH.
Jak již bylo uvedeno, STH působí prakticky na celý organizmus (ale s nespornými rozdíly v závažnosti změn). Nejvýznamnější je vliv na oběhový systém, na reprodukci a průběh těhotenství a podle nejnovějších údajů na nervový systém. Těmto oborům je věnována největší pozornost, což dokládá velký počet recentních publikací. Vybraná data jsou uvedena ve stručnosti dále.
Vliv na kardiovaskulární systém
Důležitá je zřejmě závažnost změn lipidogramu [11,12,14,23,25,26,28]. Efekt změn TSH na hladinu celkového cholesterolu a LDL frakce je výrazný zejména ve vyšším věku [8]. Naproti tomu nebyla prokázána souvislost mezi výskytem SH subklinické hypotyreózy a ischemické choroby mozkové u starších žen [28]. Některé dřívější epidemiologické studie prokazují nesporný vliv STh (jak hypotyreózy, tak tyreotoxikózy) na mortalitu – kardiovaskulárně podmíněnou i celkovou. Existují však práce, které tuto závislost nepotvrzují. Zdůrazňuje se riziko předávkování tyroxinem ve vyšším věku, které je poměrně časté a může vést ke zvýšení rizika kardiovaskulární mortality [7].
Vliv na reprodukci a graviditu
Tato problematika je v současné době asi nejpopulárnější a věnuje se jí největší pozornost [17,29–35]. Existují rozsáhlé přehledové práce [6,29], které probírají problematiku z nejrůznějších aspektů. Zejména se řeší:
nepříznivý vliv SH na průběh těhotenství (zvýšené riziko potratu a předčasného porodu)
- rizika vývojových poruch plodů u žen s přítomností SH; obecně se uznává nepříznivý vliv na některé psychické funkce, který přetrvává pravděpodobně během celého dalšího života; zejména se zdůrazňuje snížení IQ; změny povahy – hyperaktivní nezvládnutelné dítě – se pravděpodobně postupně částečně upravují
- existují údaje o tom, že v poporodním průběhu dětí matek se SH je zvýšená morbidita a mortalita; tento nález však není obecně uznáván
- u žen se SH je snad zvýšené riziko růstu strumy během gravidity
Ve všech těchto případech však lze obtížně odlišit vliv snížené saturace jodem a přítomnosti tyreoidální autoimunity. Obecně se uznává, že oba tyto vlivy mohou působit samostatně a v kombinaci se SH se nepříznivé účinky spojují. Vliv STx v těhotenství je nesporně méně významný. Významně nepříznivě působí až klinicky manifestní tyreotoxikóza.
I když současný stav znalostí neumožňuje definitivní posouzení této problematiky, existují doporučení Americké tyreoidální asociace (ATA) [30] i Evropské tyreoidální společnosti (ETA) [29] optimální léčby SH v těhotenství.
Kromě vlivu STh v graviditě je nutno zhodnotit význam pro vývoj reprodukčních funkcí a fertilitu. Je nespornou klinickou zkušeností, že i lehká hypotyreóza nepříznivě ovlivňuje zejména fertilitu žen. Do jaké míry je významný vliv SH, není dosud jednoznačně zhodnoceno, ale je pravděpodobný.
Další nepříznivé vlivy STh
Zasahují pravděpodobně do celé řady lékařských oborů včetně psychiatrie [24]. Údaje jsou značně odlišné až rozporuplné a jejich rozsah i zaměření přesahují rámec tohoto sdělení.
Závěr
Problematika subklinických tyreopatií patří mezi nejčastější náplň práce klinických endokrinologů. Zasahuje do celé řady oborů, tedy nejen do endokrinologie, ale také do kardiologie, reprodukční medicíny, gynekologie, porodnictví. Přitom v současné době je s hodnocením jejich významu mnoho nejasností. Teprve systematické prospektivní studie nejdůležitější otázky mohou vyřešit.
Doručeno do redakce 7. 9. 2015
Přijato po recenzi 25. 9. 2015
prof. MUDr. Václav Zamrazil, DrSc.
vzamrazil@endo.cz
Endokrinologický ústav, Praha
www.endo.cz
Sources
1. Dvořáková M1, Hill M, Čerovská J et al. Vliv saturace jodem na výskyt tyreopatií ve vybraných regionech u dospělé populace České republiky. Vnitř Lék 2010; 56(12): 1262–1270.
2. Zimmermann MB, Andersson M. Assessment of iodine nutrition in populations: past, present, and future. Nutr Rev 2012; 70(10): 553–570.
3. Kahaly GY, Dienes HP, Beyer J et al. Iodide induces thyroid autoimmunity in patients with endemic goitre: a randomised, double-blind, placebo-controlled trial. Eur J Endocrinol 1998; 139(3): 290–297.
4. Pedersen IB, Knudsen N, Jorgensen T et al. Thyroid peroxidase and thyroglobulin autoantibodies in a large survey of populations with mild and moderate iodine deficiency. Clin Endocrinol (Oxf) 2003; 58(1): 36–42.
5. Taylor PN, Lazarus JH. Subclinical hypothyroidism in pregnancy. What next after CATS? Thyroid Int 2014; 2 : 1–16. Dostupné z WWW: <http://www.thyrolink.com/merck_serono_thyrolink/en/images/Thyroid_Inter_2_2014_NEU_WEB_tcm1553_129405.pdf?Version=>.
6. Bliddal S, Feldt-Rassmussen N. Protilátky proti tyreoidální peroxidáze jako rizikový faktor v těhotenství. Thyroid Int (české vydání) 2015; 3 : 1–39.
7. Mammen JS, McGready J, Oxman R et al. Thyroid Hormone Therapy and Risk of Thyrotoxicosis in Community-Resident Older Adults: Findings from the Baltimore Longitudinal Study of Aging. Thyroid 2015; 25(9): 979–986.
8. Zhao M, Yang T, Chen Let al. Subclinical hypothyroidism might worsen the effects of aging on serum lipid profiles: a population-based case-control study. Thyroid 2015; 25(5): 485–493.
9. Biondi B, Cooper DS. The clinical significance of subclinical thyroid dysfunction. Endocr Rev 2008; 29(1): 76–131.
10. Duntas LH, Brenta G. The effect of thyroid disorders on lipid levels and metabolism. Med Clin North Am 2012; 96(2): 269–281.
11. Lioudaki E, Mavroeidi NG, Mikhailidis DP et al. Subclinical hypothyroidism and vascular risk: an update. Hormones (Athens) 2013; 12(4): 495–506.
12. Pearce EN. Update in lipid alteration in subclinical hypothyroidism. J Clin Endocrinol Metab 2012; 97(2): 326–333.
13. Canaris GJ, Manowitz NR, Mayor G et al. The Colorado thyroid disease prevalence study. Arch Intern Med 2000; 160(4): 526–534.
14. Pasqualetti G, Tognini S, Polini A et al. Is subclinical hypothyroidism a cardiovascular risk factor in the elderly? J Clin Endocrinol Metab 2013; 98(6): 2256–2266.
15. Meier C, Staub JJ, Roth CB et al. TSH-controlled L-thyroxine therapy reduces cholesterol levels and clinical symptoms in subclinical hypothyroidism: a double blind, placebo-controlled trial (Basel Thyroid Study). J Clin Endocrinol Metab 2001; 86(10): 4860–4866.
16. Asvold BO, Bjøro T, Platou C et al. Thyroid function and the risk of coronary heart disease: 12-year follow-up of the HUNT study in Norway. Clin Endocrinol (Oxf) 2012; 77(6): 911–917.
17. Liu H, Shan Z, Li C et al. Maternal subclinical hypothyroidism thyroid autoimmunity and risk of miseatiage: a prospective cohort study. Thyroid 2014; 24(11): 1642–1649.
18. Joung JY, Cho YY, Park SM et al. Effect of iodine restriction on thyroid function in subclinical hypothyroid patients in an iodine-replete area: a long period observation in a large-scale cohort. Thyroid 2014; 24(9): 1361–1368.
19. Zimmermann MB, Jooste PL, Pandav CJ. Iodine-deficiency disorders. Lancet 2008; 372(9645): 1251–1262.
20. Yoon SY, Choi SR, Kim DM et al. The effect of iodine restriction on thyroid function in patients with hypothyroidism due to Hashimoto’s thyroiditis. Yonsei Med J 2003; 44(2): 227–235.
21. Leung AM, Braverman LE. Consequences of excess iodine. Nat Rev Endocrinol 2014; 10(3): 136–142.
22. Rassoly L, Burek CL, Rose NR. Iodine-induced autoimmune thyroiditis in NOD-H-2h4 mice. Clin Immunolog Immunopathol 1996; 81(3): 287–292.
23. Maor E, Kivity S, Kopal E et al. Differences in heart rate profile during exercice among subjects with subclinical thyroid disease. Thyroid 2013; 23(10): 1226–1232.
24. Biondi B, Palmieri EA, Fazio S et al. Endogenous subclinical hyperthyroidism affects quality of life and cardiac morphology and function in young and middle-aged patients. J Clin Endocrinol Metab 2000; 85(12): 4701–4705.
25. Biondi B, Palmieri EA, Lombardi G et al. Effects of subclinical thyroid dysfunction on the heart. Ann Intern Med 2002; 137(11): 904–914.
26. Brenta G, Mutti LA, Schnitman H et al. Assessment of left ventricular diastolic function by radionuclide ventriculography at rest and exercise in subclinical hypothyroidism, and its response to L-thyroxine therapy. Am J Cardiol 2003; 91(11): 1327–1330.
27. Rosario PW, Calsolari MG. How selective are the new guidelines for treatment of subclinical hypothyroidism for patients with thyrotropin levels at or below 10 mIU/L? Thyroid 2013; 23(5): 562–565.
28. Giri A, Edwards TL, LeGrys VA et al. Subclinical hypothyroidism and risk for incident ischemic stroke among postmenopausal women. Thyroid 2014; 24(8): 2010–2017.
29. Lazarus J, Brown R, Daumerie C et al. 2014 European thyroid association guidelines for the management of subclinical hypothyroidism in pregnancy and in children. Eur Thyr J 2014; 3(2): 76–94.
30. Stagnaro-Green A, Abalovich M, Alexander E et al. Guidelines of the American Thyroid Association for the diagnosis and management of thyroid disease during pregnancy and postpartum. Thyroid 2011; 21(10): 1081–1125.
31. Teng W, Shzu Z. Pregnancy and thyroid diseases in China. Thyroid 2011; 21(10): 1053–1055.
32. Haddow JE. Thyroid Study Group. Subclinical hypothyroidism and pregnancy outcomes. Obstet Gynecol 2005; 106(1): 198.
33. Krassas GF, Poppe K, Glinoer D. Thyroid function and human reproductive health. Endocr Rev 2010; 31(5): 702–755.
34. Männistö T, Mendola P, Grewal J et al. Thyroid diseases and adverse pregnant outcomer in contemporaly US cohort. J Clin Endocrinol Metab 2013; 98(7): 2725–2733.
35. Wilson KL, Casey BM, Melutize DT et al. Subclinical thyroid disease and the incidence of hypertension in pregnancy. Obstred Gynecol 2012; 119(2 Pt1): 315–320.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2015 Issue 10
-
All articles in this issue
- Incidentalom nadledviny
- Adrenální insuficience
- Štítná žláza a gravidita – souhrn důležitých poznatků
- Léčba hypotyreózy a hypertyreózy
- Subklinické tyreopatie
- Chronická lymfocytární tyreoiditida a karcinom štítné žlázy
- Funkční hypotalamická amenorea
- Syndrom polycystických ovarií
- Novinky v diagnostice a léčbě MEN1
- Akromegalie: současný pohled
- Systémová léčba glukokortikoidy: praktický pohled
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Funkční hypotalamická amenorea
- Systémová léčba glukokortikoidy: praktický pohled
- Incidentalom nadledviny
- Adrenální insuficience