Epidemiologie hypercholesterolemie
Epidemiology of hypercholesterolemia
Hypercholesterolemia is one of the most important risk factors of cardiovascular (CV) disease. Epidemiology follows the prevalence, the incidence and the possibilities of risk factors or diseases intervention. A review of observation epidemiologic studies, pharmacotherapy and treatment perspectives is presented. The first epidemiologic studies, e.g. the Framingham Heart Study or MRFIT showed hyperlipidemia is associated with the incidence of CV disease. The North Karelia Project showed the intervention of CV risk factors is useful on population-based principles. Interventional studies with statins showed the usefulness of LDL cholesterol lowering to decrease CV morbidity and mortality and also total mortality. Anyway, the control of CV risk factors is unsatisfactory.
Key words:
epidemiology – hypercholesterolemia – intervention
:
Barbora Nussbaumerová; Hana Rosolová
:
Centrum preventivní kardiologie II. interní kliniky LF UK a FN Plzeň
:
Vnitř Lék 2018; 64(1): 30-37
:
Reviews
Hypercholesterolemie je významný rizikový faktor pro aterosklerotické vaskulární nemoci. Epidemiologie sleduje výskyt (prevalenci), incidenci a možnosti ovlivnění (intervence) rizikového faktoru nebo nemoci. V článku podáváme přehled observačních epidemiologických studií, intervenčních studií, dostupné farmakoterapie a perspektiv léčby hypercholesterolemie. První epidemiologické studie, jako je Framingham Heart Study nebo MRFIT, přinesly důkazy o asociaci hyperlipidemie a incidence kardiovaskulárních (KV) onemocnění. Další studie, jako např. North Karēlia Project, prokázaly, že intervence rizikových faktorů KV onemocnění na úrovni celé populace má smysl. Intervenční studie zejména se statiny potvrdily účelnost snižování hladin LDL-cholesterolu k nízkým hodnotám s cílem snížení KV morbidity a KV i celkové mortality. Kontrola rizikových faktorů KV onemocnění zůstává nedostatečná.
Klíčová slova:
epidemiologie – hypercholesterolemie – intervence
Hypercholesterolemie jako rizikový faktor
Je jasně prokázáno, že hypercholesterolemie patří spolu s arteriální hypertenzí, diabetes mellitus 2. typu a inzulinovou rezistencí, obezitou centrálního typu, kouřením, věkem, mužským pohlavím a pozitivní rodinnou anamnézou mezi nejvýznamnější rizikové faktory aterosklerotických vaskulárních nemocí.
Existence cholesterolu byla odhalena na začátku 19. století. Aterosklerotické poškození tepen zkoumal však již Leonardo da Vinci. Aterosklerotické léze měli ve svých cévách dle současných výzkumů již egyptští faraóni. V roce 1931 provádí akademik N. N. Aničkov pokus na králících krmených purifikovaným cholesterolem a prokazuje přímou souvislost s patologickými změnami v jejich cévách. Již roku 1938 popisuje Carl Müller výskyt anginy pectoris v práci Xanthomata, hypercholestrolemia angina pectoris u pacientů s fenotypem familiární hypercholesterolemie. Od 20. let 20. století jsou prováděny menší epidemiologické studie.
V poválečných Spojených státech amerických se šíří kardiovaskulární onemocnění (KVO) a úmrtí na srdeční infarkt zejména mezi jinak zdravými muži ve věku 40–60 let jako epidemie a stávají se hlavní příčinou mortality populace. V letech 1946–1948 byla American Heart Association (AHA) přeměněna z profesionální společnosti na dobrovolnou organizaci, která měla za úkol získávat finanční prostředky a stimulovat výzkum, a do kardiovaskulární (KV) prevence se zapojil více i samotný stát. Byl založen Národní kardiologický ústav (National Heart Institute – NHI) jako divize Národního ústavu zdraví (National Institute of Health – NIH) a v roce 1948 je zde formulována prozíravá pracovní hypotéza: „Abychom porozuměli srdečním chorobám, musíme identifikovat a kvantifikovat konstituční (dědičné) faktory, dále zevní faktory, umožňující uplatnění dědičných; a posléze zjistit, jak dlouho musí trvat interakce vnitřních a zevních faktorů, aby vznikla choroba“.
Framingham Heart Study
Zároveň byl zařazen první pacient do v té době průlomové a naprosto originální studie – Framingham Heart Study (FSH). Byla vytvořena originální kohorta o 5 209 dobrovolnících ve věku od 30 do 62 let s trvalým bydlištěm ve městě Framingham v Massachusetts poblíž Bostonu. Jednalo se o muže i ženy v primární prevenci KVO, v té době definované jako osoby bez zjevných symptomů KV onemocnění, nebo jako ty, kteří ještě neprodělali srdeční infarkt nebo cévní mozkovou příhodu (CMP). Po důkladné vstupní prohlídce byli účastníci vyšetřováni každé 2 roky. V průběhu sledování vedl vývoj zdravotního stavu ve framinghamské populaci poprvé k identifikaci hlavních rizikových faktorů pro výskyt různých KVO nebo „příhod“ – v té době náhlé srdeční smrti, akutního infarktu myokardu, CMP a srdečního selhání. Těmito rizikovými faktory byly shledány kromě vysoké hladiny celkového cholesterolu i vysoký krevní tlak, hladina triglyceridů, věk, pohlaví a psychosociální faktory včetně kouření. V posledních 25 letech bylo také vyšetřeno více než 5 000 dětí účastníků studie (Offspring Cohort v roce 1971, The Omni Cohort v roce 1994, Third Generation Cohort v roce 2002, New Offspring Spouse Cohort v roce 2003, Second Generation Omni Cohort v roce 2003). To mimo jiné dovoluje hodnotit i relativní podíl faktorů dědičnosti a prostředí. Klíčové poznatky z FHS shrnuje tab. 1 [1].
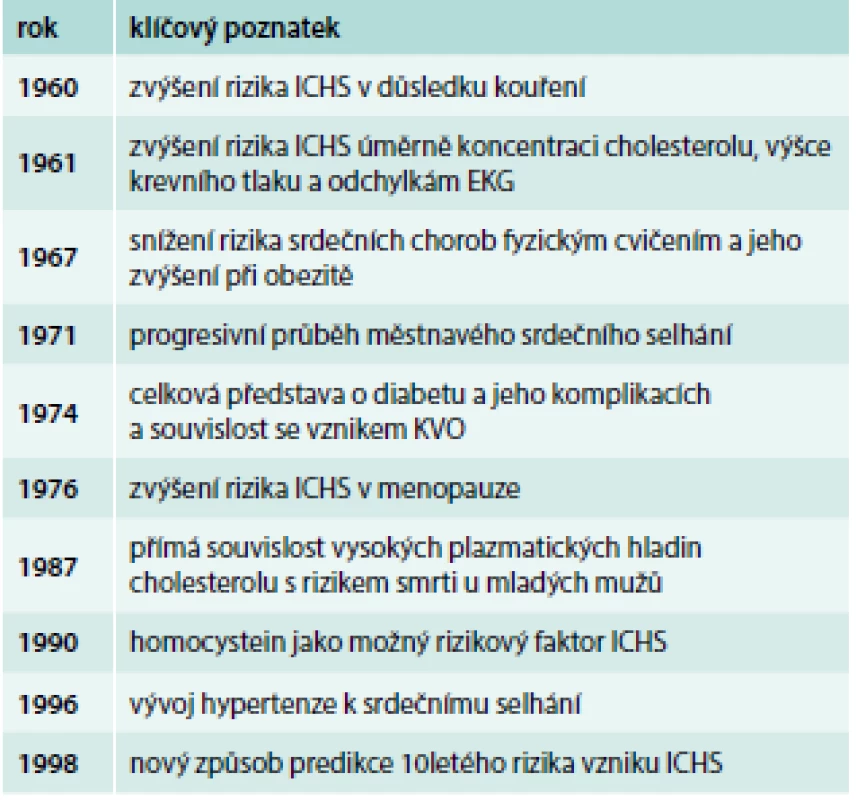
Seven Countries Study
V roce 1998 byl na základě poznatků z FHS vytvořen nový způsob predikce 10letého rizika vzniku ischemické choroby srdeční (ICHS). Dr. Ancel Keys a jeho tým začali roku 1958 na popud rozdílného výskytu ICHS v různých populacích pracovat na Studii sedmi zemí (Seven Countries Study: coronary heart disease – SCS) a první poznatky publikovali v roce 1970. Byly sledovány antropometrické parametry, EKG a laboratorní parametry včetně lipidogramu. Byla zkoumána anamnéza kouření a velmi precizně i dieta. Každý týden byly zasílány duplikáty snězeného jídla do centrální laboratoře, v níž byly analyzovány na přítomnost mastných kyselin, dusíku a popela. Keys et al se v počátcích svého výzkumu setkávali s velkou nedůvěrou, ba posměchem. Při porovnání populací z Itálie, Řecka, bývalé Jugoslávie, Finska, Nizozemí, Japonska a USA jasně prokázali souvislost mezi složením stravy a srdečními chorobami. Jednoznačně též prokázali závislost mezi hladinami cholesterolu a výskytem ICHS. Po 10 a 25 letech sledování byl celkový cholesterol významným prediktorem rozvoje ICHS. Tato asociace byla patrná i po 35 letech sledování, i když s věkem její významnost slábla. Dieta v jižních státech byla zdravější, což přineslo i výrazný rozdíl v incidenci ICHS mezi severem a jihem [2]. Ze studie vychází mimo jiné závěr, že v zemích s vysokým KV rizikem je třeba léčit hypercholesterolemii přísněji než v zemích s nízkým rizikem, což se odráží např. v tabulkách systému SCORE [3].
Multiple Risk Factor Intervention Trial
Studie MRFIT (Multiple Risk Factor Intervention Trial) je dosud nejrozsáhlejší studií zabývající se vztahem mezi cholesterolem a ICHS. Bylo do ní zařazeno přes 35 0000 mužů bez anamnézy infarktu myokardu. V průběhu celého rozložení koncentrací cholesterolu je patrný silný, kontinuální a vystupňovaný vztah mezi koncentrací cholesterolu a incidencí ICHS. Významným poznatkem ze studie MRFIT je, že výskyt ICHS narůstá již od hladiny celkového cholesterolu 3,9 mmol/l [4].
Evropské epidemiologické studie
Epidemiologické studie začaly probíhat i v Evropě, v níž došlo k nárůstu incidence ICHS o dvě desítky let později než v USA. Nejprve to bylo v severských zemích (Oslo, Trømsø, Götteborg) a poté i ve Velké Británii (prevalenční studie Whitehall Study nebo British Regional Heart Study).
Česká preventivní kardiologie
Kořeny české preventivní kardiologie sahají do roku 1928, ve kterém akademik Klement Weber 20 let před zahájením Framinghamské studie již předpokládal existenci určitých prediktivních faktorů pro aterosklerózu. V 50. letech 20. století pak kardiolog prof. Zdeněk Reiniš, zakladatel české preventivní kardiologie, zorganizoval první epidemiologickou studii sledující výskyt infarktu myokardu v severních Čechách a založil první registr srdečních infarktů myokardu v Mladé Boleslavi [5]. V té době byla pracovníky Institutu klinické a experimentální medicíny (IKEM) v Praze koordinována Národní multifaktoriální primárně preventivní studie infarktů myokardu a cévních mozkových příhod [6]. I přes znalost rizikového profilu pro ICHS byla implementace známých preventivních opatření v té době nedostatečná [7].
Projekt MONICA
Velký mezinárodní (Multinational MONItoring of trends and determinants in CArdiovascular disease) iniciovaný Světovou zdravotnickou organizací začal probíhat na přelomu 80. a 90. let ve 27 zemích světa včetně tehdejšího Československa. U nás byly zařazeny regiony Praha-východ, Cheb, Benešov, Pardubice, Chrudim a Jindřichův Hradec [8]. Vznikl náhodný 1% populační vzorek mužů a žen ve věku 25–64 let a celkem byla provedena 3 nezávislá průřezová šetření (roku 1985, 1988 a 1992). Dostali jsme informace o klesající morbiditě a mortalitě z kardiovaskulárních příčin od poloviny 80. do poloviny 90. let minulého století.
Projekt post-MONICA
Unikátní český projekt post-MONICA (s dalšími okresy Plzeň-město, Litoměřice a Kroměříž) pokračuje zejména díky prof. MUDr. Renatě Cífkové (tehdy IKEM Praha, nyní Thomayerova nemocnice Praha) jako dlouhodobé sledování reprezentativních vzorků české populace do dnešních dnů (sondy v letech 1997–1998, 2000–2001, 2007–2009, v době psaní článku probíhá další vyšetřování). Výsledky těchto studií poskytují řadu cenných informací o vývoji prevalence standardních i novějších rizikových faktorů a markerů KVO včetně hypercholesterolemie, a hlavně o důležitých změnách v mortalitě z KV příčin. Např. průměrná hladina celkového cholesterolu klesla v české populaci v průběhu posledních asi 23 let o 1,1 mmol/l u mužů a 1,06 mmol/l u žen [9,10].
Intervence hypercholesterolemie režimovými opatřeními
North Karēlia Project
Velmi ilustrativním případem intervence hypercholesterolemie a dalších rizikových faktorů KVO na úrovni celé populace přináší North Karēlia Project, zahájený roku 1972 [11]. V poválečném období došlo v tomto regionu Finska k extrémnímu nárůstu prevalence a incidence ICHS. Lidé si mohli dovolit kupovat cigarety a po letech strádání si užívali konzumace uzenin, plnotučných mléčných výrobků z tradičního chovu dobytka, másla a soli. V 70. letech byla mortalita z KV příčin v tomto regionu nejvyšší, přičemž polovina mužů umírajících na infarkt myokardu byla mladší 65 let a 40 % infarktů končilo fatálně. Desetina obyvatel mezi 45 a 59 lety byla v invalidním důchodu z důvodu ICHS. Cílem projektu bylo snížit cholesterolemii, konzumaci soli a prevalenci kouření. Ke vzniku projektu přispěla i samotná iniciativa obyvatel regionu. Puska et al dokázali zavést výuku zdravého životního stylu do škol i mezi dospělou populaci, dokázali změnit složení potravin dodávaných do supermarketů i prodávaných v restauracích. Prosadili snížení podílu soli v jídlech i zavedení rostlinných tuků na úkor živočišných. Místní farmáři byli dotováni, aby na úkor chovu dobytka pěstovali řepku speciálně vyšlechtěnou pro severské podmínky. Velkou roli sehrály sponzorované spolky žen, které pořádaly setkání spojená s vařením, ochutnávkami a předáváním zdravých receptů. Byla obnovena severská tradice pěstování lesních plodů, protože pěstování zeleniny a ovoce bylo v severské zemi obtížné. Byly budovány pěší stezky i cyklostezky a běžkařské tratě, vzhledem ke krátkým zimním dnům i osvětlené, i krytá sportoviště. Již mezi léty 1974–1979 poklesla mortalita z KV příčin v tomto regionu o 22 %, hodnoty celkového cholesterolu poklesly o 18 % a průměrná střední délka života se zvýšila o 7 let.
Projekt Rodinný ochranný režim
Velmi zajímavým a prvním projektem svého druhu v tehdejším Československu byl projekt Rodinný ochranný režim vzniklý ve spolupráci plzeňských kardiologů a pediatrů pod vedením prof. Jaroslava Šimona. Cílem bylo ochránit děti s vysokým KV rizikem před rozvojem časné aterosklerózy a jejích následků. Byly sledovány děti z vysokorizikových rodin, tj. z rodin, v nichž jeden z rodičů prodělal infarkt myokardu v mladém věku (tj. otec do 55 let věku nebo matka do 65 let věku). U těchto dětí i rodičů byla prováděna intenzivní intervence rizikových faktorů ICHS [12]. Rodinný ochranný režim navazoval na český multiregionální interdisciplinární preventivní projekt Výzkum komplexní léčebné a preventivní péče v průmyslové populaci [13]. Tento výzkumný projekt se soustředil na posouzení úrovně lékařské péče a preventivních opatření u nemocných s chronickými neinfekčními nemocemi (většinou s KVO) v české populaci. Do projektu byly zařazeny obě plzeňské epidemiologické studie PILS I (Pilsen Interventional Longitudinal Study) [14] u mužů středního věku a PILS II u mužů a žen z průmyslové populace bývalého strojírenského podniku Škoda [15].
Intervence hypercholesterolemie farmakoterapií
Primárním cílem v léčbě dyslipidemií je dosažení cílových hladin LDL-cholesterolu (LDL-C), které se řídí celkovým KV rizikem dle platných odborných doporučení [3].
Pryskyřice
Pryskyřice na sebe vážou v trávicím ústrojí žlučové kyseliny, což způsobuje jejich menší vstřebávání v zažívacím traktu a následné zvýšení jejich syntézy v játrech. To vede ke zvýšení počtu LDL receptorů na jaterních buňkách, které tak z krve dokáží navázat větší množství LDL-C. V prakticky jediné velké intervenční studii s pryskyřicemi zaměřené na KV příhody v polovině 80. let minulého století – studii LRC-CPPT (Lipid Research Clinics’ Coronary Primary Prevention Trial) – vedla léčba cholestyraminem k signifikantnímu poklesu výskytu ICHS a úmrtí na ICHS [16]. Jedinou dostupnou pryskyřicí je u nás cholestyramin (Vasosan) v rámci specifického léčebného programu, tzn. lék je na lékařský předpis a pacient musí být lékařem informován, že mu je předepisován neregistrovaný léčivý přípravek. Dle SPC je cholestyramin indikován pro děti a ženy, které mohou otěhotnět (jsou ve fertilním věku) s těžkými dědičnými poruchami látkové výměny lipidů (především familiární hypercholesterolemií a těžkou formou polygenní hypercholesterolemie), a/nebo jsou-li ve vysokém riziku KV příhody na podkladě aterosklerotického procesu v dospělém/vyšším věku [17]. Vzhledem k nepříjemnostem provázejícím užívání pryskyřic a snižující se věkové hranici pro užívání statinů u dětí je léčba pryskyřicemi na výrazném ústupu.
Statiny
První statin objevil v 70. letech 20. století při studiu hub pro účely potravinářství Japonec Akira Endo (mevastatin). Další statiny byly již syntetizovány uměle a byly účinnější a lépe tolerované. Statiny jsou inhibitory 3-hydroxy-3-metyl-glutaryl koenzymu A (HMG-CoA) reduktázy. Hlavním účinkem statinů je snížení celkového a LDL-C, ale též mírně snižují koncentrace triglyceridů a nepatrně zvyšují hodnoty protektivního HDL-cholesterolu. Statiny přinesly doslova revoluci v léčbě hypercholesterolemie a jsou zde lékem první volby. Nejvíce intervenčních studií se statiny proběhlo v 90. letech minulého století. Nejdříve byli zařazováni pacienti s vysokými hladinami cholesterolu v sekundární prevenci KVO. Postupně byli zařazování pacienti i v primární prevenci se stále nižšími vstupními hladinami cholesterolu.
Průlomovou studií byla studie 4S (Scandinavian Simvastatin Survival Study). Bylo zařazeno 4 444 mužů a žen s anamnézou ICHS (tzn. sekundárně preventivní studie), kteří byli randomizováni k podávání simvastatinu 20 mg nebo 40 mg a placeba. Vstupní hodnota celkového cholesterolu (T-C) byla v rozmezí 5,5–8,0 mmol/l. Cílová koncentrace T-C byla 3,0–5,2 mmol/l. Primární cíl studie – celková mortalita – klesl o statisticky významných 30 % (p = 0,0003), mortalita z KV příčin o 42 % (p < 0,00001). Významně poklesla incidence infarktu myokardu o 33 % a potřeba revaskularizace o 34 % i incidence CMP o 28 % [18]. Ve všech studiích pak bylo prokázáno, že pacienti v sekundární i primární prevenci profitují z terapie statiny ve smyslu snížení hodnot LDL-C, morbidity a mortality z KV příčin, ale i mortality celkové [3]. Statinová pyramida ukazuje vývoj zařazené studijní populace a hodnot lipidogramu v čase (schéma).

Statiny jsou velmi účinné ve snížení hodnot LDL-C. Dokáží zpomalit progresi aterosklerózy, jak bylo prokázáno ve studii REGRESS (REgression Growth Evaluation Statin Study). V porovnání s placebem snížil pravastatin hodnoty LDL o 30 %, zpomalil růst aterosklerotických plátů a snížil výskyt KV příhod o relativních 40 % [19]. Agresivní snižování LDL-C atorvastatinem k hodnotám < 2 mmol/l vedlo k pomalejší progresi aterosklerotických plátů než standardní léčba pravastatinem (studie REVERSAL – Reversal of Atherosclerosis with Aggressive Lipid Lowering) [20]. Agresivní léčba rosuvastatinem k hladinám LDL-C 1,6 mmol/l dokázala navodit i její regresi, jak bylo prokázáno ve studii ASTEROID (A Study to Evaluate the Effect of Rosuvastatin on Intravascular Ultrasound-Derived Coronary Atheroma Burden) [21]. Obecně je přijímán fakt, že hladina LDL-C potřebná k regresi aterosklerózy, je nižší než 2 mmol/l.
Ezetimib
Ezetimib je selektivní inhibitor absorpce cholesterolu v kartáčovém lemu membrány enterocytu. Blokáda vstřebávání je důsledkem přímého účinku ezetimibu na transportní Niemann-Pick C1 Like Protein 1 (NPC1L1). Ezetimib není metabolizován přes cytochrom CYP 450, a proto má nízký výskyt lékových interakcí, a přirozeně tedy i nežádoucích účinků. Ezetimib snižuje v monoterapii hodnotu LDL-C asi o 20 %. Pokud současně blokujeme ezetimibem vstřebávání exogenního cholesterolu, zvýšíme vylučování cholesterolu do střeva v rámci enterohepatální cirkulace a snižujeme biosyntézu cholesterolu v játrech statinem (duální inhibice), dosáhneme velmi významného snížení T-C, a zejména LDL-C. Snížení nabídky LDL-C vede současně principem zpětné vazby ke zvýšení exprese LDL receptorů v periferii a zvýšenému vychytávání LDL částic z plazmy. Pro klinickou praxi je podstatné, že kombinací statinu a ezetimibu rychleji dosáhneme cílových hodnot lipidogramu než samotným statinem. Tato kombinace má podobný účinek jako zdvojnásobení dávky statinů 3krát po sobě. Je vhodná především pro nemocné ve vysokém KV riziku včetně diabetiků a osob s prediabetem, u kterých působí kardioprotektivně a snižuje celkovou mortalitu. Účinnost kombinace statinů s ezetimibem byla prokázána bez ohledu na věk, pohlaví a rasu pacientů, stejně tak jako u různých skupin pacientů (s různým kardiometabolickým rizikem, smíšenou dyslipidemií a familiární hypercholesterolemií) [22].
Definitivní odpovědí na otázku, zda další snižování LDL-C nad rámec terapie statiny přidáním ezetimibu vede i k dalšímu snížení KV rizika, přinesla 7 let trvající studie IMPROVE-IT (IMProved Reduction of Outcomes: Vytorin Efficacy International Trial). Přes 18 000 pacientů s anamnézou akutního koronárního syndromu bylo randomizováno k podávání simvastatinu v dávce 40 mg v monoterapii nebo k podávání fixní kombinace 40 mg simvastatinu s 10 mg ezetimibu. Primárním cílovým ukazatelem studie IMPROVE-IT byl složený ukazatel zahrnující úmrtí z KV příčin, infarkt myokardu nevedoucí k úmrtí, nefatální CMP a hospitalizaci pro nestabilní anginu pectoris nebo koronární revaskularizaci vyskytující se nejméně 30 dní po randomizaci. K manifestaci primárního cíle došlo u 32,7 % pacientů užívajících kombinační léčbu a u 34,7 % pacientů užívajících monoterapii simvastatinem (p = 0,016). Tímto statisticky významným rozdílem bylo prokázáno, že přidání ezetimibu k terapii statinem vede k dalšímu snížení KV rizika, resp. KV příhod. Počet nemocných, které je třeba léčit k zabránění jedné příhody (number needed to treat – NNT), byl ve studii IMPROVE-IT pouhých 50, pokud byli odečteni nemocní, kteří nikdy neužili medikaci, bylo to dokonce 38. Při dalším porovnání hladiny LDL-C v obou léčených větvích, při kterém měla střední hladina LDL-C hodnotu 1,3 mmol/l u kombinační léčby a 1,8 mmol/l u monoterapie statinem, snížila kombinační léčba relativní riziko o 6,4 %. Tímto výsledkem byl potvrzen léčebný účinek, který byl již dříve viditelný ve studiích se statiny – byla potvrzena „LDL hypotéza“ rozvoje aterosklerózy a rovněž hypotéza, že pro LDL-C platí „čím níže, tím lépe“. Po ukončení této studie jsme dostali pozitivní data až do hodnot LDL-C 1,3 mmol/l. Ve studii IMPROVE-IT nebyl výrazný rozdíl mezi léčebnými skupinami, co se týče výskytu nežádoucích účinků [23].
Fibráty
Účinky fibrátů na úpravu hladiny lipidů jsou zprostředkovány aktivací PPARα (Peroxisome Proliferator Activated Receptor type α). Fibráty zvyšují lipolýzu a eliminaci aterogenních částic bohatých na triglyceridy. Účinky fenofibrátu vedou ke snížení frakcí o velmi nízké a nízké hustotě (VLDL a LDL) obsahujících apoprotein B a ke zvýšení frakce o vysoké hustotě (HDL) obsahující apoprotein AI a AII. Prostřednictvím úpravy syntézy a katabolizmu VLDL frakce fenofibrát zvyšuje clearance LDL a snižuje malé denzní LDL, jejichž hladiny jsou zvýšeny u aterogenního fenotypu lipoproteinu. Celkový cholesterol snižují o 20–25 %, triglyceridy o 40–55 % a HDL-C zvyšují o 10–30 %. Existují důkazy, že léčba fibráty může snížit výskyt ICHS, ale nebylo prokázáno snížení mortality z jakékoli příčiny v primární nebo sekundární prevenci KVO. V léčbě hypercholesterolemie nejsou lékem volby.
Niacin
Z historického hlediska bychom měli zmínit kyselinu nikotinovou, resp. niacin, což je nejstarší používané hypolipidemikum známé již asi 50 let. Důkazy z tehdejších studií o 20% snížení hladin LDL-C a triglyceridů a zvýšení HDL-C byly velice slibné a niacin snižoval v porovnání s placebem i morbiditu a mortalitu z KV příčin. Pro nežádoucí vazomotorické účinky bylo od léčby niacinem na dlouhá léta upuštěno. Renesancí měla být kombinace s laropiprantem, nicméně v průběhu studie HPS-THRIVE (Heart Protection Study 2 – Treatment of HDL to Reduce the Incidence of Vascular Events) nebylo prokázáno, že by kombinace statinu s niacinem vedla ke snížení úmrtí z koronárních příčin, nefatálního infarktu myokardu, CMP nebo nutnosti revaskularizace, a studie byla proto předčasně ukončena.
Lomitapid
Lomitapid snižuje tvorbu LDL-C tím, že se váže na mikrosomální triglycerid transfer protein (MTP) a inhibuje ho, čímž brání vazbě apoB lipoproteinů a triglyceridů v játrech a střevních buňkách. Lomitapid byl indikován v léčbě homozygotní familiární hypercholesterolemie. Z českého trhu byl stažen.
Hypercholesterolemie a cévní mozková příhoda
Souvislost mezi CMP a hypercholesterolemií byla objasněna později než její souvislost s ICHS. Často je zmiňován tzv. cholesterolový paradox – ve většině epidemiologických studií nebyla prokázána závislost mezi cholesterolemií a rizikem CMP. Příkladem je metaanalýza 45 prospektivních studií sledujících po dobu 16 let asi 450 000 osob, u nichž došlo během doby sledování k přibližně 13 000 CMP [24]. Potíž je, že kohorta byla vytvořena především ke studiu rizika ICHS, a navíc v ní nebyly rozlišovány CMP dle etiologie jako ischemické a hemoragické. Jiné studie vztah hypercholesterolemie a CMP prokázaly, pokud rozlišovaly mezi jednotlivými podtypy CMP. Kodaňská prospektivní studie prokázala pozitivní korelaci mezi zvýšením T-C na hodnotu > 8 mmol/ l a rizikem ischemické CMP. Již zmíněná studie MRFIT (The Multiple Risk Factor Intervention Trial) prokázala, že se zvyšující se hladinou cholesterolu se zvyšuje riziko úmrtí na ischemickou CMP.
Ve výše zmíněné studii LRC-CPPT s cholestyraminem nebyl výskyt CMP vůbec sledován [16]. V intervenčních studiích se statiny je výsledek závislý na zařazené studijní populaci, zda se jedná o pacienty v primární nebo sekundární prevenci ICHS. Drtivá většina studií s hypolipidemiky byla koncipována s cílem snížit riziko koronárních, nikoliv cerebrovaskulárních příhod. Většina z nich byla provedena u pacientů s manifestní ICHS a menší část u osob bez ICHS, pacienti po CMP do většiny z nich nebyli zařazeni.
Jediná intervenční studie s hypolipidemiky s cílem sekundární prevence CMP byla studie SPARCL (The Stroke Prevention by Aggressive Reduction in Cholesterol Levels) [25]. Byla zkoumána vysoká dávka atorvastatinu (80 mg) u pacientů bez anamnézy ICHS, po ischemickém nebo hemoragickém iktu (CMP) či tranzitorní ischemické atace. Léčba atorvastatinem snížila v porovnání s placebem relativní riziko (RR) recidivy CMP o 16 % a riziko koronárních příhod o 29 %. Pokles rizika CMP byl podobný jako v jiných statinových studiích u pacientů s ICHS. Atorvastatin je zatím jediný statin s prokázaným snížením rizika recidivy ischemické CMP u nemocných v sekundární prevenci CMP.
Údaje o snižování rizika první ischemické CMP statiny u pacientů s a bez anamnézy ICHS jsou k dispozici pouze pro předem definované populace z provedených intervenčních studií. Víme, že atorvastatin v dávce 10 mg byl účinný u mužů nad 40 let věku s hypertenzí, hypercholesterolemií a nejméně 3 rizikovými faktory (studie ASCOTT-LLA – Anglo-Scandinavian Cardiac Outcomes Trial – Lipid Lowering Arm, snížení RR CMP o 27 %, p = 0,024) [26] a u nemocných s diabetes mellitus 2. typu nad 40 let věku se zvýšeným LDL-C a nejméně jedním dalším rizikovým faktorem pro ICHS (studie CARDS – Collaborative Atorvastatin Diabetes Study, snížení RR CMP o 48 %, p = 0,016) [27]. Rosuvastatin v dávce 20 mg byl účinný u mužů nad 50 let a u žen nad 60 let věku ve vysokém riziku KVO s mírně zvýšeným LDL-C a zvýšeným CRP (studie JUPITER – Justification for the Use of Statins in Primary Prevention: an Intervention Trial Evaluating Rosuvastatin, snížení RR CMP o 48 %, p = 0,002) [28]. Pro snižování RR první ischemické CMP statiny u pacientů s ICHS máme více údajů (tab. 2). Cílové hodnoty lipidogramu pro prevenci CMP jsou shrnuty v odborných doporučených a jsou stejné jako pro ostatní aterosklerotické vaskulární nemoci [3].
![Studie se statiny u pacientů s ICHS – vliv na incidenci ischemických CMP. Upraveno dle [29]](https://www.prelekara.sk/media/cache/resolve/media_object_image_small/media/image/9417597a37c0b442b58973ec3bc23239.png)
Sledování úspěšnosti intervence hypercholesterolemie
Hlavním cílem mezinárodních studií EUROASPIRE (European Action on Secondary and Primary Prevention by Intervention to Reduce Events – EA) bylo zjistit úroveň implementace předcházejících evropských doporučení pro prevenci KVO. Česká centra v Plzni a v Praze se zúčastnila všech čtyř doposud provedených studií EA.
První studie EA probíhala v letech 1995–1996 v devíti zemích Evropy. Druhá studie EA probíhala v letech 1999–2000 v 15 zemích Evropy. Obě tyto nezávislé studie ukázaly výskyt ovlivnitelných rizikových faktorů u nemocných se stabilní ICHS ve všech zúčastněných evropských zemích. Bohužel většina rizikových faktorů nedosahovala doporučovaných cílů u všech nemocných. Třetí studie EA se uskutečnila v letech 2006–2007 již ve 22 evropských zemích; výsledky ukázaly, že byť byli muži i ženy léčeni podobně, ženy méně často dosahovaly cílových hodnot LDL-C (a také krevního tlaku a glykovaného hemoglobinu) než muži. Tento rozdíl se nezmenšil mezi léty 1994–2007. Bylo prokázáno, že životní styl je důležitý nejen v primární prevenci KVO, ale i v sekundární prevenci, a to dokonce od prvních měsíců po akutní koronární příhodě. Ve studiích EA byl zjištěn nežádoucí trend životních návyků zejména u mladých žen – více kouřily, vzrůstala prevalence obezity včetně centrální a diabetes mellitus [30]. Výsledky studií EA byly samotnými autory a koordinátory komentovány jako velké zklamání; přestože existovala doporučení založená na medicíně založené na důkazech, jejich implementace do rutinní klinické praxe byla nedostatečná.
Do studií EA se zapojovalo stále více evropských zemí; EA IV se prováděla v letech 2012–2013 již ve 25 zemích Evropy. Při porovnání kontroly standardních rizikových faktorů ve všech 4 českých vzorcích zařazených do studií EA I–IV zjišťujeme, že se zlepšila preskripce doporučené farmakoterapie – konkrétně u statinů vzrostla více než 12krát (z 7,3 % na 93,3 %) [31]. Prevalence hypercholesterolemie významně klesla z 87 % na 39 %. Celková 10letá mortalita se statisticky významně snížila mezi roky 1995 a 1999 z 28 % na 18 %. Vývoj hladiny LDL-C je prezentován v tab. 3, přičemž za zvýšenou hladinu byla považována ve studii EA I hladina celkového cholesterolu ≥ 5 mmol/l, v EA II LDL-cholesterolu ≥ 3 mmol/ a v EA III a IV LDL ≥ 2,5 mmol/l. Výsledky studií EA ukazují, že v České republice i celé Evropě je ještě velký prostor pro implementaci preventivních opatření u pacientů s KVO.

Nedostatečná farmakoterapie hypercholesterolemie statiny
V Česku je nejčastější předepisovanou dávkou statinu 20 mg, a to v primární i sekundární prevenci ICHS. Jedná se přitom o jakýkoliv statin, tzn., v této dávce jsou předepisovány statiny s různou účinností. Např. účinnost 20 mg rosuvastatinu odpovídá 40 mg atorvastatinu, ale 20 mg simvastatinu je dávka velmi malá a slabá. Důvodem jsou obavy z možných nežádoucích účinků. Poddávkování statinů ale incidenci nežádoucích účinků neřeší. Pokud má již pacient v anamnéze intoleranci statinu, je třeba zvolit méně účinný statin a titrovat dávku dle tolerance. U lehčích forem hypercholesterolemie je vhodné zahajovat léčbu nižšími dávkami statinů, protože zavedení zejména rosuvastatinu ve vyšších dávkách přináší častěji nežádoucí účinky. Je třeba se vyhnout tomu, aby byla pacientovi stanovena diagnóza statinové intolerance, aniž by se vyzkoušela jeho tolerance k nižším dávkám méně potentních statinů.
Dalším problémem je krom špatné adherence k léčbě i dlouhodobá perzistence, protože hyperlipidemie je chronická a asymptomatická. Léčba hyperlipidemie je celoživotní a nemocní si často léky vysazují podle svých úvah. Nejhorší kompliance je právě k hypolipidemické léčbě. V metaanalýze dostupných studií bylo prokázáno, že většina pacientů léčbu statiny vysazuje v průběhu 1. roku [32].
Nové trendy léčby hypercholesterolemie
„LDL hypotéza“ se stala již „LDL principem“. Na základě výsledků intervenčních studií se stále snižují cílové hladiny LDL-C [3]. Hodnotu T-C již neuvádíme v odborných doporučeních jako cílovou. U stále vyššího počtu pacientů je k dosažení cílových hladin lipidogramu potřeba farmakoterapie zejména statiny, ale i účinnějšími hypolipidemiky a jejich kombinacemi.
Nutraceutika
U pacientů s nízkým a středním KV rizikem mohou být dle současných odborných doporučení užita nutraceutika – např. kombinace extraktu z červené fermentované rýže (monakolin účinkuje jako statin), berberinu, polikosanolu, astaxantinu, koenzymu Q10 a kyseliny listové. Léčba touto kombinací nutraceutik vedla v 8týdenním sledování ke statisticky významnému snížení hladiny T-C (o 12,8 %) a LDL-C (o 21,1 %) srovnatelné s účinkem nízké dávky pravastatinu (-16 %, resp.-22,6 %). Podávání nutraceutik zvýšilo také hladinu HDL-C o 4,8 % [32].
Inhibitory PCSK9
Inhibitory PCSK9 (proprotein konvertáza subtilysin-kexin typu 9) přinášení zcela novou perspektivu v léčbě hypercholesterolemie. PCSK9 je protein, který přímo ovlivňuje degradaci a následnou recyklaci LDL receptoru na jaterní buňce. Když budeme inhibovat PCSK9, snížíme koncentraci LDL-C stimulováním schopnosti jaterní tkáně vychytávat jej z krve. Léčba PCSK9 inhibitory přináší dosažení velmi nízkých hodnot LDL-C, které není možné dosáhnout ostatní dostupnou farmakoterapií. V Evropě jsou nově registrovány 2 inhibitory PCSK9 (evolokumab a alirokumab). Aplikace probíhá subkutánně 1–2krát měsíčně. Slibné je zlepšení léčby zvláště u pacientů s těžkou hypercholesterolemií, kteří navíc netolerují současná hypolipidemika. Zajímavé je, že stále ještě nebyla objevena a doporučena dolní hranice pro hladinu LDL-C, pod kterou již není přínosné jej snižovat. Potvrzují to i data z evolokumabové studie FOURIER (Further Cardiovascular Outcomes Research With PCSK9 Inhibition in Subjects With Elevated Risk): medián hladiny LDL-C u aktivně léčených byl pacientů 0,77 mmol/l, tzn. o 59 % nižší v porovnání s placebem [34]. Do studie byli zařazeni pacienti s prodělanou aterotrombotickou příhodou a dalšími rizikovými faktory. Primární složený cíl tvořily úmrtí z KV příčin, infarkt myokardu, CMP, hospitalizace pro nestabilní anginu pectoris a koronární revaskularizace. Sekundární cíl tvořily úmrtí z KV příčin, infarkt myokardu a CMP. Medián trvání studie byl 2,2 roku. Primární složený cíl se vyskytl u 9,8 % aktivně léčených a u 11,3 % v placebové větvi (HR 0,85; 95% CI 0,79–0,92; p < 0,001) a sekundární cíl u 5,9 % vs 7,4 % (HR 0,80; 95% CI 0,73–0,88; p < 0,001). Výsledky byly konzistentní napříč sledovanými skupinami, a to i pacientů se vstupní hodnotou LDL-C 1,9 mmol/l. Ve studii FOURIER vedla tedy léčba evolokumabem k významnému snížení hladin LDL-C a snížila riziko KV příhod. Studie FOURIER je první klinickou studií, v níž všichni aktivně léčení pacienti dosáhli cílové hladiny LDL-C. Výsledky studie tedy opět potvrdily „LDL princip“.
Závěr
I přes paradigma, že LDL-cholesterol je významným rizikovým faktorem kardiovaskulárních onemocnění a že tento rizikový faktor můžeme ovlivňovat režimovými opatřeními a farmakoterapií, zůstává mortalita na kardiovaskulární onemocnění vysoká. Ve vyspělých zemích západního světa je sice prevalence KVO nižší, ale i tak jsou nejčastější příčinou úmrtí. Tzv. reziduální kardiovaskulární riziko vytváří rezerva v léčbě hypercholesterolemie i v léčbě non-LDL dyslipidemií. Přestože v České republice došlo k poklesu mortality na KVO o 50 %, stále u nás na tato onemocnění umírá téměř polovina mužů i žen. I přes léčbu statiny v sekundární prevenci KVO jsou hodnoty lipidogramu u těchto pacientů neuspokojivé. Je třeba implementovat dostupná režimová i farmakologická opatření k ovlivnění všech rizikových faktorů KVO s cílem dosažení cílových hodnot dle aktuálně platných odborných doporučení a kromě hyperlipidemie intervenovat i ostatní rizikové faktory.
Podpořeno projektem institucionálního výzkumu MZČR – FNPI, 00669806.
MUDr. Barbora Nussbaumerová, Ph.D.
Centrum preventivní kardiologie II. interní kliniky LF UK a FN v Plzni
Doručeno do redakce 11. 11. 2017
Přijato po recenzi 5. 1. 2018
Sources
1. Framingham Heart Study. Dostupné z WWW: <http://www.framinghamheartstudy.org>.
2. Keys A, Blackburn H, Taylor H. Coronary heart disease in seven countries. Circulation 1970; 41(Suppl 4): 120–139; 154–161.
3. Catapano AL, Graham I, De Backer G et al. 2016 ESC/EAS Guidelines for the management of dyslipidaemias. The task force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS). Eur Heart J 2016; 37(39): 2999–3058. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehw272>.
4. Iso H, Jacobs DR, Wentworth D. [MRFIT Research Group]. Serum cholesterol levels and six-year mortality from stroke in 350 977 men screened for the multiple risk factor intervention trial. N Engl J Med 1989; 320(14): 904–910. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJM198904063201405>.
5. Reiniš Z, Pokorný J, Bazika V et al. Epidemiologie ischemické choroby srdce u zemědělské a průmyslové populace. Thomayerova sbírka. Svazek 476. Avicenum: Praha 1977.
6. Geizerová H. Multifaktoriální primárně preventivní studie srdečních infarktů a cévních mozkových příhod. Závěrečná zpráva 1. etapy ÚSP 17–335–328–02 HE - 8/6. IKEM: Praha 1980.
7. Škodová Z. Multifaktoriální primárně preventivní studie srdečních infarktů a cévních mozkových příhod. Závěrečná zpráva VÚ-ZP: 17–335–452/03–4/2. IKEM: Praha 1985.
8. Škodová Z, Piša Z, Hejl Z et al. Mezinarodni studie MONICA – první zkušenosti v ČSSR. Praktický lekař 1986; 66(18): 668–670.
9. Cífková R, Škodová Z, Bruthans J et al. Longitudinal trends in major cardiovascular risk factors in the Czech population between 1985 and 2007/8. Czech MONICA and Czech post-MONICA. Atherosclerosis 2010; 211(2): 676–681. Dostupné z DOI: <http://dx.doi.org/10.1016/j.atherosclerosis.2010.04.007>.
10. Cífková R, Škodová Z, Bruthans J et al. Longitudinal trends in cardiovascular mortality and blood pressure levels, prevalence, awareness, treatment, and control of hypertension in the Czech population from 1985 to 2007/2008. J Hypertens 2010; 28(11): 2196–2203. Dostupné z DOI: <http://dx.doi.org/10.1097/HJH.0b013e32833d4451>.
11. Nissinen A, Tuomilehto J, Puska P. From pilot project to national implementation: experiences from the North Karelia Project. Scand J Prim Health Care Suppl 1988; 1 : 49–56.
12. Stožický F, Slabý P, Voleníková L. Serum lipid and apolipoprotein levels in children. Česk Pediatr 1983; 38(11): 646–649.
13. Šimon J, Karlíček V, Rosolová H. Závěrečná zpráva Výzkumného projektu P-12–333–810: Výzkum komplexní léčebné a preventivní péče o organizovanou (průmyslovou) populaci. Plzeň 1990.
14. Rosolová H, Šimon J, Šefrna F. Impact of cardiovascular risk factors on morbidity and mortality in Czech middle-aged men: Pilsen Interventional Longitudinal Study (PILS). Cardiology 1994; 85(1): 61–68.
15. Rosolová H, Krejsová L, Emmer J et al. Vliv věku a vzdělání na rizikový profil mužů a žen v průmyslové populaci (PILS II). Vnitř Lék 1991; 37(7–8): 678–685.
16. The Lipid Research Clinics Coronary Primary Prevention Trial results. I. Reduction in incidence of coronary heart disease. JAMA 1984; 251(3): 351–364.
17. SPC Vasosan. Dostupné z WWW: <http://www.sukl.cz>.
18. [Heart Protection Study Collaborative Group]. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 20 536 high-risk individuals: a randomised placebo controlled trial. Lancet 2002; 360(9326): 7–22.
19. Jukema JW, Bruschke AVG, van Boven AJ et al. Effects of lipid lowering by pravastatin on progression and regression of coronary artery disease in symptomatic men with normal to moderately elevated serum cholesterol levels. The Regression Growth Evaluation Statin Study (REGRESS). Circulation 1995; 91(10): 2528–2540.
20. Nissen S, Tuzcu E, Schoenhagen P et al. Effect of Intensive Compared with Moderate Lipid-Lowering Therapy on Progression of Coronary Atherosclerosis: A randomized Controlled Trial (REVERSAL). JAMA 2004; 291(9): 1071–1080.
21. Ballantyne CM, Raichlen JS, Nicholls SJ et al. [ASTEROID Investigators]. Effect of rosuvastatin therapy on coronary artery stenoses assessed by quantitative coronary angiography: a study to evaluate the effect of rosuvastatin on intravascular ultrasound derived coronary atheroma burden. Circulation 2008; 117(19): 2458–2466. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.108.773747>.
22. Catapano A, Toth PP, Tomassini JE et al. The efficacy and safety of ezetimibe coadministered with statin therapy in various patient groups. Clin Lipidol 2013; 8(1): 13–41. Dostupné z DOI: <https://doi.org/10.2217/clp.12.88>.
23. Cannon CP, Blazing MA, Giugliano RP et al. [IMPROVE-IT Investigators]. Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes. Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes. N Engl J Med 2015; 372(25): 2387–2397. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1410489>.
24. [Prospective Studies Collaboration]. Cholesterol, diastolic blood pressure and stroke: 13,000 strokes in 450,000 people in 45 prospective cohorts. Lancet 1995; 346(8991–8992): 1647–1653.
25. [The stroke prevention by agresive reduction in cholesterol levels (SPARCL) investigators]. High-dose atorvastatin after stroke or transient ischemic attack. N Engl J Med 2006; 355(6): 549–559. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa061894>.
26. Sever P, Dahlöf B, Poulter N et al. Prevention of coronary and stroke events with atorvastatin in hypertensive patients who have average or lower - than - average cholesterol concentrations, in the Anglo-Scandinavian Cardiac Outcomes Trial-Lipid Lowering Arm (ASCOT - LLA): a multicentre randomised controlled trial. Lancet 2003; 361(9364): 1149–1158. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(03)12948–0>.
27. Colhoun HM, Thomason MJ, Mackness MI et al. Design of the Collaborative AtoRvastatin Diabetes Study (CARDS) in patients with type 2 diabetes. Diabet Med 2002; 19(3): 201–211.
28. Ridker P, Danielson E, Fonseca FAH et al. Rosuvastatin to prevent vascular events in men and women with elevated C-reactive protein. N Eng J Med 2008; 359(21): 2195–2207. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa0807646>.
29. Soška V. Prevence cévních mozkových příhod léčbou hypolipidemiky. Česk Slov Neurol 2010; 73/106(1): 20–25.
30. Kotseva K, Wood D, De Backer G et al. Cardiovascular prevention guidelines in daily practice: a comparison of EUROASPIRE I, II, and III surveys in eight European countries, Lancet 2009; 373(9667): 929–940. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(09)60330–5>.
31. Mayer O Jr, J. Bruthans K. Timoracká. [Czech EUROASPIRE I–IV investigators]. The changes in cardiovascular prevention practice between 1995 and 2012 in the Czech Republic. A comparison of EUROASPIRE I, II, III and IV study. Cor et Vasa 2014; 56(2): e91-e97. Dostupné z DOI: <https://doi.org/10.1016/j.crvasa.2014.01.008>,
32. Brookhart MA, Patrick AR, Schneeweiss S et al. Physician follow-up and provider continuity are associated with long-term medication adherence: a study of the dynamics of statin use. Arch Intern Med 2007; 167(8): 847–852. Dostupné z DOI: <http://dx.doi.org/10.1001/archinte.167.8.847>.
33. Ruscica M, Gomaraschi M, Mombelli G et al. Nutraceutical approach to moderate cardiometabolic risk: results of a randomized, double-blind and crossover study with Armolipid Plus. J Clin Lipidol 2014; 8(1): 61–68. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacl.2013.11.003>.
34. Sabatine MS, Giugliano RP, Keech AC et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. N Engl J Med 2017; 376(18): 1713–1722. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1615664>.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2018 Issue 1
-
All articles in this issue
- Familial combined hyperlipidemia – the most common genetic dyslipidemia in population and in patients with premature atherothrombotic cardiovascular disease
- Epidemiology of hypercholesterolemia
- MedPed – the reality of familial hypercholesterolemia care at the biggest center
- The role of PCSK9-inhibitors and of lipoprotein apheresis in the treatment of homozygous and severe heterozygous familial hypercholesterolemia: A rivalry, or are things quite different?
- Cardiovascular risk in patients with rheumatic disease and its management
- Examination methods for coronary atherosclerosis regression with special focus on GLAGOV trial
- Effect of pulsatility on markers of vascular damage in patients with implanted continuous flow mechanical circulatory support
- Remarks on biomarkers of cardiovascular risk
- Long non-coding RNAs in the pathophysiology of atherosclerosis
- The current position of hydrochlorothiazide among thiazide and thiazide-like diuretics
- Diabetic dyslipidemia and microvascular complications of diabetes
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Familial combined hyperlipidemia – the most common genetic dyslipidemia in population and in patients with premature atherothrombotic cardiovascular disease
- Epidemiology of hypercholesterolemia
- Diabetic dyslipidemia and microvascular complications of diabetes
- The current position of hydrochlorothiazide among thiazide and thiazide-like diuretics
