Hemodynamicky významný perikardiální výpotek jako možný vzácný mimostřevní projev Crohnovy choroby
Authors:
Barbora Pipek- 1 3; Martin Pleva- 3 5; Petr Fojtík 1,3; Přemysl Falt 2
Authors‘ workplace:
Centrum péče o zažívací trakt, Nemocnice AGEL Ostrava Vítkovice, a. s.
1; II. interní klinika – gastroenterologická a geriatrická LF UP a FN Olomouc
2; Ostravská univerzita–, Lékařská fakulta, Ostrava
3; Interní oddělení–, vaskulární centrum, Nemocnice AGEL Ostrava Vítkovice, a. s.
4; Kardiologické oddělení, Nemocnice AGEL Třinec Podlesí, a. s.
5
Published in:
Vnitř Lék 2021; 67(2): 109-113
Category:
Case Reports
Overview
Crohnova choroba (CN) a ulcerózní kolitida (UC) patří do skupiny onemocnění s názvem idiopatické střevní záněty (IB – inflammatory bowel disease). IBD mají dosud ne zcela jasnou etiologii, bývají diagnostikovány převážně v mladším věku a v průměru u více než třetiny těchto pacientů se v průběhu let vyvinou mimostřevní projevy nemoci. K těm nejčastějším patří artropatie, oční a kožní manifestace zánětu, metabolická kostní choroba a hepatobiliární či urologické postižení. Terapie je obdobná jako léčba základního onemocnění a spočívá převážně v systémové imunosupresi. Perikardiální výpotek a perikarditida je raritním extraintestinálním projevem Crohnovy choroby či ulcerózní kolitidy. V diferenciální diagnostice nejasného perikardiálního postižení musíme taktéž zvažovat infekční etiologii, nežádoucí účinky podávané léčby či systémové onemocnění.
Klíčová slova:
Crohnova choroba – mimostřevní projevy IBD – perikardiální výpotek – biologická léčba – adalimumab – hepatitida C
Úvod
Crohnova choroba je autoimunitní onemocnění postihující především mladé dospělé v produktivním věku a je asociována s širokým spektrem obtíží včetně mimostřevních projevů, které se objevují u více než třetiny pacientů a značně zhoršují kvalitu života nemocných. Asociace s aktivitou zánětu nemusí být mnohdy zřejmá. Dominuje postižení kloubů ve formě axiální a periferní spondylartropatie I. a II. typu, kožní projevy s typickými zástupci pyoderma gangrenosum, erythema nodosum, vzácněji pak Sweetův syndrom. Při očním postižení se nejčastěji setkáváme s episkleritidou, konjunktivitidou a uveitidou. Zástupcem postižení jater je primární sklerotizující cholangitida (1). Onemocnění perikardu charakterizované perikarditidou či perikardiálním výpotkem je velmi vzácným až raritním extraintestinálním projevem IBD. Fyziologicky se v perikardu vyskytuje do 50 ml tekutiny a případné zmnožení perikaridálního výpotku může mít hemodynamický dopad v závislosti na jeho množství a rychlosti nárůstu. Výpotek může být způsoben řadou příčin, kdy nejčastěji dominují virové infekce (enteroviry, echoviry, parvoviry, HIV), méně často pak bakteriální (Mycobakterium tuberculosis) či mykotické (Candida albicans), dále pak nežádoucí účinky léků, systémové onemocnění pojiva, metabolické příčiny, nádorové stavy nebo traumata (2). V našem sdělení uvádíme kazuistiku mladé ženy s náhodně zjištěným hemodynamicky významným výpotkem jako mimostřevním projevem IBD.
Kazuistika
Prezentujeme kazuistiku aktuálně 26leté pacientky léčené pro Crohnovou chorobu s postižením tračníku a terminálního ilea od dětského věku, která byla převzata do dispenzarizace gastroenterologické ambulance pro dospělé v říjnu roku 2012. V době první návštěvy byla pacientka 3 měsíce po předčasném porodu prvního dítěte bez klinických potíží i při svévolném neužívání azathioprinu a aminosalicylátů indikovaných pediatrem. Následující roky pacientka na kontroly nedocházela.
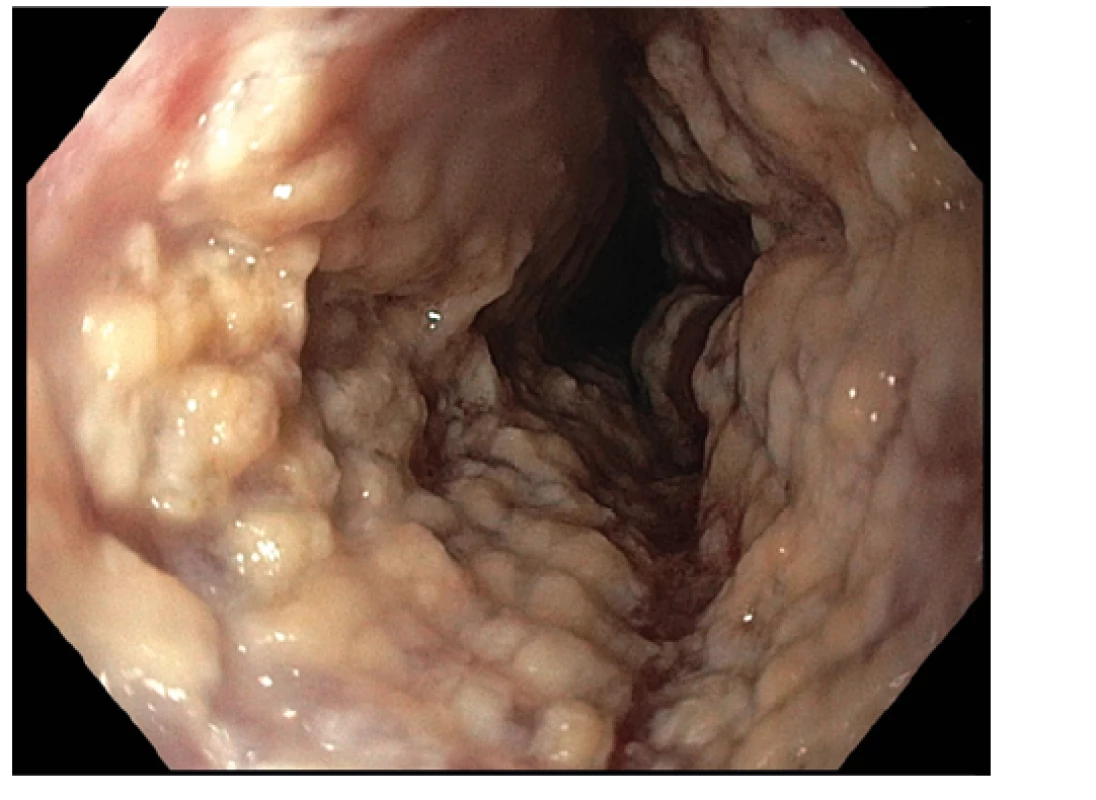
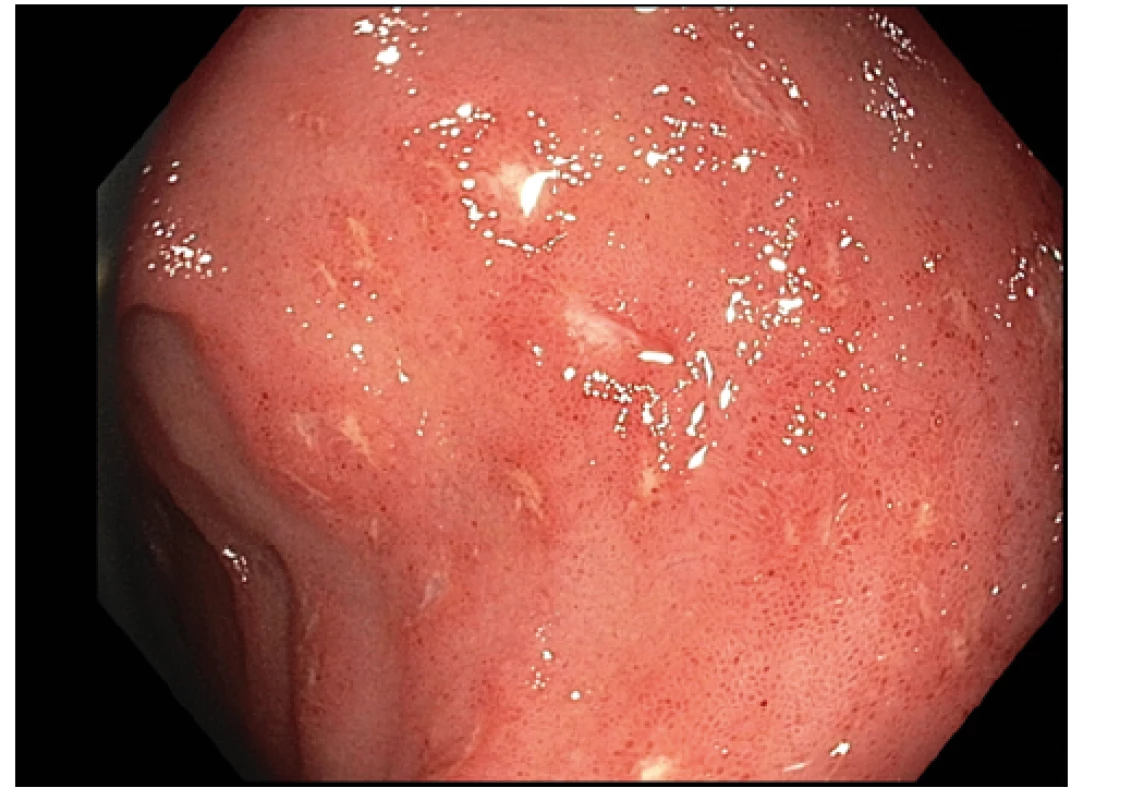
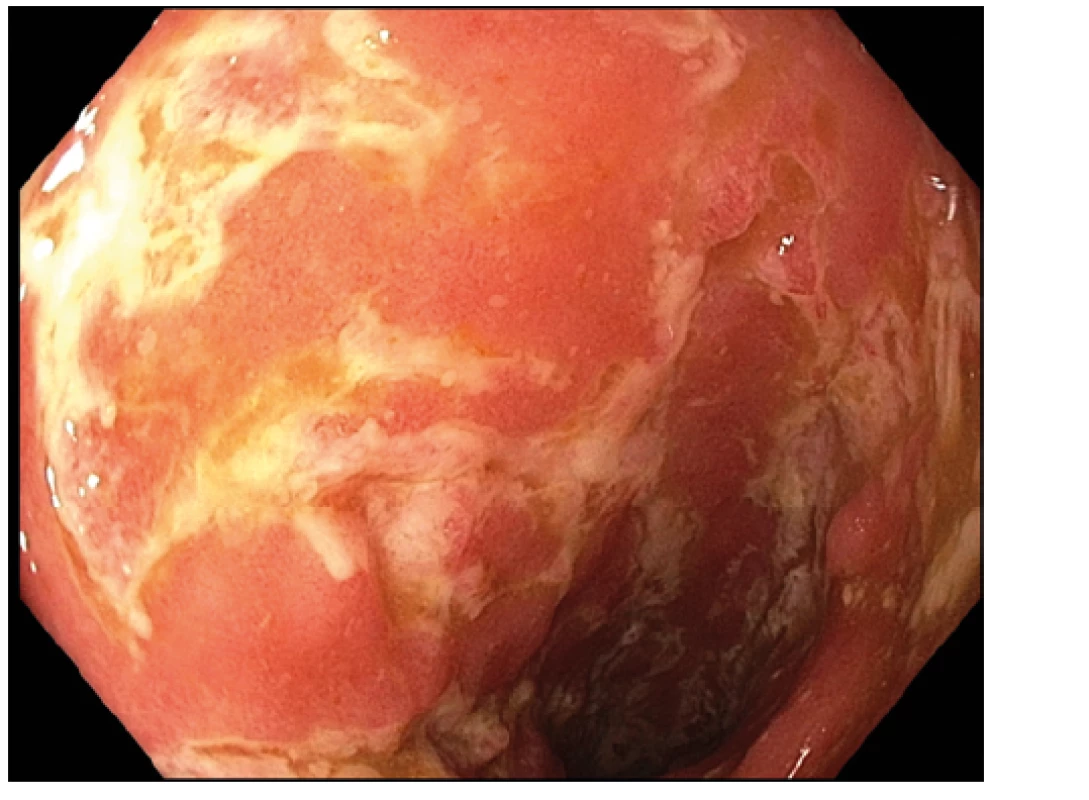
V roce 2019 přichází k akutnímu ošetření do spádového nemocničního zařízení pro zhoršení stavu, průjmy a teploty. Vstupně bylo provedeno sonografické vyšetření břicha a střevní stěny, které prokázalo známky levostranné kolitidy a terminální ileitidy, laboratorně CRP 106 g/l, celkové leukocyty 11,8 × 109/l, hemoglobin 126 g/l a trombocyty 706 × 109/l. Kultivace stolice byla negativní včetně vyšetření na clostridiový toxin a antigen. Při koloskopickém vyšetření byla popisována pankolitida s vředy od rekta do sigmatu a postižení terminálního ilea délky minimálně 15 cm taktéž se známkami zánětu vysoké aktivity s vředovými lézemi a erozemi. Pacientka byla indikována k léčbě systémovými kortikosteroidy v dávce 1 mg/kg s velmi dobrou klinickou odezvou a zlepšením celkového stavu. Velmi negativně však vnímala četné nežádoucí účinky léčby, jako přírůstek na váze, kožní strie a nespavost, které se ale s detrahující dávkou kortikoidů mírnily. Vzhledem k intoleranci výše uvedené léčby byla zvažována imunosupresivní terapie azathioprinem, se kterou již pacientka souhlasila. Od počátku užívání byl však azathioprin velmi špatně snášen, nemocná udávala trvalé bolesti v horní polovině břicha, nauzeu a v kontrolních odběrech zachycena leukopenie vedla k definitivnímu vysazení výše uvedené medikace. Pacientka poté pravidelně docházela na kontroly, plně spolupracovala a s odstupem 3 měsíců opět přichází s klin. obrazem relabujícího zánětu a progredující dysfagie. Bylo provedeno gastroskopické vyšetření s nálezem výrazné mykotické ezofagitidy, která byla zaléčena perorálním antimykotikem s dobrým efektem (Obr. 1). Koloskopicky jsme viděli známky těžké aktivity Crohnovy choroby v tračníku a terminálním ileu (Obr. 2, 3) a vzhledem k předchozím nežádoucím účinkům kortikoterapie a intoleranci azathioprinu jsme pacientku indikovali k biologické léčbě. V rámci standardního vyšetření před podáním biologické léčby byla neočekávaně diagnostikována chronická virová hepatitida typu C (genotyp 3a s pozitivní viremií) s nutností přeléčení přímo působícími antivirotiky (13. 11. 2019–7. 1. 2020). Od února 2020 nám bylo následně umožněno podat biologickou léčbu. Vzhledem k chabému perifernímu cévnímu přístupu a preferencím nemocné jsme zvolili biologikum adalimumab s možností subkutánního podání ve standardním indukčním režimu (160-80-40 mg s.c. ve 14denním intervalu) a následnou udržovací léčbu v dávce 40 mg s.c. každé 2 týdny. Medikaci pacientka tolerovala velmi dobře a došlo k rozvoji klinické, laboratorní a sonografické remise onemocnění.
Od července 2020 pacientka udávala zhoršení průjmů a teploty. Vyšetřením stolice prokazujeme clostridiovou kolitidu (pozitivní antigen i toxin stanovený metodou enzymové membránové imunoanalýzy, výsledek byl následně potvrzen i kultivací). Podávání biologické léčby jsme přerušili a nastolili léčbu perorálním vankomycinem (125 mg co 6 hodin na 10 dní). I přes zaléčení střevního infektu nadále přetrvávaly subfebrilie a systémové známky zánětu. Fyzikálním vyšetřením nebyla nalezena patologie. USG břicha a střeva bylo s přiměřeným nálezem, pro definitivní vyloučení mezikličkového abscesu bylo provedeno i CT břicha. RTG plic i vyšetření moči chemicky, sedimentem i kultivací taktéž neukazovalo závažnou atypii. Sérologické vyšetření na infekční hepatitidy (včetně HCV s přetrvávající negativní viremií), HIV, EBV, cytomegalovirus, adenoviry, viry chřipky, parvoviry, chlamydie, viry Varicella zoster a herpetické viry, Borelie, Mycoplazma, Candida albicans bylo negativní a opakované odběry hemokultur při febriliích nevykazovaly systémovou mikrobiální infekci. STD (sexual transfer disease) včetně stěrů z urogenitální oblasti byly negativní. Pro bolesti zad indikována magnetická rezonance bederní oblasti bez nálezu spondylodiscitidy či jiné patologie. V širší diferenciální diagnostice s cílem vyloučit infekční endokarditidu bylo provedeno transthorakální echo vyšetření srdce, kde nebyly nalezeny vegetace na chlopních či endokardu, ale překvapivě zde byl diagnostikován velký perikardiální výpotek. Pacientka neměla klinické příznaky, které by svědčily pro akutní perikarditidu – byla bez bolestí na hrudi a EKG křivka byla bez typických změn. Prostý snímek srdce a plic neprokazoval rozšíření srdečního stínu. Při pátrání po etiologii perikardiální tekutiny byl vyjma infekční příčiny zvažován i eventuální raritní projev serozitidy při možném adalimumabem indukovaném lupus syndromu (tzv. ATIL, anti‑TNF induced lupus) nebo jiný nežádoucí účinek adalimumabu. Ten byl naposledy podán před deseti týdny, jeho biologický poločas je 10–14 dní a nejevilo se tedy pravděpodobné, že by s takovým odstupem od vysazení mohl způsobit nežádoucí účinky (3). Antinukleární (ANA) i protilátky pro extrahovaným nukleárním antigenem (anti‑ENA) byly negativní a nejednalo se o postižení kůže, ledvin či CNS, které je pro manifestaci ATIL typičtější.
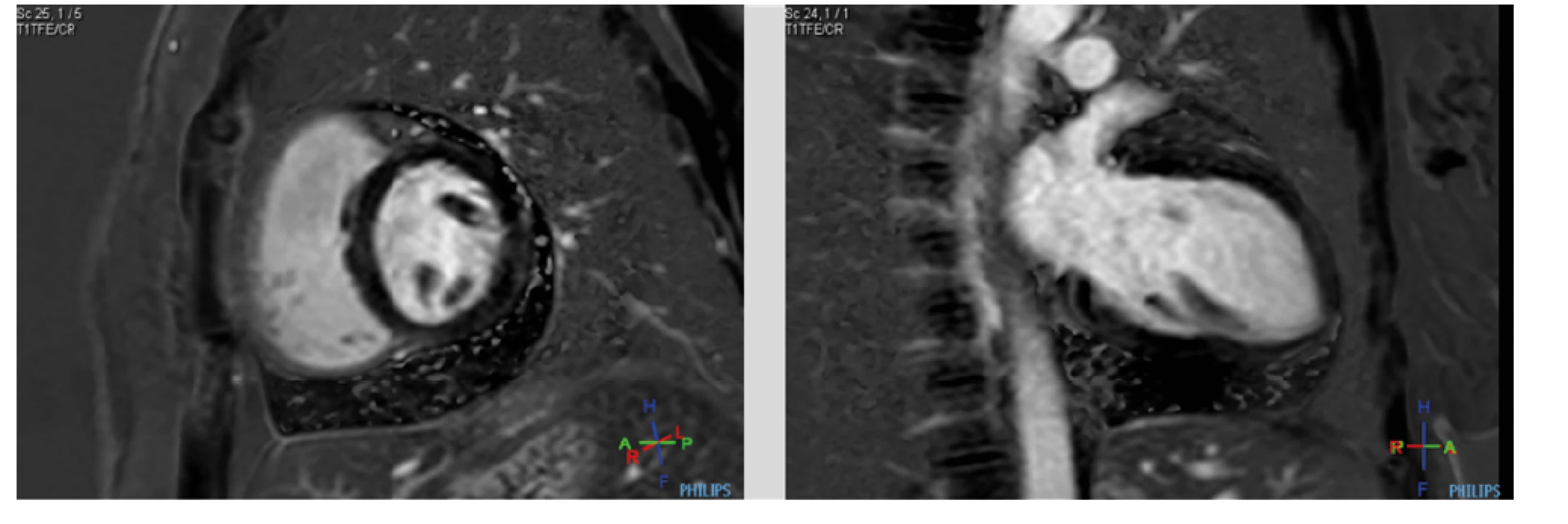
K vyloučení akutní perikarditidy byla indikována magnetická rezonance srdce (MRI srdce), která potvrdila cirkulární perikardiální výpotek s maximem pod spodní stěnou levé komory, kde dosahovala separace perikardiálních listů 26 mm (Obr. 4 a, b). V důsledku počínající oběhové nestability s projevy hypotenze a tachykardie bylo vyšetření provedeno vstupně bez podání kontrastní látky ve zkráceném režimu. Poté došlo k oběhové kompenzaci pacientky na podkladě intenzivní rehydratace a započaté terapii kortikoidy. Punkce perikardiálního výpotku byla vstupně zvažována hlavně s cílem přiblížit se etiologii výpotku. Vzhledem k promtní reakci na kortikosteroidní léčbu a časné redukci objemu perikardiální tekutiny jsme od evakuační punkce upustili.
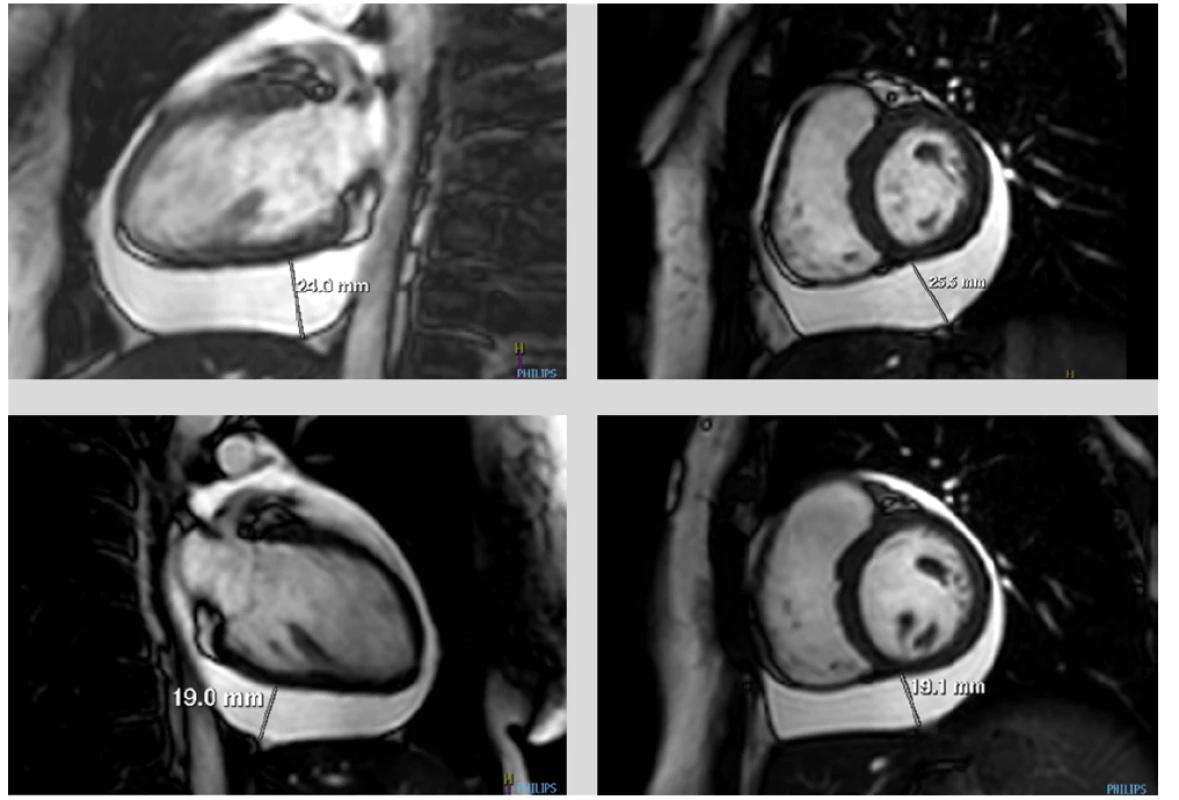
K systémové terapii kortikosteroidy jsme se přiklonili s ohledem na anamnézu Crohnovy choroby a možnost mimostřevního projevu tohoto onemocnění. Časné zlepšení klinického stavu pacientky umožnilo dokončit MRI srdce již do 48 hodin od prvovyšetření. I během takto krátké doby byl patrný jednoznačný efekt kortikoterapie s regresí perikardiálního výpotku (Obr. 4 c, d). Nález ale neprokázal edematózní ztluštění perikardiálních listů ani jejich pozdní sycení gadoliniovou kontrastní látkou, které by svědčilo pro akutní perikarditidu (Obr. 5 a, b). I přesto jsme s ohledem na jednoznačný a rychlý efekt léčby v kortikoterapii pokračovali. Následné echokardiografické kontroly pak dokazovaly další vymizení výpotku při postupné detrakci kortikoidů a došlo rovněž k normalizaci laboratorního nálezu (CRP 0.9 mg/l, WBC 8.1 g/l). Pacientka neudávala nové obtíže, cítila se dobře a byla indikována k časné kontrole v gastroenterologické ambulanci s laboratorními odběry, koloskopickému vyšetření a následně k rozhodnutí o typu udržovací léčby.
Diskuze
V naší kazuistice se věnujeme netypickému případu hemodynamicky významného perikardiálního výpotku jako možného extraintestinálního projevu idiopatického střevního zánětu.
Kardiální manifestace IBD je v literatuře popisována velmi zřídka, a to převážně ve formě kazuistických sdělení. Prevalence akutní perikarditidy jako mimostřevního projevu u IBD v dospělém věku je udávána 0,23 % a nebyla prokázána jasná asociace s aktivitou střevního zánětu (4, 5). Tíže obtíží mnohdy osciluje od sotva patrného výpotku až k těžkým život ohrožujícím srdečním tamponádám. Patofyziologicky se pravděpodobně jedná o serozitidu vyplývající ze systémové zánětlivé odpovědi, a jak již bylo uvedeno výše, mnohdy je diagnóza stanovena per exclusionem. Quazi prezentuje 2 kazuistiky periakardiálního postižení u pacientů s ulcerozní kolitidou, obě s velmi dobrou odpovědí na léčbu systémovými kortikosteroidy. Gils pak popisuje rekurentní výskyt perikarditidy po vysazení kortikoidní léčby u mladé dívky léčené s IBD (6, 7). Ve výše uvedených kazuistických sdělení ale došlo k diagnostice perikarditidy na podkladě klinické manifestace onemocnění – bolesti na hrudi doprovázené EKG změnami. V našem případě byl perikadiální výpotek náhodným nálezem při echokardiografickém vyšetření a dominantními příznaky onemocnění byly febrilie spojené s elevací zánětlivých markerů (při absenci jiné etiologie tohoto laboratorního nálezu). S ohledem na jednoznačný efekt kortikoterapie předpokládáme zánětlivou etiologii perikardiálního výpotku v rámci tohoto autoinflamatorního onemocnění i přes chybějící MR známky probíhající akutní perikarditidy.
V diferenciální diagnostice perikardiálního výpotku a perikarditidy musíme primárně odlišovat infekční etiologii zánětu a nežádoucí účinky podávaných léků. Další příčiny, jako systémové onemocnění, traumata či idiopatické postižení, jsou poměrně vzácné (5). Nejvíce dat máme k dispozici pro perikarditidy asociované s léčbou mesalazinem, méně pak s azathioprinem či biologickou léčbou infliximabem či adalimumabem. Všechna výše uvedená léčiva však musíme akceptovat jako medikaci, která potenciálně evokuje rozvoj tohoto postižení. Park a Waite ve svých sděleních popisují mesalazinem indukované postižení s dobrým efektem vysazení vyvolávající medikace a následné kortikoidní léčby (4, 8).
Naše pacientka neužívala aminosaliciláty od roku 2012, azathioprin jen krátkodobě v první polovině roku 2020 a biologická léčba adalimumabem byla nemocné vysazena z důvodů střevní clostridiové infekce více než 2 měsíce přes stanovením diagnózy. V diferenciální diagnostice etiologie výpotku jsme však zvažovali i tento faktor. Vzhledem ke krátkému biologickému poločasu adalimumabu (10–14 dní) je tato verze nepravděpodobná. V literatuře je taktéž popisován časný nález perikardiálního postižení nedlouho po infuzi či s.c. podání biologika či přímo v asociaci s aplikací (3, 9). Mirza ve své kazuistice zmiňuje asociaci perikardiálního postižení s anti‑TNF léčbou vyvolaným lupusem (10).
Závěr
Prezentovaná kazuistika nás seznámila s hemodynamicky významným perikardiálním výpotkem jako možným netypickým mimostřevním projevem Crohnovy choroby u mladé ženy. Dominantním klinickým projevem nebyly bolest na hrudi, dušnost či EKG změny, ale recidivující febrilie a elevace zánětlivých markerů. Systémová léčba kortikosteroidy vedla velmi časně k vymizení výpotku, k normalizaci laboratorních nálezu a zlepšení klinického stavu pacientky.
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Barbora Pipek
Centrum peče o zaživaci trakt, Nemocnice AGEL Ostrava Vitkovice, a. s.
Zálužanského 1 192/15
70 300 Ostrava-Vítkovice
Cit. zkr: Vnitř Lék 2021; 67(2): 110–114
Článek přijat redakcí: 15. 12. 2020
Článek přijat po recenzích: 7. 3. 2021
Sources
1. Zbořil V a kol. Idiopatické střevní záněty. Praha: Mladá fronta, 2018.
2. Zemánek D. Perikarditidy. Kardiol Rev Int Med 2015; 17(4): 300–306.
3. Mayer O et al. Adalimumab. Remedia 2005;15 (1): 3–9.
4. Park EH, Kim BJ, Huh JK et al. Recurrent mesalazine ‑ induced myopericarditis in a patient with ulcerative colitis. J. Cardiovasc. Ultrasound 2012; 20 : 154–156.
5. Fardman A, Charron P, Imazio M et al. European guidelines on pericardial diseases: A focused review of novel aspects. Curr. Cardiol. Rep. 2016; 18–46.
6. Qazi T, Christian KE, Farraye MD et al. Pericardial manifestations in inflammmatory bowel disease: A report of two cases. Crohn’s & Colitis 2019; 3(1): 28.
7. Van Gils AJM. Recurrent pericarditis as an extra ‑ intestinal manifestation of ulcerative colitis in a 14-year‑old girl. Clin Case Rep. 2018 Aug; 6(8): 1538–1542.
8. Waite RA, Malinovski JM. Possible mesalamin ‑ induced pericarditis: case report and literature review. Pharmacotherapy 2002; 22 : 391–394
9. Devasahayam J, Pillai U, Lacasse A. A rare case of pericarditis, complication of infliximab treatment for Crohn’s disease. Journal of Crohn’s and Colitis 2012; 6 (6): 730–731.
10. Mirza M et al. Pericardial Effusion due to Infliximab Therapy for Ulcerative Colitis. Case Reports in Gastrointestinal Medicine 2018. 1–3.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2021 Issue 2
-
All articles in this issue
- Imonoglobulin G4 asociované onemocnění v gastroenterologii
- Diagnostika a terapie chronické pankreatitidy dle UEG guidelines
- Mimostřevní komplikace idiopatických střevních zánětů
- Aktuální pohled na možnosti diagnostiky a léčby diabetu typu LADA
- Glukagon v léčbě hypoglykemie – novinky
- Hemodynamicky významný perikardiální výpotek jako možný vzácný mimostřevní projev Crohnovy choroby
- Masivní plicní embolie s rozsáhlým trombem ve foramen ovale patens – hrozící paradoxní embolie
- Perindopril – dlouholetá jistota v léčbě hypertenze
- Hlavní téma: gastroenterologie
-
Jak prodloužit životy našich pacientů ve zdraví?
A lze to?
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
- Diagnostika a terapie chronické pankreatitidy dle UEG guidelines
- Glukagon v léčbě hypoglykemie – novinky
- Perindopril – dlouholetá jistota v léčbě hypertenze
- Mimostřevní komplikace idiopatických střevních zánětů
