Budeme léčit srdeční selhání podle plazmatické koncentrace natriuretických peptidů?
Will the therapy of chronic heart failure be guided by plasma levels of natriuretic peptides?
Natriuretic peptides, especially BNP and NT-proBNP became useful tool for both, the diagnostics and the estimation of prognosis in chronic heart failure. As the plasma levels of natriuretic peptides copy changes in clinical status, an attractive hypothesis was formed saying that BNP/NT-proBNP guided therapy could have better clinical outcomes than therapy guided by patients’ clinical status (symptoms). In past few years this hypothesis was tested in several randomized controlled clinical trials (STARS-BNP, TIME-CHF, PRIMA). However, results of these trials are very controversial.
There are preliminary results of clinical trial OPTIMA referred in this paper, too. This one-centre study was performed at the authors’ institution. Altogether 52 patients with chronic heart failure were randomized to one of the above mentioned treatment strategies. The rate of cardiovascular events was lower in the patients in whom the treatment was guided by BNP values compared to the patients in whom the treatment was guided by their clinical status. However, the difference was not statistically significant.
Key words:
BNP/NT-proBNP, chronic heart failure, BNP-guided treatment, OPTIMA study.
Authors:
J. Hradec; J. Krupička; T. Janota
Authors‘ workplace:
Univerzita Karlova v Praze, 1. lékařská fakulta, III. interní klinika VFN
Published in:
Čas. Lék. čes. 2009; 148: 383-388
Category:
Review Article
Overview
Natriuretické peptidy, zejména BNP a NT-proBNP, se staly velmi užitečným nástrojem pro diagnostiku a odhad prognózy chronického srdečního selhání. Protože plazmatické koncentrace natriuretických peptidů kopírují změny klinického stavu, vznikla lákavá hypotéza, že léčba nemocných s chronickým srdečním selháním řízená plazmatickými koncentracemi BNP/NT-proBNP by mohla mít lepší klinické výsledky než léčba řízená klinickým stavem (symptomy) nemocného. Tato hypotéza byla v posledních letech ověřována v několika randomizovaných kontrolovaných studiích (STARS-BNP, TIME-CHF, PRIMA). Výsledky těchto studií však jsou velmi kontroverzní.
V této práci jsou také referovány předběžné výsledky klinické studie OPTIMA, která probíhala jako unicentrická na pracovišti autorů. V této studii bylo randomizováno 52 nemocných s chronickým srdečním selháním k jedné z výše uvedených léčebných strategií. Při řízení léčby koncentracemi BNP byl nižší výskyt kardiovaskulárních příhod ve srovnání s léčbou řízenou podle klinického stavu, rozdíl ale nebyl statisticky významný.
Klíčová slova:
BNP/NT-proBNP, chronické srdeční selhání, léčba řízená BNP, studie OPTIMA.
Několik vzpomínek na začátek
Profesor Josef Charvát založil v roce 1945 III. interní kliniku jako pracoviště, kde se nad rámec všeobecné interny pěstovala především endokrinologie. Není divu, prof. Charvát byl zakladatelem tohoto interního podoboru u nás a jeho pracoviště se stalo jednak nositelem endokrinologického výzkumu, jednak se na něm soustřeďovali k vyšetření a byli pak dále ambulantně sledovaní nemocní s vzácnějšími endokrinopatiemi z celého tehdejšího Československa. Na klinice tak vznikly velké a dlouhodobě sledované soubory nemocných, zcela mimořádné nejenom v národním ale i mezinárodním měřítku. I profesor Jan Petrášek byl v první části své odborné kariéry na III. interní klinice endokrinologem, věnoval se klinickému a laboratornímu výzkumu feochromocytomu, napsal o tomto nádoru i monografii (1).
Já jsem nastoupil na III. interní kliniku v roce 1971 jako externista. Byl jsem v té době řádným aspirantem 2. ústavu lékařské chemie a biochemie tehdejší FVL UK v Praze. Vlastně i já jsem měl na začátku své odborné kariéry krátké „endokrinologické“ období. Moje dizertační práce totiž byla věnována melanocyty-stimulujícímu hormonu a jeho klinickému významu. V době, kdy jsem na III. internu nastoupil, zde však vznikal a velmi dynamicky se rozvíjel i další podobor interny – kardiologie. A právě prof. J. Petrášek měl na tom, že se kardiologie stala rychle druhým nosným oborem III. interní kliniky lví podíl. Založil na klinice jednu z prvních koronárních jednotek v zemi, podílel se na vzniku diferencované péče o kardiologické nemocné, spoluinicioval vznik katetrizační laboratoře a prozíravě vycítil, že se rodí nová důležitá vyšetřovací metoda a pořídil na kliniku jeden z prvních echokardiografických přístrojů. Vznikla tak jedna z prvních echokardiografických laboratoří v zemi. Hlavně se ale kolem něho soustředila malá skupina mladých a nadšených lékařů, které on, původně endokrinolog, nadchnul, přitáhl a nasměroval ke kardiologii. Jedním z nich jsem byl i já, a tak jsem zažil to, co mohu bez rozpaků nazvat „zlatou érou“ kardiologie na III. interní klinice.
Začátkem 70. let minulého století se nezdálo, že by toho endokrinologie a kardiologie měly příliš společného. Jak se ale později ukázalo, měly a mají toho společného mnoho. Nejprve jsme využili výjimečných možností, které nám úzká koexistence dvou oborů na klinice nabídla a s pomocí tehdy nové diagnostické metody – echokardiografie – jsme studovali kardiovaskulární projevy a komplikace celé řady endokrinopatií (např. 2, 3).
Ve druhé polovině 80. let pak začala nahrazovat hemodynamickou koncepci vzniku a progrese srdečního selhání koncepce neurohumorální. Léky inhibující dlouhodobou patologickou aktivaci neurohumorálních systémů, jako jsou inhibitory angiotenzin-konvertujícího enzymu a antagonisté aldosteronu, které inhibují reninový–angiotenzinový–aldosteronový systém (RAAS), nebo beta-blokátory, blokující systém sympatoadrenální (SAS), radikálně začaly měnit osud nemocných se srdečním selháním. Nejenom, že působily symptomaticky, jako do té doby používaná diuretika a digitalis, ale snížily také významně mortalitu a prodloužily nemocným život.
Konečně v roce 1981 se s definitivní platností ukázalo to, co výzkumníci již nějaký čas tušili, že srdce má nejenom mechanickou funkci čerpadla, ale je také endokrinním orgánem. Zjistilo se totiž, že sekreční granula v myokardu síní obsahují látku, která je tvořena přímo v myokardu a která má natriuretické a vazodilatační účinky (4). Tato látka byla nazvána atriální natriuretický peptid (faktor, hormon) – ANP. V roce 1983 byla popsána jeho chemická struktura (5). V roce 1988 pak byl z mozku prasete izolován natriuretický peptid B (6) a v roce 1990 natriuretický peptid C (7).
Co jsou natriuretické peptidy a k čemu slouží?
Natriuretické peptidy se tvoří v myokardu a uvolňují se z něho do krve jako reakce na zvýšené myokardiální napětí, ať již při objemovém, nebo tlakovém přetížení. ANP je uvolňován především z myokardu srdečních předsíní, BNP z myokardu srdečních komor. Oba tyto natriuretické peptidy si jsou podobné chemickou strukturou i fyziologickými funkcemi. Jsou klíčovými regulátory v homeostáze vylučování soli a vody a regulaci krevního tlaku. Plazmatické koncentrace natriuretických peptidů se zvyšují především při srdečním selhávání. Protože BNP je uvolňován především z myokardu srdečních komor, je přímějším markerem komorové (dys)funkce než ANP. BNP je v kardiomyocytech syntetizován jako prohormon, který se nazývá proBNP. Po stimulaci kardiomyocytů zvýšeným napětím myokardu je proBNP proteolyticky štěpen na biologicky neaktivní N-terminální část molekuly (NT-proBNP) a biologicky aktivní hormon BNP. Oba peptidy jsou uvolňovány do cirkulace. Biologický poločas BNP je 20 minut, NT-proBNP 60–120 minut (8). Celá řada klinických i epidemiologických studií ukázala, že plazmatické koncentrace obou peptidů, BNP i NT-proBNP, výrazně stoupají při dysfunkci levé komory, a to jak systolické, tak diastolické. Proto mohou být využity jako citlivé biochemické markery srdečního selhání i asymptomatické komorové dysfunkce (9, 10). Plazmatické koncentrace BNP a NT-proBNP spolu velmi dobře korelují a za fyziologické situace jsou přibližně stejné. Při dysfunkci levé komory a při srdečním selhání však koncentrace NT-proBNP stoupají exponenciálně na hodnoty až několikanásobně vyšší než BNP. Výhodou stanovení NT-proBNP je jeho delší biologický poločas a daleko větší stabilita, takže odebraný vzorek krve není nutné zpracovávat okamžitě nebo ho zmrazovat.
Natriuretické peptidy vzbudily velké naděje, že se stanou jednoduchým a spolehlivým biochemickým testem (jakousi krevní zkouškou) k průkazu či vyloučení diagnózy srdečního selhání (11). Protože je diagnostika srdečního selhání, zejména v jeho mírných formách, obtížná a naprosto nedostatečná, vzbudila vidina jejího zjednodušení a zpřesnění naprosto zaslouženou pozornost. Tyto naděje se však splnily jenom částečně. V roce 1997 sice byla v Lancetu publikována britská studie, která referovala, že v rámci primární péče identifikovalo stanovení NT-proBNP nemocné se srdečním selháním se senzitivitou 97% a specificitou 84% (12). Autoři této studie naznačili, že stanovení natriuretických peptidů by se mohlo stát takřka ideálním screeningovým testem pro srdeční selhání. Bohužel, taková přesnost nebyla v dalších podobně koncipovaných studiích potvrzena. Problémem je nastavení správné diskriminační hodnoty BNP nebo NT-proBNP. Plazmatické koncentrace natriuretických peptidů totiž stoupají s věkem, jsou výrazně vyšší u žen a navíc je ovlivňují i jiné faktory včetně extrakardiálních. Nejčastěji používané diskriminační hodnoty pro BNP a NT-proBNP jsou kolem 100 pg/ml. U starších zdravých žen jsou však často hodnoty obou peptidů vyšší než 100 pg/ml. Při posunu diskriminační hodnoty směrem nahoru klesá senzitivita pro správnou diagnózu dysfunkce levé komory a řada případů tak zůstává nerozpoznána. Při jejím posunu směrem dolů klesá zase velmi rychle specificita a přibývá falešně pozitivních diagnóz. Čím dál více je jasné, že nejcennější je vysoká negativní prediktivní hodnota stanovení natriuretických peptidů, která se pohybuje kolem 96 %. Znamená to, že normální hodnota BNP/NT-proBNP s vysokou pravděpodobností blížící se jistotě vylučuje srdeční selhání. Mnohonásobně zvýšená hodnota (několik set pg/ml pro BNP a několik tisíc pg/ml pro NT-proBNP) takřka jistě znamená srdeční selhání. Problémem zůstávají mírně zvýšené hodnoty natriuretických peptidů, které mohou signalizovat poruchu funkce levé komory, ale mohou být také způsobeny jinými vlivy včetně extrakardiálních (např. chronická renální insuficience aj.). V těchto případech zasluhuje nemocný podrobnější odborné vyšetření včetně objektivního posouzení funkce levé komory, např. echokardiograficky. Je také čím dál jasnější, že diskriminační hodnoty natriuretických peptidů pro vyloučení srdečního selhání nebo dysfunkce levé komory se musí lišit podle toho, zda jde o symptomatického nemocného, který navštíví svého praktického lékaře, nebo o nemocného s akutní dušností, přivezeného na oddělení akutního příjmu nemocnice.
U nemocného, který má symptomy vzbuzující podezření, že by se mohlo jednat o srdeční selhání a zatím není léčen, znamenají podle současného doporučení Evropské kardiologické společnosti plazmatické koncentrace BNP < 100 pg/ml nebo NT-proBNP < 400 pg/ml, že diagnóza srdečního selhání je velmi nepravděpodobná. Naopak, při plazmatických koncentracích BNP > 400 pg/ml nebo NT-proBNP > 2000 pg/ml je diagnóza srdečního selhání velmi pravděpodobná. V pásmu mezi těmito hodnotami, tedy při plazmatických koncentracích BNP 100–400 pg/ml a NT-proBNP 400 až 2000 pg/ml je diagnóza srdečního selhání nejistá a je potřeba provést další diagnostické testy (obr. 1) (13). Proti tomuto diagnostickému algoritmu lze mít nepochybně řadu výhrad. Má ale nesmírnou výhodu v jednoduchosti.
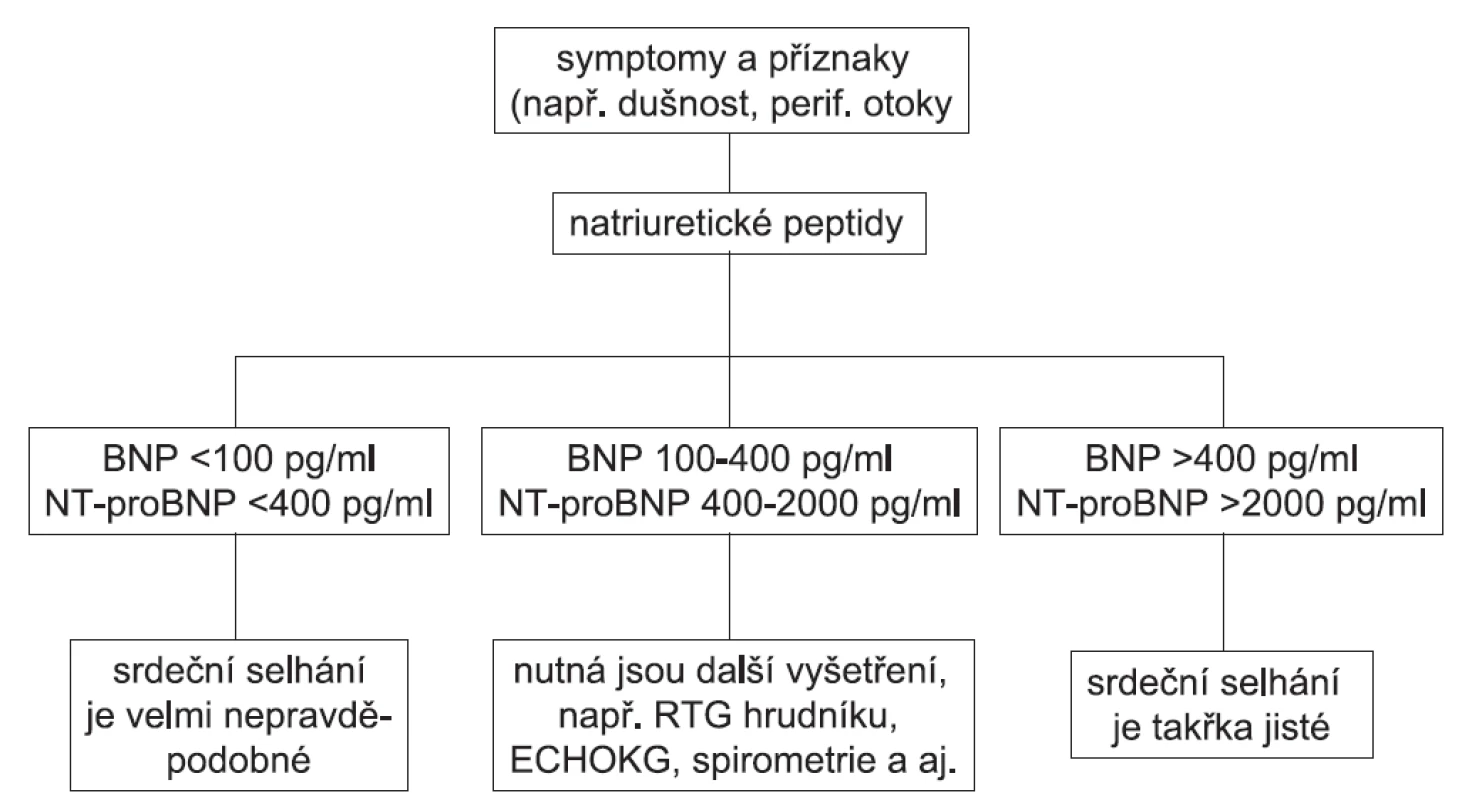
Ukázalo se, že natriuretické peptidy u chronického srdečního selhání jsou také mohutnými a nezávislými ukazateli prognózy nemocného. Čím vyšší je jejich plazmatická koncentrace, tím je prognóza nemocného horší. Hromadí se důkazy o tom, že větší předpovědní hodnotu jednoroční mortality má plazmatická koncentrace natriuretických peptidů po hemodynamické stabilizaci nemocného (14, 15). Hodnoty při propuštění z nemocnice korelují s prognózou nemocného lépe než hodnoty při přijetí, v situaci akutní hemodynamické dekompenzace. Stanovení natriuretických peptidů získává význam i v jiných oblastech kardiologie, než je diagnóza a odhad prognózy srdečního selhání. Jejich plazmatické hladiny stoupají také při akutních koronárních syndromech a jsou nezávislým prediktorem prognózy nemocných. U akutní plicní embolie předpovídají krátkodobou prognózu. Při zvýšení lze očekávat špatný průběh, delší hospitalizaci a vysoké riziko úmrtí. Při arteriální hypertenzi korelují plazmatické hladiny BNP/NT-proBNP s hmotností svaloviny levé komory (16) a zvýšené hladiny signalizují horší prognózu, a to i při antihypertenzní léčbě (17). U aortální stenózy a insuficience korelují hladiny BNP/NT-proBNP s hemodynamickou závažností vady a mají také prognostický význam. U nemocných s fibrilací síní predikuje koncentrace BNP úspěšnost elektrické kardioverze a její pokles po kardioverzi napovídá, zda a jak dlouho se udrží sinusový rytmus (18).
Stanou se natriuretické peptidy „glykovaným hemoglobinem“ léčby srdečního selhání?
S poznáním, že plazmatická koncentrace natriuretických peptidů představuje mohutnou prognostickou informaci a že změny této koncentrace odrážejí poměrně přesně změny klinického i hemodynamického stavu nemocných, vznikla velmi lákavá představa o využití monitorování natriuretických peptidů k řízení léčby srdečního selhání. Tedy uplatnit v léčbě srdečního selhání podobný koncept, jaký je v současnosti univerzálně přijímán například v léčbě hypertenze, dyslipidémií nebo diabetes mellitus. Léčit se snahou dosáhnout cílových/normálních hodnot krevního tlaku, LDL-cholesterolu nebo glykovaného hemoglobinu, v případě chronického srdečního selhání cílových/normálních hodnot BNP nebo NT‑proBNP. Nicméně, tento koncept má celou řadu úskalí. Nevíme, zda můžeme ovlivnit riziko, které natriuretické hormony předpovídají. Klinické studie u nemocných s chronickým srdečním selháním, ve kterých byly natriuretické peptidy stanovovány, nám jednoznačně ukazují, že lékaři obecně neléčí srdeční selhání dostatečně agresivně (19). Přestože agresivita léčby je u nemocných v klinických studiích nepochybně větší než v běžné klinické praxi, jsou i v nich léky, jejichž pospěšný účinek je doložen důkazy „evidence based medicíny“, podávány v podstatně nižších dávkách, než uvádějí aktuální doporučené postupy. Například z nedávno publikované analýzy farmakoterapie 500 českých nemocných s chronickým systolickým srdečním selháním ischemické etiologie, kteří byli zařazeni do studie CORONA, vyplývá, že průměrná denní dávka inhibitoru ACE ramiprilu byla jen 3,7 mg, enalaprilu 15,4 mg, lisinoprilu 8,6 mg. Průměrná denní dávka beta-blokátorů byla u bisoprololu jen 3,3 mg, karvedilolu 17,5 mg a metoprololu 74,2 mg (20). Znalost koncentrace natriuretických peptidů může být užitečnou připomínkou, že konkrétnímu nemocnému je potřeba podat více léků a/nebo jejich vyšší dávky.
Hypotéza, že léčba řízená hodnotami natriuretických peptidů je účinnější a bude mít lepší výsledky než léčba řízená klinickým stavem, tj. symptomy nemocného (nejčastěji dušností a/nebo periferními otoky), je sice lákavá a zní logicky, ale zůstává stále jenom neověřenou hypotézou. Ověřit ji je možné pouze kontrolovanými klinickými studiemi. Velké naděje vzbudila pilotní studie z Austrálie, ve které bylo randomizováno celkem 69 nemocných s nedávno dekompenzovaným srdečním selháním s ejekční frakcí ≤ 0,40 do dvou skupin s různými strategiemi léčby (21). V první skupině byla léčba vedena snahou snížit plazmatickou koncentraci NT-pro BNP na hodnotu < 200 pmol/l, ve druhé skupině pak klinickým stavem podle symptomů nemocného. U nemocných, u kterých byla léčba řízena podle NT-pro BNP, došlo k poklesu pravděpodobnosti úmrtí nebo hospitalizace pro zhoršení srdečního selhání (19 vs. 54 příhod). Tento pokles byl na hranici statistické významnosti (p = 0,049). Nemocní ve studii byli léčeni hlavně inhibitory ACE a diuretiky, beta-blokátory prakticky neužívali. Autoři výsledky této studie uzavřeli, že léčba srdečního selhání řízená podle hodnot NT-proBNP se zdá ve srovnání s léčbou řízenou klinickým stavem snižovat výskyt kardiovaskulárních příhod, a proto si tato léčebná strategie zaslouží další výzkum. Stejná skupina proto zahájila randomizovanou studii BATTLESCARRED s větším počtem nemocných, u kterých již beta-blokátory byly součástí standardní léčby srdečního selhání. V následujících letech byly sice dílčí výsledky z této studie prezentovány na různých kongresech, ale finální výsledky dosud publikovány nebyly.
Naděje, že léčba nemocných se srdečním selháním řízená natriuretickými peptidy povede k lepším klinickým výsledkům, výrazně posílily výsledky francouzské multicentrické randomizované studie STARS-BNP (22). Zařazeno do ní bylo 220 nemocných s chronickým systolickým srdečním selháním ve funkční třídě II–III podle NYHA, u kterých byla jejich ošetřujícím kardiologem léčba kombinací inhibitoru ACE, beta-blokátoru a diuretika považována za optimální. Tito nemocní byli randomizováni k léčbě podle současných doporučení (klinická skupina) nebo k léčbě, jejímž cílem bylo snížit plazmatickou koncentraci BNP < 100 pg/ml (BNP skupina). Primárním sledovaným ukazatelem byl součet úmrtí a hospitalizací ve vztahu k srdečnímu selhání. U nemocných v BNP skupině docházelo k častějším změnám v medikaci a dávkování všech tří základních skupin léků. Byla u nich také významně vyšší průměrná denní dávka inhibitorů ACE a beta-blokátorů (p < 0,05), ale nikoliv furosemidu než u nemocných v klinické skupině. Zvýšení denních dávek inhibitorů ACE i beta-blokátorů bylo nemocnými dobře tolerováno. Za průměrnou dobu sledování 15 měsíců dosáhla třetina nemocných v BNP skupině cílovou hodnotu plazmatické koncentrace BNP < 100 pg/ml. Výskyt primárního kombinovaného klinického ukazatele byl u nemocných, u kterých byla léčba řízená hladinami BNP, významně nižší než u nemocných léčených podle guidelines (24 % vs. 52 %; p < 0,001). Autoři se proto domnívali, že i u „optimálně“ léčených nemocných s chronickým srdečním selháním snižuje léčebná strategie řízená podle plazmatických koncentrací BNP riziko úmrtí na srdeční selhání a hospitalizací pro zhoršení srdečního selhání. Toto zlepšení prognózy by mělo být výsledkem vyššího dávkování léků ze skupiny inhibitorů ACE a beta-blokátorů.
Všeobecným zklamáním byly výsledky zatím největší klinické studie, která testovala léčbu srdečního selhání řízenou hladinami natriuretických peptidů – TIME-CHF. Tato randomizovaná multicentrická studie probíhala v letech 2003–2008 v 15 ambulantních centrech ve Švýcarsku (23). Bylo do ní zařazeno 499 nemocných se systolickým srdečním selháním (EF ≤ 0,45) ve věku 60 let a více, kteří měli při zařazení plazmatickou koncentraci NT-proBNP vyšší než dvojnásobek horní hranice normálních hodnot. Pracovní hypotéza, kterou měla studie potvrdit, byla, že léčba řízená podle NT-proBNP bude prospěšnější než léčba řízená podle klinického stavu především u starších nemocných. Tato hypotéza vycházela z představy, že starší nemocní jsou málo fyzicky aktivní, mají proto méně výrazné symptomy, zejména dušnost, a symptomy jsou u nich méně spolehlivé. Na druhou stranu jsou ale starší nemocní citlivější na léky a jejich nežádoucí účinky. Primárními sledovanými ukazateli byl jednak čas do hospitalizace z jakýchkoliv důvodů, jednak kvalita života hodnocená strukturovaným validovaným dotazníkem. Dávky léků byly uptitrovány častěji u nemocných léčených podle hladin NT-proBNP. Kvalita života se za průměrnou dobu sledování 18 měsíců zlepšila v obou skupinách nemocných stejně. Nebyl nalezen také žádný rozdíl mezi oběma skupinami v času do první hospitalizace (41 % vs. 40 %, HR = 0,91; p = 0,39). Klinické výsledky – hospitalizace z jakýchkoliv důvodů a hospitalizace pro zhoršení srdečního selhání – byly lepší ve skupině léčené podle NT‑proBNP pouze u mladších nemocných (< 75 let) s hodnotou p < 0,02 pro interakci. Léčba srdečního selhání řízená podle natriuretických peptidů tedy nezlepšila ani celkové klinické výsledky ani kvalitu života nemocných ve srovnání s léčbou řízenou symptomy. Nepotvrdila se také hypotéza, že natriuretickými peptidy řízená léčba bude prospěšnější u starších nemocných. Ve skutečnosti byla zjištěna přesně opačná interakce mezi věkem a prospěchem z léčby řízené BNP – větší prospěch z ní měli mladší nemocní (< 75 let). Naopak, u starších nemocných se při uptitraci denních dávek léků na základě vysoké plazmatické koncentrace NT‑proBNP objevily častěji nežádoucí účinky léků.
Podobně pesimisticky vyzněly i výsledky zatím poslední klinické studie PRIMA, které byly předneseny na letošním výročním sjezdu American College of Cardiology koncem března v Orlandu (24). V této multicentrické studii z Holandska bylo zařazeno 345 nemocných, kteří byli hospitalizovaní pro akutní zhoršení srdečního selhání, měli vstupní hodnotu NT-proBNP > 1700 pg/ml s poklesem během hospitalizace o více než 10 %. Tito nemocní byli randomizováni buď k léčbě podle klinického stavu (symptomů), nebo k léčbě řízené monitorováním NT-proBNP se snahou docílit individuální cílovou hodnotu. Individuální cílová hodnota byla nejnižší plazmatická koncentrace NT-proBNP dosažená u konkrétního nemocného při hospitalizaci. U nemocných s léčbou řízenou NT-proBNP byly častější změny medikace a jejího dávkování. Nejčastěji se změny týkaly diuretik (p = 0,018 proti nemocným léčeným podle klinického stavu). Přesto se primární sledovaný klinický ukazatel – počet dnů naživu bez hospitalizace – mezi oběma skupinami nemocných nelišil (p = 0,49). Nelišila se ani celková mortalita – 26,5 % u nemocných léčených podle NT‑proBNP vs 33,3 % u nemocných léčených podle symptomů (p = 0,196).
Studie OPTIMA a její předběžné výsledky
V roce 2005, tedy v době, kdy nebyly známy výsledky jiných studií než pilotní australské (21), jsme podobně jako na několika jiných pracovištích v různých státech zahájili klinickou studii OPTIMA (OPTIMAlization of heart failure treatment guided by plasma BNP levels). Do této randomizované studie prováděné v jednom centru bylo zařazeno 52 nemocných s nově diagnostikovaným nebo akutně zhoršeným pokročilým chronickým srdečním selháním (funkční třída III–IV dle NYHA), kteří byli hospitalizováni na III. interní klinice 1. LF UK a VFN v Praze a následně sledováni ambulantně v pravidelných tříměsíčních intervalech ve specializované ambulanci pro srdeční selhání stejného pracoviště. Tito nemocní byli randomizováni buď k léčbě srdečního selhání podle klinického stavu, tedy podle symptomů se snahou co nejlépe adherovat k platným doporučeným postupům České kardiologické společnosti (25) (klinická skupina), nebo k léčbě řízené plazmatickou koncentrací BNP se snahou o normalizaci této koncentrace (< 100 pg/ml) nebo o dosažení co nejnižší hodnoty (BNP skupina). V klinické skupině byla koncentrace BNP stanovena pouze při hospitalizaci před zařazením nemocného do studie a dále již ne, v BNP skupině byla koncentrace BNP stanovena při každé pravidelné tříměsíční kontrole stejně jako při neplánovaných kontrolách při zhoršení srdečního selhání. Znalost BNP byla ošetřujícím lékařem využívána pro léčebné rozhodování. Primárním sledovaným ukazatelem byla kombinace následujících klinických příhod: kardiovaskulární úmrtí + hospitalizace pro zhoršení srdečního selhání + zhoršení srdečního selhání vedoucí k navýšení denní dávky diuretika o ≥ 50 % bez nutnosti hospitalizace. Jako sekundární ukazatele byly vyhodnocovány: l. doba do prvního zhoršení srdečního selhání bez ohledu na nutnost hospitalizace, 2. počet úprav medikace „evidence based“ léky, tj. inhibitory ACE nebo sartany, beta-blokátory, diuretiky a spironolaktonem, 3. dosažené průměrné denní dávky „evidence based“ léků při poslední kontrole ve studii.
Průměrný věk zařazených nemocných byl 70 ± 11 let (rozmezí 36–89). Mužů bylo 35 (67 %) a žen 17 (33 %). U 32 nemocných (62 %) byla příčinou chronického srdečního selhání ischemická choroba srdeční, u 20 nemocných (38 %) byla etiologie srdečního selhání neischemická. Nemocní byli velmi dobře léčeni v souladu s platnými doporučenými postupy (25): diuretika užívalo 96 %, 90 % inhibitory ACE (preferenčně ramipril) nebo při intoleranci sartan, 92 % beta-blokátory (karvedilol nebo bisoprolol) a 62 % spironolakton. Důvodem, proč někteří nemocní neužívali některý z „evidence based“ léků, byla vždy intolerance nebo nežádoucí účinky. Tři nemocní (6 %) měli intoleranci inhibitorů ACE pro kašel, ti užívali jako alternativu losartan, další tři nemocní (6 %) neužívali žádný blokátor RAAS pro symptomatickou hypotenzi a další 2 (4 %) pro hyperkalémii, beta-blokátor neužívali čtyři nemocní (8 %) pro symptomatickou bradykardii.
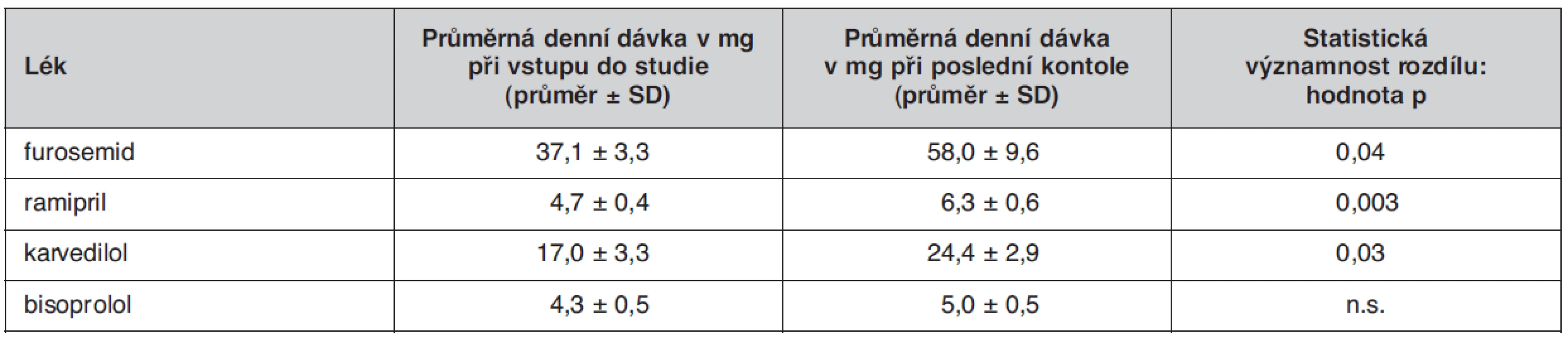
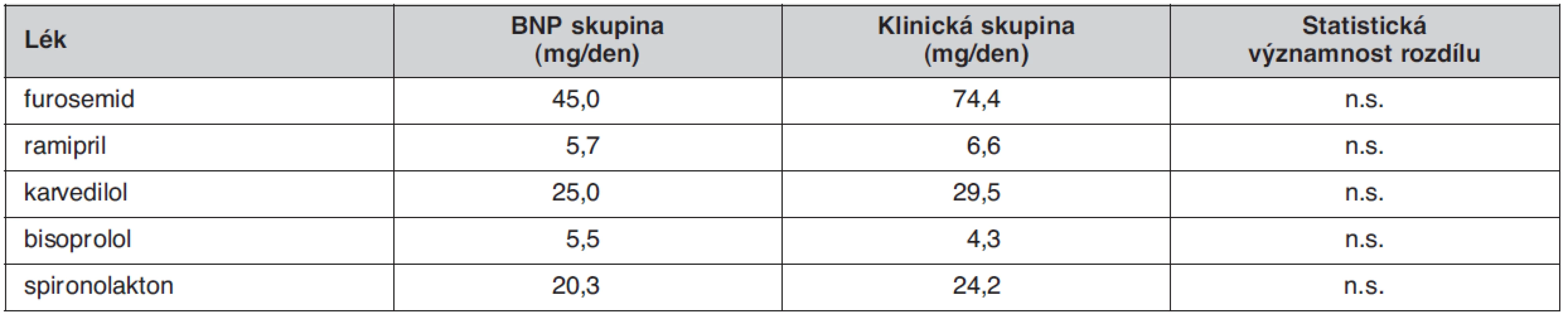
Dílčí výsledky této studie byly nedávno publikovány (26). Průměrná doba sledování byla 18 měsíců. U 90 % nemocných se podařilo v průběhu sledování snížit koncentraci BNP pod 400 pg/ml, u dvou třetin nemocných se pak podařilo dosáhnout dokonce normální plazmatickou koncentraci BNP (< 100 pg/ml). V obou skupinách se v průběhu sledování významně zvýšily průměrné denní dávky podávaných léků (tab. 1), ale při vstupu do studie ani při poslední kontrole se průměrné denní dávky v klinické skupině a BNP skupině nelišily, pouze u furosemidu byl při poslední kontrole zaznamenán trend k vyšší denní dávce, paradoxně však v klinické skupině (tab. 2). Byl patrný trend k nižšímu výskytu kardiovaskulárních příhod ve skupině nemocných, u kterých byla léčba řízena podle BNP, ve srovnání se skupinou nemocných, u kterých byla léčba řízena podle klinického stavu (16 vs. 24). Vzhledem k relativně malému absolutnímu počtu příhod však rozdíly nedosáhly statistické významnosti (obr. 2). Počet úmrtí se v obou skupinách nelišil (3 vs. 3). Zdá se, že by léčba řízená koncentracemi natriuretických peptidů mohla mít ekonomický dopad – mohla by snížit počet nutných hospitalizací.
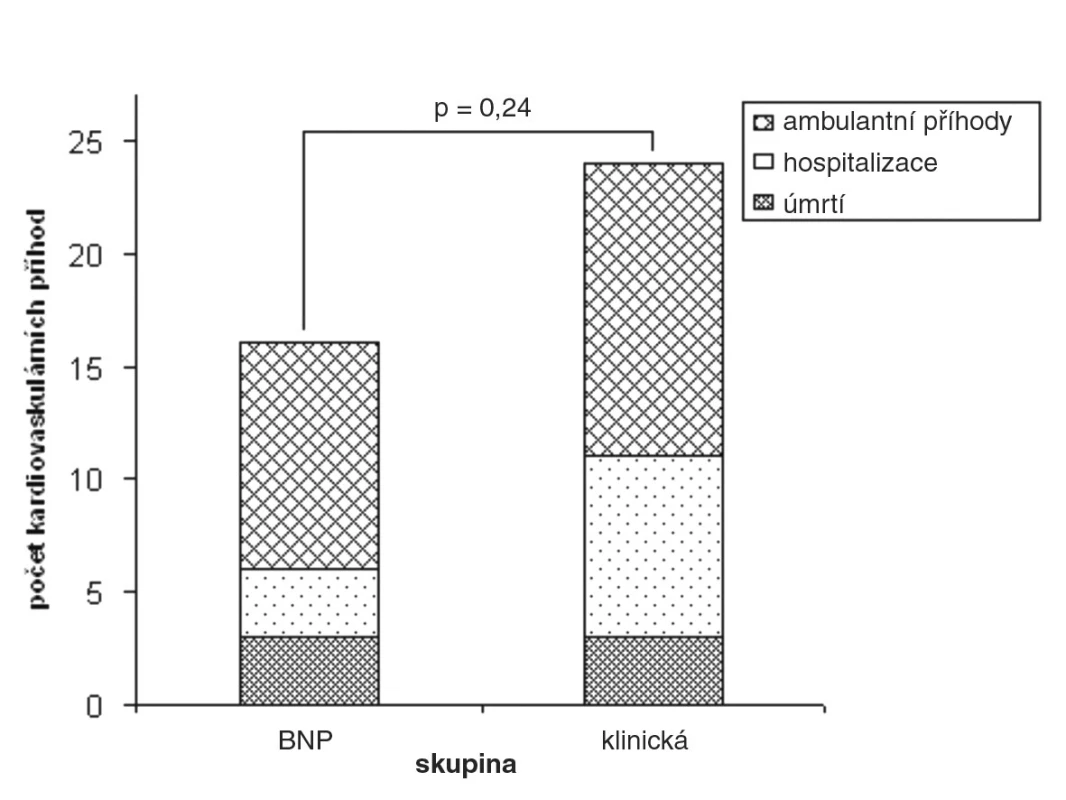
Definitivní výsledky studie OPTIMA budou publikovány do konce roku 2009.
Zkratky
ANP – atriální natriuretický peptid
RAAS – reninový–angiotenzinový–aldosteronový systém
SAS – sympatoadrenální systém
Adresa ke korespondenci:
prof. MUDr. Jaromír Hradec, CSc.,
FESC III. interní klinika 1. LF UK a VFN U Nemocnice 1,
128 08 Praha 2
fax: +420 224 922 268,
e-mail: jhradec@vfn.cz/p>
Sources
1. Petrášek J. Feochromocytom. Edice Thomayerova sbírka č. 471. Praha: Avicenum 1976.
2. Hradec J, Marek J, Král J, Janota T, Poloniecki J, Malik M. Long-term echocardiographic follow-up of acromegalic heart disease. Am J Cardiol 1993; 72 : 205–210.
3. Hradec J, Král J, Janota T, Kršek M, Hána V, Marek J, Malik M. Regression of acromegalic left ventricular hypertrophy after lanreotide (a slow release somatostatin analog). Amer J Cardiol 1999; 83 : 1506–1509.
4. De Bold AJ, Borenstein HB, Veress AT, Sonnenberg H. A rapid and potent natriuretic response to intravenous injection of atrial myocardial extract in rats. Life Sci 1981; 28 : 89–94.
5. Flynn TG, de Bold ML, de Bold AJ. The amino acid sequence of an atrial peptide with potent diuretic and natriuretic properties Biochem Biophys Res Commun 1983; 117 : 859–865.
6. Sudoh T, Kangawa K, Minamino N, Matsuo H. A new natriuretic peptide in porcine brain. Nature 1988; 332 : 78–81.
7. Sudoh T, Minamino N, Kangawa K, Matsuo H. C-type natriuretic peptide (CNP): a new member of natriuretic peptide family identified in porcine brain. Biochem Biophys Res Commun 1990; 168 : 863–870.
8. Mair J, Hammerer-Lercher A, Puschendorf B. The impact of cardiac natriuretic peptide determination on the diagnosis and management of heart failure. Clin Chem Lab Med 2001; 39 : 571–588.
9. McDonagh TA, Robb SD, Murdoch DR, et al. Biochemical detection of left-ventricular systolic dysfunction. Lancet 1998; 351 : 9–13
10. Morrison LK, Harrison A, Krishnaswamy P, et al. Utility of rapid B-natriuretic peptide assay in differentiating congestive heart failure from lung disease in patients presenting with dyspnea. J Am Coll Cardiol 2002; 39 : 202–209.
11. Hradec J. Mohou se stát natriuretické peptidy křišťálovou koulí kardiologa? J Am Coll Cardiol - CZ 2003; 5 : 255–257.
12. Cowie MR, Struthers AD, Wood DA, et al. Value of natriuretic peptides in assessment of patients with possible new heart failure in primary care. Lancet 1997; 350 : 1347–1351.
13. Dickstein K, Cohen-Solal A, Fillipatos G, et al. for the Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2008 of the Europen Society of Cardiology. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2008. Eur J Heart Fail 2008; 10 : 933–989.
14. Kirk V, Bay M, Parner J, et al. N-terminal proBNP and mortality in hospitalised patients with heart failure and preserved vs. reduced systolic function: data from the prospective Copenhagen Hospital Heart Failure Study (CHHF). Eur J Heart Fail 2004; 6 : 335–341.
15. Hartmann F, Packer M, Coats A, et al. NT-proBNP in severe heart failure: rationale, design and preliminary results of the COPERNICUS NT-proBNP substudy. Eur J Heart Fail 2004; 6 : 343–350.
16. Jakubík P, Janota T, Widimský J jr, et al. Impact of essential hypertension and primary aldosteronism on plasma brain natriuretic peptide concentration. Blood pressure 2006; 15 : 302–307.
17. Hildebrandt P, Boesen M, Olsen M, et al. N-terminal pro brain natriuretic peptide in arterial hypertension – a marker for left ventricular dimensions and prognosis. Eur J Hear Fail 2004; 6 : 313–317.
18. Janota T, Jakubík P, Wichterle D, et al. Předpovědní hodnota BNP po kardioverzi fibrilace síní pro dlouhodobé udržení sinusového rytmu. Cor Vasa 2007; 49: K273–K274.
19. The Study Group of Diagnosis of the Working Group on Heart Failure of the European Society of Cardiology. The EuroHeart Failure Survey program – a survey on the quality of care among patints with heart failure in Europe. Part 2: treatment. Eur Heart J 2003; 24 : 464–474.
20. Hradec J, Wikstrand J, Černáková L. Charakteristika a farmakoterapie nemocných s chronickým srdečním selháním ischemické etiologie v České Republice. Cor Vasa 2009; 51 : 268–273.
21. Troughton RW, Frampton CM, Yandle TG, et al. Treatment of heart failure guided by plasma amino terminal brain natriuretic peptide (N-BNP) levels improves outcome. Lancet 2000; 355 : 1126–1130.
22. Jourdain P, Jondeau G, Funck F, et al. Plasma brain natriuretic peptide-guided therapy to improve outcome in heart failure. The STARS-BNP Multicenter Study. J Am Coll Cardiol 2007; 49 : 1733–1739.
23. Pfisterer M, Buser P, Rickli H, et al. BNP-guided vs symptom-guided heart failure therapy. The trial of intensified vs standard medical therapy in elderly patients with congestive heart failure (TIME-CHF) randomized trial. JAMA 2009; 301 : 383–392.
24. Eurlings L, Pinto Y. PRIMA Study. NT-proBNP-guided management of heart failure based on individual target value. Předneseno na kongresu American College of Cardiology, Orlando, USA, 29. 3. – 1. 4. 2009.
25. Špinar J, Hradec J, Meluzín J, et al. Doporučení pro diagnostiku a léčbu chronického srdečního selhání ČKS 2006. Cor Vasa 2007; 49: K5–K34.
26. Krupička J, Janota T, Kasalová Z, Hradec J. Natriuretic peptides - physiology, patophysiology and clinical use in heart failure. Phys Res 2009; 58 : 171–177.
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental HygienistArticle was published in
Journal of Czech Physicians

- Advances in the Treatment of Myasthenia Gravis on the Horizon
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
- Metamizole vs. Tramadol in Postoperative Analgesia
- Spasmolytic Effect of Metamizole
-
All articles in this issue
- Dlouhodobý elektrokardiogram
- Elektrokardiografie včera a dnes
- Ateroskleróza v dětském věku
- Feochromocytom: diagnostika a léčba
- Hypertenzní krize – současný pohled
- Význam echokardiografie v diagnostice kardiovaskulárních onemocnění u těhotných žen
- Vliv znečištění ovzduší na kardiovaskulární mortalitu
- Budeme léčit srdeční selhání podle plazmatické koncentrace natriuretických peptidů?
- Diagnostika a léčba organického hyperinzulinismu – zkušenosti u 105 pacientů
- Od vědeckého důkazu k moderní vysoce efektivní léčbě alergicky nemocných v současné době
- Endarterektomie nebo stentování karotid: hledání pokračuje
- Diety bohaté na borůvky chrání králičí srdce před ischemickým poškozením
- Journal of Czech Physicians
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Feochromocytom: diagnostika a léčba
- Diagnostika a léčba organického hyperinzulinismu – zkušenosti u 105 pacientů
- Hypertenzní krize – současný pohled
- Elektrokardiografie včera a dnes
