Masivní krvácení do tenkého střeva: CT-angiografie a chirurgické řešení – kazuistika
Massive small intestine bleeding: CT-angiography and surgical treatment – a case report
Gastrointestinal bleeding is one of acute abdomen conditions that occur relatively frequently. Most cases can nowadays be managed endoscopically, surgery is rarely required. Approximately 5% of gastrointestinal bleeding cases are cases of so-called obscure gastrointestinal bleeding. The presented massive gastrointestinal bleed case report provides a current view on diagnostic and therapeutic modalities in the context of everyday clinical practice.
Key words:
angiectasia – obscure gastrointestinal bleeding – lower gastrointestinal bleeding – CT-angiography
:
J. Halamka 1; P. Chmátal 2
:
Chirurgické oddělení Městské nemocnice v Litoměřicích, primář: MUDr. L. Dostál
1; Ústav leteckého zdravotnictví Praha, ředitel: MUDr. P. Chmátal Ph. D., MBA
2
:
Rozhl. Chir., 2015, roč. 94, č. 4, s. 174-176.
:
Case Report
Krvácení do trávicího traktu je jednou z náhlých příhod břišních, se kterou se setkáváme relativně často. Většina těchto příhod je v současné době řešitelná endoskopicky, urgentní chirurgickou revizi si žádají spíše výjimečně. Přibližně 5 % krvácení do GIT je skrytých v jejunoileální oblasti. Předložená kazuistika masivního krvácení z tenkého střeva přináší současný názor na diagnostiku a léčebné možnosti z pohledu každodenní klinické praxe službu konajících chirurgů.
Klíčová slova:
angiektázie – krvácení do tenkého střeva – krvácení do dolní části trávicího traktu – CT-angiografie
ÚVOD
Masivní krvácení v oblasti tenkého střeva se v naší literatuře občas označuje slovem obskurní z anglického sousloví „obscure gastrointestinal bleeding − OGIB“ (český význam slova obskurní je: temný, pokoutní, nekalý, podezřelý či mravně závadný). Tvoří asi 5 % všech krvácení do trávicí trubice [1] a pro chirurga bývá diagnostickým i terapeutickým problémem.
Přitom správně lokalizovat krvácení a zvolit odpovídající chirurgický postup je pro další osud pacienta nezbytné. Ačkoliv téměř 75 % krvácení odezní spontánně, u více než 25 % pacientů dochází k recidivě se stoupající morbiditou i mortalitou [2]. V následujícím sdělení předkládáme kazuistiku mladého muže, doposud zdravého, anamnesticky bez krvácení či jiných gastrointestinálních (GIT) obtíží, který byl v naší nemocnici přijatý pro masivní krvácení do GIT.
KAZUISTIKA
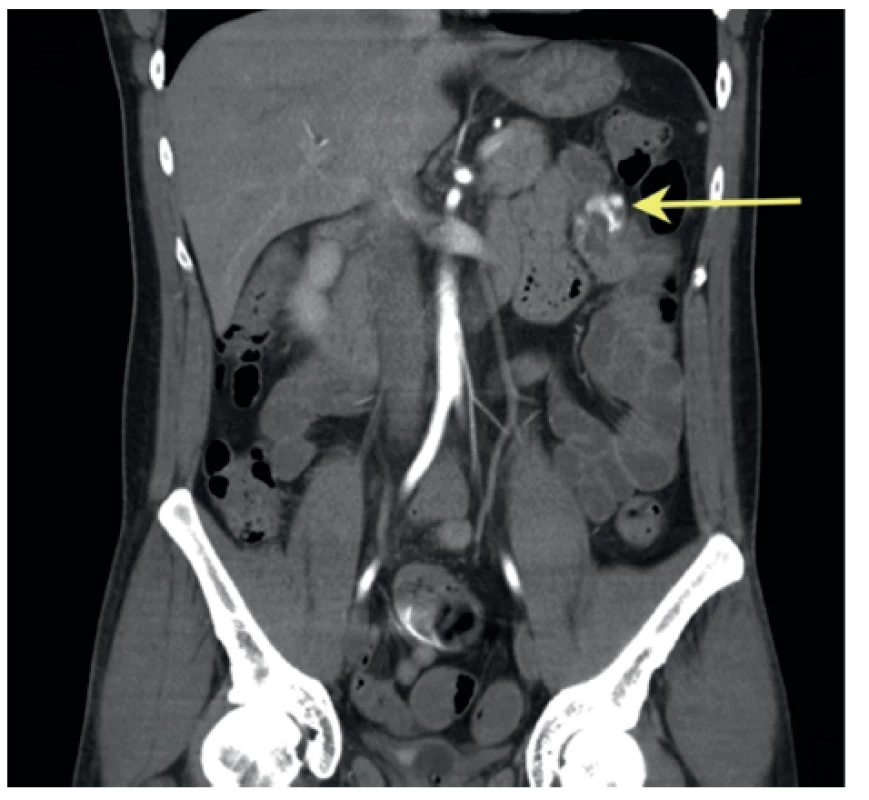
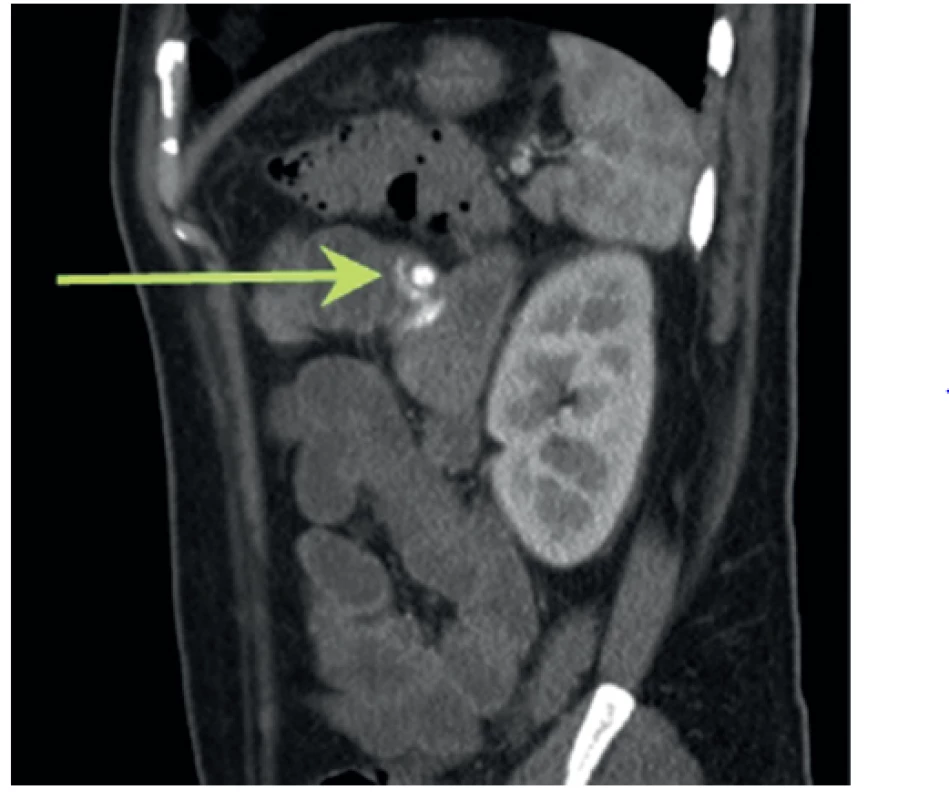
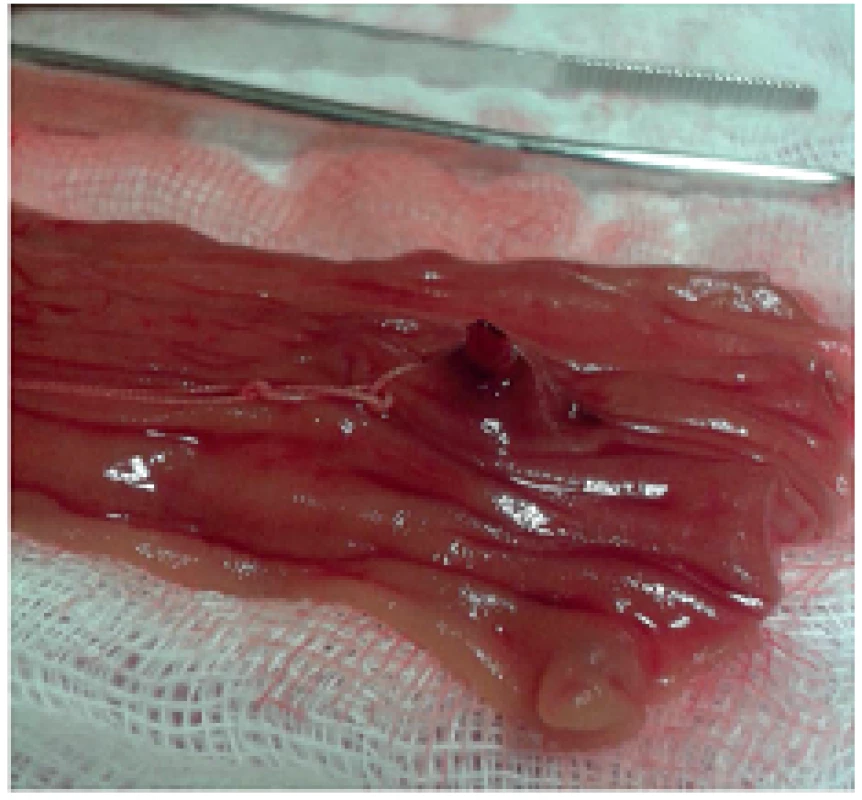
21letý pacient byl předán záchrannou službou na centrální příjem nemocnice ve sváteční den ráno. Masivní enterorrhagii udával od 4. hod. v noci, v poslední hodině prakticky nepřetržitě odcházela z konečníku tmavá krev. Po uložení na lůžko MOJIP (mezioborová jednotka intenzivní péče) byl oběhově kompenzován TK 120/80, P prav. 92, sat. O2 99 %, při vědomí, dobře orientován, spolupracující, břicho bylo měkké, palpačně nebolestivé, v ampule s tmavou krví. Akra byla bledá, chladnější. Laboratorně: HGB 91 g/l, leukocyty 15,42 tis., INR 1,33, APTT 21,00, celková bílkovina 44,5 g/l, albumin 28,5 g/l, ostatní laboratorní nálezy v mezích normy. Na lůžku byla zahájena volum-resuscitace a podány krevní převody včetně mražené plazmy, hemostyptik a Remestypu. Dvě hodiny po přijetí byla provedena akutní gastroskopie s negativním nálezem akutního krvácení, poté rektoskopie vylučující krvácení v poslední etáži střeva. Pro pokračující masivní enterorrhagii s dalším poklesem KO (HGB 50 g/l) byla indikována ve 4. hodině po přijetí CT-angiografie (CT-AG). Rentgenolog nalézá zdroj krvácení intraluminálně v orální kličce jejuna uložené v levém mezogastriu, etiologie susp. angiektázie či arteriovenózní malformace (Obr. 1,2), vedlejší nález: tenké lemy tekutiny perihepatálně a v rektovezikální exkavaci. Pacient byl indikován k urgentní operační revizi. V dutině břišní byl normální nález na parenchymových orgánech, tenké střevo naplněno obsahem, asi 80 cm aborálně od Treitzova ligamenta byla ve stěně hmatná elastická rezistence, suspektní ze zdroje krvácení. Tenká klička byla resekována v rozsahu cca 40 cm, z aborálního i orálního úseku odsáta i krev. koagula, v kličce byl makroskopicky submukózní hematom vel. cca 2x1 cm s povrchovou ragádou ve sliznici. Protože nález plně neodpovídal CT, lokalizaci pokračovala revize jejuna za pomoci svorek, která nalezla krvácení asi 30 cm orálně. V druhém resekátu jejuna v rozsahu 10 cm bylo drobné hráškovité vyklenutí sliznice s otevřenou cévou (Obr. 3). Pacient byl po výkonu 5 dní na lůžku MOJIP, 5 dní na standardním oddělení, od 3. poop. dne byl realimentován, 10. dne propuštěn do domácího ošetřování. Během operačního dne mu bylo podáno 12 TU ery masy.
V histopatologickém obraze obou resekovaných úseků jejuna byl zastižen shluk angiektázií ve sliznici a ve stěně střeva.
DISKUZE
Tradiční klasifikace obvykle rozděluje krvácení do gastrointestinálního traktu podle lokalizace zdroje na horní a dolní, dělicím místem je Treitzovo ligamentum. Incidence krvácení do dolního traktu se uvádí 20 až 27/100 tisíc osob [3,4]. Pro krvácení od oblasti Vaterské papily až po terminální ileum se objevuje v literatuře i termín „median gastrointestinal bleeding“ [5] nebo také obskurní krvácení do trávicího traktu – pro jeho nedosažitelnost běžnými endoskopickými metodami [1,6]. V symptomatologii masivního krvácení do dolního GIT dominuje hematochezie a oběhová nestabilita. Většina krvácení se zastaví spontánně (75 % až 80 %) [2,7] a je spojena s průměrnou mortalitou 8 % až 16 % [5,8]. U pacientů nad 65 let pak ale mortalita dosahuje 21 % až 40 % [9,10].
Rekurence spontánně odeznělého krvácení je uváděna mezi 25 % a 30 % [7,11].
Krvácení z cévních malformací dolního traktu se v porovnání s jinými příčinami vyskytuje relativně vzácně. Podle epidemiologických studií nejčastěji masivně krvácejí divertikly (30 %), následované afekcemi konečníku (20 %), střevní ischemií (12%), IBD – inflammatory bowel disease (9 %) a nádory (6 %). Na cévní malformace zbývají méně než 3 % [12,13], přičemž 75 % angiodysplazií se vyskytuje v pravém tračníku a krvácejí spíše v pozdním věku [13].
Vyšetřovací postup je standardně zahajován endoskopickými metodami. Gastroduodenoskopie a kolonoskopie jsou dnes považovány za vyšetření první linie u krvácení z horního i dolního traktu. Při masivním krvácení se však kolonoskopie stává bezcennou jak pro nemožnost přípravy pacienta, tak pro technickou nedosažitelnost vyšších etáží střeva. Bývá nahrazována rektoskopií.
Pro dlouhou přípravu i technickou nedostatečnost jsou u masivního krvácení nepoužitelné pertechnátová scintigrafie či kapslová enteroskopie.
Digitální subtrakční angiografie (DSA) je schopna poskytnout diagnostiku i terapeutický zásah formou cílené embolizace. DSA detekuje krvácení od 0,4 ml/min. s uváděnou senzitivitou 40–86 % [14,15]. Nevýhodou jsou nízká dostupnost i časová náročnost. Ta je v urgentních situacích jejím limitujícím faktorem. V případě využití DSA k terapeutickému výkonu jsou udávány časné komplikace ve formě akutní střevní ischemie v 7 % a pozdní ve formě jizevnatých striktur embolizovaných úseků ve 14 % [1].
CT-angiografie (CT-AG) se v posledním desetiletí zařadila do první linie vyšetřovacího postupu. Je široce dostupná. Je rychlá, je neinvazivní. Je ekonomicky efektivní. Je schopna detekovat krvácení od 0,3 ml/min. Je schopna chirurgovi pomoci v rozhodování mezi operací, arteriografií se selektivní embolizací a kolonoskopií, při kvalitním provedení dokáže relativně spolehlivě určit přesnou lokalizaci zdroje ve střevě. Vysokou účelnost použití, vysokou senzitivitu (75 % až 94 %) i vysokou specificitu (74 % až 97 %) dokládají i dvě metaanalýzy publikované v letech 2010 a 2013 [8,10]. Ve shodě dostupné literatury by CT-AG v případě pokračujícího nebo recidivujícího masivního LGIB-lower gastrointestinal bleeding měla následovat bezprostředně po negativní gastroskopii a rektoskopii [8].
Časný operační výkon je nezbytným vyústěním chirurgova postupu u pokračujícího krvácení a hemodynamické nestability. Je logické, že žádný chirurg akutní operaci pro krvácení z neznámého zdroje nemá rád, mimo jiné i proto, že tyto výkony bývají zatíženy vysokým procentem operačních nezdarů. V případě naslepo vedených resekcí se udává perzistence krvácení po výkonu 42 % a časná rekurence krvácení mezi 30 % až 75 % [8]. Naslepo vedené výkony jsou zatíženy též značnou morbiditou 20 % až 60 % [7,11] a také vysokou mortalitou uváděnou mezi 10 % až 57 % [8,11]. CT-AG vzhledem ke své rozlišovací schopnosti dokáže zpřesnit lokalizaci krvácejícího ložiska a zmírnit rizika rozsáhlé naslepo vedené resekce. Zpřesnit místo krvácení lze peroperačně endoskopií z enterotomie, v urgentním režimu však bývá organizačně problematická a intraluminální přehled nemusí být dostatečný.
Lze polemizovat o využití endovaskulárních metod jako primárního ošetření [7] s případnou chirurgickou revizí při rebleedingu. Při hemodynamické nestabilitě ale stále zůstává operace jako základní postup [6,7].
V průběhu celého procesu nelze opominout komplexní péči o pacienta, který upadá do hemorrhagického šoku. Důležitá je volumová náhrada udržením přiměřeného perfuzního tlaku – syst. 100 mm Hg s cílovou hodnotou HGB 80–100 mg/l. Hemostatická resuscitace dále znamená masivní podání krevních derivátů s omezením krystaloidů, ery masy k plazmě jsou podávány v poměru 1,5 : 1, resp. 1 : 1 [16]. Do chirurgického vyřešení krvácení lze podávat terlipresin.
V české literatuře lze nalézt od roku 1957 několik příspěvků na téma krvácení do tenkého střeva. Jedná se především o jednotlivé kazuistiky, kdy krvácení bylo na podkladě leiomyomů, stromálních tumorů, arteriovenózních malformací a sigmoideálních divertiklů. Od autorů Pastror a Adámek z roku 2013 pochází souhrnné sdělení o obskurním krvácení, které přináší současný pohled na terminologii krvácení do dolního GIT a také na možnosti diagnostiky a léčby [1].
ZÁVĚR
Kazuistika na příkladu mladého muže poukázala na obtížnost řešení masivního krvácení v oblasti tenkého střeva. Při hemodynamické nestabilitě zůstává operační výkon základním postupem. CT-angiografie může zpřesnit lokalizaci krvácejícího ložiska a zmírnit rizika naslepo vedené resekce.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
MUDr. Jaroslav Halamka
Rooseveltova 744/9
412 01 Litoměřice
e-mail: halamka.jaroslav
Sources
1. Pastor J, Adámek S. Obskurní krvácení do zažívacího traktu. Rozhl Chir 2013;92 : 424−8.
2. Imdahl A, et al. Genesis and pathophysiology of lower gastrointestinal bleeding. Langenbecks Arch Surg 2001;386 : 1−7.
3. Manning-Dimmitt LL, Dimmit SG, Wilson GR. Diagnosis of gastrointestinal bleeding in adults. Am Fam Physician 2005;71 : 1339−48.
4. Zink SI, Ohki SK, Stein B, et al. Noninvasive evaluation of active lower gastrointestinal bleeding: a prospective study. J Med Imaging Radiat Oncol 2011;55 : 252−8.
5. Martí M, Artigas JM, Garson G, et al. Acute lower intestinal bleeding: feasibility and diagnostic performance of CT angiography. Radiology 2012;262 : 109−16.
6. Kochhar GS, Sanaka MR, Vargo JJ. Therapeutic management options for patients with obscure gastrointestinal bleeding. Ther Adv Gastrenterol 2012;5 : 71−81
7. Czymek R, Kempf A, Roblick UJ, et al. Surgical treatment concepts for acute lower gastrointestinal bleeding. J Gastrointest Surg 2008;12 : 2212−20.
8. Garcia-Blásquez V, Vicente –Bártulos A, Olavarria-Delgado A, et al. Accuracy of CT angiography in the diagnosis of acute gastrointestinal bleeding: systematic review and meta-analysis. Eur Radiol 2013;23 : 1181−90.
9. Longstreth GF. Epidemiology and outcome of patients hospitalized with acute lower gastrointestinal hemorrhagy: a population – based study. Am J Gastroenterol 1997;92 : 416−23.
10. Wu LM, Xu JR, Yin Y, et al.Usefulness of CT angiography in diagnosing acute gastrointestinal bleeding: a meta-analysis. World J Gastronetrol 2010;31 : 3957−63.
11. Ríos A, Montoya MJ, Rodzíguez JM, et al. Severe acute gastrointestinal bleeding: risk factors for morbidity and mortality. Langenbecks Arch Surg 2007; 392 : 165−1.
12. Ghassemi KA, Jensen DM. Lower GI bleeding: epidemiology and management. Curr Gastroenterol Rep 2013;15 : 333.
13. Dayer C, Chino A, Lucas C. Acute lower gastrointestinal bleeding in1 112 patients admitted to an urban emergency medical center. Surgery 2009;146 : 600−6.
14. Vernava AD, Moore BA, Longo WE, et al. Lower gastrointestinal bleeding. Dis Colon Rectum 1997;40 : 846−58.
15. Cohn SM, Moller BA, Zieg PM, et al. Angiography for preoperative evaluation in patients with lower gastrointestinal bleeding: are the benefits worth the risks? Arch Surg 1998;133 : 50−5.
16. Ševčík P, Matějovič M, Černý V, et al. Intenzivní medicína. Galén, Praha 2014 : 242−5,525−37.
Labels
Surgery Orthopaedics Trauma surgeryArticle was published in
Perspectives in Surgery

2015 Issue 4
- Possibilities of Using Metamizole in the Treatment of Acute Primary Headaches
- Metamizole vs. Tramadol in Postoperative Analgesia
- Metamizole at a Glance and in Practice – Effective Non-Opioid Analgesic for All Ages
-
All articles in this issue
- How to continue the provision of care for serious injuries?
- The past and present of thumb reconstruction
- The ONSTEP inguinal hernia repair technique
- Intraoperative sentinel lymph node detection in colon cancer resection – preliminary results
- Acute necrotizing pancreatitis: traditional laparotomy vs. minimally invasive procedures
- Malignant mesothelioma in the peritoneal cavity – a case report
- Massive small intestine bleeding: CT-angiography and surgical treatment – a case report
- Sigmoid colon cancer in pregnancy – a case report
- Perspectives in Surgery
- Journal archive
- Current issue
- About the journal
Most read in this issue
- The ONSTEP inguinal hernia repair technique
- Massive small intestine bleeding: CT-angiography and surgical treatment – a case report
- The past and present of thumb reconstruction
- Acute necrotizing pancreatitis: traditional laparotomy vs. minimally invasive procedures
